Zestoretic 5/12.5g/mg Lisinopril Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Zestoretic och hur används det?
Zestoretic är ett receptbelagt läkemedel som används för att behandla symtom på hypertoni (högt blodtryck) och vätskeretention. Zestoretic 5mg kan användas ensamt eller tillsammans med andra läkemedel.
Det är inte känt om Zestoretic 5mg är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Zestoretic 5mg?
Zestoretic kan orsaka allvarliga biverkningar inklusive:
- känner sig yr,
- ögonsmärta eller synproblem,
- lite eller ingen urinering,
- svaghet,
- dåsighet,
- känner sig rastlös,
- feber ,
- frossa,
- öm hals,
- munsår,
- problem med att svälja,
- gulfärgning av hud och ögon (gulsot),
- illamående,
- kräkningar,
- pirrande känsla,
- bröstsmärta,
- oregelbundna hjärtslag eller fladdrande i bröstet,
- förlust av rörelse,
- kramper i benen,
- förstoppning,
- extrem törst,
- ökad urinering,
- domningar eller stickningar,
- muskelsvaghet,
- huvudvärk,
- förlust eller koordination, och
- känner sig ostadig
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Zestoretic inkluderar:
- hosta
- huvudvärk
- yrsel
- känner mig trött
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Zestoretic. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
- När graviditet upptäcks, avbryt behandlingen med ZESTORETIC så snart som möjligt.
- Läkemedel som verkar direkt på renin-angiotensinsystemet kan orsaka skador och dödsfall för fostret under utveckling. Ser VARNINGAR Fostertoxicitet.
BESKRIVNING
ZESTORETIC® (lisinopril och hydroklortiazid) kombinerar en angiotensinomvandlande enzymhämmare, lisinopril, och ett diuretikum, hydroklortiazid.
Lisinopril, ett syntetiskt peptidderivat, är en oral långverkande angiotensinomvandlande enzymhämmare. Det beskrivs kemiskt som (S)-1-[N2-(1-karboxi-3-fenylpropyl)-L-lysyl]-L-prolin-dihydrat. Dess empiriska formel är C21H31N3O5. 2H2O och dess strukturformel är:
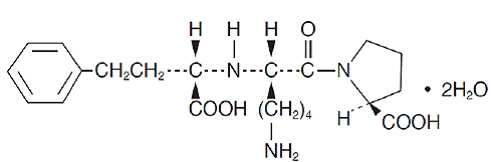
Lisinopril är ett vitt till benvitt, kristallint pulver med en molekylvikt på 441,53. Det är lösligt i vatten, svårlösligt i metanol och praktiskt taget olösligt i etanol.
Hydroklortiazid är 6-klor-3,4-dihydro-2H-1,2,4-bensotiadiazin-7-sulfonamid-1,1-dioxid. Dess empiriska formel är C7H8ClN3O4S2 och dess strukturformel är:
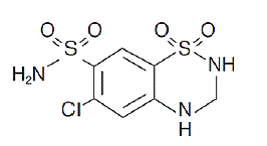
Hydroklortiazid är ett vitt, eller praktiskt taget vitt, kristallint pulver med en molekylvikt på 297,72, som är lätt lösligt i vatten, men fritt lösligt i natriumhydroxidlösning.
ZESTORETIC 5mg finns tillgängligt för oral användning i tre tablettkombinationer av lisinopril med hydroklortiazid: ZESTORETIC 10-12,5 innehållande 10 mg lisinopril och 12,5 mg hydroklortiazid; ZESTORETIC 20Referens 12.5 innehållande 20 mg lisinopril och 12,5 mg hydroklortiazid; och ZESTORETIC 20-25 innehållande 20 mg lisinopril och 25 mg hydroklortiazid.
Inaktiva Ingredienser
10-12,5 tabletter -kalciumfosfat, magnesiumstearat, mannitol, röd järnoxid, majsstärkelse, gul järnoxid.
20-12,5 tabletter -kalciumfosfat, magnesiumstearat, mannitol, majsstärkelse.
20-25 tabletter -kalciumfosfat, magnesiumstearat, mannitol, röd järnoxid, majsstärkelse, gul järnoxid.
INDIKATIONER
ZESTORETIC är indicerat för behandling av hypertoni för att sänka blodtrycket. Att sänka blodtrycket minskar risken för dödliga och icke-dödliga kardiovaskulära händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade studier av blodtryckssänkande läkemedel från en mängd olika farmakologiska klasser inklusive lisinopril och hydroklortiazid.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än 1 läkemedel för att uppnå blodtrycksmålen. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos drogerna, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad i populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras hypertoni (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter kan förväntas att dra nytta av mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa blodtryckssänkande läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi.
Dessa kombinationer med fasta doser är inte indicerade för initial behandling (se DOSERING OCH ADMINISTRERING ).
Vid användning av ZESTORETIC bör man ta hänsyn till det faktum att en hämmare av angiotensinomvandlande enzym, kaptopril, har orsakat agranulocytos, särskilt hos patienter med nedsatt njurfunktion eller kollagenkärlsjukdom, och att tillgängliga data är otillräckliga för att visa att lisinopril inte har en liknande risk (se VARNINGAR ).
Vid övervägande av användningen av ZESTORETIC mg bör det noteras att ACE-hämmare har associerats med en högre frekvens av angioödem hos svarta än hos icke-svarta patienter (se VARNINGAR , Lisinopril ).
DOSERING OCH ADMINISTRERING
Lisinopril monoterapi är en effektiv behandling av hypertoni i doser en gång dagligen på 10 mg till 80 mg, medan hydroklortiazid monoterapi är effektiv i doser på 12,5 mg per dag till 50 mg per dag. I kliniska prövningar av kombinationsbehandling med lisinopril/hydroklortiazid med lisinoprildoser på 10 mg till 80 mg och hydroklortiaziddoser på 6,25 mg till 50 mg, ökade den antihypertensiva svarsfrekvensen i allmänhet med ökande dos av någon av komponenterna.
Biverkningarna (se VARNINGAR ) av lisinopril är i allmänhet sällsynta och uppenbarligen oberoende av dos; de för hydroklortiazid är en blandning av dosberoende fenomen (främst hypokalemi) och dosberoende fenomen (t.ex. pankreatit), de förra mycket vanligare än de senare. Behandling med valfri kombination av lisinopril och hydroklortiazid kan vara associerad med endera eller båda dosberoende eller dosberoende biverkningar, men tillägg av lisinopril i kliniska prövningar dämpade den hypokalemi som normalt ses med diuretika.
För att minimera dosberoende biverkningar är det vanligtvis lämpligt att påbörja kombinationsbehandling först efter att en patient inte har uppnått önskad effekt med monoterapi.
Dostitrering styrd av klinisk effekt
En patient vars blodtryck inte är tillräckligt kontrollerat med antingen lisinopril eller hydroklortiazid som monoterapi kan bytas till lisinopril/HCTZ 10/12,5 eller lisinopril/HCTZ 20/12,5, beroende på aktuell monoterapidos. Ytterligare ökningar av endera eller båda komponenterna bör bero på kliniskt svar med blodtryck mätt vid interdoseringsintervallet för att säkerställa att det finns en adekvat antihypertensiv effekt vid den tidpunkten. Hydroklortiaziddosen bör i allmänhet inte ökas förrän 2 till 3 veckor har förflutit. Efter tillsats av diuretikum kan det vara möjligt att minska dosen av lisinopril. Patienter vars blodtryck är tillräckligt kontrollerat med 25 mg dagligen hydroklortiazid, men som upplever betydande kaliumförlust med denna regim, kan uppnå liknande eller bättre blodtryckskontroll utan elektrolytstörningar om de byter till lisinopril/HCTZ 10/12,5.
Hos patienter som för närvarande behandlas med ett diuretikum kan symtomatisk hypotoni ibland uppstå efter den initiala dosen av lisinopril. Diuretikumet ska om möjligt sättas ut i två till tre dagar innan behandling med lisinopril påbörjas för att minska sannolikheten för hypotoni (se VARNINGAR ). Om patientens blodtryck inte kontrolleras med enbart lisinopril kan diuretikabehandling återupptas.
Om diuretikumet inte kan avbrytas, bör en initial dos på 5 mg lisinopril användas under medicinsk övervakning i minst två timmar och tills blodtrycket har stabiliserats i minst ytterligare en timme (se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ).
Samtidig administrering av ZESTORETIC och kaliumtillskott, kaliumsaltersättningsmedel eller kaliumsparande diuretika kan leda till ökningar av serumkalium (se FÖRSIKTIGHETSÅTGÄRDER ).
Ersättningsterapi
Kombinationen kan ersätta de titrerade individuella komponenterna.
Användning vid nedsatt njurfunktion
Behandlingsregimer med lisinopril/HCTZ behöver inte ta hänsyn till njurfunktionen så länge som patientens kreatininclearance är >30 ml/min/1,7 m2 (serumkreatinin ungefär ≤3 mg/dL eller 265 μmol/L). Hos patienter med svårare njurfunktionsnedsättning är loopdiuretika att föredra framför tiazider, så lisinopril/HCTZ rekommenderas inte (se VARNINGAR , Anafylaktoida reaktioner under membranexponering ).
HUR LEVERERAS
ZESTORETIC 10-12,5 tabletter: Persika, runda, bikonvexa, odragerade tabletter identifierade med "141" präglad på ena sidan och "ZESTORETIC" på andra sidan levereras i flaskor med 90 tabletter ( NDC 52427-435-90) och flaskor med 100 tabletter ( NDC 52427-435-01).
ZESTORETIC 20-12,5 tabletter : Vita, runda, bikonvexa, odragerade tabletter märkta med "142" präglade på ena sidan och "ZESTORETIC" på andra sidan levereras i burkar med 90 tabletter ( NDC 52427-436-90) och flaskor med 100 tabletter ( NDC 52427-436-01).
ZESTORETIC 20-25 tabletter Persika, runda, bikonvexa, odragerade tabletter identifierade med "145" präglad på ena sidan och "ZESTORETIC" på den andra sidan levereras i burkar med 90 tabletter ( NDC 52427-43790) och flaskor med 100 tabletter ( NDC 52427-437-01).
Lagring
Förvara vid kontrollerad rumstemperatur, 20-25°C (68-77°F) [se USP]. Skydda mot överdrivet ljus och fukt.
Distribueras av: Almatica Pharma, Inc. Pine Brook, NJ 07058 USA. Reviderad: juli 2017.
BIEFFEKTER
ZESTORETIC 12,5gmg har utvärderats för säkerhet hos 930 patienter inklusive 100 patienter som behandlats i 50 veckor eller mer.
I kliniska prövningar med ZESTORETIC har inga biverkningar som är speciella för detta kombinationsläkemedel observerats. Biverkningar som har inträffat har begränsats till de som tidigare har rapporterats med lisinopril eller hydroklortiazid.
De vanligaste kliniska biverkningarna i kontrollerade prövningar (inklusive öppna förlängningar) med någon kombination av lisinopril och hydroklortiazid var: yrsel (7,5 %), huvudvärk (5,2 %), hosta (3,9 %), trötthet (3,7 %) och ortostatiska effekter (3,2 %) som alla var vanligare än hos placebobehandlade patienter. I allmänhet var negativa upplevelser milda och övergående till sin natur, men se VARNINGAR angioödem och överdriven hypotoni eller synkope. Avbrytande av behandlingen på grund av biverkningar krävdes hos 4,4 % av patienterna, främst på grund av yrsel, hosta, trötthet och muskelkramper.
Biverkningar som inträffade hos mer än en procent av patienterna som behandlades med lisinopril plus hydroklortiazid i kontrollerade kliniska prövningar visas nedan.
Procent av patienterna i kontrollerade studier
Kliniska biverkningar som inträffade hos 0,3 % till 1,0 % av patienterna i kontrollerade prövningar och sällsynta, allvarliga, möjligen läkemedelsrelaterade händelser som rapporterats i marknadsföringserfarenhet, listas nedan:
Kroppen som helhet: Bröstsmärtor, buksmärtor, synkope, obehag i bröstet, feber, trauma, virusinfektion. Kardiovaskulär: Palpitation, ortostatisk hypotoni. Matsmältningskanalen: Mag-tarmkramper, muntorrhet, förstoppning, halsbränna. Muskuloskeletala: Ryggsmärta, axelvärk, knäsmärta, ryggbristning, myalgi, fotvärk. Nervös/psykiatrisk: Minskad libido, svindel, depression, somnolens. Andningsvägar: Förkylning, nästäppa, influensa, bronkit, svalgsmärta, dyspné, lungtäppa, kronisk bihåleinflammation, allergisk rinit, svalgbesvär. Hud: Rodnad, klåda, hudinflammation, diafores, kutant pseudolymfom. Särskilda sinnen: Suddig syn, tinnitus, otalgi. Urogenital: Urinvägsinfektion.
Angioödem: Angioödem i ansikte, extremiteter, läppar, tunga, glottis och/eller struphuvud har rapporterats (se VARNINGAR ).
I sällsynta fall har intestinalt angioödem rapporterats efter marknadsföring.
Hypotoni: I kliniska prövningar inträffade biverkningar relaterade till hypotoni enligt följande: hypotoni (1,4 %), ortostatisk hypotoni (0,5 %), andra ortostatiska effekter (3,2 %). Dessutom inträffade synkope hos 0,8 % av patienterna (se VARNINGAR ).
Hosta: Ser FÖRSIKTIGHETSÅTGÄRDER - Hosta .
Resultat från kliniska laboratorietest
Serumelektrolyter
(Ser FÖRSIKTIGHETSÅTGÄRDER ).
Kreatinin, Blod Urea Kväve
Mindre reversibla ökningar av ureakväve i blodet och serumkreatinin observerades hos patienter med essentiell hypertoni som behandlades med ZESTORETIC. Mer markanta ökningar har också rapporterats och var mer benägna att inträffa hos patienter med njurartärstenos (se FÖRSIKTIGHETSÅTGÄRDER ).
Serum Urinsyra, Glukos, Magnesium, Kolesterol, Triglycerider och Kalcium
(Ser FÖRSIKTIGHETSÅTGÄRDER ).
Hemoglobin och hematokrit
Små minskningar av hemoglobin och hematokrit (genomsnittliga minskningar på cirka 0,5 g % respektive 1,5 volymprocent) förekom ofta hos hypertonipatienter som behandlades med ZESTORETIC 5 mg men var sällan av klinisk betydelse om inte en annan orsak till anemi existerade samtidigt. I kliniska prövningar avbröt 0,4 % av patienterna behandlingen på grund av anemi.
Leverfunktionstester
I sällsynta fall har förhöjda leverenzymer och/eller serumbilirubin inträffat. (Ser VARNINGAR , Leversvikt ).
Andra biverkningar som har rapporterats med de enskilda komponenterna listas nedan:
Lisinopril
I kliniska prövningar sågs även biverkningar som inträffade med lisinopril med ZESTORETIC. Dessutom, och sedan lisinopril har marknadsförts, har följande biverkningar rapporterats med lisinopril och bör betraktas som potentiella biverkningar för ZESTORETIC: Kroppen som helhet: Anafylaktoida reaktioner (se VARNINGAR , Anafylaktoida reaktioner under membranexponering ), sjukdomskänsla, ödem, ansiktsödem, smärta, bäckensmärta, flanksmärta, frossa; Kardiovaskulär: Hjärtstopp, hjärtinfarkt eller cerebrovaskulär olycka, möjligen sekundärt till överdriven hypotoni hos högriskpatienter (se VARNINGAR , Hypotoni ), lungemboli och infarkt, försämring av hjärtsvikt, arytmier (inklusive takykardi, ventrikulär takykardi, förmakstakykardi, förmaksflimmer, bradykardi och för tidiga kammarsammandragningar), angina pectoris, övergående ischemiska attacker, nocturnoxis, sänkt blodtryck, perifera ödem, vaskulit; Matsmältningskanalen: Pankreatit, hepatit (hepatocellulär eller kolestatisk gulsot) (se VARNINGAR , Leversvikt ), gastrit, anorexi, flatulens, ökad salivutsöndring; Endokrin: Diabetes mellitus, olämplig antidiuretisk hormonsekretion; Hematologiska: Sällsynta fall av benmärgsdepression, hemolytisk anemi, leukopeni/neutropeni och trombocytopeni har rapporterats där ett orsakssamband till lisinopril inte kan uteslutas; Metaboliskt: Gikt, viktminskning, uttorkning, vätskeöverbelastning, viktökning; Muskuloskeletala: Artrit, artralgi, nacksmärta, höftsmärta, ledvärk, bensmärta, armsmärta, ländryggen; Nervsystemet/psykiatrisk: Ataxi, minnesstörning, tremor, sömnlöshet, stroke, nervositet, förvirring, perifer neuropati (t.ex. parestesi, dysestesi), spasm, hypersomni, irritabilitet; humörförändringar (inklusive depressiva symtom); hallucinationer; Andningsvägar: Maligna lungneoplasmer, hemoptys, lungödem, lunginfiltrat, bronkospasm, astma, pleurautgjutning, lunginflammation, eosinofil pneumonit, väsande andning, ortopné, smärtsam andning, näsblod, laryngit, bihåleinflammation, normalinflammation; Hud: Urtikaria, alopeci, herpes zoster, ljuskänslighet, hudskador, hudinfektioner, pemfigus, erytem, psoriasis, sällsynta fall av andra allvarliga hudreaktioner, inklusive toxisk epidermal nekrolys och Stevens-Johnsons syndrom (kausalt samband har inte fastställts); Särskilda sinnen: Synförlust, dubbelsidighet, fotofobi, smakförändring, luktstörning; Urogenital: Akut njursvikt, oliguri, anuri, uremi, progressiv azotemi, njurdysfunktion (se FÖRSIKTIGHETSÅTGÄRDER och DOSERING OCH ADMINISTRERING ), pyelonefrit, dysuri, bröstsmärtor.
Diverse
Ett symtomkomplex har rapporterats som kan innefatta en positiv ANA, en förhöjd erytrocytsedimentationshastighet, artralgi/artrit, myalgi, feber, vaskulit, eosinofili och leukocytos. Utslag, ljuskänslighet eller andra dermatologiska manifestationer kan förekomma ensamma eller i kombination med dessa symtom.
Hydroklortiazid
Kroppen som helhet: Svaghet; Matsmältningskanalen: Anorexi, magirritation, kramper, gulsot (intrahepatisk kolestatisk gulsot) (se VARNINGAR , Leversvikt ), pankreatit, sialoadenit, förstoppning; Hematologiska: Leukopeni, agranulocytos, trombocytopeni, aplastisk anemi, hemolytisk anemi; Muskuloskeletala: Muskelspasm; Nervsystemet/psykiatrisk: Rastlöshet; Njur: Njursvikt, nedsatt njurfunktion, interstitiell nefrit (se VARNINGAR ); Hud: Erythema multiforme inklusive Stevens-Johnsons syndrom, exfoliativ dermatit inklusive toxisk epidermal nekrolys, alopeci; Särskilda sinnen: Xanthopsia; Överkänslighet: Purpura, ljuskänslighet, urtikaria, nekrotiserande angiit (vaskulit och kutan vaskulit), andnöd inklusive pneumonit och lungödem, anafylaktiska reaktioner.
LÄKEMEDELSINTERAKTIONER
Lisinopril
Hypotension -patienter på diuretikaterapi
Patienter på diuretika och särskilt de som nyligen påbörjat diuretikabehandling kan ibland uppleva en överdriven sänkning av blodtrycket efter att behandlingen med lisinopril påbörjats. Risken för hypotensiva effekter med lisinopril kan minimeras genom att antingen avbryta diuretikumet eller öka saltintaget innan behandling med lisinopril påbörjas. Om det är nödvändigt att fortsätta med diuretikumet, påbörja behandlingen med lisinopril med en dos på 5 mg dagligen och ge noggrann medicinsk övervakning efter den initiala dosen i minst två timmar och tills blodtrycket har stabiliserats i minst en ytterligare timme (se VARNINGAR , och DOSERING OCH ADMINISTRERING ). När ett diuretikum läggs till behandlingen av en patient som får lisinopril, observeras vanligtvis en ytterligare antihypertensiv effekt (se DOSERING OCH ADMINISTRERING ).
Icke-steroida antiinflammatoriska medel inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare)
Hos äldre patienter, volymbrist (inklusive de som får diuretikabehandling), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med ACE-hämmare, inklusive lisinopril, resultera i försämring av njurfunktionen inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som får lisinopril och NSAID-behandling.
Den antihypertensiva effekten av ACE-hämmare, inklusive lisinopril, kan försvagas av NSAID.
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, hyperkalemi och förändringar i njurfunktion (inklusive akut njursvikt) jämfört med monoterapi.
VA NEPHRON-studien inkluderade 1448 patienter med typ 2-diabetes, förhöjt urin-albuminto-kreatininförhållande och minskad uppskattad glomerulär filtrationshastighet (GFR 30 till 89,9 ml/min), randomiserade dem till lisinopril eller placebo på en bakgrund av losartanbehandling och följde dem under en median av 2,2 år. Patienter som fick kombinationen losartan och lisinopril fick ingen ytterligare fördel jämfört med monoterapi för den kombinerade endpointen av minskning av GFR, njursjukdom i sluttillståndet eller död, men upplevde en ökad incidens av hyperkalemi och akut njurskada jämfört med monoterapigruppen .
Undvik i allmänhet kombinerad användning av RAS-hämmare, övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på ZESTORETIC och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med ZESTORETIC till patienter med diabetes. Undvik användning av aliskiren med ZESTORETIC 5 mg till patienter med nedsatt njurfunktion (GFR
Andra ombud
Lisinopril har använts samtidigt med nitrater och/eller digoxin utan tecken på kliniskt signifikanta negativa interaktioner. Inga betydelsefulla kliniskt viktiga farmakokinetiska interaktioner inträffade när lisinopril användes samtidigt med propranolol, digoxin eller hydroklortiazid. Närvaron av mat i magen förändrar inte biotillgängligheten av lisinopril.
Medel som ökar serumkalium
Lisinopril dämpar kaliumförlust orsakad av diuretika av tiazidtyp. Användning av lisinopril med kaliumsparande diuretika (t.ex. spironolakton, eplerenon, triamteren eller amilorid), kaliumtillskott eller kaliuminnehållande saltersättningsmedel kan leda till signifikanta ökningar av serumkalium. Om samtidig användning av dessa medel är indicerad, på grund av påvisad hypokalemi, bör de därför användas med försiktighet och med frekvent övervakning av serumkalium.
Litium
Litiumtoxicitet har rapporterats hos patienter som får litium samtidigt med läkemedel som orsakar eliminering av natrium, inklusive ACE-hämmare. Litiumtoxicitet var vanligtvis reversibel vid utsättning av litium och ACE-hämmare. Det rekommenderas att serumlitiumnivåer övervakas ofta om lisinopril administreras samtidigt med litium.
mTOR (däggdjur Target Of Rapamycin) hämmare
Patienter som får samtidig behandling med ACE-hämmare och mTOR-hämmare (t.ex. temsirolimus, sirolimus, everolimus) kan löpa ökad risk för angioödem. (ser VARNINGAR )
Neprilysin-hämmare
Patienter som samtidigt tar neprilysinhämmare kan löpa ökad risk för angioödem. (ser VARNINGAR )
Hydroklortiazid
När de administreras samtidigt kan följande läkemedel interagera med tiaziddiuretika.
Alkohol, barbiturater eller narkotika -potentiering av ortostatisk hypotoni kan förekomma.
Antidiabetika (orala medel och insulin) -Dosjustering av det antidiabetiska läkemedlet kan behövas.
Andra antihypertensiva läkemedel -additiv effekt eller potentiering.
Kolestyramin och kolestipolhartser -Absorptionen av hydroklortiazid försämras i närvaro av anjonbytarhartser. Enstaka doser av antingen kolestyramin- eller kolestipolhartser binder hydroklortiaziden och minskar dess absorption från mag-tarmkanalen med upp till 85 % respektive 43 %.
Kortikosteroider, ACTH -förstärkt elektrolytutarmning, särskilt hypokalemi.
Pressoraminer (t.ex. noradrenalin) -möjligt minskat svar på pressoraminer men inte tillräckligt för att utesluta deras användning.
Skelettmuskelavslappnande medel, icke-depolariserande (t.ex. tubokurarin) -möjlig ökad lyhördhet för muskelavslappnande medel.
Litium -Bör i allmänhet inte ges tillsammans med diuretika. Diuretika minskar det renala clearance av litium och ökar risken för litiumtoxicitet. Se bipacksedeln för litiumpreparat före användning av sådana preparat med ZESTORETIC.
Icke-steroida antiinflammatoriska läkemedel Hos vissa patienter kan administrering av icke-steroida antiinflammatoriska medel minska de diuretiska, natriuretiska och antihypertensiva effekterna av loop-, kaliumsparande och tiaziddiuretika. Därför, när ZESTORETIC och icke-steroida antiinflammatoriska medel används samtidigt, bör patienten observeras noggrant för att avgöra om den önskade effekten av ZESTORETIC 5 mg uppnås.
Guld
Nitritoidreaktioner (symtom inkluderar rodnad i ansiktet, illamående, kräkningar och hypotoni) har rapporterats i sällsynta fall hos patienter i behandling med injicerbart guld (natriumaurotiomalat) och samtidig behandling med ACE-hämmare inklusive ZESTORETIC.
VARNINGAR
Lisinopril
Anafylaktoida och möjligen relaterade reaktioner
Förmodligen eftersom angiotensinomvandlande enzymhämmare påverkar metabolismen av eikosanoider och polypeptider, inklusive endogent bradykinin, kan patienter som får ACE-hämmare (inklusive ZESTORETIC) utsättas för en mängd olika biverkningar, några av dem allvarliga.
Huvud Och Nacke Angioödem
Angioödem i ansikte, extremiteter, läppar, tunga, glottis och/eller struphuvud har rapporterats hos patienter som behandlats med angiotensinomvandlande enzymhämmare, inklusive lisinopril. Detta kan inträffa när som helst under behandlingen. ACE-hämmare har associerats med en högre frekvens av angioödem hos svarta än hos icke-svarta patienter. ZESTORETIC 12,5gmg bör omedelbart avbrytas och lämplig behandling och övervakning bör tillhandahållas tills fullständig och ihållande upplösning av tecken och symtom har inträffat. Även i de fall där svullnad av endast tungan är inblandad, utan andningsbesvär, kan patienter behöva långvarig observation eftersom behandling med antihistaminer och kortikosteroider kanske inte är tillräcklig. I mycket sällsynta fall har dödsfall rapporterats på grund av angioödem i samband med larynxödem eller tungödem. Patienter med inblandning av tungan, glottis eller struphuvudet kommer sannolikt att uppleva luftvägsobstruktion, särskilt de som tidigare haft luftvägskirurgi. Om tungan, struphuvudet eller struphuvudet är involverat, vilket sannolikt orsakar luftvägsobstruktion, bör subkutan adrenalinlösning 1:1000 (0,3 mL till 0,5 mL) och/eller nödvändiga åtgärder för att säkerställa en fri luftväg omedelbart tillhandahållas (se BIVERKNINGAR) .
Patienter som får samtidig behandling med ACE-hämmare och mTOR-hämmare (t.ex. temsirolimus, sirolimus, everolimus) eller en neprilysinhämmare kan löpa ökad risk för angioödem (se FÖRSIKTIGHETSÅTGÄRDER ).
Intestinalt angioödem
Intestinalt angioödem har rapporterats hos patienter som behandlats med ACE-hämmare. Dessa patienter fick buksmärtor (med eller utan illamående eller kräkningar); i vissa fall fanns det ingen tidigare historia av ansiktsangioödem och C-1-esterasnivåerna var normala. Angioödem diagnostiserades genom procedurer inklusive CT-skanning av buken eller ultraljud, eller vid operation, och symtomen försvann efter att ha stoppat ACE-hämmaren. Intestinalt angioödem bör inkluderas i differentialdiagnosen för patienter på ACE-hämmare med buksmärtor.
Patienter med en historia av angioödem som inte är relaterat till behandling med ACE-hämmare kan löpa ökad risk för angioödem när de får en ACE-hämmare (se INDIKATIONER och KONTRAINDIKATIONER ).
Anafylaktoida reaktioner under desensibilisering
Två patienter som genomgick desensibiliserande behandling med hymenopteragift samtidigt som de fick ACE-hämmare fick livshotande anafylaktoida reaktioner.
Hos samma patienter undveks dessa reaktioner när ACE-hämmare tillfälligt hölls in, men de återkom vid oavsiktlig återinsättning.
Anafylaktoida reaktioner under membranexponering
Tiazidinnehållande kombinationsprodukter rekommenderas inte till patienter med allvarlig njurfunktionsnedsättning. Plötsliga och potentiellt livshotande anafylaktoida reaktioner har rapporterats hos vissa patienter som dialyserats med högflödesmembran (t.ex. AN69®**) och behandlats samtidigt med en ACE-hämmare. Hos sådana patienter måste dialys avbrytas omedelbart och aggressiv behandling för anafylaktoida reaktioner måste inledas. Symtomen har inte lindrats av antihistaminer i dessa situationer. Hos dessa patienter bör man överväga att använda en annan typ av dialysmembran eller en annan klass av antihypertensiva medel. Anafylaktoida reaktioner har också rapporterats hos patienter som genomgår lågdensitetslipoproteinaferes med dextransulfatabsorption.
Hypotoni och relaterade effekter
Överdriven hypotoni sågs sällan hos okomplicerade hypertonipatienter men är en möjlig konsekvens av lisinopril-användning hos personer med salt-/volymutarmning, såsom de som behandlats kraftigt med diuretika eller patienter i dialys (se LÄKEMEDELSINTERAKTIONER och NEGATIVA REAKTIONER ).
Synkope har rapporterats hos 0,8 procent av patienterna som fått ZESTORETIC. Hos patienter med hypertoni som fick enbart lisinopril var incidensen av synkope 0,1 procent. Den totala incidensen av synkope kan minskas genom korrekt titrering av de enskilda komponenterna (se LÄKEMEDELSINTERAKTIONER , NEGATIVA REAKTIONER och DOSERING OCH ADMINISTRERING ).
Hos patienter med svår kongestiv hjärtsvikt, med eller utan associerad njurinsufficiens, har överdriven hypotoni observerats och kan vara associerad med oliguri och/eller progressiv azotemi, och i sällsynta fall med akut njursvikt och/eller död. På grund av det potentiella blodtrycksfallet hos dessa patienter bör behandlingen påbörjas under mycket noggrann medicinsk övervakning. Sådana patienter bör följas noga under de första två veckorna av behandlingen och närhelst dosen av lisinopril och/eller diuretikum ökas. Liknande överväganden gäller för patienter med ischemisk hjärt- eller cerebrovaskulär sjukdom hos vilka ett alltför kraftigt blodtrycksfall kan resultera i en hjärtinfarkt eller cerebrovaskulär olycka.
Om hypotoni uppstår ska patienten placeras i ryggläge och vid behov få en intravenös infusion av normal koksaltlösning. Ett övergående hypotensivt svar är inte en kontraindikation för ytterligare doser som vanligtvis kan ges utan svårighet när blodtrycket har ökat efter volymexpansion.
Leukopeni/Neutropeni/Agranulocytos
En annan angiotensinomvandlande enzymhämmare, kaptopril, har visat sig orsaka agranulocytos och benmärgsdepression, sällan hos okomplicerade patienter men oftare hos patienter med nedsatt njurfunktion, särskilt om de också har en kollagenkärlsjukdom. Tillgängliga data från kliniska prövningar av lisinopril är otillräckliga för att visa att lisinopril inte orsakar agranulocytos i liknande takt. Marknadsföringserfarenhet har visat på sällsynta fall av leukopeni/neutropeni och benmärgsdepression där ett orsakssamband till lisinopril inte kan uteslutas. Regelbunden övervakning av antalet vita blodkroppar hos patienter med kollagenkärlsjukdom och njursjukdom bör övervägas.
Leversvikt
sällsynta fall har ACE-hämmare associerats med ett syndrom som börjar med kolestatisk gulsot eller hepatit och utvecklas till fulminant levernekros och (ibland) död. Mekanismen för detta syndrom är inte förstått. Patienter som får ACE-hämmare och som utvecklar gulsot eller markant förhöjda leverenzymer bör avbryta behandlingen med ACE-hämmare och få lämplig medicinsk uppföljning.
Fostertoxicitet
Graviditetskategori D
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt behandlingen med ZESTORETIC så snart som möjligt. Dessa negativa utfall är vanligtvis förknippade med användning av dessa läkemedel under andra och tredje trimestern av graviditeten. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. Lämplig hantering av maternell hypertoni under graviditeten är viktig för att optimera resultaten för både mor och foster.
det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar reninangiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret. Utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Om oligohydramnios observeras, avbryt behandlingen med ZESTORETIC, såvida det inte anses vara livräddande för modern. Fostertest kan vara lämpligt, baserat på graviditetsveckan. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada. Övervaka noggrant spädbarn med historia av exponering in utero för ZESTORETIC för hypotoni, oliguri och hyperkalemi. (Ser FÖRSIKTIGHETSÅTGÄRDER, Pediatrisk användning ).
Inga teratogena effekter av lisinopril sågs i studier på gravida råttor, möss och kaniner. På en mg/kg-basis var de använda doserna upp till 625 gånger (i möss), 188 gånger (i råttor) och 0,6 gånger (i kaniner) den maximala rekommenderade dosen för människor.
Lisinopril och hydroklortiazid
Teratogenicitetsstudier utfördes på möss och råttor med upp till 90 mg/kg/dag av lisinopril (56 gånger den maximala rekommenderade humana dosen) i kombination med 10 mg/kg/dag hydroklortiazid (2,5 gånger den maximala rekommenderade humana dosen). Maternalla eller fostertoxiska effekter sågs inte hos möss med kombinationen. Hos råttor inträffade minskad viktökning hos modern och minskad fostervikt ner till 3/10 mg/kg/dag (den lägsta testade dosen). Förenat med den minskade fostervikten var en fördröjning av fostrets förbening. Den minskade fostervikten och fördröjningen av fostrets förbening sågs inte hos djur med saltlösning som fick 90/10 mg/kg/dag.
Vid användning under graviditet, under andra och tredje trimestern, kan ACE-hämmare orsaka skador och till och med dödsfall för fostret under utveckling. När graviditet upptäcks, avbryt behandlingen med ZESTORETIC 5mg så snart som möjligt ( Se Lisinopril, Fostertoxicitet ).
Hydroklortiazid
Akut närsynthet och sekundär vinkelstängningsglaukom
Hydroklortiazid, en sulfonamid, kan orsaka en idiosynkratisk reaktion, vilket resulterar i akut övergående närsynthet och akut vinkelglaukom. Symtomen inkluderar akut uppkomst av minskad synskärpa eller ögonsmärta och uppträder vanligtvis inom timmar till veckor efter läkemedelsstart. Obehandlad akut vinkelglaukom kan leda till permanent synförlust. Den primära behandlingen är att avbryta behandlingen med hydroklortiazid så snabbt som möjligt. Snabba medicinska eller kirurgiska behandlingar kan behöva övervägas om det intraokulära trycket förblir okontrollerat. Riskfaktorer för att utveckla akut stängningsvinkelglaukom kan inkludera en historia av sulfonamid- eller penicillinallergi.
Teratogena effekter
Reproduktionsstudier på kanin, mus och råtta vid doser upp till 100 mg/kg/dag (50 gånger humandosen) visade inga tecken på yttre abnormiteter hos fostret på grund av hydroklortiazid. Hydroklortiazid som gavs i en tvåkullsstudie på råttor i doser på 4 mg/kg/dag till 5,6 mg/kg/dag (ungefär 1 till 2 gånger den vanliga dagliga dosen för människor) försämrade inte fertiliteten eller gav födelseavvikelser hos avkomman. Tiazider passerar placentabarriären och uppträder i navelsträngsblod.
Icke-ratogena effekter
Dessa kan inkludera fetal eller neonatal gulsot, trombocytopeni och eventuellt har andra biverkningar inträffat hos vuxna.
Hydroklortiazid
Tiazider ska användas med försiktighet vid svår njursjukdom. Hos patienter med njursjukdom kan tiazider utlösa azotemi. Kumulativa effekter av läkemedlet kan utvecklas hos patienter med nedsatt njurfunktion.
Tiazider bör användas med försiktighet till patienter med nedsatt leverfunktion eller progressiv leversjukdom, eftersom mindre förändringar av vätske- och elektrolytbalansen kan utlösa leverkoma.
Känslighetsreaktioner kan förekomma hos patienter med eller utan en historia av allergi eller bronkialastma.
Möjligheten för exacerbation eller aktivering av systemisk lupus erythematosus har rapporterats.
Litium ska i allmänhet inte ges tillsammans med tiazider (se LÄKEMEDELSINTERAKTIONER , Lisinopril och hydroklortiazid ).
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Lisinopril
Aortastenos/hypertrofisk kardiomyopati
Liksom alla vasodilatorer bör lisinopril ges med försiktighet till patienter med obstruktion i utflödeskanalen från vänster kammare.
Nedsatt njurfunktion
Som en konsekvens av hämning av renin-angiotensin-aldosteronsystemet kan förändringar i njurfunktionen förväntas hos känsliga individer. Hos patienter med svår kongestiv hjärtsvikt vars njurfunktion kan bero på aktiviteten hos renin-angiotensin-aldosteronsystemet, kan behandling med angiotensinomvandlande enzymhämmare, inklusive lisinopril, vara associerad med oliguri och/eller progressiv azotemi och i sällsynta fall med akut njurfunktion. misslyckande och/eller dödsfall.
Hos hypertonipatienter med unilateral eller bilateral njurartärstenos kan ökningar av ureakväve i blodet och serumkreatinin förekomma. Erfarenhet av en annan angiotensinomvandlande enzymhämmare tyder på att dessa ökningar vanligtvis är reversibla vid utsättande av lisinopril och/eller diuretikabehandling. Hos sådana patienter bör njurfunktionen övervakas under de första veckorna av behandlingen.
Vissa hypertonipatienter utan uppenbar redan existerande njurkärlsjukdom har utvecklat ökningar av blodurea och serumkreatinin, vanligtvis mindre och övergående, särskilt när lisinopril har getts samtidigt med ett diuretikum. Detta är mer sannolikt att inträffa hos patienter med redan existerande nedsatt njurfunktion. Dosminskning av lisinopril och/eller utsättande av diuretikum kan behövas.
Utvärdering av den hypertensiva patienten bör alltid inkludera bedömning av njurfunktionen (se DOSERING OCH ADMINISTRERING).
Hyperkalemi
kliniska prövningar inträffade hyperkalemi (serumkalium större än 5,7 mEq/L) hos cirka 1,4 procent av hypertensiva patienter som behandlades med lisinopril plus hydroklortiazid. I de flesta fall var dessa isolerade värden som försvann trots fortsatt behandling. Hyperkalemi var inte en orsak till att behandlingen avbröts. Riskfaktorer för utveckling av hyperkalemi inkluderar njurinsufficiens, diabetes mellitus och samtidig användning av kaliumsparande diuretika, kaliumtillskott och/eller kaliuminnehållande saltersättningsmedel. Hyperkalemi kan orsaka allvarliga, ibland dödliga, arytmier. ZESTORETIC ska användas med försiktighet, om alls, med dessa medel och med frekvent övervakning av serumkalium (se LÄKEMEDELSINTERAKTIONER ).
Hosta
Förmodligen på grund av hämningen av nedbrytningen av endogent bradykinin, har ihållande icke-produktiv hosta rapporterats med alla ACE-hämmare, och den försvinner nästan alltid efter avslutad behandling. ACE-hämmare-inducerad hosta bör beaktas vid differentialdiagnos av hosta.
Kirurgi/anestesi
Hos patienter som genomgår större operationer eller under anestesi med medel som ger hypotoni, kan lisinopril blockera angiotensin II-bildning sekundärt till kompensatorisk reninfrisättning. Om hypotoni uppstår och anses bero på denna mekanism kan den korrigeras genom volymexpansion.
Hydroklortiazid
Periodisk bestämning av serumelektrolyter för att upptäcka eventuell elektrolytobalans bör utföras med lämpliga intervall.
Alla patienter som får tiazidbehandling bör observeras för kliniska tecken på vätske- eller elektrolytbalans: nämligen hyponatremi, hypokloremisk alkalos och hypokalemi. Serum- och urinelektrolytbestämningar är särskilt viktiga när patienten kräks för mycket eller får parenterala vätskor. Varningstecken eller symtom på vätske- och elektrolytbalans, oavsett orsak, inkluderar muntorrhet, törst, svaghet, letargi, dåsighet, rastlöshet, förvirring, kramper, muskelsmärtor eller kramper, muskeltrötthet, hypotoni, oliguri, takykardi och gastrointestinala störningar som illamående och kräkningar.
Hypokalemi kan utvecklas, särskilt vid snabb diures, när allvarlig cirros är närvarande eller efter långvarig behandling.
Interferens med adekvat oralt elektrolytintag kommer också att bidra till hypokalemi. Hypokalemi kan orsaka hjärtarytmi och kan också sensibilisera eller överdriva hjärtats reaktion på de toxiska effekterna av digitalis (t.ex. ökad ventrikulär irritabilitet). Eftersom lisinopril minskar produktionen av aldosteron, dämpar samtidig behandling med lisinopril den diuretika-inducerade kaliumförlusten (se LÄKEMEDELSINTERAKTIONER , Agenter som ökar serumkalium ).
Även om eventuellt kloridunderskott i allmänhet är lindrigt och vanligtvis inte kräver specifik behandling, förutom under extraordinära omständigheter (som vid leversjukdom eller njursjukdom), kan kloridersättning krävas vid behandling av metabolisk alkalos.
Utspädd hyponatremi kan förekomma hos ödematösa patienter i varmt väder; lämplig terapi är vattenbegränsning snarare än administrering av salt förutom i sällsynta fall då hyponatremin är livshotande. Vid faktisk saltutarmning är lämplig ersättning den terapi man väljer.
Hyperurikemi kan uppstå eller frank gikt kan utlösas hos vissa patienter som får tiazidbehandling.
Hos diabetiker kan dosjusteringar av insulin eller orala hypoglykemiska medel behövas. Hyperglykemi kan förekomma med tiaziddiuretika. Sålunda kan latent diabetes mellitus bli manifest under tiazidbehandling.
De antihypertensiva effekterna av läkemedlet kan förstärkas hos postsympatiktomipatienter.
Om progressivt nedsatt njurfunktion blir uppenbart överväg att avbryta eller avbryta diuretikabehandling.
Tiazider har visats öka urinutsöndringen av magnesium; detta kan resultera i hypomagnesemi.
Tiazider kan minska kalciumutsöndringen i urinen. Tiazider kan orsaka intermittent och lätt förhöjning av serumkalcium i frånvaro av kända störningar i kalciummetabolismen. Markerad hyperkalcemi kan vara tecken på dold hyperparatyreos. Tiazider bör avbrytas innan tester för bisköldkörtelfunktion utförs.
Ökade kolesterol- och triglyceridnivåer kan vara associerade med tiaziddiuretikabehandling.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Lisinopril och hydroklortiazid
Lisinopril i kombination med hydroklortiazid var inte mutagent i ett mikrobiellt mutagent test med Salmonella typhimurium (Ames-test) eller Escherichia coli med eller utan metabolisk aktivering eller i en framåtmutationsanalys med lungceller från kinesisk hamster. Lisinopril och hydroklortiazid gav inte DNA-enkelsträngsbrott i en in vitro alkalisk eluering av råtta-hepatocytanalys. Dessutom gav det inga ökningar av kromosomavvikelser i ett in vitro-test i kinesisk hamsters äggstocksceller eller i en in vivo-studie på benmärg hos mus.
Lisinopril
Det fanns inga tecken på en tumörframkallande effekt när lisinopril administrerades under 105 veckor till han- och honråttor i doser upp till 90 mg/kg/dag (cirka 56 eller 9 gånger* den maximala dagliga dosen för människor, baserat på kroppsvikt och kroppsyta område, respektive). Det fanns inga tecken på karcinogenicitet när lisinopril administrerades under 92 veckor till (han- och honmöss) i doser upp till 135 mg/kg/dag (cirka 84 gånger* den maximala rekommenderade dagliga dosen för människor). Denna dos var 6,8 gånger den maximala humana dosen baserat på kroppsyta hos möss.
*Beräkningar antar en människovikt på 50 kg och en kroppsyta på 1,62 m2.
Lisinopril var inte mutagent i Ames mikrobiella mutagentest med eller utan metabolisk aktivering. Det var också negativt i en framåtmutationsanalys med lungceller från kinesisk hamster. Lisinopril producerade inga enkelsträngade DNA-brott i en in vitro alkalisk elueringsanalys av råttas hepatocyt. Dessutom gav lisinopril inga ökningar av kromosomavvikelser i ett in vitro-test i kinesisk hamsters äggstocksceller eller i en in vivo-studie på benmärg hos mus.
Det fanns inga negativa effekter på reproduktionsförmågan hos han- och honråttor som behandlats med upp till 300 mg/kg/dag av lisinopril. Denna dos är 188 gånger och 30 gånger den maximala dagliga dosen för människor baserat på mg/kg respektive mg/m2.
Hydroklortiazid
Tvååriga utfodringsstudier på möss och råttor utförda under överinseende av National Toxicology Program (NTP) avslöjade inga tecken på cancerframkallande potential hos hydroklortiazid hos möss av honkön (vid doser upp till cirka 600 mg/kg/dag) eller hos hanar. och honråttor (vid doser på upp till cirka 100 mg/kg/dag). Dessa doser är 150 gånger och 12 gånger för möss och 25 gånger och 4 gånger för råttor den maximala mänskliga dagliga dosen baserat på mg/kg respektive mg/m2. NTP fann dock tvetydiga bevis för hepatokarcinogenicitet hos möss av hankön.
Hydroklortiazid var inte genotoxiskt in vitro i Ames mutagenicitetsanalysen av Salmonella typhimurium-stammarna TA 98, TA 100, TA 1535, TA 1537 och TA 1538 och i äggstockstestet för kinesisk hamster (CHO) för kromosomavvikelser med användning av vibrationer, eller könscellskromosomer från mus, benmärgskromosomer från kinesisk hamster och genen Drosophila könsbundna recessiva dödliga egenskaper. Positiva testresultat erhölls endast i in vitro CHO Sister Chromatid Exchange (klastogenicitet) och i muslymfomcellsanalyser (mutagenicitet), med användning av koncentrationer av hydroklortiazid från 43 mcg/mL till 1300 mcg/mL, och i Aspergillus nidulans nondisjunction-analysen vid en ospecificerad koncentration.
Hydroklortiazid hade inga negativa effekter på fertiliteten hos möss och råttor av något kön i studier där dessa arter exponerades, via sin diet, för doser på upp till 100 mg/kg respektive 4 mg/kg före befruktningen och under hela graviditeten . Hos möss är denna dos 25 gånger och 2 gånger den maximala dagliga humandosen baserat på mg/kg respektive mg/m2. Hos råttor är denna dos 1 gånger och 0,2 gånger den maximala dagliga humandosen baserat på mg/kg respektive mg/m2.
Ammande mödrar
Det är inte känt om lisinopril utsöndras i modersmjölk. Mjölk från lakterande råttor innehåller dock radioaktivitet efter administrering av 14C lisinopril. I en annan studie fanns lisinopril i råttmjölk i nivåer som liknade plasmanivåer hos moderdjuren. Tiazider förekommer i modersmjölk. På grund av risken för allvarliga biverkningar hos ammande spädbarn från ACE-hämmare och hydroklortiazid, bör ett beslut fattas om att avbryta amningen och/eller avbryta behandlingen med ZESTORETIC 12,5 g, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Nyfödda med en historia av exponering i livmodern för ZESTORETIC
Om oliguri eller hypotoni uppstår, rikta uppmärksamheten mot stöd av blodtryck och njurperfusion. Utbytestransfusioner eller dialys kan krävas som ett sätt att vända hypotoni och/eller ersätta störd njurfunktion. Lisinopril, som passerar placentan, har avlägsnats från neonatal cirkulation genom peritonealdialys med viss klinisk fördel och kan teoretiskt tas bort genom utbytestransfusion, även om det inte finns någon erfarenhet av det senare förfarandet.
Säkerhet och effektivitet hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Kliniska studier av ZESTORETIC mg inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling.
Detta läkemedel är känt för att väsentligen utsöndras via njurarna, och risken för toxiska reaktioner på detta läkemedel kan vara större hos patienter med nedsatt njurfunktion. Eftersom äldre patienter är mer benägna att ha nedsatt njurfunktion, bör försiktighet iakttas vid val av dos. Utvärdering av den hypertensiva patienten bör alltid inkludera bedömning av njurfunktionen.
ÖVERDOS
Ingen specifik information finns tillgänglig om behandling av överdosering med ZESTORETIC. Behandlingen är symtomatisk och stödjande. Behandling med ZESTORETIC 12,5 g ska avbrytas och patienten observeras noggrant. Föreslagna åtgärder inkluderar framkallande av kräkning och/eller magsköljning, och korrigering av uttorkning, elektrolytobalans och hypotoni genom etablerade procedurer.
Lisinopril
Efter en enkel oral dos på 20 g/kg inträffade ingen dödlighet hos råttor och dödsfall inträffade hos en av 20 möss som fick samma dos. Den mest sannolika manifestationen av överdosering skulle vara hypotoni, för vilken den vanliga behandlingen skulle vara intravenös infusion av normal koksaltlösning.
Lisinopril kan avlägsnas genom hemodialys (se VARNINGAR , Anafylaktoid reaktion under membranexponering ).
Hydroklortiazid
Oral administrering av en enstaka oral dos på 10 g/kg till möss och råttor var inte dödlig. De vanligaste tecknen och symtomen som observeras är de som orsakas av elektrolytbrist (hypokalemi, hypokloremi, hyponatremi) och uttorkning till följd av överdriven diures. Om digitalis också har administrerats kan hypokalemi accentuera hjärtarytmier.
KONTRAINDIKATIONER
ZESTORETIC 12,5 g är kontraindicerat till patienter som är överkänsliga mot denna produkt och till patienter med angioödem i anamnesen relaterat till tidigare behandling med en angiotensinkonverterande enzymhämmare och till patienter med ärftligt eller idiopatiskt angioödem. På grund av hydroklortiazidkomponenten är denna produkt kontraindicerad hos patienter med anuri eller överkänslighet mot andra sulfonamidhärledda läkemedel.
ZESTORETIC 12,5 g är kontraindicerat i kombination med en neprilysinhämmare (t.ex. sacubitril). Administrera inte ZESTORETIC 5 mg inom 36 timmar efter byte till eller från sacubitril/valsartan, en neprilysinhämmare (se VARNINGAR ).
Administrera inte aliskiren samtidigt med ZESTORETIC till patienter med diabetes (se LÄKEMEDELSINTERAKTIONER ).
KLINISK FARMAKOLOGI
Lisinopril och hydroklortiazid
Som ett resultat av dess diuretiska effekter ökar hydroklortiazid plasmareninaktiviteten, ökar aldosteronsekretionen och minskar serumkalium. Administrering av lisinopril blockerar reninangiotensinaldosteronaxeln och tenderar att vända den kaliumförlust som är förknippad med diuretikumet.
I kliniska studier var graden av blodtryckssänkning som sågs med kombinationen av lisinopril och hydroklortiazid ungefär additiv. Kombinationen ZESTORETIC 10-12,5 fungerade lika bra på svarta och vita patienter. Kombinationerna ZESTORETIC 20-12.5 och ZESTORETIC 20-25 verkade något mindre effektiva hos svarta patienter, men relativt få svarta patienter studerades. Hos de flesta patienter bibehölls den antihypertensiva effekten av ZESTORETIC i minst 24 timmar.
en randomiserad, kontrollerad jämförelse var den genomsnittliga antihypertensiva effekten av ZESTORETIC 20-12.5 och ZESTORETIC 20-25 liknande, vilket tyder på att många patienter som svarar adekvat på den senare kombinationen kan kontrolleras med ZESTORETIC 20-12.5 (se DOSERING OCH ADMINISTRERING ).
Samtidig administrering av lisinopril och hydroklortiazid har liten eller ingen effekt på biotillgängligheten av båda läkemedlen. Kombinationstabletten är bioekvivalent med samtidig administrering av de separata enheterna.
Lisinopril
Handlingsmekanism
Lisinopril hämmar angiotensinomvandlande enzym (ACE) hos människor och djur. ACE är ett peptidyldipeptidas som katalyserar omvandlingen av angiotensin I till den kärlsammandragande substansen, angiotensin II. Angiotensin II stimulerar också utsöndringen av aldosteron från binjurebarken. Hämning av ACE resulterar i minskad plasmaangiotensin II vilket leder till minskad vasopressoraktivitet och till minskad aldosteronsekretion. Den senare minskningen kan resultera i en liten ökning av serumkalium. Avlägsnande av angiotensin II negativ feedback på reninsekretion leder till ökad plasmareninaktivitet. Hos hypertonipatienter med normal njurfunktion som behandlades med enbart lisinopril i upp till 24 veckor var den genomsnittliga ökningen av serumkalium mindre än 0,1 mEq/L; dock hade cirka 15 procent av patienterna ökningar större än 0,5 mEq/L och cirka sex procent hade en minskning större än 0,5 mEq/L. I samma studie visade patienter som behandlades med lisinopril plus ett tiaziddiuretikum i huvudsak ingen förändring i serumkalium (se FÖRSIKTIGHETSÅTGÄRDER ).
ACE är identisk med kininas, ett enzym som bryter ned bradykinin. Huruvida ökade nivåer av bradykinin, en potent vasodepressorpeptid, spelar en roll för de terapeutiska effekterna av lisinopril återstår att klarlägga.
Medan mekanismen genom vilken lisinopril sänker blodtrycket tros främst vara suppression av renin-angiotensin-aldosteronsystemet, är lisinopril antihypertensivt även hos patienter med lågt reninhypertoni. Även om lisinopril var antihypertensivt i alla studerade raser, hade svarta hypertonipatienter (vanligtvis en låg-reninhypertensiv population) ett lägre genomsnittligt svar på lisinopril monoterapi än icke-svarta patienter.
Farmakokinetik och metabolism
Efter oral administrering av lisinopril uppnås maximala serumkoncentrationer inom cirka 7 timmar. Sjunkande serumkoncentrationer uppvisar en förlängd terminal fas som inte bidrar till läkemedelsackumulering. Denna terminala fas representerar troligen mättbar bindning till ACE och är inte proportionell mot dosen. Lisinopril verkar inte vara bundet till andra serumproteiner.
Lisinopril metaboliseras inte och utsöndras oförändrat helt i urinen. Baserat på urinåtervinning är den genomsnittliga absorptionsgraden av lisinopril cirka 25 procent, med stor variation mellan individer (6 % till 60 %) vid alla testade doser (5 mg till 80 mg). Lisinoprilabsorptionen påverkas inte av närvaron av mat i mag-tarmkanalen.
Vid upprepad dosering uppvisar lisinopril en effektiv ackumuleringshalveringstid på 12 timmar.
Nedsatt njurfunktion minskar elimineringen av lisinopril, som huvudsakligen utsöndras via njurarna, men denna minskning blir kliniskt viktig först när den glomerulära filtrationshastigheten är under 30 ml/min. Över denna glomerulära filtrationshastighet är eliminationshalveringstiden lite förändrad. Med större försämring ökar dock topp- och dalnivåerna av lisinopril, tiden till toppkoncentrationen ökar och tiden för att uppnå steady state förlängs. Äldre patienter har i genomsnitt (ungefär fördubblats) högre blodnivåer och area under plasmakoncentrationstidskurvan (AUC) än yngre patienter (se DOSERING OCH ADMINISTRERING ). I en farmakokinetisk multipeldosstudie på äldre jämfört med unga hypertensiva patienter som använde kombinationen lisinopril/hydroklortiazid ökade AUC med cirka 120 % för lisinopril och cirka 80 % för hydroklortiazid hos äldre patienter. Lisinopril kan avlägsnas genom hemodialys.
Studier på råttor tyder på att lisinopril passerar blod-hjärnbarriären dåligt. Flera doser av lisinopril hos råttor resulterar inte i ackumulering i några vävnader; mjölk från lakterande råttor innehåller dock radioaktivitet efter administrering av 14C lisinopril. Genom helkroppsautoradiografi hittades radioaktivitet i moderkakan efter administrering av märkt läkemedel till gravida råttor, men ingen hittades hos fostret.
Farmakodynamik
Administrering av lisinopril till patienter med hypertoni resulterar i en sänkning av liggande och stående blodtryck i ungefär samma utsträckning utan kompensatorisk takykardi. Symtomatisk postural hypotoni observeras vanligtvis inte även om den kan förekomma och bör förutses hos patienter med volym och/eller saltbrist (se VARNINGAR ).
Hos de flesta studerade patienter sågs insättande av antihypertensiv aktivitet en timme efter oral administrering av en individuell dos av lisinopril, med maximal blodtryckssänkning med sex timmar.
Hos vissa patienter kan det krävas två till fyra veckors behandling för att uppnå optimal blodtryckssänkning.
Vid rekommenderade enstaka dagliga doser har antihypertensiva effekter bibehållits i minst 24 timmar efter dosering, även om effekten vid 24 timmar var väsentligt mindre än effekten sex timmar efter dosering.
De antihypertensiva effekterna av lisinopril har fortsatt under långtidsbehandling. Plötsligt utsättande av lisinopril har inte associerats med en snabb ökning av blodtrycket; inte heller med ett betydande överskridande av blodtrycket före behandling.
hemodynamiska studier på patienter med essentiell hypertoni åtföljdes blodtryckssänkningen av en minskning av perifert arteriellt motstånd med liten eller ingen förändring i hjärtminutvolym och hjärtfrekvens. I en studie på nio hypertonipatienter, efter administrering av lisinopril, fanns en ökning av det genomsnittliga njurblodflödet som inte var signifikant. Data från flera små studier är inkonsekventa med avseende på effekten av lisinopril på glomerulär filtrationshastighet hos hypertonipatienter med normal njurfunktion, men tyder på att förändringar, om några, inte är stora.
Hos patienter med renovaskulär hypertoni har lisinopril visat sig vara väl tolererat och effektivt för att kontrollera blodtrycket (se FÖRSIKTIGHETSÅTGÄRDER ).
Hydroklortiazid
Mekanismen för den antihypertensiva effekten av tiazider är okänd. Tiazider påverkar vanligtvis inte normalt blodtryck.
Hydroklortiazid är ett diuretikum och blodtryckssänkande medel. Det påverkar den distala renala tubulära mekanismen för elektrolytreabsorption. Hydroklortiazid ökar utsöndringen av natrium och klorid i ungefär motsvarande mängder. Natriures kan åtföljas av viss förlust av kalium och bikarbonat.
Efter oral användning börjar diuresen inom två timmar, toppar efter cirka fyra timmar och varar cirka 6 till 12 timmar.
Hydroklortiazid metaboliseras inte utan elimineras snabbt via njurarna. När plasmanivåerna har följts under minst 24 timmar har plasmahalveringstiden observerats variera mellan 5,6 och 14,8 timmar. Minst 61 procent av den orala dosen elimineras oförändrad inom 24 timmar. Hydroklortiazid passerar placenta men inte blod-hjärnbarriären.
PATIENTINFORMATION
Angioödem
Angioödem, inklusive larynxödem, kan uppträda när som helst under behandling med angiotensinomvandlande enzymhämmare, inklusive ZESTORETIC. Patienter bör rådas och uppmanas att omedelbart rapportera alla tecken eller symtom som tyder på angioödem (svullnad av ansikte, extremiteter, ögon, läppar, tunga, svårigheter att svälja eller andas) och att inte ta mer läkemedel förrän de har rådfrågat den förskrivande läkaren.
Symtomatisk hypotoni
Patienter bör varnas för att rapportera yrsel, särskilt under de första dagarna av behandlingen. Om faktisk synkope inträffar ska patienterna uppmanas att avbryta läkemedlet tills de har rådfrågat den förskrivande läkaren.
Alla patienter bör varnas för att överdriven svettning och uttorkning kan leda till ett överdrivet blodtrycksfall på grund av minskad vätskevolym. Andra orsaker till volymutarmning som kräkningar eller diarré kan också leda till ett blodtrycksfall; patienter bör rådas att rådfråga sin läkare.
Hyperkalemi
Patienter bör uppmanas att inte använda saltersättningsmedel som innehåller kalium utan att rådfråga sin läkare.
Leukopeni/Neutropeni
Patienterna ska uppmanas att omedelbart rapportera alla tecken på infektion (t.ex. halsont, feber) som kan vara tecken på leukopeni/neutropeni.
Graviditet
Kvinnliga patienter i fertil ålder bör informeras om konsekvenserna av exponering för ZESTORETIC under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Patienter bör uppmanas att rapportera graviditeter till sin läkare så snart som möjligt.
NOTERA: Som med många andra läkemedel är vissa råd till patienter som behandlas med ZESTORETIC 12,5 g berättigade. Denna information är avsedd att hjälpa till med säker och effektiv användning av detta läkemedel. Det är inte ett avslöjande av alla möjliga negativa eller avsedda effekter.
