Aceon 2mg, 4mg, 8mg Perindopril Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Aceon 4mg och hur används det?
Aceon 8mg är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni) och stabil kranskärlssjukdom (CAD). Aceon kan användas ensamt eller tillsammans med andra läkemedel.
Aceon tillhör en klass av läkemedel som kallas ACE-hämmare.
Det är inte känt om Aceon är säkert och effektivt hos barn.
Vilka är de möjliga biverkningarna av Aceon 4mg?
Aceon kan orsaka allvarliga biverkningar inklusive:
- nässelfeber,
- svårt att andas,
- svullnad av ansikte, läppar, tunga eller svalg,
- svaghet,
- långsam eller oregelbunden hjärtrytm,
- svimning,
- illamående,
- kräkningar,
- aptitlöshet,
- buksmärtor,
- gulfärgning av ögon eller hud (gulsot),
- mörk urin, och
- svår yrsel
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Aceon 2mg inkluderar:
- yrsel,
- yrsel,
- trötthet och
- rethosta
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Aceon. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
- När graviditet upptäcks, avbryt behandlingen med ACEON 4mg så snart som möjligt. VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER
- Läkemedel som verkar direkt på renin-angiotensinsystemet kan orsaka skador och dödsfall för fostret under utveckling. VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER
BESKRIVNING
ACEON® (perindopril erbumin) tabletter innehåller tert-butylaminsaltet av perindopril, etylestern av en icke-sulfhydrylangiotensin-omvandlande enzym (ACE)-hämmare. Perindopril erbumin beskrivs kemiskt som (2S,3DS,7DS)-1-[(S)-N-[(S)-1-karboxi-butyl]alanyl]hexahydro-2-indolinkarboxylsyra, 1-etylester, förening med tert-butylamin (1:1). Dess molekylformel är C19H32N2O5C4H11N. Dess strukturformel är:
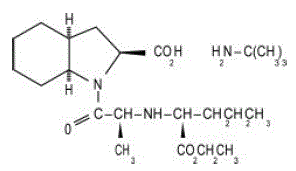
Perindopril erbumin är ett vitt, kristallint pulver med en molekylvikt på 368,47 (fri syra) eller 441,61 (saltform). Det är fritt lösligt i vatten (60 % w/w), alkohol och kloroform.
Perindopril är den fria syraformen av perindopril erbumin, är en prodrug och metaboliseras in vivo genom hydrolys av estergruppen för att bilda perindoprilat, den biologiskt aktiva metaboliten.
ACEON finns i styrkorna 2 mg, 4 mg och 8 mg för oral administrering. Förutom perindopril erbumin innehåller varje tablett följande inaktiva ingredienser: kolloidal kiseldioxid (hydrofob), laktos, magnesiumstearat och mikrokristallin cellulosa. 4 mg och 8 mg tabletterna innehåller också järnoxid.
INDIKATIONER
Hypertoni
ACEON är indicerat för behandling av patienter med essentiell hypertoni. ACEON kan användas ensamt eller ges tillsammans med andra klasser av antihypertensiva, särskilt tiaziddiuretika.
Stabil kranskärlssjukdom
ACEON 8mg är indicerat för behandling av patienter med stabil kranskärlssjukdom för att minska risken för kardiovaskulär mortalitet eller icke-fatal hjärtinfarkt. ACEON kan användas med konventionell behandling för hantering av kranskärlssjukdom, såsom blodplättsdämpande, antihypertensiv eller lipidsänkande behandling.
DOSERING OCH ADMINISTRERING
Hypertoni
Användning hos okomplicerade hypertensiva patienter
Hos patienter med essentiell hypertoni är den rekommenderade initialdosen 4 mg en gång dagligen. Dosen kan titreras efter behov till maximalt 16 mg per dag. Det vanliga underhållsdosintervallet är 4 mg till 8 mg administrerat som en daglig dos eller i två uppdelade doser.
Användning hos äldre patienter
Den rekommenderade initiala dagliga dosen av ACEON 4 mg för äldre är 4 mg dagligen, givet i en eller två uppdelade doser. Erfarenheten av ACEON är begränsad hos äldre vid doser som överstiger 8 mg. Doser över 8 mg bör administreras med noggrann blodtrycksövervakning och dostitrering [se Användning i specifika populationer ].
Använd med diuretika
Hos patienter som för närvarande behandlas med ett diuretikum kan symtomatisk hypotoni uppstå efter den initiala dosen av ACEON. Överväg att minska dosen av diuretikum innan du börjar med ACEON [se LÄKEMEDELSINTERAKTIONER ].
Stabil kranskärlssjukdom
Hos patienter med stabil kranskärlssjukdom ska ACEON 4 mg ges i en startdos på 4 mg en gång dagligen i 2 veckor och sedan ökas efter tolerans till en underhållsdos på 8 mg en gång dagligen. Till äldre patienter (över 70 år) ska ACEON ges som en dos på 2 mg en gång dagligen under den första veckan, följt av 4 mg en gång dagligen under den andra veckan och 8 mg en gång dagligen för underhållsdos om det tolereras.
Dosjustering vid nedsatt njurfunktion och dialys
Eliminationen av perindoprilat är minskad hos patienter med nedsatt njurfunktion. ACEON rekommenderas inte till patienter med kreatininclearance
HUR LEVERERAS
Doseringsformer och styrkor
Tabletterna är avlånga med ett skåra på ena sidan.
2 mg tablett är vit och präglad på sidan utan skåror med "ACN 2".
4 mg tablett är rosa och präglad på sidan utan skåror med "ACN 4".
8 mg tablett är lax och präglad på sidan utan skåror med "ACN 8".
Förvaring Och Hantering
Tabletterna är avlånga med ett skåra på ena sidan.
Förvaras oåtkomligt för barn.
Förvara vid kontrollerad rumstemperatur 20° till 25°C (68° till 77°F) [se USP]. Skydda mot fukt.
För ytterligare information, ring vår medicinska kommunikationsavdelning kostnadsfritt på 888-985-7657.
Tillverkad av: Patheon Pharmaceuticals, Inc. Cincinnati, OH 45237 USA. Reviderad: sep 2017
BIEFFEKTER
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Erfarenhet av kliniska prövningar
Följande biverkningar diskuteras på andra ställen i märkningen:
- Anafylaktoida reaktioner, inklusive angioödem [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypotoni [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Neutropeni och agranulocytos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Nedsatt njurfunktion [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hyperkalemi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hosta [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Hypertoni
ACEON 4mg har utvärderats för säkerhet hos cirka 3 400 patienter med hypertoni i amerikanska och utländska kliniska prövningar. De data som presenteras här är baserade på resultat från de 1 417 ACEON-behandlade patienterna som deltog i de amerikanska kliniska prövningarna. Över 220 av dessa patienter behandlades med ACEON® (perindopril erbumin) i minst ett år.
placebokontrollerade kliniska prövningar i USA var incidensen av för tidig utsättning av behandlingen på grund av biverkningar 6,5 % hos patienter som behandlades med ACEON 2 mg och 6,7 % hos patienter som behandlades med placebo. De vanligaste orsakerna var hosta, huvudvärk, asteni och yrsel.
Bland 1 012 patienter i placebokontrollerade amerikanska studier var den totala frekvensen av rapporterade biverkningar likartad hos patienter som behandlades med ACEON och hos de som behandlades med placebo (cirka 75 % i varje grupp). De enda biverkningarna vars incidens på ACEON 4 mg var minst 2 % högre än på placebo var hosta (12 % mot 4,5 %) och ryggsmärtor (5,8 % mot 3,1 %).
Yrsel rapporterades inte oftare i perindoprilgruppen (8,2 %) än i placebogruppen (8,5 %), men sannolikheten ökade med dosen, vilket tyder på ett orsakssamband med perindopril.
Stabil kranskärlssjukdom
Perindopril har utvärderats för säkerhet i EUROPA, en dubbelblind, placebokontrollerad studie på 12 218 patienter med stabil kranskärlssjukdom. Den totala frekvensen av utsättningar var cirka 22 % för läkemedel och placebo. De vanligaste medicinska orsakerna till behandlingsavbrott som var vanligare med perindopril än placebo var hosta, läkemedelsintolerans och hypotoni.
Erfarenhet efter marknadsföring
Frivilliga rapporter om biverkningar hos patienter som tar ACEON som har mottagits sedan marknadsintroduktionen och som är av okänt orsakssamband till ACEON 8mg inkluderar: hjärtstillestånd, eosinofil pneumonit, neutropeni/agranulocytos, pancytopeni, anemi (inklusive hemolytisk och aopeni), trombocytisk, trombocytisk lunginflammation. njursvikt, nefrit, leversvikt, gulsot (hepatocellulär eller kolestatisk), symtomatisk hyponatremi, bullös pemfigoid, pemfigus, akut pankreatit, fall, psoriasis, exfoliativ dermatit och ett syndrom som kan inkludera: artralgi/artrit, sekretor, vaskulit, vaskulit , hudutslag eller andra dermatologiska manifestationer, en positiv antinukleär antikropp (ANA), leukocytos, eosinofili eller en förhöjd erytrocytsedimentationshastighet (ESR).
Resultat från kliniska laboratorietest
Hematologi
Små minskningar av hemoglobin och hematokrit förekommer ofta hos hypertonipatienter som behandlas med ACEON 8mg, men är sällan av klinisk betydelse. I kontrollerade kliniska prövningar avbröts ingen patient från behandlingen på grund av utvecklingen av anemi. Leukopeni (inklusive neutropeni) observerades hos 0,1 % av patienterna i amerikanska kliniska prövningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Leverfunktionstester
Förhöjningar av ALAT (1,6 % ACEON mot 0,9 % placebo) och ASAT (0,5 % ACEON 2 mg mot 0,4 % placebo) har observerats i placebokontrollerade kliniska prövningar. Förhöjningarna var i allmänhet milda och övergående och försvann efter avslutad behandling.
LÄKEMEDELSINTERAKTIONER
Diuretika
Patienter på diuretika, och särskilt de som nyligen påbörjats, kan ibland uppleva en överdriven blodtryckssänkning efter påbörjad behandling med ACEON. Möjligheten för hypotensiva effekter kan minimeras genom att antingen minska dosen av eller avbryta diuretikumet eller öka saltintaget innan behandling med perindopril påbörjas. Om diuretikabehandlingen inte kan ändras, ge noggrann medicinsk övervakning med den första dosen av ACEON, i minst två timmar och tills blodtrycket har stabiliserats i ytterligare en timme [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hastigheten och omfattningen av perindoprils absorption och eliminering påverkas inte av samtidig diuretika. Biotillgängligheten av perindoprilat reducerades dock av diuretika, och detta var associerat med en minskning av ACE-hämningen i plasma.
Kaliumtillskott och kaliumsparande diuretika
ACEON 8mg kan öka serumkalium på grund av dess potential att minska aldosteronproduktionen. Användning av kaliumsparande diuretika (spironolakton, amilorid, triamteren och andra), kaliumtillskott eller andra läkemedel som kan öka serumkalium (indometacin, heparin, ciklosporin och andra) kan öka risken för hyperkalemi. Därför, om samtidig användning av sådana medel är indicerad, övervaka patientens serumkalium ofta.
Litium
Ökat serumlitium och symtom på litiumtoxicitet har rapporterats hos patienter som samtidigt behandlas med litium och ACE-hämmare. Frekvent övervakning av serumlitiumkoncentrationen rekommenderas. Användning av ett diuretikum kan ytterligare öka risken för litiumtoxicitet.
Guld
Nitritoidreaktioner (symtom inkluderar rodnad i ansiktet, illamående, kräkningar och hypotoni) har rapporterats i sällsynta fall hos patienter i behandling med injicerbart guld (natriumaurotiomalat) och samtidig behandling med ACE-hämmare inklusive ACEON.
Digoxin
En kontrollerad farmakokinetisk studie har inte visat någon effekt på plasmakoncentrationen av digoxin vid samtidig administrering med ACEON, men en effekt av digoxin på plasmakoncentrationen av perindopril/perindoprilat har inte uteslutits.
Gentamicin
Djurdata har antydt möjligheten till interaktion mellan perindopril och gentamicin. Detta har dock inte undersökts i humanstudier.
Icke-steroida antiinflammatoriska medel inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare)
Hos äldre patienter, volymbrist (inklusive de som får diuretikabehandling), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med ACE-hämmare, inklusive perindopril, resultera i försämring av njurfunktionen. inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som får perindopril och NSAID-behandling.
Den antihypertensiva effekten av ACE-hämmare, inklusive perindopril, kan försvagas av NSAID inklusive selektiva COX-2-hämmare.
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, hyperkalemi och förändringar i njurfunktion (inklusive akut njursvikt) jämfört med monoterapi. De flesta patienter som får kombinationen av två RAS-hämmare får ingen ytterligare fördel jämfört med monoterapi. Undvik i allmänhet kombinerad användning av RAS-hämmare. Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på ACEON 2 mg och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med ACEON 8mg till patienter med diabetes. Undvik användning av aliskiren med ACEON 2mg hos patienter med nedsatt njurfunktion (GFR
mTOR-hämmare
Patienter som samtidigt tar mTOR-hämmare (däggdjursmålet för rapamycin) kan löpa ökad risk för angioödem [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Neprilysin-hämmare
Patienter som samtidigt tar neprilysinhämmare kan löpa ökad risk för angioödem. [ser VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Anafylaktoida och möjligen relaterade reaktioner
Förmodligen eftersom angiotensinomvandlande enzymhämmare påverkar metabolismen av eikosanoider och polypeptider, inklusive endogent bradykinin, kan patienter som får ACE-hämmare (inklusive ACEON) utsättas för en mängd olika biverkningar, några av dem allvarliga. Svarta patienter som får ACE-hämmare har en högre incidens av angioödem jämfört med icke-svarta.
Huvud Och Nacke Angioödem
Angioödem i ansikte, extremiteter, läppar, tunga, glottis eller struphuvud har rapporterats hos patienter som behandlats med ACE-hämmare, inklusive ACEON (0,1 % av patienterna som behandlats med ACEON i amerikanska kliniska prövningar). Angioödem i samband med involvering av tungan, glottis eller struphuvudet kan vara dödlig. I sådana fall ska du omedelbart avbryta behandlingen med ACEON och observera tills svullnaden försvinner. När inblandning av tungan, glottis eller struphuvudet sannolikt orsakar luftvägsobstruktion, administrera lämplig behandling, såsom subkutan epinefrinlösning 1:1000 (0,3 till 0,5 ml), omedelbart.
Patienter som samtidigt tar behandling med mTOR-hämmare (t.ex. temsirolimus) eller en neprilysinhämmare kan löpa ökad risk för angioödem [se LÄKEMEDELSINTERAKTIONER ].
Intestinalt angioödem
Intestinalt angioödem har rapporterats hos patienter som behandlats med ACE-hämmare. Dessa patienter fick buksmärtor (med eller utan illamående eller kräkningar); i vissa fall fanns det ingen tidigare historia av ansiktsangioödem och C-1-esterasnivåerna var normala. Angioödem diagnostiserades genom procedurer inklusive CT-skanning av buken eller ultraljud, eller vid operation, och symtomen försvann efter att ha stoppat ACE-hämmaren. Intestinalt angioödem bör inkluderas i differentialdiagnosen för patienter på ACE-hämmare med buksmärtor.
Hypotoni
ACEON 4mg kan orsaka symtomatisk hypotoni. ACEON har associerats med hypotoni hos 0,3 % av okomplicerade hypertonipatienter i placebokontrollerade studier i USA. Symtom relaterade till ortostatisk hypotoni rapporterades hos ytterligare 0,8 % av patienterna.
Symtomatisk hypotoni är mest sannolikt att uppträda hos patienter som har varit volym- eller saltbrist som ett resultat av långvarig diuretikabehandling, saltbegränsning i kosten, dialys, diarré eller kräkningar [se DOSERING OCH ADMINISTRERING ].
ACE-hämmare kan orsaka överdriven hypotoni och kan associeras med oliguri eller azotemi, och i sällsynta fall med akut njursvikt och död. Hos patienter med ischemisk hjärtsjukdom eller cerebrovaskulär sjukdom kan ett överdrivet blodtrycksfall resultera i en hjärtinfarkt eller en cerebrovaskulär olycka.
Hos patienter med risk för kraftig hypotoni bör behandling med ACEON påbörjas under mycket noggrann medicinsk övervakning. Patienterna bör följas noggrant under de första två veckorna av behandlingen och närhelst dosen av ACEON 2 mg och/eller diuretikum ökas.
Om överdriven hypotoni uppstår ska patienten omedelbart placeras i ryggläge och vid behov behandlas med en intravenös infusion av fysiologisk koksaltlösning. Behandling med ACEON 4 mg kan vanligtvis fortsätta efter återställande av volym och blodtryck.

Neutropeni/Agranulocytos
ACE-hämmare har associerats med agranulocytos och benmärgsdepression, oftast hos patienter med nedsatt njurfunktion, särskilt patienter med en kollagen kärlsjukdom såsom systemisk lupus erythematosus eller sklerodermi.
Fostertoxicitet
Graviditetskategori D
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt ACEON 4mg så snart som möjligt [se Användning i specifika populationer ].
Nedsatt njurfunktion
Som en konsekvens av hämning av renin-angiotensin-aldosteronsystemet kan förändringar i njurfunktionen förväntas hos känsliga individer. Njurfunktionen ska övervakas regelbundet hos patienter som får ACEON [se DOSERING OCH ADMINISTRERING ], [ser LÄKEMEDELSINTERAKTIONER ].
Hos patienter med svår kongestiv hjärtsvikt, där njurfunktionen kan bero på aktiviteten hos renin-angiotensinaldosteronsystemet, kan behandling med ACE-hämmare, inklusive ACEON, vara associerad med oliguri, progressiv azotemi och, i sällsynta fall, akut njursvikt och död.
Hos hypertonipatienter med unilateral eller bilateral njurartärstenos kan ökningar av ureakväve i blodet och serumkreatinin förekomma; vanligtvis reversibel vid utsättning av ACE-hämmaren. Hos sådana patienter bör njurfunktionen övervakas under de första veckorna av behandlingen.
Vissa ACEON-behandlade patienter har utvecklat mindre och övergående ökningar av ureakväve i blodet och serumkreatinin, särskilt hos de som samtidigt behandlas med ett diuretikum.
Hyperkalemi
Förhöjningar av serumkalium har observerats hos vissa patienter som behandlats med ACE-hämmare, inklusive ACEON. De flesta fall var isolerade enstaka värden som inte verkade vara kliniskt relevanta och som sällan var orsak till utsättning. Riskfaktorer för utveckling av hyperkalemi inkluderar njurinsufficiens, diabetes mellitus och samtidig användning av medel som kaliumsparande diuretika, kaliumtillskott och/eller kaliuminnehållande saltersättningsmedel [se LÄKEMEDELSINTERAKTIONER ].
Serumkalium bör övervakas regelbundet hos patienter som får ACEON.
Hosta
Förmodligen på grund av hämningen av nedbrytningen av endogent bradykinin, har ihållande icke-produktiv hosta rapporterats med alla ACE-hämmare, som vanligtvis försvinner efter avslutad behandling. Överväg ACE-hämmare-inducerad hosta vid differentialdiagnos av hosta.
Leversvikt
sällsynta fall har ACE-hämmare associerats med ett syndrom som börjar med kolestatisk gulsot och utvecklas till fulminant levernekros och ibland dödsfall. Mekanismen för detta syndrom är inte förstått. Patienter som får ACE-hämmare och som utvecklar gulsot eller markant förhöjda leverenzymer bör avbryta behandlingen med ACE-hämmare och få lämplig medicinsk uppföljning.
Kirurgi/anestesi
Hos patienter som genomgår operation eller under anestesi med medel som producerar hypotoni, kan ACEON blockera angiotensin II-bildning som annars skulle inträffa sekundärt till kompensatorisk reninfrisättning. Hypotoni som kan hänföras till denna mekanism kan korrigeras genom volymexpansion.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Cancerframkallande egenskaper
Inga tecken på karcinogen effekt observerades i studier på råttor och möss när perindopril administrerades i doser upp till 20 gånger (mg/kg) eller 2 till 4 gånger (mg/m2) den maximala föreslagna kliniska dosen (16 mg/dag) för 104 veckor.
Mutagenes
Ingen genotoxisk potential upptäcktes för ACEON, perindoprilat och andra metaboliter i olika undersökningar in vitro och in vivo, inklusive Ames-testet, Saccharomyces cerevisiae D4-testet, odlade humana lymfocyter, TK ± muslymfomanalys, mikrokärntest på mus och råtta och kinesisk hamster benmärgsanalys.
Nedsättning av fertilitet
Det fanns ingen meningsfull effekt på reproduktionsförmåga eller fertilitet hos råtta som gavs upp till 30 gånger (mg/kg) eller 6 gånger (mg/m2) den föreslagna maximala kliniska dosen av ACEON 2 mg under perioden av spermatogenes hos hanar eller oogenes och dräktighet hos honor.
Användning i specifika populationer
Graviditet
Graviditetskategori D [se LÅDA VARNING och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt behandlingen med ACEON så snart som möjligt. Dessa negativa utfall är vanligtvis förknippade med användning av dessa läkemedel under andra och tredje trimestern av graviditeten. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel.
Lämplig hantering av maternell hypertoni under graviditeten är viktig för att optimera resultaten för både mor och foster.
det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar renin-angiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret. Utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Om oligohydramnios observeras, avbryt behandlingen med ACEON 2mg, såvida det inte anses vara livräddande för modern. Fostertest kan vara lämpligt, baserat på graviditetsveckan. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada. Följ noga spädbarn med historia av exponering in utero för ACEON för hypotoni, oliguri och hyperkalemi [se Pediatrisk användning ].
Radioaktivitet kunde detekteras hos foster efter administrering av 14C-perindopril till dräktiga råttor.
Ammande mödrar
Mjölk från lakterande råttor innehöll radioaktivitet efter administrering av 14C-perindopril. Det är inte känt om perindopril utsöndras i modersmjölk. Eftersom många läkemedel utsöndras i bröstmjölk bör försiktighet iakttas när ACEON ges till ammande mödrar.
Pediatrisk användning
Nyfödda med en historia av exponering för ACEON i livmodern
Om oliguri eller hypotoni uppstår, rikta uppmärksamheten mot stöd av blodtryck och njurperfusion. Utbytestransfusioner eller dialys kan krävas som ett sätt att vända hypotoni och/eller ersätta störd njurfunktion. Perindopril, som passerar placentan, kan teoretiskt tas bort från neonatalcirkulationen på dessa sätt, men begränsad erfarenhet har inte visat att sådant avlägsnande är centralt för behandlingen av dessa spädbarn.
Säkerhet och effektivitet för ACEON 8mg hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Den genomsnittliga blodtryckseffekten av perindopril var något mindre hos patienter över 60 än hos yngre patienter, även om skillnaden inte var signifikant. Plasmakoncentrationer av både perindopril och perindoprilat ökade hos äldre patienter jämfört med koncentrationer hos yngre patienter. Inga biverkningar var tydligt ökade hos äldre patienter med undantag för yrsel och eventuellt hudutslag.
Börja med en låg dos och titrera långsamt vid behov. Övervaka för yrsel på grund av risk för fall.
Erfarenhet av ACEON 8 mg hos äldre patienter vid dagliga doser över 8 mg är begränsad.
Nedsatt njurfunktion
Dosjustering kan vara nödvändig hos patienter med nedsatt njurfunktion [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Biotillgängligheten av perindoprilat är ökad hos patienter med nedsatt leverfunktion [se KLINISK FARMAKOLOGI ].
ÖVERDOS
Hos djur var doser av perindopril upp till 2 500 mg/kg hos möss, 3 000 mg/kg hos råttor och 1 600 mg/kg hos hundar icke-dödliga. Tidigare erfarenheter var knappa men antydde att överdosering med andra ACE-hämmare också tolererades ganska väl av människor. Den mest sannolika manifestationen är hypotoni, och behandlingen bör vara symtomatisk och stödjande. Behandling med ACE-hämmare bör avbrytas och patienten bör observeras. Dehydrering, elektrolytobalans och hypotoni bör behandlas med etablerade procedurer.
Bland de rapporterade fallen av överdosering av perindopril behövde patienter som var kända för att ha intagit en dos på 80 mg till 120 mg assisterad ventilation och cirkulationsstöd. Ytterligare en patient utvecklade hypotermi, cirkulationsstopp och dog efter intag av upp till 180 mg perindopril. Interventionen för överdosering av perindopril kan kräva kraftfullt stöd.
Laboratoriebestämningar av serumnivåer av perindopril och dess metaboliter är inte allmänt tillgängliga, och sådana bestämningar har i alla händelser ingen etablerad roll vid hanteringen av överdosering av perindopril.
Det finns inga tillgängliga data som tyder på fysiologiska manövrar (t.ex. manövrar för att ändra pH i urinen) som kan påskynda elimineringen av perindopril och dess metaboliter. Perindopril kan avlägsnas genom hemodialys, med clearance på 52 ml/min för perindopril och 67 ml/min för perindoprilat.
Angiotensin II skulle förmodligen kunna fungera som en specifik antagonist-motgift vid sedimentering av överdosering av perindopril, men angiotensin II är i princip inte tillgänglig utanför spridda forskningsanläggningar. Eftersom den hypotensiva effekten av perindopril uppnås genom vasodilatation och effektiv hypovolemi, är det rimligt att behandla överdosering av perindopril genom infusion av normal koksaltlösning.
KONTRAINDIKATIONER
ACEON® (perindopril erbumin) är kontraindicerat hos patienter som är kända för att vara överkänsliga (inklusive angioödem) mot denna produkt eller mot någon annan ACE-hämmare. ACEON 4mg är också kontraindicerat hos patienter med ärftligt eller idiopatiskt angioödem.
Administrera inte aliskiren samtidigt med ACEON till patienter med diabetes. [ser LÄKEMEDELSINTERAKTIONER ]
ACEON är kontraindicerat i kombination med neprilysinhämmare (t.ex. sacubitril). Administrera inte ACEON 8mg inom 36 timmar efter byte till eller från sacubitril/valsartan, en neprilysinhämmare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
ACEON® (perindopril erbumin) är en prodrug för perindoprilat, som hämmar ACE hos människor och djur. Mekanismen genom vilken perindoprilat sänker blodtrycket tros främst vara hämning av ACE-aktivitet. ACE är ett peptidyldipeptidas som katalyserar omvandlingen av den inaktiva dekapeptiden, angiotensin I, till vasokonstriktorn, angiotensin II. Angiotensin II är en potent perifer vasokonstriktor, som stimulerar aldosteronsekretionen från binjurebarken och ger negativ feedback på reninsekretionen. Hämning av ACE resulterar i minskad plasmaangiotensin II, vilket leder till minskad vasokonstriktion, ökad plasmareninaktivitet och minskad aldosteronsekretion. Det senare resulterar i diures och natriures och kan vara associerat med en liten ökning av serumkalium.
ACE är identisk med kininas II, ett enzym som bryter ned bradykinin. Huruvida ökade nivåer av bradykinin, en potent vasodepressorpeptid, spelar en roll för de terapeutiska effekterna av ACEON 4mg återstår att utreda.
Medan den huvudsakliga mekanismen för perindopril vid blodtryckssänkning tros vara genom renin-angiotensinaldosteronsystemet, har ACE-hämmare viss effekt även vid uppenbar låg-reninhypertoni. Perindopril har studerats hos relativt få svarta patienter, vanligtvis en population med låg reninhalt, och det genomsnittliga svaret av diastoliskt blodtryck på perindopril var ungefär hälften av svaret hos icke-svarta patienter, ett fynd som överensstämmer med tidigare erfarenhet av andra ACE-hämmare.
Farmakodynamik
Efter administrering av perindopril hämmas ACE på ett dos- och blodkoncentrationsrelaterat sätt, med den maximala hämningen på 80 till 90 % som uppnås med 8 mg som kvarstår i 10 till 12 timmar. Tjugofyra timmars ACE-hämning är cirka 60 % efter dessa doser. Graden av ACE-inhibering som uppnås med en given dos verkar minska med tiden (ID50 ökar). Pressorsvaret på en angiotensin I-infusion reduceras av perindopril, men denna effekt är inte lika ihållande som effekten på ACE; det finns cirka 35 % hämning 24 timmar efter en 12 mg dos.
Farmakokinetik
Absorption
Oral administrering av ACEON resulterar i maximala plasmakoncentrationer som inträffar efter cirka 1 timme. Den absoluta orala biotillgängligheten av perindopril är cirka 75 %. Efter absorption hydrolyseras cirka 30 till 50 % av systemiskt tillgängligt perindopril till dess aktiva metabolit, perindoprilat, som har en genomsnittlig biotillgänglighet på cirka 25 %. Maximala plasmakoncentrationer av perindoprilat uppnås 3 till 7 timmar efter administrering av perindopril. Oral administrering av ACEON 8 mg tillsammans med mat minskar inte signifikant hastigheten eller omfattningen av perindoprilabsorption i förhållande till fastande tillstånd. Omfattningen av biotransformation av perindopril till den aktiva metaboliten, perindoprilat, minskas dock med cirka 43 %, vilket resulterar i en minskning av ACE-hämningskurvan i plasma med cirka 20 %, troligen kliniskt obetydlig. I kliniska prövningar administrerades perindopril i allmänhet utan fasta.
Med 4 mg, 8 mg och 16 mg doser av ACEON, ökar Cmax och AUC för perindopril och perindoprilat på ett dosproportionellt sätt efter både oral engångsdosering och vid steady-state under en multipeldosering en gång om dagen.
Distribution
Ungefär 60 % av cirkulerande perindopril är bundet till plasmaproteiner och endast 10 till 20 % av perindoprilat är bundet. Därför förväntas inte läkemedelsinteraktioner förmedlade genom effekter på proteinbindning.
Metabolism och eliminering
Efter oral administrering uppvisar perindopril farmakokinetik med flera fack inklusive ett djupt vävnadskompartment (ACE-bindningsställen). Den genomsnittliga halveringstiden för perindopril i samband med det mesta av dess eliminering är cirka 0,8 till 1 timme.
Perindopril metaboliseras i stor utsträckning efter oral administrering, med endast 4 till 12 % av dosen återfanns oförändrad i urinen. Sex metaboliter orsakade av hydrolys, glukuronidering och cyklisering via dehydrering har identifierats. Dessa inkluderar den aktiva ACE-hämmaren, perindoprilat (hydrolyserad perindopril), perindopril och perindoprilat glukuronider, dehydrerad perindopril och diastereoisomererna av dehydrerat perindoprilat. Hos människor verkar hepatiskt esteras vara ansvarigt för hydrolysen av perindopril.
Den aktiva metaboliten, perindoprilat, uppvisar också multikompartment farmakokinetik efter oral administrering av ACEON. Bildningen av perindoprilat sker gradvis med maximala plasmakoncentrationer mellan 3 och 7 timmar. Den efterföljande minskningen av plasmakoncentrationen visar en uppenbar genomsnittlig halveringstid på 3 till 10 timmar för majoriteten av elimineringen, med en förlängd terminal halveringstid på 30 till 120 timmar som ett resultat av långsam dissociation av perindoprilat från plasma/vävnad ACE-bindning webbplatser. Vid upprepad oral dosering en gång dagligen med perindopril ackumuleras perindoprilat cirka 1,5 till 2 gånger och uppnår steady state plasmanivåer inom 3 till 6 dagar. Clearance av perindoprilat och dess metaboliter är nästan uteslutande renalt.
Äldre
Plasmakoncentrationer av både perindopril och perindoprilat hos äldre patienter (över 70 år) är ungefär två gånger de som observerats hos yngre patienter, vilket återspeglar både ökad omvandling av perindopril till perindoprilat och minskad renal utsöndring av perindoprilat [se DOSERING OCH ADMINISTRERING och Användning i specifika populationer ].
Hjärtsvikt
Perindoprilatclearance reduceras hos patienter med kronisk hjärtsvikt, vilket resulterar i ett 40 % högre dosintervall AUC.
Nedsatt njurfunktion
Med perindoprildoser på 2 mg till 4 mg ökar perindoprilats AUC med minskad njurfunktion. Vid kreatininclearance på 30 till 80 ml/min är AUC ungefär dubbelt så högt som vid 100 ml/min. När kreatininclearance sjunker under 30 ml/min ökar AUC mer markant.
Hos ett begränsat antal studerade patienter varierade clearance av perindopril genom dialys från cirka 40 till 80 ml/min. Perindoprilatclearance genom dialys varierade från cirka 40 till 90 ml/min [se DOSERING OCH ADMINISTRERING ].
Nedsatt leverfunktion
Biotillgängligheten av perindoprilat är ökad hos patienter med nedsatt leverfunktion. Plasmakoncentrationer av perindoprilat hos patienter med nedsatt leverfunktion var cirka 50 % högre än de som observerades hos friska försökspersoner eller hypertonipatienter med normal leverfunktion.
Kliniska studier
Hypertoni
placebokontrollerade studier av perindopril monoterapi (2 mg till 16 mg en gång dagligen) hos patienter med ett medelblodtryck på cirka 150/100 mm Hg, hade 2 mg liten effekt, men doser på 4 mg till 16 mg sänkte blodtrycket. Doserna på 8 mg och 16 mg var omöjliga att särskilja och båda hade en större effekt än dosen på 4 mg. I dessa studier gav doser på 8 mg och 16 mg per dag liggande, dalvärde blodtryckssänkningar på 9 till 15/5 till 6 mm Hg. När dosering en gång dagligen och två gånger dagligen jämfördes, var doseringsregimen två gånger dagligen i allmänhet något överlägsen, men med inte mer än cirka 0,5 mm Hg till 1 mm Hg. Efter 2 mg till 16 mg doser av perindopril, var den lägsta genomsnittliga systoliska och diastoliska blodtryckseffekten cirka 75 till 100 % av toppeffekterna.
Perindoprils effekter på blodtrycket var liknande när det gavs ensamt eller på en bakgrund av 25 mg hydroklortiazid. Generellt sett inträdde effekten av perindopril omedelbart, med effekter som ökade något under flera veckor.
Formella interaktionsstudier av ACEON® (perindopril erbumin) har inte utförts med andra antihypertensiva medel än tiazider. Begränsad erfarenhet av kontrollerade och okontrollerade studier med samtidig administrering av ACEON 2mg med en kalciumkanalblockerare, ett loopdiuretikum eller trippelbehandling (betablockerare, vasodilator och ett diuretikum), tyder inte på några oväntade interaktioner. Generellt sett har ACE-hämmare mindre än additiva effekter när de ges tillsammans med beta-adrenerga blockerare, förmodligen för att båda delvis verkar genom renin-angiotensinsystemet.
I okontrollerade studier på patienter med insulinberoende diabetes verkade perindopril inte påverka den glykemiska kontrollen. Vid långvarig användning sågs ingen effekt på proteinutsöndringen i urinen hos dessa patienter.
Effekten av ACEON 4mg påverkades inte av sex och det var mindre effektivt hos svarta patienter än hos icke-svarta patienter. Hos äldre patienter (större än eller lika med 60 år) var den genomsnittliga blodtryckseffekten något mindre än hos yngre patienter, även om skillnaden inte var signifikant.
Stabil kranskärlssjukdom
Den europeiska studien på minskning av hjärthändelser med Perindopril vid stabil kranskärlssjukdom (EUROPA) var en multicenter, randomiserad, dubbelblind och placebokontrollerad studie utförd på 12 218 patienter som hade tecken på stabil kranskärlssjukdom utan klinisk hjärtsvikt. Patienterna hade tecken på kranskärlssjukdom dokumenterad av tidigare hjärtinfarkt mer än 3 månader före screening, koronar revaskularisering mer än 6 månader före screening, angiografiska tecken på stenos (minst 70 % förträngning av en eller flera större kranskärl) eller positiv stress test på män med en historia av bröstsmärtor. Efter en inkörningsperiod på 4 veckor under vilken alla patienter fick perindopril 2 mg till 8 mg, tilldelades patienterna slumpmässigt perindopril 8 mg en gång dagligen (n=6 110) eller matchande placebo (n=6 108). Den genomsnittliga uppföljningen var 4,2 år. Studien undersökte de långsiktiga effekterna av perindopril i tid till första händelsen av kardiovaskulär mortalitet, icke-fatal hjärtinfarkt eller hjärtstillestånd hos patienter med stabil kranskärlssjukdom.
Patienternas medelålder var 60 år; 85 % var män, 92 % tog trombocythämmare, 63 % tog β-blockerare och 56 % tog lipidsänkande behandling. EUROPA-studien visade att perindopril signifikant minskade den relativa risken för de primära endpointhändelserna (tabell 1). Denna gynnsamma effekt är till stor del hänförlig till en minskning av risken för icke-fatal hjärtinfarkt. Denna gynnsamma effekt av perindopril på det primära resultatet var uppenbar efter cirka ett års behandling (Figur 1). Resultatet var liknande för alla fördefinierade undergrupper efter ålder, underliggande sjukdom eller samtidig medicinering (Figur 2).
Figur 1. Tid till första förekomsten av primär ändpunkt 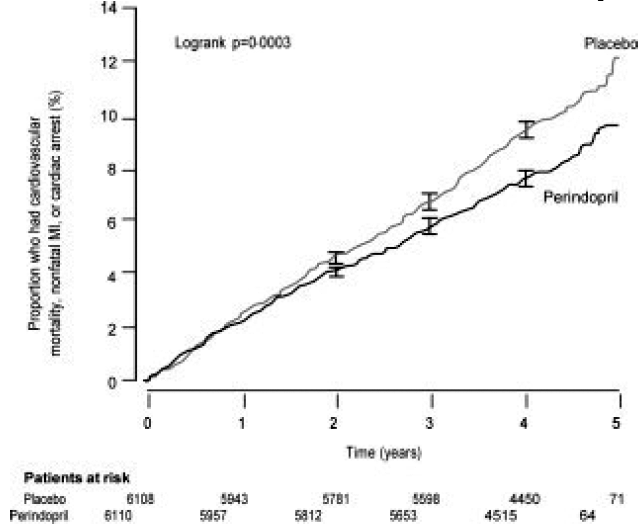
Figur 2. Fördelaktig effekt av perindoprilbehandling på primärt effektmått i fördefinierade undergrupper 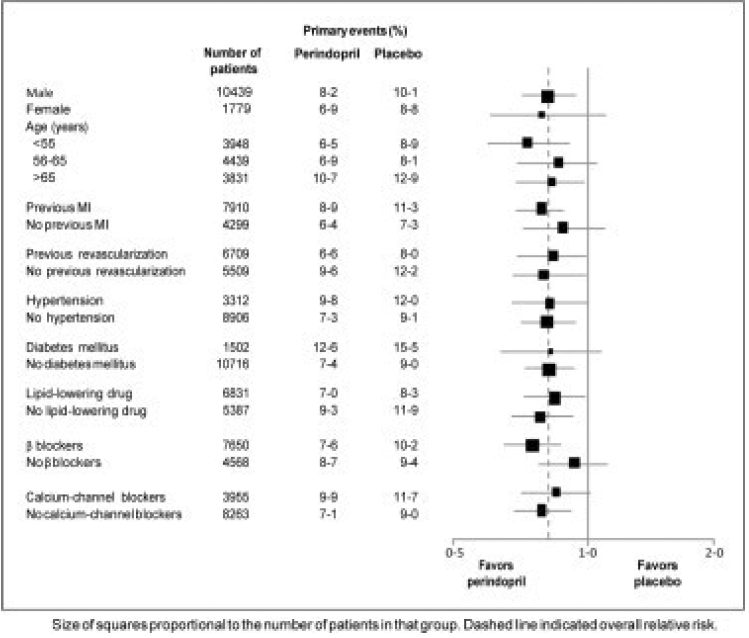
PATIENTINFORMATION
Kvinnliga patienter i fertil ålder bör informeras om konsekvenserna av exponering för ACEON 2 mg under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Patienter bör uppmanas att rapportera graviditeter till sin läkare så snart som möjligt.
Be patienterna att omedelbart rapportera alla tecken på infektion (t.ex. halsont, feber) som kan vara ett tecken på neutropeni.
