Hyzaar 12.5mg Hydrochlorothiazide Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Hyzaar och hur används det?
Hyzaar 12,5 mg är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni). Hyzaar kan användas ensamt eller tillsammans med andra läkemedel.
Hyzaar tillhör en klass av läkemedel som kallas ARB/HCTZ Combos.
Det är inte känt om Hyzaar är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Hyzaar 12,5 mg?
Hyzaar kan orsaka allvarliga biverkningar inklusive:
- yrsel,
- oregelbundna hjärtslag,
- ögonsmärta,
- synproblem,
- lite eller ingen urinering,
- snabb viktökning,
- svullnad i dina händer, fötter eller vrister,
- ledvärk,
- hudutslag på kinderna eller armarna som förvärras i solljus,
- ökad törst,
- ökad urinering,
- förvirring,
- kräkningar,
- förstoppning,
- träningsvärk,
- kramper i benen,
- allvarlig svaghet,
- domningar eller stickningar,
- förlust av rörelse, och
- känner sig nervös eller ostadig
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Hyzaar inkluderar:
- yrsel,
- ryggont, och
- förkylningssymtom (täppt näsa, nysningar, ont i halsen)
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Hyzaar. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
När graviditet upptäcks, avbryt HYZAAR så snart som möjligt. Läkemedel som verkar direkt på renin-angiotensinsystemet kan orsaka skador och dödsfall för fostret under utveckling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
BESKRIVNING
HYZAAR 50/12.5 (losartan kalium-hydroklortiazid), HYZAAR 100/12.5 (losartan kaliumhydroklortiazid) och HYZAAR 100/25 (losartan kalium-hydroklortiazid) tabletter kombinerar en angiotensin II receptor blockerare, subtyp AT1-receptorn och diklorazidreceptorn hydroklorazid.
Losartankalium, en icke-peptidmolekyl, beskrivs kemiskt som 2-butyl-4-klor-1-[p-(o-1H-tetrazol-5-ylfenyl)bensyl]imidazol-5-metanolmonokaliumsalt. Dess empiriska formel är C22H22ClKN6O, och dess strukturformel är:
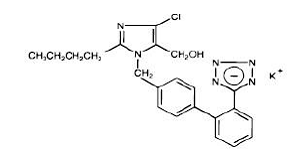
Losartankalium är ett vitt till benvitt fririnnande kristallint pulver med en molekylvikt på 461,01. Det är fritt lösligt i vatten, lösligt i alkoholer och något lösligt i vanliga organiska lösningsmedel, såsom acetonitril och metyletylketon.
Oxidation av 5-hydroximetylgruppen på imidazolringen resulterar i den aktiva metaboliten av losartan.
Hydroklortiazid är 6-klor-3,4-dihydro-2H-1,2,4-bensotiadiazin-7-sulfonamid-1,1-dioxid. Dess empiriska formel är C7H8ClN3O4S2 och dess strukturformel är:
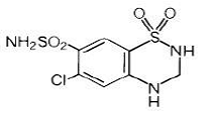
Hydroklortiazid är ett vitt, eller praktiskt taget vitt, kristallint pulver med en molekylvikt på 297,74, som är lätt lösligt i vatten, men fritt lösligt i natriumhydroxidlösning.
HYZAAR finns tillgängligt för oral administrering i tre tablettkombinationer av losartan och hydroklortiazid. HYZAAR 50/12,5 innehåller 50 mg losartankalium och 12,5 mg hydroklortiazid. HYZAAR 100/12,5 innehåller 100 mg losartankalium och 12,5 mg hydroklortiazid. HYZAAR 100/25 innehåller 100 mg losartankalium och 25 mg hydroklortiazid. Inaktiva ingredienser är mikrokristallin cellulosa, vattenhaltig laktos, förgelatinerad stärkelse, magnesiumstearat, hydroxipropylcellulosa, hypromellos och titandioxid.
HYZAAR 50/12.5 och HYZAAR 100/25 innehåller också D&C gul nr 10 aluminiumsjö. HYZAAR 50/12.5, HYZAAR 100/12.5 och HYZAAR 100/25 kan också innehålla karnaubavax.
HYZAAR 50/12,5 innehåller 4,24 mg (0,108 mEq) kalium, HYZAAR 100/12,5 innehåller 8,48 mg (0,216 mEq) kalium och HYZAAR 100/25 innehåller 8,48 mg (0,216 mEq) kalium.
INDIKATIONER
Hypertoni
HYZAAR® är indicerat för behandling av hypertoni, för att sänka blodtrycket. Att sänka blodtrycket minskar risken för dödliga och icke-dödliga kardiovaskulära (CV) händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade studier av blodtryckssänkande läkemedel från en mängd olika farmakologiska klasser inklusive losartan och hydroklortiazid.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än 1 läkemedel för att uppnå blodtrycksmålen. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos drogerna, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad i populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras hypertoni (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter kan förväntas att dra nytta av mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa blodtryckssänkande läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi.
Denna fasta doskombination är inte indicerad för initial behandling av hypertoni, förutom när hypertoni är tillräckligt allvarlig för att värdet av att uppnå snabb blodtryckskontroll överstiger risken för att påbörja kombinationsbehandling hos dessa patienter [se Kliniska studier och DOSERING OCH ADMINISTRERING ].
HYZAAR kan administreras tillsammans med andra antihypertensiva medel.
Hypertonipatienter med vänsterkammarhypertrofi
HYZAAR är indicerat för att minska risken för stroke hos patienter med hypertoni och vänsterkammarhypertrofi, men det finns bevis för att denna fördel inte gäller för svarta patienter. [Ser Användning i specifika populationer , KLINISK FARMAKOLOGI , och DOSERING OCH ADMINISTRERING .]
DOSERING OCH ADMINISTRERING
Hypertoni
Den vanliga startdosen av HYZAAR är 50/12,5 (losartan 50 mg/hydroklortiazid 12,5 mg) en gång dagligen. Dosen kan ökas efter 3 veckors behandling till maximalt 100/25 (losartan 100 mg/hydroklortiazid 25 mg) en gång dagligen vid behov för att kontrollera blodtrycket [se Kliniska studier ].
Inled en patient vars blodtryck inte är tillräckligt kontrollerat med losart en 50 mg monoterapi med HYZAAR 50/12,5 en gång dagligen. Om blodtrycket förblir solkontrollerat efter cirka 3 veckors behandling, kan dosen ökas till två tabletter HYZAAR 50/12,5 en gång dagligen eller en tablett HYZAAR 100/25 en gång dagligen.
Inled en patient vars blodtryck inte är tillräckligt kontrollerat med losartan 100 mg monoterapi med HYZAAR 100/12,5 (losartan 100 mg/hydroklortiazid 12,5 mg) en gång dagligen. Om blodtrycket förblir okontrollerat efter cirka 3 veckors behandling, öka dosen till två tabletter HYZAAR 50/12,5 en gång dagligen eller en tablett HYZAAR 100/25 en gång dagligen.
Initiera en patient vars blodtryck är otillräckligt kontrollerat med hydroklortiazid 25 mg en gång dagligen, eller är kontrollerat men som upplever hypokalemi med denna regim, med HYZAAR 50/12,5 en gång dagligen, minska dosen av hydroklortiazid utan att minska det totala förväntade antihypertensiva svaret. Utvärdera det kliniska svaret på HYZAAR 50/12,5 och, om blodtrycket förblir okontrollerat efter cirka 3 veckors behandling, öka dosen till två tabletter HYZAAR 50/12,5 en gång dagligen eller en tablett HYZAAR 100/25 en gång dagligen.
Hypertonipatienter med vänsterkammarhypertrofi
Inled behandling med HYZAAR 50/12,5 hos patienter vars blodtryck inte är tillräckligt kontrollerat med 50 mg losartankalium. Om ytterligare blodtryckssänkning behövs, öka dosen till HYZAAR 100/12,5, följt av HYZAAR 100/25. För ytterligare blodtryckssänkning lägg till andra blodtryckssänkande medel [se Kliniska studier ].
HUR LEVERERAS
Doseringsformer och styrkor
- HYZAAR 50/12.5 är gula, ovala, filmdragerade tabletter med kod 717 på ena sidan.
- HYZAAR 100/12.5 är vita, ovala, filmdragerade tabletter med kod 745 på ena sidan.
- HYZAAR 100/25 är ljusgula, ovala, filmdragerade tabletter med kod 747 på ena sidan.
Förvaring Och Hantering
HYZAAR levereras som en filmdragerad tablett.
Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur ]. Förvara behållaren väl tillsluten. Skydda från ljus.
Tillverkad för: Organon LLC, ett dotterbolag till ORGANON & Co., Jersey City, NJ 07302, USA. Reviderad: juni 2021
BIEFFEKTER
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Losartan-kalium-hydroklortiazid har utvärderats för säkerhet hos 858 patienter som behandlats för essentiell hypertoni och 3 889 patienter som behandlats för hypertoni och vänsterkammarhypertrofi. De flesta biverkningar har varit milda och övergående och har inte krävt att behandlingen avbryts. I kontrollerade kliniska prövningar krävdes avbrytande av behandlingen på grund av kliniska biverkningar hos endast 2,8 % och 2,3 % av patienterna som behandlades med kombinationen respektive placebo.
I dessa dubbelblinda kontrollerade kliniska prövningar var biverkningar som uppträdde hos mer än 2 % av patienterna som behandlades med losartan-hydroklortiazid och i en högre frekvens än placebo: ryggsmärta (2,1 % mot 0,6 %), yrsel (5,7 % mot 2,9 %). och övre luftvägsinfektion (6,1 % mot 4,6 %).
Följande ytterligare biverkningar har rapporterats i kliniska prövningar med HYZAAR och/eller de enskilda komponenterna:
Blodet och lymfsystemet: Anemi, aplastisk anemi, hemolytisk anemi, leukopeni, agranulocytos.
Metabolism och näringsstörningar: Anorexi, hyperglykemi, hyperurikemi, elektrolytobalans inklusive hyponatremi och hypokalemi.
Psykiatriska störningar: Sömnlöshet, rastlöshet.
Störningar i nervsystemet: Dysgeusi, huvudvärk, migrän, parestesier.
Ögonbesvär: Xantopsi, övergående dimsyn.
Hjärtsjukdomar: Hjärtklappning, takykardi.
Vaskulära störningar: Dosrelaterade ortostatiska effekter, nekrotiserande angiit (vaskulit, kutan vaskulit).
Andningsvägar, bröstkorg och mediastinum: Nästäppa.
Gastrointestinala störningar: Dyspepsi, buksmärtor, magirritation, kramper, illamående, kräkningar, pankreatit, sialoadenit.
Lever- och gallvägar: Gulsot (intrahepatisk kolestatisk gulsot).
Hud och subkutan vävnad: Utslag, klåda, purpura, toxisk epidermal nekrolys, urtikaria, ljuskänslighet, kutan lupus erythematosus.
Muskuloskeletala och bindvävssjukdomar: Muskelkramper, muskelspasmer.
Njur- och urinvägssjukdomar: Glykosuri, nedsatt njurfunktion, interstitiell nefrit, njursvikt.
Reproduktionssystemet och bröststörningar: Erektil dysfunktion/impotens.
Allmänna symtom och tillstånd på administreringsstället: Bröstsmärta, sjukdomskänsla, svaghet.
Undersökningar: Avvikelser i leverfunktionen.
Hosta
Ihållande torrhosta har associerats med användning av ACE-hämmare och kan i praktiken vara en orsak till att behandlingen med ACE-hämmare avbryts. Två prospektiva, dubbelblinda, randomiserade, kontrollerade prövningar i parallellgrupp genomfördes för att bedöma effekterna av losartan på incidensen av hosta hos hypertonipatienter som hade upplevt hosta medan de fick ACE-hämmare. Patienter som hade typisk ACE-hämmare hosta när de utmanades med lisinopril, vars hosta försvann på placebo, randomiserades till losartan 50 mg, lisinopril 20 mg, eller antingen placebo (en studie, n=97) eller 25 mg hydroklortiazid (n=135). Den dubbelblinda behandlingsperioden varade upp till 8 veckor. Förekomsten av hosta visas i tabell 1 nedan.
Dessa studier visar att incidensen av hosta i samband med behandling med losartan, i en population som alla hade hosta i samband med behandling med ACE-hämmare, liknar den som är förknippad med hydroklortiazid eller placebobehandling.
Fall av hosta, inklusive positiva re-utmaningar, har rapporterats efter användning av losartan efter marknadsföring.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av HYZAAR efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att uppskatta deras frekvens tillförlitligt eller att fastställa ett orsakssamband till läkemedelsexponering.
Matsmältningskanalen: Hepatit har rapporterats i sällsynta fall hos patienter som behandlats med losartan.
Hematologiska: Trombocytopeni.
Överkänslighet: Angioödem, inklusive svullnad av struphuvudet och glottis, som orsakar luftvägsobstruktion och/eller svullnad av ansikte, läppar, svalg och/eller tunga har rapporterats i sällsynta fall hos patienter som behandlats med losartan; några av dessa patienter har tidigare upplevt angioödem med andra läkemedel inklusive ACE-hämmare. Vaskulit, inklusive Henoch-Schönlein purpura, har rapporterats med losartan. Anafylaktiska reaktioner har rapporterats.
Muskuloskeletala: Rabdomyolys.
Hud: Erytrodermi.
Icke-melanom hudcancer: Hydroklortiazid är associerat med en ökad risk för icke-melanom hudcancer. I en studie utförd i Sentinel System var den ökade risken främst för skivepitelcancer (SCC) och hos vita patienter som tog stora kumulativa doser. Den ökade risken för SCC i den totala populationen var cirka 1 ytterligare fall per 16 000 patienter per år, och för vita patienter som tog en kumulativ dos på ≥50 000 mg var riskökningen cirka 1 ytterligare SCC-fall för varje 6 700 patienter per år.
LÄKEMEDELSINTERAKTIONER
Medel som ökar serumkalium
Samtidig administrering av losartan med andra läkemedel som höjer serumkaliumnivåerna kan resultera i hyperkalemi. Övervaka serumkalium hos sådana patienter.
Litium
Ökning av serumlitiumkoncentrationer och litiumtoxicitet har rapporterats vid samtidig användning av angiotensin II-receptorantagonister eller tiaziddiuretika. Övervaka litiumnivåer hos patienter som får HYZAAR 12,5 mg och litium.
Icke-steroida antiinflammatoriska medel inklusive selektiva cyklooxygenas-2-hämmare
Losartan kalium
Hos äldre patienter, volymbrist (inklusive de som får diuretikabehandling), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med angiotensin II-receptorantagonister (inklusive losartan) resultera i försämring av njurfunktion, inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som behandlas med losartan och NSAID.
Den antihypertensiva effekten av angiotensin II-receptorantagonister, inklusive losartan, kan försvagas av NSAID, inklusive selektiva COX-2-hämmare.
Hydroklortiazid
Administrering av ett icke-steroid antiinflammatoriskt medel inklusive en selektiv COX-2-hämmare kan minska de diuretiska, natriuretiska och antihypertensiva effekterna av loop-, kaliumsparande och tiaziddiuretika. Därför, när HYZAAR och icke-steroida antiinflammatoriska medel inklusive selektiva COX-2-hämmare används samtidigt, observera noga för att avgöra om den önskade effekten av diuretikumet uppnås.
Hos patienter som får diuretikabehandling kan samtidig administrering av NSAID och angiotensinreceptorblockerare, inklusive losartan, resultera i försämring av njurfunktionen, inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som behandlas med hydroklortiazid, losartan och NSAID.
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, synkope, hyperkalemi och förändringar i njurfunktionen (inklusive akut njursvikt) jämfört med monoterapi.
Veterans Affairs Nephropathy in Diabetes-studien (VA NEPHRON-D) inkluderade 1448 patienter med typ 2-diabetes, förhöjt urin-albumin-till-kreatinin-förhållande och minskad uppskattad glomerulär filtrationshastighet (GFR 30 till 89,9 mL/min), randomiserade dem till lisinopril eller placebo på en bakgrund av losartanbehandling och följde dem under en median av 2,2 år. Patienter som fick kombinationen losartan och lisinopril fick ingen ytterligare fördel jämfört med monoterapi för den kombinerade effektmåttet minskning av GFR, njursjukdom i slutstadiet eller död, men upplevde en ökad incidens av hyperkalemi och akut njurskada jämfört med monoterapin. grupp.
Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på HYZAAR 12,5 mg och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med HYZAAR 12,5 mg till patienter med diabetes. Undvik användning av aliskiren med HYZAAR 12,5 mg till patienter med nedsatt njurfunktion (GFR
Användningen av hydroklortiazid med andra droger
När de administreras samtidigt kan följande läkemedel interagera med tiaziddiuretika [se KLINISK FARMAKOLOGI ]:
Antidiabetika (orala medel och insulin) - dosjustering av det antidiabetiska läkemedlet kan behövas.
Kolestyramin- och kolestipolhartser - Absorptionen av hydroklortiazid försämras i närvaro av anjonbytarhartser. Enstaka doser av antingen kolestyramin- eller kolestipolhartser binder hydroklortiaziden och minskar dess absorption från mag-tarmkanalen med upp till 85 respektive 43 procent.
Fördela doseringen av hydroklortiazid och hartset så att hydroklortiazid administreras minst 4 timmar före eller 4 till 6 timmar efter administrering av hartset.
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Fostertoxicitet
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt HYZAAR 12,5 mg så snart som möjligt.
Tiazider passerar placentabarriären och uppträder i navelsträngsblod. Biverkningar inkluderar fetal eller neonatal gulsot, trombocytopeni [se Användning i specifika populationer ].
Hypotension hos patienter med volym- eller saltbrist
Hos patienter med ett aktiverat renin-angiotensinsystem, såsom volym- eller saltbristade patienter (t.ex. de som behandlas med höga doser diuretika), kan symtomatisk hypotoni förekomma efter påbörjad behandling med HYZAAR. Korrigera volym eller saltutarmning före administrering av HYZAAR. Använd inte HYZAAR som initial behandling hos patienter med utarmning av intravaskulär volym.
Nedsatt njurfunktion
Förändringar i njurfunktionen inklusive akut njursvikt kan orsakas av läkemedel som hämmar reninangiotensinsystemet och av diuretika. Patienter vars njurfunktion kan bero delvis på aktiviteten hos renin-angiotensinsystemet (t.ex. patienter med njurartärstenos, kronisk njursjukdom, svår kronisk hjärtsvikt eller volymutarmning) kan ha en särskild risk att utveckla akut njursvikt på HYZAAR. Övervaka njurfunktionen regelbundet hos dessa patienter. Överväg att avbryta eller avbryta behandlingen hos patienter som utvecklar en kliniskt signifikant minskning av njurfunktionen på HYZAAR [se LÄKEMEDELSINTERAKTIONER och Användning i specifika populationer ].
Överkänslighet
Överkänslighetsreaktioner mot hydroklortiazid kan förekomma hos patienter med eller utan en historia av allergi eller bronkialastma, men är mer sannolikt hos patienter med sådan historia.
Elektrolyter och metaboliska effekter
dubbelblinda kliniska prövningar av olika doser av losartankalium och hydroklortiazid, var incidensen av hypertonipatienter som utvecklade hypokalemi (serumkalium 5,7 mEq/L) var 0,4 % mot 0 % för placebo.
HYZAAR innehåller hydroklortiazid som kan orsaka hypokalemi, hyponatremi och hypomagnesemi. Hypomagnesemi kan resultera i hypokalemi som kan vara svår att behandla trots kaliumtillskott. HYZAAR 12,5 mg innehåller även losartan som kan orsaka hyperkalemi. Övervaka serumelektrolyter regelbundet [se LÄKEMEDELSINTERAKTIONER ].
Samtidig användning av andra läkemedel som kan öka serumkalium kan leda till hyperkalemi [se LÄKEMEDELSINTERAKTIONER ].
Hydroklortiazid kan förändra glukostoleransen och höja serumnivåerna av kolesterol och triglycerider.
Hyperurikemi kan förekomma eller frank gikt kan utlösas hos patienter som får tiazidbehandling. Eftersom losartan minskar urinsyran, dämpar losartan i kombination med hydroklortiazid den diuretikainducerade hyperurikemin.
Hydroklortiazid minskar utsöndringen av kalcium i urinen och kan orsaka förhöjda serumkalcium. Övervaka kalciumnivåerna.
Akut närsynthet och sekundär vinkelstängningsglaukom
Hydroklortiazid, en sulfonamid, kan orsaka en idiosynkratisk reaktion, vilket resulterar i akut övergående närsynthet och akut vinkelglaukom. Symtomen inkluderar akut uppkomst av minskad synskärpa eller ögonsmärta och uppträder vanligtvis inom timmar till veckor efter läkemedelsstart. Obehandlad akut vinkelglaukom kan leda till permanent synförlust. Den primära behandlingen är att avbryta behandlingen med hydroklortiazid så snabbt som möjligt. Snabba medicinska eller kirurgiska behandlingar kan behöva övervägas om det intraokulära trycket förblir okontrollerat. Riskfaktorer för att utveckla akut stängningsvinkelglaukom kan inkludera en historia av sulfonamid- eller penicillinallergi.
Systemisk lupus erythematosus
Tiaziddiuretika har rapporterats orsaka exacerbation eller aktivering av systemisk lupus erythematosus.
Postsympatiktomipatienter
De antihypertensiva effekterna av läkemedlet kan förstärkas hos postsympatiktomipatienter.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION ).
Graviditet
Informera kvinnliga patienter i fertil ålder om konsekvenserna av exponering för HYZAAR 12,5 mg under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Säg till patienterna att rapportera graviditeter till sin läkare så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].

Symtomatisk hypotoni
Informera patienter om att yrsel kan uppstå, särskilt under de första dagarna av behandlingen, och att rapportera detta symptom till en vårdgivare. Informera patienterna om att uttorkning på grund av otillräckligt vätskeintag, överdriven svettning, kräkningar eller diarré kan leda till ett överdrivet blodtrycksfall. Om synkope uppstår, råd patienter att kontakta sin vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kaliumtillskott
Rekommendera patienter att inte använda kaliumtillskott eller saltersättningsmedel som innehåller kalium utan att rådfråga sin vårdgivare [se LÄKEMEDELSINTERAKTIONER ].
Akut närsynthet och sekundär vinkelstängningsglaukom
Råda patienter att avbryta behandlingen med HYZAAR 12,5 mg och omedelbart uppsöka läkarvård om de upplever symtom på akut närsynthet eller sekundär vinkelstängningsglaukom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Losartan Kalium-Hydroklortiazid
Inga karcinogenicitetsstudier har utförts med losartan-kalium-hydroklortiazid-kombinationen.
Losartan-kalium-hydroklortiazid, när den testades i ett viktförhållande på 4:1, var negativ i Ames mikrobiella mutagenesanalysen och V-79 kinesisk hamster lungcellsmutagenesanalysen. Dessutom fanns det inga tecken på direkt genotoxicitet i den alkaliska elueringsanalysen in vitro i råtthepatocyter och in vitro analys av kromosomavvikelser i äggstocksceller från kinesisk hamster vid icke-cytotoxiska koncentrationer.
Losartankalium, tillsammans med hydroklortiazid, hade ingen effekt på fertiliteten eller parningsbeteendet hos hanråttor vid doser upp till 135 mg/kg/dag av losartan och 33,75 mg/kg/dag av hydroklortiazid. Dessa doser har visat sig ge respektive systemisk exponering (AUC) för losartan, dess aktiva metabolit och hydroklortiazid som är cirka 60, 60 och 30 gånger högre än de som uppnås hos människor med 100 mg losartankalium i kombination med 25 mg hydroklortiazid. Hos honråttor var dock samtidig administrering av så låga doser som 10 mg/kg/dag av losartan och 2,5 mg/kg/dag av hydroklortiazid associerad med en liten men statistiskt signifikant minskning av fruktbarhets- och fertilitetsindex. AUC-värden för losartan, dess aktiva metabolit och hydroklortiazid, extrapolerade från data erhållna med losartan administrerat till råttor i en dos på 50 mg/kg/dag i kombination med 12,5 mg/kg/dag hydroklortiazid, var cirka 6, 2 och 2 gånger större än de som uppnås hos människor med 100 mg losartan i kombination med 25 mg hydroklortiazid.
Losartan kalium
Losartankalium var inte karcinogent när det administrerades i maximalt tolererade doser till råttor och möss under 105 respektive 92 veckor. Råttor av honkön som fick den högsta dosen (270 mg/kg/dag) hade en något högre incidens av pankreas acinar adenom. De maximalt tolererade doserna (270 mg/kg/dag hos råttor, 200 mg/kg/dag hos möss) gav systemisk exponering för losartan och dess farmakologiskt aktiva metabolit som var cirka 160 och 90 gånger (råttor) och 30 och 15 gånger (möss) ) exponeringen av en människa på 50 kg som fick 100 mg per dag.
Losartankalium var negativt i analysen av mikrobiell mutagenes och V-79 däggdjurscellmutagenes och i in vitro alkalisk eluering och in vitro och in vivo kromosomavvikelseanalyser. Dessutom visade den aktiva metaboliten inga tecken på genotoxicitet i mikrobiell mutagenes, in vitro alkalisk eluering och in vitro kromosomavvikelseanalyser.
Fertilitet och reproduktionsförmåga påverkades inte i studier med hanråttor som fick orala doser av losartankalium upp till cirka 150 mg/kg/dag. Administrering av toxiska dosnivåer hos kvinnor (300/200 mg/kg/dag) var associerad med en signifikant (p
Hydroklortiazid
Tvååriga utfodringsstudier på möss och råttor utförda under överinseende av National Toxicology Program (NTP) avslöjade inga tecken på cancerframkallande potential hos hydroklortiazid hos möss av honkön (vid doser upp till cirka 600 mg/kg/dag) eller hos hanar. och honråttor (vid doser på upp till cirka 100 mg/kg/dag). NTP fann dock tvetydiga bevis för hepatokarcinogenicitet hos möss av hankön.
Hydroklortiazid var inte genotoxiskt in vitro i Ames mutagenicitetsanalysen av Salmonella typhimurium-stammarna TA 98, TA 100, TA 1535, TA 1537 och TA 1538 och i äggstockstestet för kinesisk hamster (CHO) för kromosomavvikelser med användning av vibrationer, eller könscellskromosomer från mus, benmärgskromosomer från kinesisk hamster och genen Drosophila könsbundna recessiva dödliga egenskaper. Positiva testresultat erhölls endast i in vitro CHO Sister Chromatid Exchange (klastogenicitet) och i muslymfomcellsanalyser (mutagenicitet), med användning av koncentrationer av hydroklortiazid från 43 till 1300 mcg/ml, och i Aspergillus nidulans icke-disjunktionsanalys kl. en ospecificerad koncentration.
Hydroklortiazid hade inga negativa effekter på fertiliteten hos möss och råttor av båda könen i studier där dessa arter exponerades, via sin diet, för doser på upp till 100 respektive 4 mg/kg, före parning och under hela graviditeten.
Användning i specifika populationer
Graviditet
Graviditetskategori D
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt behandlingen med losartan så snart som möjligt. Dessa negativa utfall är vanligtvis förknippade med användning av dessa läkemedel under andra och tredje trimestern av graviditeten. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. Lämplig hantering av maternell hypertoni under graviditeten är viktig för att optimera resultaten för både mor och foster.
det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar reninangiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret. Utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Om oligohydramnios observeras, avbryt HYZAAR, såvida det inte anses vara livräddande för modern. Fostertest kan vara lämpligt, baserat på graviditetsveckan. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada. Följ noga spädbarn med historik av exponering in utero för HYZAAR 12,5 mg för hypotoni, oliguri och hyperkalemi [se Pediatrisk användning ].
Det fanns inga tecken på teratogenicitet hos råttor eller kaniner som behandlats med en maximal dos av losartankalium på 10 mg/kg/dag i kombination med 2,5 mg/kg/dag hydroklortiazid. Vid dessa doser var respektive exponering (AUC) av losartan, dess aktiva metabolit och hydroklortiazid hos kanin cirka 5, 1,5 och 1,0 gånger den som uppnåddes hos människor med 100 mg losartan i kombination med 25 mg hydroklortiazid. AUC-värden för losartan, dess aktiva metabolit och hydroklortiazid, extrapolerade från data erhållna med losartan administrerat till råttor i en dos på 50 mg/kg/dag i kombination med 12,5 mg/kg/dag hydroklortiazid, var cirka 6, 2 och 2 gånger större än de som uppnås hos människor med 100 mg losartan i kombination med 25 mg hydroklortiazid. Fostertoxicitet hos råttor, som bevisats av en lätt ökning av överflödiga revben, observerades när honor behandlades före och under hela graviditeten med 10 mg/kg/dag losartan i kombination med 2,5 mg/kg/dag hydroklortiazid. Som också observerats i studier med enbart losartan, inträffade negativa foster- och neonatala effekter, inklusive minskad kroppsvikt, njurtoxicitet och mortalitet, när gravida råttor behandlades under sen dräktighet och/eller amning med 50 mg/kg/dag losartan i kombination med 12,5 mg/kg/dag hydroklortiazid. Respektive AUC för losartan, dess aktiva metabolit och hydroklortiazid vid dessa doser hos råttor var cirka 35, 10 och 10 gånger högre än de som uppnåddes hos människor med administrering av 100 mg losartan i kombination med 25 mg hydroklortiazid. När hydroklortiazid administrerades utan losartan till gravida möss och råttor under deras respektive perioder av större organogenes, i doser upp till 3000 respektive 1000 mg/kg/dag, fanns inga tecken på skada på fostret.
Tiazider passerar placentabarriären och uppträder i navelsträngsblod. Det finns risk för fetal eller neonatal gulsot, trombocytopeni och möjligen andra biverkningar som har inträffat hos vuxna.
Ammande mödrar
Det är inte känt om losartan utsöndras i modersmjölk, men signifikanta nivåer av losartan och dess aktiva metabolit visades finnas i råttmjölk. Tiazider förekommer i bröstmjölk. På grund av risken för negativa effekter på det ammande barnet bör ett beslut fattas om att avbryta amningen eller avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Säkerhet och effektivitet av HYZAAR hos pediatriska patienter har inte fastställts.
Nyfödda med en historia av exponering för HYZAAR i livmodern
Om oliguri eller hypotoni uppstår, rikta uppmärksamheten mot stöd av blodtryck och njurperfusion. Utbytestransfusion eller dialys kan krävas för att vända hypotoni och/eller ersätta störd njurfunktion.
Geriatrisk användning
en kontrollerad klinisk studie för minskning av den kombinerade risken för kardiovaskulär död, stroke och hjärtinfarkt hos hypertonipatienter med vänsterkammarhypertrofi, var 2857 patienter (62%) 65 år och äldre, medan 808 patienter (18%) var 75 år och över. I ett försök att kontrollera blodtrycket i denna studie fick patienterna samtidigt losartan och hydroklortiazid 74 % av den totala tiden de fick studieläkemedlet. Inga övergripande skillnader i effektivitet observerades mellan dessa patienter och yngre patienter. Biverkningar var något vanligare hos äldre jämfört med icke-äldre patienter för både losartan-hydroklortiazid- och kontrollgruppen [se KLINISK FARMAKOLOGI ].
Lopp
studien Losartan Intervention For Endpoint Reduction in hypertension (LIFE) hade svarta patienter med hypertoni och vänsterkammarhypertrofi behandlade med atenolol en lägre risk för stroke, den primära sammansatta endpointen, jämfört med svarta patienter som behandlades med losartan (båda samtidigt behandlade med hydroklortiazid hos majoriteten av patienterna). I undergruppen av svarta patienter (n=533, 6 % av patienterna i LIFE-studien) fanns det 29 primära effektmått bland 263 patienter på atenolol (11 %, 26 per 1 000 patientår) och 46 primära effektmått bland 270 patienter (17) %, 42 per 1000 patientår) på losartan. Detta fynd kunde inte förklaras på basis av skillnader i andra populationer än ras eller på eventuella obalanser mellan behandlingsgrupper. Dessutom var blodtryckssänkningar i båda behandlingsgrupperna konsekventa mellan svarta och icke-svarta patienter. Med tanke på svårigheten att tolka skillnader i delmängder i stora försök kan man inte veta om den observerade skillnaden är ett resultat av slumpen. LIFE-studien ger dock inga bevis för att fördelarna med losartan när det gäller att minska risken för kardiovaskulära händelser hos hypertonipatienter med vänsterkammarhypertrofi gäller för svarta patienter [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Initiering av HYZAAR 12,5 mg rekommenderas inte för patienter med nedsatt leverfunktion eftersom lämplig startdos av losartan, 25 mg, inte är tillgänglig.
Nedsatt njurfunktion
Förändringar i njurfunktionen har rapporterats hos känsliga individer [se DOSERING OCH ADMINISTRERING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , och KLINISK FARMAKOLOGI ]. Säkerhet och effektivitet för HYZAAR hos patienter med gravt nedsatt njurfunktion (kreatininclearance
ÖVERDOS
Losartan kalium
Signifikant dödlighet observerades hos möss och råttor efter oral administrering av 1000 mg/kg respektive 2000 mg/kg, cirka 44 och 170 gånger den maximala rekommenderade humana dosen på mg/m-basis.
Begränsade data finns tillgängliga med avseende på överdosering hos människor. Den mest sannolika manifestationen av överdosering skulle vara hypotoni och takykardi; bradykardi kan uppstå från parasympatisk (vagal) stimulering. Om symtomatisk hypotoni skulle uppstå, bör stödbehandling sättas in.
Varken losartan eller dess aktiva metabolit kan avlägsnas genom hemodialys.
Hydroklortiazid
Den orala LD av hydroklortiazid är högre än 10 g/kg hos både möss och råttor. De vanligaste tecknen och symtomen som observeras är de som orsakas av elektrolytbrist (hypokalemi, hypokloremi, hyponatremi) och uttorkning till följd av överdriven diures. Om digitalis också har administrerats kan hypokalemi accentuera hjärtarytmier. Graden i vilken hydroklortiazid avlägsnas genom hemodialys har inte fastställts.
KONTRAINDIKATIONER
HYZAAR 12,5 mg är kontraindicerat:
- Hos patienter som är överkänsliga mot någon komponent i denna produkt.
- Hos patienter med anuri
- För samtidig administrering med aliskiren till patienter med diabetes
KLINISK FARMAKOLOGI
Handlingsmekanism
Losartan kalium
Angiotensin II [bildat från angiotensin I i en reaktion katalyserad av angiotensinomvandlande enzym (ACE, kininas II)], är en potent vasokonstriktor, det primära vasoaktiva hormonet i renin-angiotensinsystemet och en viktig komponent i patofysiologin för hypertoni. Det stimulerar också utsöndringen av aldosteron från binjurebarken. Losartan och dess huvudsakliga aktiva metabolit blockerar de vasokonstriktor- och aldosteronutsöndrande effekterna av angiotensin II genom att selektivt blockera bindningen av angiotensin II till AT1-receptorn som finns i många vävnader (t.ex. vaskulär glatt muskulatur, binjure). Det finns också en AT2-receptor som finns i många vävnader, men den är inte känd för att vara associerad med kardiovaskulär homeostas. Varken losartan eller dess huvudsakliga aktiva metabolit uppvisar någon partiell agonistaktivitet vid AT1-receptorn, och båda har mycket större affinitet (cirka 1000 gånger) för AT1-receptorn än för AT2-receptorn. In vitro-bindningsstudier indikerar att losartan är en reversibel, kompetitiv hämmare av AT1-receptorn. Den aktiva metaboliten är 10 till 40 gånger mer potent i vikt än losartan och verkar vara en reversibel, icke-kompetitiv hämmare av AT1-receptorn.
Varken losartan eller dess aktiva metabolit hämmar ACE (kininas II, enzymet som omvandlar angiotensin I till angiotensin II och bryter ned bradykinin), inte heller binder de till eller blockerar andra hormonreceptorer eller jonkanaler som är kända för att vara viktiga för kardiovaskulär reglering.
Hydroklortiazid
Hydroklortiazid är ett tiaziddiuretikum. Tiazider påverkar de renala tubulära mekanismerna för elektrolytreabsorption, vilket direkt ökar utsöndringen av natrium och klorid i ungefär motsvarande mängder. Indirekt minskar den diuretiska effekten av hydroklortiazid plasmavolymen, med åtföljande ökning av plasmareninaktivitet, ökad aldosteronsekretion, ökning av urinförlust av kalium och minskning av serumkalium. Renin-aldosteron-kopplingen medieras av angiotensin II, så samtidig administrering av en angiotensin II-receptorantagonist tenderar att vända den kaliumförlust som är förknippad med dessa diuretika. Mekanismen för den antihypertensiva effekten av tiazider är okänd.
Farmakodynamik
Losartan kalium
Losartan hämmar pressoreffekten av angiotensin II (liksom angiotensin I) infusioner. En dos på 100 mg hämmar pressoreffekten med cirka 85 % vid topp med 25-40 % hämning som kvarstår i 24 timmar. Avlägsnande av den negativa återkopplingen av angiotensin II orsakar en fördubbling till tredubbling av plasmareninaktiviteten och en åtföljande ökning av angiotensin II-plasmakoncentrationen hos hypertonipatienter. Losartan påverkar inte svaret på bradykinin, medan ACE-hämmare ökar svaret på bradykinin. Aldosteronplasmakoncentrationerna faller efter administrering av losartan. Trots effekten av losartan på aldosteronsekretionen observerades mycket liten effekt på serumkalium.
Effekten av losartan är väsentligen närvarande inom en vecka, men i vissa studier inträffade den maximala effekten inom 3-6 veckor. I långtidsuppföljningsstudier (med outplacebokontroll) verkade effekten av losartan bibehållas i upp till ett år. Det finns ingen uppenbar rebound-effekt efter abrupt utsättande av losartan. Det var i huvudsak ingen förändring i genomsnittlig hjärtfrekvens hos losartanbehandlade patienter i kontrollerade studier.
Hydroklortiazid
Efter oral administrering av hydroklortiazid börjar diuresen inom 2 timmar, toppar efter cirka 4 timmar och varar cirka 6 till 12 timmar.
Läkemedelsinteraktioner
Hydroklortiazid
Alkohol, barbiturater eller narkotika - potentiering av ortostatisk hypotoni kan förekomma.
Andra antihypertensiva läkemedel - additiv effekt eller potentiering.
Skelettmuskelavslappnande medel, icke-depolariserande (t.ex. tubokurarin) - möjlig ökad känslighet för muskelavslappnande medel.
Kortikosteroider, ACTH eller glycyrrhizin (finns i lakrits) - intensifierad elektrolytutarmning, särskilt hypokalemi.
Pressoraminer (t.ex. noradrenalin) - eventuellt minskat svar på pressoraminer men inte tillräckligt för att utesluta deras användning.
Farmakokinetik
Losartan kalium
Absorption
Efter oral administrering absorberas losartan väl och genomgår en betydande first-pass-metabolism. Den systemiska biotillgängligheten för losartan är cirka 33 %. Genomsnittlig maximal koncentration av losartan och dess aktiva metabolit uppnås inom 1 timme respektive efter 3-4 timmar. Medan maximala plasmakoncentrationer av losartan och dess aktiva metabolit är ungefär lika, är AUC (area under kurvan) för metaboliten cirka 4 gånger så stor som den för losartan. En måltid saktar ner absorptionen av losartan och minskar dess Cmax max men har endast mindre effekter på losartans AUC eller på metabolitens AUC (~10 % minskning). Farmakokinetiken för losartan och dess aktiva metabolit är linjär med orala losartandoser upp till 200 mg och förändras inte över tiden.
Distribution
Distributionsvolymen för losartan och den aktiva metaboliten är cirka 34 liter respektive 12 liter. Både losartan och dess aktiva metabolit är i hög grad bundna till plasmaproteiner, främst albumin, med plasmafria fraktioner på 1,3 % respektive 0,2 %. Plasmaproteinbindningen är konstant över det koncentrationsintervall som uppnås med rekommenderade doser. Studier på råttor tyder på att losartan passerar blod-hjärnbarriären dåligt, om alls.
Ämnesomsättning
Losartan är ett oralt aktivt medel som genomgår betydande första-passage-metabolism av cytokrom P450-enzymer. Det omvandlas delvis till en aktiv karboxylsyrametabolit som är ansvarig för det mesta av angiotensin II-receptorantagonismen som följer efter behandling med losartan. Cirka 14 % av en oralt administrerad dos av losartan omvandlas till den aktiva metaboliten. Förutom den aktiva karboxylsyrametaboliten bildas flera inaktiva metaboliter. In vitro-studier indikerar att cytokrom P450 2C9 och 3A4 är involverade i biotransformationen av losartan till dess metaboliter.
Eliminering
Totalt plasmaclearance av losartan och den aktiva metaboliten är cirka 600 ml/min respektive 50 ml/min, med njurclearance på cirka 75 ml/min respektive 25 ml/min. Den terminala halveringstiden för losartan är cirka 2 timmar och för metaboliten är cirka 6-9 timmar. Efter orala engångsdoser av losartan utsöndras cirka 4 % av dosen oförändrad i urinen och cirka 6 % utsöndras i urinen som aktiv metabolit. Gallutsöndring bidrar till elimineringen av losartan och dess metaboliter. Efter oral 14C-märkt losartan återfinns cirka 35 % av radioaktiviteten i urinen och cirka 60 % i avföringen. Efter en intravenös dos av 14C-märkt losartan återfinns cirka 45 % av radioaktiviteten i urinen och 50 % i avföringen. Varken losartan eller dess metabolit ackumuleras i plasma vid upprepad dosering en gång dagligen.
Hydroklortiazid
Hydroklortiazid metaboliseras inte utan elimineras snabbt via njurarna. När plasmanivåerna har följts under minst 24 timmar har plasmahalveringstiden observerats variera mellan 5,6 och 14,8 timmar. Minst 61 procent av den orala dosen elimineras oförändrad inom 24 timmar. Hydroklortiazid passerar placenta men inte blod-hjärnbarriären och utsöndras i bröstmjölk.
Specifika populationer
Geriatrik och genus
Losartans farmakokinetik har undersökts hos äldre (65-75 år) och hos båda könen. Plasmakoncentrationerna av losartan och dess aktiva metabolit är likartade hos äldre och unga hypertoniker. Plasmakoncentrationerna av losartan var ungefär dubbelt så höga hos kvinnliga hypertensiva som hos manliga hypertensiva, men koncentrationerna av den aktiva metaboliten var likartade hos män och kvinnor.
Lopp
Farmakokinetiska skillnader på grund av ras har inte studerats [se även Användning i specifika populationer ].
Leverinsufficiens
Efter oral administrering till patienter med mild till måttlig alkoholisk levercirros var plasmakoncentrationerna av losartan och dess aktiva metabolit fem gånger respektive cirka 1,7 gånger högre än hos unga frivilliga män. Jämfört med normala försökspersoner var den totala plasmaclearancen av losartan hos patienter med leverinsufficiens cirka 50 % lägre och den orala biotillgängligheten cirka fördubblades. Den lägre startdosen av losartan som rekommenderas för användning till patienter med nedsatt leverfunktion kan inte ges med HYZAAR. Användning av detta till sådana patienter som ett sätt för losartan-titrering rekommenderas därför inte [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Njurinsufficiens
Losartan
Efter oral administrering ökar plasmakoncentrationerna och AUC för losartan och dess aktiva metabolit med 50-90 % hos patienter med mild (kreatininclearance på 50 till 74 ml/min) eller måttlig (kreatininclearance 30 till 49 ml/min) njurinsufficiens. I denna studie reducerades njurclearance med 55-85 % för bådelosartan och dess aktiva metabolit hos patienter med mild eller måttlig njurinsufficiens. Varken losartan eller dess aktiva metabolit kan avlägsnas genom hemodialys.
Hydroklortiazid
Efter oral administrering ökas AUC för hydroklortiazid med 70 och 700 % för patienter med mild respektive måttlig njurinsufficiens. I denna studie minskade njurclearance av hydroklortiazid med 45 respektive 85 % hos patienter med lätt respektive måttligt nedsatt njurfunktion.
Använd de vanliga behandlingsregimerna med HYZAAR så länge som patientens kreatininclearance är större än 30 ml/min. Säkerhet och effektivitet för HYZAAR 12,5 mg slutenvårdspatienter med gravt nedsatt njurfunktion (kreatininclearance mindre än 30 ml/min) har inte fastställts [se Användning i specifika populationer ].
Läkemedelsinteraktioner
Losartan kalium
Inga kliniskt signifikanta läkemedelsinteraktioner har hittats i studier av losartankalium med hydroklortiazid, digoxin, warfarin, cimetidin och fenobarbital. Rifampin har dock visats minska AUC för losartan och dess aktiva metabolit med 30 % respektive 40 %. Flukonazol, en hämmare av cytokromP450 2C9, minskade AUC för den aktiva metaboliten med cirka 40 %, men ökade AUC för losartan med cirka 70 % efter flera doser. Omvandlingen av losartan till dess aktiva metabolit efter intravenös administrering påverkas inte av ketokonazol, en hämmare av P450 3A4. AUC för aktiv metabolit efter oral losartan påverkades inte av erytromycin, en hämmare av P450 3A4, men AUC för losartan ökade med 30 %.
De farmakodynamiska konsekvenserna av samtidig användning av losartan och hämmare av P450 2C9 har inte undersökts. Patienter som inte metaboliserar losartan till aktiv metabolit har visats ha en specifik, sällsynt defekt i cytokrom P450 2C9. Dessa data tyder på att omvandlingen av losartan till dess aktiva metabolit medieras främst av P450 2C9 och inte P450 3A4.
Kliniska studier
Losartan monoterapi
Minskning av risken för stroke
LIFE-studien var en multinationell, dubbelblind studie som jämförde losartan och atenolol hos 9193 hypertonipatienter med EKG-dokumenterad vänsterkammarhypertrofi. Patienter med hjärtinfarkt eller stroke inom sex månader före randomisering exkluderades. Patienterna randomiserades till att få losartan en gång dagligen 50 mg eller atenolol 50 mg. Om målblodtrycket (
försök att kontrollera blodtrycket fick patienterna i båda armarna av LIFE-studien hydroklortiazid samtidigt under större delen av tiden de fick studieläkemedlet (73,9 % och 72,4 % av dagarna i losartan- respektive atenololarmarna).
Av de randomiserade patienterna var 4963 (54%) kvinnor och 533 (6%) var svarta. Medelåldern var 67 med 5704 (62%) ålder ≥65. Vid baslinjen hade 1195 (13%) diabetes, 1326 (14%) hade isolerad systolisk hypertoni, 1469 (16%) hade kranskärlssjukdom och 728 (8%) hade cerebrovaskulär sjukdom. Baslinjemedelblodtrycket var 174/98 mmHg i båda behandlingsgrupperna. Den genomsnittliga uppföljningslängden var 4,8 år. I slutet av studien eller vid det sista besöket före ett primärt effektmått tog fortfarande 77 % av gruppen som behandlades med losartan och 73 % av gruppen som behandlades med atenolol studiemedicin. Av de patienter som fortfarande tog studieläkemedel var medeldoserna av losartan och atenolol båda cirka 80 mg/dag, och 15 % tog atenolol eller losartan som monoterapi, medan 77 % också fick hydroklortiazid (med en genomsnittlig dos på 20 mg/dag i varje grupp). Blodtryckssänkningen uppmätt vid dalgången var likartad för båda behandlingsgrupperna men blodtrycket mättes inte vid någon annan tidpunkt på dagen. I slutet av studien eller vid det sista besöket före ett primärt effektmått var medelblodtrycket 144,1/81,3 mmHg för gruppen som behandlades med losartan och 145,4/80,9 mmHg för gruppen som behandlades med atenolol [skillnaden i SBP på 1,3 mmHg var signifikant (p
Det primära effektmåttet var den första förekomsten av kardiovaskulär död, icke-fatal stroke eller icke-fatal hjärtinfarkt. Patienter med icke-dödliga händelser stannade kvar i prövningen, så att det också gjordes en undersökning av den första händelsen av varje typ även om det inte var den första händelsen (t.ex. en stroke efter en initial hjärtinfarkt skulle räknas i analysen av stroke). . Behandling med losartan resulterade i en 13 % minskning (p=0,021) av risken för det primära effektmåttet jämfört med atenololgruppen; denna skillnad var främst resultatet av en effekt på dödlig och icke-dödlig stroke. Behandling med losartan minskade risken för stroke med 25 % jämfört med atenolol (p=0,001).
Losartan Kalium-Hydroklortiazid
De 3 kontrollerade studierna av losartan och hydroklortiazid inkluderade över 1300 patienter som utvärderade den antihypertensiva effekten av olika doser av losartan (25, 50 och 100 mg) och samtidig hydroklortiazid (6,25, 12,5 och 25 mg). En faktoriell studie jämförde kombinationen losartan/hydroklortiazid 50/12,5 mg med dess komponenter och placebo. Kombinationen av losartan/hydroklortiazid 50/12,5 mg resulterade i ett ungefär additivt placebojusterat systoliskt/diastoliskt svar (15,5/9,0 mmHg för kombinationen jämfört med 8,5/5,0 mmHg för enbart losartan och 7,0/3,0 mmHg för enbart hydroklortiazid). En annan studie undersökte dos-responssambandet mellan olika doser av hydroklortiazid (6,25, 12,5 och 25 mg) eller placebo på en bakgrund av losartan (50 mg) hos patienter som inte var tillräckligt kontrollerade (sittande diastoliskt blodtryck [SiDBP] 93-120 mmHg) på losartan (50 mg) enbart. Den tredje studien undersökte dos-responssambandet mellan olika doser losartan (25, 50 och 100 mg) eller placebo på en bakgrund av hydroklortiazid (25 mg) hos patienter som inte var tillräckligt kontrollerade (SiDBP93-120 mmHg) på hydroklortiazid (25 mg). ensam. Dessa studier visade ett ökat antihypertensivt svar vid dalgången (24 timmar efter dosering) av hydroklortiazid 12,5 eller 25 mg tillsatt losartan 50 mg på 5,5/3,5 respektive 10,0/6,0 mmHg. På liknande sätt blev det ett ökat antihypertensivt svar när losartan 50 eller 100 mg sattes till hydroklortiazid 25 mg av 9,0/5,5 respektive 12,5/6,5 mmHg. Det fanns ingen signifikant effekt på hjärtfrekvensen.
Det fanns ingen skillnad i svar för män och kvinnor eller hos patienter över eller under 65 år.
Svarta patienter hade ett större svar på hydroklortiazid än icke-svarta patienter och ett mindre svar på losartan. Det övergripande svaret på kombinationen var liknande för svarta och icke-svarta patienter.
Svår hypertoni (SiDBP ≥110 mmHg)
Säkerheten och effekten av HYZAAR som initial behandling för svår hypertoni (definierad som ett genomsnittligt SiDBP ≥110 mmHg bekräftat vid 2 separata tillfällen av all antihypertensiv behandling) studerades i en 6-veckors dubbelblind, randomiserad multicenterstudie. Patienterna randomiserades till antingen losartan och hydroklortiazid (50/12,5 mg, en gång dagligen) eller till losartan (50 mg, en gång dagligen) och följdes för blodtryckssvar. Patienterna titrerades med 2 veckors intervall om deras SiDBP inte nådde målet (
Studien inkluderade 585 patienter, inklusive 264 (45 %) kvinnor, 124 (21 %) svarta och 21 (4 %) ≥65 år. Medelblodtrycket vid baslinjen för den totala populationen var 171/113 mmHg. Medelåldern var 53 år. Efter 4 veckors behandling var den genomsnittliga SiDBP 3,1 mmHg lägre och den genomsnittliga SiSBP var 5,6 mmHglower i gruppen som behandlades med HYZAAR. Som ett resultat nådde en större andel av patienterna på HYZAAR 12,5 mg måldiastoliskt blodtryck (17,6 % för HYZAAR 12,5 mg, 9,4 % för losartan; p=0,006). Liknande trender sågs när patienterna grupperades efter kön, ras eller ålder (
Efter 6 veckors behandling nådde fler patienter som fick kombinationsregimen måldiastoliskt blodtryck än de som fick monoterapiregimen (29,8 % mot 12,5 %).
PATIENTINFORMATION
HYZAAR® (HY-zar) (losartan kalium och hydroklortiazid tabletter)50/12,5 mg, 100/12,5 mg, 100/25 mg
Läs patientinformationen som följer med HYZAAR ® innan du börjar ta den och varje gång du får en påfyllning. Det kan komma ny information. Denna bipacksedel ersätter inte att prata med din läkare om ditt tillstånd och din behandling.
Vilken är den viktigaste informationen jag borde veta om HYZAAR?
- HYZAAR kan orsaka skada eller dödsfall för ett ofött barn.
- Tala med din läkare om andra sätt att sänka ditt blodtryck om du planerar att bli gravid.
- Om du blir gravid medan du tar HYZAAR 12,5 mg, berätta omedelbart för din läkare.
Vad är HYZAAR 12,5 mg?
HYZAAR 12,5 mg innehåller 2 receptbelagda läkemedel, en angiotensinreceptorblockerare (ARB) och ett diuretikum (vattenpiller). Det används för att:
- lägre högt blodtryck (hypertoni). HYZAAR är vanligtvis inte det första läkemedlet som används för att behandla högt blodtryck.
- minska risken för stroke hos patienter med högt blodtryck och ett hjärtproblem som kallas vänsterkammarhypertrofi (LVH). HYZAAR kanske inte hjälper svarta patienter med detta problem.
HYZAAR har inte studerats på barn under 18 år.
Högt blodtryck (hypertoni). Blodtrycket är kraften i dina blodkärl när ditt hjärta slår och när ditt hjärta vilar. Du har högt blodtryck när kraften är för stor. Losartaningrediensen i HYZAAR 12,5 mg kan hjälpa dina blodkärl att slappna av så att ditt blodtryck blir lägre. Hydroklortiaziden i gredientin HYZAAR verkar genom att få dina njurar att passera mer vatten och salt.
Vänsterkammarhypertrofi (LVH) är en förstoring av väggarna i hjärtats vänstra kammare (hjärtats huvudpumpkammare). LVH kan hända av flera saker. Högt blodtryck är den vanligaste orsaken till LVH.
Vem ska inte ta HYZAAR?
Ta inte HYZAAR 12,5 mg om du:
- är allergiska mot någon ingrediens i HYZAAR. Se en komplett lista över ingredienser i HYZAAR i slutet av denna bipacksedel.
- inte kissar.
- har diabetes och tar ett läkemedel som heter aliskiren för att sänka blodtrycket.
Vad ska jag berätta för min läkare innan jag tar HYZAAR?
Berätta för din läkare om alla dina medicinska tillstånd inklusive om du:
- är gravid eller planerar att bli gravid. Se "Vad är den viktigaste informationen jag borde veta om HYZAAR?"
- ammar eller planerar att amma. HYZAAR kan passera över i din mjölk och kan skada ditt barn. Du och din läkare bör bestämma om du ska ta HYZAAR eller amma. Du ska inte göra båda.
- har kräkts (kräkts upp), haft diarré, svettats mycket eller inte druckit tillräckligt med vätska. Dessa kan leda till att du har lågt blodtryck.
- har leverproblem
- har njurproblem
- har systemisk lupus erythematosus (Lupus; SLE)
- har diabetes
- har gikt
- har någon allergi
- har haft hudcancer eller om du utvecklar en ny hudskada under behandlingen. Behandling med hydroklortiazid kan öka risken för vissa typer av hudcancer (icke-melanom hudcancer). Diskutera med din läkare hur du skyddar din hud från solexponering och hur ofta du bör genomgå hudcancerscreening.
Berätta för din läkare om alla läkemedel du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott.
HYZAAR 12,5 mg och vissa andra läkemedel kan interagera med varandra. Tala särskilt om för din läkare om du tar:
- kaliumtillskott
- saltersättningsmedel innehållande kalium
- andra läkemedel som kan öka serumkalium
- vattenpiller (diuretika)
- litium (ett läkemedel som används för att behandla en viss typ av depression)
- läkemedel som används för att behandla smärta och artrit, som kallas icke-steroida antiinflammatoriska läkemedel (NSAID), inklusive COX-2-hämmare
- andra läkemedel för att sänka blodtrycket.
Vet vilka mediciner du tar. Håll en lista över dina läkemedel och visa den för din läkare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag ta HYZAAR 12,5 mg?
- Ta HYZAAR 12,5 mg precis som din läkare har ordinerat. Din läkare kan ändra din dos om det behövs.
- HYZAAR kan tas med eller utan mat.
- Om du missar en dos, ta den så snart du kommer ihåg det. Om det är nära din nästa dos, ta inte den missade dosen. Ta bara nästa dos vid din vanliga tid.
- Om du tar för mycket HYZAAR 12,5 mg, ring din läkare eller Giftinformationscentralen eller gå till närmaste akutmottagning direkt.
- Din läkare kan ta blodprov då och då medan du tar HYZAAR.
Vilka är de möjliga biverkningarna av HYZAAR?
HYZAAR kan orsaka följande biverkningar som kan vara allvarliga:
- Skada eller död hos ofödda barn. Se "Vad är den viktigaste informationen jag borde veta om HYZAAR?"
- Allergisk reaktion. Symtom på en allergisk reaktion är svullnad av ansikte, läppar, svalg eller tunga. Få akut medicinsk hjälp omedelbart och sluta ta HYZAAR.
- Lågt blodtryck (hypotension). Lågt blodtryck kan göra att du känner dig svimfärdig eller yr. Lägg dig ner om du känner dig svimfärdig eller yr. Ring din läkare direkt.
- Om du har njurproblem kan du se en försämring av hur väl dina njurar fungerar. Ring din läkare om du får svullnad i dina fötter, vrister eller händer, eller oförklarlig viktökning.
- Ett nytt eller förvärrat tillstånd som kallas systemisk lupus erythematosus (Lupus; SLE)
- Ögonproblem. Ett av läkemedlen i HYZAAR 12,5 mg kan orsaka ögonproblem som, om de lämnas obehandlade, kan leda till synförlust. Symtom på ögonproblem kan inträffa inom timmar till veckor efter att HYZAAR påbörjats. Tala genast om för din läkare om du har:
- minskad syn
- ögonsmärta
- Hudens känslighet för sol och risk för hudcancer.
De vanligaste biverkningarna av HYZAAR 12,5 mg hos personer med högt blodtryck är:
- "förkylningar" (infektion i övre luftvägarna)
- yrsel
- Täppt i näsan
- ryggont
Tala om för din läkare om du får någon biverkning som stör dig eller som inte kommer att försvinna. Detta är inte en komplett lista över biverkningar. För en fullständig lista, fråga din läkare eller apotekspersonal.
Hur ska jag förvara HYZAAR 12,5 mg?
- Förvara HYZAAR i rumstemperatur vid 59°F till 86°F (15°C till 30°C).
- Förvara HYZAAR i en tättsluten behållare och förvara HYZAAR borta från ljuset.
- Förvara HYZAAR 12,5 mg och alla läkemedel utom räckhåll för barn.
Allmän information om HYZAAR
Läkemedel skrivs ibland ut för tillstånd som inte nämns i patientinformationsblad. Använd inte HYZAAR för ett tillstånd som det inte har ordinerats för. Ge inte HYZAAR till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Denna broschyr sammanfattar den viktigaste informationen om HYZAAR. Om du vill ha mer information, prata med din läkare. Du kan be din apotekspersonal eller läkare om information som är skriven för vårdpersonal.
Vilka är ingredienserna i HYZAAR?
Aktiva ingredienser: losartan kalium, hydroklortiazid
Inaktiva Ingredienser:
mikrokristallin cellulosa, vattenhaltig laktos, förgelatinerad stärkelse, magnesiumstearat, hydroxipropylcellulosa, hypromellos, titandioxid. HYZAAR 50/12.5 och HYZAAR 100/25 innehåller också D&C gul nr 10 aluminiumsjö.
HYZAAR 50/12.5, HYZAAR 100/12.5 och HYZAAR 100/25 kan också innehålla karnaubavax.
