Avapro 150mg, 300mg Irbesartan Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Avapro 300mg och hur används det?
Avapro 300mg är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni), nervsmärta orsakad av typ 2-diabetes. Avapro kan användas ensamt eller tillsammans med andra läkemedel.
Avapro 300mg tillhör en klass av läkemedel ARB.
Det är inte känt om Avapro 150mg är säkert och effektivt för barn yngre än 6 år.
Vilka är de möjliga biverkningarna av Avapro 300mg?
Avapro kan orsaka allvarliga biverkningar inklusive:
- oförklarlig muskelsmärta,
- ömhet eller svaghet,
- feber,
- ovanlig trötthet,
- mörkfärgad urin,
- yrsel,
- lite eller ingen urinering,
- svullnad,
- snabb viktökning,
- förvirring,
- aptitlöshet,
- kräkningar och
- smärta i sidan eller nedre delen av ryggen
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Avapro inkluderar:
- diarre,
- halsbränna,
- orolig mage, och
- trött känsla
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Avapro. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
- När graviditet upptäcks, avbryt AVAPRO så snart som möjligt.
- Läkemedel som verkar direkt på renin-angiotenerna i systemet kan orsaka skador och dödsfall för fostret under utveckling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
BESKRIVNING
AVAPRO (irbesartan) är en angiotensin II-receptor (AT1 subtyp) antagonist.
Irbesartan är en icke-peptidförening, kemiskt beskriven som en 2-butyl-3-[p-(o-1H-tetrazol-5-ylfenyl)bensyl]-1,3-diazaspiro[4.4]non-1-en-4 -ett.
Dess empiriska formel är C25H28N6O, och strukturformeln:
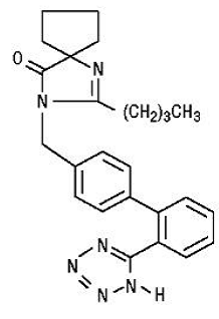
Irbesartan är ett vitt till benvitt kristallint pulver med en molekylvikt på 428,5. Det är en opolär förening med en fördelningskoefficient (oktanol/vatten) på 10,1 vid pH 7,4. Irbesartan är svagt lösligt i alkohol och metylenklorid och praktiskt taget olösligt i vatten.
AVAPRO är tillgängligt för oral administrering i tabletter utan skåror innehållande 75 mg, 150 mg eller 300 mg irbesartan. Inaktiva ingredienser inkluderar: laktos, mikrokristallin cellulosa, förgelatinerad stärkelse, kroskarmellosnatrium, poloxamer 188, kiseldioxid och magnesiumstearat.
INDIKATIONER
Hypertoni
AVAPRO® är indicerat för behandling av hypertoni, för att sänka blodtrycket. Att sänka blodtrycket sänker risken för dödliga och icke-dödliga kardiovaskulära (CV) händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade prövningar av antihypertensiva läkemedel från en mängd olika farmakologiska klasser inklusive detta läkemedel.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än 1 läkemedel för att uppnå blodtrycksmålen. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos drogerna, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad i populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras hypertoni (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter kan förväntas att dra nytta av mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa blodtryckssänkande läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi.
AVAPRO 300 mg kan användas ensamt eller i kombination med andra antihypertensiva medel.
Nefropati hos typ 2-diabetespatienter
AVAPRO är indicerat för behandling av diabetisk nefropati hos patienter med typ 2-diabetes och hypertoni, förhöjt serumkreatinin och proteinuri (>300 mg/dag). I denna population minskar AVAPRO graden av progression av nefropati mätt som förekomsten av fördubbling av serumkreatinin eller njursjukdom i slutstadiet (behov av dialys eller njurtransplantation) [se Kliniska studier ].
DOSERING OCH ADMINISTRERING
allmänna överväganden
AVAPRO kan administreras tillsammans med andra antihypertensiva medel och med eller utan mat.
Hypertoni
Den rekommenderade initialdosen av AVAPRO 300 mg är 150 mg en gång dagligen. Dosen kan ökas till en maximal dos på 300 mg en gång dagligen efter behov för att kontrollera blodtrycket [se Kliniska studier ].
Nefropati hos typ 2-diabetespatienter
Den rekommenderade dosen är 300 mg en gång dagligen [se Kliniska studier ].
Dosjustering för patienter med volym och saltbrist
Den rekommenderade initialdosen är 75 mg en gång dagligen hos patienter med utarmning av intravaskulär volym eller salt (t.ex. patienter som behandlas kraftigt med diuretika eller i hemodialys) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
HUR LEVERERAS
Doseringsformer och styrkor
AVAPRO 75 mg är en vit till benvit, bikonvex oval, filmdragerad tablett präglad med ett hjärta på ena sidan och "2871" på den andra.
AVAPRO 150 mg är en vit till benvit, bikonvex oval, filmdragerad tablett präglad med ett hjärta på ena sidan och "2872" på den andra.
AVAPRO 300 mg är en vit till benvit, bikonvex oval, filmdragerad tablett präglad med ett hjärta på ena sidan och "2873" på den andra.
Förvaring Och Hantering
AVAPRO (irbesartan) finns som vita till benvita, bikonvexa ovala, filmdragerade tabletter, präglade med en hjärtform på ena sidan och en kod på den andra (se tabell nedan). Enhetsflaskor innehåller 30 eller 90 filmdragerade tabletter enligt följande:
Förvara vid 25°C (77°F); utflykter tillåtna till 15°C–30°C (59°F–86°F) [se USP-kontrollerad rumstemperatur ].
sanofi-aventis US LLC, Bridgewater, NJ 08807, ETT SANOFI-FÖRETAG. Reviderad: september 2021
BIEFFEKTER
Följande viktiga biverkningar beskrivs på andra ställen i märkningen:
- Hypotension hos patienter med volym eller saltbrist [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Nedsatt njurfunktion [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken. Biverkningsinformationen från kliniska prövningar ger dock en grund för att identifiera de biverkningar som verkar vara relaterade till läkemedelsanvändning och för att uppskatta antalet.
Hypertoni
AVAPRO har utvärderats för säkerhet hos mer än 4300 patienter med hypertoni och cirka 5000 patienter totalt. Denna erfarenhet inkluderar 1303 patienter som behandlats i över 6 månader och 407 patienter i 1 år eller mer.
placebokontrollerade kliniska prövningar rapporterades följande biverkningar hos minst 1 % av patienterna som behandlades med AVAPRO (n=1965) och med en högre incidens jämfört med placebo (n=641), exklusive de som är för allmänna för att vara informativa och de inte rimligt förknippade med användningen av läkemedel eftersom de var förknippade med det tillstånd som behandlas eller är mycket vanliga i den behandlade befolkningen, inklusive: diarré (3% mot 2%), dyspepsi/halsbränna (2% mot 1%) och trötthet (4 % mot 3 %).
Användning av irbesartan var inte associerad med en ökad förekomst av torrhosta, vilket vanligtvis är associerat med användning av ACE-hämmare. I placebokontrollerade studier var incidensen av hosta hos irbesartanbehandlade patienter 2,8 % jämfört med 2,7 % hos patienter som fick placebo.
Nefropati hos typ 2-diabetespatienter
Hyperkalemi
Irbesartan Diabetic Nephropathy Trial (IDNT) (proteinuri ≥900 mg/dag och serumkreatinin varierande från 1,0-3,0 mg/dL), var procentandelen patienter med kalium >6 mEq/L 18,6 % i AVAPRO 300 mg-gruppen jämfört med 6,0 % i placebogruppen. Utsättningar på grund av hyperkalemi i AVAPRO 150 mg-gruppen var 2,1 % jämfört med 0,4 % i placebogruppen.
I IDNT liknade biverkningarna de som sågs hos patienter med hypertoni med undantag för en ökad förekomst av ortostatiska symtom som förekom oftare i AVAPRO 150 mg jämfört med placebogruppen: yrsel (10,2 % mot 6,0 %), ortostatisk yrsel (5,4 %) % vs 2,7 %) och ortostatisk hypotoni (5,4 % vs 3,2 %).
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats under användning av AVAPRO efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller att fastställa ett orsakssamband till läkemedelsexponering.
Urtikaria; angioödem (som involverar svullnad av ansikte, läppar, svalg och/eller tunga); anafylaktisk reaktion inklusive anafylaktisk chock; ökade leverfunktionstester; gulsot; hepatit; hyperkalemi; anemi; trombocytopeni; ökad CPK; tinnitus; och hypoglykemi hos diabetespatienter.
LÄKEMEDELSINTERAKTIONER
Medel som ökar serumkalium
Samtidig administrering av AVAPRO med andra läkemedel som höjer serumkaliumnivåerna kan resultera i hyperkalemi, ibland allvarlig. Övervaka serumkalium hos sådana patienter.
Litium
Ökning av serumlitiumkoncentrationer och litiumtoxicitet har rapporterats vid samtidig användning av irbesartan och litium. Övervaka litiumnivåer hos patienter som får irbesartan och litium.
Icke-steroida antiinflammatoriska läkemedel (NSAID) inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare)
Hos äldre patienter, volymbrist (inklusive de som behandlas med diuretika), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med angiotensin II-receptorantagonister (inklusive irbesartan) resultera i försämring av njurfunktionen. inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som får irbesartan och NSAID-behandling.
Den antihypertensiva effekten av angiotensin II-receptorantagonister, inklusive irbesartan, kan försvagas av NSAID inklusive selektiva COX-2-hämmare.
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, hyperkalemi och förändringar i njurfunktion (inklusive akut njursvikt) jämfört med monoterapi. De flesta patienter som får kombinationen av två RAS-hämmare får ingen ytterligare fördel jämfört med monoterapi. Undvik i allmänhet kombinerad användning av RAS-hämmare. Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på AVAPRO 150 mg och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med AVAPRO till patienter med diabetes. Undvik användning av aliskiren med AVAPRO till patienter med nedsatt njurfunktion (GFR
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Fostertoxicitet
AVAPRO 150mg kan orsaka fosterskador när det administreras till en gravid kvinna. Användning av läkemedel som verkar på reninangiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt AVAPRO så snart som möjligt [se Användning i specifika populationer ].
Hypotension hos patienter med volym eller saltbrist
Hos patienter med ett aktiverat renin-angiotensinsystem, såsom volym- eller saltfattiga patienter (t.ex. de som behandlas med höga doser diuretika), kan symtomatisk hypotoni uppträda efter initialisering av behandling med AVAPRO. Korrigera volym eller saltutarmning före administrering av AVAPRO 300 mg eller använd en lägre startdos [se DOSERING OCH ADMINISTRERING ].
Nedsatt njurfunktion
Förändringar i njurfunktionen inklusive akut njursvikt kan orsakas av läkemedel som hämmar renin-angiotensinsystemet. Patienter vars njurfunktion kan bero delvis på aktiviteten hos renin-angiotensinsystemet (t.ex. patienter med njurartärstenos, kronisk njursjukdom, allvarlig hjärtsvikt eller volymutarmning) kan ha en särskild risk att utveckla akut njursvikt eller dödsfall på AVAPRO. Övervaka njurfunktionen regelbundet hos dessa patienter. Överväg att avbryta eller avbryta behandlingen hos patienter som utvecklar en kliniskt signifikant minskning av njurfunktionen på AVAPRO [se LÄKEMEDELSINTERAKTIONER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Inga tecken på karcinogenicitet observerades när irbesartan administrerades i doser på upp till 500/1000 mg/kg/dag (hanar/honor, respektive) till råttor och 1000 mg/kg/dag till möss i upp till 2 år. För han- och honråttor gav 500 mg/kg/dag en genomsnittlig systemisk exponering för irbesartan (AUC 0–24 timmar, bundet plus obundet) cirka 3 respektive 11 gånger den genomsnittliga systemiska exponeringen hos människor som fick den maximala rekommenderade humana exponeringen. dos (MRHD) på 300 mg irbesartan/dag, medan 1000 mg/kg/dag (enbart till kvinnor) gav en genomsnittlig systemisk exponering ungefär 21 gånger den som rapporterades för människor vid MRHD. För han- och honmöss gav 1000 mg/kg/dag en exponering för irbesartan cirka 3 respektive 5 gånger den mänskliga exponeringen vid 300 mg/dag.
Irbesartan var inte mutagent i ett antal in vitro-tester (Ames mikrobiellt test, DNA-reparationstest för hepatocyter från råtta, V79 däggdjurscell framåt gen-mutationsanalys). Irbesartan var negativ i flera tester för induktion av kromosomavvikelser (in vitro-analys av humana lymfocyter; in vivo-studie av mikrokärnor på mus).
Irbesartan hade inga negativa effekter på fertilitet eller parning av han- eller honråttor vid orala doser ≤650 mg/kg/dag, den högsta dosen gav en systemisk exponering för irbesartan (AUC 0–24 timmar, bundet plus obundet) cirka 5 gånger så mycket som hittas hos människor som får MRHD på 300 mg/dag.
Användning i specifika populationer
Graviditet
Risksammanfattning
AVAPRO kan orsaka fosterskador när det ges till en gravid kvinna. Användning av läkemedel som verkar på reninangiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död [se Kliniska överväganden ]. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. När graviditet upptäcks, avbryt AVAPRO 150mg så snart som möjligt.
Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall oavsett läkemedelsexponering. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för mödrar och/eller embryo-foster
Hypertoni under graviditet ökar moderns risk för havandeskapsförgiftning, graviditetsdiabetes, för tidig förlossning och förlossningskomplikationer (t.ex. behov av kejsarsnitt och postpartumblödning). Hypertoni ökar fostrets risk för intrauterin tillväxtbegränsning och intrauterin död. Gravida kvinnor med högt blodtryck bör övervakas noggrant och hanteras därefter.
Fetala/neonatala biverkningar
Oligohydramnios hos gravida kvinnor som använder läkemedel som påverkar renin-angiotensinsystemet under andra och tredje trimestern av graviditeten kan resultera i följande: nedsatt fosterns njurfunktion som leder till anuri och njursvikt, fosterlunghypoplasi, skelettdeformationer, inklusive skallhypoplasi, hypotoni , och döden.
I det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar renin-angiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret.
Utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Fostertest kan vara lämpligt, baserat på graviditetsveckan. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada. Om oligohydramnios observeras, överväg alternativ behandling. Observera noga spädbarn med tidigare exponering för AVAPRO in utero för hypotoni, oliguri och hyperkalemi och andra symtom på nedsatt njurfunktion. Hos nyfödda med en historia av exponering för AVAPRO 300 mg in utero, om oliguri eller hypotoni inträffar, rikta uppmärksamheten mot att stödja blodtryck och njurperfusion. Utbytestransfusion eller dialys kan krävas för att vända hypotoni och/eller ersätta störd njurfunktion.
Data
Djurdata
Irbesartan passerar placentan hos råttor och kaniner. Hos honråttor som fått irbesartan före parning genom dräktighet och laktation i orala doser på 50, 180 eller 650 mg/kg/dag (1,6 till 21,1 gånger den maximala rekommenderade dosen för människor (MRHD) baserat på kroppsyta), undersöktes foster på Dräktighetsdag 20 visade ökad förekomst av hydroureter och njurbäckenkavitation och/eller frånvaro av njurpapill i alla irbesartanbehandlade grupper. Subkutant ödem förekom även hos foster vid moderns doser ≥180 mg/kg/dag (5,8 gånger MRHD). Dessa anomalier inträffade när honråttor fick irbesartan från före parning till och med dag 20 av dräktigheten men inte observerades hos ungar postnatalt i samma studie, eller när irbesartan endast gavs till dräktiga råttor under organogenesen (dräktighetsdag 6 till och med dräktighetsdag 15) kl. orala doser från 50 till 450 mg/kg/dag (upp till 14,6 gånger MRHD). Dessutom observerades inga negativa effekter på njurutvecklingen hos ungar från mödrar som fick irbesartan från dräktighetsdag 15 till och med digivningsdag 24 vid doser på 50, 180 eller 650 mg/kg/dag (upp till 21,1 gånger MRHD). De observerade effekterna tros vara sena graviditetseffekter av läkemedlet. Dräktiga kaniner som fick orala doser av irbesartan på 30 mg/kg/dag (1,9 gånger MRHD baserat på kroppsyta) upplevde en hög grad av mödradödlighet och abort. Överlevande honor hade en liten ökning av tidiga resorptioner och en motsvarande minskning av levande foster.
Radioaktivitet fanns hos rått- och kaninfostret under sen dräktighet efter orala doser av radiomärkt irbesartan.
Laktation
Det finns inga tillgängliga data om förekomsten av irbesartan i modersmjölk, effekter på mjölkproduktionen eller det ammade barnet. Irbesartan eller någon metabolit av irbesartan utsöndras i mjölken hos lakterande råttor [se KLINISK FARMAKOLOGI ]. På grund av risken för negativa effekter på ammande spädbarn, rekommenderas inte användning av AVAPRO 150 mg till ammande kvinnor.
Pediatrisk användning
Irbesartan, i en studie med en dos på upp till 4,5 mg/kg/dag, en gång dagligen, verkade inte sänka blodtrycket effektivt hos pediatriska patienter i åldrarna 6 till 16 år.
AVAPRO har inte studerats på pediatriska patienter yngre än 6 år.
Geriatrisk användning
Av 4925 försökspersoner som fick AVAPRO i kontrollerade kliniska studier av hypertoni var 911 (18,5 %) 65 år och äldre, medan 150 (3,0 %) var 75 år och äldre. Inga övergripande skillnader i effektivitet eller säkerhet observerades mellan dessa försökspersoner och yngre försökspersoner, men större känslighet hos vissa äldre individer kan inte uteslutas. [Ser KLINISK FARMAKOLOGI och Kliniska studier ]
ÖVERDOS
Det finns inga tillgängliga data angående överdosering hos människor. Men dagliga doser på 900 mg under 8 veckor tolererades väl. De mest sannolika manifestationerna av överdosering förväntas vara hypotoni och takykardi; bradykardi kan också uppstå vid överdosering. Irbesartan avlägsnas inte genom hemodialys.
Akut orala toxicitetsstudier med irbesartan på möss och råttor indikerade att akuta letala doser var över 2000 mg/kg, cirka 25-faldigt respektive 50-faldigt MRHD (300 mg) baserat på kroppsyta.
KONTRAINDIKATIONER
AVAPRO 150mg är kontraindicerat för patienter som är överkänsliga mot någon komponent i denna produkt.
Administrera inte aliskiren samtidigt med AVAPRO 300mg till patienter med diabetes.
KLINISK FARMAKOLOGI
Handlingsmekanism
Angiotensin II är en potent vasokonstriktor som bildas av angiotensin I i en reaktion som katalyseras av angiotensinomvandlande enzym (ACE, kininas II). Angiotensin II är det primära vasoaktiva hormonet i reninangiotensinsystemet och en viktig komponent i patofysiologin för hypertoni. Det stimulerar också utsöndringen av aldosteron från binjurebarken. Irbesartan blockerar de vasokonstriktor- och aldosteronutsöndrande effekterna av angiotensin II genom att selektivt binda till AT1-angiotensin II-receptorn som finns i många vävnader (t.ex. vaskulär glatt muskulatur, binjure). Det finns också en AT2-receptor i många vävnader, men den är inte involverad i kardiovaskulär homeostas.
Irbesartan är en specifik kompetitiv antagonist av AT1-receptorer med en mycket större affinitet (mer än 8500 gånger) för AT1-receptorn än för AT2-receptorn och ingen agonistaktivitet.
Blockad av AT1-receptorn tar bort den negativa återkopplingen av angiotensin II på reninsekretion, men den resulterande ökade plasmareninaktiviteten och cirkulerande angiotensin II övervinner inte effekterna av irbesartan på blodtrycket.
Irbesartan hämmar inte ACE eller renin eller påverkar andra hormonreceptorer eller jonkanaler som är kända för att vara involverade i den kardiovaskulära regleringen av blodtryck och natriumhomeostas.
Farmakodynamik
Hos friska försökspersoner gav enstaka orala irbesartandoser på upp till 300 mg en dosberoende hämning av pressoreffekten av angiotensin II-infusioner. Hämningen var fullständig (100 %) 4 timmar efter orala doser på 150 mg eller 300 mg och partiell hämning upprätthölls i 24 timmar (60 % och 40 % vid 300 mg respektive 150 mg).
Hos hypertonipatienter orsakar hämning av angiotensin II-receptorn efter kronisk administrering av irbesartan en 1,5- till 2-faldig ökning av angiotensin II-plasmakoncentrationen och en 2- till 3-faldig ökning av plasmareninnivåerna. Aldosteronplasmakoncentrationer minskar i allmänhet efter administrering av irbesartan, men serumkaliumnivåerna påverkas inte signifikant vid rekommenderade doser.
Hos hypertensiva patienter hade kroniska orala doser av irbesartan (upp till 300 mg) ingen effekt på glomerulär filtrationshastighet, renalt plasmaflöde eller filtrationsfraktion. I flerdosstudier på hypertonipatienter fanns inga kliniskt viktiga effekter på fastande triglycerider, totalkolesterol eller HDL-kolesterolkoncentrationer. Det fanns ingen effekt på serumurinsyra under kronisk oral administrering och ingen urikosurisk effekt.
Farmakokinetik
Absorption
Den orala absorptionen av irbesartan är snabb och fullständig med en genomsnittlig absolut biotillgänglighet på 60 % till 80 %. Efter oral administrering av AVAPRO uppnås maximala plasmakoncentrationer av irbesartan 1,5 till 2 timmar efter dosering. Mat påverkar inte biotillgängligheten av irbesartan.
Irbesartan uppvisar linjär farmakokinetik över det terapeutiska dosintervallet.
Distribution
Irbesartan är till 90 % bundet till serumproteiner (främst albumin och α-syraglykoprotein) med försumbar bindning till cellulära komponenter i blodet. Den genomsnittliga distributionsvolymen är 53 till 93 liter.
Djurstudier tyder på att radiomärkt irbesartan svagt passerar blod-hjärnbarriären och placenta. Irbesartan utsöndras i mjölken hos digivande råttor.
Eliminering
Totalt plasma- och renalt clearance ligger i intervallet 157 till 176 ml/min respektive 3,0 till 3,5 ml/min. Den terminala halveringstiden för irbesartan är i genomsnitt 11 till 15 timmar. Steady-state-koncentrationer uppnås inom 3 dagar. Begränsad ackumulering av irbesartan (
Ämnesomsättning
Irbesartan är ett oralt aktivt medel som inte kräver biotransformation till en aktiv form. Irbesartan metaboliseras via glukuronidkonjugering och oxidation. Efter oral eller intravenös administrering av Clabeled irbesartan kan mer än 80 % av den cirkulerande plasmaradioaktiviteten tillskrivas oförändrat irbesartan. Den primära cirkulerande metaboliten är det inaktiva irbesartanglukuronidkonjugatet (cirka 6%). De återstående oxidativa metaboliterna bidrar inte nämnvärt till irbesartans farmakologiska aktivitet.
In vitro-studier tyder på att irbesartan oxideras främst av CYP2C9; metabolismen av CYP3A4 är försumbar.
Exkretion
Irbesartan och dess metaboliter utsöndras via både galla och njurar. Efter antingen oral eller intravenös administrering av 14C-märkt irbesartan, återfinns cirka 20 % av radioaktiviteten i urinen och resten i avföringen, som irbesartan eller irbesartanglukuronid.
Specifika populationer
Sex
Inga könsrelaterade skillnader i farmakokinetiken har observerats hos friska äldre (ålder 65–80 år) eller hos friska unga (ålder 18–40 år). I studier av hypertonipatienter förelåg ingen könsskillnad i halveringstid eller ackumulering, men något högre plasmakoncentrationer av irbesartan har observerats hos kvinnor (11%–44%). Ingen könsrelaterad dosjustering är nödvändig.
Geriatri
Hos äldre försökspersoner (ålder 65–80 år) är halveringstiden för irbesartan inte signifikant förändrad, men AUC- och Cmax-värdena är cirka 20 % till 50 % högre än hos unga försökspersoner (åldern 18–40 år). Ingen dosjustering är nödvändig hos äldre.
Ras/etnicitet
Hos friska svarta försökspersoner är AUC-värdena för irbesartan cirka 25 % högre än hos vita; det finns ingen skillnad i Cmax-värden.
Nedsatt njurfunktion
Farmakokinetiken för irbesartan förändras inte hos patienter med nedsatt njurfunktion eller hos patienter i hemodialys. Irbesartan avlägsnas inte genom hemodialys. Ingen dosjustering är nödvändig hos patienter med lätt till gravt nedsatt njurfunktion såvida inte en patient med nedsatt njurfunktion också är volymbrist [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och DOSERING OCH ADMINISTRERING ].
Leverinsufficiens
Farmakokinetiken för irbesartan efter upprepad oral administrering påverkas inte signifikant hos patienter med mild till måttlig levercirros. Ingen dosjustering är nödvändig hos patienter med leverinsufficiens.
Läkemedelsinteraktioner
In vitro-studier visar signifikant hämning av bildningen av oxiderade irbesartanmetaboliter med de kända cytokrom CYP2C9-substraten/hämmarna sulfenazol, tolbutamid och nifedipin. I kliniska studier var dock konsekvenserna av samtidig behandling med irbesartan på farmakodynamiken för warfarin försumbara. Baserat på in vitro-data kan ingen interaktion förväntas med läkemedel vars metabolism är beroende av cytokrom P450 isoenzymer 1A1, 1A2, 2A6, 2B6, 2D6, 2E1 eller 3A4.
I separata studier av patienter som fått underhållsdoser av warfarin, hydroklortiazid eller digoxin, har administrering av irbesartan under 7 dagar ingen effekt på farmakodynamiken för warfarin (protrombintid) eller farmakokinetiken för digoxin. Irbesartans farmakokinetik påverkas inte av samtidig administrering av nifedipin eller hydroklortiazid.
Kliniska studier
Hypertoni
De antihypertensiva effekterna av AVAPRO undersöktes i 7 placebokontrollerade 8- till 12-veckorsstudier på patienter med ett diastoliskt blodtryck på 95 till 110 mmHg. Doser på 1 till 900 mg inkluderades i dessa prövningar för att helt utforska dosintervallet för irbesartan. Dessa studier möjliggjorde jämförelse av kurer en eller två gånger dagligen vid 150 mg/dag, jämförelser av topp- och daleffekter och jämförelser av respons efter kön, ålder och ras. Två av de sju placebokontrollerade studierna som identifierats ovan undersökte de antihypertensiva effekterna av irbesartan och hydroklortiazid i kombination.
De 7 studierna av irbesartan monoterapi omfattade totalt 1915 patienter randomiserade till irbesartan (1–900 mg) och 611 patienter randomiserade till placebo. En gång dagligen doser på 150 mg och 300 mg gav statistiskt och kliniskt signifikanta sänkningar av systoliskt och diastoliskt blodtryck med daleffekter (24 timmar efter dosering) efter 6 till 12 veckors behandling jämfört med placebo, på cirka 8–10/ 5–6 mmHg respektive 8–12/5–8 mmHg. Ingen ytterligare ökning av effekten sågs vid doser större än 300 mg. Dos-responssambanden för effekter på systoliskt och diastoliskt tryck visas i figurerna 1 och 2.
Figur 1: Placebo-subtraherad minskning i dal SeSBP; integrerad analys
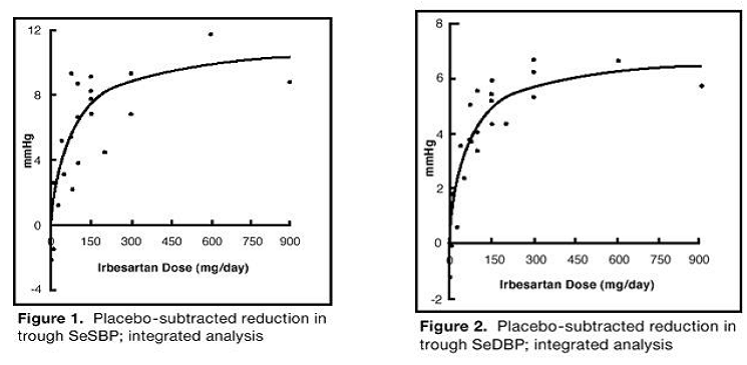
Figur 2: Placebo-subtraherad minskning av dal SeSBP; integrerad analys
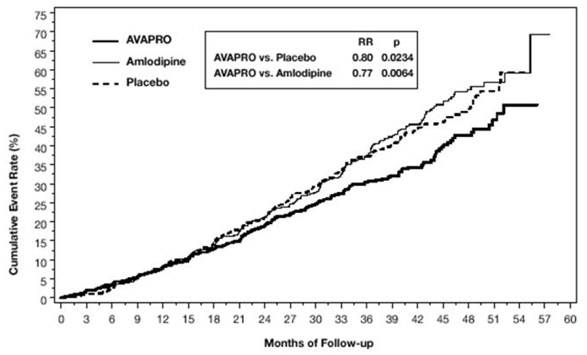
Administrering en gång dagligen av terapeutiska doser av irbesartan gav maximala effekter efter cirka 3 till 6 timmar och, i en ambulatorisk blodtrycksövervakningsstudie, återigen cirka 14 timmar. Detta sågs med både dosering en gång dagligen och två gånger dagligen. Förhållandet mellan dal och topp för systoliskt och diastoliskt svar var i allmänhet mellan 60 % och 70 %. I en kontinuerlig ambulatorisk blodtrycksövervakningsstudie gav dosering en gång dagligen med 150 mg dalsvar och genomsnittliga 24-timmarssvar liknande de som observerades hos patienter som fick dosering två gånger dagligen med samma totala dagliga dos.
I kontrollerade studier gav tillägg av irbesartan till hydroklortiaziddoser på 6,25 mg, 12,5 mg eller 25 mg ytterligare dosrelaterade blodtryckssänkningar liknande de som uppnås med samma monoterapidos av irbesartan. HCTZ hade också en ungefär additiv effekt.
Analys av ålder, kön och ras undergrupper av patienter visade att män och kvinnor, och patienter över och under 65 år, hade generellt liknande svar. Irbesartan var effektivt för att sänka blodtrycket oavsett ras, även om effekten var något mindre hos svarta (vanligtvis en population med låg reninhalt).
Effekten av irbesartan är uppenbar efter den första dosen och den är nära sin fulla observerade effekt efter 2 veckor. Vid slutet av en 8-veckors exponering var cirka 2/3 av den antihypertensiva effekten fortfarande närvarande en vecka efter den sista dosen. Rebound-hypertoni observerades inte. Det var i huvudsak ingen förändring i genomsnittlig hjärtfrekvens hos irbesartanbehandlade patienter i kontrollerade studier.
Nefropati hos typ 2-diabetespatienter
Irbesartan Diabetic Nephropathy Trial (IDNT) var en randomiserad, placebo- och aktivkontrollerad, dubbelblind, multicenterstudie utförd över hela världen på 1715 patienter med typ 2-diabetes, hypertoni (SeSBP >135 mmHg eller SeDBP >85 mmHg) och nefropati (serum) kreatinin 1,0 till 3,0 mg/dL hos kvinnor eller 1,2 till 3,0 mg/dL hos män och proteinuri ≥900 mg/dag). Patienterna randomiserades till att få AVAPRO 75 mg, amlodipin 2,5 mg eller matchande placebo en gång dagligen. Patienterna titrerades till en underhållsdos av AVAPRO 300 mg, eller amlodipin 10 mg, allt efter tolerans. Ytterligare antihypertensiva medel (exklusive ACE-hämmare, angiotensin II-receptorantagonister och kalciumkanalblockerare) tillsattes vid behov för att uppnå blodtrycksmålet (≤135/85 eller 10 mmHg sänkning av systoliskt blodtryck om högre än 160 mmHg) för patienter i alla grupper .
Studiepopulationen var 66,5 % män, 72,9 % under 65 år och 72 % vita (asiatiska/Stillahavsöbor 5,0 %, svarta 13,3 %, latinamerikaner 4,8 %). Medelvärdet för sittande systoliska och diastoliska blodtryck vid baslinjen var 159 mmHg respektive 87 mmHg. Patienterna gick in i studien med ett genomsnittligt serumkreatinin på 1,7 mg/dL och en genomsnittlig proteinuri på 4144 mg/dag.
Det genomsnittliga blodtrycket som uppnåddes var 142/77 mmHg för AVAPRO, 142/76 mmHg för amlodipin och 145/79 mmHg för placebo. Totalt fick 83,0 % av patienterna måldosen av irbesartan mer än 50 % av gångerna. Patienterna följdes under en genomsnittlig varaktighet av 2,6 år.
Det primära sammansatta effektmåttet var tiden tills någon av följande händelser inträffade: fördubbling av baslinjeserumkreatinin, njursjukdom i slutstadiet (ESRD; definierad av serumkreatinin ≥6 mg/dL, dialys eller njurtransplantation) eller dödsfall . Behandling med AVAPRO 150 mg resulterade i 20 % riskreduktion jämfört med placebo (p=0,0234) (se figur 3 och tabell 1). Behandling med AVAPRO 150 mg minskade också förekomsten av ihållande fördubbling av serumkreatinin som ett separat effektmått (33 %), men hade ingen signifikant effekt på enbart ESRD och ingen effekt på den totala dödligheten (se tabell 1).
Figur 3: IDNT: Kaplan-Meier-uppskattningar av primärt slutpunkt (fördubbling av serumkreatinin, njursjukdom i slutstadiet eller dödlighet av alla orsaker)
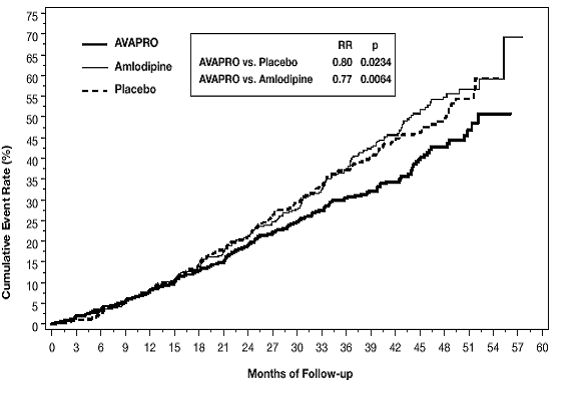
Andelen patienter som upplever en händelse under studiens gång kan ses i tabell 1 nedan:
Studiens sekundära effektmått var en sammansättning av kardiovaskulär mortalitet och sjuklighet (hjärtinfarkt, sjukhusvistelse för hjärtsvikt, stroke med permanent neurologisk underskott, amputation). Det fanns inga statistiskt signifikanta skillnader mellan behandlingsgrupperna i dessa effektmått. Jämfört med placebo minskade AVAPRO 150 mg proteinuri signifikant med cirka 27 %, en effekt som var uppenbar inom 3 månader efter påbörjad behandling. AVAPRO minskade signifikant graden av förlust av njurfunktion (glomerulär filtrationshastighet), mätt som den reciproka serumkreatininkoncentrationen, med 18,2 %.
Tabell 2 visar resultat för demografiska undergrupper. Undergruppsanalyser är svåra att tolka, och det är inte känt om dessa observationer representerar verkliga skillnader eller slumpmässiga effekter. För den primära effektmåttet sågs AVAPROs gynnsamma effekter hos patienter som också tog andra blodtryckssänkande läkemedel (angiotensin II-receptorantagonister, angiotensin-konverterande enzym-hämmare och kalciumkanalblockerare var inte tillåtna), orala hypoglykemiska medel och lipid- sänkningsmedel.
PATIENTINFORMATION
Graviditet
Informera kvinnliga patienter i fertil ålder om konsekvenserna av exponering för AVAPRO under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Patienter bör uppmanas att rapportera graviditeter till sin läkare så snart som möjligt.
Kaliumtillskott
Råda patienter som får AVAPRO att inte använda kaliumtillskott eller saltersättningsmedel som innehåller kalium utan att rådfråga sin vårdgivare [se LÄKEMEDELSINTERAKTIONER ].
