Adalat 10mg, 20mg, 30mg Nifedipine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Adalat och hur används det?
Adalat är ett receptbelagt läkemedel som används för att behandla symtomen på bröstsmärtor (Angina), högt blodtryck (hypertoni) och pulmonell hypertoni. Adalat 30mg kan användas ensamt eller tillsammans med andra läkemedel.
Adalat 20mg tillhör en klass av läkemedel som kallas kalciumkanalblockerare; Kalciumkanalblockerare, dihydropyridin.
Det är inte känt om Adalat 30 mg är säkert och effektivt för barn yngre än 6 år.
Vilka är de möjliga biverkningarna av Adalat 10mg?
Adalat kan orsaka allvarliga biverkningar inklusive:
- nässelfeber,
- svårt att andas,
- svullnad i ansiktet eller halsen,
- feber,
- öm hals,
- brännande ögon,
- smärta i huden,
- röda eller lila hudutslag med blåsor och fjällning,
- förvärrade bröstsmärtor,
- bultande hjärtslag,
- fladdrande i ditt bröst,
- yrsel,
- svullnad i händer eller underben,
- ont i övre magen, och
- gulfärgning av huden eller ögonen (gulsot)
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Adalat inkluderar:
- svullnad,
- rodnad (värme, rodnad eller stickningar),
- huvudvärk,
- yrsel,
- illamående,
- halsbränna och
- känner sig svag eller trött
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Adalat. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Adalat® CC är en tablettdoseringsform med förlängd frisättning av kalciumkanalblockeraren nifedipin. Nifedipin är 3,5-pyridindikarboxylsyra, 1,4-dihydro-2,6-dimetyl-4-(2-nitrofenyl)-dimetylester, C17H18N2O6, och har strukturformeln:
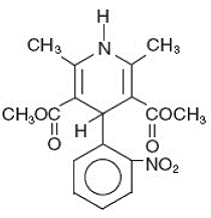
Nifedipin är ett gult kristallint ämne, praktiskt taget olösligt i vatten men lösligt i etanol. Den har en molekylvikt på 346,3. Adalat CC tabletter består av ett yttre hölje och en inre kärna. Båda innehåller nifedipin, pälsen som en formulering med långsam frisättning och kärnan som en formulering med snabb frisättning. Adalat CC tabletter innehåller antingen: 30, 60 eller 90 mg nifedipin för oral administrering en gång om dagen.
Inerta ingredienser i formuleringen är: hydroxipropylcellulosa, laktos, majsstärkelse, krospovidon, mikrokristallin cellulosa, kiseldioxid och magnesiumstearat. De inerta ingredienserna i filmbeläggningen för Adalat 30mg CC 30 och 60 är: hypromellos, polyetylenglykol, järnoxid och titandioxid. De inerta ingredienserna i filmbeläggningen för Adalat 20mg CC 90 är: hypromellos, polyetylenglykol och järnoxid
INDIKATIONER
Adalat 10mg CC är indicerat för behandling av hypertoni. Det kan användas ensamt eller i kombination med andra antihypertensiva medel.
DOSERING OCH ADMINISTRERING
Doseringen bör anpassas efter varje patients behov. Det rekommenderas att Adalat 20 mg CC administreras oralt en gång dagligen på fastande mage. Adalat 10mg CC är en doseringsform med förlängd frisättning och tabletter ska sväljas hela, inte bitas eller delas. I allmänhet bör titreringen fortgå under en 7-14 dagars period med början med 30 mg en gång dagligen. Titrering uppåt bör baseras på terapeutisk effekt och säkerhet. Den vanliga underhållsdosen är 30 mg till 60 mg en gång dagligen. Titrering till doser över 90 mg dagligen rekommenderas inte.
Om avbrytande av Adalat 30 mg CC är nödvändigt, tyder god klinisk praxis på att dosen bör minskas gradvis under noggrann övervakning av läkare.
Samtidig administrering av nifedipin och grapefruktjuice ska undvikas (se KLINISK FARMAKOLOGI och FÖRSIKTIGHETSÅTGÄRDER ).
Försiktighet bör iakttas vid dispensering av Adalat CC för att säkerställa att doseringsformen för förlängd frisättning har ordinerats.
HUR LEVERERAS
Adalat CC tabletter med förlängd frisättning tillhandahålls som 30 mg, 60 mg och 90 mg runda filmdragerade tabletter. De olika styrkorna kan identifieras enligt följande:
Adalat® CC tabletter levereras i:
Tabletterna ska skyddas från ljus och fukt och förvaras under 86°F (30°C). Dispensera i täta, ljusbeständiga behållare.
Tillverkad för: Bayer HealthCare Pharmaceuticals Inc., Wayne, NJ 07470. Tillverkad i Tyskland. Reviderad: Dec 2015
BIEFFEKTER
Negativa upplevelser
Incidensen av biverkningar under behandling med Adalat CC i doser upp till 90 mg dagligen härleddes från placebokontrollerade multicenterstudier på 370 hypertensiva patienter. Atenolol 50 mg en gång dagligen användes samtidigt hos 187 av de 370 patienterna på Adalat CC och hos 64 av de 126 patienterna på placebo. Alla biverkningar som rapporterats under Adalat 30 mg CC-behandling tabellerades oberoende av deras orsakssamband till medicinering.
Den vanligaste biverkningen som rapporterades med Adalat 10 mg CC var perifert ödem. Detta var dosrelaterat och frekvensen var 18 % på Adalat 30 mg CC 30 mg dagligen, 22 % på Adalat 30 mg CC 60 mg dagligen och 29 % på Adalat 10 mg CC 90 mg dagligen jämfört med 10 % på placebo.
Andra vanliga biverkningar som rapporterats i ovanstående placebokontrollerade studier inkluderar:
Om frekvensen av biverkningar med Adalat 20 mg CC och placebo är likartad kan orsakssamband inte fastställas.
Följande biverkningar rapporterades med en incidens på 3 % eller mindre i dagliga doser upp till 90 mg:
Kroppen som helhet/systemisk: bröstsmärtor, smärta i benen
Centrala nervsystemet: parestesi, svindel
Dermatologiska: utslag
Gastrointestinala: förstoppning
Muskuloskeletala: benkramper
Andningsvägar: näsblod, rinit
Urogenital: impotens, urinfrekvens
Andra biverkningar som rapporterades med en incidens på mindre än 1,0 % var:
Kroppen som helhet/systemisk: allergisk reaktion, asteni, cellulit, substernal bröstsmärta, frossa, ansiktsödem, onormalt labbtest, sjukdomskänsla, nacksmärta, bäckensmärta, smärta, ljuskänslighetsreaktion Kardiovaskulär: förmaksflimmer, bradykardi, hjärtstillestånd, extrasystoli, hypotoni, migrän, hjärtklappning , flebit, postural hypotoni, takykardi, kutana angiektaser
Centrala nervsystemet: ångest, förvirring, minskad libido, depression, hypertoni, hypestesi, sömnlöshet, somnolens
Dermatologiska: angioödem, petekialutslag, klåda, svettning
Gastrointestinala: buksmärtor, diarré, muntorrhet, dysfagi, dyspepsi, eruktation, esofagit, flatulens, gastrointestinala störningar, gastrointestinala blödningar, ökad GGT, tandköttsstörning, tandköttsblödning, kräkningar
Hematologiska: eosinofili, lymfadenopati
Metaboliskt: gikt, viktminskning
Muskuloskeletala: artralgi, artrit, ledsjukdom, myalgi, myasteni
Andningsvägar: dyspné, ökad hosta, raser, faryngit, stridor
Särskilda sinnen: onormal syn, amblyopi, konjunktivit, diplopi, ögonsjukdom, ögonblödning, tinnitus
Urogenital/reproduktiv: dysuri, njursten, natturi, bröstöverfyllnad, polyuri, urogenital störning, erektil dysfunktion (ED)
Följande biverkningar har rapporterats i sällsynta fall hos patienter som fått nifedipin i pälskärnan eller andra formuleringar: allergen hepatit, alopeci, anafylaktisk reaktion, anemi, artrit med ANA (+), depression, erytromelalgi, exfoliativ dermatit, feber, gingival hyperplasi, gynekomasti, hyperglykemi, gulsot, leukopeni, humörförändringar, muskelkramper, nervositet, paranoid syndrom, purpura, skakighet, sömnstörningar, Stevens-Johnsons syndrom, synkope, smakperversion, trombocytopeni, toxisk epidermal nekrolys, övergående blindhet vid toppen av plasmanivån, tremor och urtikaria.
LÄKEMEDELSINTERAKTIONER
Nifedipin elimineras huvudsakligen genom metabolism och är ett substrat för CYP3A. Hämmare och inducerare av CYP3A kan påverka exponeringen för nifedipin och följaktligen dess önskvärda och oönskade effekter. In vitro- och in vivo-data indikerar att nifedipin kan hämma metabolismen av läkemedel som är substrat för CYP3A och därigenom öka exponeringen för andra läkemedel. Nifedipin är ett vasodilator, och samtidig administrering av andra läkemedel som påverkar blodtrycket kan resultera i farmakodynamiska interaktioner.
CYP3A-hämmare
CYP3A-hämmare såsom ketokonazol, flukonazol, itrakonazol, klaritromycin, erytromycin (Azitromycin, även om det är strukturellt besläktat med klassen av makrolidantibiotika saknar kliniskt relevant CYP3A4-hämning), grapefrukt, ritazodon, fluquinaviretin, fluquinaviretin, mayfina, savira, indianvirona, savira i ökad exponering för nifedipin vid samtidig administrering. Noggrann övervakning och dosjustering kan vara nödvändig; överväg att påbörja nifedipin med den lägsta tillgängliga dosen om det ges samtidigt med dessa mediciner.
Starka CYP3A-inducerare
Starka CYP3A-inducerare, såsom rifampin, rifabutin, fenobarbital, fenytoin, karbamazepin och johannesört minskar biotillgängligheten och effekten av nifedipin; därför ska nifedipin inte användas i kombination med starka CYP3A-inducerare som rifampin (se KONTRAINDIKATIONER ).
Kardiovaskulära läkemedel
Antiarytmika
Kinidin: Kinidin är ett substrat för CYP3A och har visats hämma CYP3A in vitro. Samtidig administrering av flera doser kinidinsulfat, 200 mg tid, och nifedipin, 20 mg tid, ökade Cmax och AUC för nifedipin hos friska frivilliga med faktorer på 2,30 respektive 1,37. Hjärtfrekvensen i det initiala intervallet efter läkemedelsadministrering ökades med upp till 17,9 slag/minut. Exponeringen för kinidin förändrades inte väsentligt i närvaro av nifedipin. Övervakning av hjärtfrekvens och justering av nifedipindosen, om nödvändigt, rekommenderas när kinidin läggs till en behandling med nifedipin.
Flekainid: Det har funnits för lite erfarenhet av samtidig administrering av Tambocor och nifedipin för att rekommendera samtidig användning.
Kalciumkanalblockerare
Diltiazem: Förbehandling av friska frivilliga med 30 mg eller 90 mg tid diltiazem po ökade AUC för nifedipin efter en engångsdos på 20 mg nifedipin med faktorer på 2,2 respektive 3,1. Motsvarande Cmax-värden för nifedipin ökade med faktorerna 2,0 respektive 1,7. Försiktighet bör iakttas vid samtidig administrering av diltiazem och nifedipin och en minskning av dosen av nifedipin bör övervägas.
Verapamil: Verapamil, en CYP3A-hämmare, kan hämma metabolismen av nifedipin och öka exponeringen för nifedipin vid samtidig behandling. Blodtrycket bör övervakas och minskning av nifedipindosen övervägas.
ACE-hämmare
Benazepril: Hos friska frivilliga som fick en engångsdos på 20 mg nifedipin ER och benazepril 10 mg var plasmakoncentrationerna av benazeprilat och nifedipin i närvaro och frånvaro av varandra inte statistiskt signifikant olika. En hypotensiv effekt sågs endast efter samtidig administrering av de två läkemedlen. Den takykardiska effekten av nifedipin försvagades i närvaro av benazepril.
Angiotensin-II-blockerare
Irbesartan: In vitro-studier visar signifikant hämning av nifedipins bildning av oxiderade irbesartanmetaboliter. I kliniska studier hade dock samtidig nifedipin ingen effekt på irbesartans farmakokinetik.
Candesartan: Inga signifikanta läkemedelsinteraktioner har rapporterats i studier med candesartan cilexitil givet tillsammans med nifedipin. Eftersom kandesartan inte metaboliseras signifikant av cytokrom P450-systemet och vid terapeutiska koncentrationer inte har någon effekt på cytokrom P450-enzymer, skulle interaktioner med läkemedel som hämmar eller metaboliseras av dessa enzymer inte förväntas.
Betablockerare
Adalat 10 mg CC tolererades väl när det administrerades i kombination med betablockerare till 187 hypertensiva patienter i en placebokontrollerad klinisk prövning. Det har dock förekommit enstaka litteraturrapporter som tyder på att kombinationen nifedipin och beta-adrenerga blockerande läkemedel kan öka sannolikheten för kronisk hjärtsvikt, allvarlig hypotoni eller förvärring av angina hos patienter med hjärt-kärlsjukdom. Klinisk övervakning rekommenderas och en dosjustering av nifedipin bör övervägas.
Timolol: Hypotension är mer sannolikt att uppstå om dihydropryridinkalciumantagonister som nifedipin administreras samtidigt med timolol.
Centrala Alpha1-blockerare
Doxazosin: Friska frivilliga som deltog i en interaktionsstudie med flera doser av doxazosin-nifedipin fick 2 mg doxazosin en gång dagligen eller i kombination med 20 mg nifedipin ER två gånger dagligen. Samtidig administrering av nifedipin resulterade i en minskning av AUC och Cmax för doxazosin till 83 % och 86 % av värdena i frånvaro av nifedipin, respektive. I närvaro av doxazosin ökade AUC och Cmax för nifedipin med faktorer på 1,13 respektive 1,23. Jämfört med nifedipin monoterapi var blodtrycket lägre i närvaro av doxazosin. Blodtrycket bör övervakas när doxazosin administreras samtidigt med nifedipin, och dosminskning av nifedipin bör övervägas.
Digitalis
Digoxin: Samtidig administrering av nifedipin och digoxin kan leda till minskat clearance vilket resulterar i en ökning av plasmakoncentrationen av digoxin. Eftersom det har förekommit enstaka rapporter om patienter med förhöjda digoxinnivåer, och det finns en möjlig interaktion mellan digoxin och Adalat CC, rekommenderas att digoxinnivåerna övervakas vid start, justering och utsättning av Adalat 10 mg CC för att undvika eventuell över- eller under- digitalisering.
Antitrombotika
Kumariner: Det har förekommit sällsynta rapporter om ökad protrombintid hos patienter som tar kumarinantikoagulantia till vilka nifedipin administrerats. Relationen till nifedipinbehandling är dock osäker.
Trombocytaggregationshämmare
Clopidogrel: Inga kliniskt signifikanta farmakodynamiska interaktioner observerades när klopidrogrel administrerades samtidigt med nifedipin.
Tirofiban: Samtidig administrering av nifedipin förändrade inte exponeringen för tirofiban väsentligt.
Övrig
Diuretika, PDE5-hämmare, alfa-metyldopa: Nifedipin kan öka den blodtryckssänkande effekten av dessa samtidigt administrerade medel.
Icke-kardiovaskulära läkemedel
Antimykotika
Ketokonazol, itrakonazol och flukonazol är CYP3A-hämmare och kan hämma metabolismen av nifedipin och öka exponeringen för nifedipin vid samtidig behandling. Blodtrycket bör övervakas och en dosreduktion av nifedipin övervägas.
Antisekretoriska droger
Omeprazol: Hos friska frivilliga som fick en engångsdos på 10 mg nifedipin var AUC och Cmax för nifedipin efter förbehandling med omeprazol 20 mg dagligen under 8 dagar 1,26 och 0,87 gånger högre än efter förbehandling med placebo. Förbehandling med eller samtidig administrering av omeprazol påverkade inte effekten av nifedipin på blodtryck eller hjärtfrekvens. Effekten av omeprazol på nifedipin är sannolikt inte av klinisk relevans.
Pantoprazol: Hos friska frivilliga förändrades exponeringen för inget av läkemedlen signifikant i närvaro av det andra läkemedlet.
Ranitidin: Fem studier på friska frivilliga undersökte effekten av multipla ranitidindoser på farmakokinetiken för enkel- eller multipeldos av nifedipin. Två studier undersökte effekten av samtidigt administrerat ranitidin på blodtrycket hos hypertensiva patienter på nifedipin. Samtidig administrering av ranitidin hade inga relevanta effekter på exponeringen för nifedipin som påverkade blodtrycket eller hjärtfrekvensen hos normotensiva eller hypertensiva patienter.
Cimetidin: Fem studier på friska frivilliga undersökte effekten av multipla cimetidindoser på farmakokinetiken för enkel- eller multipeldos av nifedipin. Två studier undersökte effekten av samtidigt administrerat cimetidin på blodtrycket hos hypertensiva patienter på nifedipin. Hos normotensiva patienter som fick engångsdoser på 10 mg eller flera doser på upp till 20 mg nifedipin enbart eller tillsammans med cimetidin upp till 1000 mg/dag, var AUC-värdena för nifedipin i närvaro av cimetidin mellan 1,52 och 2,01 gånger de i frånvaro av cimetidin. Cmax-värdena för nifedipin i närvaro av cimetidin ökade med faktorer som sträckte sig mellan 1,60 och 2,02. Ökningen av exponeringen för nifedipin av cimetidin åtföljdes av relevanta förändringar i blodtryck eller hjärtfrekvens hos normotensiva patienter. Hypertonipatienter som fick 10 mg qd nifedipin ensamt eller i kombination med cimetidin 1000 mg qd upplevde också relevanta förändringar i blodtrycket när cimetidin lades till nifedipin. Interaktionen mellan cimetidin och nifedipin är av klinisk relevans och blodtrycket bör övervakas och en minskning av nifedipindosen övervägas.
Cisaprid: Samtidig administrering av cisaprid och nifedipin kan leda till ökade plasmakoncentrationer av nifedipin.
Antibakteriella läkemedel
Quinupristin/Dalfopristin: In vitro läkemedelsinteraktionsstudier har visat att quinupristin/dalfopristin signifikant hämmar CYP3A-metabolismen av nifedipin. Samtidig administrering av quinupristin/dalfopristin och nifedipin (upprepad oral dos) till friska frivilliga ökade AUC och Cmax för nifedipin med faktorer på 1,44 respektive 1,18 jämfört med nifedipin monoterapi. Vid samtidig administrering av quinupristin/dalfopristin och nifedipin bör blodtrycket övervakas och en minskning av nifedipindosen övervägas.
Erytromycin: Erytromycin, en CYP3A-hämmare, kan hämma metabolismen av nifedipin och öka exponeringen för nifedipin under samtidig behandling. Blodtrycket bör övervakas och minskning av nifedipindosen övervägas.
Antituberkulära läkemedel
Rifampin: Starka CYP3A-inducerare, såsom rifampin, rifapentin och rifabutin minskar biotillgängligheten av nifedipin, vilket kan minska effekten av nifedipin; därför ska nifedipin inte användas i kombination med starka CYP3A-inducerare som rifampin (se KONTRAINDIKATIONER ). Effekten av flera orala doser på 600 mg rifampin på farmakokinetiken för nifedipin efter en oral engångsdos på 20 mg nifedipinkapsel utvärderades i en klinisk studie. Tolv friska frivilliga män fick en oral engångsdos på 20 mg nifedipinkapsel på studiedag 1. Från och med studiedag 2 fick försökspersonerna 600 mg rifampin en gång dagligen i 14 dagar. På studiedag 15 administrerades en andra oral engångsdos på 20 mg nifedipinkapsel tillsammans med den sista dosen rifampin. Jämfört med studiedag 1 minskade 14 dagars förbehandling med rifampin Cmax och AUC för samtidigt administrerat nifedipin i genomsnitt med 95 % respektive 97 %.

Antivirala läkemedel
Amprenavir, atanazavir, delavirin, fosamprinavir, indinavir, nelfinavir och ritonavir, som CYP3A-hämmare, kan hämma metabolismen av nifedipin och öka exponeringen för nifedipin. Försiktighet är motiverad och klinisk övervakning av patienter rekommenderas.
CNS-läkemedel
Nefazodon, en CYP3A-hämmare, kan hämma metabolismen av nifedipin och öka exponeringen för nifedipin under samtidig behandling. Blodtrycket bör övervakas och en minskning av nifedipindosen bör övervägas.
Fluoxetin, en CYP3A-hämmare, kan hämma metabolismen av nifedipin och öka exponeringen för nifedipin vid samtidig behandling. Blodtrycket bör övervakas och en minskning av nifedipindosen bör övervägas.
Valproinsyra kan öka exponeringen för nifedipin under samtidig behandling. Blodtrycket bör övervakas och en dosreduktion av nifedipin övervägas.
fenytoin, fenobarbital och karbamazepin: Nifedipin metaboliseras av CYP3A. Samtidig administrering av nifedipin 10 mg kapsel och 60 mg nifedipin kapseltablett med fenytoin, en inducerare av CYP3A, sänkte AUC och Cmax för nifedipin med cirka 70 %. Fenobarbital och karbamazepin är också inducerare av CYP3A. Alternativ antihypertensiv behandling bör övervägas hos patienter som tar fenytoin, fenobarbital och karbamazepin.
Antiemetiska droger
Dolasetron: Hos patienter som tog dolasetron oralt eller intravenöst och nifedipin visades ingen effekt på clearance av hydrodolasetron.
Immunsuppressiva läkemedel
Takrolimus: Takrolimus har visats metaboliseras via CYP3A-systemet. Nifedipin har visat sig hämma metabolismen av takrolimus in vitro. Transplanterade patienter på takrolimus och nifedipin krävde från 26 % till 38 % mindre doser än patienter som inte fick nifedipin. Nifedipin kan öka exponeringen för takrolimus. När nifedipin administreras samtidigt med takrolimus bör blodkoncentrationerna av takrolimus övervakas och en minskning av takrolimusdosen övervägas.
Sirolimus: En engångsdos på 60 mg nifedipin och en engångsdos på 10 mg sirolimus oral lösning administrerades till 24 friska frivilliga. Kliniskt signifikanta farmakokinetiska läkemedelsinteraktioner observerades inte.
Glukossänkande läkemedel
Pioglitazon: Samtidig administrering av pioglitazon i 7 dagar med 30 mg nifedipin ER administrerat oralt varje dag i 4 dagar till frivilliga manliga och kvinnliga försökspersoner resulterade i minsta kvadratiska medelvärden (90 % KI) för oförändrat nifedipin på 0,83 (0,73-0,95) för Cmax och 0,88 ( 0,80-0,96) för AUC jämfört med nifedipin monoterapi. Med tanke på den höga variabiliteten av nifedipins farmakokinetik är den kliniska betydelsen av detta fynd okänd.
Rosiglitazon: Samtidig administrering av rosiglitazon (4 mg två gånger dagligen) visade sig inte ha någon kliniskt relevant effekt på farmakokinetiken för nifedipin.
Metformin: En interaktionsstudie med engångsdos metformin-nifedipin på normala friska frivilliga visade att samtidig administrering av nifedipin ökade plasmametformin Cmax och AUC med 20 % respektive 9 % och ökade mängden metformin som utsöndras i urinen. Tmax och halveringstid påverkades inte. Nifedipin verkar förbättra absorptionen av metformin.
Miglitol: Ingen effekt av miglitol observerades på farmakokinetiken och farmakodynamiken för nifedipin.
Repaglinid: Samtidig administrering av 10 mg nifedipin med en singeldos på 2 mg repaglinid (efter 4 dagar nifedipin 10 mg tid och repaglinid 2 mg tid) resulterade i oförändrade AUC- och Cmax-värden för båda läkemedlen.
akarbos: Nifedipin tenderar att producera hyperglykemi och kan leda till förlust av glukoskontrollen. Om nifedipin administreras samtidigt med akarbos, bör blodsockernivåerna övervakas noggrant och en dosjustering av nifedipin övervägas.
Läkemedel som stör matabsorptionen
Orlistat: Hos 17 normalviktiga försökspersoner som fick orlistat 120 mg tre gånger dagligen under 6 dagar, förändrade inte orlistat biotillgängligheten för 60 mg nifedipin (tabletter med förlängd frisättning).
Kosttillskott
Grapefruktjuice: Hos friska frivilliga ökade en enkeldos samtidig administrering av 250 ml dubbelstyrka grapefruktjuice med 10 mg nifedipin AUC och Cmax med faktorer på 1,35 respektive 1,13. Intag av upprepade doser av grapefruktjuice (5 x 200 ml på 12 timmar) efter administrering av 20 mg nifedipin ER ökade AUC och Cmax för nifedipin med en faktor 2. Grapefruktjuice bör undvikas av patienter på nifedipin. Intaget av grapefruktjuice ska avbrytas minst 3 dagar innan patienter påbörjas med nifedipin.
Örter
Johannesört: Johannesört är en inducerare av CYP3A och kan minska exponeringen för nifedipin. Alternativ antihypertensiv behandling bör övervägas hos patienter där johannesörtbehandling är nödvändig.
CYP2D6 probläkemedel
Debrisoquine: Hos friska frivilliga förändrade inte förbehandling med nifedipin 20 mg tre gånger dagligen under 5 dagar det metaboliska förhållandet mellan hydroxydebrisokin och debrisokin mätt i urin efter en engångsdos på 10 mg debrisokin. Det är således osannolikt att nifedipin in vivo hämmar metabolismen av andra läkemedel som är substrat för CYP2D6.
VARNINGAR
Överdriven hypotoni
Även om den hypotensiva effekten av nifedipin hos de flesta patienter är måttlig och väl tolererad, har enstaka patienter haft överdriven och dåligt tolererad hypotoni. Dessa svar har vanligtvis inträffat under initial titrering eller vid tidpunkten för efterföljande uppjustering av dos, och kan vara mer sannolikt hos patienter som samtidigt använder betablockerare.
Allvarlig hypotoni och/eller ökat behov av vätskevolym har rapporterats hos patienter som fått kapslar med omedelbar frisättning tillsammans med ett betablockerare och som genomgått kranskärlsbypassoperation med högdos fentanylanestesi. Interaktionen med högdos fentanyl verkar bero på kombinationen av nifedipin och en betablockerare, men möjligheten att den kan uppstå med enbart nifedipin, med låga doser fentanyl, vid andra kirurgiska ingrepp eller med andra narkotiska analgetika kan inte vara utesluten. Hos nifedipinbehandlade patienter där operation med högdos fentanylanestesi övervägs, bör läkaren vara medveten om dessa potentiella problem och, om patientens tillstånd tillåter det, bör tillräckligt med tid (minst 36 timmar) ges för nifedipin att tvättas ut ur kroppen före operationen.
Ökad angina och/eller hjärtinfarkt
sällsynta fall har patienter, särskilt de som har allvarlig obstruktiv kranskärlssjukdom, utvecklat väldokumenterad ökad frekvens, varaktighet och/eller svårighetsgrad av angina eller akut hjärtinfarkt vid start av nifedipin eller vid tidpunkten för dosökning. Mekanismen för denna effekt är inte fastställd.
Uttag av betablockerare
När du avbryter behandlingen med en betablockerare är det viktigt att minska dosen, om möjligt, snarare än att sluta abrupt innan du börjar med nifedipin. Patienter som nyligen avbrutits från betablockerare kan utveckla ett abstinenssyndrom med ökad angina, troligen relaterad till ökad känslighet för katekolaminer. Initiering av nifedipinbehandling kommer inte att förhindra denna förekomst och har ibland rapporterats öka den.
Hjärtsvikt
sällsynta fall har patienter (vanligtvis när de får en betablockerare) utvecklat hjärtsvikt efter att ha börjat med nifedipin. Patienter med tät aortastenos kan löpa större risk för en sådan händelse, eftersom den avlastande effekten av nifedipin förväntas vara till mindre fördel för dessa patienter, på grund av deras fasta impedans att strömma över aortaklaffen.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Hypotoni
Eftersom nifedipin minskar det perifera vaskulära motståndet, rekommenderas noggrann övervakning av blodtrycket under den initiala administreringen och titreringen av Adalat CC. Noggrann observation rekommenderas särskilt för patienter som redan tar mediciner som är kända för att sänka blodtrycket (se VARNINGAR ).
Perifert ödem
Milt till måttligt perifert ödem uppstår på ett dosberoende sätt med Adalat CC. Den placebosubtraherade frekvensen är cirka 8 % vid 30 mg, 12 % vid 60 mg och 19 % vid 90 mg dagligen. Detta ödem är ett lokaliserat fenomen som tros vara associerat med vasodilatation av beroende arterioler och små blodkärl och inte på grund av vänsterkammardysfunktion eller generaliserad vätskeretention. Hos patienter vars hypertoni kompliceras av kongestiv hjärtsvikt, bör försiktighet iakttas för att skilja detta perifera ödem från effekterna av ökande vänsterkammardysfunktion.
Användning hos cirrospatienter
Clearance av nifedipin minskar och systemisk exponering ökar hos patienter med cirros. Det är okänt hur systemisk exponering kan förändras hos patienter med måttligt eller gravt nedsatt leverfunktion. Noggrann övervakning och dosreduktion kan vara nödvändig; överväg att påbörja behandlingen med den lägsta tillgängliga dosen.
Laboratorietester
Sällsynta, vanligtvis övergående, men ibland signifikanta ökningar av enzymer såsom alkaliskt fosfatas, CPK, LDH, SGOT och SGPT har noterats. Förhållandet till nifedipinbehandling är i de flesta fall osäkert, men troligt i vissa. Dessa laboratorieavvikelser har sällan associerats med kliniska symtom; kolestas med eller utan gulsot har dock rapporterats. En liten ökning (
Nifedipin, liksom andra kalciumkanalblockerare, minskar trombocytaggregationen in vitro. Begränsade kliniska studier har visat en måttlig men statistiskt signifikant minskning av trombocytaggregation och ökad blödningstid hos vissa nifedipinpatienter. Detta tros vara en funktion av hämning av kalciumtransport över trombocytmembranet. Ingen klinisk betydelse för dessa fynd har visats.
Positivt direkt Coombs-test med eller utan hemolytisk anemi har rapporterats men ett orsakssamband mellan administrering av nifedipin och positiviteten hos detta laboratorietest, inklusive hemolys, kunde inte fastställas.
Även om nifedipin har använts på ett säkert sätt hos patienter med nedsatt njurfunktion och har rapporterats ha en gynnsam effekt i vissa fall, har sällsynta reversibla förhöjningar av BUN och serumkreatinin rapporterats hos patienter med redan existerande kronisk njurinsufficiens. Förhållandet till nifedipinbehandling är osäkert i de flesta fall men troligt i vissa.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Nifedipin administrerades oralt till råttor i två år och visade sig inte vara cancerframkallande. När nifedipin gavs till råttor före parning orsakade nifedipin minskad fertilitet vid en dos som var ungefär 30 gånger den maximala rekommenderade dosen för människor. Det finns en litteraturrapport om reversibel minskning av förmågan hos mänsklig sperma erhållen från ett begränsat antal infertila män som tar rekommenderade doser av nifedipin för att binda till och befrukta ett ägg in vitro. Mutagenicitetsstudier in vivo var negativa.
Graviditet
Graviditetskategori C
Hos gnagare, kaniner och apor har nifedipin visat sig ha en mängd olika embryotoxiska, placentotoxiska, teratogena och fetotoxiska effekter, inklusive hämmade foster (råttor, möss och kaniner), digitala anomalier (råttor och kaniner), revbensdeformiteter (möss), gomspalt (möss), små moderkakor och underutvecklade chorionvilli (apor), embryonala och fosterdödsfall (råttor, möss och kaniner), förlängd graviditet (råttor; ej utvärderad hos andra arter) och minskad neonatal överlevnad (råttor; ej utvärderad i andra arter). På basis av mg/kg eller mg/m² är vissa av doserna förknippade med dessa olika effekter högre än den maximala rekommenderade dosen för människor och vissa är lägre, men alla är inom en storleksordning av den.
De digitala anomalierna som ses hos nifedipinexponerade kaninungar är slående lika de som ses hos valpar exponerade för fenytoin, och dessa liknar i sin tur de falangeala deformiteterna som är den vanligaste missbildningen som ses hos mänskliga barn med in utero exponering för fenytoin.
Utifrån tillgängliga kliniska bevis har en specifik prenatal risk inte identifierats. En ökning av perinatal asfyxi, kejsarsnitt, prematuritet och intrauterin tillväxthämning har dock rapporterats.
Noggrann övervakning av blodtrycket måste utövas hos gravida kvinnor vid administrering av nifedipin i kombination med IV magnesiumsulfat på grund av risken för ett överdrivet blodtrycksfall som kan skada modern och fostret.
Det finns inga adekvata och välkontrollerade studier på gravida kvinnor.
Ammande mödrar
Nifedipin utsöndras i modersmjölk. Ammande mödrar rekommenderas att inte amma sina barn när de tar drogen.
Pediatrisk användning
Säkerheten och effektiviteten av Adalat 30 mg CC hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Även om små farmakokinetiska studier har identifierat en ökad halveringstid och ökad Cmax och AUC (se KLINISK FARMAKOLOGI : Farmakokinetik och metabolism ), inkluderade kliniska studier av nifedipin inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling.
Patienter med galaktosintolerans
Eftersom detta läkemedel innehåller laktos bör patienter med sällsynta ärftliga problem med galaktosintolerans, total laktasbrist eller glukos-galaktosmalabsorption inte ta detta läkemedel.
ÖVERDOS
Erfarenhet av överdosering av nifedipin är begränsad. Symtom associerade med allvarlig överdosering av nifedipin inkluderar medvetslöshet, blodtrycksfall, hjärtrytmrubbningar, metabol acidos, hypoxi, kardiogen chock med lungödem. Generellt kräver överdosering med nifedipin, som leder till uttalad hypotoni, aktivt kardiovaskulärt stöd inklusive övervakning av kardiovaskulär funktion och andningsfunktion, förhöjning av extremiteter, förnuftig användning av kalciuminfusion, pressormedel och vätskor. Efter oralt intag är noggrann magsköljning indicerad, vid behov i kombination med spolning av tunntarmen. I fall som involverar överdosering av en produkt med långsam frisättning som nifedipin måste elimineringen vara så fullständig som möjligt, inklusive från tunntarmen, för att förhindra efterföljande absorption av den aktiva substansen. Ytterligare vätska eller volym måste administreras med försiktighet på grund av risken för vätskeöverbelastning.
Clearance av nifedipin förväntas vara förlängt hos patienter med nedsatt leverfunktion. Eftersom nifedipin är starkt proteinbundet är det inte troligt att dialys är till någon fördel; dock kan plasmaferes vara fördelaktigt.
Det har rapporterats ett fall av massiv överdosering med tabletter av en annan formulering med förlängd frisättning av nifedipin. De huvudsakliga effekterna av intag av cirka 4800 mg nifedipin hos en ung man som försökte begå självmord till följd av kokaininducerad depression var initial yrsel, hjärtklappning, rodnad och nervositet. Inom flera timmar efter intag utvecklades illamående, kräkningar och generaliserat ödem. Ingen signifikant hypotoni var uppenbar vid presentationen, 18 timmar efter intag. Blodkemiska abnormiteter bestod av en mild, övergående höjning av serumkreatinin och måttliga höjningar av LDH och CPK, men normal SGOT. Vitala tecken förblev stabila, inga elektrokardiografiska avvikelser noterades och njurfunktionen återgick till det normala inom 24 till 48 timmar med enbart rutinmässiga stödåtgärder. Inga långvariga följdsjukdomar observerades.
Effekten av ett enstaka 900 mg intag av nifedipinkapslar hos en deprimerad anginapatient på tricykliska antidepressiva medel var medvetslöshet inom 30 minuter efter intag, och djup hypotoni, som svarade på kalciuminfusion, pressormedel och vätskeersättning. En mängd olika EKG-avvikelser sågs hos denna patient med en historia av grenblock, inklusive sinusbradykardi och olika grader av AV-block. Dessa dikterade den profylaktiska placeringen av en temporär ventrikulär pacemaker, men försvann i övrigt spontant. Signifikant hyperglykemi sågs initialt hos denna patient, men plasmaglukosnivåerna normaliserades snabbt utan ytterligare behandling.
En ung hypertonipatient med avancerad njursvikt intog 280 mg nifedipinkapslar på en gång, vilket resulterade i markant hypotoni som svarade på kalciuminfusion och vätskor. Inga AV-överledningsavvikelser, arytmier eller uttalade förändringar i hjärtfrekvens noterades, och det fanns inte heller någon ytterligare försämring av njurfunktionen.
Bradykardiära hjärtrytmrubbningar kan behandlas symtomatiskt med ß-sympathomimetika, och vid livshotande bradykardiella störningar av hjärtrytmen kan tillfällig pacemakerbehandling rekommenderas.
KONTRAINDIKATIONER
Samtidig administrering med starka P450-inducerare, såsom rifampin, är kontraindicerad eftersom effekten av nifedipin tabletter kan minska avsevärt. (Ser LÄKEMEDELSINTERAKTIONER )
Nifedipin får inte användas i fall av kardiogen chock.
Adalat är kontraindicerat hos patienter med känd överkänslighet mot någon komponent i tabletten.
KLINISK FARMAKOLOGI
Nifedipin är en kalciumjoninflödeshämmare (långsamkanalblockerare eller kalciumjonantagonist) som hämmar det transmembrana inflödet av kalciumjoner till vaskulär glatt muskulatur och hjärtmuskel. De kontraktila processerna för vaskulär glatt muskulatur och hjärtmuskel är beroende av rörelsen av extracellulära kalciumjoner in i dessa celler genom specifika jonkanaler. Nifedipin hämmar selektivt kalciumjoninflöde över cellmembranet i vaskulär glatt muskulatur och hjärtmuskel utan att förändra serumkalciumkoncentrationerna.
Handlingsmekanism
Mekanismen genom vilken nifedipin sänker det arteriella blodtrycket involverar perifer arteriell vasodilatation och följaktligen en minskning av det perifera vaskulära motståndet. Det ökade perifera vaskulära motståndet, en underliggande orsak till hypertoni, är ett resultat av en ökning av aktiv spänning i den vaskulära glatta muskulaturen. Studier har visat att ökningen av aktiv spänning återspeglar en ökning av cytosoliskt fritt kalcium.
Nifedipin är en perifer arteriell vasodilator som verkar direkt på vaskulär glatt muskulatur. Bindningen av nifedipin till spänningsberoende och möjligen receptoropererade kanaler i vaskulär glatt muskulatur resulterar i en hämning av kalciuminflödet genom dessa kanaler. Förråd av intracellulärt kalcium i vaskulär glatt muskulatur är begränsade och beror sålunda på inflödet av extracellulärt kalcium för att sammandragning ska inträffa. Minskningen av kalciuminflödet av nifedipin orsakar arteriell vasodilatation och minskat perifert vaskulärt motstånd vilket resulterar i minskat arteriellt blodtryck.
Farmakokinetik och metabolism
Nifedipin absorberas fullständigt efter oral administrering. Biotillgängligheten för nifedipin som Adalat CC i förhållande till nifedipin med omedelbar frisättning är i intervallet 84%-89%. Efter intag av Adalat CC-tabletter under fasta, toppar plasmakoncentrationerna cirka 2,5-5 timmar med en andra liten topp eller skuldra uppenbar cirka 6-12 timmar efter dosering. Elimineringshalveringstiden för nifedipin administrerat som Adalat CC är cirka 7 timmar i motsats till den kända halveringstiden på 2 timmar för nifedipin administrerat som en kapsel med omedelbar frisättning.
När Adalat CC administreras som multipler av 30 mg tabletter över ett dosintervall på 30 mg till 90 mg, är arean under kurvan (AUC) dosproportionell; dock är den maximala plasmakoncentrationen för 90 mg dosen som ges som 3 x 30 mg 29 % högre än förutspått från 30 mg och 60 mg doserna.
Två 30 mg Adalat CC tabletter kan bytas ut mot en 60 mg Adalat CC tablett. Tre 30 mg Adalat CC-tabletter ger dock betydligt högre Cmax-värden än de efter en enstaka 90 mg Adalat 20 mg CC-tablett. Tre 30 mg tabletter bör därför inte anses utbytbara mot en 90 mg tablett.
Dosering en gång dagligen av Adalat CC under fasta resulterar i minskade fluktuationer i plasmakoncentrationen av nifedipin jämfört med tiddosering med nifedipinkapslar med omedelbar frisättning. Den genomsnittliga maximala plasmakoncentrationen av nifedipin efter en 90 mg Adalat 30 mg CC-tablett, administrerad under fasta, är cirka 115 ng/ml. När Adalat CC ges omedelbart efter en måltid med hög fetthalt hos friska frivilliga, sker en genomsnittlig ökning med 60 % av maximal plasmakoncentration av nifedipin, en förlängning av tiden till toppkoncentration, men ingen signifikant förändring av AUC. Plasmakoncentrationer av nifedipin när Adalat 20 mg CC tas efter en fet måltid resulterar i något lägre toppar jämfört med samma dagliga dos av formuleringen med omedelbar frisättning administrerad i tre uppdelade doser. Detta kan delvis bero på att Adalat CC är mindre biotillgängligt än formuleringen för omedelbar frisättning.
Nifedipin metaboliseras i stor utsträckning till mycket vattenlösliga, inaktiva metaboliter som står för 60 % till 80 % av dosen som utsöndras i urinen. Endast spår (mindre än 0,1 % av dosen) av den oförändrade formen kan detekteras i urinen. Resten utsöndras i avföringen i metaboliserad form, troligen som ett resultat av gallutsöndring.
Nifedipin metaboliseras via cytokrom P450 3A4-systemet. Läkemedel som är kända för att antingen hämma eller inducera detta enzymsystem kan förändra den första passagen eller clearance av nifedipin.
Inga studier har utförts med Adalat 30 mg CC på patienter med njursvikt; signifikanta förändringar i farmakokinetiken för nifedipin kapslar med omedelbar frisättning har dock inte rapporterats hos patienter som genomgår hemodialys eller kronisk ambulatorisk peritonealdialys. Eftersom absorptionen av nifedipin från Adalat CC kan modifieras av njursjukdom, bör försiktighet iakttas vid behandling av sådana patienter.
Eftersom nifedipin metaboliseras via cytokrom P450 3A4-systemet kan dess farmakokinetik förändras hos patienter med kronisk leversjukdom. Adalat 20 mg CC har inte studerats hos patienter med leversjukdom; Hos patienter med nedsatt leverfunktion (levercirros) har nifedipin dock en längre eliminationshalveringstid och högre biotillgänglighet än hos friska frivilliga.
Nifedipins proteinbindningsgrad är hög (92%-98%). Proteinbindningen kan vara kraftigt reducerad hos patienter med nedsatt njur- eller leverfunktion.
Efter administrering av Adalat 30 mg CC till friska äldre män och kvinnor (ålder > 60 år) är medel-Cmax 36 % högre och den genomsnittliga plasmakoncentrationen är 70 % högre än hos yngre patienter.
Hos friska försökspersoner var elimineringshalveringstiden för en annan nifedipinformulering med fördröjd frisättning längre hos äldre försökspersoner (6,7 timmar) jämfört med unga försökspersoner (3,8 timmar) efter oral administrering. Ett minskat clearance observerades också hos äldre (348 ml/min) jämfört med unga försökspersoner (519 ml/min) efter intravenös administrering.
Samtidig administrering av nifedipin och grapefruktjuice resulterar i upp till en 2-faldig ökning av AUC och Cmax på grund av hämning av CYP3A-relaterad first-pass metabolism. Intag av grapefrukt och grapefruktjuice bör undvikas när du tar nifedipin.
Kliniska studier
Adalat 10 mg CC gav dosrelaterade sänkningar av systoliskt och diastoliskt blodtryck, vilket visats i två dubbelblinda, randomiserade, placebokontrollerade studier där över 350 patienter behandlades med Adalat CC 30, 60 eller 90 mg en gång dagligen i 6 veckor. I den första studien gavs Adalat 10 mg CC som monoterapi och i den andra studien lades Adalat 20 mg CC till en betablockerare hos patienter som inte kontrollerades med enbart en betablockerare. Det genomsnittliga dalvärdet (24 timmar efter dosering) blodtrycksresultat från dessa studier visas nedan:
MEDEL REDUKTIONER I DAGLIGA BLODTRYCK (mmHg) SYSTOLISK/DIASTOLISK
Lägsta/topp-kvoten uppskattad från 24-timmars blodtrycksövervakning varierade från 41%-78% för diastoliskt och 46%-91% för systoliskt blodtryck.
Hemodynamik
Liksom andra långsamma-kanalblockerare utövar nifedipin en negativ inotrop effekt på isolerad myokardvävnad. Detta ses sällan, om aldrig, hos intakta djur eller människor, förmodligen på grund av reflexsvar på dess vasodilaterande effekter. Hos människa minskar nifedipin det perifera vaskulära motståndet vilket leder till ett fall i systoliskt och diastoliskt tryck, vanligtvis minimalt hos normotensiva frivilliga (mindre än 5-10 mm Hg systoliskt), men ibland större. Med Adalat 30mg CC åtföljs dessa blodtryckssänkningar inte av någon signifikant förändring i hjärtfrekvensen. Hemodynamiska studier av formuleringen av nifedipin med omedelbar frisättning hos patienter med normal ventrikulär funktion har generellt sett en liten ökning av hjärtindex utan större effekter på ejektionsfraktion, vänsterkammars slutdiastoliska tryck (LVEDP) eller volym (LVEDV). Hos patienter med nedsatt kammarfunktion har de flesta akuta studier visat en viss ökning av ejektionsfraktionen och minskning av fyllnadstrycket i vänster kammare.
Elektrofysiologiska effekter
Även om nifedipin, liksom andra medlemmar i sin klass, orsakar en lätt försämring av sinoatrial nodfunktion och atrioventrikulär ledning i isolerade myokardpreparat, har sådana effekter inte setts i studier på intakta djur eller på människa. I formella elektrofysiologiska studier, huvudsakligen hos patienter med normala ledningssystem, har nifedipin administrerat som kapsel med omedelbar frisättning inte haft någon tendens att förlänga atrioventrikulär överledning eller sinusknutans återhämtningstid, eller att sakta ner sinushastigheten.
PATIENTINFORMATION
Adalat CC är en tablett med förlängd frisättning och ska sväljas hel och tas på fastande mage. Det ska inte administreras tillsammans med mat. Tugga, dela eller krossa inte tabletter.
