Benicar 10mg, 20mg, 40mg Olmesartan Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Benicar 40mg och hur används det?
Benicar är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni). Benicar 10mg kan användas ensamt eller tillsammans med andra läkemedel.
Benicar är en angiotensin II-receptorblockerare eller ARB.
Det är inte känt om Benicar är säkert och effektivt för barn yngre än 6 år.
Vilka är de möjliga biverkningarna av Benicar 40mg?
Benicar kan orsaka allvarliga biverkningar inklusive:
- yrsel
- lite eller ingen urinering
- svullnad i händer eller fötter
- illamående
- svaghet
- pirrig känsla
- bröstsmärta
- snabba eller oregelbundna hjärtslag
- förlust av rörelse
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Benicar inkluderar:
- yrsel
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Benicar. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
- När graviditet upptäcks, avbryt Benicar 40mg så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER]
- Läkemedel som verkar direkt på renin-angiotenerna i systemet kan orsaka skador och dödsfall för fostret under utveckling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER]
BESKRIVNING
Olmesartanmedoxomil, en prodrug, hydrolyseras till olmesartan under absorption från mag-tarmkanalen. Olmesartan är en selektiv AT1-subtyp angiotensin II-receptorantagonist.
Olmesartanmedoxomil beskrivs kemiskt som 2,3-dihydroxi-2-butenyl 4-(1 hydroxi-1-metyletyl)-2-propyl-1-[p-(o-1H-tetrazol-5-ylfenyl)bensyl]imidazol- 5 karboxylat, cykliskt 2,3-karbonat.
Dess empiriska formel är C29H30N6O6 och dess strukturformel är:
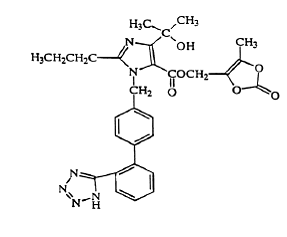
Olmesartanmedoxomil är ett vitt till ljust gulvitt pulver eller kristallint pulver med en molekylvikt på 558,59. Det är praktiskt taget olösligt i vatten och svårlösligt i metanol. Benicar 20 mg finns för oral användning som filmdragerade tabletter innehållande 5 mg, 20 mg eller 40 mg olmesartanmedoxomil och följande inaktiva ingredienser: hydroxipropylcellulosa, hypromellos, laktosmonohydrat, lågsubstituerad hydroxipropylcellulosa, magnesiumstearat, mikrokristallin cellulosa , talk, titandioxid och (endast 5 mg) gul järnoxid.
INDIKATIONER
Benicar 40 mg är indicerat för behandling av hypertoni hos vuxna och barn från sex år och äldre, för att sänka blodtrycket. Sänkning av blodtrycket minskar risken för dödliga och icke-dödliga kardiovaskulära händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade prövningar av antihypertensiva läkemedel från en mängd olika farmakologiska klasser inklusive den klass som detta läkemedel huvudsakligen tillhör. Det finns inga kontrollerade studier som visar riskminskning med Benicar.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än ett läkemedel för att uppnå blodtrycksmål. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos drogerna, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad i populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras hypertoni (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter kan förväntas att dra nytta av mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa blodtryckssänkande läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi.
Det kan användas ensamt eller i kombination med andra antihypertensiva medel.
DOSERING OCH ADMINISTRERING
Hypertoni för vuxna
Doseringen måste vara individuell. Den vanliga rekommenderade startdosen av Benicar 20 mg är 20 mg en gång dagligen när den används som monoterapi hos patienter som inte är volymkontrakterade. För patienter som behöver ytterligare sänkning av blodtrycket efter 2 veckors behandling kan dosen av Benicar ökas till 40 mg. Doser över 40 mg verkar inte ha större effekt. Dosering två gånger dagligen ger ingen fördel jämfört med samma totala dos som ges en gång dagligen.
För patienter med möjlig utarmning av intravaskulär volym (t.ex. patienter som behandlas med diuretika, särskilt de med nedsatt njurfunktion), påbörja Benicar under noggrann medicinsk övervakning och överväg att använda en lägre startdos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Pediatrisk hypertoni (6 år och äldre)
Doseringen måste vara individuell. För barn som kan svälja tabletter är den vanliga rekommenderade startdosen av Benicar 10 mg en gång dagligen för patienter som väger 20 till
Användning av Benicar 10 mg till barn VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
För barn som inte kan svälja tabletter kan samma dos ges med en extempore suspension enligt beskrivningen nedan [se KLINISK FARMAKOLOGI ]. Följ instruktionerna för beredning av suspensionen nedan för att administrera Benicar som en suspension.
Beredning av suspension (för 200 ml av en 2 mg/ml suspension)
Tillsätt 50 mL renat vatten till en bärnstensfärgad polyetylentereftalat (PET) flaska innehållande tjugo Benicar 20 mg tabletter och låt stå i minst 5 minuter. Skaka behållaren i minst 1 minut och låt suspensionen stå i minst 1 minut. Upprepa 1 minuts skakning och 1 minut stående ytterligare fyra gånger. Tillsätt 100 mL ORA-Sweet® och 50 mL ORA-Plus®* till suspensionen och skaka väl i minst 1 minut. Suspensionen ska förvaras i kylskåp vid 2-8°C (36-46°F) och kan förvaras i upp till 4 veckor. Skaka suspensionen väl före varje användning och återställ omedelbart till kylskåpet.
HUR LEVERERAS
Doseringsformer och styrkor
- 5 mg gula, runda, filmdragerade tabletter utan skåror präglade med Sankyo på ena sidan och C12 på andra sidan
- 20 mg vita, runda, filmdragerade tabletter utan skåror präglade med Sankyo på ena sidan och C14 på den andra sidan
- 40 mg vita, ovala, filmdragerade tabletter utan skåror präglade med Sankyo på ena sidan och C15 på den andra sidan
Förvaring Och Hantering
Benicar levereras som gula, runda, filmdragerade tabletter utan skåror innehållande 5 mg olmesartanmedoxomil, som vita, runda, filmdragerade, icke skårade tabletter innehållande 20 mg olmesartanmedoxomil och som vita, ovala. , filmdragerade tabletter utan skåror innehållande 40 mg olmesartanmedoxomil. Tabletterna är präglade med Sankyo på ena sidan och C12, C14 eller C15 på den andra sidan av 5, 20 respektive 40 mg tabletterna.
Tabletter levereras enligt följande:
Lagring
Förvara vid 20-25°C (68-77°F) [se USP-kontrollerad rumstemperatur].
Tillverkad för Daiichi Sankyo, Inc., Basking Ridge, NJ 07920. Reviderad: okt 2019
BIEFFEKTER
Erfarenhet av kliniska prövningar
Eftersom kliniska studier utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska studierna av ett läkemedel inte direkt jämföras med frekvensen i de kliniska studierna av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Hypertoni för vuxna
Benicar har utvärderats för säkerhet hos fler än 3825 patienter/subjekt, inklusive fler än 3275 patienter som behandlats för hypertoni i kontrollerade studier. Denna erfarenhet inkluderade cirka 900 patienter som behandlats i minst 6 månader och fler än 525 under minst 1 år. Händelserna var i allmänhet milda, övergående och hade inget samband med dosen av Benicar.
Analys av köns-, ålders- och rasgrupper visade inga skillnader mellan Benicar 40 mg och placebobehandlade patienter. Andelen utsättningar på grund av biverkningar i alla studier med hypertonipatienter var 2,4 % (dvs. 79/3278) av patienterna som behandlades med Benicar 40 mg och 2,7 % (dvs. 32/1179) av kontrollpatienterna. I placebokontrollerade studier var den enda biverkning som inträffade hos mer än 1 % av patienterna som behandlades med Benicar 20 mg och med en högre incidens jämfört med placebo yrsel (3 % vs. 1 %).
Ansiktsödem rapporterades hos fem patienter som fick Benicar. Angioödem har rapporterats med angiotensin II-antagonister.
Pediatrisk hypertoni
Inga relevanta skillnader identifierades mellan biverkningsprofilen för pediatriska patienter i åldern 1 till 16 år och den som tidigare rapporterats för vuxna patienter.
Erfarenhet efter marknadsföring
Följande biverkningar har rapporterats efter marknadsföring. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Kroppen som helhet: Asteni, angioödem, anafylaktiska reaktioner
Gastrointestinala: Kräkningar, sprue-liknande enteropati [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Metaboliska och näringsmässiga störningar: Hyperkalemi
Muskuloskeletala: Rabdomyolys
Urogenitala systemet: Akut njursvikt, ökade kreatininnivåer i blodet
Hud och bihang: Alopeci, klåda, urtikaria
Data från en kontrollerad studie och en epidemiologisk studie har antytt att högdos olmesartan kan öka kardiovaskulär (CV) risk hos diabetespatienter, men de övergripande uppgifterna är inte avgörande. Den randomiserade, placebokontrollerade, dubbelblinda ROADMAP-studien (Randomized Olmesartan And Diabetes MicroAlbuminuria Prevention trial, n=4447) undersökte användningen av olmesartan, 40 mg dagligen, kontra placebo hos patienter med typ 2-diabetes mellitus, normoalbuminuri och kl. minst en ytterligare riskfaktor för CV-sjukdom. Studien uppnådde sitt primära effektmått, fördröjd uppkomst av mikroalbuminuri, men olmesartan hade ingen gynnsam effekt på minskningen av glomerulär filtrationshastighet (GFR). Det fanns ett fynd av ökad CV-mortalitet (bedömd plötslig hjärtdöd, dödlig hjärtinfarkt, dödlig stroke, revaskulariseringsdöd) i olmesartangruppen jämfört med placebogruppen (15 olmesartan vs. 3 placebo, HR 4,9, 95 % konfidensintervall [CI ], 1,4, 17), men risken för icke-fatal hjärtinfarkt var lägre med olmesartan (HR 0,64, 95 % KI 0,35, 1,18).
Den epidemiologiska studien inkluderade patienter 65 år och äldre med en total exponering på > 300 000 patientår. I undergruppen av diabetespatienter som fick högdos olmesartan (40 mg/d) i > 6 månader verkade det finnas en ökad risk för dödsfall (HR 2,0, 95 % CI 1,1, 3,8) jämfört med liknande patienter som tog andra angiotensinreceptorblockerare. Däremot verkade högdosanvändning av olmesartan till icke-diabetespatienter vara associerad med en minskad risk för dödsfall (HR 0,46, 95 % KI 0,24, 0,86) jämfört med liknande patienter som tog andra angiotensinreceptorblockerare. Inga skillnader observerades mellan grupperna som fick lägre doser av olmesartan jämfört med andra angiotensinblockerare eller de som fick behandling i
Sammantaget väcker dessa data en oro för en möjlig ökad CV-risk i samband med användning av högdos olmesartan hos diabetespatienter. Det finns dock oro för trovärdigheten i upptäckten av ökad CV-risk, särskilt observationen i den stora epidemiologiska studien för en överlevnadsfördel hos icke-diabetiker av en storleksordning som liknar det negativa fyndet hos diabetiker.
LÄKEMEDELSINTERAKTIONER
Medel som ökar serumkalium
Samtidig användning av olmesartan med andra medel som blockerar renin-angiotensinsystemet, kaliumsparande diuretika (t.ex. spironolakton, triamteren, amilorid), kaliumtillskott, saltersättningsmedel som innehåller kalium eller andra läkemedel som kan öka kaliumnivåerna (t.ex. heparin) kan leda till ökningar av serumkalium. Om samtidig medicinering anses nödvändig är övervakning av serumkalium tillrådligt.
Icke-steroida antiinflammatoriska medel inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare)
Hos äldre patienter, volymbrist (inklusive de som får diuretikabehandling), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med angiotensin II-receptorantagonister, inklusive olmesartanmedoxomil, resultera i försämring njurfunktion, inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som får olmesartanmedoxomil och NSAID-behandling.
Den antihypertensiva effekten av angiotensin II-receptorantagonister, inklusive olmesartanmedoxomil, kan försvagas av NSAID inklusive selektiva COX-2-hämmare.
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, hyperkalemi och förändringar i njurfunktion (inklusive akut njursvikt) jämfört med monoterapi. De flesta patienter som får kombinationen av två RAS-hämmare får ingen ytterligare fördel jämfört med monoterapi. Undvik i allmänhet kombinerad användning av RAS-hämmare. Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på Benicar och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med Benicar till patienter med diabetes [se KONTRAINDIKATIONER ]. Undvik användning av aliskiren med Benicar 40 mg till patienter med nedsatt njurfunktion (GFR
Litium
Ökning av serumlitiumkoncentrationer och litiumtoxicitet har rapporterats vid samtidig administrering av litium och angiotensin II-receptorantagonister, inklusive BENICAR. Övervaka serumlitiumnivåerna vid samtidig användning.
Colesevelam hydroklorid
Samtidig administrering av gallsyrabindande medel kolesevelamhydroklorid minskar den systemiska exponeringen och maximal plasmakoncentration av olmesartan. Administrering av olmesartan minst 4 timmar före kolesevelamhydroklorid minskade läkemedelsinteraktionseffekten. Överväg att administrera olmesartan minst 4 timmar före dosen av kolesevelamhydroklorid [se KLINISK FARMAKOLOGI ].
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Fostertoxicitet
Benicar 10mg kan orsaka fosterskador när det administreras till en gravid kvinna. Användning av läkemedel som verkar på renin-angiotensinsystemet (RAS) under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt Benicar så snart som möjligt [se Användning i specifika populationer ].
Sjuklighet hos spädbarn
Användning av Benicar till barn Användning i specifika populationer ].
Hypotension hos patienter med volym- eller saltbrist
Hos patienter med ett aktiverat renin-angiotensin-aldosteronsystem, såsom volym- och/eller saltfattiga patienter (t.ex. de som behandlas med höga doser diuretika), kan symtomatisk hypotoni förväntas efter påbörjad behandling med Benicar. Inled behandlingen under noggrann medicinsk övervakning och överväg att börja med en lägre dos. Om hypotoni inträffar, placera patienten i ryggläge och vid behov ge en intravenös infusion av normal koksaltlösning [se DOSERING OCH ADMINISTRERING ]. Ett övergående hypotensivt svar är inte en kontraindikation för ytterligare behandling, som vanligtvis kan fortsätta utan svårighet när blodtrycket har stabiliserats.
Nedsatt njurfunktion
Som en konsekvens av hämning av renin-angiotensin-aldosteronsystemet kan förändringar i njurfunktionen förväntas hos känsliga personer som behandlas med Benicar. Hos patienter vars njurfunktion kan bero på aktiviteten hos renin-angiotensinaldosteronsystemet (t.ex. patienter med svår kronisk hjärtsvikt), har behandling med angiotensinkonverterande enzym (ACE)-hämmare och angiotensinreceptorantagonister associerats med oliguri och/eller progressiv azotemi. och sällan med akut njursvikt och/eller död. Liknande resultat kan förväntas hos patienter som behandlas med Benicar [se DOSERING OCH ADMINISTRERING , LÄKEMEDELSINTERAKTIONER , Användning i specifika populationer och KLINISK FARMAKOLOGI ].
I studier av ACE-hämmare hos patienter med unilateral eller bilateral njurartärstenos har ökningar av serumkreatinin eller blodureakväve (BUN) rapporterats. Det har inte förekommit någon långtidsanvändning av Benicar hos patienter med unilateral eller bilateral njurartärstenos, men liknande resultat kan förväntas.
Sprue-liknande enteropati
Allvarlig, kronisk diarré med betydande viktminskning har rapporterats hos patienter som tar olmesartan månader till år efter behandlingsstart. Intestinala biopsier av patienter visade ofta villös atrofi. Om en patient utvecklar dessa symtom under behandling med olmesartan, uteslut andra etiologier. Överväg alternativ antihypertensiv behandling i fall där ingen annan etiologi identifieras.
Hyperkalemi
Serumkalium bör övervakas hos patienter som får Benicar. Läkemedel som hämmar renin-angiotensinsystemet kan orsaka hyperkalemi. Riskfaktorer för utveckling av hyperkalemi inkluderar njurinsufficiens, diabetes mellitus och samtidig användning av kaliumsparande diuretika, kaliumtillskott och/eller kaliuminnehållande saltersättningsmedel [se LÄKEMEDELSINTERAKTIONER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Olmesartanmedoxomil var inte karcinogent när det administrerades via diet till råttor i upp till 2 år. Den högsta testade dosen (2000 mg/kg/dag) var, på mg/m2-basis, cirka 480 gånger den maximala rekommenderade humandosen (MRHD) på 40 mg/dag. Två karcinogenicitetsstudier utförda på möss, en 6-månaders sondmatningsstudie i p53 knockout-musen och en 6-månaders dietadministreringsstudie på den transgena Hras2-musen, i doser på upp till 1000 mg/kg/dag (cirka 120 gånger MRHD) , visade inga tecken på en karcinogen effekt av olmesartanmedoxomil.
Både olmesartanmedoxomil och olmesartan testades negativt i in vitro-analysen för syrisk hamsterembryocellstransformation och visade inga tecken på genetisk toxicitet i Ames-testet (bakteriell mutagenicitet). Båda visades dock inducera kromosomavvikelser i odlade celler in vitro (kinesisk hamsterlunga) och testades positivt för tymidinkinasmutationer i in vitro muslymfomanalysen. Olmesartanmedoxomil testades negativt in vivo för mutationer i MutaMouse-tarmen och njurarna och för klastogenicitet i benmärg hos mus (mikronukleustest) vid orala doser på upp till 2000 mg/kg (olmesartan ej testat).
Fertiliteten hos råttor påverkades inte av administrering av olmesartanmedoxomil i dosnivåer så höga som 1000 mg/kg/dag (240 gånger MRHD) i en studie där dosering påbörjades 2 (honor) eller 9 (hane) veckor före parning.
Användning i specifika populationer
Graviditet
Risksammanfattning
Benicar 10mg kan orsaka fosterskador när det administreras till en gravid kvinna. Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. I reproduktionsstudier på djur resulterade behandling med Benicar under organogenes i ökad embryofetal toxicitet hos råttor vid doser lägre än maternellt toxiska doser.
När graviditet upptäcks, avbryt behandlingen med Benicar så snart som möjligt. Överväg alternativ antihypertensiv behandling under graviditet.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för stora fosterskador och missfall i kliniskt erkända graviditeter 2%–4% respektive 15%–20%.
Kliniska överväganden
Sjukdomsrelaterad risk för mödrar och/eller embryo/foster
Hypertoni under graviditeten ökar moderns risk för havandeskapsförgiftning, graviditetsdiabetes, för tidig förlossning och förlossningskomplikationer (t.ex. behov av kejsarsnitt och postpartumblödning). Hypertoni ökar fostrets risk för intrauterin tillväxtbegränsning och intrauterin död. Gravida kvinnor med högt blodtryck bör övervakas noggrant och hanteras därefter.
Fetala/neonatala biverkningar
Oligohydramnios hos gravida kvinnor som använder läkemedel som påverkar renin-angiotensinsystemet under andra och tredje trimestern av graviditeten kan resultera i följande: nedsatt fosterns njurfunktion som leder till anuri och njursvikt, fosterlunghypoplasi, skelettdeformationer, inklusive skallhypoplasi, hypotoni och döden. Hos patienter som tar Benicar 20 mg under graviditet, utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Fostertestning kan vara lämpligt, baserat på graviditetsveckan. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada.
Observera noga spädbarn med tidigare exponering för Benicar 40 mg under livmodern för hypotoni, oliguri och hyperkalemi. Om oliguri eller hypotoni uppstår hos nyfödda med en historia av exponering in utero för Benicar, använd åtgärder för att upprätthålla adekvat blodtryck och renal perfusion. Utbytestransfusioner eller dialys kan krävas som ett sätt att vända hypotoni och stödja njurfunktionen.
Data
Djurdata
Inga teratogena effekter observerades när olmesartanmedoxomil administrerades till dräktiga råttor i orala doser upp till 1000 mg/kg/dag (240 gånger den maximala rekommenderade humandosen (MRHD) på mg/m2-basis) eller dräktiga kaniner i orala doser upp till 1 mg/kg/dag (halva MRHD på mg/m2-basis; högre doser kunde inte utvärderas för effekter på fosterutvecklingen eftersom de var dödliga för dosarna). Hos råttor observerades signifikanta minskningar av valparnas födelsevikt och viktökning vid doser ≥1,6 mg/kg/dag, och förseningar i utvecklingsmilstolpar (fördröjd separation av öron aurikula, utbrott av nedre framtänder, utseende av bukhår, nedstigning av testiklar, och separering av ögonlock) och dosberoende ökningar av incidensen av dilatation av njurbäckenet observerades vid doser ≥ 8 mg/kg/dag. Dosen utan observerad effekt för utvecklingstoxicitet hos råttor är 0,3 mg/kg/dag, ungefär en tiondel av MRHD på 40 mg/dag.
Laktation
Risksammanfattning
Det finns ingen information om förekomsten av olmesartan i bröstmjölk, effekterna på det ammade barnet eller effekterna på mjölkproduktionen. Olmesartan utsöndras i låg koncentration i mjölken från digivande råttor (se Data ). På grund av risken för negativa effekter på det ammande barnet bör ett beslut fattas om att avbryta amningen eller avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern.
Data
Förekomst av olmesartan i mjölk observerades efter en enstaka oral administrering av 5 mg/kg [14C] olmesartanmedoxomil till lakterande råttor.
Pediatrisk användning
De antihypertensiva effekterna av Benicar utvärderades i en randomiserad, dubbelblind klinisk studie på pediatriska patienter i åldern 1 till 16 år [se Kliniska studier ]. Farmakokinetiken för Benicar utvärderades hos pediatriska patienter i åldern 1 till 16 år [se KLINISK FARMAKOLOGI ]. Benicar 10 mg tolererades generellt väl hos pediatriska patienter och biverkningsprofilen liknade den som beskrivs för vuxna.
Benicar 20mg har inte visats vara effektivt för högt blodtryck hos barn
Användning av Benicar till barn VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Renin-angiotensin-aldosteronsystemet (RAAS) spelar en avgörande roll i njurutvecklingen. RAAS-blockad har visat sig leda till onormal njurutveckling hos mycket unga möss. Administrering av läkemedel som verkar direkt på reninangiotensinaldosteronsystemet (RAAS) kan förändra den normala njurutvecklingen.
Geriatrisk användning
Av det totala antalet hypertonipatienter som fick Benicar i kliniska studier var mer än 20 % 65 år och äldre, medan mer än 5 % var 75 år eller äldre. Inga övergripande skillnader i effektivitet eller säkerhet observerades mellan äldre patienter och yngre patienter. Andra rapporterade kliniska erfarenheter har inte identifierat skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Ökning av AUC0-∞ och Cmax observerades hos patienter med måttligt nedsatt leverfunktion jämfört med de hos matchade kontroller, med en ökning av AUC på cirka 60 %. Ingen initial dosjustering rekommenderas för patienter med måttlig till markant leverdysfunktion [se KLINISK FARMAKOLOGI ].
Nedsatt njurfunktion
Patienter med njurinsufficiens har förhöjda serumkoncentrationer av olmesartan jämfört med patienter med normal njurfunktion. Efter upprepad dosering var AUC ungefär tredubblad hos patienter med gravt nedsatt njurfunktion (kreatininclearance DOSERING OCH ADMINISTRERING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och KLINISK FARMAKOLOGI ].
Svarta patienter
Den antihypertensiva effekten av Benicar 10 mg var mindre hos svarta patienter (vanligtvis en lågreninpopulation), vilket har setts med ACE-hämmare, betablockerare och andra angiotensinreceptorblockerare.
ÖVERDOS
Begränsade data finns tillgängliga om överdosering hos människor. De mest sannolika manifestationerna av överdosering är hypotoni och takykardi; bradykardi kan uppstå om parasympatisk (vagal) stimulering inträffar. Om symptomatisk hypotoni uppstår, påbörja stödjande behandling. Dialyserbarheten av olmesartan är okänd.
KONTRAINDIKATIONER
Administrera inte aliskiren samtidigt med Benicar 20 mg till patienter med diabetes [se LÄKEMEDELSINTERAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Angiotensin II bildas från angiotensin I i en reaktion som katalyseras av angiotensinomvandlande enzym (ACE, kininas II). Angiotensin II är det huvudsakliga pressormedlet i renin-angiotensinsystemet, med effekter som inkluderar vasokonstriktion, stimulering av syntes och frisättning av aldosteron, hjärtstimulering och renal reabsorption av natrium. Olmesartan blockerar de vasokonstriktoreffekter av angiotensin II genom att selektivt blockera bindningen av angiotensin II till AT1-receptorn i vaskulär glatt muskulatur. Dess verkan är därför oberoende av vägarna för angiotensin II-syntes.
En AT2-receptor finns också i många vävnader, men denna receptor är inte känd för att vara associerad med kardiovaskulär homeostas. Olmesartan har mer än 12 500 gånger större affinitet för AT1-receptorn än för AT2-receptorn.
Blockad av renin-angiotensin-systemet med ACE-hämmare, som hämmar biosyntesen av angiotensin II från angiotensin I, är en mekanism för många läkemedel som används för att behandla hypertoni. ACE-hämmare hämmar också nedbrytningen av bradykinin, en reaktion som också katalyseras av ACE. Eftersom olmesartanmedoxomil inte hämmar ACE (kininas II), påverkar det inte svaret på bradykinin. Huruvida denna skillnad har klinisk relevans är ännu inte känt.
Blockad av angiotensin II-receptorn hämmar den negativa regulatoriska återkopplingen av angiotensin II på reninsekretion, men den resulterande ökade plasmareninaktiviteten och cirkulerande angiotensin II-nivåer övervinner inte effekten av olmesartan på blodtrycket.
Farmakodynamik
Benicar-doser på 2,5 mg till 40 mg hämmar pressoreffekterna av angiotensin I-infusion. Varaktigheten av den hämmande effekten var relaterad till dosen, med doser av Benicar >40 mg som gav >90 % hämning efter 24 timmar.
Plasmakoncentrationerna av angiotensin I och angiotensin II och plasmareninaktivitet (PRA) ökar efter engångs- och upprepad administrering av Benicar 10 mg till friska försökspersoner och hypertonipatienter. Upprepad administrering av upp till 80 mg Benicar hade minimal inverkan på aldosteronnivåerna och ingen effekt på serumkalium.
Farmakokinetik
Absorption
Olmesartanmedoxomil bioaktiveras snabbt och fullständigt genom esterhydrolys till olmesartan under absorption från mag-tarmkanalen.
Benicar-tabletter och suspensionsformuleringen framställd av Benicar-tabletter är bioekvivalenta [se DOSERING OCH ADMINISTRERING ].
Den absoluta biotillgängligheten för olmesartan är cirka 26 %. Efter oral administrering uppnås maximal plasmakoncentration (Cmax) av olmesartan efter 1 till 2 timmar. Mat påverkar inte biotillgängligheten av olmesartan. Benicar kan administreras med eller utan mat.
Distribution
Distributionsvolymen för olmesartan är cirka 17 L. Olmesartan är starkt bundet till plasmaproteiner (99 %) och penetrerar inte röda blodkroppar. Proteinbindningen är konstant vid plasmakoncentrationer av olmesartan långt över det intervall som uppnås med rekommenderade doser.
Hos råttor passerade olmesartan blod-hjärnbarriären dåligt, om alls. Olmesartan passerade över placentabarriären hos råttor och distribuerades till fostret. Olmesartan distribuerades till mjölk i låga nivåer hos råttor.
Metabolism och utsöndring
Efter den snabba och fullständiga omvandlingen av olmesartanmedoxomil till olmesartan under absorption sker praktiskt taget ingen ytterligare metabolism av olmesartan. Totalt plasmaclearance av olmesartan är 1,3 l/timme, med ett renalt clearance på 0,6 l/timme. Cirka 35 % till 50 % av den absorberade dosen återvinns i urinen medan resten elimineras i avföring via gallan.
Olmesartan verkar elimineras på ett bifasiskt sätt med en terminal halveringstid på cirka 13 timmar. Olmesartan visar linjär farmakokinetik efter orala engångsdoser på upp till 320 mg och multipla orala doser på upp till 80 mg. Steady-state-nivåer av olmesartan uppnås inom 3 till 5 dagar och ingen ackumulering i plasma sker vid dosering en gång dagligen.
Specifika populationer
Geriatriska patienter
Olmesartans farmakokinetik studerades hos äldre (≥65 år). Totalt sett var maximala plasmakoncentrationer av olmesartan likartade hos unga vuxna och äldre. Måttlig ackumulering av olmesartan observerades hos äldre vid upprepad dosering; AUCss, τ var 33 % högre hos äldre patienter, vilket motsvarar en cirka 30 % minskning av CLR [se DOSERING OCH ADMINISTRERING och Användning i specifika populationer ].
Pediatriska patienter
Olmesartans farmakokinetik studerades hos pediatriska hypertonipatienter i åldern 1 till 16 år. Clearance av olmesartan hos pediatriska patienter liknade det hos vuxna patienter när det justerades efter kroppsvikten [se Användning i specifika populationer ].
Olmesartans farmakokinetik har inte undersökts hos pediatriska patienter yngre än 1 år [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Manliga Och Kvinnliga Patienter
Mindre skillnader observerades i farmakokinetiken för olmesartan hos kvinnor jämfört med män. AUC och Cmax var 10-15 % högre hos kvinnor än hos män.
Patienter med nedsatt leverfunktion
Ökning av AUC0-∞ och Cmax observerades hos patienter med måttligt nedsatt leverfunktion jämfört med de hos matchade kontroller, med en ökning av AUC på cirka 60 % [se DOSERING OCH ADMINISTRERING och Användning i specifika populationer ].
Patienter med nedsatt njurfunktion
Hos patienter med njurinsufficiens var serumkoncentrationerna av olmesartan förhöjda jämfört med patienter med normal njurfunktion. Efter upprepad dosering var AUC ungefär tredubblad hos patienter med gravt nedsatt njurfunktion (kreatininclearance DOSERING OCH ADMINISTRERING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Läkemedelsinteraktionsstudier
Gallsyrabindande medel Colesevelam
Samtidig administrering av 40 mg olmesartanmedoxomil och 3750 mg kolesevelamhydroklorid till friska försökspersoner resulterade i 28 % minskning av Cmax och 39 % minskning av AUC för olmesartan. Mindre effekter, 4 % och 15 % minskning av Cmax respektive AUC, observerades när olmesartanmedoxomil administrerades 4 timmar före kolesevelamhydroklorid [se LÄKEMEDELSINTERAKTIONER ].
Andra studier
Inga signifikanta läkemedelsinteraktioner rapporterades i studier där olmesartanmedoxomil administrerades samtidigt med digoxin eller warfarin hos friska frivilliga.
Biotillgängligheten av olmesartan förändrades inte signifikant genom samtidig administrering av antacida [Al(OH)3/Mg(OH)2].
Olmesartanmedoxomil metaboliseras inte av cytokrom P450-systemet och har ingen effekt på P450-enzymer; således förväntas inte interaktioner med läkemedel som hämmar, inducerar eller metaboliseras av dessa enzymer.
Kliniska studier
Hypertoni för vuxna
De antihypertensiva effekterna av Benicar 10 mg har visats i sju placebokontrollerade studier vid doser från 2,5 mg till 80 mg under 6 till 12 veckor, var och en visar statistiskt signifikanta sänkningar av topp- och dalblodtryck. Totalt 2693 patienter (2145 Benicar; 548 placebo) med essentiell hypertoni studerades. Benicar 40 mg en gång dagligen sänkte det diastoliska och systoliska blodtrycket. Svaret var dosrelaterat, som visas i följande graf. En Benicar-dos på 20 mg dagligen ger en sänkning av sittande blodtryck (trough-sittande blodtryck) jämfört med placebo på cirka 10/6 mmHg och en dos på 40 mg dagligen ger en dal-sittande BP-sänkning jämfört med placebo på cirka 12/7 mmHg. Benicar 10 mg doser större än 40 mg hade liten ytterligare effekt. Början av den antihypertensiva effekten inträffade inom 1 vecka och var i stort sett manifest efter 2 veckor.
Benicar 40 mg dosrespons Placebojusterad sänkning av blodtrycket (mmHg) 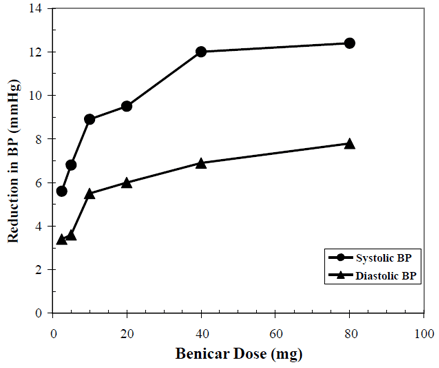
Data ovan är från sju placebokontrollerade studier (2145 Benicar-patienter, 548 placebopatienter). Den blodtryckssänkande effekten bibehölls under hela 24-timmarsperioden med Benicar en gång dagligen, med dal-till-topp-kvoter för systoliskt och diastoliskt svar mellan 60 och 80 %.
Den blodtryckssänkande effekten av Benicar 40 mg, med och utan hydroklortiazid, bibehölls hos patienter som behandlades i upp till 1 år. Det fanns inga tecken på takyfylax under långtidsbehandling med Benicar eller rebound-effekt efter abrupt utsättande av olmesartanmedoxomil efter 1 års behandling.
Den antihypertensiva effekten av Benicar var liknande hos män och kvinnor och hos patienter äldre och yngre än 65 år. Effekten var mindre hos svarta patienter (vanligtvis en population med låg reninhalt), vilket har setts med ACE-hämmare, betablockerare och andra angiotensinreceptorblockerare. Benicar hade en ytterligare blodtryckssänkande effekt när den lades till hydroklortiazid.
Det finns inga prövningar av Benicar som visar minskad kardiovaskulär risk hos patienter med hypertoni, men minst ett farmakologiskt liknande läkemedel har visat sådana fördelar.
Pediatrisk hypertoni
De antihypertensiva effekterna av Benicar 40 mg i den pediatriska populationen utvärderades i en randomiserad, dubbelblind studie med 302 hypertensiva patienter i åldern 6 till 16 år. Studiepopulationen bestod av en helt svart kohort på 112 patienter och en blandad rasgrupp på 190 patienter, inklusive 38 svarta patienter. Etiologin för hypertoni var övervägande essentiell hypertoni (87 % av den svarta kohorten och 67 % av den blandade kohorten). Patienter som vägde 20 till
samma studie fick 59 patienter i åldern 1 till 5 år som vägde ≥5 kg 0,3 mg/kg Benicar 10 mg en gång dagligen i tre veckor i en öppen fas och randomiserades sedan till att få Benicar eller placebo i en dubbelblind fas. I slutet av den andra utsättningsveckan var det genomsnittliga systoliska/diastoliska blodtrycket vid dalgången 3/3 mmHg lägre i gruppen som randomiserades till Benicar; denna skillnad i blodtryck var inte statistiskt signifikant (95 % KI -2 till 7/-1 till 7).
PATIENTINFORMATION
Graviditet
Informera kvinnliga patienter i fertil ålder om konsekvenserna av exponering för Benicar 20 mg under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Säg till patienterna att rapportera graviditeter till sin läkare så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Laktation
Avråda ammande kvinnor att inte amma under behandling med BENICAR [se Användning i specifika populationer ].
Hyperkalemi
Rekommendera patienter att inte använda kaliumtillskott eller saltersättningsmedel som innehåller kalium utan att rådfråga sin vårdgivare [se LÄKEMEDELSINTERAKTIONER ].
