Minipress 1mg, 2mg Prazosin Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Minipress och hur används det?
Minipress (prazosinhydroklorid) är en alfa-adrenerg blockerare som används för att behandla hypertoni (högt blodtryck).
Vilka är biverkningarna av Minipress 2mg?
Vanliga biverkningar av Minipress 1mg inkluderar:
- huvudvärk,
- dåsighet,
- trötthet,
- svaghet,
- suddig syn,
- illamående,
- kräkningar,
- diarré, eller
- förstoppning när din kropp anpassar sig till medicinen
Andra biverkningar av Minipress 2mg inkluderar:
- yrsel eller yrsel när du står upp, särskilt efter den första dosen och kort efter att ha tagit en dos av läkemedlet under den första veckan av behandlingen.
Tala om för din läkare om du upplever allvarliga biverkningar av Minipress 1mg inklusive snabba eller bultande hjärtslag eller fladder i bröstet, känsla av att du kan svimma, andningssvårigheter, svullnad i händer eller fötter, eller en erektion som är smärtsam eller varar i 4 timmar eller längre.
BESKRIVNING
MINIPRESS® (prazosinhydroklorid), ett kinazolinderivat, är det första i en ny kemisk klass av antihypertensiva. Det är hydrokloridsaltet av 1-(4-amino-6,7-dimetoxi-2-kinazolinyl)-4-(2-furoyl) piperazin och dess strukturformel är:
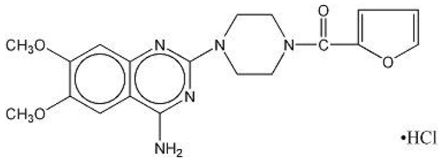
Molekylformel C19H21N5O4•HCl
Det är ett vitt, kristallint ämne, lätt lösligt i vatten och isoton saltlösning, och har en molekylvikt på 419,87. Varje 1 mg kapsel av MINIPRESS för oral användning innehåller läkemedel motsvarande 1 mg fri bas.
Inerta ingredienser i formuleringarna är: hårda gelatinkapslar (som kan innehålla Blue 1, Red 3, Red 28, Red 40 och andra inerta ingredienser); magnesiumstearat; natriumlaurylsulfat; stärkelse; sackaros.
INDIKATIONER
MINIPRESS 1mg är indicerat för behandling av hypertoni, för att sänka blodtrycket. Sänkning av blodtrycket minskar risken för dödliga och icke-dödliga kardiovaskulära händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade prövningar av antihypertensiva läkemedel från en mängd olika farmakologiska klasser, inklusive detta läkemedel.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än ett läkemedel för att uppnå blodtrycksmål. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos drogerna, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad i populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras hypertoni (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter kan förväntas att dra nytta av mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa blodtryckssänkande läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi.
MINIPRESS kan användas ensamt eller i kombination med andra blodtryckssänkande läkemedel såsom diuretika eller beta-adrenerga blockerande medel.
DOSERING OCH ADMINISTRERING
Dosen av MINIPRESS 1 mg ska justeras efter patientens individuella blodtryckssvar. Följande är en guide till dess administration:
Initial dos
1 mg två eller tre gånger om dagen (se VARNINGAR .)
Underhållsdos
Doseringen kan långsamt ökas till en total daglig dos på 20 mg i uppdelade doser. De terapeutiska doserna som oftast används har varierat från 6 mg till 15 mg dagligen, givet i uppdelade doser. Doser högre än 20 mg ökar vanligtvis inte effekten, men ett fåtal patienter kan dra nytta av ytterligare ökningar upp till en daglig dos på 40 mg i uppdelade doser. Efter initial titrering kan vissa patienter bibehållas adekvat på en doseringsregim två gånger dagligen.
Använd med andra droger
När ett diuretikum eller annat blodtryckssänkande medel tillsätts, bör dosen av MINIPRESS 1 mg minskas till 1 mg eller 2 mg tre gånger dagligen och sedan upprepas.
Samtidig administrering av MINIPRESS 1 mg med en PDE-5-hämmare kan resultera i additiv blodtryckssänkande effekt och symptomatisk hypotoni; därför bör behandling med PDE-5-hämmare inledas med den lägsta dosen hos patienter som tar MINIPRESS.
HUR LEVERERAS
Distribuerat av: Pfizer Labs, Division of Pfizer Inc., NY, NY 10017. Reviderad: feb 2015
BIEFFEKTER
Kliniska prövningar genomfördes på mer än 900 patienter. Under dessa prövningar och efterföljande marknadsföringserfarenhet är de vanligaste reaktionerna i samband med MINIPRESS-behandling: yrsel 10,3 %, huvudvärk 7,8 %, dåsighet 7,6 %, brist på energi 6,9 %, svaghet 6,5 %, hjärtklappning 5,3 % och illamående 4,9 %. I de flesta fall har biverkningar försvunnit med fortsatt behandling eller har tolererats utan någon minskning av läkemedelsdosen.
Mindre frekventa biverkningar som rapporteras förekomma hos 1-4 % av patienterna är:
Gastrointestinala: kräkningar, diarré, förstoppning.
Kardiovaskulär: ödem, ortostatisk hypotoni, dyspné, synkope.
Centrala nervsystemet: svindel, depression, nervositet.
Dermatologiska: utslag.
Genitourinära: Urinfrekvens.
EENT: dimsyn, rodnad sklera, näsblod, muntorrhet, nästäppa.
Dessutom har färre än 1 % av patienterna rapporterat följande (i vissa fall har exakta orsakssamband inte fastställts):
Gastrointestinala: bukbesvär och/eller smärta, avvikelser i leverfunktionen, pankreatit.
Kardiovaskulär: takykardi.
Centrala nervsystemet: parestesi, hallucinationer.
Dermatologiska: klåda, alopeci, lichen planus.
Genitourinära: inkontinens, impotens, priapism.
EENT: tinnitus.
Övrig: diafores, feber, positiv ANA-titer, artralgi.
Enstaka rapporter om pigmentfläckar och serös retinopati och ett fåtal rapporter om kataraktutveckling eller försvinnande har rapporterats. I dessa fall har det exakta orsakssambandet inte fastställts eftersom baslinjeobservationerna ofta var otillräckliga.
I mer specifika spaltlamps- och funduskopiska studier, som inkluderade adekvata baslinjeundersökningar, har inga läkemedelsrelaterade onormala oftalmologiska fynd rapporterats.
Det finns litteraturrapporter som associerar MINIPRESS 1 mg-behandling med en försämring av redan existerande narkolepsi. Ett orsakssamband är osäkert i dessa fall.
Efter marknadsföring har följande biverkningar rapporterats:
Autonoma nervsystemet: spolning.
Kroppen som helhet: allergisk reaktion, asteni, sjukdomskänsla, smärta.
Kardiovaskulär, allmän: angina pectoris, hypotoni.
Endokrin: gynekomasti.
Puls/rytm: bradykardi.
Psykiatrisk: sömnlöshet.
Hud/bihang: urtikaria.
Vaskulär (extrakardiell): vaskulit.
Syn: ögonsmärta.
Särskilda sinnen: Under kataraktkirurgi har en variant av småpupillsyndrom, känt som Intraoperativt Floppy Iris Syndrome (IFIS) rapporterats i samband med alfa-1-blockerare (se FÖRSIKTIGHETSÅTGÄRDER ).
LÄKEMEDELSINTERAKTIONER
MINIPRESS 2mg har administrerats utan några negativa läkemedelsinteraktioner i begränsad klinisk erfarenhet hittills med följande: (1) hjärtglykosider-digitalis och digoxin; (2) hypoglykemikalier-insulin, klorpropamid, fenformin, tolazamid och tolbutamid; (3) lugnande och lugnande medel - klordiazepoxid, diazepam och fenobarbital; (4) anti-out-allopurinol, kolchicin och probenecid; (5) antiarytmika-prokainamid, propranolol (se VARNINGAR dock) och kinidin; och (6) smärtstillande medel, febernedsättande och antiinflammatoriska medel - propoxifen, aspirin, indometacin och fenylbutazon.
Tillsats av ett diuretikum eller annat blodtryckssänkande medel till MINIPRESS 2mg har visat sig orsaka en additiv hypotensiv effekt. Denna effekt kan minimeras genom att reducera dosen av MINIPRESS till 1 till 2 mg tre gånger dagligen, genom att försiktigt införa ytterligare blodtryckssänkande läkemedel och sedan genom att retitrera MINIPRESS baserat på kliniskt svar. Samtidig administrering av MINIPRESS och en fosfodiesteras-5 (PDE-5)-hämmare kan resultera i additiv blodtryckssänkande effekt och symptomatisk hypotoni (se DOSERING OCH ADMINISTRERING ).
Interaktioner med läkemedel/laboratorietest
en studie på fem patienter som gavs från 12 till 24 mg prazosin per dag under 10 till 14 dagar, var det en genomsnittlig ökning på 42 % i urinmetaboliten av noradrenalin och en genomsnittlig ökning av urin-VMA på 17 %. Därför kan falskt positiva resultat förekomma i screeningtester för feokromocytom hos patienter som behandlas med prazosin. Om en förhöjd VMA konstateras ska prazosin avbrytas och patienten testas igen efter en månad.
Laboratorietester
I kliniska studier där lipidprofiler följdes, noterades i allmänhet inga negativa förändringar mellan lipidnivåer före och efter behandling.
VARNINGAR
Som med alla alfablockerare kan MINIPRESS orsaka synkope med plötslig förlust av medvetande. I de flesta fall tros detta bero på en överdriven postural hypotensiv effekt, även om syncopalepis-oden ibland har föregåtts av en anfall av svår takykardi med hjärtfrekvenser på 120-160 slag per minut. Syncopalepis-oder har vanligtvis inträffat inom 30 till 90 minuter efter den initiala dosen av läkemedlet; Ibland har de rapporterats i samband med snabba dosökningar av ålder eller införande av ett annat blodtryckssänkande läkemedel i behandlingen av en patient som tar höga doser av MINIPRESS. Incidensen av syncopalepis odes är cirka 1 % hos patienter som får en initial dos på 2 mg eller mer. Kliniska prövningar som utförts under undersökningsfasen av detta läkemedel tyder på att synkopala episoder kan minimeras genom att begränsa den initiala dosen av läkemedlet till 1 mg, genom att därefter öka dosen långsamt och genom att introducera eventuella ytterligare antihypertensiva läkemedel i patientens regim. med försiktighet (se DOSERING OCH ADMINISTRERING). Hypotension kan utvecklas hos patienter som får MINIPRESS som också får en betablockerare som propranolol.
Om synkope uppstår ska patienten placeras i liggande ställning och behandlas stödjande vid behov. Denna negativa effekt är självbegränsande och återkommer i de flesta fall inte efter den första behandlingsperioden eller under efterföljande dostitrering.
Patienterna ska alltid startas med 1 mg kapslar av MINIPRESS. Kapslarna på 2 och 5 mg är inte indicerade för initial behandling.
Vanligare än medvetslöshet är de symtom som ofta förknippas med sänkning av blodtrycket, nämligen yrsel och yrsel. Patienten bör varnas för dessa möjliga biverkningar och informeras om vilka åtgärder som ska vidtas om de skulle utvecklas. Patienten bör också varnas för att undvika situationer där skada kan uppstå om synkope skulle uppstå under inledningen av behandlingen med MINIPRESS 2 mg.
Priapism
Långvariga erektioner och priapism har rapporterats med alfa-1-blockerare inklusive prazosin efter marknadsföring. I händelse av en erektion som varar längre än 4 timmar, sök omedelbar medicinsk hjälp. Om priapism inte behandlas omedelbart kan penisvävnadsskada och permanent förlust av styrka resultera.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Intraoperativt Floppy Iris Syndrome (IFIS) har observerats under kataraktkirurgi hos vissa patienter som behandlats med alfa-1-blockerare. Denna variant av småpupillsyndrom kännetecknas av kombinationen av en slapp iris som böljar som svar på intraoperativa spolningsströmmar, progressiv intraoperativ mios trots preoperativ utvidgning med vanliga mydriatiska läkemedel och potentiell prolaps av iris mot fakoemulsifieringssnitten. Patientens ögonläkare bör vara förberedd på eventuella modifieringar av den kirurgiska tekniken, såsom användning av iriskrokar, irisdilatatorringar eller viskoelastiska substanser. Det verkar inte finnas någon fördel med att avbryta alfa-1-blockerare före operation för grå starr.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Ingen karcinogen potential påvisades i en 18 månader lång studie på råttor med MINIPRESS 1 mg vid dosnivåer mer än 225 gånger den vanliga maximala rekommenderade humana dosen på 20 mg per dag. MINIPRESS 2mg var inte mutagent i in vivo genetiska toxikologiska studier. I en fertilitets- och allmän reproduktionsstudie på råttor, visade både hanar och honor, behandlade med 75 mg/kg (225 gånger den vanliga maximala rekommenderade humana dosen), minskad fertilitet, medan de som behandlades med 25 mg/kg (75 gånger den vanliga maximal rekommenderad humandos) inte.
kroniska studier (ett år eller mer) av MINIPRESS på råttor och hundar inträffade testikelförändringar bestående av atrofi och nekros vid 25 mg/kg/dag (75 gånger den vanliga maximala rekommenderade humana dosen). Inga testikelförändringar sågs hos råttor eller hundar vid 10 mg/kg/dag (30 gånger den vanliga maximala rekommenderade humandosen). Med tanke på de testikelförändringar som observerats hos djur, övervakades 105 patienter på långtidsbehandling med MINIPRESS för utsöndring av 17-ketosteroider och inga förändringar som tydde på en läkemedelseffekt observerades. Dessutom hade 27 män på MINIPRESS 1 mg i upp till 51 månader inga förändringar i spermiemorfologi som tyder på läkemedelseffekt.
Användning under graviditet
Graviditetskategori C. MINIPRESS 1mg har visats vara associerat med minskad kullstorlek vid födseln, 1, 4 och 21 dagars ålder hos råttor när de ges doser mer än 225 gånger den vanliga maximala rekommenderade dosen för människor. Inga tecken på läkemedelsrelaterade yttre, viscerala eller skelettavvikelser observerades. Inga läkemedelsrelaterade yttre, viscerala eller skelettavvikelser observerades hos foster till dräktiga kaniner och dräktiga apor vid doser mer än 225 respektive 12 gånger den vanliga maximala rekommenderade humana dosen.
Användningen av prazosin och en betablockerare för kontroll av svår hypertoni hos 44 gravida kvinnor visade inga läkemedelsrelaterade fosteravvikelser eller biverkningar. Behandling med prazosin fortsatte så länge som 14 veckor.1
Prazosin har också använts ensamt eller i kombination med andra blodtryckssänkande medel vid svår hypertoni under graviditeten av andra utredare. Inga foster- eller neonatala abnormiteter har rapporterats vid användning av prazosin.2
Det finns inga adekvata och välkontrollerade studier som fastställer säkerheten för MINIPRESS hos gravida kvinnor. MINIPRESS ska endast användas under graviditet om den potentiella nyttan överväger den potentiella risken för modern och fostret.
Ammande mödrar
MINIPRESS 1mg har visats utsöndras i små mängder i modersmjölk. Försiktighet bör iakttas när MINIPRESS 2 mg ges till en ammande kvinna.
Användning hos barn
Säkerhet och effektivitet hos barn har inte fastställts.
REFERENSER
1. Lubbe, WF och Hodge, JV: New Zealand Med J, 94 (691) 169-172, 1981.
2. Davey, DA och Dommisse, J: SA Med J, 4 oktober 1980 (551-556).
ÖVERDOS
Oavsiktligt intag av minst 50 mg MINIPRESS hos ett tvåårigt barn resulterade i djup dåsighet och deprimerade reflexer. Ingen minskning av blodtrycket noterades. Återhämtningen var händelselös.
Om överdosering skulle leda till hypotoni är stöd för det kardiovaskulära systemet av största vikt. Återställande av blodtrycket och normalisering av hjärtfrekvensen kan åstadkommas genom att hålla patienten i ryggläge. Om denna åtgärd är otillräcklig bör chock först behandlas med volymexpanderare. Vid behov bör då vasopressorer användas. Njurfunktionen ska övervakas och stödjas vid behov. Laboratoriedata indikerar att MINIPRESS inte är dialyserbart eftersom det är proteinbundet.
KONTRAINDIKATIONER
MINIPRESS är kontraindicerat till patienter med känd känslighet för kinazoliner, prazosin eller någon av de inerta ingredienserna.
KLINISK FARMAKOLOGI
Den exakta mekanismen för den hypotensiva effekten av prazosin är okänd. Prazosin orsakar en minskning av totalt perifert motstånd och ansågs ursprungligen ha en direkt avslappnande effekt på vaskulär glatt muskulatur. Nyligen genomförda djurstudier har emellertid föreslagit att den vasodilaterande effekten av prazosin också är relaterad till blockad av postsynaptiska alfa-adrenoceptorer. Resultaten av hundförexperiment på frambenen visar att den perifera vasodilaterande effekten av prazosin huvudsakligen är begränsad till nivån av motståndskärlen (arteriolerna). Till skillnad från konventionella alfablockerare åtföljs den antihypertensiva effekten av prazosin vanligtvis inte av reflextakykardi. Tolerans har inte observerats utvecklas vid långtidsbehandling.
Hemodynamiska studier har utförts på människa efter akut administrering av engångsdos och under långvarig underhållsbehandling. Resultaten bekräftar att den terapeutiska effekten är ett blodtrycksfall som inte åtföljs av en kliniskt signifikant förändring i hjärtminutvolym, hjärtfrekvens, renalt blodflöde och glomerulär filtrationshastighet. Det finns ingen mätbar negativ kronotropisk effekt.
I hittills kliniska studier har prazosinhydroklorid inte ökat plasmareninaktiviteten.
Hos människan sänks blodtrycket i både liggande och stående position. Denna effekt är mest uttalad på det diastoliska blodtrycket.
Efter oral administrering når humana plasmakoncentrationer en topp efter cirka tre timmar med en plasmahalveringstid på två till tre timmar. Läkemedlet är starkt bundet till plasmaprotein. Biotillgänglighetsstudier har visat att den totala absorptionen i förhållande till läkemedlet i en 20 % alkohollösning är 90 %, vilket resulterar i toppnivåer på cirka 65 % av läkemedlet i lösning. Djurstudier tyder på att prazosinhydroklorid metaboliseras i stor utsträckning, främst genom demetylering och konjugering, och utsöndras huvudsakligen via galla och feces. Mindre omfattande humanstudier tyder på liknande metabolism och utsöndring hos människa.
I kliniska studier där lipidprofiler följdes, noterades i allmänhet inga negativa förändringar mellan lipidnivåer före och efter behandling.
PATIENTINFORMATION
Yrsel eller dåsighet kan uppstå efter den första dosen av detta läkemedel. Undvik att köra bil eller utföra farliga uppgifter under de första 24 timmarna efter att du tagit detta läkemedel eller när dosen ökas. Yrsel, yrsel eller svimning kan förekomma, särskilt när man reser sig från liggande eller sittande ställning. Att gå upp långsamt kan hjälpa till att minska problemet. Dessa effekter kan också uppstå om du dricker alkohol, står under långa stunder, tränar eller om vädret är varmt. När du tar MINIPRESS, var försiktig med mängden alkohol du dricker. Var också extra försiktig under träning eller varmt väder, eller om du står under långa perioder. Kontrollera med din läkare om du har några frågor.
