Vasotec 2.5mg, 5mg, 10mg Enalapril Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Vasotec och hur används det?
Vasotec är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni), vänsterkammardysfunktion och kronisk hjärtsvikt. Vasotec kan användas ensamt eller tillsammans med andra läkemedel.
- Vasotec tillhör en klass av läkemedel som kallas ACE-hämmare.
- Det är inte känt om Vasotec är säkert och effektivt för barn yngre än 1 månad.
Vilka är de möjliga biverkningarna av Vasotec 2,5 mg?
Vasotec 2,5 mg kan orsaka allvarliga biverkningar inklusive:
- yrsel,
- bröstsmärta,
- gulfärgning av huden eller ögonen (gulsot),
- lite eller ingen urinering,
- feber,
- frossa,
- öm hals,
- illamående,
- svaghet,
- pirrande känsla,
- oregelbundna hjärtslag och
- förlust av rörelse
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Vasotec inkluderar:
- yrsel,
- trötthet och
- yrsel
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Vasotec. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
- När graviditet upptäcks, avbryt VASOTEC® så snart som möjligt.
- Läkemedel som verkar direkt på renin-angiotensinsystemet kan orsaka skador och dödsfall för fostret under utveckling. Se VARNINGAR: Fostertoxicitet
BESKRIVNING
VASOTEC® (Enalapril Maleate) är maleatsaltet av enalapril, etylestern av en långverkande angiotensinomvandlande enzymhämmare, enalaprilat. Enalaprilmaleat beskrivs kemiskt som (S)-1[N-[1-(etoxikarbonyl)-3-fenylpropyl]-L-alanyl]-L-prolin, (Z)-2-butendioatsalt (1:1). Dess empiriska formel är C20H28N2O5•C4H4O4, och dess strukturformel är:
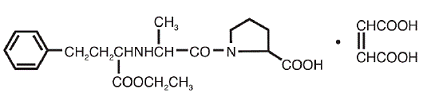
Enalaprilmaleat är ett vitt till benvitt, kristallint pulver med en molekylvikt på 492,53. Det är svårlösligt i vatten, lösligt i etanol och fritt lösligt i metanol.
Enalapril är en prodrug; efter oral administrering bioaktiveras det genom hydrolys av etylestern till enalaprilat, som är den aktiva angiotensinomvandlande enzymhämmaren.
Enalaprilmaleat tillhandahålls som 2,5 mg, 5 mg, 10 mg och 20 mg tabletter för oral administrering. Förutom den aktiva ingrediensen enalaprilmaleat innehåller varje tablett följande inaktiva ingredienser: laktos, magnesiumstearat, natriumbikarbonat och stärkelse. Tabletterna 10 mg och 20 mg innehåller också järnoxider.
INDIKATIONER
Hypertoni
VASOTEC är indicerat för behandling av hypertoni.
VASOTEC är effektivt ensamt eller i kombination med andra blodtryckssänkande medel, särskilt diuretika av tiazidtyp. De blodtryckssänkande effekterna av VASOTEC 10 mg och tiazider är ungefär additiva.
Hjärtsvikt
VASOTEC är indicerat för behandling av symtomatisk kongestiv hjärtsvikt, vanligtvis i kombination med diuretika och digitalis. Hos dessa patienter förbättrar VASOTEC 5mg symtomen, ökar överlevnaden och minskar frekvensen av sjukhusvistelser (se KLINISK FARMAKOLOGI , Hjärtsvikt , Mortality Trials för detaljer och begränsningar av överlevnadsprövningar ).
Asymptomatisk vänsterkammardysfunktion
Hos kliniskt stabila asymtomatiska patienter med vänsterkammardysfunktion (ejektionsfraktion ≤ 35 procent), minskar VASOTEC 5 mg utvecklingshastigheten för uppenbar hjärtsvikt och minskar incidensen av sjukhusvistelse för hjärtsvikt (se KLINISK FARMAKOLOGI , Hjärtsvikt , Mortality Trials för detaljer och begränsningar av överlevnadsprövningar ).
Vid användning av VASOTEC 2,5 mg bör hänsyn tas till det faktum att en annan angiotensinomvandlande enzymhämmare, kaptopril, har orsakat agranulocytos, särskilt hos patienter med nedsatt njurfunktion eller kollagen kärlsjukdom, och att tillgängliga data är otillräckliga för att visa att VASOTEC 2,5 mg inte har en liknande risk (se VARNINGAR ).
Vid övervägande av användning av VASOTEC bör det noteras att i kontrollerade kliniska prövningar har ACE-hämmare en effekt på blodtrycket som är mindre hos svarta patienter än hos icke-svarta. Dessutom bör det noteras att svarta patienter som får ACE-hämmare har rapporterats ha en högre incidens av angioödem jämfört med icke-svarta (se VARNINGAR , Angioödem i huvud och nacke ).
DOSERING OCH ADMINISTRERING
Hypertoni
Hos patienter som för närvarande behandlas med ett diuretikum kan symtomatisk hypotoni ibland uppstå efter den initiala dosen av VASOTEC. Diuretikumet ska om möjligt sättas ut i två till tre dagar innan behandling med VASOTEC påbörjas för att minska sannolikheten för hypotoni (se VARNINGAR ). Om patientens blodtryck inte kontrolleras med enbart VASOTEC kan diuretikabehandlingen återupptas.
Om diuretikumet inte kan avbrytas bör en initial dos på 2,5 mg användas under medicinsk övervakning i minst två timmar och tills blodtrycket har stabiliserats under minst en ytterligare timme (se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ).
Den rekommenderade initialdosen för patienter som inte tar diuretika är 5 mg en gång dagligen. Doseringen bör anpassas efter blodtryckssvar. Det vanliga dosintervallet är 10 till 40 mg per dag administrerat i en enkel dos eller två uppdelade doser. Hos vissa patienter som behandlas en gång dagligen kan den antihypertensiva effekten avta mot slutet av doseringsintervallet. Hos sådana patienter bör en ökning av dosen eller administrering två gånger dagligen övervägas. Om blodtrycket inte kontrolleras med enbart VASOTEC 2,5 mg kan ett diuretikum tillsättas. Samtidig administrering av VASOTEC 5 mg med kaliumtillskott, kaliumsaltersättning eller kaliumsparande diuretika kan leda till ökningar av serumkalium (se FÖRSIKTIGHETSÅTGÄRDER ).
Dosjustering hos hypertensiva patienter med nedsatt njurfunktion
Den vanliga dosen av enalapril rekommenderas för patienter med ett kreatininclearance på mer än 30 ml/min (serumkreatinin på upp till cirka 3 mg/dL). För patienter med kreatininclearance mindre än eller lika med 30 ml/min (serumkreatinin mer än eller lika med 3 mg/dL), är den första dosen 2,5 mg en gång dagligen. Dosen kan titreras uppåt tills blodtrycket är kontrollerat eller till maximalt 40 mg dagligen.
Hjärtsvikt
VASOTEC är indicerat för behandling av symtomatisk hjärtsvikt, vanligtvis i kombination med diuretika och digitalis. I de placebokontrollerade studierna som visade förbättrad överlevnad titrerades patienterna som tolererade upp till 40 mg, administrerat i två uppdelade doser.
Den rekommenderade initialdosen är 2,5 mg. Det rekommenderade doseringsintervallet är 2,5 till 20 mg givet två gånger om dagen. Doserna bör titreras uppåt, allteftersom de tolereras, under en period av några dagar eller veckor. Den maximala dagliga dosen som administrerades i kliniska prövningar var 40 mg i uppdelade doser.
Efter den initiala dosen av VASOTEC ska patienten observeras under medicinsk övervakning i minst två timmar och tills blodtrycket har stabiliserats under minst ytterligare en timme (se VARNINGAR och LÄKEMEDELSINTERAKTIONER ). Om möjligt bör dosen av eventuellt samtidigt diuretika minskas, vilket kan minska sannolikheten för hypotoni. Uppkomsten av hypotoni efter den initiala dosen av VASOTEC utesluter inte efterföljande noggrann dostitrering med läkemedlet, efter effektiv behandling av hypotoni.
Asymptomatisk vänsterkammardysfunktion
I studien som visade effekt påbörjades patienterna med 2,5 mg två gånger dagligen och titrerades efter tolerans till den avsedda dagliga dosen på 20 mg (uppdelade doser).
Efter den initiala dosen av VASOTEC 10 mg ska patienten observeras under medicinsk övervakning i minst två timmar och tills blodtrycket har stabiliserats i ytterligare minst en timme (se VARNINGAR och LÄKEMEDELSINTERAKTIONER ). Om möjligt bör dosen av eventuellt samtidigt diuretika minskas, vilket kan minska sannolikheten för hypotoni. Uppkomsten av hypotoni efter den initiala dosen av VASOTEC 5 mg utesluter inte efterföljande noggrann dostitrering med läkemedlet, efter effektiv behandling av hypotoni.
Dosjustering hos patienter med hjärtsvikt och nedsatt njurfunktion eller hyponatremi
Hos patienter med hjärtsvikt som har hyponatremi (serumnatrium mindre än 130 mEq/L) eller med serumkreatinin högre än 1,6 mg/dL, bör behandlingen inledas med 2,5 mg dagligen under noggrann medicinsk övervakning (se Hjärtsvikt , VARNINGAR och LÄKEMEDELSINTERAKTIONER ). Dosen kan ökas till 2,5 mg två gånger dagligen, sedan 5 mg två gånger dagligen och högre vid behov, vanligtvis med fyra dagars intervall eller mer om det vid tidpunkten för dosjustering inte finns överdriven hypotoni eller signifikant försämring av njurfunktionen. Den maximala dagliga dosen är 40 mg.
Pediatriska hypertensiva patienter
Den vanliga rekommenderade startdosen är 0,08 mg/kg (upp till 5 mg) en gång dagligen. Doseringen bör anpassas efter blodtryckssvar. Doser över 0,58 mg/kg (eller över 40 mg) har inte studerats hos pediatriska patienter (se KLINISK FARMAKOLOGI , Klinisk farmakologi hos pediatriska patienter ).
VASOTEC 5mg rekommenderas inte till nyfödda och till pediatriska patienter med glomerulär filtrationshastighet mindre än 30 ml/min/1,73 m², eftersom inga data finns tillgängliga.
Beredning av suspension (för 200 ml av en 1,0 mg/ml suspension)
Tillsätt 50 mL Bicitra® i en polyetylentereftalat (PET)-flaska innehållande tio 20 mg tabletter av VASOTEC 10 mg och skaka i minst 2 minuter. Låt koncentratet stå i 60 minuter. Efter 60 minuters uppehållstid, skaka koncentratet i ytterligare en minut. Tillsätt 150 mL Ora-Sweet SF™2 till koncentratet i PET-flaskan och skaka suspensionen för att dispergera ingredienserna. Suspensionen ska förvaras i kylskåp vid 2-8°C (36-46°F) och kan förvaras i upp till 30 dagar. Skaka suspensionen före varje användning.
HUR LEVERERAS
Lagring
Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur ].
Förvara behållaren väl tillsluten.
Skydda mot fukt.
Dispensera i en tät behållare enligt USP, om produktförpackningen är uppdelad.
Tillverkad för: Valeant Pharmaceuticals North America LLC Bridgewater, NJ 08807 USA. Tillverkad av: Valeant Pharmaceuticals International, Inc. Steinbach, MB R5G 1Z7 Kanada. Revision: juli 2017.
BIEFFEKTER
VASOTEC har utvärderats för säkerhet hos mer än 10 000 patienter, inklusive över 1 000 patienter som behandlats under ett år eller mer. VASOTEC 10 mg har visat sig vara allmänt väl tolererad i kontrollerade kliniska prövningar med 2987 patienter. För det mesta var negativa upplevelser milda och övergående till sin natur. I kliniska prövningar krävdes avbrytande av behandlingen på grund av kliniska biverkningar hos 3,3 procent av patienterna med hypertoni och hos 5,7 procent av patienterna med hjärtsvikt. Frekvensen av biverkningar var inte relaterad till total daglig dos inom de vanliga dosintervallen. Hos patienter med hypertoni var den totala andelen patienter som behandlades med VASOTEC som rapporterade biverkningar jämförbar med placebo.
Hypertoni
Biverkningar som inträffade hos mer än en procent av patienterna med hypertoni som behandlats med VASOTEC 2,5 mg i kontrollerade kliniska prövningar visas nedan. Hos patienter som behandlades med VASOTEC var den maximala behandlingstiden tre år; Hos placebobehandlade patienter var den maximala behandlingstiden 12 veckor.
Hjärtsvikt
Biverkningar som förekommer hos mer än en procent av patienterna med hjärtsvikt som behandlats med VASOTEC 5 mg visas nedan. Incidensen representerar erfarenheterna från både kontrollerade och okontrollerade kliniska prövningar (maximal behandlingslängd var cirka ett år). Hos placebobehandlade patienter kommer de rapporterade incidenserna från de kontrollerade studierna (maximal behandlingslängd är 12 veckor). Andelen patienter med svår hjärtsvikt (NYHA klass IV) var 29 procent och 43 procent för patienter som behandlades med VASOTEC 2,5 mg respektive placebo.
Andra allvarliga kliniska biverkningar som inträffat sedan läkemedlet marknadsfördes eller biverkningar som inträffat hos 0,5 till 1,0 procent av patienterna med högt blodtryck eller hjärtsvikt i kliniska prövningar listas nedan och, inom varje kategori, är de sorterade efter minskande svårighetsgrad.
Kroppen Som Helhet
Anafylaktoida reaktioner (se VARNINGAR , Anafylaktoida och eventuellt relaterade reaktioner ).
Kardiovaskulär
Hjärtstopp; hjärtinfarkt eller cerebrovaskulär olycka, möjligen sekundärt till överdriven hypotoni hos högriskpatienter (se VARNINGAR , Hypotoni ); lungemboli och infarkt; lungödem; rytmrubbningar inklusive atriell takykardi och bradykardi; förmaksflimmer; hjärtklappning, Raynauds fenomen.
Matsmältningskanalen
Ileus, pankreatit, leversvikt, hepatit (hepatocellulär [bevisat vid återinflammation] eller kolestatisk gulsot) (se VARNINGAR , Leversvikt ), melena, anorexi, dyspepsi, förstoppning, glossit, stomatit, muntorrhet.
Hematologiska
Sällsynta fall av neutropeni, trombocytopeni och benmärgsdepression.
Muskuloskeletala
Muskelkramp.
Nervös/psykiatrisk
Depression, förvirring, ataxi, somnolens, sömnlöshet, nervositet, perifer neuropati (t.ex. parestesi, dysestesi), drömavvikelse.
Andningsorgan
Bronkospasm, rinorré, halsont och heshet, astma, övre luftvägsinfektion, lunginfiltrat, eosinofil pneumonit.
Hud
Exfoliativ dermatit, giftig epidermal nekrolys, Stevens-Johnsons syndrom, pemfigus, herpes zoster, erythema multiforme, urtikaria, klåda, alopeci, rodnad, diafores, ljuskänslighet.
Särskilda sinnen
Suddig syn, smakförändring, anosmi, tinnitus, konjunktivit, torra ögon, tårar.
Urogenital
Njursvikt, oliguri, nedsatt njurfunktion (se FÖRSIKTIGHETSÅTGÄRDER och DOSERING OCH ADMINISTRERING ), flanksmärta, gynekomasti, impotens.
Diverse
Ett symtomkomplex har rapporterats som kan inkludera några eller alla av följande: en positiv ANA, en förhöjd erytrocytsedimentationshastighet, artralgi/artrit, myalgi/myosit, feber, serosit, vaskulit, leukocytos, eosinofili, ljuskänslighet, hudutslag och andra dermatologiska manifestationer.
Angioödem
Angioödem har rapporterats hos patienter som får VASOTEC 2,5 mg, med en högre incidens hos svarta patienter än hos icke-svarta patienter. Angioödem i samband med larynxödem kan vara dödligt. Om angioödem i ansikte, extremiteter, läppar, tunga, glottis och/eller struphuvud uppträder, ska behandling med VASOTEC avbrytas och lämplig behandling sättas in omedelbart (se VARNINGAR ).
Hypotoni
Hos de hypertensiva patienterna uppträdde hypotoni hos 0,9 procent och synkope hos 0,5 procent av patienterna efter den initiala dosen eller under förlängd behandling. Hypotension eller synkope var en orsak till att behandlingen avbröts hos 0,1 procent av patienterna med hypertoni. Hos patienter med hjärtsvikt uppträdde hypotoni hos 6,7 procent och synkope hos 2,2 procent av patienterna. Hypotension eller synkope var en orsak till att behandlingen avbröts hos 1,9 procent av patienterna med hjärtsvikt (se VARNINGAR ).
Hosta
Ser FÖRSIKTIGHETSÅTGÄRDER , Hosta .
Pediatriska patienter
Biverkningsprofilen för pediatriska patienter verkar likna den som ses hos vuxna patienter.
Resultat från kliniska laboratorietest
Serumelektrolyter
Hyperkalemi (se FÖRSIKTIGHETSÅTGÄRDER ), hyponatremi.
Kreatinin, Blod Urea Kväve
kontrollerade kliniska prövningar observerades mindre ökningar av ureakväve i blodet och serumkreatinin, reversibla vid avbrytande av behandlingen, hos cirka 0,2 procent av patienterna med essentiell hypertoni som behandlades med enbart VASOTEC. Det är mer sannolikt att ökningar inträffar hos patienter som samtidigt får diuretika eller hos patienter med njurartärstenos (se FÖRSIKTIGHETSÅTGÄRDER ). Hos patienter med hjärtsvikt som också fick diuretika med eller utan digitalis, observerades ökningar av ureakväve i blodet eller serumkreatinin, vanligtvis reversibel vid utsättning av VASOTEC 5 mg och/eller annan samtidig diuretikabehandling, hos cirka 11 procent av patienterna. Ökade ureakväve eller kreatinin i blodet var en orsak till att behandlingen avbröts hos 1,2 procent av patienterna.
Hematologi
Små minskningar av hemoglobin och hematokrit (genomsnittliga minskningar på cirka 0,3 g procent respektive 1,0 volymprocent) förekommer ofta hos patienter med antingen hypertoni eller kronisk hjärtsvikt som behandlas med VASOTEC 5 mg men är sällan av klinisk betydelse om inte en annan orsak till anemi existerar samtidigt. I kliniska prövningar avbröt mindre än 0,1 procent av patienterna behandlingen på grund av anemi. Hemolytisk anemi, inklusive fall av hemolys hos patienter med G6PD-brist, har rapporterats; ett orsakssamband till enalapril kan inte uteslutas.
Leverfunktionstester
Förhöjningar av leverenzymer och/eller serumbilirubin har inträffat (se VARNINGAR , Leversvikt ).
För att rapportera MISSTÄNKTA BIVERKNINGAR, kontakta Valeant Pharmaceuticals North America LLC på 1-800-321-4576 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
LÄKEMEDELSINTERAKTIONER
Neprilysin-hämmare
Patienter som samtidigt tar neprilysinhämmare kan löpa ökad risk för angioödem. (ser VARNINGAR )
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, hyperkalemi och förändringar i njurfunktion (inklusive akut njursvikt) jämfört med monoterapi. De flesta patienter som får kombinationen av två RAS-hämmare får ingen ytterligare fördel jämfört med monoterapi. Undvik i allmänhet kombinerad användning av RAS-hämmare. Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på VASOTEC 2,5 mg och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med VASOTEC 5 mg till patienter med diabetes. Undvik användning av aliskiren med VASOTEC hos patienter med nedsatt njurfunktion (GFR
Hypotension - Patienter på diuretikaterapi
Patienter som behandlas med diuretika och särskilt de hos vilka diuretikabehandling nyligen påbörjats, kan ibland uppleva en överdriven blodtryckssänkning efter påbörjad behandling med enalapril. Möjligheten för hypotensiva effekter med enalapril kan minimeras genom att antingen avbryta diuretikumet eller öka saltintaget innan behandling med enalapril påbörjas. Om det är nödvändigt att fortsätta med diuretika, ge noggrann medicinsk övervakning efter den initiala dosen i minst två timmar och tills blodtrycket har stabiliserats i minst en ytterligare timme (se VARNINGAR och DOSERING OCH ADMINISTRERING ).
Agenter som orsakar reninfrisättning
Den antihypertensiva effekten av VASOTEC 10 mg förstärks av antihypertensiva medel som orsakar reninfrisättning (t.ex. diuretika).
Icke-steroida antiinflammatoriska medel inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare)
Hos patienter som är äldre, volymbrist (inklusive de som behandlas med diuretika), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med ACE-hämmare, inklusive enalapril, resultera i försämring av njurfunktionen, inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som får enalapril- och NSAID-behandling.
I en klinisk farmakologisk studie gavs indometacin eller sulindak till hypertonipatienter som fick VASOTEC. I denna studie fanns det inga tecken på avtrubbning av den antihypertensiva effekten av VASOTEC. Rapporter tyder dock på att NSAID kan minska den antihypertensiva effekten av ACE-hämmare.
Andra kardiovaskulära medel
VASOTEC 10 mg har använts samtidigt med beta-adrenerga blockerande medel, metyldopa, nitrater, kalciumblockerare, hydralazin, prazosin och digoxin utan tecken på kliniskt signifikanta biverkningar.
Medel som ökar serumkalium
VASOTEC dämpar kaliumförlust orsakad av diuretika av tiazidtyp. Kaliumsparande diuretika (t.ex. spironolakton, triamteren eller amilorid), kaliumtillskott eller kaliuminnehållande saltersättningsmedel kan leda till betydande ökningar av serumkalium. Om samtidig användning av dessa medel är indicerad på grund av påvisad hypokalemi, bör de därför användas med försiktighet och med frekvent övervakning av serumkalium. Kaliumsparande medel ska i allmänhet inte användas till patienter med hjärtsvikt som får VASOTEC.
Litium
Litiumtoxicitet har rapporterats hos patienter som får litium samtidigt med läkemedel som orsakar eliminering av natrium, inklusive ACE-hämmare. Ett fåtal fall av litiumtoxicitet har rapporterats hos patienter som samtidigt fått VASOTEC och litium och var reversibla efter utsättande av båda läkemedlen. Det rekommenderas att serumlitiumnivåer övervakas ofta om enalapril administreras samtidigt med litium.
Guld
Nitritoidreaktioner (symtom inkluderar rodnad i ansiktet, illamående, kräkningar och hypotoni) har rapporterats i sällsynta fall hos patienter i behandling med injicerbart guld (natriumaurotiomalat) och samtidig behandling med ACE-hämmare inklusive VASOTEC.
mTOR (Däggdjur Target Of Rapamycin) hämmare
Patienter som får samtidig behandling med ACE-hämmare och mTOR-hämmare (t.ex. temsirolimus, sirolimus, everolimus) kan löpa ökad risk för angioödem (se VARNINGAR ).
VARNINGAR
Anafylaktoida och möjligen relaterade reaktioner
Förmodligen eftersom angiotensinomvandlande enzymhämmare påverkar metabolismen av eikosanoider och polypeptider, inklusive endogent bradykinin, kan patienter som får ACE-hämmare (inklusive VASOTEC) utsättas för en mängd olika biverkningar, några av dem allvarliga.
Huvud Och Nacke Angioödem
Angioödem i ansikte, extremiteter, läppar, tunga, glottis och/eller struphuvud har rapporterats hos patienter som behandlats med angiotensinkonverterande enzymhämmare, inklusive VASOTEC. Detta kan inträffa när som helst under behandlingen. I sådana fall ska VASOTEC 2,5 mg omedelbart avbrytas och lämplig behandling och övervakning bör tillhandahållas tills fullständig och ihållande upplösning av tecken och symtom har inträffat. I fall där svullnad har begränsats till ansikte och läppar har tillståndet i allmänhet löst sig utan behandling, även om antihistaminer har varit användbara för att lindra symtomen. Angioödem i samband med larynxödem kan vara dödligt. Om tungan, struphuvudet eller struphuvudet är involverat, vilket sannolikt orsakar luftvägsobstruktion, bör lämplig behandling, t.ex. subkutan epinefrinlösning 1:1000 (0,3 mL till 0,5 mL) och/eller åtgärder som är nödvändiga för att säkerställa en fri luftväg, omedelbart göras försedd (ser NEGATIVA REAKTIONER ).
Patienter som får samtidig behandling med ACE-hämmare och mTOR-hämmare (t.ex. temsirolimus, sirolimus, everolimus) eller en neprilysinhämmare kan löpa ökad risk för angioödem (se FÖRSIKTIGHETSÅTGÄRDER ).
Intestinalt angioödem
Intestinalt angioödem har rapporterats hos patienter som behandlats med ACE-hämmare. Dessa patienter fick buksmärtor (med eller utan illamående eller kräkningar); i vissa fall fanns det ingen tidigare historia av ansiktsangioödem och C-1-esterasnivåerna var normala. Angioödem diagnostiserades genom procedurer inklusive CT-skanning av buken eller ultraljud, eller vid operation, och symtomen försvann efter att ha stoppat ACE-hämmaren. Intestinalt angioödem bör inkluderas i differentialdiagnosen för patienter på ACE-hämmare med buksmärtor.
Patienter med en historia av angioödem som inte är relaterat till behandling med ACE-hämmare kan löpa ökad risk för angioödem när de får en ACE-hämmare (se även INDIKATIONER OCH ANVÄNDNING och KONTRAINDIKATIONER ).
Anafylaktoida reaktioner under desensibilisering
Två patienter som genomgick desensibiliserande behandling med hymenopteragift samtidigt som de fick ACE-hämmare fick livshotande anafylaktoida reaktioner. Hos samma patienter undveks dessa reaktioner när ACE-hämmare tillfälligt hölls in, men de återkom vid oavsiktlig återinsättning.
Anafylaktoida reaktioner under membranexponering
Anafylaktoida reaktioner har rapporterats hos patienter som dialyserats med högflödesmembran och behandlats samtidigt med en ACE-hämmare. Anafylaktoida reaktioner har också rapporterats hos patienter som genomgår lågdensitetslipoproteinaferes med dextransulfatabsorption.
Hypotoni
Överdriven hypotoni är sällsynt hos okomplicerade hypertonipatienter som behandlas med enbart VASOTEC 5 mg. Patienter med hjärtsvikt som ges VASOTEC har vanligtvis en viss sänkning av blodtrycket, särskilt med den första dosen, men avbrytande av behandlingen för fortsatt symptomatisk hypotoni är vanligtvis inte nödvändigt när doseringsinstruktionerna följs; försiktighet bör iakttas när behandlingen påbörjas (se DOSERING OCH ADMINISTRERING ). Patienter med risk för överdriven hypotoni, ibland förknippad med oliguri och/eller progressiv azotemi, och sällan med akut njursvikt och/eller död, inkluderar de med följande tillstånd eller egenskaper: hjärtsvikt, hyponatremi, högdosbehandling med diuretika, nyligen intensiv behandling diures eller ökning av diuretikados, njurdialys eller allvarlig volym- och/eller saltutarmning av någon etiologi. Det kan vara tillrådligt att eliminera diuretikumet (förutom hos patienter med hjärtsvikt), minska diuretikadosen eller öka saltintaget försiktigt innan behandling med VASOTEC 10 mg påbörjas hos patienter med risk för överdriven hypotoni som kan tolerera sådana justeringar (se LÄKEMEDELSINTERAKTIONER och NEGATIVA REAKTIONER ). Hos patienter med risk för överdriven hypotoni bör behandlingen påbörjas under mycket noggrann medicinsk övervakning och sådana patienter bör följas noga under de första två veckorna av behandlingen och närhelst dosen av enalapril och/eller diuretikum ökas. Liknande överväganden kan gälla patienter med ischemisk hjärt- eller cerebrovaskulär sjukdom, hos vilka ett alltför kraftigt blodtrycksfall kan resultera i en hjärtinfarkt eller cerebrovaskulär olycka.
Om överdriven hypotoni uppstår ska patienten placeras i ryggläge och vid behov få en intravenös infusion av normal koksaltlösning. Ett övergående hypotensivt svar är inte en kontraindikation för ytterligare doser av VASOTEC 2,5 mg, som vanligtvis kan ges utan svårighet när blodtrycket har stabiliserats. Om symtomatisk hypotoni utvecklas kan dosreduktion eller utsättning av VASOTEC eller samtidig diuretikum vara nödvändigt.
Neutropeni/Agranulocytos
En annan angiotensinomvandlande enzymhämmare, kaptopril, har visat sig orsaka agranulocytos och benmärgsdepression, sällan hos okomplicerade patienter men oftare hos patienter med nedsatt njurfunktion, särskilt om de också har en kollagenkärlsjukdom. Tillgängliga data från kliniska prövningar av enalapril är otillräckliga för att visa att enalapril inte orsakar agranulocytos i liknande takt. Marknadsföringserfarenhet har visat fall av neutropeni eller agranulocytos där ett orsakssamband till enalapril inte kan uteslutas. Regelbunden övervakning av antalet vita blodkroppar hos patienter med kollagenkärlsjukdom och njursjukdom bör övervägas.
Leversvikt
sällsynta fall har ACE-hämmare associerats med ett syndrom som börjar med kolestatisk gulsot och utvecklas till fulminant levernekros och (ibland) död. Mekanismen för detta syndrom är inte förstått. Patienter som får ACE-hämmare och som utvecklar gulsot eller markant förhöjda leverenzymer bör avbryta behandlingen med ACE-hämmare och få lämplig medicinsk uppföljning.
Fostertoxicitet
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt VASOTEC 10 mg så snart som möjligt. Dessa negativa utfall är vanligtvis förknippade med användning av dessa läkemedel under andra och tredje trimestern av graviditeten. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. Lämplig hantering av maternell hypertoni under graviditeten är viktig för att optimera resultaten för både mor och foster.
det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar reninangiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret. Utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Om oligohydramnios observeras, avbryt VASOTEC, såvida det inte anses vara livräddande för modern. Fostertest kan vara lämpligt, baserat på graviditetsveckan. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada. Följ noga spädbarn med tidigare exponering in utero för VASOTEC för hypotoni, oliguri och hyperkalemi (se FÖRSIKTIGHETSÅTGÄRDER , Pediatrisk användning ).
Inga teratogena effekter av enalapril sågs i studier på gravida råttor och kaniner. På basis av kroppsytan var de använda doserna 57 gånger respektive 12 gånger den maximala rekommenderade dagliga dosen för människor (MRHDD).
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Aortastenos/hypertrofisk kardiomyopati
Som med alla vasodilatorer bör enalapril ges med försiktighet till patienter med obstruktion i utflödeskanalen från vänster kammare.
Nedsatt njurfunktion
Som en konsekvens av hämning av renin-angiotensin-aldosteronsystemet kan förändringar i njurfunktionen förväntas hos känsliga individer. Hos patienter med svår hjärtsvikt vars njurfunktion kan bero på aktiviteten hos renin-angiotensin-aldosteronsystemet, kan behandling med angiotensinkonverterande enzymhämmare, inklusive VASOTEC, vara associerad med oliguri och/eller progressiv azotemi och i sällsynta fall med akut njursvikt och /eller döden (se LÄKEMEDELSINTERAKTIONER ).
I kliniska studier på hypertonipatienter med unilateral eller bilateral njurartärstenos observerades ökningar av ureakväve i blodet och serumkreatinin hos 20 procent av patienterna. Dessa ökningar var nästan alltid reversibla vid utsättning av enalapril och/eller diuretikabehandling. Hos sådana patienter bör njurfunktionen övervakas under de första veckorna av behandlingen.
Vissa patienter med hypertoni eller hjärtsvikt utan uppenbar redan existerande njurkärlsjukdom har utvecklat ökningar av blodurea och serumkreatinin, vanligtvis mindre och övergående, särskilt när VASOTEC har getts samtidigt med ett diuretikum. Detta är mer sannolikt att inträffa hos patienter med redan existerande nedsatt njurfunktion. Dosminskning och/eller utsättande av diuretika och/eller VASOTEC 5 mg kan behövas.
Utvärdering av patienter med hypertoni eller hjärtsvikt bör alltid innefatta bedömning av njurfunktionen (ser DOSERING OCH ADMINISTRERING ).
Hyperkalemi
Förhöjt serumkalium (mer än 5,7 mEq/L) observerades hos cirka en procent av hypertonipatienterna i kliniska prövningar. I de flesta fall var dessa isolerade värden som försvann trots fortsatt behandling. Hyperkalemi var en orsak till att behandlingen avbröts hos 0,28 procent av hypertonipatienterna. I kliniska prövningar av hjärtsvikt observerades hyperkalemi hos 3,8 procent av patienterna men var inte en orsak till att behandlingen avbröts.
Riskfaktorer för utveckling av hyperkalemi inkluderar njurinsufficiens, diabetes mellitus och samtidig användning av kaliumsparande diuretika, kaliumtillskott och/eller kaliumhaltiga saltersättningar, som bör användas med försiktighet, om alls, med VASOTEC (se LÄKEMEDELSINTERAKTIONER ).
Hosta
Antagligen på grund av hämningen av nedbrytningen av endogent bradykinin, har ihållande icke-produktiv hosta rapporterats med alla ACE-hämmare, som alltid försvinner efter avslutad behandling. ACE-hämmare-inducerad hosta bör beaktas vid differentialdiagnos av hosta.
Kirurgi/anestesi
Hos patienter som genomgår större operationer eller under anestesi med medel som ger hypotoni, kan enalapril blockera angiotensin II-bildning sekundärt till kompensatorisk reninfrisättning. Om hypotoni uppstår och anses bero på denna mekanism kan den korrigeras genom volymexpansion.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Det fanns inga tecken på en tumörframkallande effekt när enalapril administrerades under 106 veckor till han- och honråttor i doser upp till 90 mg/kg/dag eller under 94 veckor till han- och honmöss i doser upp till 90 och 180 mg/kg/ dag, respektive. Dessa doser är 26 gånger (i råttor och honmöss) och 13 gånger (i hanmöss) den maximala rekommenderade dagliga dosen för människor (MRHDD) jämfört med kroppsyta.
Varken enalaprilmaleat eller den aktiva disyran var mutagen i Ames mikrobiella mutagentest med eller utan metabolisk aktivering. Enalapril var också negativ i följande genotoxicitetsstudier: rec-assay, omvänd mutationsanalys med E. coli, systerkromatidutbyte med odlade däggdjursceller och mikrokärntestet med möss, såväl som i en in vivo cytogen studie med musbenmärg .
Det fanns inga negativa effekter på reproduktionsförmågan hos han- och honråttor som behandlats med upp till 90 mg/kg/dag av enalapril (26 gånger MRHDD jämfört med kroppsyta).
Graviditet
Ammande mödrar
Enalapril och enalaprilat har påvisats i human bröstmjölk. På grund av risken för allvarliga biverkningar hos ammande spädbarn från enalapril, bör ett beslut fattas om att avbryta amningen eller att avbryta behandlingen med VASOTEC 2,5 mg, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Nyfödda med en historia av exponering i livmodern för VASOTEC
Om oliguri eller hypotoni uppstår, rikta uppmärksamheten mot stöd av blodtryck och njurperfusion. Utbytestransfusioner eller dialys kan krävas som ett sätt att vända hypotoni och/eller ersätta störd njurfunktion. Enalapril, som passerar placentan, har avlägsnats från neonatal cirkulation genom peritonealdialys med viss klinisk fördel och kan teoretiskt avlägsnas genom utbytestransfusion, även om det inte finns någon erfarenhet av det senare förfarandet.
Antihypertensiva effekter av VASOTEC har fastställts hos hypertensiva pediatriska patienter i åldern 1 månad till 16 år. Användning av VASOTEC 5 mg i dessa åldersgrupper stöds av bevis från adekvata och välkontrollerade studier av VASOTEC 2,5 mg på pediatriska och vuxna patienter samt av publicerad litteratur på pediatriska patienter (se KLINISK FARMAKOLOGI , Klinisk farmakologi hos pediatriska patienter och DOSERING OCH ADMINISTRERING ).
VASOTEC rekommenderas inte till nyfödda och till pediatriska patienter med glomerulär filtrationshastighet
ÖVERDOS
Begränsade data finns tillgängliga med avseende på överdosering hos människor.
Enstaka orala doser av enalapril över 1 000 mg/kg och ≥ 1 775 mg/kg associerades med dödlighet hos möss respektive råttor.
Den mest sannolika manifestationen av överdosering skulle vara hypotoni, för vilken den vanliga behandlingen skulle vara intravenös infusion av normal koksaltlösning.
Enalaprilat kan avlägsnas från den allmänna cirkulationen genom hemodialys och har avlägsnats från neonatal cirkulation genom peritonealdialys (se VARNINGAR , Anafylaktoida reaktioner under membranexponering ).
KONTRAINDIKATIONER
VASOTEC 2,5 mg är kontraindicerat till patienter som är överkänsliga mot denna produkt och till patienter med angioödem i anamnesen relaterat till tidigare behandling med en angiotensinkonverterande enzymhämmare och till patienter med ärftligt eller idiopatiskt angioödem.
Administrera inte aliskiren samtidigt med VASOTEC till patienter med diabetes (se LÄKEMEDELSINTERAKTIONER ).
VASOTEC 10 mg är kontraindicerat i kombination med en neprilysinhämmare (t.ex. sacubitril). Administrera inte VASOTEC inom 36 timmar efter byte till eller från sacubitril/valsartan, en neprilysinhämmare (se VARNINGAR ).
KLINISK FARMAKOLOGI
Handlingsmekanism
Enalapril, efter hydrolys till enalaprilat, hämmar angiotensinomvandlande enzym (ACE) hos människor och djur. ACE är ett peptidyldipeptidas som katalyserar omvandlingen av angiotensin I till den kärlsammandragande substansen, angiotensin II. Angiotensin II stimulerar också utsöndringen av aldosteron från binjurebarken. De gynnsamma effekterna av enalapril vid hypertoni och hjärtsvikt tycks främst bero på undertryckande av renin-angiotensin-aldosteronsystemet. Hämning av ACE resulterar i minskad plasmaangiotensin II, vilket leder till minskad vasopressoraktivitet och till minskad aldosteronsekretion. Även om den senare minskningen är liten, resulterar den i små ökningar av serumkalium. Hos hypertonipatienter som behandlats med enbart VASOTEC i upp till 48 veckor observerades en genomsnittlig ökning av serumkalium på cirka 0,2 mEq/L. Hos patienter som behandlades med VASOTEC 5 mg plus ett tiaziddiuretikum fanns det i princip ingen förändring i serumkalium (se FÖRSIKTIGHETSÅTGÄRDER ). Avlägsnande av angiotensin II negativ feedback på reninsekretion leder till ökad plasmareninaktivitet.
ACE är identisk med kininas, ett enzym som bryter ned bradykinin. Huruvida ökade nivåer av bradykinin, en potent vasodepressorpeptid, spelar en roll för de terapeutiska effekterna av VASOTEC återstår att utreda.
Medan mekanismen genom vilken VASOTEC 5 mg sänker blodtrycket tros främst vara suppression av renin-angiotensin-aldosteronsystemet, är VASOTEC 10 mg antihypertensivt även hos patienter med lågt reninhypertoni. Även om VASOTEC var antihypertensivt i alla studerade raser, hade svarta hypertonipatienter (vanligtvis en låg-reninhypertensiv population) ett lägre genomsnittligt svar på enalapril monoterapi än icke-svarta patienter.
Farmakokinetik och metabolism
Efter oral administrering av VASOTEC uppnås maximala serumkoncentrationer av enalapril inom cirka en timme. Baserat på urinåtervinning är absorptionsgraden av enalapril cirka 60 procent. Enalaprils absorption påverkas inte av närvaron av mat i mag-tarmkanalen. Efter absorption hydrolyseras enalapril till enalaprilat, som är en mer potent angiotensinomvandlande enzymhämmare än enalapril; enalaprilat absorberas dåligt när det administreras oralt. Maximala serumkoncentrationer av enalaprilat inträffar tre till fyra timmar efter en oral dos av enalaprilmaleat. Utsöndring av VASOTEC sker huvudsakligen via njurarna. Cirka 94 procent av dosen återvinns i urin och avföring som enalaprilat eller enalapril. De huvudsakliga komponenterna i urinen är enalaprilat, som står för cirka 40 procent av dosen, och intakt enalapril. Det finns inga tecken på metaboliter av enalapril, förutom enalaprilat.
Serumkoncentrationsprofilen för enalaprilat uppvisar en förlängd terminal fas, som uppenbarligen representerar en liten del av den administrerade dosen som har bundits till ACE. Mängden bunden ökar inte med dosen, vilket indikerar ett mättbart bindningsställe. Den effektiva halveringstiden för ackumulering av enalaprilat efter flera doser av enalaprilmaleat är 11 timmar. Fördelningen av enalapril och enalaprilat hos patienter med njurinsufficiens liknar den hos patienter med normal njurfunktion tills den glomerulära filtrationshastigheten är 30 ml/min eller mindre. Med glomerulär filtrationshastighet ≤ 30 ml/min ökar topp- och dalnivåerna för enalaprilat, tiden till toppkoncentrationen ökar och tiden till steady state kan försenas. Den effektiva halveringstiden för enalaprilat efter flera doser av enalaprilmaleat förlängs vid denna nivå av njurinsufficiens (se DOSERING OCH ADMINISTRERING ). Enalaprilat är dialyserbart med en hastighet av 62 ml/min.
Studier på hundar tyder på att enalapril passerar blod-hjärnbarriären dåligt, om alls; enalaprilat kommer inte in i hjärnan. Flera doser av enalaprilmaleat hos råttor resulterar inte i ackumulering i några vävnader. Mjölk från lakterande råttor innehåller radioaktivitet efter administrering av 14C-enalaprilmaleat. Radioaktivitet befanns passera placentan efter administrering av märkt läkemedel till gravida hamstrar.
Farmakodynamik och kliniska effekter
Hypertoni
Administrering av VASOTEC till patienter med hypertoni av svårighetsgrad från mild till svår resulterar i en sänkning av både liggande och stående blodtryck, vanligtvis utan ortostatisk komponent. Symtomatisk postural hypotension är därför sällsynt, även om den kan förväntas hos patienter med volymbrist (se VARNINGAR ).
Hos de flesta studerade patienter, efter oral administrering av en singeldos av enalapril, sågs en antihypertensiv aktivitet efter en timme med en maximal sänkning av blodtrycket uppnådd med fyra till sex timmar.
Vid rekommenderade doser har antihypertensiva effekter bibehållits i minst 24 timmar. Hos vissa patienter kan effekterna avta mot slutet av doseringsintervallet (se DOSERING OCH ADMINISTRERING ).
Hos vissa patienter kan det krävas flera veckors behandling för att uppnå optimal blodtryckssänkning.
De antihypertensiva effekterna av VASOTEC har fortsatt under långtidsbehandling. Plötsligt utsättande av VASOTEC 10 mg har inte associerats med en snabb ökning av blodtrycket.
hemodynamiska studier på patienter med essentiell hypertoni åtföljdes blodtryckssänkningen av en minskning av det perifera arteriella motståndet med en ökning av hjärtminutvolymen och liten eller ingen förändring i hjärtfrekvensen. Efter administrering av VASOTEC finns en ökning av njurblodflödet; glomerulär filtrationshastighet är vanligtvis oförändrad. Effekterna verkar vara liknande hos patienter med renovaskulär hypertoni.
När det ges tillsammans med diuretika av tiazidtyp är de blodtryckssänkande effekterna av VASOTEC 5 mg ungefär additiva.
I en klinisk farmakologisk studie gavs indometacin eller sulindak till hypertonipatienter som fick VASOTEC. I denna studie fanns det inga tecken på avtrubbning av den antihypertensiva effekten av VASOTEC (se LÄKEMEDELSINTERAKTIONER ).
Hjärtsvikt
studier på patienter som behandlats med digitalis och diuretika, resulterade behandling med enalapril i minskat systemiskt kärlmotstånd, blodtryck, pulmonärt kapillärt kiltryck och hjärtstorlek samt ökad hjärtminutvolym och träningstolerans. Hjärtfrekvensen var oförändrad eller något reducerad, och den genomsnittliga ejektionsfraktionen var oförändrad eller ökad. Det fanns en gynnsam effekt på svårighetsgraden av hjärtsvikt mätt enligt New York Heart Association (NYHA) klassificering och på symtom på dyspné och trötthet. Hemodynamiska effekter observerades efter den första dosen och verkade bibehållas i okontrollerade studier som varade så länge som fyra månader. Effekter på träningstolerans, hjärtstorlek och svårighetsgrad och symtom på hjärtsvikt observerades i placebokontrollerade studier som varade från åtta veckor till över ett år.
Hjärtsvikt, dödlighetsprövningar
en multicenter, placebokontrollerad klinisk prövning randomiserades 2 569 patienter med alla grader av symtomatisk hjärtsvikt och ejektionsfraktion ≤ 35 procent till placebo eller enalapril och följdes upp i upp till 55 månader (SOLVD-Treatment). Användning av enalapril associerades med en 11 procents minskning av dödligheten av alla orsaker och en 30 procents minskning av sjukhusvistelsen för hjärtsvikt. Sjukdomar som uteslöt patienter från att delta i studien inkluderade svår stabil angina (>2 attacker/dag), hemodynamiskt signifikant obstruktion av klaff- eller utflödeskanal, njursvikt (kreatinin >2,5 mg/dL), cerebrovaskulär sjukdom (t.ex. signifikant carotisartärsjukdom) , avancerad lungsjukdom, maligniteter, aktiv myokardit och konstriktiv perikardit. Mortalitetsfördelen förknippad med enalapril verkar inte bero på att digitalis förekommer.
En andra multicenterstudie använde SOLVD-protokollet för studier av asymtomatiska eller minimalt symtomatiska patienter. SOLVD-Prevention-patienter, som hade vänsterkammarejektionsfraktion ≤ 35 % och ingen historia av symtomatisk hjärtsvikt, randomiserades till placebo (n=2117) eller enalapril (n=2111) och följdes upp i upp till 5 år. Majoriteten av patienterna i SOLVD-preventionstudien hade en historia av ischemisk hjärtsjukdom. En historia av hjärtinfarkt fanns hos 80 procent av patienterna, nuvarande angina pectoris hos 34 procent och en historia av hypertoni hos 37 procent. Ingen statistiskt signifikant dödlighetseffekt påvisades i denna population. Enalaprilbehandlade försökspersoner hade 32 % färre första sjukhusinläggningar för hjärtsvikt och 32 % färre totala hjärtsviktsinläggningar. Jämfört med placebo utvecklade 32 procent färre patienter som fick enalapril symtom på uppenbar hjärtsvikt. Sjukhusinläggningar av kardiovaskulära skäl minskade också. Det fanns en obetydlig minskning av sjukhusinläggningar oavsett orsak i enalaprilbehandlingsgruppen (för enalapril vs. placebo, 1166 respektive 1201 första sjukhusinläggningar, 2649 vs. 2840 totala sjukhusinläggningar), även om studien inte hade möjlighet att leta efter en sådan effekt.
SOLVD-förebyggande studien var inte utformad för att avgöra om behandling av asymtomatiska patienter med låg ejektionsfraktion skulle vara överlägsen, med avseende på att förhindra sjukhusvistelse, än närmare uppföljning och användning av enalapril vid de tidigaste tecknen på hjärtsvikt. Under villkoren för uppföljning i SOLVD-preventionstudien (var 4:e månad på studiekliniken; personlig läkare vid behov), hade 68 % av patienterna på placebo som var inlagda på sjukhus för hjärtsvikt inga tidigare symtom som skulle ha signalerade behandlingsstart.
SOLVD-preventionsstudien var inte heller utformad för att visa om enalapril modifierade utvecklingen av underliggande hjärtsjukdom.
I ett annat multicenter, placebokontrollerad studie (CONSENSUS) begränsad till patienter med NYHA klass IV hjärtsvikt och radiografiska tecken på kardiomegali, var användning av enalapril associerad med förbättrad överlevnad. Resultaten visas i följande tabell.
både CONSENSUS- och SOLVD-Treatment-studier fick patienter också vanligtvis digitalis, diuretika eller båda.
Klinisk farmakologi hos pediatriska patienter
En farmakokinetisk multipeldosstudie utfördes på 40 hypertensiva manliga och kvinnliga pediatriska patienter i åldern 2 månader till ≤ 16 år efter daglig oral administrering av 0,07 till 0,14 mg/kg enalaprilmaleat. Vid steady state var den genomsnittliga effektiva halveringstiden för ackumulering av enalaprilat 14 timmar, och den genomsnittliga urinåtervinningen av totalt enalapril och enalaprilat under 24 timmar var 68 % av den administrerade dosen. Omvandlingen av enalapril till enalaprilat var i intervallet 63-76%. De övergripande resultaten av denna studie indikerar att farmakokinetiken för enalapril hos hypertensiva barn i åldern 2 månader till ≤ 16 år är konsekvent över de studerade åldersgrupperna och överensstämmer med farmakokinetiska historiska data hos friska vuxna.
en klinisk studie med 110 hypertensiva pediatriska patienter i åldern 6 till 16 år fick patienter som vägde
I ovanstående pediatriska studier gavs enalaprilmaleat som tabletter av VASOTEC och för de barn och spädbarn som inte kunde svälja tabletter eller som behövde en lägre dos än vad som finns tillgängligt i tablettform, gavs enalapril i en suspensionsformulering (se DOSERING OCH ADMINISTRERING , Förberedelse av upphängning ).
PATIENTINFORMATION
Angioödem
Angioödem, inklusive larynxödem, kan uppträda när som helst under behandling med angiotensinkonverterande enzymhämmare, inklusive enalapril. Patienter bör rådas och uppmanas att omedelbart rapportera alla tecken eller symtom som tyder på angioödem (svullnad av ansikte, extremiteter, ögon, läppar, tunga, svårigheter att svälja eller andas) och att inte ta mer läkemedel förrän de har rådfrågat den förskrivande läkaren.
Hypotoni
Patienter bör varnas för att rapportera yrsel, särskilt under de första dagarna av behandlingen. Om faktisk synkope inträffar ska patienterna uppmanas att avbryta läkemedlet tills de har rådfrågat den förskrivande läkaren. Alla patienter bör varnas för att överdriven svettning och uttorkning kan leda till ett överdrivet blodtrycksfall på grund av minskad vätskevolym. Andra orsaker till volymutarmning som kräkningar eller diarré kan också leda till ett blodtrycksfall; patienter bör rådas att rådgöra med läkaren.
Hyperkalemi
Patienter bör uppmanas att inte använda saltersättningsmedel som innehåller kalium utan att rådfråga sin läkare.
Neutropeni
Patienter bör uppmanas att omedelbart rapportera alla tecken på infektion (t.ex. halsont, feber) som kan vara tecken på neutropeni.
Graviditet
Kvinnliga patienter i fertil ålder bör informeras om konsekvenserna av exponering för VASOTEC under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Patienter bör uppmanas att rapportera graviditeter till sin läkare så snart som möjligt.
OBS: Som med många andra läkemedel är vissa råd till patienter som behandlas med enalapril berättigade. Denna information är avsedd att hjälpa till med säker och effektiv användning av detta läkemedel. Det är inte ett avslöjande av alla möjliga negativa eller avsedda effekter.
