Cozaar 25mg, 50mg, 100mg Losartan Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Cozaar 50mg och hur används det?
Cozaar är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni), minska risken för stroke hos vissa personer med hjärtsjukdom och diabetisk nervsmärta (neuropati). Cozaar 100mg kan användas ensamt eller tillsammans med andra läkemedel.
Cozaar 25mg tillhör en klass av läkemedel som kallas angiotensin II-receptorantagonister (ARB).
Det är inte känt om Cozaar 25mg är säkert och effektivt för barn yngre än 6 år.
Vilka är de möjliga biverkningarna av Cozaar 100mg?
Cozaar 100mg kan orsaka allvarliga biverkningar inklusive:
- yrsel,
- smärta eller sveda när du kissar,
- illamående,
- svaghet,
- pirrande känsla,
- bröstsmärta,
- oregelbundna hjärtslag,
- förlust av rörelser,
- lite eller ingen urinering,
- snabb viktökning, och
- svullnad i händer, fötter eller vrister
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Cozaar inkluderar:
- yrsel,
- ryggont, och
- förkylningssymtom (täppt näsa, nysningar, ont i halsen)
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Cozaar. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
När graviditet upptäcks, avbryt COZAAR så snart som möjligt. Läkemedel som verkar direkt på renin-angiotensinsystemet kan orsaka skador och dödsfall för fostret under utveckling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
BESKRIVNING
COZAAR (losartankalium) är en angiotensin II-receptorblockerare som verkar på AT1-receptorsubtypen. Losartankalium, en icke-peptidmolekyl, beskrivs kemiskt som 2-butyl-4-klor-1-[p-(o-1H-tetrazol-5-ylfenyl)bensyl]imidazol-5-metanolmonokaliumsalt.
Dess empiriska formel är C22H22ClKN6O, och dess strukturformel är:
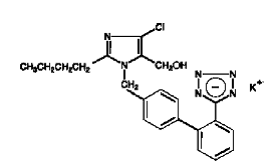
Losartankalium är ett vitt till benvitt fririnnande kristallint pulver med en molekylvikt på 461,01. Det är fritt lösligt i vatten, lösligt i alkoholer och något lösligt i vanliga organiska lösningsmedel, såsom acetonitril och metyletylketon. Oxidation av 5-hydroximetylgruppen på imidazolringen resulterar i den aktiva metaboliten av losartan.
COZAAR 100mg finns som tabletter för oral administrering innehållande antingen 25 mg, 50 mg eller 100 mg kaliumlosartan och följande inaktiva ingredienser: mikrokristallin cellulosa, vattenhaltig laktos, förgelatinerad stärkelse, magnesiumstearat, hydroxipropylcellulosa, hypromellos och titandioxid.
COZAAR 25 mg, 50 mg och 100 mg tabletter innehåller kalium i följande mängder: 2,12 mg (0,054 mekv), 4,24 mg (0,108 mekv) respektive 8,48 mg (0,216 mekv.). COZAAR 25 mg, COZAAR 50 mg och COZAAR 100 mg kan också innehålla karnaubavax.
INDIKATIONER
Hypertoni
COZAAR® är indicerat för behandling av hypertoni hos vuxna och pediatriska patienter 6 år och äldre, för att sänka blodtrycket. Att sänka blodtrycket sänker risken för dödliga och icke-dödliga kardiovaskulära (CV) händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade studier av blodtryckssänkande läkemedel från en mängd olika farmakologiska klasser inklusive losartan.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än 1 läkemedel för att uppnå blodtrycksmålen. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committeeon Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos droger, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad över populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras högt blodtryck (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter skulle förväntas gynnas från mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa antihypertensiva läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi.
COZAAR kan administreras tillsammans med andra antihypertensiva medel.
Hypertonipatienter med vänsterkammarhypertrofi
COZAAR 25 mg är indicerat för att minska risken för stroke hos patienter med hypertoni och vänsterkammarhypertrofi, men det finns bevis för att denna fördel inte gäller svarta patienter [se Användning i specifika populationer och KLINISK FARMAKOLOGI ] .
Nefropati hos typ 2-diabetespatienter
COZAAR är indicerat för behandling av diabetisk nefropati med förhöjt serumkreatinin och proteinuri (urinalbumin till kreatininförhållande ≥300 mg/g) slutenvårdspatienter med typ 2-diabetes och en historia av hypertoni. I denna population minskar COZAAR 50 mg progressionshastigheten för nefropati mätt som förekomsten av fördubbling av serumkreatinin eller njursjukdom i slutstadiet (behov av dialys eller njurtransplantation) [se Kliniska studier ] .
DOSERING OCH ADMINISTRERING
Hypertoni
Hypertoni för vuxna
Den vanliga startdosen av COZAAR 50 mg är 50 mg en gång dagligen. Dosen kan ökas till en maximal dos på 100 mg en gång dagligen efter behov för att kontrollera blodtrycket [se Kliniska studier ] . En startdos på 25 mg rekommenderas för patienter med möjlig intravaskulär utarmning (t.ex. på diuretikabehandling).
Pediatrisk hypertoni
Den vanliga rekommenderade startdosen är 0,7 mg per kg en gång dagligen (upp till 50 mg totalt) administrerat som en tablett eller suspension [se Beredning av suspension (för 200 ml av en 2,5 mg/ml suspension) ] .Dosering bör justeras efter blodtryckssvar. Doser över 1,4 mg per kg (eller över 100 mg) dagligen har inte studerats hos pediatriska patienter [se KLINISK FARMAKOLOGI , Kliniska studier och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ] .
COZAAR rekommenderas inte till pediatriska patienter under 6 år eller till pediatriska patienter med uppskattad glomerulär filtrationshastighet mindre än 30 ml/min/1,73 m 2 [se Användning i specifika populationer , KLINISK FARMAKOLOGI och Kliniska studier ] .
Hypertonipatienter med vänsterkammarhypertrofi
Den vanliga startdosen är 50 mg COZAAR en gång dagligen. Hydroklortiazid 12,5 mg dagligen bör läggas till och/eller dosen av COZAAR bör ökas till 100 mg en gång dagligen följt av en ökning av hydroklortiazid till 25 mg en gång dagligen baserat på blodtryckssvar [se Kliniska studier ] .
Nefropati hos typ 2-diabetespatienter
Den vanliga startdosen är 50 mg en gång dagligen. Dosen bör ökas till 100 mg en gång dagligen baserat på blodtryckssvar [se Kliniska studier ] .
Dosändringar hos patienter med nedsatt leverfunktion
Hos patienter med lätt till måttligt nedsatt leverfunktion är den rekommenderade startdosen av COZAAR 25 mg en gång dagligen. COZAAR har inte studerats hos patienter med gravt nedsatt leverfunktion [se Användning i specifika populationer och KLINISK FARMAKOLOGI ] .
Beredning av suspension (för 200 ml av en 2,5 mg/ml suspension)
Tillsätt 10 mL renat vatten USP till en 8 ounce (240 mL) bärnstensfärgad polyetylentereftalat (PET) flaska innehållande tio 50 mg COZAAR tabletter. Skaka omedelbart i minst 2 minuter. Låt koncentratet stå i 1 timme och skaka sedan i 1 minut för att skingra tablettinnehållet. Förbered separat en 50/50 volymetrisk blandning av Ora-Plus™ och Ora-Sweet SF™. Tillsätt 190 mL av 50/50 Ora-Plus™/Ora-Sweet SF™-blandningen till tabletten och vattenuppslamningen i PET-flaskan och skaka i 1 minut för att dispergera ingredienserna. Suspensionen ska förvaras i kylskåp vid 2-8°C (36-46°F) och kan förvaras i upp till 4 veckor. Skaka suspensionen före varje användning och ställ omedelbart tillbaka till kylskåpet.
HUR LEVERERAS
Doseringsformer och styrkor
- COZAAR 100 mg, 25 mg, är vita, ovala, filmdragerade tabletter med kod 951 på ena sidan.
- COZAAR, 50 mg, är vita, ovala, filmdragerade tabletter med kod 952 på ena sidan och skåra på den andra.
- COZAAR 25 mg, 100 mg, är vita, droppformade, filmdragerade tabletter med kod 960 på ena sidan.
Förvaring Och Hantering
COZAAR är en vit filmdragerad tablett som levereras enligt följande:
Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur]. Förvara behållaren väl tillsluten. Skydda från ljus.
Tillverkad för: Organon LLC, ett dotterbolag till ORGANON & Co., Jersey City, NJ 07302, USA. Reviderad: oktober 2021.
BIEFFEKTER
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Hypertoni
COZAAR har utvärderats för säkerhet hos mer än 3300 vuxna patienter som behandlats för essentiell hypertoni och 4058 patienter/subjekt totalt. Över 1200 patienter behandlades i över 6 månader och mer än 800 i över ett år.
Behandling med COZAAR 25 mg tolererades väl med en total förekomst av biverkningar liknande den för placebo. I kontrollerade kliniska prövningar inträffade avbrytande av behandlingen för biverkningar hos 2,3 % av patienterna som behandlades med COZAAR 25 mg och 3,7 % av patienterna som fick placebo. I 4 kliniska prövningar som involverade över 1 000 patienter på olika doser (10-150 mg) losartankalium och över 300 patienter som fick placebo, var de biverkningar som inträffade hos ≥2 % av patienterna som behandlades med COZAAR 25 mg och vanligare än placebo: yrsel (3 % vs. 2 %), övre luftvägsinfektion (8 % vs. 7 %), nästäppa (2 % vs. 1 %) och ryggsmärtor (2 % vs. 1 %).
Följande mindre vanliga biverkningar har rapporterats:
Blod- och lymfsystemet: Anemi.
Psykiatriska störningar: Depression.
Störningar i nervsystemet: Somnolens, huvudvärk, sömnstörningar, parestesi, migrän.
Öron- och labyrintsjukdomar: Vertigo, tinnitus.
Hjärtsjukdomar: Palpitationer, synkope, förmaksflimmer, CVA.
Andningsvägar, bröstkorg och mediastinum: Dyspné.
Gastrointestinala störningar: Buksmärtor, förstoppning, illamående, kräkningar.
Hud och subkutan vävnad: Urtikaria, klåda, hudutslag, ljuskänslighet.
Muskuloskeletala och bindvävssjukdomar: Myalgi, artralgi.
Reproduktionssystemet och bröststörningar: Impotens.
Allmänna symtom och tillstånd på administreringsstället: Ödem.
Hosta
Ihållande torrhosta (med en incidens på några procent) har associerats med användning av ACE-hämmare och kan i praktiken vara en orsak till utsättande av ACE-hämmare. Två prospektiva, dubbelblinda, randomiserade, kontrollerade prövningar i parallellgrupp genomfördes för att bedöma effekterna av losartan på förekomsten av patienter med hosta och hypertensiva patienter som hade upplevt hosta under behandling med ACE-hämmare. Patienter som hade typisk ACE-hämmande hosta när de utmanades med lisinopril, vars hosta försvann med placebo, randomiserades till losartan 50 mg, lisinopril 20 mg eller antingen placebo (en studie, n=97) eller 25 mg hydroklortiazid (n=135). Den dubbelblinda behandlingsperioden varade upp till 8 veckor. Förekomsten av hosta visas i tabell 1 nedan.
Dessa studier visar att incidensen av hosta i samband med behandling med losartan, i en population som alla hade hosta i samband med behandling med ACE-hämmare, liknar den som är förknippad med hydroklortiazid eller placebobehandling.
Fall av hosta, inklusive positiva re-utmaningar, har rapporterats efter användning av losartan efter marknadsföring.
Hypertonipatienter med vänsterkammarhypertrofi
I Losartan Intervention for Endpoint-studien (LIFE) liknade biverkningarna med COZAAR 100 mg de som tidigare rapporterats för patienter med hypertoni.
Nefropati hos typ 2-diabetespatienter
reduktionen av effektmått i NIDDM med angiotensin II-receptorantagonist Losartan (RENAAL)-studien som involverade 1513 patienter som behandlades med COZAAR 100 mg eller placebo, var den totala incidensen av rapporterade biverkningar liknande för de två grupperna. Utsättningar av COZAAR på grund av biverkningar liknade placebo (19 % för COZAAR 100 mg, 24 % för placebo). Biverkningarna, oavsett läkemedelssamband, som rapporterades med en incidens på ≥4 % av patienterna som behandlades med COZAAR 50 mg och som inträffade med ≥2 % skillnad i losartangruppen jämfört med placebo på en bakgrund av konventionell antihypertensiv behandling, var asteni/trötthet, bröstsmärta , hypotoni, ortostatisk hypotoni, diarré, anemi, hyperkalemi, hypoglykemi, ryggsmärta, muskelsvaghet och urinvägsinfektion.
Erfarenhet efter marknadsföring
Följande ytterligare biverkningar har rapporterats efter marknadsföring av COZAAR. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att uppskatta deras frekvens på ett tillförlitligt sätt eller att fastställa ett orsakssamband till läkemedelsexponering:
Matsmältningskanalen: Hepatit.
Allmänna störningar och villkor för administrationsplatsen: Obehag.
Hematologiska: Trombocytopeni.
Överkänslighet: Angioödem, inklusive svullnad av struphuvudet och glottis, som orsakar luftvägsobstruktion och/eller svullnad av ansikte, läppar, svalg och/eller tunga har rapporterats i sällsynta fall hos patienter som behandlats med losartan; några av dessa patienter har tidigare upplevt angioödem med andra läkemedel inklusive ACE-hämmare. Vaskulit, inklusive Henoch-Schönlein purpura, har rapporterats. Anafylaktiska reaktioner har rapporterats.
Metabolism och näring: Hyponatremi.
Muskuloskeletala: Rabdomyolys.
Störningar i nervsystemet: Dysgeusi.
Hud: Erytrodermi.
LÄKEMEDELSINTERAKTIONER
Medel som ökar serumkalium
Samtidig administrering av losartan med andra läkemedel som höjer serumkaliumnivåerna kan resultera i hyperkalemi. Övervaka serumkalium hos sådana patienter.
Litium
Ökning av serumlitiumkoncentrationer och litiumtoxicitet har rapporterats vid samtidig administrering av litium och angiotensin II-receptorantagonister. Övervaka serumlitiumnivåer vid samtidig användning.
Icke-steroida antiinflammatoriska läkemedel (NSAID) inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare)
Hos äldre patienter, volymbrist (inklusive de som får diuretikabehandling), eller med nedsatt njurfunktion, kan samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med angiotensin II-receptorantagonister (inklusive losartan) resultera i försämring av njurfunktionen, inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Övervaka njurfunktionen regelbundet hos patienter som behandlas med losartan och NSAID.
Den antihypertensiva effekten av angiotensin II-receptorantagonister, inklusive losartan, kan försvagas av NSAID, inklusive selektiva COX-2-hämmare.
Dubbel blockad av renin-angiotensinsystemet (RAS)
Dubbel blockad av RAS med angiotensinreceptorblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, synkope, hyperkalemi och förändringar i njurfunktionen (inklusive akut njursvikt) jämfört med monoterapi.
Veterans Affairs Nephropathy in Diabetes (VA NEPHRON-D) studien inkluderade 1448 patienter med typ 2-diabetes, förhöjt urin-albumin-till-kreatinin-förhållande och minskad uppskattad glomerulär filtrationshastighet (GFR 30 till 89,9 ml/min), randomiserade dem till lisinopril eller placebo på en bakgrund av losartanterapi och följde dem i median 2,2 år. Patienter som fick kombinationen losartan och lisinopril fick ingen ytterligare fördel jämfört med monoterapi för den kombinerade endpointen av minskning av GFR, njursjukdom i slutstadiet eller död, men upplevde en ökad incidens av hyperkalemi och akut njurskada jämfört med monoterapigruppen.
Hos de flesta patienter har ingen fördel associerats med att använda två RAS-hämmare samtidigt. Undvik i allmänhet kombinerad användning av RAS-hämmare. Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på COZAAR 100 mg och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med COZAAR 100 mg till patienter med diabetes. Undvik användning av aliskiren med COZAAR till patienter med nedsatt njurfunktion (GFR
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Fostertoxicitet
COZAAR kan orsaka fosterskador när det ges till en gravid kvinna. Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt COZAAR 100 mg så snart som möjligt [se Användning i specifika populationer ] .
Hypotension hos patienter med volym- eller saltbrist
Hos patienter med ett aktiverat renin-angiotensinsystem, såsom volym- eller saltfattiga patienter (t.ex. de som behandlas med höga doser diuretika), kan symtomatisk hypotension uppstå efter påbörjad behandling med COZAAR. Korrigera volym eller saltutarmning före administrering av COZAAR [se DOSERING OCH ADMINISTRERING ] .
Försämrad njurfunktion
Förändringar i njurfunktionen inklusive akut njursvikt kan orsakas av läkemedel som hämmar renin-angiotensinsystemet och av diuretika. Patienter vars njurfunktion kan bero delvis på aktiviteten hos renin-angiotensinsystemet (t.ex. patienter med njurartärstenos, kronisk njursjukdom, svår kronisk hjärtsvikt eller volymutarmning) kan ha en särskild risk att utveckla akut njursvikt på COZAAR. Övervaka njurfunktionen regelbundet hos dessa patienter. Överväg att avbryta eller avbryta behandlingen hos patienter som utvecklar en kliniskt signifikant minskning av njurfunktionen på COZAAR [se LÄKEMEDELSINTERAKTIONER och Användning i specifika populationer ] .
Hyperkalemi
Övervaka serumkalium regelbundet och behandla på lämpligt sätt. Dosminskning eller utsättande av COZAAR 25 mg kan behövas [se NEGATIVA REAKTIONER ] .
Samtidig användning av andra läkemedel som kan öka serumkalium kan leda till hyperkalemi [se LÄKEMEDELSINTERAKTIONER ] .
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen (patientinformation).
Graviditet
Informera kvinnliga patienter i fertil ålder om konsekvenserna av exponering för COZAAR 100 mg under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Säg till patienterna att rapportera graviditeter till sin läkare så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ] .
Kaliumtillskott
Råda patienter som får COZAAR att inte använda kaliumtillskott eller saltersättningsmedel som innehåller kalium utan att rådfråga sin vårdgivare [se LÄKEMEDELSINTERAKTIONER ] .
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Losartankalium var inte karcinogent när det administrerades i maximalt tolererade doser till råttor och möss under 105 respektive 92 veckor. Råttor av honkön som fick den högsta dosen (270 mg/kg/dag) hade en något högre incidens av pankreas acinar adenom. De maximalt tolererade doserna (270 mg/kg/dag hos råttor, 200 mg/kg/dag hos möss) gav systemisk exponering för losartan och dess farmakologiskt aktiva metabolit som var cirka 160 och 90 gånger (råttor) och 30 och 15 gånger (möss) exponeringen av en människa på 50 kg som fick 100 mg per dag.
Losartankalium var negativt i analysen av mikrobiell mutagenes och V-79 däggdjurscellmutagenes och i in vitro alkalisk eluering och in vitro och in vivo kromosomavvikelseanalyser. Dessutom visade den aktiva metaboliten inga tecken på genotoxicitet i mikrobiell mutagenes, in vitro alkalisk eluering och in vitro kromosomavvikelseanalyser.
Fertilitet och reproduktionsförmåga påverkades inte i studier med hanråttor som fick orala doser av losartankalium upp till cirka 150 mg/kg/dag. Administrering av toxiska dosnivåer hos kvinnor (300/200 mg/kg/dag) var associerad med en signifikant (p
Användning i specifika populationer
Graviditet
Risksammanfattning
COZAAR kan orsaka fosterskador när det ges till en gravid kvinna. Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. När graviditet upptäcks, avbryt COZAAR så snart som möjligt (se Kliniska överväganden ).
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa resultat. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för modern och/eller embryo/foster
Hypertoni under graviditeten ökar moderns risk för havandeskapsförgiftning, graviditetsdiabetes, för tidig förlossning och förlossningskomplikationer (t.ex. behov av kejsarsnitt, blödning efter förlossningen). Hypertoni ökar fostrets risk för intrauterin tillväxtbegränsning och intrauterin död. Gravida kvinnor med högt blodtryck bör övervakas noggrant och hanteras därefter.
Fetala/neonatala biverkningar
Oligohydramnios hos gravida kvinnor som använder läkemedel som påverkar renin-angiotensinsystemet under andra och tredje trimestern av graviditeten kan resultera i följande: nedsatt fosterns njurfunktion som leder till anuri och njursvikt, fosterlunghypoplasi, skelettdeformationer, inklusive skallhypoplasi, hypotoni , och döden. I det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar renin-angiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret.
Hos patienter som tar COZAAR under graviditet, utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Fostertest kan vara lämpligt, baserat på graviditetsveckan. Om oligohydramnios observeras, avbryt COZAAR 50 mg, såvida det inte anses vara livräddande för modern. Patienter och läkare bör dock vara uppmärksamma på att oligohydramnios kanske inte uppträder förrän efter att fostret har ådragit sig irreversibel skada.
Övervaka noggrant nyfödda med historik av exponering in utero för COZAAR för hypotoni, oliguri och hyperkalemi. Hos nyfödda med en historia av exponering in utero för COZAAR 100 mg, om oliguri eller hypotoni inträffar, stödja blodtryck och njurperfusion. Utbytestransfusioner eller dialys kan krävas som ett sätt att vända hypotension och ersätta njurfunktionen.
Data
Djurdata
Losartankalium administrerades oralt till råttor under perioden av sen dräktighet till och med laktation (dräktighetsdag 15 till och med laktationsdag 20) i doser på 10, 25 och 100 mg/kg/dag. Losartankalium har visat sig ge biverkningar hos råttfoster och nyfödda, inklusive minskad kroppsvikt, försenad fysisk utveckling och beteendeutveckling, mortalitet och njurtoxicitet. Med undantag för neonatal viktökning (som påverkades vid doser så låga som 10 mg/kg/dag), översteg doser associerade med dessa effekter 25 mg/kg/dag (ungefär tre gånger den maximala rekommenderade dosen för människa på 100 mg per mg /m basis). Dessa fynd tillskrivs läkemedelsexponering i sen dräktighet och under amning. Signifikanta nivåer av losartan och dess aktiva metabolit visades vara närvarande i råttfosterplasma under sen dräktighet och i råttmjölk.
Laktation
Risksammanfattning
Det är inte känt om losartan utsöndras i modersmjölk, men signifikanta nivåer av losartan och dess aktiva metabolit visades finnas i råttmjölk. På grund av risken för negativa effekter på det ammande barnet, bör ett beslut fattas om att avbryta amningen eller avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Antihypertensiva effekter av COZAAR har fastställts hos hypertensiva pediatriska patienter i åldern 6 till 16 år. Säkerhet och effektivitet har inte fastställts hos inpediatriska patienter under 6 år eller hos pediatriska patienter med glomerulär filtrationshastighet DOSERING OCH ADMINISTRERING , KLINISK FARMAKOLOGI och Kliniska studier ] .
Geriatrisk användning
Av det totala antalet patienter som fick COZAAR 25 mg i kontrollerade kliniska studier för hypertoni var 391 patienter (19 %) 65 år och äldre, medan 37 patienter (2 %) var 75 år och äldre. I en kontrollerad klinisk studie för njurskydd hos patienter med typ 2-diabetes med proteinuri var 248 patienter (33%) 65 år och äldre. I en kontrollerad klinisk studie för minskning av den kombinerade risken för kardiovaskulär död, stroke och hjärtinfarkt hos hypertonipatienter med vänsterkammarhypertrofi, var 2857 patienter (62%) 65 år och äldre, medan 808 patienter (18%) var 75 år och äldre. . Inga övergripande skillnader i effektivitet eller säkerhet observerades mellan dessa patienter och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas.
Lopp
LIFE-studien löpte svarta patienter med hypertoni och vänsterkammarhypertrofi behandlade med atenolol lägre risk att uppleva den primära sammansatta endpointen jämfört med svarta patienter som behandlades med COZAAR (båda behandlade samtidigt med hydroklortiazid hos majoriteten av patienterna). Det primära effektmåttet var den första förekomsten av stroke, hjärtinfarkt eller kardiovaskulär död, analyserad med en intention-to-treat (ITT) metod. I subgruppen av svarta patienter (n=533, 6 % av patienterna i LIFE-studien) fanns det 29 primära effektmått bland 263 patienter på atenolol (11 %, 26 per 1 000 patientår) och 46 primära effektmått bland 270 patienter (17 %). , 42 per 1000 patientår) på COZAAR. Detta fynd kunde inte förklaras på basis av skillnader i andra populationer än ras eller på någon obalans mellan behandlingsgrupper. Dessutom var blodtryckssänkningar i båda behandlingsgrupperna konsekventa mellan svarta och icke-svarta patienter. Med tanke på svårigheten att tolka skillnader i delmängder i stora försök, kan det inte vara känt om den observerade skillnaden är ett resultat av slumpen. LIFE-studien ger dock inga bevis för att fördelarna med COZAAR 100 mg för att minska risken för kardiovaskulära händelser hos hypertonipatienter med vänsterkammarhypertrofi gäller för svarta patienter [se Kliniska studier ] .
Nedsatt njurfunktion
Patienter med njurinsufficiens har förhöjda plasmakoncentrationer av losartan och dess aktiva metabolit jämfört med patienter med normal njurfunktion. Ingen dosjustering är nödvändig hos patienter med nedsatt njurfunktion såvida inte en patient med nedsatt njurfunktion också är volymbrist [se DOSERING OCH ADMINISTRERING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och KLINISK FARMAKOLOGI ] .
Nedsatt leverfunktion
Den rekommenderade startdosen av COZAAR är 25 mg till patienter med lätt till måttligt nedsatt leverfunktion. Efter oral administrering till patienter med lätt till måttligt nedsatt leverfunktion var plasmakoncentrationerna av losartan och dess aktiva metabolit 5 gånger respektive 1,7 gånger de som ses hos friska frivilliga. COZAAR har inte studerats hos patienter med gravt nedsatt leverfunktion [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ] .
ÖVERDOS
Signifikant dödlighet observerades hos möss och råttor efter oral administrering av 1000 mg/kg respektive 2000 mg/kg, cirka 44 och 170 gånger den maximala rekommenderade dosen för människor på mg/m2-basis.
Begränsade data finns tillgängliga med avseende på överdosering hos människor. Den mest sannolika manifestationen av överdosering skulle vara hypotoni och takykardi; bradykardi kan uppstå från parasympatisk (vagal) stimulering. Om symtomatisk hypotoni skulle uppstå, bör stödbehandling sättas in.
Varken losartan eller dess aktiva metabolit kan avlägsnas genom hemodialys.
KONTRAINDIKATIONER
COZAAR 50 mg är kontraindicerat:
- Hos patienter som är överkänsliga mot någon komponent i denna produkt.
- För samtidig administrering med aliskiren hos patienter med diabetes.
KLINISK FARMAKOLOGI
Handlingsmekanism
Angiotensin II [bildat från angiotensin I i en reaktion katalyserad av angiotensinomvandlande enzym (ACE, kininas II)] är en potent vasokonstriktor, det primära vasoaktiva hormonet i renin-angiotensinsystemet, och en viktig komponent i patofysiologin för hypertoni. Det stimulerar också utsöndringen av aldosteron från binjurebarken. Losartan och dess huvudsakliga aktiva metabolit blockerar de vasokonstriktor- och aldosteronutsöndrande effekterna av angiotensin II genom att selektivt blockera bindningen av angiotensin II till AT1-receptorn som finns i många vävnader, (t.ex. vaskulär glatt muskulatur, binjure). Det finns också en AT1-receptor i många vävnader, men den är inte känd för att vara associerad med kardiovaskulär homeostas. Varken losartan eller dess huvudsakliga aktiva metabolit uppvisar någon partiell agonistaktivitet vid AT1-receptorn, och båda har mycket större affinitet (cirka 1000 gånger) för AT1-receptorn än för AT1-receptorn. In vitro-bindningsstudier indikerar att losartan är en reversibel, kompetitiv hämmare av AT1-receptorn. Den aktiva metaboliten är 10 till 40 gånger mer potent i vikt än losartan och verkar vara en reversibel, icke-kompetitiv hämmare av AT1-receptorn.
Varken losartan eller dess aktiva metabolit hämmar ACE (kininas II, enzymet som omvandlar angiotensin I till angiotensin II och bryter ned bradykinin), inte heller binder de till eller blockerar andra hormonreceptorer eller jonkanaler som är kända för att vara viktiga för kardiovaskulär reglering.
Farmakodynamik
Losartan hämmar pressoreffekten av angiotensin II (liksom angiotensin I) infusioner. En dos på 100 mg hämmar pressoreffekten med cirka 85 % vid topp med 25-40 % hämning som kvarstår i 24 timmar. Avlägsnande av den negativa återkopplingen av angiotensin II orsakar en fördubbling till tredubbling av plasmareninaktiviteten och en åtföljande höjning av plasmakoncentrationen av inangiotensin II hos hypertonipatienter. Losartan påverkar inte svaret på bradykinin, medan ACE-hämmare ökar svaret på bradykinin. Aldosteronplasmakoncentrationerna faller efter administrering av losartan. Trots effekten av losartan på aldosteronsekretionen, observerades mycket liten effekt på kalium i serum.
Effekten av losartan är väsentligen närvarande inom en vecka, men i vissa studier inträffade den maximala effekten inom 3-6 veckor. I långtidsuppföljningsstudier (utan placebokontroll) verkade effekten av losartan bibehållas i upp till ett år. Det finns ingen uppenbar rebound-effekt efter abrupt utsättande av losartan. Det var i huvudsak ingen förändring i genomsnittlig hjärtfrekvens hos losartanbehandlade patienter i kontrollerade studier.
Farmakokinetik
Absorption
Efter oral administrering absorberas losartan väl och genomgår en betydande first-pass-metabolism. Den systemiska biotillgängligheten för losartan är cirka 33 %. Genomsnittlig maximal koncentration av losartan och dess aktiva metabolit uppnås inom 1 timme respektive efter 3-4 timmar. Medan maximala plasmakoncentrationer av losartan och dess aktiva metabolit är ungefär lika, är AUC (area under kurvan) för metaboliten cirka 4 gånger så stor som den för losartan. En måltid saktar ner absorptionen av losartan och minskar dess Cmax men har endast mindre effekter på losartans AUC eller på metabolitens AUC (~10 % minskning). Farmakokinetiken för losartan och dess aktiva metabolit är linjär med orala losartandoser upp till 200 mg och förändras inte över tiden.
Distribution
Distributionsvolymen för losartan och den aktiva metaboliten är cirka 34 liter respektive 12 liter. Både losartan och dess aktiva metabolit är i hög grad bundna till plasmaproteiner, främst albumin, med plasmafria fraktioner på 1,3 % respektive 0,2 %. Plasmaproteinbindningen är konstant över det koncentrationsintervall som uppnås med rekommenderade doser. Studier på råttor tyder på att losartan passerar blod-hjärnbarriären dåligt, om alls.
Ämnesomsättning
Losartan är ett oralt aktivt medel som genomgår betydande första-passage-metabolism av cytokrom P450-enzymer. Det omvandlas delvis till en aktiv karboxylsyrametabolit som är ansvarig för det mesta av angiotensin II-receptorantagonismen som följer efter behandling med losartan. Cirka 14 % av en oralt administrerad dos av losartan omvandlas till den aktiva metaboliten. Förutom den aktiva karboxylsyrametaboliten bildas flera inaktiva metaboliter. In vitro-studier indikerar att cytokrom P450 2C9 och 3A4 är involverade i biotransformationen av losartan till dess metaboliter.
Eliminering
Totalt plasmaclearance av losartan och den aktiva metaboliten är cirka 600 ml/min respektive 50 ml/min, med njurclearance på cirka 75 ml/min respektive 25 ml/min. Den terminala halveringstiden för losartan är cirka 2 timmar och för metaboliten är cirka 6-9 timmar. Efter engångsdoser av losartan administrerat oralt utsöndras cirka 4 % av dosen oförändrad i urinen och cirka 6 % utsöndras i urinen som aktiv metabolit. Gallutsöndring bidrar till elimineringen av losartan och dess metaboliter. Efter oral 14C-märkt losartan återfinns cirka 35 % av radioaktiviteten i urinen och cirka 60 % i avföringen. Efter en intravenös dos av 14C-märkt losartan återfinns cirka 45 % av radioaktiviteten i urinen och 50 % i avföringen. Varken losartan eller dess metabolit ackumuleras i plasma vid upprepad dosering en gång dagligen.
Specifika populationer
Pediatrisk
Farmakokinetiska parametrar efter flera doser av losartan (genomsnittlig dos 0,7 mg/kg, intervall 0,36 till 0,97 mg/kg) som en tablett till 25 hypertensiva patienter i åldern 6 till 16 år visas i Tabell 4 nedan. Farmakokinetiken för losartan och dess aktiva metabolit var i allmänhet likartad i de studerade åldersgrupperna och liknande historiska farmakokinetiska data hos vuxna. De viktigaste farmakokinetiska parametrarna hos vuxna och barn visas i tabellen nedan.
Biotillgängligheten för suspensionsformuleringen jämfördes med losartantabletter hos friska vuxna. Suspensionen och tabletten liknar sin biotillgänglighet med avseende på både losartan och den aktiva metaboliten [se DOSERING OCH ADMINISTRERING ] .
Geriatrik och genus
Losartans farmakokinetik har undersökts hos äldre (65-75 år) och hos båda könen. Plasmakoncentrationerna av losartan och dess aktiva metabolit är likartade hos äldre och unga hypertoniker. Plasmakoncentrationerna av losartan var ungefär dubbelt så höga hos kvinnliga hypertensiva som malehypertensiva, men koncentrationerna av den aktiva metaboliten var likartade hos män och kvinnor. Ingen dosjustering är nödvändig [se DOSERING OCH ADMINISTRERING ] .
Lopp
Farmakokinetiska skillnader på grund av ras har inte studerats [se Användning i specifika populationer ] .
Njurinsufficiens
Efter oral administrering ökar plasmakoncentrationerna och AUC för losartan och dess aktiva metabolit med 50-90 % hos patienter med mild (kreatininclearance på 50 till 74 ml/min) eller måttlig (kreatininclearance 30 till 49 ml/min) njurinsufficiens . I denna studie reducerades njurclearance med 55-85 % för både losartan och dess aktiva metabolit hos patienter med mild eller måttlig njurinsufficiens. Varken losartan eller dess aktiva metabolit kan avlägsnas genom hemodialys [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ] .
Leverinsufficiens
Efter oral administrering till patienter med mild till måttlig alkoholisk levercirros var plasmakoncentrationerna av losartan och dess aktiva metabolit fem gånger respektive cirka 1,7 gånger högre än hos unga frivilliga män. Jämfört med normala försökspersoner var den totala plasmaclearancen för slutenvårdspatienter med losartan med leverinsufficiens cirka 50 % lägre och den orala biotillgängligheten cirka fördubblades. Använd en startdos på 25 mg för patienter med lätt till måttligt nedsatt leverfunktion. COZAAR 50 mg har inte studerats hos patienter med gravt nedsatt leverfunktion [se DOSERING OCH ADMINISTRERING och Användning i specifika populationer ] .
Läkemedelsinteraktioner
Inga kliniskt signifikanta läkemedelsinteraktioner har hittats i studier av losartankalium med hydroklortiazid, digoxin, warfarin, cimetidin och fenobarbital. Rifampin har dock visats minska AUC för losartan och dess aktiva metabolit med 30 % respektive 40 %. Flukonazol, en hämmare av cytokromP450 2C9, minskade AUC för den aktiva metaboliten med cirka 40 %, men ökade AUC för losartan med cirka 70 % efter flera doser. Omvandling av losartan till dess aktiva metabolit efter intravenös administrering påverkas inte av ketokonazol, en hämmare av P450 3A4. AUC för aktiv metabolit efter oral losartan påverkades inte av erytromycin, en hämmare av P450 3A4, men AUC för losartan ökade med 30 %.
De farmakodynamiska konsekvenserna av samtidig användning av losartan och hämmare av P450 2C9 har inte undersökts. Patienter som inte metaboliserar losartan till aktiv metabolit har visats ha en specifik, sällsynt defekt i cytokrom P450 2C9. Dessa data tyder på att omvandlingen av losartan till dess aktiva metabolit huvudsakligen förmedlas av P450 2C9 och inte av P450 3A4.
Kliniska studier
Hypertoni
Hypertoni för vuxna
De antihypertensiva effekterna av COZAAR 25 mg demonstrerades huvudsakligen i 4 placebokontrollerade, 6- till 12-veckorsstudier med doser från 10 till 150 mg per dag hos patienter med ett diastoliskt blodtryck vid baslinjen på 95-115. Studierna möjliggjorde jämförelser av två doser (50-100 mg/dag) som en gång dagligen eller två gånger dagligen, jämförelser av topp- och daleffekter och jämförelser av respons efter kön, ålder och ras. Tre ytterligare studier undersökte de antihypertensiva effekterna av losartan och hydroklortiazid i kombination.
De 4 studierna av losartan monoterapi omfattade totalt 1075 patienter randomiserade till flera doser losartan och 334 till placebo. Doserna på 10 och 25 mg gav viss effekt vid topp (6 timmar efter dosering) men små och inkonsekventa dalsvar (24 timmar). Doser på 50, 100 och 150 mg en gång dagligen gav statistiskt signifikanta systoliska/diastoliska medelblodtryckssänkningar, jämfört med placebo i intervallet 5,5-10,5/3,5-7,5 mmHg, där dosen på 150 mg inte gav större effekt än 50- 100 mg. Dosering två gånger dagligen vid 50-100 mg/dag gav genomgående större dalsvar än dosering en gång dagligen vid samma totala dos. Toppeffekter (6 timmar) var enhetliga, men måttliga, större än daleffekter, med dal-till-topp-förhållandet för systoliska och diastoliska svar 50-95% respektive 60-90%.
Tillägg av en låg dos hydroklortiazid (12,5 mg) till losartan 50 mg en gång dagligen resulterade i placebojusterade blodtryckssänkningar på 15,5/9,2 mmHg.
Analys av ålder, kön och ras undergrupper av patienter visade att män och kvinnor, och patienter över och under 65, hade generellt liknande svar. COZAAR 25 mg var effektivt för att sänka blodtrycket oavsett ras, även om effekten var något mindre hos svarta patienter (vanligtvis en population med låg reninhalt).
Pediatrisk hypertoni
Den antihypertensiva effekten av losartan studerades i en studie med 177 hypertensiva pediatriska patienter i åldern 6 till 16 år. Barn som vägde DOSERING OCH ADMINISTRERING . Majoriteten av barnen hade hypertoni associerad med njursjukdom och urogenital sjukdom. Det sittande diastoliska blodtrycket (SiDBP) vid inträdet i studien var högre än 95:e percentilnivån för patientens ålder, kön och längd. I slutet av tre veckor minskade losartan det systoliska och diastoliska blodtrycket, mätt vid dalgången, på ett dosberoende sätt. Sammantaget minskade de två högre doserna (25 till 50 mg hos patienter
Hypertonipatienter med vänsterkammarhypertrofi
LIFE-studien var en multinationell, dubbelblind studie som jämförde COZAAR 50 mg och atenolol hos 9193 hypertonipatienter med EKG-dokumenterad vänsterkammarhypertrofi. Patienter med hjärtinfarkt eller stroke inom sex månader före randomisering exkluderades. Patienterna randomiserades till att få COZAAR 50 mg en gång dagligen eller 50 mg atenolol. Om målblodtrycket (
Av de randomiserade patienterna var 4963 (54%) kvinnor och 533 (6%) var svarta. Medelåldern var 67 med 5704 (62%) ålder ≥65. Vid baslinjen hade 1195 (13%) diabetes, 1326 (14%) hade isolerad systolisk hypertoni, 1469 (16%) hade kranskärlssjukdom och 728 (8%) hade cerebrovaskulär sjukdom. Baslinjemedelblodtrycket var 174/98 mmHg i båda behandlingsgrupperna. Den genomsnittliga uppföljningslängden var 4,8 år. I slutet av studien eller vid det sista besöket före ett primärt effektmått tog fortfarande 77 % av gruppen som behandlades med COZAAR 50 mg och 73 % av gruppen som behandlades med atenolol studiemedicin. Av de patienter som fortfarande tog studieläkemedel var medeldoserna av COZAAR och atenolol båda cirka 80 mg/dag, och 15 % tog atenolol eller losartan som monoterapi, medan 77 % också fick hydroklortiazid (med en genomsnittlig dos på 20 mg/dag i varje grupp). Blodtryckssänkningen uppmätt vid dal var likartad för båda behandlingsgrupperna men blodtrycket mättes inte vid någon annan tidpunkt på dagen. Vid slutet av studien eller vid det sista besöket före ett primärt effektmått var medelblodtrycket 144,1/81,3 mmHg för gruppen som behandlades med COZAAR och 145,4/80,9 mmHg för gruppen som behandlades med atenolol; skillnaden i systoliskt blodtryck (SBP) på 1,3 mmHg var signifikant (p
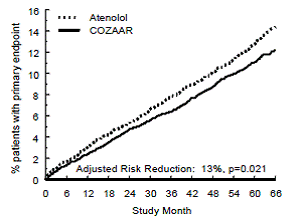
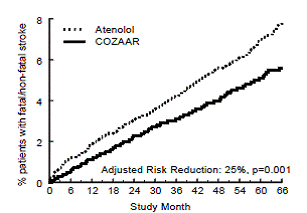
Det primära effektmåttet var den första förekomsten av kardiovaskulär död, icke-fatal stroke eller icke-fatal hjärtinfarkt. Patienter med icke-dödliga händelser stannade kvar i försöket, så att det också gjordes en undersökning av den första händelsen av varje typ även om det inte var den första händelsen (t.ex. en stroke efter en initial hjärtinfarkt skulle räknas med i analysen av stroke). Behandling med COZAAR 50 mg resulterade i en 13 % minskning (p=0,021) av risken för det primära effektmåttet jämfört med atenololgruppen (se figur 1 och tabell 3); denna skillnad var främst resultatet av en effekt på dödlig och icke-dödlig stroke. Behandling med COZAAR minskade risken för stroke med 25 % i förhållande till atenolol (p=0,001) (se figur 2 och tabell 3).
Figur 1: Kaplan-Meier uppskattningar av den primära slutpunkten för tid till kardiovaskulär död, icke-fatal stroke eller icke-dödlig hjärtinfarkt i grupperna som behandlades med COZAAR 100 mg och atenolol. Riskminskningen är justerad för Framingham-riskpoäng vid baslinjen och nivån av elektrokardiografisk vänsterkammarhypertrofi
Figur 2: Kaplan-Meier uppskattningar av tiden till dödlig/icke-dödlig stroke i grupperna som behandlats med COZAAR 50 mg och atenolol. Riskminskningen är justerad för baslinjeFramingham riskpoäng och nivå av elektrokardiografisk vänsterkammarhypertrofi
Tabell 3 visar resultaten för den primära sammansatta endpointen och de individuella endpoints. Det primära effektmåttet var den första förekomsten av stroke, myokardinfarkt eller kardiovaskulär död, analyserad med ITT-metoden. Tabellen visar antalet händelser för varje komponent på två olika sätt. Komponenterna i den primära slutpunkten (som en första händelse) räknar endast de händelser som definierar den primära slutpunkten, medan de sekundära slutpunkterna räknar alla första händelser av en viss typ, oavsett om de föregicks av en annan typ av händelse eller inte.
Även om LIFE-studien gynnade COZAAR framför atenolol med avseende på det primära effektmåttet (p=0,021), är detta resultat från en enda studie och är därför mindre övertygande än skillnaden mellan COZAAR och placebo. Även om den inte mäts direkt, är skillnaden mellan COZAAR och placebo övertygande eftersom det finns bevis för att atenolol i sig är effektivt (mot placebo) för att minska kardiovaskulära händelser, inklusive stroke, hos hypertonipatienter.
Andra kliniska effektmått för LIFE-studien var: total dödlighet, sjukhusvistelse för hjärtsvikt eller angina pectoris, koronar eller perifera revaskulariseringsprocedurer och återupplivat hjärtstillestånd. Det fanns inga signifikanta skillnader i frekvensen av dessa effektmått mellan COZAAR- och atenololgrupperna.
För det primära effektmåttet och stroke visas effekterna av COZAAR 25 mg i patientundergrupper definierade av ålder, kön, ras och närvaro eller frånvaro av isolerad systolisk hypertoni (ISH), diabetes och historia av kardiovaskulär sjukdom (CVD) i figur 3 nedan. . Subgruppsanalyser kan vara svåra att tolka och det är inte känt om dessa representerar verkliga skillnader eller slumpmässiga effekter.
Figur 3: Primära slutpunktshändelser† inom demografiska undergrupper
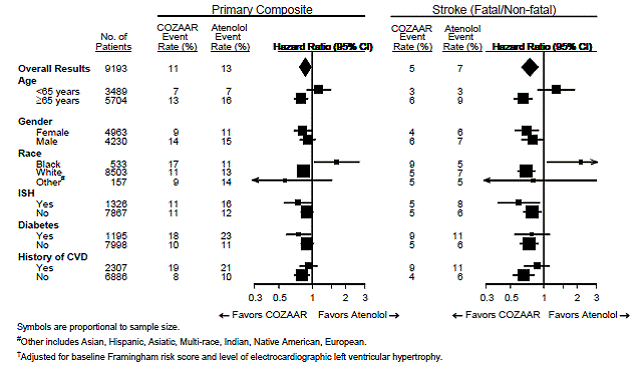
Nefropati hos typ 2-diabetespatienter
RENAAL-studien var en randomiserad, placebokontrollerad, dubbelblind, multicenterstudie utförd över hela världen på 1513 patienter med typ 2-diabetes med nefropati (definierad som serumkreatinin 1,3 till 3,0 mg/dL hos kvinnor eller män ≤60 kg och 1,5 till 3,0 mg /dL hos män >60 kg och proteinuri [urinalbumin-tokreatininförhållande ≥300 mg/g]).
Patienterna randomiserades till att få COZAAR 50 mg en gång dagligen eller placebo på en bakgrund av konventionell antihypertensiv terapi exklusive ACE-hämmare och angiotensin II-antagonister. Efter en månad instruerades utredarna att titrera studieläkemedlet till 100 mg en gång dagligen om det dalta blodtrycksmålet (140/90 mmHg) inte uppnåddes. Totalt sett fick 72 % av patienterna den dagliga dosen på 100 mg mer än 50 % av tiden de fick studieläkemedlet. Eftersom studien utformades för att uppnå lika blodtryckskontroll i båda grupperna, kunde andra antihypertensiva medel (diuretika, kalciumkanalblockerare, alfa- eller betablockerare och centralt verkande medel) läggas till efter behov i båda grupperna. Patienterna följdes under en genomsnittlig varaktighet på 3,4 år.
Studiepopulationen var olika med avseende på ras (asiatiska 16,7 %, svarta 15,2 %, latinamerikaner 18,3 %, vita 48,6 %). Totalt var 63,2 % av patienterna män och 66,4 % var under 65 år. Nästan alla patienter (96,6%) hade en historia av hypertoni, och patienterna gick in i studien med ett genomsnittligt serumkreatinin på 1,9 mg/dL och en genomsnittlig proteinuri (urinalbumin/kreatinin) på 1808 mg/g vid baslinjen.
Studiens primära effektmått var tiden till första inträffandet av någon av följande händelser: fördubbling av serumkreatinin, slutstadiet av njursjukdom (ESRD) (behov av dialys eller transplantation) eller dödsfall. Behandling med COZAAR resulterade i en riskminskning på 16 % i denna effektmått (se figur 4 och tabell 4). Behandling med COZAAR minskade också förekomsten av ihållande fördubbling av serumkreatinin med 25 % och ESRD med 29 % som separata effektmått, men hade ingen effekt på den totala dödligheten (se tabell 4).
Det genomsnittliga utgångsblodtrycket var 152/82 mmHg för COZAAR plus konventionell antihypertensiv behandling och 153/82 mmHg för placebo plus konventionell antihypertensiv behandling. Vid slutet av studien var medelblodtrycket 143/76 mmHg för gruppen som behandlades med COZAAR 100 mg och 146/77 mmHg för gruppen som behandlades med placebo.
Figur 4: Kaplan-Meier-kurva för den primära sammansatta slutpunkten för fördubbling av serumkreatinin, njursjukdom i slutstadiet (behov av dialys eller transplantation) eller död
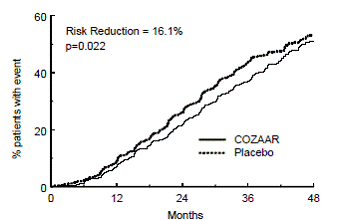
Studiens sekundära effektmått var förändring i proteinuri, förändring i progressionshastigheten av njursjukdom och sammansättningen av sjuklighet och dödlighet från kardiovaskulära orsaker (sjukhusinläggning för hjärtsvikt, hjärtinfarkt, revaskularisering, stroke, sjukhusvistelse för instabil angina eller kardiovaskulär sjukdom Jämfört med placebo minskade COZAAR proteinuri signifikant med i genomsnitt 34 %, en effekt som var uppenbar inom 3 månader efter påbörjad behandling, och minskade signifikant graden av minskning av glomerulär filtrationshastighet under studien med 13 %, mätt med den reciproka av serumkreatininkoncentrationen. Det fanns ingen signifikant skillnad i incidensen av den sammansatta endpointen av kardiovaskulär sjuklighet och mortalitet.
De gynnsamma effekterna av COZAAR sågs hos patienter som också tog andra blodtryckssänkande läkemedel (angiotensin II-receptorantagonister och angiotensinkonverteringszymhämmare var inte tillåtna), orala hypoglykemiska medel och lipidsänkande medel.
För det primära effektmåttet och ESRD visas effekterna av COZAAR i patientundergrupper definierade av ålder, kön och ras i Tabell 5 nedan. Undergruppsanalyser kan vara svåra att tolka och det är inte känt om dessa representerar verkliga skillnader eller slumpmässiga effekter.
PATIENTINFORMATION
COZAAR® (CO-zar) (losartan kalium tabletter) 25 mg, 50 mg, 100 mg
Läs patientinformationen som följer med COZAAR innan du börjar ta den och varje gång du får en påfyllning. Det kan komma ny information. Denna bipacksedel ersätter inte att prata med din läkare om ditt tillstånd och din behandling.
Vilken är den viktigaste informationen jag borde veta om COZAAR?
- COZAAR kan orsaka skada eller dödsfall för ett ofött barn.
- Tala med din läkare om andra sätt att sänka ditt blodtryck om du planerar att bli gravid.
- Om du blir gravid medan du tar COZAAR, berätta omedelbart för din läkare.
Vad är COZAAR 100mg?
COZAAR 100mg är ett receptbelagt läkemedel som kallas angiotensinreceptorblockerare (ARB). Den är använd:
- enbart eller tillsammans med andra blodtrycksmediciner för att sänka högt blodtryck (hypertoni).
- för att minska risken för stroke hos patienter med högt blodtryck och ett hjärtproblem som kallas vänsterkammarhypertrofi. COZAAR kanske inte hjälper svarta patienter med detta problem.
- för att bromsa försämringen av diabetisk njursjukdom (nefropati) hos patienter med typ 2-diabetes som har eller haft högt blodtryck.
COZAAR 25 mg har inte studerats på barn yngre än 6 år eller på barn med vissa njurproblem.
Högt blodtryck (hypertoni) Blodtrycket är kraften i dina blodkärl när ditt hjärta slår och när ditt hjärta vilar. Du har högt blodtryck när kraften är för stor. COZAAR 25mg kan hjälpa dina blodkärl att slappna av så att ditt blodtryck blir lägre.
Vänsterkammarhypertrofi (LVH) är en förstoring av väggarna i hjärtats vänstra kammare (hjärtats huvudpumpkammare). LVH kan hända från flera saker. Högt blodtryck är den vanligaste orsaken till LVH.
Typ 2-diabetes med nefropati . Typ 2-diabetes är en typ av diabetes som förekommer främst hos vuxna. Om du har diabetisk nefropati betyder det att dina njurar inte fungerar korrekt på grund av skador från diabetes.
Vem bör inte ta COZAAR 100mg?
- Ta inte COZAAR 25 mg om du är allergisk mot något av innehållsämnena i COZAAR . Se slutet av denna bipacksedel för en komplett lista över ingredienser i COZAAR.
- Ta inte COZAAR om du har diabetes och tar ett läkemedel som heter aliskiren för att sänka blodtrycket.
Vad ska jag berätta för min läkare innan jag tar COZAAR 50mg?
Berätta för din läkare om alla dina medicinska tillstånd inklusive om du:
- är gravid eller planerar att bli gravid. Ser " Vilken är den viktigaste informationen jag borde veta om COZAAR 25mg? "
- ammar . Det är inte känt om COZAAR 50 mg går över i din bröstmjölk. Du bör välja att antingen ta COZAAR 50 mg eller amma, men inte båda.
- kräks mycket eller har mycket diarré
- har leverproblem
- har njurproblem
Berätta för din läkare om alla läkemedel du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. COZAAR och vissa andra läkemedel kan interagera med varandra. Tala särskilt om för din läkare om du tar:
- kaliumtillskott
- saltersättningsmedel innehållande kalium
- andra läkemedel som kan öka serumkalium
- vattenpiller (diuretika)
- litium (ett läkemedel som används för att behandla en viss typ av depression)
- läkemedel som används för att behandla smärta och artrit, som kallas icke-steroida antiinflammatoriska läkemedel (NSAID), inklusive COX-2-hämmare
- andra läkemedel för att sänka blodtrycket
Hur ska jag ta COZAAR 25mg?
- Ta COZAAR 100 mg precis som din läkare har ordinerat. Din läkare kan ändra din dos om det behövs.
- COZAAR 50 mg kan tas med eller utan mat.
- Om du missar en dos, ta den så snart du kommer ihåg det. Om det är nära din nästa dos, ta inte den missade dosen. Ta bara nästa dos vid din vanliga tid.
- Om du tar för mycket COZAAR, ring din läkare eller Giftinformationscentralen eller gå till närmaste akutmottagning direkt.
Vilka är de möjliga biverkningarna av COZAAR?
COZAAR 25 mg kan orsaka följande biverkningar som kan vara allvarliga:
- Skada eller död hos ofödda barn. Se "Vilken är den viktigaste informationen jag borde veta om COZAAR?"
- Allergisk reaktion Symtom på en allergisk reaktion är svullnad av ansikte, läppar, svalg eller tunga. Få akut medicinsk hjälp omedelbart och sluta ta COZAAR.
- Lågt blodtryck (hypotension) . Lågt blodtryck kan göra att du känner dig svimfärdig eller yr. Lägg dig ner om du känner dig svimfärdig eller yr. Ring din läkare direkt.
- För personer som redan har njurproblem kan du se en försämring av hur väl dina njurar fungerar. Ring din läkare om du får svullnad i dina fötter, vrister eller händer, eller oförklarlig viktökning.
- Höga blodnivåer av kalium
De vanligaste biverkningarna av COZAAR 50 mg hos personer med högt blodtryck är:
- "förkylningar" (infektion i övre luftvägarna)
- yrsel
- Täppt i näsan
- ryggont
De vanligaste biverkningarna av COZAAR 50 mg hos personer med typ 2-diabetes med diabetisk njursjukdom är:
- diarre
- trötthet
- lågt blodsocker
- bröstsmärta
- högt blodkalium
- lågt blodtryck
Tala om för din läkare om du får någon biverkning som stör dig eller som inte kommer att försvinna.
Detta är inte en komplett lista över biverkningar. För en fullständig lista, fråga din läkare eller apotekspersonal.
Hur förvarar jag COZAAR 100mg?
- Förvara COZAAR-tabletter vid 59°F till 86°F (15°C till 30°C).
- Förvara COZAAR i en tättsluten behållare som skyddar läkemedlet från ljus.
- Förvara COZAAR och alla läkemedel utom räckhåll för barn.
Allmän information om COZAAR
Läkemedel skrivs ibland ut för tillstånd som inte nämns i patientinformationsblad. Använd inte COZAAR för ett tillstånd som det inte har ordinerats för. Ge inte COZAAR till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Denna broschyr sammanfattar den viktigaste informationen om COZAAR. Om du vill ha mer information, prata med din läkare. Du kan fråga din farmaceut eller läkare om information om COZAAR som är skriven för vårdpersonal.
Vilka är ingredienserna i COZAAR 25mg?
Aktiva ingredienser: losartan kalium
Inaktiva Ingredienser:
mikrokristallin cellulosa, vattenhaltig laktos, förgelatinerad stärkelse, magnesiumstearat, hydroxipropylcellulosa, hypromellos och titandioxid. COZAAR 25 mg, COZAAR 50 mg och COZAAR 100 mg kan också innehålla karnaubavax.
