Catapres 100mcg Clonidine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Catapres och hur används det?
Catapres är ett receptbelagt läkemedel som används för att behandla symtom högt blodtryck, ADHD och cancersmärta. Catapres 100mcg kan användas ensamt eller tillsammans med andra läkemedel.
Catapres 100mcg tillhör en klass av läkemedel som kallas Alpha2-agonister, centralverkande, ADHD-medel.
Det är inte känt om Catapres 100mcg är säkert och effektivt för barn yngre än 12 år.
Vilka är de möjliga biverkningarna av Catapres?
Catapres kan orsaka allvarliga biverkningar inklusive:
- abstinenssymptom,
- nervositet,
- agitation,
- huvudvärk,
- tremor och
- snabb ökning av blodtrycket
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Catapres 100mcg inkluderar:
- torr mun,
- yrsel,
- dåsighet,
- Trötthet,
- förstoppning,
- huvudvärk,
- illamående, och
- sömnsvårigheter (sömnlöshet)
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Catapres. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Catapres® (klonidinhydroklorid, USP) är ett centralt verkande alfa-agonist hypotensivt medel tillgängligt som tabletter för oral administrering i tre doseringsstyrkor: 0,1 mg, 0,2 mg och 0,3 mg. 0,1 mg tabletten motsvarar 0,087 mg av den fria basen.
De inaktiva ingredienserna är kolloidal kiseldioxid, majsstärkelse, dibasiskt kalciumfosfat, FD&C Yellow No. 6, gelatin, glycerin, laktos och magnesiumstearat. Catapres 0,1 mg tablett innehåller även FD&C Blue No.1 och FD&C Red No.3.
Klonidinhydroklorid är ett imidazolinderivat och existerar som en mesomer förening. Det kemiska namnet är 2-(2,6-diklorfenylamino)-2-imidazolinhydroklorid. Följande är strukturformeln:
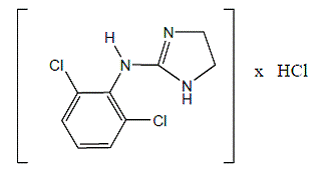 C9H9Cl2N3 · HCl Mol. Wt. 266,56
C9H9Cl2N3 · HCl Mol. Wt. 266,56 Klonidinhydroklorid är en luktfri, bitter, vit, kristallin substans som är löslig i vatten och alkohol.
INDIKATIONER
CATAPRES tabletter är indicerade för behandling av hypertoni. CATAPRES tabletter kan användas ensamma eller samtidigt med andra antihypertensiva medel.
DOSERING OCH ADMINISTRERING
Vuxna
Dosen av Catapres® (klonidinhydroklorid, USP) tabletter måste justeras efter patientens individuella blodtryckssvar. Följande är en allmän vägledning för dess administration.
Initial dos
0,1 mg tablett två gånger dagligen (morgon och läggdags). Äldre patienter kan ha nytta av en lägre initial dos.
Underhållsdos
Ytterligare ökningar på 0,1 mg per dag kan göras med veckointervall om nödvändigt tills önskat svar uppnås. Att ta den större delen av den orala dagliga dosen vid sänggåendet kan minimera övergående anpassningseffekter av muntorrhet och dåsighet. De terapeutiska doserna som oftast används har varierat från 0,2 mg till 0,6 mg per dag givet i uppdelade doser. Studier har visat att 2,4 mg är den maximala effektiva dagliga dosen, men så höga doser som detta har sällan använts.
Nedsatt njurfunktion
Patienter med nedsatt njurfunktion kan ha nytta av en lägre initial dos. Patienter bör övervakas noggrant. Eftersom endast en minimal mängd klonidin avlägsnas under rutinmässig hemodialys, finns det inget behov av att ge extra klonidin efter dialys.
HUR LEVERERAS
Catapres® (klonidinhydroklorid, USP) tabletter levereras enligt följande:
Förvara vid 25°C (77°F); utflykter tillåtna till 15°-30°C (59°-86°F) [ser USP-kontrollerad rumstemperatur ].
Fördela i tät, ljusbeständig behållare.
Distribueras av: Boehringer Ingelheim Pharmaceuticals, Inc., Ridgefield, CT 06877 USA. Tillverkad av: Boehringer Ingelheim Promeco SA de CV, Mexico City, Mexiko. Licensierad från: Boehringer Ingelheim, International GmbH, Adressera medicinska frågor till: (800) 542-6257 eller (800) 459-9906. Reviderad: maj 2012
BIEFFEKTER
De flesta biverkningarna är milda och tenderar att minska med fortsatt behandling. De vanligaste (som verkar vara dosrelaterade) är muntorrhet, som förekommer hos cirka 40 av 100 patienter; dåsighet, cirka 33 av 100; yrsel, cirka 16 av 100; förstoppning och sedering, vardera cirka 10 av 100.
Följande mindre frekventa biverkningar har också rapporterats hos patienter som fått CATAPRES 100 mikrogram tabletter, men i många fall fick patienterna samtidigt medicinering och ett orsakssamband har inte fastställts.
Kroppen som helhet: Trötthet, feber, huvudvärk, blekhet, svaghet och abstinenssyndrom. Även ett svagt positivt Coombs test och ökad känslighet för alkohol rapporterades.
Kardiovaskulär: Bradykardi, kongestiv hjärtsvikt, elektrokardiografiska abnormiteter (dvs. sinusknutestopp, junctional bradykardi, höggradig AV-blockering och arytmier), ortostatiska symtom, hjärtklappning, Raynauds fenomen, synkope och takykardi. Fall av sinusbradykardi och atrioventrikulär blockering har rapporterats, både med och utan användning av samtidig digitalis.
Centrala nervsystemet: Agitation, ångest, delirium, vanföreställningar, hallucinationer (inklusive syn och hörsel), sömnlöshet, mental depression, nervositet, andra beteendeförändringar, parestesi, rastlöshet, sömnstörningar och livliga drömmar eller mardrömmar.
Dermatologiska: Alopeci, angioneurotiskt ödem, nässelfeber, klåda, hudutslag och urtikaria.
Gastrointestinala: Buksmärtor, anorexi, förstoppning, hepatit, sjukdomskänsla, lindriga övergående avvikelser i leverfunktionstester, illamående, parotit, pseudo-obstruktion (inklusive kolon-pseudo-obstruktion), spottkörtelsmärta och kräkningar.
Genitourinära: Minskad sexuell aktivitet, svårigheter med urinering, erektil dysfunktion, förlust av libido, nocturi och urinretention.
Hematologiska: Trombocytopeni.
Metaboliskt: Gynekomasti, övergående höjning av blodsocker eller serumkreatinfosfokinas och viktökning.
Muskuloskeletala: Benkramper och muskel- eller ledvärk.
Oro-otolaryngeal: Torrhet i nässlemhinnan.
Oftalmologiska: Ackommodationsstörning, dimsyn, sveda i ögonen, minskad tårbildning och torra ögon.
LÄKEMEDELSINTERAKTIONER
Klonidin kan förstärka de CNS-depressiva effekterna av alkohol, barbiturater eller andra lugnande läkemedel. Om en patient som får klonidinhydroklorid också tar tricykliska antidepressiva medel, kan den hypotensiva effekten av klonidin minska, vilket kräver en ökning av klonidindosen. Om en patient som får klonidin också tar neuroleptika, kan ortostatiska regleringsstörningar (t.ex. ortostatisk hypotoni, yrsel, trötthet) induceras eller förvärras.
Övervaka hjärtfrekvensen hos patienter som får klonidin samtidigt med medel som är kända för att påverka sinusknutans funktion eller AV-knutöverledning, t.ex. digitalis, kalciumkanalblockerare och betablockerare. Sinusbradykardi som resulterar i sjukhusvistelse och pacemakerinsättning har rapporterats i samband med användning av klonidin samtidigt med diltiazem eller verapamil.
Amitriptylin i kombination med klonidin förstärker manifestationen av hornhinneskador hos råttor (se Toxikologi ).
Baserat på observationer hos patienter i ett tillstånd av alkoholiskt delirium har det föreslagits att höga intravenösa doser av klonidin kan öka den arytmogena potentialen (QT-förlängning, ventrikelflimmer) av höga intravenösa doser av haloperidol. Orsakssamband och relevans för klonidin orala tabletter har inte fastställts.
VARNINGAR
Uttag
Patienter bör instrueras att inte avbryta behandlingen utan att rådfråga sin läkare. Plötsligt upphörande av klonidinbehandling har i vissa fall resulterat i symtom som nervositet, agitation, huvudvärk och tremor åtföljd av eller följt av en snabb ökning av blodtrycket och förhöjda katekolaminkoncentrationer i plasma. Sannolikheten för sådana reaktioner vid utsättande av klonidinbehandling verkar vara större efter administrering av högre doser eller fortsatt behandling med betablockerare och särskild försiktighet rekommenderas därför i dessa situationer. Sällsynta fall av hypertensiv encefalopati, cerebrovaskulära olyckor och dödsfall har rapporterats efter utsättande av klonidin. När behandlingen med CATAPRES tabletter avbryts, bör läkaren minska dosen gradvis under 2 till 4 dagar för att undvika abstinenssymptom.
En överdriven ökning av blodtrycket efter avslutad behandling med CATAPRES 100 mcg tabletter kan vändas genom administrering av oral klonidinhydroklorid eller genom intravenös fentolamin. Om behandlingen ska avbrytas hos patienter som får en betablockerare och klonidin samtidigt, ska betablockeraren sättas ut flera dagar innan det gradvisa avbrytandet av CATAPRES 100 mcg tabletter.
Eftersom barn ofta har gastrointestinala sjukdomar som leder till kräkningar, kan de vara särskilt mottagliga för hypertensiva episoder till följd av plötslig oförmåga att ta medicin.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Hos patienter som har utvecklat lokal kontaktsensibilisering mot Catapres-TTS® (klonidin), kan fortsatt behandling med Catapres-TTS eller utbyte av oral klonidinhydrokloridbehandling vara associerad med utvecklingen av ett generaliserat hudutslag.
Hos patienter som utvecklar en allergisk reaktion mot Catapres-TTS kan utbyte av oral klonidinhydroklorid också framkalla en allergisk reaktion (inklusive generaliserat utslag, urtikaria eller angioödem).
Den sympatolytiska effekten av klonidin kan förvärra sinusknutedysfunktion och atrioventrikulär (AV) blockering, särskilt hos patienter som tar andra sympatolytiska läkemedel. Det finns rapporter efter marknadsföringen av patienter med överledningsstörningar och/eller som tagit andra sympatolytiska läkemedel som utvecklat svår bradykardi som kräver IV atropin, IV isoproterenol och temporär hjärtstimulering medan de tog klonidin.
Vid hypertoni orsakad av feokromocytom kan ingen terapeutisk effekt av CATAPRES 100 mcg tabletter förväntas.
Perioperativ användning
Administrering av Catapres® (klonidinhydroklorid, USP) tabletter ska fortsätta till inom 4 timmar efter operationen och återupptas så snart som möjligt därefter. Blodtrycket bör övervakas noggrant under operationen och ytterligare åtgärder för att kontrollera blodtrycket bör finnas tillgängliga vid behov.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Kronisk kostadministrering av klonidin var inte cancerframkallande för råttor (132 veckor) eller möss (78 veckor) respektive doserade med upp till 46 eller 70 gånger den maximala rekommenderade dagliga dosen för människor som mg/kg (9 eller 6 gånger MRDHD på en mg/m²). Det fanns inga tecken på genotoxicitet i Ames-testet för mutagenicitet eller mus-mikronkärntestet för klastogenicitet.
Fertiliteten hos han- eller honråttor påverkades inte av klonidindoser så höga som 150 μg/kg (ungefär 3 gånger MRDHD). I ett separat experiment verkade fertiliteten hos honråttor påverkas vid dosnivåer på 500 till 2000 μg/kg (10 till 40 gånger den orala MRDHD på en mg/kg-basis; 2 till 8 gånger MRDHD på en mg/m²-basis ).
Graviditet
Teratogena effekter
Graviditetskategori C
Reproduktionsstudier utförda på kaniner vid doser upp till cirka 3 gånger den orala maximala rekommenderade dagliga humandosen (MRDHD) av Catapres® (klonidinhydroklorid, USP) tabletter gav inga tecken på en teratogen eller embryotoxisk potential hos kaniner. Hos råttor var dock doser så låga som 1/3 av den orala MRDHD (1/15 MRDHD på mg/m²-basis) av klonidin associerade med ökade resorptioner i en studie där mödrarna behandlades kontinuerligt från 2 månader före parning . Ökade resorptioner var inte associerade med behandling samtidigt eller vid högre dosnivåer (upp till 3 gånger den orala MRDHD) när moderdjuren behandlades på dräktighetsdagarna 6 till 15. Ökning av resorption observerades vid mycket högre dosnivåer (40 gånger oral MRDHD på mg/kg-basis, 4 till 8 gånger MRDHD på mg/m²-basis) hos möss och råttor som behandlades på dräktighetsdag 1 till 14 (lägsta dos som användes i studien var 500 μg/kg).
Inga adekvata, välkontrollerade studier har utförts på gravida kvinnor. Klonidin passerar placentabarriären (se KLINISK FARMAKOLOGI , Farmakokinetik ). Eftersom reproduktionsstudier på djur inte alltid förutsäger mänskligt svar, bör detta läkemedel endast användas under graviditet om det verkligen behövs.
Ammande mödrar
Eftersom klonidinhydroklorid utsöndras i bröstmjölk, bör försiktighet iakttas när CATAPRES 100 mikrogram tabletter administreras till en ammande kvinna.
Pediatrisk användning
Säkerhet och effektivitet hos pediatriska patienter har inte fastställts i adekvata och välkontrollerade studier (se VARNINGAR , Uttag ).
ÖVERDOS
Hypertoni kan utvecklas tidigt och kan följas av hypotoni, bradykardi, andningsdepression, hypotermi, dåsighet, minskade eller frånvarande reflexer, svaghet, irritabilitet och mios. Frekvensen av CNS-depression kan vara högre hos barn än hos vuxna. Stora överdoser kan resultera i reversibla hjärtledningsdefekter eller dysrytmier, apné, koma och kramper. Tecken och symtom på överdosering uppträder vanligtvis inom 30 minuter till två timmar efter exponering. Så lite som 0,1 mg klonidin har gett tecken på toxicitet hos barn.
Det finns ingen specifik motgift mot överdosering av klonidin. Överdosering av klonidin kan resultera i en snabb utveckling av CNS-depression; därför rekommenderas inte framkallande av kräkningar med ipecac sirap. Magsköljning kan vara indicerat efter nyligen genomförda och/eller stora intag. Administrering av aktivt kol och/eller ett renande medel kan vara fördelaktigt. Understödjande vård kan inkludera atropinsulfat för bradykardi, intravenösa vätskor och/eller vasopressorer för hypotoni och vasodilatorer för hypertoni. Naloxon kan vara ett användbart komplement för hanteringen av klonidininducerad andningsdepression, hypotoni och/eller koma; blodtrycket bör övervakas eftersom administrering av naloxon ibland har resulterat i paradoxal hypertoni. Dialys kommer sannolikt inte att signifikant öka elimineringen av klonidin.
Den största överdosen som hittills rapporterats involverade en 28-årig man som fick i sig 100 mg klonidinhydrokloridpulver. Denna patient utvecklade hypertoni följt av hypotoni, bradykardi, apné, hallucinationer, semikom och prematura ventrikulära sammandragningar. Patienten återhämtade sig helt efter intensiv behandling. Klonidinnivåerna i plasma var 60 ng/ml efter 1 timme, 190 ng/ml efter 1,5 timmar, 370 ng/ml efter 2 timmar och 120 ng/ml efter 5,5 och 6,5 timmar. Hos möss och råttor är den orala LD50 för klonidin 206 respektive 465 mg/kg.
KONTRAINDIKATIONER
Catapres® (klonidinhydroklorid, USP) tabletter ska inte användas till patienter med känd överkänslighet mot klonidin (se FÖRSIKTIGHETSÅTGÄRDER ).
KLINISK FARMAKOLOGI
Klonidin stimulerar alfa-adrenoreceptorer i hjärnstammen. Denna verkan resulterar i minskat sympatiskt utflöde från det centrala nervsystemet och i minskningar av perifert motstånd, njurvaskulärt motstånd, hjärtfrekvens och blodtryck. CATAPRES 100mcg tabletter verkar relativt snabbt. Patientens blodtryck sjunker inom 30 till 60 minuter efter en oral dos, den maximala minskningen sker inom 2 till 4 timmar. Renalt blodflöde och glomerulär filtrationshastighet förblir i huvudsak oförändrade. Normala posturala reflexer är intakta; därför är ortostatiska symtom milda och sällsynta.
Akuta studier med klonidinhydroklorid på människor har visat en måttlig minskning (15 % till 20 %) av hjärtminutvolymen i ryggläge utan förändring av det perifera motståndet: vid en 45° lutning finns en mindre minskning av hjärtminutvolymen och en minskning av perifert motstånd. Under långtidsbehandling tenderar hjärtminutvolymen att återgå till kontrollvärden, medan det perifera motståndet förblir minskat. En långsammare pulsfrekvens har observerats hos de flesta patienter som fått klonidin, men läkemedlet förändrar inte det normala hemodynamiska svaret på träning.
Tolerans mot den antihypertensiva effekten kan utvecklas hos vissa patienter, vilket kräver en omvärdering av behandlingen.
Andra studier på patienter har visat på en minskning av plasmareninaktiviteten och i utsöndringen av aldosteron och katekolaminer. Det exakta sambandet mellan dessa farmakologiska effekter och den antihypertensiva effekten av klonidin har inte klarlagts helt.
Klonidin stimulerar akut frisättning av tillväxthormon hos både barn och vuxna, men ger inte en kronisk ökning av tillväxthormon vid långvarig användning.
Farmakokinetik
Farmakokinetiken för klonidin är dosproportionell i intervallet 100 till 600 μg. Den absoluta biotillgängligheten för klonidin vid oral administrering är 70 % till 80 %. Toppnivåer av klonidin i plasma uppnås inom cirka 1 till 3 timmar.
Efter intravenös administrering uppvisar klonidin bifasisk disposition med en distributionshalveringstid på cirka 20 minuter och en eliminationshalveringstid på 12 till 16 timmar. Halveringstiden ökar upp till 41 timmar hos patienter med gravt nedsatt njurfunktion. Klonidin passerar placentabarriären. Det har visat sig passera blod-hjärnbarriären hos råttor.
Efter oral administrering återfinns cirka 40 % till 60 % av den absorberade dosen i urinen som oförändrat läkemedel inom 24 timmar. Cirka 50 % av den absorberade dosen metaboliseras i levern. Varken mat eller patientens ras påverkar klonidins farmakokinetik.
Den antihypertensiva effekten uppnås vid plasmakoncentrationer mellan cirka 0,2 och 2,0 ng/ml hos patienter med normal utsöndringsfunktion. En ytterligare ökning av plasmanivåerna kommer inte att förstärka den antihypertensiva effekten.
Toxikologi
I flera studier med oral klonidinhydroklorid sågs en dosberoende ökning av incidensen och svårighetsgraden av spontan retinal degeneration hos albinoråttor som behandlats i sex månader eller längre. Studier av vävnadsfördelning på hundar och apor visade en koncentration av klonidin i åderhinnan.
Med tanke på den retinala degeneration som ses hos råttor, utfördes ögonundersökningar under kliniska prövningar på 908 patienter före och periodvis efter starten av klonidinbehandling. Hos 353 av dessa 908 patienter utfördes ögonundersökningarna under perioder på 24 månader eller längre. Förutom viss torrhet i ögonen registrerades inga läkemedelsrelaterade onormala oftalmologiska fynd och enligt specialiserade tester som elektroretinografi och makularbländning var näthinnans funktion oförändrad.
I kombination med amitriptylin ledde administrering av klonidinhydroklorid till utveckling av hornhinneskador hos råttor inom 5 dagar.
PATIENTINFORMATION
Patienter bör varnas för att avbryta behandlingen med CATAPRES 100 mcg tabletter utan läkares råd.
Eftersom patienter kan uppleva en möjlig lugnande effekt, yrsel eller ackommodationsstörning vid användning av klonidin, varna patienterna för att delta i aktiviteter som att köra fordon eller använda apparater eller maskiner. Informera också patienterna om att denna lugnande effekt kan öka vid samtidig användning av alkohol, barbiturater eller andra lugnande läkemedel.
Patienter som använder kontaktlinser bör varnas för att behandling med CATAPRES tabletter kan orsaka torra ögon.
