Coreg 3.12mg, 6.25mg, 12.5mg, 25mg Carvedilol Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Coreg 25mg och hur används det?
Coreg är ett receptbelagt läkemedel som används för att behandla symtom på hjärtsvikt och högt blodtryck (hypertoni). Coreg 25mg kan användas ensamt eller tillsammans med andra läkemedel.
Coreg tillhör en klass av läkemedel som kallas Beta-blockerare, Alpha Activity.
Det är inte känt om Coreg 25mg är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Coreg?
Coreg kan orsaka allvarliga biverkningar inklusive:
- yrsel,
- långsamma eller ojämna hjärtslag,
- kall känsla eller domningar i fingrar eller tår,
- bröstsmärta,
- rethosta,
- väsande andning,
- tryck över bröstet,
- svullnad,
- snabb viktökning,
- känner andfåddhet,
- ökad törst,
- ökad urinering,
- muntorrhet och
- fruktig andedräkt lukt
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Coreg 6,25 mg inkluderar:
- yrsel,
- långsamma hjärtslag,
- diarre,
- viktökning,
- torra ögon och
- svårigheter att använda kontaktlinser
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Coreg. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Karvedilol är ett icke-selektivt β-adrenergt blockerande medel med α1-blockerande aktivitet. Det är (±)-1(karbazol-4-yloxi)-3-[[2-(o-metoxifenoxi)etyl]amino]-2-propanol. Karvedilol är en racemisk blandning med följande struktur:
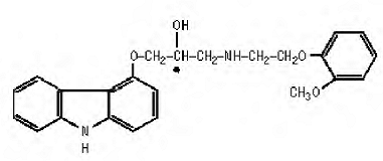
COREG 6,25 mg är en vit, oval, filmdragerad tablett som innehåller 3,125 mg, 6,25 mg, 12,5 mg eller 25 mg karvedilol. Tabletterna 6,25 mg, 12,5 mg och 25 mg är TILTAB-tabletter. Inaktiva ingredienser består av kolloidal kiseldioxid, krospovidon, hypromellos, laktos, magnesiumstearat, polyetylenglykol, polysorbat 80, povidon, sackaros och titandioxid.
Carvedilol är ett vitt till benvitt pulver med en molekylvikt på 406,5 och en molekylformel på C24H26N2O4. Det är fritt lösligt i dimetylsulfoxid; löslig i metylenklorid och metanol; svårlöslig i 95 % etanol och isopropanol; lätt löslig i etyleter; och praktiskt taget olöslig i vatten, magvätska (simulerad, TS, pH 1,1) och tarmvätska (simulerad, TS utan pankreatin, pH 7,5).
INDIKATIONER
Hjärtsvikt
COREG är indicerat för behandling av mild till svår kronisk hjärtsvikt av ischemisk eller kardiomyopatisk ursprung, vanligtvis förutom diuretika, ACE-hämmare och digitalis, för att öka överlevnaden och även för att minska risken för sjukhusvistelse [se LÄKEMEDELSINTERAKTIONER , Kliniska studier ].
Vänsterkammardysfunktion efter hjärtinfarkt
COREG är indicerat för att minska kardiovaskulär mortalitet hos kliniskt stabila patienter som har överlevt den akuta fasen av en hjärtinfarkt och som har en vänsterkammars ejektionsfraktion på mindre än eller lika med 40 % (med eller utan symtomatisk hjärtsvikt) [se Kliniska studier ].
Hypertoni
COREG 25 mg är indicerat för behandling av essentiell hypertoni [se Kliniska studier ]. Det kan användas ensamt eller i kombination med andra antihypertensiva medel, särskilt diuretika av tiazidtyp [se LÄKEMEDELSINTERAKTIONER ].
DOSERING OCH ADMINISTRERING
COREG ska tas med mat för att bromsa absorptionshastigheten och minska förekomsten av ortostatiska effekter.
Hjärtsvikt
DOSERING MÅSTE VARA INDIVIDUALISERAD OCH NOGA ÖVERVAKAS AV EN LÄKARE UNDER UPPTITRERING. Innan initiering av COREG 12,5 mg rekommenderas att vätskeretentionen minimeras. Den rekommenderade startdosen av COREG är 3,125 mg två gånger dagligen i 2 veckor. Om patienten tolereras kan dosen ökas till 6,25, 12,5 och 25 mg två gånger dagligen under på varandra följande intervall på minst 2 veckor. Patienter bör hållas på lägre doser om högre doser inte tolereras. En maximal dos på 50 mg två gånger dagligen har administrerats till patienter med mild till måttlig hjärtsvikt som väger över 85 kg (187 lbs).
Patienter bör informeras om att inledande av behandling och (i mindre utsträckning) dosökningar kan vara associerade med övergående symtom på yrsel eller yrsel (och sällan synkope) inom den första timmen efter dosering. Under dessa perioder bör patienter undvika situationer som bilkörning eller farliga uppgifter, där symtom kan leda till skada. Kärlvidgande symtom kräver ofta ingen behandling, men det kan vara användbart att separera tiden för dosering av COREG 6,25 mg från den för ACE-hämmaren eller att tillfälligt minska dosen av ACE-hämmaren. Dosen av COREG 12,5 mg ska inte ökas förrän symtom på förvärrad hjärtsvikt eller vasodilatation har stabiliserats.
Vätskeretention (med eller utan övergående förvärrade symtom på hjärtsvikt) bör behandlas med en ökning av dosen av diuretika.
Dosen av COREG bör minskas om patienter upplever bradykardi (puls mindre än 55 slag per minut).
Episoder av yrsel eller vätskeretention under påbörjande av COREG 3,12 mg kan i allmänhet hanteras utan att behandlingen avbryts och utesluter inte efterföljande framgångsrik titrering av eller ett gynnsamt svar på karvedilol.
Vänsterkammardysfunktion efter hjärtinfarkt
DOSERING MÅSTE INDIVIDUALISERAS OCH ÖVERVAKAS UNDER UPPTITRERING. Behandling med COREG kan påbörjas som slutenvård eller öppenvård och bör påbörjas efter att patienten är hemodynamiskt stabil och vätskeretention har minimerats. Det rekommenderas att COREG 3,12 mg startas med 6,25 mg två gånger dagligen och ökas efter 3 till 10 dagar, baserat på tolerans, till 12,5 mg två gånger dagligen, sedan igen till måldosen på 25 mg två gånger dagligen. En lägre startdos kan användas (3,125 mg två gånger dagligen) och/eller upptitreringshastigheten kan bromsas om det är kliniskt indicerat (t.ex. på grund av lågt blodtryck eller puls, eller vätskeretention). Patienter bör hållas på lägre doser om högre doser inte tolereras. Den rekommenderade doseringsregimen behöver inte ändras hos patienter som fick behandling med en IV eller oral β-blockerare under den akuta fasen av hjärtinfarkten.
Hypertoni
DOSERING MÅSTE INDIVIDUALISERAS. Den rekommenderade startdosen av COREG 6,25 mg är 6,25 mg två gånger dagligen. Om denna dos tolereras, med stående systoliskt tryck mätt cirka 1 timme efter dosering som vägledning, bör dosen bibehållas i 7 till 14 dagar och sedan ökas till 12,5 mg två gånger dagligen vid behov, baserat på dalblodtryck, igen med stående systoliskt tryck 1 timme efter dosering som vägledning för tolerans. Denna dos bör också bibehållas i 7 till 14 dagar och kan sedan justeras upp till 25 mg två gånger dagligen om det tolereras och behövs. Den fullständiga antihypertensiva effekten av COREG 6,25 mg ses inom 7 till 14 dagar. Den totala dagliga dosen bör inte överstiga 50 mg.
Samtidig administrering med ett diuretikum kan förväntas ge additiva effekter och överdriva den ortostatiska komponenten av karvedilols verkan.
Nedsatt leverfunktion
COREG 25 mg ska inte ges till patienter med gravt nedsatt leverfunktion [se KONTRAINDIKATIONER ].
HUR LEVERERAS
Dosering och styrkor
De vita, ovala, filmdragerade tabletterna finns i följande styrkor:
- 3,125 mg – graverad med "39" och "SB"
- 6,25 mg – graverad med "4140" och "SB"
- 12,5 mg – graverad med "4141" och "SB"
- 25 mg – graverad med "4142" och "SB"
Förvaring Och Hantering
De vita, ovala, filmdragerade tabletterna finns i följande styrkor:
- 3,125 mg – graverad med "39" och "SB"
- 6,25 mg – graverad med "4140" och "SB"
- 12,5 mg – graverad med "4141" och "SB"
- 25 mg – graverad med "4142" och "SB"
Tabletterna 6,25 mg, 12,5 mg och 25 mg är TILTAB-tabletter.
- 3,125 mg flaskor med 100: NDC 0007-4139-20
- 6,25 mg flaskor med 100: NDC 0007-4140-20
- 12,5 mg flaskor med 100: NDC 0007-4141-20
- 25 mg flaskor à 100: NDC 0007-4142-20
Förvaras under 30°C (86°F). Skydda mot fukt. Dispensera i en tät, ljusbeständig behållare.
Tillverkad för: GlaxoSmithKline Research Triangle Park, NC 27709. Reviderad: sep 2017.
BIEFFEKTER
Erfarenhet av kliniska studier
Eftersom kliniska prövningar utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i kliniska prövningar av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i praktiken.
COREG 25 mg har utvärderats för säkerhet hos patienter med hjärtsvikt (lindrig, måttlig och svår), hos patienter med vänsterkammardysfunktion efter hjärtinfarkt och hos patienter med hypertoni. Den observerade biverkningsprofilen överensstämde med läkemedlets farmakologi och hälsotillståndet för försökspersonerna i de kliniska prövningarna. Biverkningar som rapporterats för var och en av dessa patientpopulationer ges nedan. Undantagna är biverkningar som anses vara för generella för att vara informativa, och sådana som inte rimligen är förknippade med användningen av läkemedlet eftersom de var förknippade med det tillstånd som behandlas eller är mycket vanliga i den behandlade befolkningen. Frekvensen av biverkningar var i allmänhet likartade över demografiska undergrupper (män och kvinnor, äldre och icke-äldre, svarta och icke-svarta).
Hjärtsvikt
COREG 12,5 mg har utvärderats för säkerhet vid hjärtsvikt hos mer än 4 500 försökspersoner över hela världen, av vilka mer än 2 100 deltog i placebokontrollerade kliniska prövningar. Ungefär 60 % av den totala behandlade populationen i placebokontrollerade kliniska prövningar fick COREG 3,12 mg i minst 6 månader och 30 % fick COREG i minst 12 månader. I COMET-studien behandlades 1 511 försökspersoner med mild till måttlig hjärtsvikt med COREG i upp till 5,9 år (medelvärde: 4,8 år). Både i amerikanska kliniska prövningar av mild till måttlig hjärtsvikt som jämförde COREG 3,12 mg i dagliga doser upp till 100 mg (n = 765) med placebo (n = 437), och i en multinationell klinisk prövning av allvarlig hjärtsvikt (COPERNICUS ) som jämförde COREG i dagliga doser upp till 50 mg (n = 1 156) med placebo (n = 1 133), var avbrottsfrekvensen för biverkningar liknande hos patienter med karvedilol och placebo. I placebokontrollerade kliniska prövningar var den enda orsaken till att behandlingen avbröts mer än 1 % och som förekom oftare med karvedilol yrsel (1,3 % på karvedilol, 0,6 % på placebo i COPERNICUS-studien).
Tabell 1 visar biverkningar som rapporterats hos försökspersoner med mild till måttlig hjärtsvikt inkluderade i placebokontrollerade kliniska prövningar i USA och med allvarlig hjärtsvikt inkluderade i COPERNICUS-studien. Biverkningar som förekom oftare hos läkemedelsbehandlade patienter än placebobehandlade med en incidens på mer än 3 % hos patienter som behandlats med karvedilol, oavsett orsakssamband, visas. Medianexponeringen för läkemedelsexponering var 6,3 månader för både karvedilol- och placebopersoner i försöken med mild till måttlig hjärtsvikt och 10,4 månader i försöket med patienter med svår hjärtsvikt. Biverkningsprofilen för COREG 3,12 mg som observerades i långtidsstudien med COMET liknade i allmänhet den som observerades i de amerikanska hjärtsviktstudierna.
Hjärtsvikt och dyspné rapporterades också i dessa studier, men frekvensen var lika eller högre hos försökspersoner som fick placebo.
Följande biverkningar rapporterades med en frekvens på mer än 1 % men mindre än eller lika med 3 % och mer frekvent med COREG 3,12 mg i antingen de amerikanska placebokontrollerade studierna på försökspersoner med mild till måttlig hjärtsvikt eller hos försökspersoner med allvarlig hjärtsvikt i COPERNICUS-försöket.
Incidens större än 1 % till mindre än eller lika med 3 %
Kroppen som helhet: Allergi, sjukdomskänsla, hypovolemi, feber, benödem.
Kardiovaskulär: Vätskeöverbelastning, postural hypotoni, förvärrad angina pectoris, AV-block, hjärtklappning, hypertoni.
Centrala och perifera nervsystemet: Hypestesi, svindel, parestesi.
Gastrointestinala: Melena, parodontit.
Lever och gallvägar: SGPT ökade, SGOT ökade.
Metaboliskt och näringsmässigt: Hyperurikemi, hypoglykemi, hyponatremi, ökat alkaliskt fosfatas, glykosuri, hypervolemi, diabetes mellitus, ökad GGT, viktminskning, hyperkalemi, ökad kreatinin.
Muskuloskeletala: Muskelkramp.
Trombocyter, blödningar och koagulering: Protrombin minskat, purpura, trombocytopeni.
Psykiatrisk: Sömnighet.
Reproduktiv, manlig: Impotens.
Särskilda sinnen: Suddig syn.
Urinvägarna: Njurinsufficiens, albuminuri, hematuri.
Vänsterkammardysfunktion efter hjärtinfarkt
COREG har utvärderats för säkerhet hos överlevande av en akut hjärtinfarkt med vänsterkammardysfunktion i CAPRICORN-studien som involverade 969 försökspersoner som fick COREG 6,25 mg och 980 som fick placebo. Ungefär 75 % av försökspersonerna fick COREG 25 mg i minst 6 månader och 53 % fick COREG 12,5 mg i minst 12 månader. Försökspersonerna behandlades i genomsnitt 12,9 månader och 12,8 månader med COREG 12,5 mg respektive placebo.
De vanligaste biverkningarna som rapporterades med COREG 25 mg i CAPRICORN-studien överensstämde med läkemedlets profil i de amerikanska hjärtsviktsprövningarna och COPERNICUS-studien. De enda ytterligare biverkningar som rapporterades i STENBOCK hos mer än 3 % av försökspersonerna och vanligare på karvedilol var dyspné, anemi och lungödem. Följande biverkningar rapporterades med en frekvens på mer än 1 % men mindre än eller lika med 3 % och mer frekvent med COREG: influensasyndrom, cerebrovaskulär olycka, perifer vaskulär störning, hypotoni, depression, gastrointestinala smärtor, artrit och gikt. Den totala frekvensen av avbrott på grund av biverkningar var likartad i båda grupperna av försökspersoner. I denna databas var den enda orsaken till att behandlingen avbröts mer än 1 % och som förekom oftare med karvedilol hypotoni (1,5 % på karvedilol, 0,2 % på placebo).
Hypertoni
COREG har utvärderats för säkerhet vid högt blodtryck hos mer än 2 193 försökspersoner i amerikanska kliniska prövningar och i 2 976 försökspersoner i internationella kliniska prövningar. Ungefär 36 % av den totala behandlade populationen fick COREG i minst 6 månader. De flesta biverkningar som rapporterades under behandling med COREG 25 mg var av mild till måttlig svårighetsgrad. I USA-kontrollerade kliniska prövningar som direkt jämförde COREG 12,5 mg i doser upp till 50 mg (n = 1 142) med placebo (n = 462), avbröt 4,9 % av patienterna som fick COREG 6,25 mg på grund av biverkningar jämfört med 5,2 % av patienterna med placebo. Även om det inte fanns någon övergripande skillnad i utsättningsfrekvens, var utsättningar vanligare i karvedilolgruppen för postural hypotoni (1 % mot 0). Den totala förekomsten av biverkningar i placebokontrollerade prövningar i USA ökade med ökande dos av COREG. För enskilda biverkningar kunde detta endast särskiljas för yrsel, som ökade i frekvens från 2 % till 5 % när den totala dagliga dosen ökade från 6,25 mg till 50 mg.
Tabell 2 visar biverkningar i amerikanska placebokontrollerade kliniska prövningar för hypertoni som inträffade med en incidens på mer än eller lika med 1 % oavsett orsakssamband och som var vanligare hos läkemedelsbehandlade försökspersoner än placebobehandlade försökspersoner.
Dyspné och trötthet rapporterades också i dessa studier, men frekvensen var lika eller högre hos försökspersoner som fick placebo.
Följande biverkningar som inte beskrivits ovan har rapporterats som möjligen eller troligen relaterade till COREG 25 mg i öppna eller kontrollerade världsomspännande studier med COREG 12,5 mg hos patienter med hypertoni eller hjärtsvikt.
Incidens större än 0,1 % till mindre än eller lika med 1 %
Kardiovaskulär: Perifer ischemi, takykardi.
Centrala och perifera nervsystemet m: Hypokinesi.
Gastrointestinala: Bilirubinemi, ökade leverenzymer (0,2 % av patienterna med hypertoni och 0,4 % av patienterna med hjärtsvikt avbröts från behandlingen på grund av ökningar av leverenzymer) [se Erfarenhet efter marknadsföring ].
Psykiatrisk: Nervositet, sömnstörning, förvärrad depression, nedsatt koncentrationsförmåga, onormalt tänkande, paroniria, emotionell labilitet.
Andningssystem: Astma [se KONTRAINDIKATIONER ].
Reproduktiv, manlig: Minskad libido.
Hud och bihang: Klåda, erytematösa utslag, makulopapulära utslag, psoriaform utslag, ljuskänslighetsreaktion.
Särskilda sinnen: Tinnitus.
Urinvägarna: Miktionsfrekvensen ökade.
Autonoma nervsystemet: Muntorrhet, ökad svettning.
Metaboliskt och näringsmässigt: Hypokalemi, hypertriglyceridemi.
Hematologiska: Anemi, leukopeni.
Följande händelser rapporterades hos mindre än eller lika med 0,1 % av försökspersonerna och är potentiellt viktiga: fullständigt AV-block, grenblock, myokardischemi, cerebrovaskulär störning, kramper, migrän, neuralgi, pares, anafylaktoid reaktion, alopeci, exfoliativ dermatit, amnesi, GI-blödning, bronkospasm, lungödem, nedsatt hörsel, respiratorisk alkalos, ökad BUN, minskad HDL, pancytopeni och atypiska lymfocyter.
Laboratorieavvikelser
Reversibla förhöjningar av serumtransaminaser (ALAT eller ASAT) har observerats under behandling med COREG. Frekvensen av transaminashöjningar (2 till 3 gånger den övre normalgränsen) som observerats under kontrollerade kliniska prövningar har i allmänhet varit likartade mellan patienter som behandlats med COREG och de som behandlats med placebo. Emellertid har transaminashöjningar, bekräftade genom återprovokation, observerats med COREG. I en långvarig, placebokontrollerad studie av allvarlig hjärtsvikt, hade försökspersoner som behandlats med COREG 25 mg lägre värden för levertransaminaser än försökspersoner som behandlats med placebo, möjligen på grund av att förbättringar i hjärtfunktionen inducerad av COREG 6,25 mg ledde till mindre leverstockning och/ eller förbättrat blodflöde i levern.
COREG 25mg har inte associerats med kliniskt signifikanta förändringar i serumkalium, totala triglycerider, totalkolesterol, HDL-kolesterol, urinsyra, ureakväve i blodet eller kreatinin. Inga kliniskt relevanta förändringar noterades i fastande serumglukos hos hypertonipatienter; Fastande serumglukos utvärderades inte i de kliniska prövningarna för hjärtsvikt.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av COREG efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Blod- och lymfsystemet
Aplastisk anemi.
Immunsystemets störningar
Överkänslighet (t.ex. anafylaktiska reaktioner, angioödem, urtikaria).
Njur- och urinvägsstörningar
Urininkontinens.
Andnings-, bröst- och mediastinumsjukdomar
Interstitiell pneumonit.
Hud och subkutan vävnad
Stevens-Johnsons syndrom, toxisk epidermal nekrolys, erythema multiforme.
LÄKEMEDELSINTERAKTIONER
CYP2D6-hämmare och dåliga metaboliserare
Interaktioner mellan karvedilol och potenta hämmare av CYP2D6 isoenzym (såsom kinidin, fluoxetin, paroxetin och propafenon) har inte studerats, men dessa läkemedel skulle förväntas öka blodnivåerna av R(+)-enantiomeren av karvedilol [se KLINISK FARMAKOLOGI ]. Retrospektiv analys av biverkningar i kliniska prövningar visade att dåliga 2D6-metaboliserare hade en högre grad av yrsel under upptitrering, förmodligen ett resultat av vasodilaterande effekter av de högre koncentrationerna av den α-blockerande R(+)-enantiomeren.
Hypotensiva medel
Patienter som tar en β-blockerare och ett läkemedel som kan tömma katekolaminer (t.ex. reserpin och monoaminoxidashämmare) bör observeras noggrant för tecken på hypotoni och/eller svår bradykardi.
Samtidig administrering av klonidin och en β-blockerare kan orsaka hypotoni och bradykardi. När samtidig behandling med en β-blockerare och klonidin ska avslutas, ska β-blockeraren avbrytas först. Klonidinbehandling kan sedan avbrytas flera dagar senare genom att gradvis minska dosen.
Cyklosporin
Måttliga ökningar i genomsnittliga dalkoncentrationer av ciklosporin observerades efter påbörjad karvedilolbehandling hos 21 njurtransplanterade patienter som led av kronisk vaskulär avstötning. Hos cirka 30 % av försökspersonerna behövde dosen av ciklosporin minskas för att bibehålla ciklosporinkoncentrationerna inom det terapeutiska intervallet, medan i resten ingen justering behövdes. I genomsnitt för gruppen reducerades dosen av ciklosporin med cirka 20 % hos dessa försökspersoner. På grund av stor interindividuell variation i den dosjustering som krävs, rekommenderas att ciklosporinkoncentrationerna övervakas noggrant efter påbörjad karvedilolbehandling och att dosen av ciklosporin justeras på lämpligt sätt.
Digitalis glykosider
Både digitalisglykosider och β-blockerare bromsar atrioventrikulär ledning och minskar hjärtfrekvensen. Samtidig användning kan öka risken för bradykardi. Digoxinkoncentrationerna ökar med cirka 15 % när digoxin och karvedilol administreras samtidigt. Därför rekommenderas ökad övervakning av digoxin vid start, justering eller avbrytande av COREG [se KLINISK FARMAKOLOGI ].
Inducerare/hämmare av levermetabolism
Rifampin reducerade plasmakoncentrationerna av karvedilol med cirka 70 % [se KLINISK FARMAKOLOGI ]. Cimetidin ökade AUC med cirka 30 % men orsakade ingen förändring i Cmax [se KLINISK FARMAKOLOGI ].
Amiodaron
Amiodaron och dess metabolit desetylamiodaron, hämmare av CYP2C9 och P-glykoprotein ökade koncentrationerna av S(-)-enantiomeren av karvedilol med minst 2 gånger [se KLINISK FARMAKOLOGI ]. Samtidig administrering av amiodaron eller andra CYP2C9-hämmare såsom flukonazol och COREG kan förstärka den β-blockerande aktiviteten, vilket resulterar i ytterligare sänkning av hjärtfrekvensen eller hjärtöverledningen. Patienter bör observeras för tecken på bradykardi eller hjärtblockad, särskilt när det ena medlet läggs till redan existerande behandling med det andra.
Kalciumkanalblockerare
Ledningsstörning (sällan med hemodynamisk kompromiss) har observerats när COREG 25 mg administreras samtidigt med diltiazem. Som med andra β-blockerare, om COREG 25 mg administreras med kalciumkanalblockerare av verapamil- eller diltiazem-typ, rekommenderas att EKG och blodtryck övervakas.
Insulin eller orala hypoglykemikalier
β-blockerare kan förstärka den blodsockerreducerande effekten av insulin och orala hypoglykemikalier. Därför rekommenderas regelbunden kontroll av blodsocker hos patienter som tar insulin eller orala hypoglykemikalier [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Anestesi
Om behandlingen med COREG ska fortsätta perioperativt, bör särskild försiktighet iakttas när anestesimedel som hämmar myokardfunktionen, såsom eter, cyklopropan och trikloretylen, används [se ÖVERDOS ].
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Avbrytande av terapi
Patienter med kranskärlssjukdom, som behandlas med COREG, bör avrådas från abrupt avbrytande av behandlingen. Allvarlig exacerbation av angina och förekomsten av hjärtinfarkt och ventrikulära arytmier har rapporterats hos patienter med angina efter ett abrupt avbrott av behandling med β-blockerare. De sista 2 komplikationerna kan uppstå med eller utan föregående exacerbation av angina pectoris. Liksom med andra β-blockerare, när avbrytande av COREG är planerad, bör patienterna observeras noggrant och rådas att begränsa fysisk aktivitet till ett minimum. COREG bör avbrytas under 1 till 2 veckor när så är möjligt. Om kärlkrampen förvärras eller om akut kranskärlssvikt utvecklas, rekommenderas att COREG omedelbart återupptas, åtminstone tillfälligt. Eftersom kranskärlssjukdom är vanlig och kanske inte upptäcks, kan det vara klokt att inte avbryta behandlingen med COREG 3,12 mg abrupt även hos patienter som endast behandlas för högt blodtryck eller hjärtsvikt.
Bradykardi
kliniska prövningar orsakade COREG 25 mg bradykardi hos cirka 2 % av patienterna med hypertoni, 9 % av patienterna med hjärtsvikt och 6,5 % av patienterna med hjärtinfarkt och vänsterkammardysfunktion. Om pulsen sjunker under 55 slag per minut, bör dosen minskas.
Hypotoni
kliniska prövningar av primärt mild till måttlig hjärtsvikt förekom hypotoni och postural hypotoni hos 9,7 % och synkope hos 3,4 % av patienterna som fick COREG jämfört med 3,6 % respektive 2,5 % av placebopatienterna. Risken för dessa händelser var högst under de första 30 dagarna av doseringen, motsvarande upptitreringsperioden och var en orsak till att behandlingen avbröts hos 0,7 % av patienterna som fick COREG 12,5 mg, jämfört med 0,4 % av placebopatienterna. I en långtidsstudie med placebokontrollerad svår hjärtsvikt (COPERNICUS) förekom hypotoni och postural hypotoni hos 15,1 % och synkope hos 2,9 % av patienterna med hjärtsvikt som fick COREG jämfört med 8,7 % respektive 2,3 % av placebopatienterna. Dessa händelser var en orsak till att behandlingen avbröts hos 1,1 % av patienterna som fick COREG, jämfört med 0,8 % av patienterna med placebo.
Postural hypotoni förekom hos 1,8 % och synkope hos 0,1 % av hypertonipatienterna, främst efter den initiala dosen eller vid tidpunkten för dosökningen och var en orsak till att behandlingen avbröts hos 1 % av försökspersonerna.
I CAPRICORN-studien med överlevande av en akut hjärtinfarkt inträffade hypotoni eller postural hypotoni hos 20,2 % av patienterna som fick COREG jämfört med 12,6 % av placebopatienterna. Synkope rapporterades hos 3,9 % respektive 1,9 % av försökspersonerna. Dessa händelser var en orsak till att behandlingen avbröts hos 2,5 % av patienterna som fick COREG, jämfört med 0,2 % av patienterna med placebo.
Att börja med en låg dos, administrering med mat och gradvis upptitrering bör minska sannolikheten för synkope eller överdriven hypotoni [se DOSERING OCH ADMINISTRERING ]. När behandlingen påbörjas ska patienten varnas för att undvika situationer som bilkörning eller farliga uppgifter, där skada kan uppstå om synkope skulle uppstå.
Hjärtsvikt/vätskeretention
Förvärrad hjärtsvikt eller vätskeretention kan inträffa under upptitrering av karvedilol. Om sådana symtom uppstår, bör diuretika ökas och karvediloldosen bör inte ökas förrän den kliniska stabiliteten återupptas [se DOSERING OCH ADMINISTRERING ]. Ibland är det nödvändigt att sänka karvediloldosen eller tillfälligt avbryta den. Sådana episoder utesluter inte efterföljande framgångsrik titrering av, eller ett gynnsamt svar på, karvedilol. I en placebokontrollerad studie av försökspersoner med allvarlig hjärtsvikt rapporterades försämrad hjärtsvikt under de första 3 månaderna i liknande grad med karvedilol och med placebo. När behandlingen upprätthölls längre än 3 månader rapporterades försämrad hjärtsvikt mer sällan hos patienter som behandlats med karvedilol än med placebo. Förvärrad hjärtsvikt som observerats under långtidsbehandling är mer sannolikt relaterad till patientens underliggande sjukdom än till behandling med karvedilol.
Icke-allergisk bronkospasm
Patienter med bronkospastisk sjukdom (t.ex. kronisk bronkit, emfysem) bör i allmänhet inte få β-blockerare. COREG kan dock användas med försiktighet till patienter som inte svarar på eller inte kan tolerera andra antihypertensiva medel. Det är klokt, om COREG används, att använda den minsta effektiva dosen, så att hämning av endogena eller exogena β-agonister minimeras.
I kliniska prövningar av patienter med hjärtsvikt inkluderades patienter med bronkospastisk sjukdom om de inte behövde oral eller inhalerad medicin för att behandla sin bronkospastiska sjukdom. Hos sådana patienter rekommenderas att karvedilol används med försiktighet. Doseringsrekommendationerna bör följas noggrant och dosen bör sänkas om några tecken på bronkospasm observeras under upptitreringen.
Glykemisk kontroll vid typ 2-diabetes
allmänhet kan β-blockerare maskera några av manifestationerna av hypoglykemi, särskilt takykardi. Icke-selektiva β-blockerare kan potentiera insulininducerad hypoglykemi och fördröja återhämtningen av serumglukosnivåerna. Patienter som lider av spontan hypoglykemi eller diabetespatienter som får insulin eller orala hypoglykemiska medel bör varnas för dessa möjligheter.
Hos patienter med hjärtsvikt och diabetes kan karvedilolbehandling leda till försämrad hyperglykemi, som svarar på intensifiering av hypoglykemisk behandling. Det rekommenderas att blodsockret övervakas när karvediloldosering påbörjas, justeras eller avbryts. Studier utformade för att undersöka effekterna av karvedilol på glykemisk kontroll hos patienter med diabetes och hjärtsvikt har inte genomförts.
en studie utformad för att undersöka effekterna av karvedilol på glykemisk kontroll i en population med mild till måttlig hypertoni och välkontrollerad typ 2-diabetes mellitus, hade karvedilol ingen negativ effekt på glykemisk kontroll, baserat på HbA1c-mätningar [se Kliniska studier ].
Perifer kärlsjukdom
β-blockerare kan utlösa eller förvärra symtom på arteriell insufficiens hos patienter med perifer vaskulär sjukdom. Försiktighet bör iakttas hos sådana individer.
Försämring av njurfunktionen
sällsynta fall har användning av karvedilol hos patienter med hjärtsvikt resulterat i försämring av njurfunktionen. Patienter i riskzonen verkar vara de med lågt blodtryck (systoliskt blodtryck mindre än 100 mm Hg), ischemisk hjärtsjukdom och diffus kärlsjukdom och/eller underliggande njurinsufficiens. Njurfunktionen har återgått till baslinjen när karvedilol stoppades. Hos patienter med dessa riskfaktorer rekommenderas att njurfunktionen övervakas under upptitrering av karvedilol och att läkemedlet sätts ut eller dosen minskas om försämring av njurfunktionen inträffar.
Stor operation
Kroniskt administrerad β-blockerande behandling bör inte rutinmässigt avbrytas före större operation; dock kan hjärtats försämrade förmåga att svara på reflexadrenerga stimuli öka riskerna för allmän anestesi och kirurgiska ingrepp.
Tyreotoxikos
β-adrenerg blockad kan maskera kliniska tecken på hypertyreos, såsom takykardi. Plötsligt upphörande av β-blockad kan följas av en förvärring av symtomen på hypertyreos eller kan utlösa sköldkörtelstorm.
Feokromocytom
Hos patienter med feokromocytom bör ett α-blockerande medel sättas in före användning av något β-blockerande medel. Även om karvedilol har både α- och β-blockerande farmakologiska aktiviteter, har det inte funnits någon erfarenhet av dess användning vid detta tillstånd. Därför bör försiktighet iakttas vid administrering av karvedilol till patienter som misstänks ha feokromocytom.
Prinzmetals variant Angina
Medel med icke-selektiv β-blockerande aktivitet kan framkalla bröstsmärtor hos patienter med Prinzmetals variant angina. Det har inte funnits någon klinisk erfarenhet av karvedilol hos dessa patienter även om den α-blockerande aktiviteten kan förhindra sådana symtom. Försiktighet bör dock iakttas vid administrering av karvedilol till patienter som misstänks ha Prinzmetals variant angina.
Risk för anafylaktisk reaktion
Medan de tar β-blockerare kan patienter med en historia av allvarlig anafylaktisk reaktion på en mängd olika allergener vara mer reaktiva mot upprepad utmaning, antingen oavsiktlig, diagnostisk eller terapeutisk. Sådana patienter kan inte svara på de vanliga doser av adrenalin som används för att behandla allergiska reaktioner.
Intraoperativt Floppy Iris Syndrome
Intraoperativt Floppy Iris Syndrome (IFIS) har observerats under kataraktkirurgi hos vissa patienter som behandlats med alfa-1-blockerare (COREG är en alfa/beta-blockerare). Denna variant av småpupillsyndrom kännetecknas av kombinationen av en slapp iris som böljar som svar på intraoperativa spolningsströmmar, progressiv intraoperativ mios trots preoperativ utvidgning med vanliga mydriatiska läkemedel och potentiell prolaps av iris mot fakoemulsifieringssnitten. Patientens ögonläkare bör vara förberedd på möjliga modifieringar av den kirurgiska tekniken, såsom användning av iriskrokar, irisdilatatorringar eller viskoelastiska substanser. Det verkar inte finnas någon fördel med att avbryta alfa-1-blockerare före operation för grå starr.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION ).
Patienter som tar COREG bör informeras om följande:
- Patienter ska ta COREG med mat.
- Patienter ska inte avbryta eller sluta använda COREG 25 mg utan läkares råd.
- Patienter med hjärtsvikt bör rådfråga sin läkare om de upplever tecken eller symtom på förvärrad hjärtsvikt, såsom viktökning eller ökad andnöd.
- Patienter kan uppleva ett blodtrycksfall när de står upp, vilket resulterar i yrsel och, i sällsynta fall, svimning. Patienter ska sitta eller ligga ner när dessa symtom på sänkt blodtryck uppträder.
- Om de upplever yrsel eller trötthet, bör patienter undvika att köra bil eller farliga uppgifter.
- Patienter bör konsultera en läkare om de upplever yrsel eller svimning, om dosen skulle justeras.
- Diabetespatienter bör rapportera alla förändringar i blodsockernivån till sin läkare.
- Kontaktlinsbärare kan uppleva minskad tårbildning.
COREG 25mg, COREG 3,12mg CR och TILTAB är varumärken som ägs av eller licensieras till GSK-gruppen av företag.
Det andra varumärket som anges är ett varumärke som ägs av eller licensieras till dess ägare och ägs inte av eller licensieras till GSK-gruppen av företag. Tillverkaren av detta varumärke är inte ansluten till och stöder inte GSK-gruppen av företag eller dess produkter.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
I 2-åriga studier utförda på råttor som gavs karvedilol i doser upp till 75 mg per kg per dag (12 gånger MRHD som mg per m2) eller på möss som gavs upp till 200 mg per kg per dag (16 gånger MRHD som mg per dag). m2), hade karvedilol ingen cancerframkallande effekt.
Karvedilol var negativ när den testades i ett antal genotoxicitetsanalyser, inklusive Ames- och CHO/HGPRT-analyserna för mutagenicitet och in vitro-hamstermikronukleus och in vivo humana lymfocytcellstester för klastogenicitet.
en kombinerad fertilitets-/utvecklings-/postnatal toxicitetsstudie gavs råttor karvedilol (12, 60, 300 mg per kg per dag) oralt genom sondmatning i 2 veckor före parning och genom parning, dräktighet och avvänjning för honor och för 62 dagar före och genom parning för hanar. Vid en dos på 300 mg per kg per dag (större än eller lika med 50 gånger MRHD som mg per m2) var karvedilol giftigt för vuxna råttor (sedation, minskad viktökning) och associerades med ett minskat antal framgångsrika parningar, förlängd parningstid, färre corpora lutea och implantat per moder, färre levande ungar per kull och förseningar i fysisk tillväxt/utveckling. No-effect-nivån för öppen toxicitet och försämrad fertilitet var 60 mg per kg per dag (10 gånger MRHD som mg per m2).
Användning i specifika populationer
Graviditet
Risksammanfattning
Tillgängliga data om användning av COREG 12,5 mg hos gravida kvinnor är otillräckliga för att avgöra om det finns läkemedelsrelaterade risker för ogynnsamma utvecklingsresultat. Det finns risker för modern och fostret i samband med dåligt kontrollerad hypertoni under graviditeten. Användning av betablockerare under graviditetens tredje trimester kan öka risken för hypotoni, bradykardi, hypoglykemi och andningsdepression hos nyfödda [ se Kliniska överväganden ]. I reproduktionsstudier på djur fanns inga tecken på negativa utvecklingsresultat vid kliniskt relevanta doser [ se Data ]. Oral administrering av karvedilol till gravida råttor under organogenes resulterade i post-implantation förlust, minskad fosterkroppsvikt och en ökad frekvens av försenad fosterskelettutveckling vid maternellt toxiska doser som var 50 gånger den maximala rekommenderade humana dosen (MRHD). Dessutom resulterade oral administrering av karvedilol till dräktiga kaniner under organogenesen i ökad post-implantationsförlust vid doser 25 gånger MRHD [ se Data ].
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för de angivna populationerna är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för mödrar och/eller embryo/foster
Hypertoni under graviditeten ökar moderns risk för havandeskapsförgiftning, graviditetsdiabetes, för tidig förlossning och förlossningskomplikationer (t.ex. behov av kejsarsnitt och postpartumblödning). Hypertoni ökar fostrets risk för intrauterin tillväxtbegränsning och intrauterin död. Gravida kvinnor med högt blodtryck bör övervakas noggrant och hanteras därefter.
Fetala/neonatala biverkningar
Nyfödda till kvinnor med högt blodtryck som behandlas med betablockerare under graviditetens tredje trimester kan löpa ökad risk för hypotoni, bradykardi, hypoglykemi och andningsdepression. Observera nyfödda för symtom på hypotoni, bradykardi, hypoglykemi och andningsdepression och hantera därefter.
Data
Djurdata
Studier utförda på råttor och kaniner som fick karvedilol under fostrets organogenes avslöjade ökad post-implantationsförlust hos råttor vid en maternellt toxisk dos på 300 mg per kg per dag (50 gånger MRHD som mg per m2) och hos kaniner (i frånvaro av modern toxicitet) vid doser på 75 mg per kg per dag (25 gånger MRHD som mg per m2). Hos råttorna var det också en minskning av fostrets kroppsvikt med 300 mg per kg per dag (50 gånger MRHD som mg per m2) åtföljd av en ökad förekomst av foster med försenad skelettutveckling. Hos råttor var nivån utan effekt för embryo-fetal toxicitet 60 mg per kg per dag (10 gånger MRHD som mg per m2); hos kaniner var det 15 mg per kg per dag (5 gånger MRHD som mg per m2). I en pre- och postnatal utvecklingsstudie på råttor som administrerades karvedilol från sen dräktighet till laktation, observerades ökad embryodödlighet vid en maternellt toxisk dos på 200 mg per kg per dag (ungefär 32 gånger MRHD som mg per m2), och dödlighet av ungar och förseningar i fysisk tillväxt/utveckling observerades vid 60 mg per kg per dag (10 gånger MRHD som mg per m2) i frånvaro av maternell toxicitet. Ingen effektnivån var 12 mg per kg per dag (2 gånger MRHD som mg per m2). Karvedilol fanns i fetal råttvävnad.
Laktation
Risksammanfattning
Det finns inga data om förekomsten av karvedilol i bröstmjölk, effekterna på det ammade barnet eller effekterna på mjölkproduktionen. Karvedilol finns i mjölken från digivande råttor. Utvecklings- och hälsofördelarna med amning bör övervägas tillsammans med moderns kliniska behov av COREG och eventuella negativa effekter på det ammade barnet från COREG 3,12 mg eller från det underliggande moderns tillståndet.
Pediatrisk användning
Effektiviteten av COREG 3,12 mg hos patienter yngre än 18 år har inte fastställts.
en dubbelblind studie, 161 barn (medelålder: 6 år; intervall: 2 månader till 17 år; 45 % yngre än 2 år) med kronisk hjärtsvikt [NYHA klass II-IV, vänsterkammars ejektionsfraktion mindre än 40 % för barn med systemisk vänsterkammar (LV) och måttlig-svår kammardysfunktion kvalitativt genom eko för de med en systemisk kammare som inte var en LV] som fick standardbakgrundsbehandling randomiserades till placebo eller till 2 dosnivåer av karvedilol. Dessa dosnivåer gav placebokorrigerad hjärtfrekvenssänkning med 4 till 6 hjärtslag per minut, vilket tyder på β-blockadaktivitet. Exponeringen verkade vara lägre hos pediatriska försökspersoner än hos vuxna. Efter 8 månaders uppföljning fanns ingen signifikant effekt av behandlingen på kliniska resultat. Biverkningar i denna studie som inträffade hos mer än 10 % av patienterna som behandlades med COREG och dubbelt så många som placebobehandlade var bröstsmärtor (17 % mot 6 %), yrsel (13 % mot 2 %) och dyspné ( 11 % mot 0 %).
Geriatrisk användning
Av de 765 försökspersonerna med hjärtsvikt randomiserade till COREG 6,25 mg i amerikanska kliniska prövningar, var 31 % (235) 65 år eller äldre och 7,3 % (56) var 75 år eller äldre. Av de 1 156 försökspersoner som randomiserades till COREG 3,12 mg i en långtidsstudie med placebokontrollerad svår hjärtsvikt, var 47 % (547) 65 år eller äldre och 15 % (174) var 75 år eller äldre. Av 3 025 försökspersoner som fick COREG 6,25 mg i hjärtsviktsförsök över hela världen var 42 % 65 år eller äldre.
Av de 975 försökspersonerna med hjärtinfarkt randomiserade till COREG i CAPRICORN-studien var 48 % (468) 65 år eller äldre och 11 % (111) var 75 år eller äldre.
Av de 2 065 hypertensiva försökspersonerna i amerikanska kliniska prövningar av effekt eller säkerhet som behandlades med COREG 25 mg, var 21 % (436) 65 år eller äldre. Av 3 722 försökspersoner som fick COREG i kliniska prövningar med hypertoni som genomfördes över hela världen, var 24 % i åldern 65 år eller äldre.
Med undantag för yrsel hos hypertensiva försökspersoner (incidens 8,8 % hos äldre mot 6 % hos yngre försökspersoner), observerades inga övergripande skillnader i säkerhet eller effektivitet (se figurerna 2 och 4) mellan de äldre och yngre försökspersonerna i var och en av patienterna. dessa populationer. På liknande sätt har annan rapporterad klinisk erfarenhet inte identifierat skillnader i svar mellan äldre och yngre försökspersoner, men större känslighet hos vissa äldre individer kan inte uteslutas.
ÖVERDOS
Överdosering kan orsaka allvarlig hypotoni, bradykardi, hjärtinsufficiens, kardiogen chock och hjärtstillestånd. Andningsproblem, bronkospasmer, kräkningar, medvetslöshet och generaliserade anfall kan också förekomma.
Patienten ska placeras i ryggläge och vid behov hållas under observation och behandlas under intensivvårdsförhållanden. Följande medel kan administreras:
För överdriven bradykardi : Atropin, 2 mg IV.
För att stödja kardiovaskulär funktion Glukagon, 5 till 10 mg IV snabbt under 30 sekunder, följt av en kontinuerlig infusion av 5 mg per timme; sympatomimetika (dobutamin, isoprenalin, adrenalin) i doser beroende på kroppsvikt och effekt.
Om perifer vasodilatation dominerar kan det bli nödvändigt att administrera adrenalin eller noradrenalin med kontinuerlig övervakning av cirkulationsförhållandena. För terapiresistent bradykardi bör pacemakerbehandling utföras. För bronkospasm bör β-sympatomimetika (som aerosol eller IV) eller aminofyllin IV ges. Vid anfall rekommenderas långsam IV-injektion av diazepam eller klonazepam.
OBS: Vid allvarlig förgiftning där det finns symtom på chock, måste behandling med motgift fortsätta under en tillräckligt lång tidsperiod som överensstämmer med halveringstiden på 7 till 10 timmar för karvedilol.
Fall av överdosering med COREG 3,12 mg enbart eller i kombination med andra läkemedel har rapporterats. Intagna kvantiteter översteg i vissa fall 1 000 milligram. Upplevda symtom var bland annat lågt blodtryck och hjärtfrekvens. Standardstödjande behandling gavs och individer återhämtade sig.
KONTRAINDIKATIONER
COREG 25mg är kontraindicerat under följande tillstånd:
- Bronkialastma eller relaterade bronkospastiska tillstånd. Dödsfall från status asthmaticus har rapporterats efter engångsdoser av COREG.
- Andra eller tredje gradens AV-block.
- Sick sinus syndrome.
- Allvarlig bradykardi (såvida inte en permanent pacemaker finns på plats).
- Patienter med kardiogen chock eller som har dekompenserad hjärtsvikt som kräver användning av intravenös inotrop terapi. Sådana patienter bör först avvänjas från intravenös behandling innan COREG påbörjas.
- Patienter med gravt nedsatt leverfunktion.
- Patienter med en historia av en allvarlig överkänslighetsreaktion (t.ex. Stevens-Johnsons syndrom, anafylaktisk reaktion, angioödem) mot någon komponent i detta läkemedel eller andra läkemedel som innehåller karvedilol.
KLINISK FARMAKOLOGI
Handlingsmekanism
COREG 3,12mg är en racemisk blandning där icke-selektiv β-adrenoreceptorblockerande aktivitet finns i S(-)-enantiomeren och α1-adrenerg blockerande aktivitet är närvarande i både R(+)- och S(-)-enantiomerer med samma styrka. COREG 6,25 mg har ingen inneboende sympatomimetisk aktivitet.
Farmakodynamik
Hjärtsvikt
Grunden för de gynnsamma effekterna av COREG vid hjärtsvikt är inte fastställd.
Två placebokontrollerade studier jämförde de akuta hemodynamiska effekterna av COREG med baslinjemätningar hos 59 och 49 patienter med NYHA klass II-IV hjärtsvikt som fick diuretika, ACE-hämmare och digitalis. Det fanns signifikanta minskningar av systemiskt blodtryck, lungartärtryck, pulmonellt kapillärkiltryck och hjärtfrekvens. De initiala effekterna på hjärtminutvolymen, slagvolymindex och systemiskt vaskulärt motstånd var små och varierande.
Dessa försök mätte hemodynamiska effekter igen efter 12 till 14 veckor. COREG 25 mg reducerade signifikant systemiskt blodtryck, lungartärtryck, höger förmakstryck, systemiskt vaskulärt motstånd och hjärtfrekvens, medan slagvolymindex ökade.
Bland 839 patienter med NYHA klass II-III hjärtsvikt som behandlats under 26 till 52 veckor i 4 placebokontrollerade prövningar i USA, ökade den genomsnittliga vänsterkammarnas ejektionsfraktion (EF) mätt med radionuklidventrikulografi med 9 EF-enheter (%) hos försökspersoner som fick COREG 6,25 mg och med 2 EF-enheter hos placebopatienter vid en måldos på 25 till 50 mg två gånger dagligen. Effekterna av karvedilol på ejektionsfraktionen var relaterade till dosen. Doser på 6,25 mg två gånger dagligen, 12,5 mg två gånger dagligen och 25 mg två gånger dagligen var associerade med placebokorrigerade ökningar av EF på 5 EF-enheter, 6 EF-enheter respektive 8 EF-enheter; var och en av dessa effekter var nominellt statistiskt signifikanta.
Vänsterkammardysfunktion efter hjärtinfarkt
Grunden för de gynnsamma effekterna av COREG 25mg hos patienter med vänsterkammardysfunktion efter en akut hjärtinfarkt är inte fastställd.
Hypertoni
Mekanismen genom vilken β-blockad ger en antihypertensiv effekt har inte fastställts.
β-adrenoreceptorblockerande aktivitet har visats i djur- och humanstudier som visar att karvedilol (1) minskar hjärtminutvolymen hos normala försökspersoner, (2) minskar tränings- och/eller isoproterenol-inducerad takykardi och (3) minskar reflexortostatisk takykardi. Signifikant β-adrenoreceptorblockerande effekt ses vanligtvis inom 1 timme efter läkemedelsadministrering.
α1-adrenoreceptorblockerande aktivitet har visats i studier på människor och djur, vilket visar att karvedilol (1) dämpar pressoreffekterna av fenylefrin, (2) orsakar vasodilatation och (3) minskar perifert vaskulärt motstånd. Dessa effekter bidrar till att sänka blodtrycket och ses vanligtvis inom 30 minuter efter läkemedelsadministrering.
På grund av karvedilols α1-receptorblockerande aktivitet sänks blodtrycket mer i stående än i ryggläge, och symtom på postural hypotoni (1,8 %), inklusive sällsynta fall av synkope, kan förekomma. Efter oral administrering, när postural hypotoni har inträffat, har den varit övergående och är ovanlig när COREG administreras med föda i den rekommenderade startdosen och titreringsökningarna följs noggrant [se DOSERING OCH ADMINISTRERING ].
Hos hypertensiva patienter med normal njurfunktion minskade terapeutiska doser av COREG det renala vaskulära motståndet utan förändring i glomerulär filtrationshastighet eller renalt plasmaflöde. Förändringar i utsöndring av natrium, kalium, urinsyra och fosfor hos hypertonipatienter med normal njurfunktion var liknande efter COREG och placebo.
COREG 3,12 mg har liten effekt på plasmakatekolaminer, plasmaaldosteron eller elektrolytnivåer, men det minskar signifikant plasmareninaktiviteten när den ges under minst 4 veckor. Det ökar också nivåerna av atrial natriuretisk peptid.
Farmakokinetik
COREG absorberas snabbt och omfattande efter oral administrering, med en absolut biotillgänglighet på cirka 25 % till 35 % på grund av en signifikant grad av first-pass metabolism. Efter oral administrering varierar den skenbara genomsnittliga terminala halveringstiden för karvedilol i allmänhet från 7 till 10 timmar. Plasmakoncentrationer som uppnås är proportionella mot den orala dosen som administreras. Vid administrering med föda saktas absorptionshastigheten, vilket framgår av en fördröjning av tiden för att nå maximala plasmanivåer, utan någon signifikant skillnad i graden av biotillgänglighet. Att ta COREG med mat bör minimera risken för ortostatisk hypotoni.
Karvedilol metaboliseras i stor utsträckning. Efter oral administrering av radiomärkt karvedilol till friska frivilliga, stod karvedilol endast för cirka 7 % av den totala radioaktiviteten i plasma mätt som area under kurvan (AUC). Mindre än 2 % av dosen utsöndrades oförändrat i urinen. Karvedilol metaboliseras främst genom aromatisk ringoxidation och glukuronidering.
De oxidativa metaboliterna metaboliseras vidare genom konjugering via glukuronidering och sulfatering. Metaboliterna av karvedilol utsöndras främst via gallan i avföringen. Demetylering och hydroxylering vid fenolringen producerar 3 aktiva metaboliter med β-receptorblockerande aktivitet. Baserat på prekliniska studier är 4'-hydroxifenylmetaboliten ungefär 13 gånger mer potent än karvedilol för β-blockad.
Jämfört med karvedilol uppvisar de 3 aktiva metaboliterna svag vasodilaterande aktivitet. Plasmakoncentrationerna av de aktiva metaboliterna är ungefär en tiondel av de som observerats för karvedilol och har farmakokinetik som liknar moderkroppen.
Karvedilol genomgår stereoselektiv first-pass-metabolism med plasmanivåer av R(+)-karvedilol cirka 2 till 3 gånger högre än S(-)-karvedilol efter oral administrering till friska försökspersoner. Den genomsnittliga skenbara terminala eliminationshalveringstiden för R(+)-karvedilol varierar från 5 till 9 timmar jämfört med 7 till 11 timmar för S(-)-enantiomeren.
De primära P450-enzymer som ansvarar för metabolismen av både R(+) och S(-)-karvedilol i humana levermikrosomer var CYP2D6 och CYP2C9 och i mindre utsträckning CYP3A4, 2C19, 1A2 och 2E1. CYP2D6 tros vara huvudenzymet i 4'- och 5'-hydroxyleringen av karvedilol, med ett potentiellt bidrag från 3A4. CYP2C9 tros vara av primär betydelse i O-metyleringsvägen för S(-)-karvedilol.
Karvedilol är föremål för effekterna av genetisk polymorfism med dåliga metaboliserare av debrisoquin (en markör för cytokrom P450 2D6) som uppvisar 2- till 3 gånger högre plasmakoncentrationer av R(+)-karvedilol jämfört med omfattande metaboliserare. Däremot ökar plasmanivåerna av S(-)-karvedilol endast med cirka 20% till 25% hos dåliga metaboliserare, vilket indikerar att denna enantiomer metaboliseras i mindre utsträckning av cytokrom P450 2D6 än R(+)-karvedilol. Farmakokinetiken för karvedilol tycks inte vara annorlunda hos dåliga metaboliserare av S-mefenytoin (patienter med brist på cytokrom P450 2C19).
Karvedilol är mer än 98 % bundet till plasmaproteiner, främst med albumin. Plasmaproteinbindningen är oberoende av koncentrationen över det terapeutiska området. Karvedilol är en basisk, lipofil förening med en steady-state distributionsvolym på cirka 115 L, vilket indikerar betydande distribution i extravaskulära vävnader. Plasmaclearance sträcker sig från 500 till 700 ml/min.
Specifika populationer
Hjärtsvikt
Steady-state plasmakoncentrationer av karvedilol och dess enantiomerer ökade proportionellt över dosintervallet 6,25 till 50 mg hos patienter med hjärtsvikt. Jämfört med friska försökspersoner hade försökspersoner med hjärtsvikt ökade medelvärden för AUC och Cmax för karvedilol och dess enantiomerer, med upp till 50 % till 100 % högre värden observerade hos 6 försökspersoner med NYHA klass IV hjärtsvikt. Den genomsnittliga skenbara terminala eliminationshalveringstiden för karvedilol liknade den som observerats hos friska försökspersoner.
Geriatrisk
Plasmanivåer av karvedilol är i genomsnitt cirka 50 % högre hos äldre jämfört med unga försökspersoner. Nedsatt leverfunktion Jämfört med friska försökspersoner uppvisar patienter med gravt nedsatt leverfunktion (cirros) en 4- till 7-faldig ökning av karvedilolnivåerna. Karvedilol är kontraindicerat hos patienter med gravt nedsatt leverfunktion.
Nedsatt njurfunktion
Även om karvedilol huvudsakligen metaboliseras av levern, har plasmakoncentrationer av karvedilol rapporterats öka hos patienter med nedsatt njurfunktion. Baserat på genomsnittliga AUC-data observerades cirka 40 % till 50 % högre plasmakoncentrationer av karvedilol hos patienter med hypertoni och måttligt till gravt nedsatt njurfunktion jämfört med en kontrollgrupp av patienter med hypertoni och normal njurfunktion. Intervallet för AUC-värden var emellertid likartade för båda grupperna. Förändringar i genomsnittliga maximala plasmanivåer var mindre uttalade, cirka 12 % till 26 % högre hos patienter med nedsatt njurfunktion.
I överensstämmelse med dess höga grad av plasmaproteinbindning, verkar karvedilol inte elimineras signifikant genom hemodialys.
Läkemedelsinteraktioner
Eftersom karvedilol genomgår en betydande oxidativ metabolism, kan metabolismen och farmakokinetiken för karvedilol påverkas av induktion eller hämning av cytokrom P450-enzymer.
Amiodaron
en farmakokinetisk prövning utförd på 106 japanska försökspersoner med hjärtsvikt, resulterade samtidig administrering av små laddnings- och underhållsdoser av amiodaron med karvedilol i minst en 2-faldig ökning av steady-state dalkoncentrationerna av S(-)-karvedilol [se LÄKEMEDELSINTERAKTIONER ].
Cimetidin
I en farmakokinetisk prövning utförd på 10 friska manliga försökspersoner ökade cimetidin (1 000 mg per dag) steady-state AUC för karvedilol med 30 % utan förändring i Cmax [se LÄKEMEDELSINTERAKTIONER ].
Digoxin
Efter samtidig administrering av karvedilol (25 mg en gång dagligen) och digoxin (0,25 mg en gång dagligen) i 14 dagar, ökade steady-state AUC och dalkoncentrationer av digoxin med 14 % respektive 16 % hos 12 försökspersoner med hypertoni [se LÄKEMEDELSINTERAKTIONER ].
Glyburide
Hos 12 friska försökspersoner resulterade inte kombinerad administrering av karvedilol (25 mg en gång dagligen) och en engångsdos av glyburid i en kliniskt relevant farmakokinetisk interaktion för någon av substanserna.
Hydroklortiazid
En oral engångsdos av karvedilol 25 mg förändrade inte farmakokinetiken för en oral engångsdos av hydroklortiazid 25 mg hos 12 patienter med hypertoni. På samma sätt hade hydroklortiazid ingen effekt på farmakokinetiken för karvedilol.
Rifampin
I en farmakokinetisk prövning utförd på 8 friska manliga försökspersoner, minskade rifampin (600 mg dagligen i 12 dagar) AUC och Cmax för karvedilol med cirka 70 % [se LÄKEMEDELSINTERAKTIONER ].
Torsemid
I en studie med 12 friska försökspersoner resulterade kombinerad oral administrering av karvedilol 25 mg en gång dagligen och torsemid 5 mg en gång dagligen under 5 dagar inte i några signifikanta skillnader i deras farmakokinetik jämfört med administrering av enbart läkemedlen.
Warfarin
Karvedilol (12,5 mg två gånger dagligen) hade ingen effekt på steady-state protrombintidsförhållanden och förändrade inte farmakokinetiken för R(+)- och S(-)-warfarin efter samtidig administrering med warfarin hos 9 friska frivilliga.
Kliniska studier
Hjärtsvikt
Totalt 6 975 försökspersoner med mild till svår hjärtsvikt utvärderades i placebokontrollerade studier med karvedilol.
Mild till måttlig hjärtsvikt
Carvedilol studerades i 5 multicenter, placebokontrollerade prövningar och i 1 aktivt kontrollerad prövning (COMET-studie) som involverade personer med mild till måttlig hjärtsvikt.
Fyra amerikanska multicenter, dubbelblinda, placebokontrollerade studier inkluderade 1 094 försökspersoner (696 randomiserade till karvedilol) med NYHA klass II-III hjärtsvikt och ejektionsfraktion mindre än eller lika med 0,35. De allra flesta var på digitalis, diuretika och en ACE-hämmare vid inträde i prövningen. Patienterna tilldelades prövningarna baserat på träningsförmåga. En dubbelblind, placebokontrollerad studie mellan Australien och Nya Zeeland inkluderade 415 försökspersoner (hälften randomiserade till karvedilol) med mindre allvarlig hjärtsvikt. Alla protokoll exkluderade försökspersoner som förväntades genomgå hjärttransplantation under de 7,5 till 15 månaderna av dubbelblind uppföljning. Alla randomiserade försökspersoner hade tolererat en 2-veckors kur med karvedilol 6,25 mg två gånger dagligen.
varje försök fanns det en primär slutpunkt, antingen progression av hjärtsvikt (1 amerikansk prövning) eller träningstolerans (2 amerikanska prövningar som uppfyller inskrivningsmålen och försöket Australien-Nya Zeeland). Det fanns många sekundära slutpunkter specificerade i dessa prövningar, inklusive NYHA-klassificering, globala bedömningar av patient och läkare och kardiovaskulär sjukhusvistelse. Andra analyser som inte var planerade inkluderade summan av dödsfall och totala kardiovaskulära sjukhusvistelser. I situationer där de primära slutpunkterna för en studie inte visar någon signifikant nytta av behandlingen, är tilldelningen av signifikansvärden till de andra resultaten komplex, och sådana värden måste tolkas med försiktighet.
Resultaten av försöken i USA och Australien-Nya Zeeland var följande:
Bromsar utvecklingen av hjärtsvikt
En amerikansk multicenterstudie (366 försökspersoner) hade som primär slutpunkt summan av kardiovaskulär dödlighet, kardiovaskulär sjukhusvistelse och ihållande ökning av hjärtsviktsmediciner. Hjärtsviktsprogression minskade, under en genomsnittlig uppföljning på 7 månader, med 48 % (P = 0,008).
I försöket Australien-Nya Zeeland minskade dödsfall och totala sjukhusvistelser med cirka 25 % under 18 till 24 månader. I de tre största amerikanska försöken minskade dödsfall och totala sjukhusvistelser med 19 %, 39 % och 49 %, nominellt statistiskt signifikant i de två senaste försöken. Resultaten från Australien och Nya Zeeland var statistiskt på gränsen.
Funktionella åtgärder
Ingen av multicenterförsöken hade NYHA-klassificering som primär slutpunkt, men alla sådana försök hade den som sekundär slutpunkt. Det fanns åtminstone en trend mot förbättring i NYHA-klassen i alla försök. Träningstolerans var den primära slutpunkten i 3 försök; hos ingen hittades en statistiskt signifikant effekt.
Subjektiva åtgärder
Hälsorelaterad livskvalitet, mätt med ett standard frågeformulär (en primär slutpunkt i 1 studie), var opåverkad av karvedilol. Patienternas och utredarnas globala bedömningar visade dock betydande förbättringar i de flesta prövningar.
Dödlighet
Döden var inte en fördefinierad slutpunkt i någon prövning, utan analyserades i alla prövningar. Totalt sett minskade dödligheten i dessa 4 amerikanska prövningar, nominellt signifikant i 2 prövningar.
COMET-rättegången
denna dubbelblinda studie randomiserades 3 029 försökspersoner med NYHA klass II-IV hjärtsvikt (vänsterkammars ejektionsfraktion mindre än eller lika med 35%) för att få antingen karvedilol (måldos: 25 mg två gånger dagligen) eller metoprolol med omedelbar frisättning tartrat (måldos: 50 mg två gånger dagligen). Medelåldern för försökspersonerna var cirka 62 år, 80 % var män och den genomsnittliga vänsterkammarejektionsfraktionen vid baslinjen var 26 %. Ungefär 96 % av försökspersonerna hade NYHA klass II eller III hjärtsvikt. Samtidig behandling inkluderade diuretika (99 %), ACE-hämmare (91 %), digitalis (59 %), aldosteronantagonister (11 %) och "statin" lipidsänkande medel (21 %). Den genomsnittliga uppföljningstiden var 4,8 år. Medeldosen av karvedilol var 42 mg per dag.
Studien hade två primära slutpunkter: dödlighet av alla orsaker och sammansättningen av död plus sjukhusvistelse av någon anledning. Resultaten av COMET presenteras i tabell 3 nedan. Dödlighet av alla orsaker hade det mesta av den statistiska vikten och var den primära bestämningsfaktorn för försökets storlek. Dödligheten av alla orsaker var 34 % hos försökspersonerna som behandlades med karvedilol och var 40 % i metoprololgruppen med omedelbar frisättning (P = 0,0017; riskkvot = 0,83, 95 % KI: 0,74 till 0,93). Effekten på dödligheten berodde främst på en minskning av kardiovaskulär död. Skillnaden mellan de två grupperna med avseende på den sammansatta slutpunkten var inte signifikant (P = 0,122). Den uppskattade medelöverlevnaden var 8,0 år med karvedilol och 6,6 år med metoprolol med omedelbar frisättning.
Det är inte känt om denna formulering av metoprolol i någon dos eller denna låga dos av metoprolol i någon formulering har någon effekt på överlevnad eller sjukhusvistelse hos patienter med hjärtsvikt. Således förlänger denna studie den tid över vilken karvedilol visar fördelar på överlevnad vid hjärtsvikt, men det är inte bevis för att karvedilol förbättrar resultatet jämfört med formuleringen av metoprolol (TOPROL-XL) med fördelar vid hjärtsvikt.
Svår hjärtsvikt (COPERNICUS)
en dubbelblind studie (COPERNICUS), 2 289 försökspersoner med hjärtsvikt i vila eller med minimal ansträngning och vänsterkammars ejektionsfraktion mindre än 25 % (medelvärde 20 %), trots digitalis (66 %), diuretika (99 %) och ACE-hämmare (89%) randomiserades till placebo eller karvedilol. Karvedilol titrerades från en startdos på 3,125 mg två gånger dagligen till den maximalt tolererade dosen eller upp till 25 mg två gånger dagligen under minst 6 veckor. De flesta försökspersoner uppnådde måldosen på 25 mg. Rättegången genomfördes i Öst- och Västeuropa, USA, Israel och Kanada. Liknande antal försökspersoner per grupp (cirka 100) drog sig ur under titreringsperioden.
Den primära slutpunkten för studien var dödlighet av alla orsaker, men orsaksspecifik dödlighet och risken för dödsfall eller sjukhusvistelse (totalt, kardiovaskulär [CV] eller hjärtsvikt [HF]) undersöktes också. De utvecklande försöksdata följdes av en dataövervakningskommitté, och dödlighetsanalyser justerades för dessa flera utseenden. Studien avbröts efter en medianuppföljning på 10 månader på grund av en observerad 35 % minskning av dödligheten (från 19,7 % per patientår på placebo till 12,8 % på karvedilol; riskkvot 0,65, 95 % KI: 0,52 till 0,81, P = 0,0014, justerat) (se figur 1). Resultaten av COPERNICUS visas i tabell 4.
Figur 1. Överlevnadsanalys för COPERNICUS (intention-to-treat) 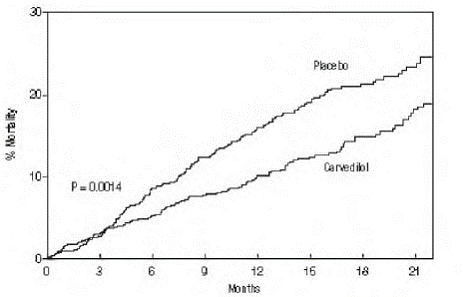
Effekten på dödligheten var främst resultatet av en minskning av antalet plötsliga dödsfall bland försökspersoner utan förvärrad hjärtsvikt.
Patienternas globala bedömningar, där karvedilolbehandlade försökspersoner jämfördes med placebo, baserades på förspecificerade, periodiska självbedömningar av patienten avseende huruvida klinisk status efter behandling visade förbättring, försämring eller ingen förändring jämfört med baslinjen. Patienter som behandlats med karvedilol visade signifikanta förbättringar i globala bedömningar jämfört med de som behandlades med placebo i COPERNICUS.
I protokollet angavs också att sjukhusvistelser skulle bedömas. Färre patienter på COREG 6,25 mg än på placebo lades in på sjukhus av någon anledning (372 mot 432, P = 0,0029), av kardiovaskulära skäl (246 mot 314, P = 0,0003), eller för förvärrad hjärtsvikt (198 mot 2600, P = 010). ).
COREG 6,25 mg hade en konsekvent och gynnsam effekt på dödlighet av alla orsaker såväl som de kombinerade slutpunkterna för dödlighet av alla orsaker plus sjukhusvistelse (totalt, CV eller hjärtsvikt) i den totala försökspopulationen och i alla undersökta undergrupper, inklusive män och kvinnor, äldre och icke-äldre, svarta och icke-svarta, samt diabetiker och icke-diabetiker (se figur 2).
Figur 2. Effekter på dödlighet för undergrupper i COPERNICUS 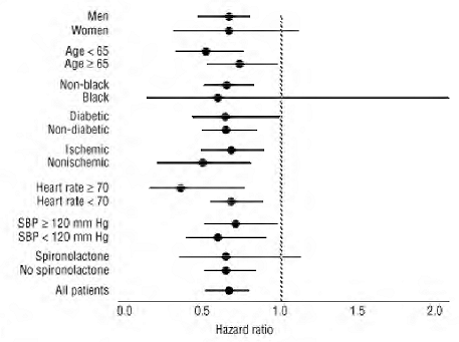
Vänsterkammardysfunktion efter hjärtinfarkt
CAPRICORN var en dubbelblind studie som jämförde karvedilol och placebo på 1 959 försökspersoner med en nyligen genomförd hjärtinfarkt (inom 21 dagar) och vänsterkammars ejektionsfraktion på mindre än eller lika med 40 %, med (47 %) eller utan symtom på hjärtsvikt. Försökspersoner som fick karvedilol fick 6,25 mg två gånger dagligen, titrerad som tolererad till 25 mg två gånger dagligen. Försökspersonerna måste ha ett systoliskt blodtryck som överstiger 90 mm Hg, en sittande hjärtfrekvens på mer än 60 slag per minut och ingen kontraindikation för användning av β-blockerare. Behandling av indexinfarkten inkluderade acetylsalicylsyra (85 %), IV eller orala β-blockerare (37 %), nitrater (73 %), heparin (64 %), trombolytika (40 %) och akut angioplastik (12 %). Bakgrundsbehandlingen inkluderade ACE-hämmare eller angiotensinreceptorblockerare (97 %), antikoagulantia (20 %), lipidsänkande medel (23 %) och diuretika (34 %). Baslinjepopulationens egenskaper inkluderade en medelålder på 63 år, 74 % män, 95 % kaukasiska, medelblodtryck 121/74 mm Hg, 22 % med diabetes och 54 % med hypertoni i anamnesen. Genomsnittlig dos av karvedilol var 20 mg två gånger dagligen; den genomsnittliga uppföljningstiden var 15 månader.
Dödligheten av alla orsaker var 15 % i placebogruppen och 12 % i karvedilolgruppen, vilket tyder på en riskminskning på 23 % hos patienter som behandlats med karvedilol (95 % KI: 2 % till 40 %, P = 0,03), som visas i figuren 3. Effekterna på dödligheten i olika undergrupper visas i figur 4. Nästan alla dödsfall var kardiovaskulära (som minskade med 25 % av karvedilol), och de flesta av dessa dödsfall var plötsliga eller relaterade till pumpfel (båda dödsfallen minskade av karvedilol). En annan studieslutpunkt, total dödlighet och sjukhusvistelse av alla orsaker, visade ingen signifikant förbättring.
Det observerades också en signifikant 40 % minskning av dödlig eller icke-dödlig hjärtinfarkt i gruppen som behandlades med karvedilol (95 % KI: 11 % till 60 %, P = 0,01). En liknande minskning av risken för hjärtinfarkt observerades också i en metaanalys av placebokontrollerade studier av karvedilol vid hjärtsvikt.
Figur 3. Överlevnadsanalys för STENBOCK (Intent-to-Treat) 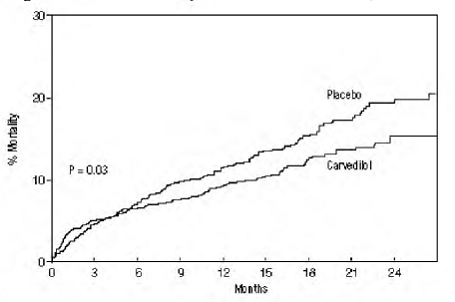
Figur 4. Effekter på dödlighet för undergrupper i STENBOCK 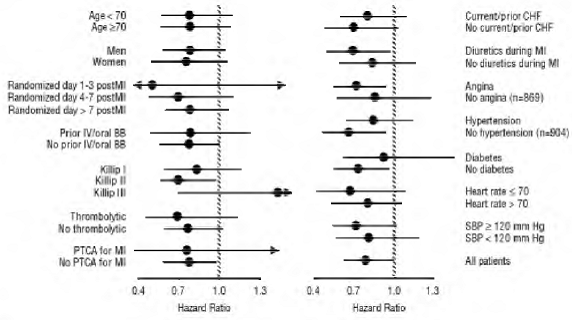
Hypertoni
COREG 25 mg studerades i 2 placebokontrollerade studier som använde dosering två gånger dagligen med totala dagliga doser på 12,5 till 50 mg. I dessa och andra prövningar översteg startdosen inte 12,5 mg. Vid 50 mg per dag minskade COREG sittande dalblodtryck (12 timmar) med cirka 9/5,5 mm Hg; vid 25 mg per dag var effekten ca 7,5/3,5 mm Hg. Jämförelser av dal-till-topp-blodtryck visade ett dal-till-topp-förhållande för blodtryckssvar på cirka 65 %. Pulsen sjönk med cirka 7,5 slag per minut vid 50 mg per dag. I allmänhet, som är sant för andra β-blockerare, var svaren mindre hos svarta än icke-svarta försökspersoner. Det fanns inga ålders- eller könsrelaterade skillnader i svar.
Den maximala antihypertensiva effekten inträffade 1 till 2 timmar efter en dos. Det dosrelaterade blodtryckssvaret åtföljdes av en dosrelaterad ökning av biverkningar [se NEGATIVA REAKTIONER ].
Hypertoni med typ 2-diabetes mellitus
en dubbelblind studie (GEMINI) utvärderades COREG 25 mg, tillsatt till en ACE-hämmare eller angiotensinreceptorblockerare, i en population med mild till måttlig hypertoni och välkontrollerad typ 2-diabetes mellitus. Medelvärdet för HbA1c vid baslinjen var 7,2 %. COREG titrerades till en medeldos på 17,5 mg två gånger dagligen och bibehölls i 5 månader. COREG hade ingen negativ effekt på glykemisk kontroll, baserat på HbA1c-mätningar (medelförändring från baslinjen på 0,02 %, 95 % KI: -0,06 till 0,10, P = NS) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
PATIENTINFORMATION
COREG (Co-REG) (karvedilol) Tabletter
Läs patientinformationen som följer med COREG innan du börjar ta den och varje gång du får en påfyllning. Det kan komma ny information. Denna information ersätter inte att prata med din läkare om ditt medicinska tillstånd eller din behandling. Om du har några frågor om COREG 3,12mg, fråga din läkare eller apotekspersonal.
Vad är COREG 3,12mg?
COREG är ett receptbelagt läkemedel som tillhör en grupp läkemedel som kallas "betablockerare". COREG 6,25 mg används, ofta tillsammans med andra läkemedel, för följande tillstånd:
- för att behandla patienter med vissa typer av hjärtsvikt
- för att behandla patienter som fick en hjärtinfarkt som förvärrade hur väl hjärtat pumpar
- för att behandla patienter med högt blodtryck (hypertoni)
COREG är inte godkänt för användning av barn under 18 år.
Vem ska inte ta Coreg?
Ta inte COREG 6,25 mg om du:
- har allvarlig hjärtsvikt och är inlagd på intensivvårdsavdelning eller kräver vissa intravenösa mediciner som hjälper till att stödja cirkulationen (inotropa mediciner).
- är benägna att få astma eller andra andningsproblem.
- har en långsam hjärtrytm eller ett hjärta som hoppar över ett slag (oregelbunden hjärtslag).
- har leverproblem.
- är allergiska mot någon av ingredienserna i COREG. Den aktiva ingrediensen är karvedilol. Se slutet av denna broschyr för en lista över alla ingredienser i COREG.
Vad ska jag berätta för min läkare innan jag tar COREG?
Berätta för din läkare om alla dina medicinska tillstånd, inklusive om du:
- har astma eller andra lungproblem (som bronkit eller emfysem).
- har problem med blodflödet i fötter och ben (perifer kärlsjukdom). COREG 3,12 mg kan förvärra vissa av dina symtom.
- har diabetes.
- har problem med sköldkörteln.
- har ett tillstånd som kallas feokromocytom.
- har haft svåra allergiska reaktioner.
- är gravid eller försöker bli gravid. Det är inte känt om COREG är säkert för ditt ofödda barn. Du och din läkare bör prata om det bästa sättet att kontrollera ditt höga blodtryck under graviditeten.
- ammar. Det är inte känt om COREG går över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar COREG.
- är planerade för operation och kommer att ges bedövningsmedel.
- är planerade för gråstarrsoperation och har tagit eller tar för närvarande COREG.
- tar receptbelagda eller receptfria läkemedel, vitaminer och växtbaserade kosttillskott. COREG och vissa andra läkemedel kan påverka varandra och orsaka allvarliga biverkningar. COREG 3,12 mg kan påverka hur andra läkemedel fungerar. Andra läkemedel kan också påverka hur väl COREG 25mg fungerar.
Håll en lista över alla mediciner du tar. Visa denna lista för din läkare och apotekspersonal innan du börjar med ett nytt läkemedel.
Hur ska jag ta COREG?
Det är viktigt för dig att ta din medicin varje dag enligt din läkares anvisningar. Om du slutar ta COREG plötsligt kan du få bröstsmärtor och/eller hjärtinfarkt. Om din läkare beslutar att du ska sluta ta COREG 6,25 mg, kan din läkare sakta sänka din dos under en viss tid innan den slutar helt.
- Ta COREG exakt som föreskrivet. Din läkare kommer att tala om för dig hur många tabletter du ska ta och hur ofta. För att minimera möjliga biverkningar kan din läkare börja med en låg dos och sedan långsamt öka dosen.
- Sluta inte ta COREG och ändra inte mängden COREG du tar utan att tala med din läkare.
- Tala om för din läkare om du går upp i vikt eller har svårt att andas medan du tar COREG.
- Ta COREG med mat.
- Om du missar en dos av COREG 3,12 mg, ta din dos så snart du kommer ihåg, om det inte är dags att ta din nästa dos. Ta din nästa dos vid den vanliga tiden. Ta inte 2 doser samtidigt.
- Om du tar för mycket COREG 25mg, ring din läkare eller giftkontrollcentral omedelbart.
Vad ska jag undvika när jag tar COREG 3,12mg?
- COREG kan göra att du känner dig yr, trött eller svimmar. Kör inte bil, använd inte maskiner eller gör något som kräver att du är uppmärksam om du har dessa symtom.
Vilka är möjliga biverkningar av COREG?
- Lågt blodtryck (vilket kan orsaka yrsel eller svimning när du står upp). Om dessa händer, sitt eller lägg dig ner direkt och berätta för din läkare.
- Trötthet. Om du känner dig trött eller yr ska du inte köra bil, använda maskiner eller göra något som kräver att du är uppmärksam.
- Långsam hjärtslag.
- Förändringar i ditt blodsocker. Om du har diabetes, tala om för din läkare om du har några förändringar i dina blodsockernivåer.
- COREG kan dölja några av symtomen på lågt blodsocker, särskilt snabba hjärtslag.
- COREG kan maskera symtomen på hypertyreos (överaktiv sköldkörtel).
- Försämring av allvarliga allergiska reaktioner.
- Sällsynta men allvarliga allergiska reaktioner (inklusive nässelutslag eller svullnad av ansikte, läppar, tunga och/eller svalg som kan orsaka svårigheter att andas eller svälja) har inträffat hos patienter som har fått COREG. Dessa reaktioner kan vara livshotande.
Andra biverkningar av COREG inkluderar andnöd, viktökning, diarré och färre tårar eller torra ögon som blir besvärande om du använder kontaktlinser.
Ring din läkare om du har några biverkningar som stör dig eller inte försvinner.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA1088.
Hur ska jag förvara COREG 6,25mg?
- Förvara COREG vid mindre än 86°F (30°C). Håll tabletterna torra.
- Säkert, släng COREG som är inaktuell eller inte längre behövs.
- Förvara COREG 6,25mg och alla läkemedel utom räckhåll för barn.
Allmän information om COREG
Läkemedel skrivs ibland ut för andra tillstånd än de som beskrivs i patientinformationsblad. Använd inte COREG 3,12 mg för ett tillstånd som det inte har ordinerats för. Ge inte COREG till andra människor, även om de har samma symtom som du har. Det kan skada dem.
Denna broschyr sammanfattar den viktigaste informationen om COREG. Om du vill ha mer information, prata med din läkare. Du kan fråga din läkare eller apotekspersonal om information om COREG 6,25mg som är skriven för vårdpersonal.
Vilka är ingredienserna i COREG?
Aktiv ingrediens: karvedilol.
Inaktiva ingredienser: kolloidal kiseldioxid, krospovidon, hypromellos, laktos, magnesiumstearat, polyetylenglykol, polysorbat 80, povidon, sackaros och titandioxid.
Carvedilol tabletter finns i följande styrkor: 3,125 mg, 6,25 mg, 12,5 mg, 25 mg.
Vad är högt blodtryck (hypertoni)?
Blodtrycket är blodets kraft i dina blodkärl när ditt hjärta slår och när ditt hjärta vilar. Du har högt blodtryck när kraften är för stor. Högt blodtryck gör att hjärtat arbetar hårdare för att pumpa blod genom kroppen och orsakar skador på blodkärlen. COREG kan hjälpa dina blodkärl att slappna av så att ditt blodtryck blir lägre. Läkemedel som sänker blodtrycket kan minska din chans att få en stroke eller hjärtinfarkt.
