Minocin 50mg, 100mg Minocycline Hydrochloride Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Minocin Oral Suspension och hur används det?
Minocin (minocyklinhydroklorid) är ett tetracyklinantibiotikum som används för att behandla många olika bakterieinfektioner, såsom urinvägsinfektioner, luftvägsinfektioner, hudinfektioner, svår akne, gonorré, fästingfeber, klamydia och andra.
Vilka är biverkningarna av Minocin oral suspension?
Vanliga biverkningar av Minocin inkluderar:
- yrsel,
- trött känsla,
- snurrande känsla,
- led- eller muskelvärk,
- missfärgning av din hud eller naglar eller tandkött,
- illamående,
- diarre,
- orolig mage,
- hudutslag eller klåda,
- svullen tunga, eller
- vaginal klåda eller flytningar.
Tala om för din läkare om du har allvarliga biverkningar av Minocin 50mg inklusive:
- magkramper,
- diarré som är vattnig eller blodig,
- influensa symptom,
- sår i mun och hals,
- svaghet,
- mörkfärgad urin,
- ovanlig blödning,
- lila eller röda spetsiga fläckar under huden,
- feber,
- hudutslag,
- blåmärken,
- svår stickningar eller domningar,
- muskelsvaghet,
- aptitlöshet,
- gulfärgning av huden eller ögonen,
- bröstsmärta,
- oregelbunden hjärtrytm,
- hosta,
- väsande andning,
- andnöd,
- förvirring,
- kräkningar,
- svullnad,
- viktökning,
- kissa mindre än vanligt eller inte alls,
- huvudvärk eller smärta bakom ögonen,
- ringer i dina öron,
- synproblem,
- ledvärk eller svullnad med feber,
- svullna körtlar,
- muskelvärk,
- allmän dålig känsla,
- ovanliga tankar eller beteende,
- anfall (kramper), eller
- en allvarlig hudreaktion.
För att minska utvecklingen av läkemedelsresistenta bakterier och bibehålla effektiviteten hos MINOCIN® Oral Suspension och andra antibakteriella läkemedel, bör MINOCIN Oral Suspension endast användas för att behandla eller förebygga infektioner som är bevisade eller starkt misstänkta vara orsakade av bakterier.
BESKRIVNING
MINOCIN 100mg minocyklinhydroklorid, är ett semisyntetiskt derivat av tetracyklin, 4,7Bis(dimetylamino)-1,4,4a,5,5a,6,11,12a-oktahydro-3,10,12,12a-tetrahydroxi-1,11 -dioxo-2-naftacenkarboxamidmonohydroklorid.
Dess strukturformel är:
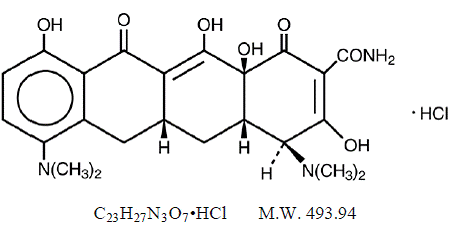 C23H27N3O7•HCl MW 493,94
C23H27N3O7•HCl MW 493,94 MINOCIN 50 mg oral suspension innehåller minocyklinhydroklorid motsvarande 50 mg minocyklin per 5 ml (10 mg/ml) och följande inaktiva ingredienser: alkohol, butylparaben, kalciumhydroxid, cellulosa, dekaglyceryltetraoleat, edetatkalciumgummi-dinatrium, sorbatkalciumg80, , Propylparaben, propylenglykol, natriumsackarin, natriumsulfit (se VARNINGAR ) och sorbitol.
INDIKATIONER
MINOCIN 100 mg oral suspension är indicerat för behandling av följande infektioner på grund av känsliga stammar av de angivna mikroorganismerna:
Rocky Mountain fläckfeber, tyfusfeber och tyfusgruppen, Q-feber, rickettsialpox och fästingfeber orsakade av rickettsiae.
Luftvägsinfektioner orsakade av Mycoplasma pneumoniae.
Lymphogranuloma venereum orsakat av Chlamydia trachomatis.
Psittacosis (Ornithosis) på grund av Chlamydophila psittaci.
Trakom orsakat av Chlamydia trachomatis, även om smittämnet inte alltid elimineras, enligt immunfluorescens.
Inklusionskonjunktivit orsakad av Chlamydia trachomatis.
Nongonokock uretrit, endocervikala eller rektala infektioner hos vuxna orsakade av Ureaplasma urealyticum eller Chlamydia trachomatis.
Återfallande feber på grund av Borrelia recurrentis.
Chancroid orsakad av Haemophilus ducreyi.
Pest på grund av Yersinia pestis.
Tularemi på grund av Francisella tularensis.
Kolera orsakad av Vibrio cholerae.
Campylobacter fetus infektioner orsakade av Campylobacter fetus.
Brucellos på grund av Brucella-arter (i kombination med streptomycin).
Bartonellos på grund av Bartonella bacilliformis.
Granuloma inguinale orsakad av Klebsiella granulomatis.
Minocyklin är indicerat för behandling av infektioner orsakade av följande gramnegativa mikroorganismer när bakteriologiska tester indikerar lämplig mottaglighet för läkemedlet:
Escherichia coli.
Enterobacter aerogenes.
Shigella art.
Acinetobacter arter.
Luftvägsinfektioner orsakade av Haemophilus influenzae.
Luftvägs- och urinvägsinfektioner orsakade av Klebsiella-arter.
MINOCIN Oral Suspension är indicerat för behandling av infektioner orsakade av följande grampositiva mikroorganismer när bakteriologiska tester indikerar lämplig känslighet för läkemedlet:
Övre luftvägsinfektioner orsakade av Streptococcus pneumoniae. Hud- och hudstrukturinfektioner orsakade av Staphylococcus aureus (notera: Minocyklin är inte det valda läkemedlet vid behandling av någon typ av stafylokockinfektion).
När penicillin är kontraindicerat är minocyklin ett alternativt läkemedel för behandling av följande infektioner:
Okomplicerad uretrit hos män på grund av Neisseria gonorrhoeae och för behandling av andra gonokockinfektioner.
Infektioner hos kvinnor orsakade av Neisseria gonorrhoeae.
Syfilis orsakad av Treponema pallidum underart pallidum.
Yaws orsakade av Treponema pallidum underart pertenue.
Listerios på grund av Listeria monocytogenes.
Mjältbrand på grund av Bacillus anthracis.
Vincents infektion orsakad av Fusobacterium fusiforme.
Aktinomykos orsakad av Actinomyces israelii.
Infektioner orsakade av Clostridium-arter.
Vid akut intestinal amebiasis kan minocyklin vara ett användbart komplement till amebicider.
Vid svår akne kan minocyklin vara användbar tilläggsterapi.
Oralt minocyklin är indicerat för behandling av asymtomatiska bärare av Neisseria meningitidis för att eliminera meningokocker från nasofarynx. För att bevara användbarheten av minocyklin vid behandling av asymtomatiska meningokockbärare, bör diagnostiska laboratorieförfaranden, inklusive serotypning och känslighetstestning, utföras för att fastställa bärartillståndet och korrekt behandling. Det rekommenderas att profylaktisk användning av minocyklin reserveras för situationer där risken för meningokock meningit är hög.
Oral Minocyklin är inte indicerat för behandling av meningokockinfektion.
Även om inga kontrollerade kliniska effektstudier har utförts, visar begränsade kliniska data att oral minocyklinhydroklorid har använts framgångsrikt vid behandling av infektioner orsakade av Mycobacterium marinum.
För att minska utvecklingen av läkemedelsresistenta bakterier och bibehålla effektiviteten av MINOCIN 100mg oral suspension och andra antibakteriella läkemedel, ska MINOCIN oral suspension endast användas för att behandla eller förebygga infektioner som är bevisade eller starkt misstänkta orsakas av känsliga bakterier. När information om odling och känslighet finns tillgänglig bör de övervägas vid val eller modifiering av antibakteriell terapi. I avsaknad av sådana data kan lokal epidemiologi och känslighetsmönster bidra till det empiriska valet av terapi.
DOSERING OCH ADMINISTRERING
DEN VANLIGA DOSERINGEN OCH FREKVENSEN FÖR ADMINISTRERING AV MINOCYKLIN SKILLER FRÅN DEN FÖR ANDRA TETRACYKLINER. ÖKAD FÖREKOMST AV BIVERKNINGAR OM DEN REKOMMENDERADE DOSERINGEN ÖVERskrids.
Behandlingen ska fortsätta i minst 24 till 48 timmar efter att symtomen och febern har avtagit.
Studier hittills har visat att absorptionen av MINOCIN Oral Suspension inte påverkas särskilt av livsmedel och mejeriprodukter.
Farmakokinetiken för minocyklin hos patienter med nedsatt njurfunktion (CLCR VARNINGAR ).
Vid behandling av streptokockinfektioner bör en terapeutisk dos av tetracyklin ges under minst tio dagar.
För pediatriska patienter över 8 år
Vanlig pediatrisk dos av MINOCIN är 4 mg/kg initialt följt av 2 mg/kg var 12:e timme, för att inte överskrida den vanliga vuxendosen.
Vuxna
Den vanliga dosen av MINOCIN är 200 mg initialt följt av 100 mg var 12:e timme.
För behandling av syfilis bör den vanliga dosen av MINOCIN administreras under en period av 10 till 15 dagar. Noggrann uppföljning, inklusive laboratorietester, rekommenderas.
Gonorrépatienter som är känsliga för penicillin kan behandlas med MINOCIN 50 mg, administrerat som 200 mg initialt, följt av 100 mg var 12:e timme i minst 4 dagar, med odlingar efter behandling inom 2 till 3 dagar.
Vid behandling av meningokockbärartillstånd är den rekommenderade dosen 100 mg var 12:e timme i 5 dagar.
Mycobacterium marinum-infektioner: Även om optimala doser inte har fastställts, har 100 mg var 12:e timme i 6 till 8 veckor använts framgångsrikt i ett begränsat antal fall.
Okomplicerad urinrörsinfektion, endocervikal eller rektal infektion hos vuxna orsakad av Chlamydia trachomatis eller Ureaplasma urealyticum: 100 mg oralt, var 12:e timme i minst 7 dagar.
Vid behandling av okomplicerad gonokockuretrit hos män rekommenderas 100 mg två gånger dagligen oralt i 5 dagar.
HUR LEVERERAS
MINOCIN (minocyklinhydroklorid) Oral suspension innehåller minocyklinhydroklorid motsvarande 50 mg minocyklin per tesked (5 ml). Konserverad med propylparaben 0,10 % och butylparaben 0,06 % med alkohol USP 5 % v/v. Vaniljsåssmak.
NDC 16781-473-60 - Flaska 2 fl. Uns. (60 ml)
Förvara vid kontrollerad rumstemperatur 20° till 25°C (68° till 77°F).
FRYS INTE.
Tillverkad för: Onset Dermatologics, LLC Cumberland, RI 02864. Reviderad: nov 2018
BIEFFEKTER
På grund av oralt minocyklins praktiskt taget fullständiga absorption har biverkningar på nedre tarmen, särskilt diarré, varit sällsynta. Följande biverkningar har observerats hos patienter som får tetracykliner.
Kroppen som helhet: Feber och missfärgning av sekret.
Gastrointestinala: Anorexi, illamående, kräkningar, diarré, dyspepsi, stomatit, glossit, dysfagi, emaljhypoplasi, enterokolit, pseudomembranös kolit, pankreatit, inflammatoriska lesioner (med monilial överväxt) i de orala och anogenitala regionerna.
Genitourinära: Vulvovaginit.
Levertoxicitet: Hyperbilirubinemi, leverkolestas, ökningar av leverenzymer, dödlig leversvikt och gulsot. Hepatit, inklusive autoimmun hepatit, och leversvikt har rapporterats (se FÖRSIKTIGHETSÅTGÄRDER ).

Hud: Alopeci, erythema nodosum, hyperpigmentering av naglar, klåda, giftig epidermal nekrolys, vaskulit, makulopapulära utslag och erytematösa utslag. Exfoliativ dermatit har rapporterats. Fasta läkemedelsutbrott, inklusive balanit, har rapporterats. Erythema multiforme och Stevens-Johnsons syndrom har rapporterats. Fotosensitivitet diskuteras ovan (se VARNINGAR ). Pigmentering av hud och slemhinnor har rapporterats.
Andningsvägar: Hosta, dyspné, bronkospasm, exacerbation av astma och lunginflammation.
Renal toxicitet: Interstitiell nefrit. Förhöjningar i BUN har rapporterats och är uppenbarligen dosrelaterade (se VARNINGAR ). Reversibel akut njursvikt har rapporterats.
Muskuloskeletala: Artralgi, artrit, benmissfärgning, myalgi, stelhet i lederna och svullnad i lederna.
Överkänslighetsreaktioner: Urtikaria, angioneurotiskt ödem, polyartralgi, anafylaxi/anafylaktoid reaktion (inklusive chock och dödsfall), anafylaktoid purpura, myokardit, perikardit, exacerbation av systemisk lupus erythematosus och lunginfiltrat med eosinofili har rapporterats. Ett övergående lupusliknande syndrom och serumsjukeliknande reaktioner har också rapporterats.
Blod: Agranulocytos, hemolytisk anemi, trombocytopeni, leukopeni, neutropeni, pancytopeni och eosinofili har rapporterats.
Centrala nervsystemet: Kramper, yrsel, hypestesi, parestesi, sedering och svindel. Pseudotumor cerebri (benign intrakraniell hypertoni) hos vuxna och utbuktande fontaneller hos spädbarn (se FÖRSIKTIGHETSÅTGÄRDER - Allmän ). Huvudvärk har också rapporterats.
Övrig: Sköldkörtelcancer har rapporterats efter marknadsföring i samband med minocyklinprodukter. När minocyklinbehandling ges under längre perioder bör övervakning av tecken på sköldkörtelcancer övervägas. När tetracykliner ges under längre perioder har det rapporterats producera brunsvart mikroskopisk missfärgning av sköldkörteln. Fall av onormal sköldkörtelfunktion har rapporterats.
Tandmissfärgning hos barn under 8 år (se VARNINGAR ) och även hos vuxna har rapporterats.
Missfärgning av munhålan (inklusive tunga, läpp och tandkött) har rapporterats.
Tinnitus och nedsatt hörsel har rapporterats hos patienter på MINOCIN (minocyklinhydroklorid).
Följande syndrom har rapporterats. I vissa fall som involverar dessa syndrom har dödsfall rapporterats. Som med andra allvarliga biverkningar, om något av dessa syndrom upptäcks, ska läkemedlet avbrytas omedelbart:
Överkänslighetssyndrom bestående av kutan reaktion (såsom hudutslag eller exfoliativ dermatit), eosinofili och en eller flera av följande: hepatit, pneumonit, nefrit, myokardit och perikardit. Feber och lymfadenopati kan förekomma.
Lupus-liknande syndrom som består av positiv antinukleär antikropp; artralgi, artrit, ledstelhet eller ledsvullnad; och en eller flera av följande: feber, myalgi, hepatit, hudutslag och vaskulit.
Serumsjukeliknande syndrom som består av feber; urtikaria eller utslag; och artralgi, artrit, ledstelhet eller ledsvullnad och lymfadenopati. Eosinofili kan förekomma.
För att rapportera MISSTÄNKTA BIVERKNINGAR, kontakta Valeant Pharmaceuticals North America LLC på 1-800-321-4576 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
LÄKEMEDELSINTERAKTIONER
Eftersom tetracykliner har visat sig sänka plasmaprotrombinaktiviteten kan patienter som behandlas med antikoagulantia behöva justera ned dosen av antikoagulantia.
Eftersom bakteriostatiska läkemedel kan störa den bakteriedödande effekten av penicillin, är det tillrådligt att undvika att ge läkemedel av tetracyklinklass tillsammans med penicillin.
Absorptionen av tetracykliner försämras av antacida som innehåller aluminium, kalcium eller magnesium och preparat som innehåller järn.
Samtidig användning av tetracyklin och metoxifluran har rapporterats leda till dödlig njurtoxicitet.
Samtidig användning av tetracykliner och p-piller kan göra p-piller mindre effektiva.
Administrering av isotretinoin bör undvikas kort före, under och kort efter minocyklinbehandling. Varje läkemedel ensamt har associerats med pseudotumor cerebri (se FÖRSIKTIGHETSÅTGÄRDER ).
Ökad risk för ergotism när ergotalkaloider eller deras derivat ges tillsammans med tetracykliner.
VARNINGAR
Tandutveckling
MINOCIN Oral Suspension, liksom andra antibiotika av tetracyklinklass, kan orsaka fosterskador när det ges till en gravid kvinna. Om något tetracyklin används under graviditeten eller om patienten blir gravid medan du tar dessa läkemedel, bör patienten informeras om den potentiella faran för fostret. Användning av läkemedel av tetracyklinklassen under tandutveckling (sista halvan av graviditeten, spädbarnsåldern och barndomen till 8 års ålder) kan orsaka permanent missfärgning av tänderna (gul-grå-brun).
Denna biverkning är vanligare under långvarig användning av läkemedlet men har observerats efter upprepade korttidskurer. Emaljhypoplasi har också rapporterats. Tetracyklinläkemedel bör därför inte användas under tandutveckling om inte andra läkemedel sannolikt inte är effektiva eller är kontraindicerade.
Skelettutveckling
Alla tetracykliner bildar ett stabilt kalciumkomplex i vilken benbildande vävnad som helst. En minskning av fibulans tillväxthastighet har observerats hos prematura spädbarn som fått oralt tetracyklin i doser på 25 mg/kg var sjätte timme. Denna reaktion visade sig vara reversibel när läkemedlet avbröts.
Använd under graviditet
Resultat från djurstudier tyder på att tetracykliner passerar placentan, finns i fostervävnad och kan ha toxiska effekter på fostret under utveckling (ofta relaterat till försenad skelettutveckling). Bevis på embryotoxicitet har noterats hos djur som behandlats tidigt i dräktigheten. Säkerheten för MINOCIN för användning under graviditet har inte fastställts.
Dermatologisk reaktion
Läkemedelsutslag med eosinofili och systemiska symtom (DRESS) inklusive dödliga fall har rapporterats vid användning av minocyklin. Om detta syndrom upptäcks ska läkemedlet avbrytas omedelbart.
Antianabol verkan
Tetracyklinernas antianabola verkan kan orsaka en ökning av BUN. Även om detta inte är ett problem hos personer med normal njurfunktion, kan högre serumnivåer av tetracyklin hos patienter med signifikant försämrad funktion leda till azotemi, hyperfosfatemi och acidos. Under sådana förhållanden rekommenderas övervakning av kreatinin och BUN, och den totala dagliga dosen bör inte överstiga 200 mg på 24 timmar (se DOSERING OCH ADMINISTRERING ). Om nedsatt njurfunktion finns kan även vanliga orala eller parenterala doser leda till systemisk ackumulering av läkemedlet och möjlig levertoxicitet.
Ljuskänslighet
Ljuskänslighet manifesterad av en överdriven solbränna reaktion har observerats hos vissa individer som tar tetracykliner. Detta har rapporterats med minocyklin.
Effekter på centrala nervsystemet
Biverkningar på centrala nervsystemet inklusive yrsel, yrsel eller svindel har rapporterats med minocyklinbehandling. Patienter som upplever dessa symtom bör varnas för att köra fordon eller använda farliga maskiner under minocyklinbehandling. Dessa symtom kan försvinna under behandlingen och försvinner vanligtvis snabbt när läkemedlet avbryts.
Clostridium Difficile associerad diarré
Clostridium difficile associerad diarré (CDAD) har rapporterats vid användning av nästan alla antibakteriella medel, inklusive MINOCIN 50 mg, och kan variera i svårighetsgrad från mild diarré till fatal kolit. Behandling med antibakteriella medel förändrar den normala floran i tjocktarmen vilket leder till överväxt av C. difficile.
C. difficile producerar toxiner A och B som bidrar till utvecklingen av CDAD. Hypertoxinproducerande stammar av C. difficile orsakar ökad sjuklighet och mortalitet, eftersom dessa infektioner kan vara motståndskraftiga mot antimikrobiell terapi och kan kräva kolektomi. CDAD måste övervägas hos alla patienter som får diarré efter antibiotikaanvändning. Noggrann medicinsk historia är nödvändig eftersom CDAD har rapporterats inträffa mer än två månader efter administrering av antibakteriella medel.
Om CDAD misstänks eller bekräftas kan pågående antibiotikaanvändning som inte är riktad mot C. difficile behöva avbrytas. Lämplig vätske- och elektrolythantering, proteintillskott, antibiotikabehandling av C. difficile och kirurgisk utvärdering bör sättas in efter klinisk indikation.
Överkänslighet mot natriumsulfit
MINOCIN Oral Suspension innehåller natriumsulfit, en sulfit som kan orsaka allergiska reaktioner inklusive anafylaktiska symtom och livshotande eller mindre allvarliga astmatiska episoder hos vissa känsliga personer. Den totala prevalensen av sulfitkänslighet i den allmänna befolkningen är okänd och troligen låg. Sulfitkänslighet ses oftare hos astmatiker än hos personer som inte har astma.
Intrakraniell hypertoni
Intrakraniell hypertoni (IH, pseudotumor cerebri) har associerats med användning av tetracykliner inklusive MINOCIN. Kliniska manifestationer av IH inkluderar huvudvärk, suddig syn, dubbelsidighet och synförlust; papillödem kan hittas på fundoskopi. Kvinnor i fertil ålder som är överviktiga eller har en historia av IH löper större risk att utveckla tetracyklinassocierad IH. Samtidig användning av isotretinoin och MINOCIN bör undvikas eftersom isotretinoin också är känt för att orsaka pseudotumor cerebri.
Även om IH vanligtvis försvinner efter avslutad behandling, finns möjligheten för permanent synförlust. Om visuella symtom utvecklas under behandlingen är omedelbar oftalmologisk utvärdering motiverad. Eftersom det intrakraniella trycket kan förbli förhöjt i veckor efter att läkemedlet avslutats bör patienterna övervakas tills de stabiliseras.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Som med andra antibiotikapreparat kan användning av detta läkemedel resultera i överväxt av icke-mottagliga organismer, inklusive svampar. Om superinfektion inträffar ska antibiotikabehandlingen avbrytas och lämplig behandling inledas.
Hepatotoxicitet har rapporterats med minocyklin; därför bör minocyklin användas med försiktighet till patienter med nedsatt leverfunktion och i kombination med andra hepatotoxiska läkemedel.
Snitt och dränering eller andra kirurgiska ingrepp bör utföras i samband med antibiotikabehandling när så är indicerat.
Att förskriva MINOCIN oral suspension i frånvaro av en bevisad eller starkt misstänkt bakterieinfektion eller en profylaktisk indikation kommer sannolikt inte att ge patienten någon nytta och ökar risken för utveckling av läkemedelsresistenta bakterier.
Laboratorietester
Regelbundna laboratorieutvärderingar av organsystem, inklusive hematopoetiska, njur- och lever, bör utföras.
Alla patienter med gonorré bör ha ett serologiskt test för syfilis vid tidpunkten för diagnosen. Patienter som behandlas med minocyklin bör göra ett uppföljande serologiskt test för syfilis efter 3 månader.
Interaktioner med läkemedel/laboratorietest
Falska förhöjda katekolaminnivåer i urinen kan förekomma på grund av störning av fluorescenstestet.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Dietadministrering av minocyklin i långtidsstudier av tumörframkallande egenskaper hos råttor resulterade i tecken på produktion av sköldkörteltumör. Minocyklin har också visat sig producera sköldkörtelhyperplasi hos råttor och hundar. Dessutom har det förekommit bevis på onkogen aktivitet hos råttor i studier med ett relaterat antibiotikum, oxytetracyklin (dvs. binjure- och hypofystumörer). På samma sätt, även om mutagenicitetsstudier av minocyklin inte har utförts, har positiva resultat i in vitro däggdjurscellanalyser (dvs. muslymfom och kinesiska hamsterlungceller) rapporterats för relaterade antibiotika (tetracyklinhydroklorid och oxytetracyklin). Segment I (fertilitet och allmän reproduktion) studier har gett bevis för att minocyklin försämrar fertiliteten hos hanråttor.
Graviditet
Risksammanfattning
Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa resultat oavsett läkemedelsexponering. Det finns inga adekvata och välkontrollerade studier på användningen av minocyklin hos gravida kvinnor. Minocyklin, liksom andra antibiotika av tetracyklinklassen, passerar placentan och kan orsaka fosterskador när det administreras till en gravid kvinna. Sällsynta spontana rapporter om medfödda anomalier inklusive lemminskning har rapporterats efter marknadsföring. Endast begränsad information finns tillgänglig om dessa rapporter; därför kan ingen slutsats om orsakssamband fastställas. Om minocyklin används under graviditet eller om patienten blir gravid medan du tar detta läkemedel, bör patienten informeras om den potentiella faran för fostret.
Icke-ratogena effekter: (se VARNINGAR ).
Arbete och leverans
Effekten av tetracykliner på förlossningen och förlossningen är okänd.
Ammande mödrar
Tetracykliner utsöndras i modersmjölk. På grund av risken för allvarliga biverkningar hos ammande spädbarn från tetracyklinerna, bör ett beslut fattas om att avbryta amningen eller avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern (se VARNINGAR ).
Pediatrisk användning
Minocyklin rekommenderas inte för användning till barn under 8 år om inte de förväntade fördelarna med behandlingen uppväger riskerna (se VARNINGAR ).
Geriatrisk användning
Kliniska studier av oralt minocyklin inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion och samtidig sjukdom eller annan läkemedelsbehandling (se VARNINGAR , DOSERING OCH ADMINISTRERING ).
MINOCIN 50 mg oral suspension innehåller 4,3 mg (0,18 mEq) natrium per 5 ml.
ÖVERDOS
De biverkningar som är vanligare vid överdosering är yrsel, illamående och kräkningar.
Ingen specifik antidot för minocyklin är känd.
Vid överdosering, avbryt medicinering, behandla symtomatiskt och sätt in stödjande åtgärder. Minocyklin avlägsnas inte i betydande mängder genom hemodialys eller peritonealdialys.
KONTRAINDIKATIONER
Detta läkemedel är kontraindicerat hos personer som har visat överkänslighet mot någon av tetracyklinerna eller mot någon av komponenterna i produktformuleringen.
KLINISK FARMAKOLOGI
Efter en engångsdos av två 100 mg minocyklin HCl pulverfyllda kapslar administrerade till tio normala vuxna frivilliga, varierade serumnivåerna från 0,74 till 4,45 mcg/ml på 1 timme (genomsnitt 2,24); efter 12 timmar varierade de från 0,34 till 2,36 mcg/ml (genomsnitt 1,25). Serumhalveringstiden efter en engångsdos på 200 mg hos 12 i huvudsak normala frivilliga varierade från 11 till 17 timmar. Hos sju patienter med nedsatt leverfunktion varierade det från 11 till 16 timmar, och hos 5 patienter med nedsatt njurfunktion varierade det från 18 till 69 timmar. Urin- och fekal återhämtning av minocyklin när det administrerades till 12 normala frivilliga var hälften till en tredjedel av andra tetracykliner.
Mikrobiologi
Handlingsmekanism
Tetracyklinerna är främst bakteriostatiska och tros utöva sin antimikrobiella effekt genom att hämma proteinsyntesen. Tetracyklinerna, inklusive minocyklin, har ett liknande antimikrobiellt aktivitetsspektrum mot ett stort antal grampositiva och gramnegativa organismer. Korsresistens hos dessa organismer mot tetracyklin är vanligt.
Antimikrobiell aktivitet
Minocyklin har visat sig vara aktivt mot de flesta stammar av följande mikroorganismer, både in vitro och vid kliniska infektioner som beskrivs i INDIKATIONER sektion:
Gram-positiva bakterier
Bacillus anthracis Listeria monocytogenes Staphylococcus aureus Streptococcus pneumoniae
Gram-negativa bakterier
Bartonella bacilliformis Brucella-arter Klebsiella granulomatis Campylobacter fetus Francisella tularensis Haemophilus ducreyi Vibrio cholerae Yersinia pestis Acinetobacter-arter Enterobacter aerogenes Escherichia coli Haemophilus influenzae Klebsiella-arter Neisiella-arter Neisiella-arter meningeriashoee
Andra mikroorganismer
Actinomyces-arter Borrelia recurrentis Chlamydophila psittaci Chlamydia trachomatis Clostridium-arter Entamoeba-arter Fusobacterium nucleatum underart fusiforme Mycobacterium marinum Mycoplasma pneumoniae Propionibacterium acnes Rickettsiae Treponema pallidum underart pallidum subspecies Ureale subspecies pallidum subspecies Treponplasen
Känslighetstestning
För specifik information om tolkningskriterier för känslighetstest och tillhörande testmetoder och kvalitetskontrollstandarder som erkänns av FDA för detta läkemedel, se: https://www.fda.gov/STIC.
Djurfarmakologi och toxikologi
Minocyklin HCl har observerats orsaka en mörk missfärgning av sköldkörteln hos försöksdjur (råttor, minigrisar, hundar och apor). Hos råtta har kronisk behandling med minocyklinhydroklorid resulterat i struma åtföljd av förhöjt upptag av radioaktivt jod och tecken på produktion av sköldkörteltumör. Minocyklinhydroklorid har också visat sig producera sköldkörtelhyperplasi hos råttor och hundar.
PATIENTINFORMATION
Diarré är ett vanligt problem som orsakas av antibiotika som vanligtvis upphör när antibiotikan avbryts. Ibland kan patienter efter påbörjad behandling med antibiotika utveckla vattnig och blodig avföring (med eller utan magkramper och feber) även så sent som två eller fler månader efter att ha tagit den sista dosen av antibiotikan. Om detta inträffar ska patienter kontakta sin läkare så snart som möjligt.
Ljuskänslighet manifesterad av en överdriven solbränna reaktion har observerats hos vissa individer som tar tetracykliner. Patienter som är benägna att exponeras för direkt solljus eller ultraviolett ljus bör informeras om att denna reaktion kan uppstå med tetracyklinläkemedel, och behandlingen bör avbrytas vid första tecken på huderytem. Denna reaktion har rapporterats vid användning av minocyklin.
Patienter som upplever symtom från centrala nervsystemet bör varnas för att köra fordon eller använda farliga maskiner under minocyklinbehandling (se VARNINGAR ).
Samtidig användning av tetracyklin och orala preventivmedel kan göra p-piller mindre effektiva (se LÄKEMEDELSINTERAKTIONER ).
Patienter bör informeras om att antibakteriella läkemedel inklusive MINOCIN 50 mg oral suspension endast bör användas för att behandla bakterieinfektioner. De behandlar inte virusinfektioner (t.ex. förkylning). När MINOCIN Oral Suspension förskrivs för att behandla en bakteriell infektion, bör patienterna informeras om att även om det är vanligt att må bättre tidigt under behandlingen, bör läkemedlet tas exakt enligt anvisningarna. Att hoppa över doser eller inte fullfölja hela behandlingsförloppet kan (1) minska effektiviteten av den omedelbara behandlingen och (2) öka sannolikheten för att bakterier utvecklar resistens och inte kommer att kunna behandlas med MINOCIN 50 mg oral suspension eller andra antibakteriella läkemedel i framtiden .
Oanvända förråd av tetracyklinantibiotika ska kasseras före utgångsdatumet.
