Cleocin 150mg, 300mg Clindamycin Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Cleocin 300mg hydrokloridkapslar?
Cleocin Hydrochloride Capsules innehåller ett antibiotikum som är indicerat för behandling av allvarliga infektioner orsakade av känsliga anaeroba bakterier. Cleocin 150 mg hydroklorid är också indicerat för behandling av allvarliga infektioner på grund av känsliga stammar av streptokocker, pneumokocker och stafylokocker. Dess användning bör reserveras för penicillinallergiska patienter eller andra patienter för vilka, enligt läkarens bedömning, ett penicillin är olämpligt. Cleocin Hydrochloride är tillgänglig i generisk form.
Vilka är biverkningarna av Cleocin 300mg hydrokloridkapslar?
Vanliga biverkningar av Cleocin Hydrochloride inkluderar:
- Clostridium difficile kolit,
- buksmärtor,
- pseudomembranös kolit,
- esofagit,
- illamående,
- kräkningar,
- diarre,
- hudutslag,
- nässelfeber,
- allvarliga allergiska reaktioner (anafylaxi),
- överkänslighetsreaktioner,
- klåda,
- flytningar och obehag,
- hud svullnad,
- gulnande hud och ögon (gulsot),
- onormala leverfunktionstester och
- ledvärk.
För att minska utvecklingen av läkemedelsresistenta bakterier och bibehålla effektiviteten av CLEOCIN 300mg HCl och andra antibakteriella läkemedel, bör CLEOCIN 300mg HCl endast användas för att behandla eller förebygga infektioner som är bevisade eller starkt misstänkta vara orsakade av bakterier.
VARNING
Clostridium difficile associerad diarré (CDAD) har rapporterats vid användning av nästan alla antibakteriella medel, inklusive CLEOCIN HCl och kan variera i svårighetsgrad från mild diarré till fatal kolit. Behandling med antibakteriella medel förändrar den normala floran i tjocktarmen, vilket leder till överväxt av C. difficle.
Eftersom behandling med CLEOCIN 150 mg HCl har associerats med svår kolit som kan sluta dödligt, bör den reserveras för allvarliga infektioner där mindre toxiska antimikrobiella medel är olämpliga, som beskrivs i INDIKATIONER OCH ANVÄNDNING sektion. Det ska inte användas till patienter med icke-bakteriella infektioner som de flesta övre luftvägsinfektioner.
C. difficle producerar toxiner A och B, som bidrar till utvecklingen av CDAD. Hypertoxinproducerande stammar av C. difficle orsakar ökad sjuklighet och mortalitet, eftersom dessa infektioner kan vara motståndskraftiga mot antimikrobiell behandling och kan kräva kolektomi. CDAD måste övervägas hos alla patienter som får diarré efter antibiotikaanvändning. Noggrann medicinsk historia är nödvändig eftersom CDAD har rapporterats inträffa mer än två månader efter administrering av antibakteriella medel.
Om CDAD misstänks eller bekräftas kan pågående antibiotikaanvändning som inte är riktad mot C. difficle behöva avbrytas. Lämplig vätske- och elektrolythantering, proteintillskott, antibiotikabehandling av C. difficle och kirurgisk utvärdering bör sättas in efter klinisk indikation.
BESKRIVNING
Klindamycinhydroklorid är det hydratiserade hydrokloridsaltet av klindamycin. Klindamycin är ett semisyntetiskt antibiotikum som produceras genom en 7(S)-kloro-substitution av 7(R)-hydroxylgruppen i moderföreningen lincomycin.
CLEOCIN HCl-kapslar innehåller klindamycinhydroklorid motsvarande 75 mg, 150 mg eller 300 mg klindamycin.
Inaktiva ingredienser: 75 mg - majsstärkelse, FD&C blå nr. 1, FD&C gult nr. 5, gelatin, laktos, magnesiumstearat och talk; 150 mg - majsstärkelse, FD&C blå nr. 1, FD&C gult nr. 5, gelatin, laktos, magnesiumstearat, talk och titandioxid; 300 mg - majsstärkelse, FD&C blå nr. 1, gelatin, laktos, magnesiumstearat, talk och titandioxid.
Strukturformeln är representerad nedan:
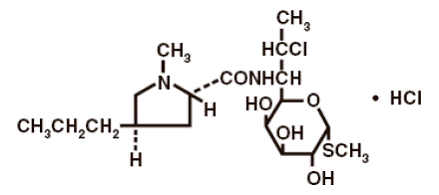
Det kemiska namnet för klindamycinhydroklorid är metyl-7-klor-6,7,8-trideoxi-6-(1-metyl-trans-4-propyl-L-2-pyrrolidinkarboxamido)-1-tio-L-treo-a- D-galakto-oktopyranosidmonohydroklorid.
INDIKATIONER
Klindamycin är indicerat för behandling av allvarliga infektioner orsakade av känsliga anaeroba bakterier.
Klindamycin är också indicerat för behandling av allvarliga infektioner på grund av känsliga stammar av streptokocker, pneumokocker och stafylokocker. Dess användning bör reserveras för penicillinallergiska patienter eller andra patienter för vilka, enligt läkarens bedömning, ett penicillin är olämpligt. På grund av risken för kolit, som beskrivs i VARNING I RUTA, bör läkaren överväga infektionens art och lämpligheten av mindre toxiska alternativ (t.ex. erytromycin) innan du väljer klindamycin.
Anaerober: Allvarliga luftvägsinfektioner såsom empyem, anaerob pneumonit och lungabscess; allvarliga hud- och mjukdelsinfektioner; sepsis; intraabdominala infektioner såsom peritonit och intraabdominal abscess (typiskt härrörande från anaeroba organismer som finns i den normala mag-tarmkanalen); infektioner i det kvinnliga bäckenet och könsorganen såsom endometrit, nongonokock tubo-ovarial abscess, bäckencellulit och postkirurgisk vaginal manschettinfektion.
Streptokocker: Allvarliga luftvägsinfektioner; allvarliga hud- och mjukdelsinfektioner.
Stafylokocker: Allvarliga luftvägsinfektioner; allvarliga hud- och mjukdelsinfektioner.
Pneumokocker: Allvarliga luftvägsinfektioner.
Bakteriologiska studier bör utföras för att fastställa de orsakande organismerna och deras känslighet för klindamycin.
För att minska utvecklingen av läkemedelsresistenta bakterier och bibehålla effektiviteten av CLEOCIN HCl och andra antibakteriella läkemedel, bör CLEOCIN HCl endast användas för att behandla eller förebygga infektioner som är bevisade eller starkt misstänkta vara orsakade av känsliga bakterier. När information om odling och känslighet finns tillgänglig bör de övervägas vid val eller modifiering av antibakteriell terapi. I avsaknad av sådana data kan lokal epidemiologi och känslighetsmönster bidra till det empiriska valet av terapi.
DOSERING OCH ADMINISTRERING
Om betydande diarré uppstår under behandlingen, bör detta antibiotikum avbrytas (se LÅDA VARNING ).
Vuxna
Allvarliga infektioner - 150 till 300 mg var 6:e timme. Svårare infektioner - 300 till 450 mg var 6:e timme.
Pediatriska patienter (för barn som kan svälja kapslar):
Allvarliga infektioner 8 till 16 mg/kg/dag (4 till 8 mg/lb/dag) uppdelat på tre eller fyra lika doser. Svårare infektioner - 16 till 20 mg/kg/dag (8 till 10 mg/lb/dag) uppdelat på tre eller fyra lika doser.
För att undvika risken för irritation i matstrupen bör CLEOCIN 300mg HCl-kapslar tas med ett helt glas vatten.
CLEOCIN HCl-kapslar är inte lämpliga för barn som inte kan svälja dem hela. Kapslarna ger inte exakta mg/kg doser, därför kan det vara nödvändigt att använda clindamycinpalmitat oral lösning i vissa fall.
Allvarliga infektioner på grund av anaeroba bakterier behandlas vanligtvis med CLEOCIN PHOSPHATE® Sterile Solution. Under kliniskt lämpliga omständigheter kan dock läkaren välja att påbörja behandlingen eller fortsätta behandlingen med CLEOCIN 150 mg HCl-kapslar.
I fall av β-hemolytiska streptokockinfektioner bör behandlingen fortsätta i minst 10 dagar.
HUR LEVERERAS
CLEOCIN HCl-kapslar finns i följande styrkor, färger och storlekar:
75 mg Gröna flaskor med 100 st NDC 0009-0331-02
150 mg Ljusblå och gröna flaskor med 100 st NDC 0009-0225-02
300 mg Ljusblå flaskor med 100 st NDC 0009-0395-14
Förvara i kontrollerad rumstemperatur 20° till 25° C (68° till 77° F) [se USP ].
Distribuerat av: Pharmacia & Upjohn Co, Division of Pfizer Inc, NY, NY 10017. Reviderad 2017
BIEFFEKTER
Följande reaktioner har rapporterats vid användning av klindamycin.
Infektioner och angrepp: Clostridium difficile kolit
Gastrointestinala: Buksmärta, pseudomembranös kolit, esofagit, illamående, kräkningar och diarré (se LÅDA VARNING ). Symtom på pseudomembranös kolit kan uppträda under eller efter antibakteriell behandling (se VARNINGAR ). Esofagussår har rapporterats. En obehaglig eller metallisk smak har rapporterats efter oral administrering.
Överkänslighetsreaktioner: Generaliserade milda till måttliga morbilliforma (makulopapulära) hudutslag är de vanligast rapporterade biverkningarna. Vesikulobulösa utslag, såväl som urtikaria, har observerats under läkemedelsbehandling. Allvarliga hudreaktioner såsom toxisk epidermal nekrolys, några med dödlig utgång, har rapporterats (se VARNINGAR ). Fall av akut generaliserad exantematös pustulos (AGEP), erythema multiforme, några som liknar Stevens-Johnsons syndrom, anafylaktisk chock, anafylaktisk reaktion och överkänslighet har också rapporterats.
Hud och slemhinnor: Klåda, vaginit, angioödem och sällsynta fall av exfoliativ dermatit har rapporterats. (Ser Överkänslighetsreaktioner .)
Lever: Gulsot och avvikelser i leverfunktionstester har observerats under behandling med klindamycin.
Njur: Även om inget direkt samband mellan klindamycin och njurskada har fastställts, har njurdysfunktion observerats genom azotemi, oliguri och/eller proteinuri.
Hematopoetisk: Övergående neutropeni (leukopeni) och eosinofili har rapporterats. Rapporter om agranulocytos och trombocytopeni har gjorts. Inget direkt etiologiskt samband med samtidig clindamycinterapi kunde göras i något av det föregående.
Immunförsvar: Läkemedelsreaktioner med eosinofili och systemiska symptom (DRESS) har rapporterats.
Muskuloskeletala: Fall av polyartrit har rapporterats.
LÄKEMEDELSINTERAKTIONER
Klindamycin har visat sig ha neuromuskulärt blockerande egenskaper som kan förstärka verkan av andra neuromuskulära blockerande medel. Därför bör det användas med försiktighet hos patienter som får sådana medel.
Klindamycin metaboliseras huvudsakligen av CYP3A4, och i mindre utsträckning av CYP3A5, till huvudmetaboliten klindamycinsulfoxid och mindre metabolit N-desmetylclindamycin. Därför kan hämmare av CYP3A4 och CYP3A5 öka plasmakoncentrationerna av klindamycin och inducerare av dessa isoenzymer kan minska plasmakoncentrationerna av klindamycin. I närvaro av starka CYP3A4-hämmare, övervaka för biverkningar. I närvaro av starka CYP3A4-inducerare som rifampicin, kontrollera för förlust av effektivitet.
In vitro-studier indikerar att klindamycin inte hämmar CYP1A2, CYP2C9, CYP2C19, CYP2E1 eller CYP2D6 och endast måttligt hämmar CYP3A4.
Antagonism har visats mellan klindamycin och erytromycin in vitro. På grund av möjlig klinisk betydelse bör dessa två läkemedel inte administreras samtidigt.
VARNINGAR
Ser LÅDA VARNING
Clostridium Difficile associerad diarré
Clostridium difficile associerad diarré (CDAD) har rapporterats vid användning av nästan alla antibakteriella medel, inklusive CLEOCIN 300 mg HCl, och kan variera i svårighetsgrad från mild diarré till fatal kolit. Behandling med antibakteriella medel förändrar den normala floran i tjocktarmen, vilket leder till överväxt av C. difficle.
C. difficle producerar toxiner A och B, som bidrar till utvecklingen av CDAD. Hypertoxinproducerande stammar av C. difficle orsakar ökad sjuklighet och mortalitet, eftersom dessa infektioner kan vara motståndskraftiga mot antimikrobiell behandling och kan kräva kolektomi. CDAD måste övervägas hos alla patienter som får diarré efter antibiotikaanvändning. Noggrann medicinsk historia är nödvändig eftersom CDAD har rapporterats inträffa mer än två månader efter administrering av antibakteriella medel.
Om CDAD misstänks eller bekräftas kan pågående antibiotikaanvändning som inte är riktad mot C. difficle behöva avbrytas. Lämplig vätske- och elektrolythantering, proteintillskott, antibiotikabehandling av C. difficle och kirurgisk utvärdering bör sättas in efter klinisk indikation.
Anafylaktiska och svåra överkänslighetsreaktioner
Anafylaktisk chock och anafylaktiska reaktioner har rapporterats (se NEGATIVA REAKTIONER ).
Allvarliga överkänslighetsreaktioner, inklusive allvarliga hudreaktioner såsom toxisk epidermal nekrolys (TEN), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) och Stevens-Johnsons syndrom (SJS), några med dödlig utgång, har rapporterats (se NEGATIVA REAKTIONER ).
I händelse av en sådan anafylaktisk eller allvarlig överkänslighetsreaktion, avbryt behandlingen permanent och sätt in lämplig behandling.
En noggrann utredning bör göras angående tidigare känslighet för läkemedel och andra allergener.
Användning vid meningit
Eftersom klindamycin inte diffunderar tillräckligt in i cerebrospinalvätskan bör läkemedlet inte användas vid behandling av meningit.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Genomgång av hittillsvarande erfarenheter tyder på att en undergrupp av äldre patienter med tillhörande svår sjukdom kan tolerera diarré sämre. När klindamycin är indicerat till dessa patienter, bör de övervakas noggrant med avseende på förändringar i tarmfrekvens.
CLEOCIN 300mg HCl bör förskrivas med försiktighet till personer med en historia av gastrointestinala sjukdomar, särskilt kolit.
CLEOCIN 300mg HCl bör förskrivas med försiktighet till atopiska individer.
Indikerade kirurgiska ingrepp bör utföras i samband med antibiotikabehandling.
Användningen av CLEOCIN 150mg HCl resulterar ibland i överväxt av okänsliga organismer, särskilt jästsvampar. Om superinfektioner inträffar bör lämpliga åtgärder vidtas enligt den kliniska situationen.
Dosjustering av klindamycin är kanske inte nödvändig hos patienter med njursjukdom. Hos patienter med måttlig till svår leversjukdom har förlängd halveringstid för klindamycin konstaterats. Emellertid postulerades det från studier att när det ges var åttonde timme, skulle ackumulering sällan inträffa. Därför är det kanske inte nödvändigt med dosjustering hos patienter med leversjukdom. Emellertid bör periodiska leverenzymbestämningar göras vid behandling av patienter med allvarlig leversjukdom.
Kapslarna på 75 mg och 150 mg innehåller FD&C gult nr. 5 (tartrazin), som kan orsaka allergiska reaktioner (inklusive bronkial astma) hos vissa känsliga individer. Även om den totala förekomsten av FD&C gult nr. 5 (tartrazin)-känsligheten i den allmänna befolkningen är låg, den ses ofta hos patienter som också har aspirinöverkänslighet.
Att förskriva CLEOCIN 150 mg HCl i frånvaro av en bevisad eller starkt misstänkt bakterieinfektion eller en profylaktisk indikation kommer sannolikt inte att ge patienten någon nytta och ökar risken för utveckling av läkemedelsresistenta bakterier.
Laboratorietester
Under långvarig behandling bör periodiska lever- och njurfunktionstester och blodvärden utföras.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Långtidsstudier på djur har inte utförts med klindamycin för att utvärdera karcinogen potential. Genotoxicitetstester som utfördes inkluderade ett mikrokärntest på råtta och ett Ames Salmonella-reversionstest. Båda testerna var negativa.
Fertilitetsstudier på råttor som behandlats oralt med upp till 300 mg/kg/dag (cirka 1,6 gånger den högsta rekommenderade dosen för vuxna baserat på mg/m²) visade inga effekter på fertilitet eller parningsförmåga.
Graviditet
Teratogena effekter
I kliniska prövningar med gravida kvinnor har systemisk administrering av klindamycin under andra och tredje trimestern inte associerats med en ökad frekvens av medfödda avvikelser.
Klindamycin ska endast användas under graviditetens första trimester om det är absolut nödvändigt. Det finns inga adekvata och välkontrollerade studier på gravida kvinnor under graviditetens första trimester. Eftersom reproduktionsstudier på djur inte alltid förutsäger det mänskliga svaret, bör detta läkemedel endast användas under graviditet om det verkligen behövs.
Reproduktionsstudier utförda på råttor och möss med orala doser av klindamycin upp till 600 mg/kg/dag (3,2 respektive 1,6 gånger den högsta rekommenderade dosen för vuxna baserat på mg/m²) eller subkutana doser av klindamycin upp till 250 mg/kg /dag (1,3 respektive 0,7 gånger den högsta rekommenderade dosen för vuxna baserat på mg/m²) visade inga tecken på teratogenicitet.
Ammande mödrar
Klindamycin har rapporterats förekomma i bröstmjölk i intervallet 0,7 till 3,8 mcg/ml. Klindamycin har potential att orsaka negativa effekter på det ammade barnets mag-tarmflora. Om oralt eller intravenöst klindamycin krävs av en ammande mamma är det ingen anledning att avbryta amningen, men ett alternativt läkemedel kan vara att föredra. Övervaka barnet för eventuella negativa effekter på mag-tarmfloran, såsom diarré, candidiasis (trast, blöjutslag) eller sällan blod i avföringen som indikerar möjlig antibiotikarelaterad kolit.
De utvecklingsmässiga och hälsomässiga fördelarna med amning bör beaktas tillsammans med moderns kliniska behov av klindamycin och eventuella negativa effekter på det ammade barnet från klindamycin eller från det underliggande moderns tillståndet.
Pediatrisk användning
När CLEOCIN 300 mg HCl administreras till den pediatriska populationen (födelse till 16 år), är lämplig övervakning av organsystemfunktioner önskvärt.
Geriatrisk användning
Kliniska studier av klindamycin inkluderade inte tillräckligt många patienter i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre patienter. Andra rapporterade kliniska erfarenheter tyder dock på att antibiotikarelaterad kolit och diarré (på grund av Clostridium difficile) som ses i samband med de flesta antibiotika förekommer oftare hos äldre (> 60 år) och kan vara mer allvarliga. Dessa patienter bör övervakas noggrant med avseende på utveckling av diarré.
Farmakokinetiska studier med klindamycin har inte visat några kliniskt viktiga skillnader mellan unga och äldre patienter med normal leverfunktion och normal (åldersjusterad) njurfunktion efter oral eller intravenös administrering.
ÖVERDOS
Signifikant dödlighet observerades hos möss vid en intravenös dos på 855 mg/kg och hos råttor vid en oral eller subkutan dos på cirka 2618 mg/kg. Hos mössen observerades kramper och depression.
Hemodialys och peritonealdialys är inte effektiva för att avlägsna klindamycin från serumet.
KONTRAINDIKATIONER
CLEOCIN 150mg HCl är kontraindicerat hos personer med en historia av överkänslighet mot preparat som innehåller klindamycin eller lincomycin.
KLINISK FARMAKOLOGI
Human farmakologi
Absorption
Serumnivåstudier med en 150 mg oral dos av klindamycinhydroklorid hos 24 normala vuxna frivilliga visade att klindamycin absorberades snabbt efter oral administrering. En genomsnittlig toppserumnivå på 2,50 mcg/ml nåddes på 45 minuter; serumnivåerna var i genomsnitt 1,51 mcg/ml efter 3 timmar och 0,70 mcg/ml efter 6 timmar. Absorptionen av en oral dos är praktiskt taget fullständig (90 %), och samtidig administrering av mat förändrar inte serumkoncentrationerna nämnvärt; serumnivåerna har varit enhetliga och förutsägbara från person till person och dos till dos. Serumnivåstudier efter flera doser av CLEOCIN 150 mg HCl i upp till 14 dagar visar inga tecken på ackumulering eller förändrad metabolism av läkemedel. Doser på upp till 2 gram klindamycin per dag i 14 dagar har tolererats väl av friska frivilliga, förutom att förekomsten av gastrointestinala biverkningar är större med de högre doserna.
Distribution
Koncentrationerna av klindamycin i serumet ökade linjärt med ökad dos. Serumnivåerna överstiger MIC (minimum hämmande koncentration) för de flesta indikerade organismer i minst sex timmar efter administrering av de vanligtvis rekommenderade doserna. Klindamycin är brett distribuerat i kroppsvätskor och vävnader (inklusive ben). Inga signifikanta nivåer av klindamycin uppnås i cerebrospinalvätskan, även i närvaro av inflammerade hjärnhinnor.
Ämnesomsättning
In vitro-studier på humana lever- och tarmmikrosomer indikerade att klindamycin huvudsakligen metaboliseras av Cytokrom P450 3A4 (CYP3A4), med mindre bidrag från CYP3A5, för att bilda klindamycinsulfoxid och en mindre metabolit, N-desmetylklindamycin.
Exkretion
Den genomsnittliga biologiska halveringstiden är 2,4 timmar. Cirka 10 % av bioaktiviteten utsöndras i urinen och 3,6 % i avföringen; resten utsöndras som bioinaktiva metaboliter.
Särskilda populationer
Nedsatt njurfunktion
Serumhalveringstid för klindamycin ökar något hos patienter med markant nedsatt njurfunktion. Hemodialys och peritonealdialys är inte effektiva för att avlägsna klindamycin från serumet.
Används hos äldre
Farmakokinetiska studier på äldre frivilliga (61-79 år) och yngre vuxna (18-39 år) indikerar att enbart ålder inte förändrar klindamycins farmakokinetik (clearance, halveringstid för eliminering, distributionsvolym och area under serumkoncentration-tidskurvan) ) efter IV-administrering av klindamycinfosfat. Efter oral administrering av klindamycinhydroklorid ökas eliminationshalveringstiden till cirka 4,0 timmar (intervall 3,4-5,1 timmar) hos äldre jämfört med 3,2 timmar (intervall 2,1-4,2 timmar) hos yngre vuxna. Absorptionsgraden skiljer sig dock inte åt mellan åldersgrupperna och ingen dosförändring är nödvändig för äldre med normal leverfunktion och normal (åldersanpassad) njurfunktion1.
Mikrobiologi
Handlingsmekanism
Klindamycin hämmar bakteriell proteinsyntes genom att binda till 23S RNA från 50S subenheten av ribosomen. Klindamycin är bakteriostatiskt.
Motstånd
Resistens mot klindamycin orsakas oftast av modifiering av specifika baser av 23S ribosomalt RNA. Korsresistens mellan klindamycin och linkomycin är fullständig. Eftersom bindningsställena för dessa antibakteriella läkemedel överlappar, observeras ibland korsresistens bland linkosamider, makrolider och streptogramin B. Makrolidinducerbar resistens mot klindamycin förekommer i vissa isolat av makrolidresistenta bakterier. Makrolidresistenta isolat av stafylokocker och beta-hemolytiska streptokocker bör screenas för induktion av klindamycinresistens med D-zontestet.
Antimikrobiell aktivitet
Klindamycin har visat sig vara aktivt mot de flesta isolaten av följande mikroorganismer, både in vitro och vid kliniska infektioner, som beskrivs i INDIKATIONER OCH ANVÄNDNING sektion.
Grampositiva bakterier
Staphylococcus aureus (meticillinkänsliga stammar) Streptococcus pneumoniae (penicillinkänsliga stammar) Streptococcus pyogenes
Anaeroba bakterier
Clostridium perfringens Fusobacterium necrophorum Fusobacterium nucleatum Peptostreptococcus anaerobius Prevotella melaninogenica
Minst 90 % av mikroorganismerna listade nedan uppvisar in vitro lägsta hämmande koncentrationer (MIC) som är mindre än eller lika med den klindamycinkänsliga MIC-brytpunkten för organismer av liknande typ som de som visas i tabell 1. Effekten av klindamycin vid behandling av klinisk infektioner på grund av dessa mikroorganismer har inte fastställts i adekvata och välkontrollerade kliniska prövningar.
Grampositiva bakterier
Staphylococcus epidermidis (meticillinkänsliga stammar) Streptococcus agalactiae Streptococcus anginosus Streptococcus mitis Streptococcus oralis
Anaeroba bakterier
Actinomyces israelii Clostridium clostridioforme Eggertella lenta Finegoldia (Peptostreptococcus) magna Micromonas (Peptostreptokocker) micros Prevotella bivia Prevotella intermedia Propionibacterium acnes
Testmetoder för känslighet
När det är tillgängligt bör det kliniska mikrobiologiska laboratoriet tillhandahålla kumulativa in vitro-känslighetstestresultat för antimikrobiella läkemedel som används på lokala sjukhus och övningsområden till läkaren som periodiska rapporter som beskriver känslighetsprofilen för nosokomiala och samhällsförvärvade patogener. Dessa rapporter bör hjälpa läkaren att välja ett antibakteriellt läkemedel för behandling.
Spädningstekniker
Kvantitativa metoder används för att bestämma antimikrobiella minimiinhibitoriska koncentrationer (MIC). Dessa MIC ger uppskattningar av bakteriers känslighet för antimikrobiella föreningar. MIC bör bestämmas med en standardiserad testmetod2,3 (buljong och/eller agar). MIC-värdena ska tolkas enligt kriterierna i tabell 1.
Diffusionstekniker
Kvantitativa metoder som kräver mätning av zondiametrar kan också ge reproducerbara uppskattningar av bakteriers mottaglighet för antimikrobiella föreningar. Zonstorleken bör bestämmas med en standardiserad metod2,5. Denna procedur använder pappersskivor impregnerade med 2 mcg klindamycin för att testa bakteriers känslighet för klindamycin. Diskdiffusionsbrytpunkterna finns i tabell 1.
Anaeroba tekniker
För anaeroba bakterier kan känsligheten för klindamycin bestämmas med en standardiserad testmetod2,4. De erhållna MIC-värdena ska tolkas enligt kriterierna i tabell 1.
En rapport om mottaglig (S ) indikerar att det antimikrobiella läkemedlet sannolikt kommer att hämma tillväxten av patogenen om det antimikrobiella läkemedlet når den koncentration som vanligtvis kan uppnås vid infektionsstället. En rapport av Intermediär (I) indikerar att resultatet bör anses tvetydigt, och om mikroorganismen inte är fullt mottaglig för alternativa, kliniskt genomförbara läkemedel, bör testet upprepas. Denna kategori innebär möjlig klinisk tillämpbarhet på kroppsställen där läkemedlet är fysiologiskt koncentrerat eller i situationer där höga doser av läkemedel kan användas. Denna kategori ger också en buffertzon som förhindrar att små okontrollerade tekniska faktorer orsakar stora tolkningsskillnader. En rapport om resistent (R) indikerar att det antimikrobiella läkemedlet sannolikt inte kommer att hämma tillväxten av patogenen om det antimikrobiella läkemedlet når den koncentration som vanligtvis kan uppnås på infektionsplatsen; annan terapi bör väljas.
Kvalitetskontroll
Standardiserade rutiner för känslighetstest kräver användning av laboratoriekontroller för att övervaka och säkerställa noggrannheten och precisionen hos de tillbehör och reagenser som används i analysen, och teknikerna för de individer som utför testet. 2,3,4,5 Standard klindamycinpulver bör tillhandahålla MIC-intervallen i Tabell 2. För diskdiffusionstekniken med användning av 2 mcg klindamycinskivan bör kriterierna i Tabell 2 uppnås.
anaerober kan testas med antingen buljongmikrospädning eller agarutspädningsmetoder. NA=Ej tillämpligt ATCC® är ett registrerat varumärke som tillhör American Type Culture Collection
REFERENSER
1. Smith RB, Phillips JP: Utvärdering av CLEOCIN HCl och CLEOCIN Fosfat i en åldrad befolkning. Upjohn TR 8147-82-9122-021, december 1982.
2. CLSI. Prestandastandarder för antimikrobiell känslighetstestning: 26:e upplagan. CLSI tillägg M100S. Wayne, PA: Clinical and Laboratory Standards Institute; 2016.
3. CLSI. Metoder för utspädning Antimikrobiella känslighetstester för bakterier som växer aerobt; Godkänd standard - tionde upplagan. CLSI dokument M07-A10. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.
4. CLSI. Metoder för antimikrobiell känslighetstestning av anaeroba bakterier; Godkänd Standard-åttonde upplagan. CLSI dokument M11-A8. Wayne, PA: Clinical and Laboratory Standards Institute; 2012.
5. CLSI. Prestandastandarder för antimikrobiella diskkänslighetstest; Godkänd standard - tolfte upplagan. CLSI dokument M02-A12. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.
PATIENTINFORMATION
Patienter bör informeras om att antibakteriella läkemedel, inklusive CLEOCIN HCl, endast bör användas för att behandla bakterieinfektioner. De behandlar inte virusinfektioner (t.ex. förkylning). När CLEOCIN HCl ordineras för att behandla en bakteriell infektion, bör patienterna få veta att även om det är vanligt att må bättre tidigt under behandlingen, bör läkemedlet tas exakt enligt anvisningarna. Att hoppa över doser eller inte fullfölja hela terapiförloppet kan (1) minska effektiviteten av den omedelbara behandlingen och (2) öka sannolikheten för att bakterier kommer att utveckla resistens och inte kommer att kunna behandlas med CLEOCIN 150mg HCl eller andra antibakteriella läkemedel i framtiden.
Diarré är ett vanligt problem som orsakas av antibiotika som vanligtvis upphör när antibiotikan avbryts. Ibland kan patienter efter påbörjad behandling med antibiotika utveckla vattnig och blodig avföring (med eller utan magkramper och feber) även så sent som två eller fler månader efter att ha tagit den sista dosen av antibiotikan. Om detta inträffar ska patienter kontakta sin läkare så snart som möjligt.
