Zyprexa 2.5mg, 5mg, 7.5mg, 10mg, 15mg, 20mg Olanzapine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Zyprexa 10mg och hur används det?
Zyprexa är ett receptbelagt läkemedel som används för att behandla symptomen på schizofreni och bipolär sjukdom (manodepression). Zyprexa kan användas ensamt eller tillsammans med andra läkemedel.
- Zyprexa tillhör en klass av läkemedel som kallas antipsykotika, 2:a generationens, antimaniska medel.
- Det är inte känt om Zyprexa är säkert och effektivt för barn yngre än 13 år.
Vilka är de möjliga biverkningarna av Zyprexa 15mg?
Zyprexa kan orsaka allvarliga biverkningar inklusive:
- okontrollerade muskelrörelser i ansiktet (tugga, smälla läpparna, rynka pannan, tungrörelser, blinka eller ögonrörelser),
- problem med att tala eller svälja,
- svullnad i händer eller fötter,
- förvirring,
- ovanliga tankar eller beteende,
- hallucinationer,
- tankar om att skada dig själv,
- plötslig svaghet eller dålig känsla,
- feber,
- frossa,
- öm hals,
- svullna tandkött,
- smärtsamma munsår,
- smärta vid sväljning,
- hudsår,
- symtom för förkylning eller influensa,
- hosta,
- känner mig väldigt törstig eller varm,
- oförmåga att urinera,
- kraftig svettning,
- varm eller torr hud,
- ont i övre magen,
- klåda,
- aptitlöshet,
- mörk urin,
- lerfärgad avföring,
- gulfärgning av huden eller ögonen (gulsot),
- ökad törst,
- ökad urinering,
- hunger,
- torr mun,
- fruktig andedräkt lukt,
- dåsighet,
- suddig syn,
- viktminskning,
- mycket stela muskler,
- hög feber,
- förvirring,
- snabba eller ojämna hjärtslag,
- skakningar och
- yrsel
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Zyprexa inkluderar:
- viktökning (vanligare hos tonåringar),
- ökad aptit,
- huvudvärk,
- yrsel,
- dåsighet,
- känner sig trött eller rastlös,
- problem med tal eller minne,
- skakningar eller skakningar,
- domningar eller stickningar,
- personlighetsförändringar,
- torr mun,
- ökad salivutsöndring,
- magont,
- förstoppning och
- smärta i dina armar eller ben
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Zyprexa. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
ÖKAD DÖDLIGHET HOS ÄLDRE PATIENTER MED DEMENSREATERAT PSYKOS
Äldre patienter med demensrelaterad psykos som behandlas med antipsykotiska läkemedel löper en ökad risk att dö. Analyser av sjutton placebokontrollerade studier (modal varaktighet på 10 veckor), huvudsakligen på patienter som tog atypiska antipsykotiska läkemedel, visade en risk för död hos läkemedelsbehandlade patienter på mellan 1,6 till 1,7 gånger risken för död hos placebobehandlade patienter. Under loppet av en typisk 10-veckors kontrollerad studie var dödsfrekvensen hos läkemedelsbehandlade patienter cirka 4,5 %, jämfört med en frekvens på cirka 2,6 % i placebogruppen. Även om dödsorsakerna varierade, verkade de flesta av dödsfallen vara antingen kardiovaskulära (t.ex. hjärtsvikt, plötslig död) eller infektionssjukdomar (t.ex. lunginflammation). Observationsstudier tyder på att i likhet med atypiska antipsykotiska läkemedel kan behandling med konventionella antipsykotiska läkemedel öka dödligheten. I vilken utsträckning fynden av ökad mortalitet i observationsstudier kan tillskrivas det antipsykotiska läkemedlet i motsats till vissa egenskaper hos patienterna är inte klart. ZYPREXA (olanzapin) är inte godkänt för behandling av patienter med demensrelaterad psykos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och PATIENTINFORMATION ].
När du använder ZYPREXA 15 mg och fluoxetin i kombination, se även avsnittet om varningsförpackning i bipacksedeln för Symbyax.
BESKRIVNING
ZYPREXA (olanzapin) är ett atypiskt antipsykotiskt medel som tillhör tienobensodiazepinklassen. Den kemiska beteckningen är 2-metyl-4-(4-metyl-1-piperazinyl)-10H-tieno[2,3-b] [1,5]bensodiazepin. Molekylformeln är C17H20N4S, vilket motsvarar en molekylvikt på 312,44. Den kemiska strukturen är:
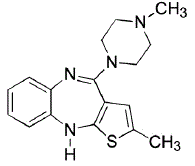
Olanzapin är ett gult kristallint fast ämne som är praktiskt taget olösligt i vatten.
ZYPREXA 7,5 mg tabletter är endast avsedda för oral administrering.
Varje tablett innehåller olanzapin motsvarande 2,5 mg (8 μmol), 5 mg (16 μmol), 7,5 mg (24 μmol), 10 mg (32 μmol), 15 mg (48 μmol) eller 20 mg (64 μmol). Inaktiva ingredienser är karnaubavax, krospovidon, hydroxipropylcellulosa, hypromellos, laktos, magnesiumstearat, mikrokristallin cellulosa och andra inaktiva ingredienser. Färgbeläggningen innehåller titandioxid (alla styrkor), FD&C Blue No. 2 Aluminium Lake (15 mg), eller syntetisk röd järnoxid (20 mg). Tabletterna 2,5, 5, 7,5 och 10 mg är präglade med ätbart bläck som innehåller FD&C Blue No. 2 Aluminium Lake.
ZYPREXA 2,5 mg ZYDIS (olanzapin oralt sönderfallande tabletter) är endast avsedd för oral administrering.
Varje oralt sönderfallande tablett innehåller olanzapin motsvarande 5 mg (16 μmol), 10 mg (32 μmol), 15 mg (48 μmol) eller 20 mg (64 μmol). Det börjar sönderfalla i munnen inom några sekunder, vilket gör att dess innehåll kan sväljas med eller utan vätska. ZYPREXA 15 mg ZYDIS (olanzapin oralt sönderfallande tabletter) innehåller också följande inaktiva ingredienser: gelatin, mannitol, aspartam, natriummetylparaben och natriumpropylparaben.
ZYPREXA 2,5 mg IntraMuscular (olanzapin för injektion) är endast avsedd för intramuskulär användning.
Varje injektionsflaska möjliggör administrering av 10 mg (32 μmol) olanzapin med inaktiva ingredienser 50 mg laktosmonohydrat och 3,5 mg vinsyra. Saltsyra och/eller natriumhydroxid kan ha tillsatts under tillverkningen för att justera pH.
INDIKATIONER
Schizofreni
Oral ZYPREXA är indicerat för behandling av schizofreni. Effekten fastställdes i tre kliniska prövningar på vuxna patienter med schizofreni: två 6-veckorsstudier och en underhållsstudie. Hos ungdomar med schizofreni (åldrar 13-17) fastställdes effekten i en 6-veckors studie [se Kliniska studier ].
När de bestämmer bland de alternativa behandlingar som är tillgängliga för ungdomar bör läkare överväga den ökade potentialen (hos ungdomar jämfört med vuxna) för viktökning och dyslipidemi. Läkare bör överväga de potentiella riskerna på lång sikt när de förskriver till ungdomar, och i många fall kan detta leda till att de överväger att förskriva andra läkemedel först till ungdomar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Bipolär störning I (manisk eller blandad episod)
Monoterapi
Oral ZYPREXA är indicerat för akut behandling av maniska eller blandade episoder associerade med bipolär I sjukdom och underhållsbehandling av bipolär I sjukdom. Effekten fastställdes i tre kliniska prövningar på vuxna patienter med maniska eller blandade episoder av bipolär störning I: två prövningar på 3 till 4 veckor och en underhållsstudie för monoterapi. Hos tonårspatienter med maniska eller blandade episoder associerade med bipolär störning I (åldrar 13-17), fastställdes effekten i en 3-veckors studie [se Kliniska studier ].
När de bestämmer bland de alternativa behandlingar som är tillgängliga för ungdomar bör läkare överväga den ökade potentialen (hos ungdomar jämfört med vuxna) för viktökning och dyslipidemi. Läkare bör överväga de potentiella riskerna på lång sikt när de förskriver till ungdomar, och i många fall kan detta leda till att de överväger att förskriva andra läkemedel först till ungdomar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Tilläggsterapi till litium eller valproat
Oral ZYPREXA 5 mg är indicerat för behandling av maniska eller blandade episoder associerade med bipolär störning I som ett komplement till litium eller valproat. Effekten fastställdes i två 6-veckors kliniska prövningar på vuxna. Effektiviteten av tilläggsbehandling för långvarig användning har inte utvärderats systematiskt i kontrollerade studier [se Kliniska studier ].
Särskilda överväganden vid behandling av pediatrisk schizofreni och bipolär störning I
Pediatrisk schizofreni och bipolär störning I är allvarliga psykiska störningar; dock kan diagnosen vara utmanande. För pediatrisk schizofreni kan symtomprofilerna variera, och för bipolär störning I kan pediatriska patienter ha varierande mönster av periodicitet av maniska eller blandade symtom. Det rekommenderas att läkemedelsbehandling för pediatrisk schizofreni och bipolär störning I påbörjas först efter att en noggrann diagnostisk utvärdering har gjorts och noggrant övervägt riskerna förknippade med läkemedelsbehandling. Läkemedelsbehandling för både pediatrisk schizofreni och bipolär störning I bör ingå i ett totalt behandlingsprogram som ofta innefattar psykologiska, pedagogiska och sociala insatser.
ZYPREXA 15 mg intramuskulärt: Agitation associerad med schizofreni och bipolär I-mani
ZYPREXA 15mg IntraMuscular är indicerat för behandling av akut agitation i samband med schizofreni och bipolär I-mani.
Effekten visades i 3 kortvariga (24 timmars IM-behandling) placebokontrollerade studier på upprörda vuxna slutenvårdspatienter med: schizofreni eller bipolär störning I (maniska eller blandade episoder) [se Kliniska studier ].
"Psykomotorisk agitation" definieras i DSM-IV som "överdriven motorisk aktivitet förknippad med en känsla av inre spänning." Patienter som upplever agitation uppvisar ofta beteenden som stör deras diagnos och vård, t.ex. hotfulla beteenden, eskalerande eller akut plågsamma beteende, eller självutmattande beteende, vilket leder till att läkare använder intramuskulära antipsykotiska mediciner för att uppnå omedelbar kontroll av agitationen.
ZYPREXA och fluoxetin i kombination: depressiva episoder associerade med bipolär sjukdom I
Oral ZYPREXA och fluoxetin i kombination är indicerat för behandling av depressiva episoder associerade med bipolär störning I, baserat på kliniska studier. När du använder ZYPREXA 10 mg och fluoxetin i kombination, se avsnittet om kliniska studier i bipacksedeln för Symbyax.
ZYPREXA monoterapi är inte indicerat för behandling av depressiva episoder associerade med bipolär störning I.
ZYPREXA och fluoxetin i kombination: behandlingsresistent depression
Oral ZYPREXA och fluoxetin i kombination är indicerade för behandling av behandlingsresistent depression (självgående depressiv sjukdom hos patienter som inte svarar på 2 separata studier av olika antidepressiva medel av adekvat dos och varaktighet i den aktuella episoden), baserat på kliniska studier på vuxna patienter . När du använder ZYPREXA och fluoxetin i kombination, se avsnittet om kliniska studier i bipacksedeln för Symbyax.
ZYPREXA 5 mg monoterapi är inte indicerat för behandling av behandlingsresistent depression.
DOSERING OCH ADMINISTRERING
Schizofreni
Vuxna
Val av dos
Oralt olanzapin ska administreras enligt ett schema en gång om dagen utan hänsyn till måltider, vanligtvis med början på 5 till 10 mg initialt, med en måldos på 10 mg/dag inom flera dagar. Ytterligare dosjusteringar, om så är indicerat, bör i allmänhet ske med minst 1 veckas intervall, eftersom steady state för olanzapin inte skulle uppnås under cirka 1 vecka hos den typiska patienten. När dosjusteringar är nödvändiga rekommenderas dosökningar/minskningar på 5 mg dagligen.
Effekt vid schizofreni visades i ett dosintervall på 10 till 15 mg/dag i kliniska prövningar. Doser över 10 mg/dag visades dock inte vara mer effektiva än dosen 10 mg/dag. En ökning till en dos högre än måldosen på 10 mg/dag (dvs. till en dos på 15 mg/dag eller mer) rekommenderas endast efter klinisk bedömning. Olanzapin är inte indicerat för användning i doser över 20 mg/dag.
Dosering i speciella populationer
Den rekommenderade startdosen är 5 mg till patienter som är försvagade, som har en predisposition för hypotensiva reaktioner, som annars uppvisar en kombination av faktorer som kan resultera i långsammare metabolism av olanzapin (t.ex. icke-rökare kvinnliga patienter ≥65 år), eller som kan vara mer farmakodynamiskt känsliga för olanzapin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER , och KLINISK FARMAKOLOGI ]. Vid indikation bör dosökning utföras med försiktighet hos dessa patienter.
Underhållsbehandling
Effekten av oralt olanzapin, 10 mg/dag till 20 mg/dag, för att upprätthålla behandlingssvar hos schizofrena patienter som varit stabila på ZYPREXA i cirka 8 veckor och sedan följdes för återfall har visats i en placebokontrollerad studie [se Kliniska studier ]. Den vårdgivare som väljer att använda ZYPREXA under längre perioder bör med jämna mellanrum omvärdera läkemedlets långsiktiga användbarhet för den enskilda patienten.
Tonåringar
Val av dos
Oralt olanzapin ska administreras enligt ett schema en gång om dagen utan hänsyn till måltider med en rekommenderad startdos på 2,5 eller 5 mg, med en måldos på 10 mg/dag. Effekt hos ungdomar med schizofreni visades baserat på ett flexibelt dosintervall på 2,5 till 20 mg/dag i kliniska prövningar, med en genomsnittlig modal dos på 12,5 mg/dag (medeldos på 11,1 mg/dag). När dosjusteringar är nödvändiga rekommenderas dosökningar/minskningar på 2,5 eller 5 mg.
Säkerheten och effektiviteten av doser över 20 mg/dag har inte utvärderats i kliniska prövningar [se Kliniska studier ].
Underhållsbehandling
Effekten av ZYPREXA för underhållsbehandling av schizofreni hos ungdomar har inte utvärderats systematiskt; dock kan underhållseffekt extrapoleras från vuxna data tillsammans med jämförelser av olanzapins farmakokinetiska parametrar hos vuxna och ungdomar. Det rekommenderas därför generellt att patienter som svarar fortsätter efter det akuta svaret, men med den lägsta dos som behövs för att bibehålla remission. Patienter bör regelbundet utvärderas för att fastställa behovet av underhållsbehandling.
Bipolär störning I (manisk eller blandad episod)
Vuxna
Dosval för monoterapi
Oralt olanzapin ska administreras enligt ett schema en gång om dagen utan hänsyn till måltider, vanligtvis med början på 10 eller 15 mg. Dosjusteringar, om indicerat, bör i allmänhet ske med minst 24 timmars intervall, vilket återspeglar procedurerna i de placebokontrollerade studierna. När dosjusteringar är nödvändiga rekommenderas dosökningar/minskningar på 5 mg dagligen.
Kortvarig (3-4 veckor) antimanisk effekt har visats i ett dosintervall på 5 mg till 20 mg/dag i kliniska prövningar. Säkerheten för doser över 20 mg/dag har inte utvärderats i kliniska prövningar [se Kliniska studier ].
Monoterapi för underhåll
Fördelen med att bibehålla bipolära I-patienter på monoterapi med oral ZYPREXA 10 mg i en dos på 5 till 20 mg/dag, efter att ha uppnått en responderstatus under en genomsnittlig varaktighet på 2 veckor, visades i en kontrollerad studie [se Kliniska studier ]. Den vårdgivare som väljer att använda ZYPREXA under längre perioder bör med jämna mellanrum omvärdera läkemedlets långsiktiga användbarhet för den enskilda patienten.
Dosval för tilläggsbehandling
Vid administrering som tilläggsbehandling till litium eller valproat bör oral olanzapindosering i allmänhet börja med 10 mg en gång dagligen utan hänsyn till måltider.
Antimanisk effekt har visats i ett dosintervall på 5 mg till 20 mg/dag i kliniska prövningar [se Kliniska studier ]. Säkerheten för doser över 20 mg/dag har inte utvärderats i kliniska prövningar.
Tonåringar
Val av dos
Oralt olanzapin ska administreras enligt ett schema en gång om dagen utan hänsyn till måltider med en rekommenderad startdos på 2,5 eller 5 mg, med en måldos på 10 mg/dag. Effekt hos ungdomar med bipolär störning I (maniska eller blandade episoder) visades baserat på ett flexibelt dosintervall på 2,5 till 20 mg/dag i kliniska prövningar, med en genomsnittlig modal dos på 10,7 mg/dag (medeldos på 8,9 mg/dag) ). När dosjusteringar är nödvändiga rekommenderas dosökningar/minskningar på 2,5 eller 5 mg.
Säkerheten och effektiviteten av doser över 20 mg/dag har inte utvärderats i kliniska prövningar [se Kliniska studier ].
Underhållsbehandling
Effekten av ZYPREXA 7,5 mg för underhållsbehandling av bipolär störning I hos ungdomar har inte utvärderats; dock kan underhållseffekt extrapoleras från vuxna data tillsammans med jämförelser av olanzapins farmakokinetiska parametrar hos vuxna och ungdomar. Det rekommenderas därför generellt att patienter som svarar fortsätter efter det akuta svaret, men med den lägsta dos som behövs för att bibehålla remission. Patienter bör regelbundet utvärderas för att fastställa behovet av underhållsbehandling.
Administrering av ZYPREXA ZYDIS (olanzapin oralt sönderfallande tabletter)
Efter att påsen har öppnats, dra av folien på blistern. Tryck inte tabletten genom folien. Omedelbart efter att blistern öppnats, med torra händer, ta bort tabletten och placera hela ZYPREXA 15 mg ZYDIS i munnen. Tablettsönderdelning sker snabbt i saliv så att den lätt kan sväljas med eller utan vätska.
ZYPREXA Intramuskulär: Agitation associerad med schizofreni och bipolär I-mani
Dosval för upprörda vuxna patienter med schizofreni och bipolär I-mani
Effekten av intramuskulärt olanzapin för injektion för att kontrollera agitation vid dessa störningar har visats i ett dosintervall på 2,5 mg till 10 mg. Den rekommenderade dosen för dessa patienter är 10 mg. En lägre dos på 5 eller 7,5 mg kan övervägas när kliniska faktorer motiverar [se Kliniska studier ]. Om agitation som motiverar ytterligare intramuskulära doser kvarstår efter den initiala dosen, kan efterföljande doser upp till 10 mg ges. Effekten av upprepade doser av intramuskulär olanzapin för injektion hos upprörda patienter har dock inte utvärderats systematiskt i kontrollerade kliniska prövningar. Säkerheten för totala dagliga doser större än 30 mg eller 10 mg injektioner som ges oftare än 2 timmar efter den initiala dosen och 4 timmar efter den andra dosen har inte utvärderats i kliniska prövningar. Maximal dosering av intramuskulärt olanzapin (t.ex. 3 doser på 10 mg administrerade med 2-4 timmars mellanrum) kan vara associerad med en betydande förekomst av signifikant ortostatisk hypotoni [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Det rekommenderas därför att patienter som behöver efterföljande intramuskulära injektioner utvärderas för ortostatisk hypotoni före administrering av eventuella efterföljande doser av intramuskulär olanzapin för injektion. Administrering av ytterligare en dos till en patient med en kliniskt signifikant postural förändring av systoliskt blodtryck rekommenderas inte.
Om pågående olanzapinbehandling är kliniskt indicerad, kan oralt olanzapin initieras i ett intervall av 5-20 mg/dag så snart som det är kliniskt lämpligt [se Schizofreni och Bipolär störning I (manisk eller blandad episod) ].
Intramuskulär dosering i speciella populationer
En dos på 5 mg/injektion bör övervägas för geriatriska patienter eller när andra kliniska faktorer motiverar det. En lägre dos på 2,5 mg/injektion bör övervägas för patienter som annars kan vara försvagade, vara predisponerade för hypotensiva reaktioner eller vara mer farmakodynamiskt känsliga för olanzapin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER , och KLINISK FARMAKOLOGI ].
Administrering av ZYPREXA intramuskulärt
ZYPREXA Intra Muscular är endast avsedd för intramuskulär användning. Administreras inte intravenöst eller subkutant. Injicera långsamt, djupt in i muskelmassan. Parenterala läkemedelsprodukter bör inspekteras visuellt med avseende på partiklar och missfärgning före administrering, närhelst lösning och behållare tillåter.
Instruktioner för beredning av ZYPREXA 2,5 mg intramuskulärt med sterilt vatten för injektion
Lös upp innehållet i injektionsflaskan med 2,1 ml sterilt vatten för injektion för att ge en lösning som innehåller cirka 5 mg/ml olanzapin. Den resulterande lösningen ska se klar och gul ut. ZYPREXA 7,5 mg IntraMuscular beredd med sterilt vatten för injektion ska användas omedelbart (inom 1 timme) efter beredning. Kassera eventuell oanvänd del.
Följande tabell visar injektionsvolymer för att tillföra olika doser av intramuskulärt olanzapin för injektion rekonstituerat med sterilt vatten för injektion.
Information om fysisk inkompatibilitet
ZYPREXA 15mg IntraMuscular ska endast beredas med sterilt vatten för injektion. ZYPREXA 20mg IntraMuscular ska inte kombineras i en spruta med diazepaminjektion eftersom utfällning sker när dessa produkter blandas. Lorazepam-injektion ska inte användas för att rekonstituera ZYPREXA IntraMuscular eftersom denna kombination resulterar i en försenad rekonstitutionstid. ZYPREXA IntraMuscular ska inte kombineras i en spruta med haloperidolinjektion eftersom det resulterande låga pH-värdet har visat sig bryta ned olanzapin över tid.
ZYPREXA 20mg och fluoxetin i kombination: depressiva episoder associerade med bipolär störning I
När du använder ZYPREXA 7,5 mg och fluoxetin i kombination, se även avsnittet om kliniska studier i bipacksedeln för Symbyax.
Vuxna
Oralt olanzapin ska administreras i kombination med fluoxetin en gång dagligen på kvällen, utan hänsyn till måltider, vanligtvis med 5 mg oralt olanzapin och 20 mg fluoxetin. Dosjusteringar, om indicerat, kan göras i enlighet med effekt och tolerabilitet inom dosintervall för oralt olanzapin 5 till 12,5 mg och fluoxetin 20 till 50 mg. Antidepressiv effekt visades med ZYPREXA 10 mg och fluoxetin i kombination hos vuxna patienter med dosintervallet olanzapin 6 till 12 mg och fluoxetin 25 till 50 mg. Säkerheten vid samtidig administrering av doser över 18 mg olanzapin och 75 mg fluoxetin har inte utvärderats i kliniska studier.
Barn och ungdomar (10-17 år)
Oralt olanzapin ska administreras i kombination med fluoxetin en gång dagligen på kvällen, utan hänsyn till måltider, vanligtvis med början på 2,5 mg oralt olanzapin och 20 mg fluoxetin. Dosjusteringar, om indikerat, kan göras i enlighet med effekt och tolerabilitet. Säkerheten vid samtidig administrering av doser över 12 mg olanzapin och 50 mg fluoxetin har inte utvärderats i pediatriska kliniska studier.
Säkerhet och effekt av ZYPREXA och fluoxetin i kombination fastställdes i kliniska prövningar som stödde godkännande av Symbyax (fast doskombination av ZYPREXA och fluoxetin). Symbyax doseras mellan 3 mg/25 mg (olanzapin/fluoxetin) per dag och 12 mg/50 mg (olanzapin/fluoxetin) per dag. Följande tabell visar lämpliga individuella komponentdoser av ZYPREXA 10 mg och fluoxetin jämfört med Symbyax. Dosjusteringar, om indikerat, bör göras med de individuella komponenterna enligt effekt och tolerabilitet.
Även om det inte finns några bevis för att besvara frågan om hur länge en patient som behandlas med ZYPREXA och fluoxetin i kombination ska stanna kvar på det, är det allmänt accepterat att bipolär störning I, inklusive depressiva episoder förknippade med bipolär störning I, är en kronisk sjukdom. sjukdom som kräver kronisk behandling. Vårdgivaren bör med jämna mellanrum ompröva behovet av fortsatt farmakoterapi.
ZYPREXA 5 mg monoterapi är inte indicerat för behandling av depressiva episoder associerade med bipolär störning I.
ZYPREXA 7,5 mg och fluoxetin i kombination: behandling av resistent depression
När du använder ZYPREXA och fluoxetin i kombination, se även avsnittet om kliniska studier i bipacksedeln för Symbyax.
Oralt olanzapin ska administreras i kombination med fluoxetin en gång dagligen på kvällen, utan hänsyn till måltider, vanligtvis med 5 mg oralt olanzapin och 20 mg fluoxetin. Dosjusteringar, om indicerat, kan göras enligt effekt och tolerabilitet inom dosintervallen för oralt olanzapin 5 till 20 mg och fluoxetin 20 till 50 mg. Antidepressiv effekt visades med olanzapin och fluoxetin i kombination hos vuxna patienter med dosintervallet olanzapin 6 till 18 mg och fluoxetin 25 till 50 mg.
Säkerhet och effekt av olanzapin i kombination med fluoxetin fastställdes i kliniska prövningar som stödde godkännandet av Symbyax (kombination med fast dos av olanzapin och fluoxetin). Symbyax doseras mellan 3 mg/25 mg (olanzapin/fluoxetin) per dag och 12 mg/50 mg (olanzapin/fluoxetin) per dag. Tabell 1 ovan visar de lämpliga individuella komponentdoserna av ZYPREXA och fluoxetin jämfört med Symbyax. Dosjusteringar, om indikerat, bör göras med de individuella komponenterna enligt effekt och tolerabilitet.
Även om det inte finns några bevis för att besvara frågan om hur länge en patient som behandlas med ZYPREXA och fluoxetin i kombination ska stanna kvar på det, är det allmänt accepterat att behandlingsresistent depression (självständig depression hos vuxna patienter som inte svarar på 2 separata prövningar av olika antidepressiva medel av adekvat dos och varaktighet i det aktuella avsnittet) är en kronisk sjukdom som kräver kronisk behandling. Vårdgivaren bör med jämna mellanrum ompröva behovet av fortsatt farmakoterapi.
Säkerheten vid samtidig administrering av doser över 18 mg olanzapin och 75 mg fluoxetin har inte utvärderats i kliniska studier.
ZYPREXA 7,5 mg monoterapi är inte indicerat för behandling av behandlingsresistent depression (sjävlig depressiv sjukdom hos patienter som inte svarar på 2 antidepressiva medel med tillräcklig dos och varaktighet i den aktuella episoden).
ZYPREXA 10 mg och fluoxetin i kombination: dosering i speciella populationer
Startdosen av oral olanzapin 2,5-5 mg med fluoxetin 20 mg bör användas för patienter med anlag för hypotensiva reaktioner, patienter med nedsatt leverfunktion eller patienter som uppvisar en kombination av faktorer som kan bromsa metabolismen av olanzapin eller fluoxetin i kombination. (kvinnligt kön, geriatrisk ålder, icke-rökare), eller de patienter som kan vara farmakodynamiskt känsliga för olanzapin. Dosjustering kan vara nödvändig hos patienter som uppvisar en kombination av faktorer som kan bromsa metabolismen. Vid indikation bör dosökning utföras med försiktighet hos dessa patienter. ZYPREXA och fluoxetin i kombination har inte studerats systematiskt hos patienter över 65 år eller hos patienter under 10 år [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER , och KLINISK FARMAKOLOGI ].
HUR LEVERERAS
Doseringsformer och styrkor
ZYPREXA 2,5 mg, 5 mg, 7,5 mg och 10 mg tabletter är vita, runda och märkta med blått bläck med LILLY och tablettnummer. 15 mg tabletterna är elliptiska, blå och präglade med LILLY och tablettnummer. 20 mg tabletterna är elliptiska, rosa och präglade med LILLY och tablettnummer. Tabletter poängsätts inte. Tabletterna finns tillgängliga enligt följande:
ZYPREXA 10mg ZYDIS (olanzapin oralt sönderfallande tabletter) är gula, runda och präglade med tablettstyrkan. Tabletter poängsätts inte. Tabletterna finns tillgängliga enligt följande:
ZYPREXA 15 mg intramuskulärt finns i 10 mg injektionsflaska (1s).
ZYPREXA 2,5 mg, 5 mg, 7,5 mg och 10 mg tabletter är vita, runda och märkta med blått bläck med LILLY och tablettnummer. 15 mg tabletterna är elliptiska, blå och präglade med LILLY och tablettnummer. 20 mg tabletterna är elliptiska, rosa och präglade med LILLY och tablettnummer. Tabletterna finns tillgängliga enligt följande:
ZYPREXA 2,5 mg ZYDIS (olanzapin oralt sönderfallande tabletter) är gula, runda och präglade med tablettstyrkan. Tabletterna finns tillgängliga enligt följande:
ZYPREXA Intramuskulär finns i:
NDC 0002-7597-01 (nr VL7597) – 10 mg injektionsflaska (1s)
Förvaring Och Hantering
Förvara ZYPREXA tabletter, ZYPREXA ZYDIS och ZYPREXA intramuskulära injektionsflaskor (före beredning) vid kontrollerad rumstemperatur, 20° till 25°C (68° till 77°F) [se USP ]. Rekonstituerad ZYPREXA 20mg IntraMuscular kan förvaras i kontrollerad rumstemperatur, 20° till 25°C (68° till 77°F) [se USP i upp till 1 timme vid behov. Kassera eventuell oanvänd del av rekonstituerad ZYPREXA IntraMuscular. USP definierar kontrollerad rumstemperatur som en temperatur som hålls termostatiskt och som omfattar den vanliga och vanliga arbetsmiljön på 20° till 25°C (68° till 77°F); som resulterar i en kinetisk medeltemperatur beräknad till högst 25°C; och som möjliggör utflykter mellan 15° och 30°C (59° och 86°F) som finns på apotek, sjukhus och lager.
Skydda ZYPREXA tabletter och ZYPREXA ZYDIS från ljus och fukt. Skydda ZYPREXA IntraMuscular från ljus, frys inte.
Marknadsförs av: Lilly USA, LLC, Indianapolis, IN 46285, USA. Reviderad: oktober 2019
BIEFFEKTER
När du använder ZYPREXA 2,5 mg och fluoxetin i kombination, se även avsnittet Biverkningar i bipacksedeln för Symbyax.
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och kanske inte återspeglar eller förutsäger frekvensen som observeras i praktiken.
Kliniska prövningar hos vuxna
Informationen nedan för olanzapin härrör från en databas för kliniska prövningar för olanzapin bestående av 10 504 vuxna patienter med cirka 4765 patientår av exponering för olanzapin plus 722 patienter med exponering för intramuskulärt olanzapin för injektion. Denna databas inkluderar: (1) 2 500 patienter som deltog i flerdosförsök med oralt olanzapin för marknadsföring av schizofreni och Alzheimers sjukdom, vilket representerar ungefär 1 122 patientår av exponering per den 14 februari 1995; (2) 182 patienter som deltog i prövningar av oral olanzapin bipolär störning I (maniska eller blandade episoder) före marknadsföring, vilket representerade cirka 66 patientår av exponering; (3) 191 patienter som deltog i en oral olanzapinstudie med patienter som hade olika psykiatriska symtom i samband med Alzheimers sjukdom, vilket representerade cirka 29 patientår av exponering; (4) 5788 ytterligare patienter från 88 orala olanzapin kliniska prövningar per den 31 december 2001; (5) 1843 ytterligare patienter från 41 kliniska prövningar med olanzapin den 31 oktober 2011; och (6) 722 patienter som deltog i intramuskulära olanzapin för injektion premarketingstudier på upprörda patienter med schizofreni, bipolär störning I (maniska eller blandade episoder) eller demens. Nedan ingår också information från den 6 veckor långa kliniska studiedatabasen för olanzapin i kombination med litium eller valproat, som består av 224 patienter som deltog i prövningar med bipolär störning I (manisk eller blandad episod) med cirka 22 patientårs exponering.
Tillstånden och varaktigheten av behandlingen med olanzapin varierade mycket och inkluderade (i överlappande kategorier) öppna och dubbelblinda faser av studier, slutenvård och öppenvård, studier med fasta doser och dostitrering samt korttids- eller längre tids exponering . Biverkningar bedömdes genom att samla in biverkningar, resultat av fysiska undersökningar, vitala tecken, vikter, laboratorieanalyter, EKG, lungröntgen och resultat av oftalmologiska undersökningar.
Vissa delar av diskussionen nedan som rör objektiva eller numeriska säkerhetsparametrar, nämligen dosberoende biverkningar, förändringar av vitala tecken, viktökning, laboratorieförändringar och EKG-förändringar härrör från studier på patienter med schizofreni och har inte duplicerats för bipolär störning I. (maniska eller blandade episoder) eller agitation. Denna information är emellertid också allmänt tillämplig på bipolär störning I (maniska eller blandade episoder) och agitation.
Biverkningar under exponering erhölls genom spontanrapportering och registrerades av kliniska utredare med terminologi som de själva valt. Följaktligen är det inte möjligt att ge en meningsfull uppskattning av andelen individer som upplever biverkningar utan att först gruppera liknande typer av reaktioner i ett mindre antal standardiserade reaktionskategorier. I tabellerna och tabellerna som följer har MedDRA och COSTART Dictionary terminologi använts för att klassificera rapporterade biverkningar.
De angivna frekvenserna av biverkningar representerar andelen individer som åtminstone en gång upplevt en behandlingsuppkommande biverkning av den listade typen. En reaktion ansågs vara framträdande av behandling om den inträffade för första gången eller förvärrades under behandling efter baslinjeutvärdering. De rapporterade reaktionerna inkluderar inte de reaktionstermer som var så generella att de inte var informativa. Reaktioner som anges på andra ställen i märkningen får inte upprepas nedan. Det är viktigt att betona att även om reaktionerna inträffade under behandling med olanzapin, var de inte nödvändigtvis orsakade av det. Hela etiketten bör läsas för att få en fullständig förståelse av säkerhetsprofilen för olanzapin.
Förskrivaren bör vara medveten om att siffrorna i tabellerna och tabellerna inte kan användas för att förutsäga förekomsten av biverkningar under sedvanlig medicinsk praxis där patientegenskaper och andra faktorer skiljer sig från de som rådde i de kliniska prövningarna. På liknande sätt kan de angivna frekvenserna inte jämföras med siffror som erhållits från andra kliniska undersökningar som involverar olika behandlingar, användningar och utredare. De citerade siffrorna ger dock den förskrivande vårdgivaren viss grund för att uppskatta det relativa bidraget av läkemedel och icke-läkemedelsfaktorer till biverkningsincidensen i den studerade populationen.
Förekomst av biverkningar i kortsiktiga, placebokontrollerade och kombinationsförsök
Följande fynd är baserade på förmarknadsföringsstudier av (1) oralt olanzapin för schizofreni, bipolär I-störning (maniska eller blandade episoder), en efterföljande studie med patienter som har olika psykiatriska symtom i samband med Alzheimers sjukdom, och kombinationsstudier före marknadsföring, och (2 ) intramuskulärt olanzapin för injektion hos upprörda patienter med schizofreni eller bipolär I-mani.
Biverkningar associerade med avbrytande av behandling i kortvariga, placebokontrollerade prövningar
Schizofreni
Totalt sett var det ingen skillnad i incidensen av avbrott på grund av biverkningar (5 % för oralt olanzapin mot 6 % för placebo). Utsättningar på grund av ökningar av ALAT ansågs dock vara läkemedelsrelaterade (2 % för oralt olanzapin mot 0 % för placebo).
Bipolär störning I (manisk eller blandad episod) Monoterapi
Totalt sett fanns det ingen skillnad i incidensen av utsättning på grund av biverkningar (2 % för oralt olanzapin vs 2 % för placebo).
Agitation
Totalt sett fanns det ingen skillnad i incidensen av avbrott på grund av biverkningar (0,4 % för intramuskulärt olanzapin för injektion kontra 0 % för placebo).
Biverkningar associerade med avbrytande av behandling i korttidskombinationsförsök
Bipolär störning I (manisk eller blandad episod), olanzapin som tillägg till litium eller valproat
I en studie av patienter som redan tolererade antingen litium eller valproat som monoterapi, var utsättningsfrekvensen på grund av biverkningar 11 % för kombinationen av oralt olanzapin med litium eller valproat jämfört med 2 % för patienter som fortsatte med litium- eller valproatmonoterapi. Avbrott med kombinationen av oral olanzapin och litium eller valproat som inträffade hos mer än 1 patient var: somnolens (3 %), viktökning (1 %) och perifert ödem (1 %).
Vanligt observerade biverkningar i kortsiktiga, placebokontrollerade försök
De vanligast observerade biverkningarna förknippade med användning av oralt olanzapin (incidens på 5 % eller mer) och som inte observerats vid en likvärdig incidens bland placebobehandlade patienter (olanzapinincidensen minst dubbelt så stor som för placebo) var:
Olanzapin intramuskulärt
Det observerades 1 biverkning (somnolens) med en incidens på 5 % eller mer bland intramuskulärt olanzapin för injektionsbehandlade patienter och inte observerat med en motsvarande incidens bland placebobehandlade patienter (olanzapinincidensen minst dubbelt så stor som för placebo) under placebo -kontrollerade förmarknadsföringsstudier. Incidensen av somnolens under den 24 timmar långa IM-behandlingsperioden i kliniska prövningar på upprörda patienter med schizofreni eller bipolär I-mani var 6 % för intramuskulärt olanzapin för injektion och 3 % för placebo.
Biverkningar som inträffar med en incidens på 2 % eller mer bland orala olanzapinbehandlade patienter i kortvariga, placebokontrollerade prövningar
Tabell 11 räknar upp incidensen, avrundad till närmaste procent, av behandlingsuppkomna biverkningar som inträffade hos 2 % eller fler av patienterna som behandlades med oralt olanzapin (doser ≥2,5 mg/dag) och med incidensen större än placebo som deltog i den akuta fas av placebokontrollerade prövningar.
Dosberoende av biverkningar
En dosgruppsskillnad har observerats för trötthet, yrsel, viktökning och prolaktinhöjning. I en enda 8-veckors randomiserad, dubbelblind studie med fast dos som jämförde 10 (N=199), 20 (N=200) och 40 (N=200) mg/dag oralt olanzapin hos vuxna patienter med schizofreni eller schizoaffektiv störning, incidens av trötthet (10 mg/dag: 1,5 %; 20 mg/dag: 2,1 %; 40 mg/dag: 6,6 %) observerades med signifikanta skillnader mellan 10 vs 40 och 20 vs 40 mg/dag. Incidensen av yrsel (10 mg/dag: 2,6 %; 20 mg/dag: 1,6 %; 40 mg/dag: 6,6 %) observerades med signifikanta skillnader mellan 20 och 40 mg. Dosgruppsskillnader noterades också för viktökning och prolaktinhöjning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Följande tabell tar upp dosrelaterad effekt för andra biverkningar med hjälp av data från en schizofrenistudie som involverar fasta dosintervall av oralt olanzapin. Den räknar upp procentandelen patienter med behandlingsuppkomna biverkningar för de tre fasta dosgrupperna och placebo. Data analyserades med hjälp av Cochran-Armitage-testet, exklusive placebogruppen, och tabellen inkluderar endast de biverkningar för vilka det fanns en trend.
Vanliga observerade biverkningar i korttidsförsök med oralt olanzapin som tillägg till litium eller valproat
I bipolär sjukdom I (maniska eller blandade episoder) tilläggs placebokontrollerade studier var de vanligaste observerade biverkningarna förknippade med kombinationen av olanzapin och litium eller valproat (incidens av ≥5 % och minst två gånger placebo):
Biverkningar som inträffar med en frekvens av 2 % eller mer bland orala olanzapinbehandlade patienter i korttidsförsök med olanzapin som tillägg till litium eller valproat
Tabell 14 räknar upp incidensen, avrundad till närmaste procent, av behandlingsuppkomna biverkningar som inträffade hos 2 % eller fler av patienterna som behandlades med kombinationen av olanzapin (doser ≥5 mg/dag) och litium eller valproat och med en incidens högre än litium eller valproat enbart som deltog i den akuta fasen av placebokontrollerade kombinationsstudier.
För specifik information om de biverkningar som observerats med litium eller valproat, se avsnittet Biverkningar i bipacksedeln för dessa andra produkter.
Biverkningar som uppträder med en incidens av 1 % eller mer bland intramuskulärt olanzapin för injektionsbehandlade patienter i kortvariga, placebokontrollerade prövningar
Tabell 15 räknar upp incidensen, avrundad till närmaste procent, av behandlingsuppkomna biverkningar som inträffade hos 1 % eller fler av patienterna som behandlats med intramuskulärt olanzapin för injektion (dosintervall på 2,5-10 mg/injektion) och med incidensen större än placebo som deltog i de kortsiktiga, placebokontrollerade studierna på upprörda patienter med schizofreni eller bipolär I-mani.
Extrapyramidala symtom
Följande tabell räknar upp procentandelen patienter med extrapyramidala symtom som uppstår vid behandling, utvärderade genom kategoriska analyser av formella betygsskalor under akut terapi i en kontrollerad klinisk prövning som jämför oralt olanzapin vid 3 fasta doser med placebo vid behandling av schizofreni under en 6-veckorsperiod. rättegång.
Följande tabell räknar upp procentandelen av patienter med extrapyramidala symtom som uppstår vid behandling, bedömda av spontant rapporterade biverkningar under akut behandling i samma kontrollerade kliniska studie som jämförde olanzapin vid 3 fasta doser med placebo vid behandling av schizofreni i en 6-veckors studie.
Följande tabell räknar upp procentandelen ungdomar med extrapyramidala symtom som uppstår vid behandling, bedömda av spontant rapporterade biverkningar under akut behandling (dosintervall: 2,5 till 20 mg/dag).
Följande tabell räknar upp procentandelen patienter med extrapyramidala symtom som uppstår vid behandling, utvärderade genom kategoriska analyser av formella betygsskalor under kontrollerade kliniska prövningar som jämför fasta doser av intramuskulärt olanzapin för injektion med placebo vid agitation. Patienter i varje dosgrupp kunde få upp till 3 injektioner under försöken [se Kliniska studier ]. Patientbedömningar utfördes under 24 timmar efter den initiala dosen av intramuskulär olanzapin för injektion.
Följande tabell räknar upp procentandelen av patienter med extrapyramidala symtom som uppstår vid behandling, bedömda av spontant rapporterade biverkningar i samma kontrollerade kliniska prövning som jämför fasta doser av intramuskulärt olanzapin för injektion med placebo hos upprörda patienter med schizofreni.
Dystoni, klasseffekt
Symtom på dystoni, långvariga onormala sammandragningar av muskelgrupper, kan förekomma hos känsliga individer under de första dagarna av behandlingen. Dystoniska symtom inkluderar: spasmer i nackmusklerna, som ibland utvecklas till täthet i halsen, sväljsvårigheter, andningssvårigheter och/eller utskjutande tunga. Även om dessa symtom kan uppträda vid låga doser, är frekvensen och svårighetsgraden större med hög potens och vid högre doser av första generationens antipsykotiska läkemedel. I allmänhet kan en förhöjd risk för akut dystoni observeras hos män och yngre åldersgrupper som får antipsykotika; dock har händelser av dystoni rapporterats sällan (
Andra biverkningar
Andra biverkningar som observerats under utvärderingen av den kliniska prövningen av oralt olanzapin
Följande är en lista över behandlingsuppkomna biverkningar som rapporterats av patienter som behandlats med oralt olanzapin (vid flera doser ≥1 mg/dag) i kliniska prövningar. Denna förteckning är inte avsedd att inkludera reaktioner (1) som redan har listats i tidigare tabeller eller någon annanstans i märkningen, (2) för vilka en drogorsak var avlägsen, (3) som var så allmänna att de var oinformativa, (4) som inte var anses ha signifikanta kliniska implikationer, eller (5) som inträffade i en takt lika med eller mindre än placebo. Reaktioner klassificeras efter kroppssystem med hjälp av följande definitioner: frekventa biverkningar är de som inträffar hos minst 1/100 patienter; sällsynta biverkningar är de som inträffar hos 1/100 till 1/1000 patienter; sällsynta reaktioner är de som inträffar hos färre än 1/1000 patienter.
Kroppen som helhet - Sällsynt: frossa, ansiktsödem, ljuskänslighetsreaktion, självmordsförsök1; Sällsynta: frossa och feber, baksmällaeffekt, plötslig död1.
Kardiovaskulära systemet - Sällan: cerebrovaskulär olycka, vasodilatation.
Matsmältningssystemet - Sällsynt: utspänd buk, illamående och kräkningar, tungödem; Sällsynta: ileus, tarmobstruktion, fettavlagringar i levern.
Hemiska och lymfatiska systemet - Sällsynt: trombocytopeni.
Metaboliska och näringsmässiga störningar - Frekvent: ökat alkaliskt fosfatas; Sällsynt: bilirubinemi, hypoproteinemi.
Muskuloskeletala systemet - Sällsynt: osteoporos.
Nervsystem - Sällsynt: ataxi, dysartri, minskad libido, stupor; Sällsynt: koma.
Andningssystem - Sällsynt: näsblod; Sällsynt: lungödem.
Hud och bihang - Sällsynt: alopeci.
Särskilda sinnen - Sällsynt: onormalt boende, torra ögon; Sällsynt: mydriasis.
Urogenitala systemet - Sällsynta: amenorré2, bröstsmärtor, minskad menstruation, impotens2, ökad menstruation2, menorragi2, metrorragi2, polyuri2, urinfrekvens, urinretention, urinträngning, nedsatt urinering.
1 Dessa termer representerar allvarliga biverkningar men uppfyller inte definitionen för biverkningar av läkemedel. De är med här på grund av deras allvar. 2 Justerat för kön.
Andra biverkningar som observerats under den kliniska prövningens utvärdering av intramuskulärt olanzapin för injektion
Följande är en lista över behandlingsuppkomna biverkningar som rapporterats av patienter som behandlats med intramuskulärt olanzapin för injektion (vid 1 eller fler doser ≥2,5 mg/injektion) i kliniska prövningar. Denna förteckning är inte avsedd att inkludera reaktioner (1) som redan har listats i tidigare tabeller eller någon annanstans i märkningen, (2) för vilka en drogorsak var avlägsen, (3) som var så allmänna att de var oinformativa, (4) som inte var anses ha signifikanta kliniska implikationer, eller (5) för vilka inträffade i en takt lika med eller mindre än placebo. Reaktioner klassificeras efter kroppssystem med hjälp av följande definitioner: frekventa biverkningar är de som inträffar hos minst 1/100 patienter; sällsynta biverkningar är de som inträffar hos 1/100 till 1/1000 patienter.
Kroppen som helhet - Frekvent: smärta på injektionsstället.
Kardiovaskulära systemet - Sällsynt: synkope.
Matsmältningssystemet - Sällsynt: illamående.
Metaboliska och näringsmässiga störningar - Sällsynt: ökad kreatinfosfokinas.
Kliniska prövningar på ungdomar (ålder 13 till 17 år)
Vanliga observerade biverkningar i orala olanzapin kortvariga, placebokontrollerade studier
Biverkningar hos ungdomar som behandlats med oralt olanzapin (doser ≥2,5 mg) rapporterade med en incidens på 5 % eller mer och rapporterade minst dubbelt så ofta som placebobehandlade patienter listas i Tabell 21.
Biverkningar som inträffar med en incidens på 2 % eller mer bland orala olanzapinbehandlade patienter under kortvariga (3-6 veckor), placebokontrollerade prövningar
Biverkningar hos ungdomar som behandlats med oralt olanzapin (doser ≥2,5 mg) rapporterade med en incidens på 2 % eller mer och mer än placebo listas i Tabell 22.
Vitala tecken och laboratoriestudier
Vital Sign Changes
Oral olanzapin associerades med ortostatisk hypotoni och takykardi i kliniska prövningar. Intramuskulärt olanzapin för injektion associerades med bradykardi, hypotoni och takykardi i kliniska prövningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Laboratorieförändringar
Olanzapin monoterapi hos vuxna
En bedömning av erfarenheten av olanzapin före marknadsföring avslöjade ett samband med asymtomatiska ökningar av ALAT, ASAT och GGT. Inom den ursprungliga premarketingdatabasen med cirka 2400 vuxna patienter med baseline-ALAT ≤90 IE/L var incidensen av ALAT-höjningar till >200 IE/l 2 % (50/2381). Ingen av dessa patienter upplevde gulsot eller andra symtom som kan hänföras till nedsatt leverfunktion och de flesta hade övergående förändringar som tenderade att normaliseras medan behandlingen med olanzapin fortsatte.
placebokontrollerade monoterapistudier med olanzapin på vuxna observerades kliniskt signifikanta ALAT-höjningar (förändring från
Från en analys av laboratoriedata i en integrerad databas med 41 avslutade kliniska studier på vuxna patienter som behandlats med oralt olanzapin, registrerades höga GGT-nivåer hos ≥1 % (88/5245) av patienterna.
Försiktighet bör iakttas hos patienter med tecken och symtom på nedsatt leverfunktion, hos patienter med redan existerande tillstånd associerade med begränsad leverfunktionsreserv och hos patienter som behandlas med potentiellt hepatotoxiska läkemedel.
Administrering av olanzapin var också associerad med ökningar av serumprolaktin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ] med en asymtomatisk ökning av antalet eosinofiler hos 0,3 % av patienterna och med en ökning av CPK.
Från en analys av laboratoriedata i en integrerad databas med 41 avslutade kliniska studier på vuxna patienter som behandlats med oralt olanzapin, registrerades förhöjd urinsyra hos ≥3 % (171/4641) av patienterna.
Olanzapin monoterapi hos ungdomar
placebokontrollerade kliniska prövningar av tonårspatienter med schizofreni eller bipolär störning I (maniska eller blandade episoder) observerades högre frekvenser för följande behandlingsuppkomna fynd, när som helst, i laboratorieanalyter jämfört med placebo: förhöjt ALAT (≥3X ULN) hos patienter med ALAT vid baseline
placebokontrollerade monoterapistudier med olanzapin på ungdomar observerades kliniskt signifikanta ALAT-höjningar (förändring från
EKG-förändringar
poolade studier av vuxna såväl som poolade studier av ungdomar fanns det inga signifikanta skillnader mellan olanzapin och placebo i andelen patienter som upplever potentiellt viktiga förändringar i EKG-parametrar, inklusive QT, QTc (Fridericia korrigerad) och PR-intervall. Olanzapinanvändning var associerad med en genomsnittlig ökning av hjärtfrekvensen jämfört med placebo (vuxna: +2,4 slag per minut vs ingen förändring med placebo; ungdomar: +6,3 slag per minut vs -5,1 slag per minut med placebo). Denna ökning av hjärtfrekvensen kan vara relaterad till olanzapins potential att inducera ortostatiska förändringar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av ZYPREXA efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det svårt att på ett tillförlitligt sätt uppskatta deras frekvens eller utvärdera ett orsakssamband till läkemedelsexponering.
Biverkningar som rapporterats sedan marknadsintroduktionen och som var temporärt (men inte nödvändigtvis kausalt) relaterade till ZYPREXA-behandling inkluderar följande: allergisk reaktion (t.ex. anafylaktoid reaktion, angioödem, klåda eller urtikaria), kolestatisk eller blandad leverskada, diabetisk koma, diabetisk ketoacidos, utsättningsreaktion (diafores, illamående eller kräkningar), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS), hepatit, gulsot, neutropeni, pankreatit, priapism, hudutslag, rastlösa bensyndrom, rabdomyolys, stamning1 och venösa tromboemboliska händelser (lungembolism) djup ventrombos). Slumpmässiga kolesterolnivåer på ≥240 mg/dL och slumpmässiga triglyceridnivåer på ≥1000 mg/dL har rapporterats.
1 Stamning studerades endast i orala och långverkande injektionsformuleringar (LAI).
LÄKEMEDELSINTERAKTIONER
Riskerna med att använda olanzapin i kombination med andra läkemedel har inte utvärderats utförligt i systematiska studier.
Potentiell för andra droger att påverka olanzapin
Diazepam
Samtidig administrering av diazepam och olanzapin förstärkte den ortostatiska hypotoni som observerades med olanzapin.
Cimetidin och antacida
Engångsdoser av cimetidin (800 mg) eller antacida innehållande aluminium och magnesium påverkade inte den orala biotillgängligheten av olanzapin.
Inducerare av CYP1A2
Karbamazepinbehandling (200 mg två gånger dagligen) orsakar en cirka 50 % ökning av clearance av olanzapin. Denna ökning beror sannolikt på det faktum att karbamazepin är en potent inducerare av CYP1A2-aktivitet. Högre dagliga doser av karbamazepin kan orsaka en ännu större ökning av olanzapinclearance.
Alkohol
Etanol (45 mg/70 kg engångsdos) hade ingen effekt på olanzapins farmakokinetik. Samtidig administrering av alkohol (dvs. etanol) med olanzapin förstärkte den ortostatiska hypotoni som observerades med olanzapin [se LÄKEMEDELSINTERAKTIONER ].
CYP1A2-hämmare
Fluvoxamin
Fluvoxamin, en CYP1A2-hämmare, minskar clearance av olanzapin. Detta resulterar i en genomsnittlig ökning av olanzapin Cmax efter fluvoxamin på 54 % hos kvinnliga icke-rökare och 77 % hos manliga rökare. Den genomsnittliga ökningen av AUC för olanzapin är 52 % respektive 108 %. Lägre doser av olanzapin bör övervägas hos patienter som får samtidig behandling med fluvoxamin.
CYP2D6-hämmare
Fluoxetin
Fluoxetin (60 mg engångsdos eller 60 mg daglig dos i 8 dagar) orsakar en liten (i genomsnitt 16 %) ökning av den maximala koncentrationen av olanzapin och en liten (i genomsnitt 16 %) minskning av olanzapin-clearance. Storleken på effekten av denna faktor är liten i jämförelse med den totala variationen mellan individer, och därför rekommenderas inte dosjustering rutinmässigt. När du använder ZYPREXA och fluoxetin i kombination, se även avsnittet Läkemedelsinteraktioner i bipacksedeln för Symbyax.
Warfarin
Warfarin (20 mg engångsdos) påverkade inte olanzapins farmakokinetik.
Inducerare av CYP1A2 eller glukuronyltransferas
Omeprazol och rifampin kan orsaka en ökning av olanzapinclearance.
Träkol
Administrering av aktivt kol (1 g) minskade Cmax och AUC för oralt olanzapin med cirka 60 %. Eftersom maximala olanzapinnivåer vanligtvis inte uppnås förrän cirka 6 timmar efter dosering, kan träkol vara en användbar behandling för överdosering av olanzapin.
Potentiell för Olanzapin att påverka andra droger
CNS-verkande droger
Med tanke på de primära CNS-effekterna av olanzapin, bör försiktighet iakttas när olanzapin tas i kombination med andra centralt verkande läkemedel och alkohol.
Antihypertensiva medel
Olanzapin kan, på grund av dess potential att inducera hypotoni, förstärka effekten av vissa antihypertensiva medel.
Levodopa och dopaminagonister
Olanzapin kan motverka effekterna av levodopa och dopaminagonister.
Lorazepam (IM)
Administrering av intramuskulär lorazepam (2 mg) 1 timme efter intramuskulär olanzapin för injektion (5 mg) påverkade inte farmakokinetiken för olanzapin, okonjugerat lorazepam eller total lorazepam signifikant. Denna samtidiga administrering av intramuskulär lorazepam och intramuskulär olanzapin för injektion bidrog dock till den somnolens som observerades med endera läkemedlet enbart [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Litium
Flera doser av olanzapin (10 mg under 8 dagar) påverkade inte kinetiken för litium. Därför kräver samtidig administrering av olanzapin inte dosjustering av litium [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Valproat
Olanzapin (10 mg dagligen i 2 veckor) påverkade inte steady state-plasmakoncentrationerna av valproat. Därför kräver samtidig administrering av olanzapin inte dosjustering av valproat [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Effekt av olanzapin på läkemedelsmetaboliserande enzymer
In vitro-studier med humana levermikrosomer tyder på att olanzapin har liten potential att hämma CYP1A2, CYP2C9, CYP2C19, CYP2D6 och CYP3A. Det är därför osannolikt att olanzapin orsakar kliniskt viktiga läkemedelsinteraktioner medierade av dessa enzymer.
Imipramin
Enstaka doser av olanzapin påverkade inte farmakokinetiken för imipramin eller dess aktiva metabolit desipramin.
Warfarin
Enstaka doser av olanzapin påverkade inte farmakokinetiken för warfarin.
Diazepam
Olanzapin påverkade inte farmakokinetiken för diazepam eller dess aktiva metabolit Ndesmetyldiazepam. Diazepam administrerat samtidigt med olanzapin ökade dock den ortostatiska hypotoni som observerades med endera läkemedlet givet ensamt.
Alkohol
Flera doser av olanzapin påverkade inte kinetiken för etanol.
Biperiden
Flera doser av olanzapin påverkade inte biperidens kinetik.
Teofyllin
Flera doser av olanzapin påverkade inte farmakokinetiken för teofyllin eller dess metaboliter.
Narkotikamissbruk och beroende
Beroende
studier som prospektivt utformats för att bedöma missbruk och beroendepotential visades olanzapin ha akuta depressiva CNS-effekter men liten eller ingen risk för missbruk eller fysiskt beroende hos råttor som administrerades orala doser upp till 15 gånger den dagliga orala MRHD (20 mg) och rhesusapor administrerade orala doser upp till 8 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta.
Olanzapin har inte systematiskt studerats på människor för dess potential för missbruk, tolerans eller fysiskt beroende. Även om de kliniska prövningarna inte avslöjade någon tendens till något läkemedelssökande beteende, var dessa observationer inte systematiska, och det är inte möjligt att utifrån denna begränsade erfarenhet förutsäga i vilken utsträckning ett CNS-aktivt läkemedel kommer att missbrukas, avledas , och/eller missbrukas när den väl har marknadsförts. Följaktligen bör patienter utvärderas noggrant med avseende på en historia av drogmissbruk, och sådana patienter bör observeras noggrant med avseende på tecken på felaktig användning eller missbruk av olanzapin (t.ex. utveckling av tolerans, ökad dos, läkemedelssökande beteende).
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
När du använder ZYPREXA 7,5 mg och fluoxetin i kombination, se även avsnittet Varningar och försiktighet i bipacksedeln för Symbyax.
Äldre patienter med demensrelaterad psykos
Ökad dödlighet
Äldre patienter med demensrelaterad psykos som behandlas med antipsykotiska läkemedel löper en ökad risk att dö. ZYPREXA 20mg är inte godkänt för behandling av patienter med demensrelaterad psykos [se VARNING I RUTA, Användning hos patienter med samtidig sjukdom och PATIENTINFORMATION].
I placebokontrollerade kliniska prövningar av äldre patienter med demensrelaterad psykos var incidensen av dödsfall hos olanzapinbehandlade patienter signifikant högre än placebobehandlade patienter (3,5 % respektive 1,5 %).
Cerebrovaskulära biverkningar (CVAE), inklusive stroke
Cerebrovaskulära biverkningar (t.ex. stroke, övergående ischemisk attack), inklusive dödsfall, rapporterades hos patienter i studier med olanzapin hos äldre patienter med demensrelaterad psykos. I placebokontrollerade studier var det en signifikant högre incidens av cerebrovaskulära biverkningar hos patienter behandlade med olanzapin jämfört med patienter behandlade med placebo. Olanzapin är inte godkänt för behandling av patienter med demensrelaterad psykos [se LÅDA VARNING och PATIENTINFORMATION ].
Självmord
Möjligheten till självmordsförsök är inneboende i schizofreni och vid bipolär störning I, och noggrann övervakning av högriskpatienter bör åtfölja läkemedelsbehandling. Recept för olanzapin bör skrivas ut för den minsta mängden tabletter som överensstämmer med god patienthantering, för att minska risken för överdosering.
Malignt neuroleptikasyndrom (NMS)
Ett potentiellt dödligt symtomkomplex som ibland kallas malignt neuroleptikasyndrom (NMS) har rapporterats i samband med administrering av antipsykotiska läkemedel, inklusive olanzapin. Kliniska manifestationer av NMS är hyperpyrexi, muskelstelhet, förändrad mental status och tecken på autonom instabilitet (oregelbunden puls eller blodtryck, takykardi, diafores och hjärtrytmrubbningar). Ytterligare tecken kan vara förhöjt kreatininfosfokinas, myoglobinuri (rabdomyolys) och akut njursvikt.
Den diagnostiska utvärderingen av patienter med detta syndrom är komplicerad. För att komma fram till en diagnos är det viktigt att utesluta fall där den kliniska presentationen inkluderar både allvarlig medicinsk sjukdom (t.ex. lunginflammation, systemisk infektion etc.) och obehandlade eller otillräckligt behandlade extrapyramidala tecken och symtom (EPS). Andra viktiga överväganden i differentialdiagnosen inkluderar central antikolinerg toxicitet, värmeslag, läkemedelsfeber och primär patologi i centrala nervsystemet.
Hanteringen av NMS bör innefatta: 1) omedelbart utsättande av antipsykotiska läkemedel och andra läkemedel som inte är nödvändiga för samtidig behandling; 2) intensiv symtomatisk behandling och medicinsk övervakning; och 3) behandling av eventuella samtidiga allvarliga medicinska problem för vilka specifika behandlingar finns tillgängliga. Det finns ingen allmän enighet om specifika farmakologiska behandlingsregimer för NMS.
Om en patient behöver antipsykotisk läkemedelsbehandling efter återhämtning från NMS, bör det potentiella återinförandet av läkemedelsbehandling noggrant övervägas. Patienten bör övervakas noggrant, eftersom återfall av NMS har rapporterats [se PATIENTINFORMATION ].
Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS)
Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) har rapporterats vid exponering för olanzapin. DRESS kan uppträda med en kutan reaktion (såsom hudutslag eller exfoliativ dermatit), eosinofili, feber och/eller lymfadenopati med systemiska komplikationer såsom hepatit, nefrit, pneumonit, myokardit och/eller perikardit. KLÄNNING är ibland ödesdigert. Avbryt behandlingen med olanzapin om du misstänker DRESS [se PATIENTINFORMATION ].
Metaboliska förändringar
Atypiska antipsykotiska läkemedel har associerats med metabola förändringar inklusive hyperglykemi, dyslipidemi och viktökning. Metaboliska förändringar kan vara associerade med ökad kardiovaskulär/cerebrovaskulär risk. Olanzapins specifika metaboliska profil presenteras nedan.
Hyperglykemi och diabetes mellitus
Sjukvårdsgivare bör överväga riskerna och fördelarna när de förskriver olanzapin till patienter med en fastställd diagnos av diabetes mellitus, eller som har gränsöverskridande förhöjd blodsockernivå (fastande 100-126 mg/dL, icke-fastande 140-200 mg/dL). Patienter som tar olanzapin bör övervakas regelbundet med avseende på försämrad glukoskontroll. Patienter som påbörjar behandling med olanzapin bör genomgå fasteblodsockertest i början av behandlingen och regelbundet under behandlingen. Alla patienter som behandlas med atypiska antipsykotika bör övervakas för symtom på hyperglykemi inklusive polydipsi, polyuri, polyfagi och svaghet. Patienter som utvecklar symtom på hyperglykemi under behandling med atypiska antipsykotika bör genomgå fasteblodsockertest. I vissa fall har hyperglykemi försvunnit när det atypiska antipsykotiska medlet avbröts; dock krävde vissa patienter fortsatt behandling mot diabetes trots utsättning av det misstänkta läkemedlet [se PATIENTINFORMATION ].
Hyperglykemi, i vissa fall extrem och förknippad med ketoacidos eller hyperosmolär koma eller död, har rapporterats hos patienter som behandlats med atypiska antipsykotika inklusive olanzapin. Bedömning av sambandet mellan atypisk antipsykotisk användning och glukosavvikelser kompliceras av möjligheten av en ökad bakgrundsrisk för diabetes mellitus hos patienter med schizofreni och den ökande incidensen av diabetes mellitus i den allmänna befolkningen. Epidemiologiska studier tyder på en ökad risk för behandlingsuppkomna hyperglykemirelaterade biverkningar hos patienter som behandlas med de atypiska antipsykotika. Även om relativa riskuppskattningar är inkonsekventa, verkar sambandet mellan atypiska antipsykotika och ökningar av glukosnivåer falla på ett kontinuum och olanzapin verkar ha ett större samband än vissa andra atypiska antipsykotika.
Genomsnittliga ökningar av blodsocker har observerats hos patienter som behandlats (medianexponering på 9,2 månader) med olanzapin i fas 1 av Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE). Den genomsnittliga ökningen av serumglukos (fastande och icke-fastande prover) från baslinjen till genomsnittet av de två högsta serumkoncentrationerna var 15,0 mg/dL.
I en studie med friska frivilliga försökspersoner som fick olanzapin (N=22) under 3 veckor hade en genomsnittlig ökning av fasteblodsockret på 2,3 mg/dL jämfört med baslinjen. Placebobehandlade försökspersoner (N=19) hade en genomsnittlig ökning av fastande blodsocker jämfört med baslinjen på 0,34 mg/dL.
Olanzapin monoterapi hos vuxna
en analys av 5 placebokontrollerade vuxna olanzapin monoterapistudier med en medianbehandlingstid på cirka 3 veckor, var olanzapin associerad med en större genomsnittlig förändring av fasteglukosnivåer jämfört med placebo (2,76 mg/dL mot 0,17 mg/dL). Skillnaden i genomsnittliga förändringar mellan olanzapin och placebo var större hos patienter med tecken på glukosdysregulation vid baslinjen (patienter diagnostiserade med diabetes mellitus eller relaterade biverkningar, patienter som behandlats med antidiabetika, patienter med en slumpmässig slumpmässig glukosnivå vid baslinjen ≥200 mg/ dL och/eller en baslinjevärde för fasteglukosnivå ≥126 mg/dL). Olanzapinbehandlade patienter hade en större genomsnittlig HbA1c-ökning från baslinjen på 0,04 % (medianexponering 21 dagar), jämfört med en genomsnittlig HbA1c-minskning på 0,06 % hos placebobehandlade försökspersoner (medianexponering 17 dagar).
en analys av 8 placebokontrollerade studier (medianbehandlingsexponering 4-5 veckor) hade 6,1 % av de olanzapinbehandlade försökspersonerna (N=855) behandlingsutlöst glykosuri jämfört med 2,8 % av de placebobehandlade försökspersonerna (N=599) . Tabell 2 visar kortsiktiga och långvariga förändringar i fastande glukosnivåer från monoterapistudier med olanzapin hos vuxna.
Den genomsnittliga förändringen i fasteglukos för patienter exponerade i minst 48 veckor var 4,2 mg/dL (N=487). I analyser av patienter som fullföljt 9-12 månaders behandling med olanzapin, fortsatte den genomsnittliga förändringen i fastande och icke-fastande glukosnivåer att öka över tiden.
Olanzapin monoterapi hos ungdomar
Säkerheten och effekten av olanzapin har inte fastställts hos patienter under 13 år. I en analys av 3 placebokontrollerade monoterapistudier av olanzapin på ungdomar, inklusive de med schizofreni (6 veckor) eller bipolär störning I (maniska eller blandade episoder) (3 veckor), var olanzapin associerat med en större genomsnittlig förändring från baslinjen vid fasta glukosnivåer jämfört med placebo (2,68 mg/dL mot -2,59 mg/dL). Den genomsnittliga förändringen i fasteglukos för ungdomar exponerade i minst 24 veckor var 3,1 mg/dL (N=121). Tabell 3 visar kortsiktiga och långvariga förändringar i fastande blodsocker från monoterapistudier med olanzapin hos ungdomar.
Dyslipidemi
Oönskade förändringar i lipider har observerats vid användning av olanzapin. Klinisk övervakning, inklusive baslinje och periodisk uppföljning av lipidutvärderingar hos patienter som använder olanzapin, rekommenderas [se PATIENTINFORMATION ].
Kliniskt signifikanta, och ibland mycket höga (>500 mg/dL), förhöjda triglyceridnivåer har observerats vid användning av olanzapin. Måttliga genomsnittliga ökningar av totalt kolesterol har också setts vid användning av olanzapin.
Olanzapin monoterapi hos vuxna
en analys av 5 placebokontrollerade monoterapistudier med olanzapin med behandlingslängd upp till 12 veckor, hade olanzapinbehandlade patienter ökningar från baslinjen i genomsnittligt fastande totalkolesterol, LDL-kolesterol och triglycerider på 5,3 mg/dL, 3,0 mg/dL och 20,8 mg/dL respektive minskning från baslinjen i genomsnittligt fastande totalkolesterol, LDL-kolesterol och triglycerider på 6,1 mg/dL, 4,3 mg/dL och 10,7 mg/dL för placebobehandlade patienter. För fastande HDL-kolesterol observerades inga kliniskt betydelsefulla skillnader mellan olanzapinbehandlade patienter och placebobehandlade patienter. Genomsnittliga ökningar av fastande lipidvärden (totalkolesterol, LDL-kolesterol och triglycerider) var större hos patienter utan tecken på lipiddysregulation vid baslinjen, där lipiddysregulation definierades som patienter med diagnosen dyslipidemi eller relaterade biverkningar, patienter behandlade med lipidsänkande medel, eller patienter med höga lipidnivåer vid baslinjen.
långtidsstudier (minst 48 veckor) hade patienterna ökningar från baslinjen i genomsnittligt fastande totalkolesterol, LDL-kolesterol och triglycerider på 5,6 mg/dL, 2,5 mg/dL respektive 18,7 mg/dL och ett medelvärde minskning av HDL-kolesterol vid fastande med 0,16 mg/dL. I en analys av patienter som fullföljde 12 månaders behandling ökade inte det genomsnittliga totala kolesterolet vid fastande ytterligare efter cirka 4-6 månader.
Andelen patienter som hade förändringar (minst en gång) i totalt kolesterol, LDL-kolesterol eller triglycerider från normalt eller borderline till högt, eller förändringar i HDL-kolesterol från normalt eller borderline till lågt, var större i långtidsstudier (minst 48 veckor) jämfört med korttidsstudier. Tabell 4 visar kategoriska förändringar i fastande lipidvärden.
fas 1 av Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE), över en medianexponering på 9,2 månader, var den genomsnittliga ökningen av triglycerider hos patienter som tog olanzapin 40,5 mg/dL. I fas 1 av CATIE var den genomsnittliga ökningen av totalt kolesterol 9,4 mg/dL.
Olanzapin monoterapi hos ungdomar
Säkerheten och effekten av olanzapin har inte fastställts hos patienter under 13 år. I en analys av 3 placebokontrollerade olanzapin monoterapistudier av ungdomar, inklusive de med schizofreni (6 veckor) eller bipolär störning I (maniska eller blandade episoder) (3 veckor), hade olanzapinbehandlade ungdomar ökningar från baslinjen i genomsnittligt fastande totalkolesterol, LDL kolesterol och triglycerider på 12,9 mg/dL, 6,5 mg/dL respektive 28,4 mg/dL, jämfört med ökningar från baslinjen i genomsnittligt fastande totalkolesterol och LDL-kolesterol på 1,3 mg/dL och 1,0 mg/dL, och en minskning i triglycerider på 1,1 mg/dL för placebobehandlade ungdomar. För fastande HDL-kolesterol observerades inga kliniskt betydelsefulla skillnader mellan olanzapinbehandlade ungdomar och placebobehandlade ungdomar.
långtidsstudier (minst 24 veckor) hade ungdomar ökningar från baslinjen i genomsnittligt fastande totalkolesterol, LDL-kolesterol och triglycerider på 5,5 mg/dL, 5,4 mg/dL respektive 20,5 mg/dL och ett medelvärde minskning av HDL-kolesterol vid fastande med 4,5 mg/dL. Tabell 5 visar kategoriska förändringar i fastande lipidvärden hos ungdomar.
Viktökning
Potentiella konsekvenser av viktökning bör övervägas innan behandling med olanzapin påbörjas. Patienter som får olanzapin bör få regelbunden kontroll av vikten [se Information om patientrådgivning ].
Olanzapin monoterapi hos vuxna
en analys av 13 placebokontrollerade monoterapistudier med olanzapin ökade olanzapinbehandlade patienter i genomsnitt 2,6 kg (5,7 lb) jämfört med en genomsnittlig viktminskning på 0,3 kg (0,6 lb) hos placebobehandlade patienter med en medianexponering på 6 veckor ; 22,2 % av olanzapinbehandlade patienter gick upp minst 7 % av sin baslinjevikt, jämfört med 3 % av placebobehandlade patienter, med en medianexponering för händelsen på 8 veckor; 4,2 % av olanzapinbehandlade patienter gick upp minst 15 % av sin baslinjevikt, jämfört med 0,3 % av placebobehandlade patienter, med en medianexponering för händelsen på 12 veckor. Kliniskt signifikant viktökning observerades över alla baseline Body Mass Index (BMI) kategorier. Utsättning på grund av viktökning inträffade hos 0,2 % av olanzapinbehandlade patienter och hos 0 % av placebobehandlade patienter.
långtidsstudier (minst 48 veckor) var den genomsnittliga viktökningen 5,6 kg (12,3 lb) (medianexponering på 573 dagar, N=2021). Andelen patienter som gick upp minst 7 %, 15 % eller 25 % av sin kroppsvikt vid långtidsexponering var 64 %, 32 % respektive 12 %. Utsättning på grund av viktökning inträffade hos 0,4 % av olanzapinbehandlade patienter efter minst 48 veckors exponering.
Tabell 6 inkluderar data om viktökning hos vuxna med olanzapin sammanslagna från 86 kliniska prövningar. Uppgifterna i varje kolumn representerar data för de patienter som fullföljt behandlingsperioder av den angivna varaktigheten.
Skillnader i dosgrupper med avseende på viktökning har observerats. I en enda 8-veckors randomiserad, dubbelblind studie med fast dos som jämförde 10 (N=199), 20 (N=200) och 40 (N=200) mg/dag oralt olanzapin hos vuxna patienter med schizofreni eller schizoaffektiv sjukdom, genomsnittlig viktökning från baslinjen till slutpunkten (10 mg/dag: 1,9 kg; 20 mg/dag: 2,3 kg; 40 mg/dag: 3 kg) observerades med signifikanta skillnader mellan 10 och 40 mg/dag.
Olanzapin monoterapi hos ungdomar
Säkerheten och effekten av olanzapin har inte fastställts hos patienter under 13 år. Den genomsnittliga viktökningen hos ungdomar var större än hos vuxna. I 4 placebokontrollerade studier inträffade avbrott på grund av viktökning hos 1 % av olanzapinbehandlade patienter, jämfört med 0 % av placebobehandlade patienter.
långtidsstudier (minst 24 veckor) var den genomsnittliga viktökningen 11,2 kg (24,6 lb); (medianexponering på 201 dagar, N=179). Andelen ungdomar som gick upp minst 7 %, 15 % eller 25 % av sin baslinjekroppsvikt med långvarig exponering var 89 %, 55 % respektive 29 %. Bland ungdomar var den genomsnittliga viktökningen efter BMI-kategori vid baslinjen 11,5 kg (25,3 lb), 12,1 kg (26,6 lb) respektive 12,7 kg (27,9 lb) för normal (N=106), övervikt (N=26) och fetma (N=17). Avbrott på grund av viktökning inträffade hos 2,2 % av olanzapinbehandlade patienter efter minst 24 veckors exponering.
Tabell 8 visar data om viktökning hos ungdomar med olanzapin sammanslagna från 6 kliniska prövningar. Uppgifterna i varje kolumn representerar data för de patienter som fullföljt behandlingsperioder av den angivna varaktigheten. Det finns få data från kliniska prövningar om viktökning hos ungdomar med olanzapin efter 6 månaders behandling.
Tardiv dyskinesi
Ett syndrom med potentiellt irreversibla, ofrivilliga, dyskinetiska rörelser kan utvecklas hos patienter som behandlas med antipsykotiska läkemedel. Även om prevalensen av syndromet verkar vara högst bland äldre, särskilt äldre kvinnor, är det omöjligt att förlita sig på prevalensuppskattningar för att förutsäga, vid inledningen av antipsykotisk behandling, vilka patienter som sannolikt kommer att utveckla syndromet. Huruvida antipsykotiska läkemedel skiljer sig i deras potential att orsaka tardiv dyskinesi är okänt.
Risken för att utveckla tardiv dyskinesi och sannolikheten att den blir irreversibel tros öka när behandlingstiden och den totala kumulativa dosen av antipsykotiska läkemedel som ges till patienten ökar. Syndromet kan dock utvecklas, även om det är mycket mindre vanligt, efter relativt korta behandlingsperioder vid låga doser eller kan till och med uppstå efter avslutad behandling.
Tardiv dyskinesi kan försvinna, delvis eller helt, om antipsykotisk behandling avbryts. Antipsykotisk behandling i sig kan dock undertrycka (eller delvis undertrycka) tecknen och symtomen på syndromet och kan därigenom eventuellt maskera den underliggande processen. Effekten som symtomatisk suppression har på det långvariga förloppet av syndromet är okänd.
Mot bakgrund av dessa överväganden bör olanzapin förskrivas på ett sätt som med största sannolikhet minimerar förekomsten av tardiv dyskinesi. Kronisk antipsykotisk behandling bör i allmänhet reserveras för patienter (1) som lider av en kronisk sjukdom som är känd för att svara på antipsykotiska läkemedel, och (2) för vilka alternativa, lika effektiva men potentiellt mindre skadliga behandlingar inte är tillgängliga eller lämpliga. Hos patienter som behöver kronisk behandling bör den minsta dosen och den kortaste behandlingstiden som ger ett tillfredsställande kliniskt svar eftersträvas. Behovet av fortsatt behandling bör omprövas med jämna mellanrum.
Om tecken och symtom på tardiv dyskinesi uppträder hos en patient som behandlas med olanzapin, bör utsättning av läkemedel övervägas. Vissa patienter kan dock behöva behandling med olanzapin trots förekomsten av syndromet.
För specifik information om varningarna för litium eller valproat, se avsnittet Varningar i bipacksedeln för dessa andra produkter.
Ortostatisk hypotension
Olanzapin kan inducera ortostatisk hypotoni associerad med yrsel, takykardi, bradykardi och, hos vissa patienter, synkope, särskilt under den initiala dostitreringsperioden, vilket troligen återspeglar dess α1-adrenerga antagonistiska egenskaper [se Information om patientrådgivning ].
Från en analys av data om vitala tecken i en integrerad databas med 41 avslutade kliniska studier på vuxna patienter som behandlats med oralt olanzapin, registrerades ortostatisk hypotoni hos ≥20 % (1277/6030) av patienterna.
För oral olanzapinbehandling kan risken för ortostatisk hypotoni och synkope minimeras genom att inleda behandlingen med 5 mg QD [se DOSERING OCH ADMINISTRERING ]. En mer gradvis titrering till måldosen bör övervägas om hypotoni inträffar.
Hypotension, bradykardi med eller utan hypotoni, takykardi och synkope rapporterades också under de kliniska prövningarna med intramuskulärt olanzapin för injektion. I en öppen klinisk farmakologisk studie på icke-agiterade patienter med schizofreni där säkerheten och tolerabiliteten för intramuskulärt olanzapin utvärderades under en maximal doseringsregim (tre 10 mg doser administrerade med 4 timmars mellanrum), upplevde ungefär en tredjedel av dessa patienter en signifikant ortostatisk minskning av systoliskt blodtryck (dvs minskning ≥30 mmHg) [se DOSERING OCH ADMINISTRERING ]. Synkope rapporterades hos 0,6 % (15/2500) av olanzapinbehandlade patienter i fas 2-3 orala olanzapinstudier och hos 0,3 % (2/722) av olanzapinbehandlade patienter med agitation i intramuskulära olanzapin för injektionsstudier. Tre normala frivilliga i fas 1-studier med intramuskulärt olanzapin upplevde hypotoni, bradykardi och sinuspauser på upp till 6 sekunder som spontant försvann (i 2 fall inträffade reaktionerna på intramuskulärt olanzapin och i 1 fall på oralt olanzapin). Risken för denna sekvens av hypotoni, bradykardi och sinuspaus kan vara större hos icke-psykiatriska patienter jämfört med psykiatriska patienter som möjligen är mer anpassade till vissa effekter av psykofarmaka. För intramuskulär olanzapin för injektionsbehandling ska patienter förbli liggande om de är dåsiga eller yra efter injektionen tills undersökning har visat att de inte upplever postural hypotoni, bradykardi och/eller hypoventilation.
Olanzapin ska användas med särskild försiktighet till patienter med känd hjärt-kärlsjukdom (historia av hjärtinfarkt eller ischemi, hjärtsvikt eller överledningsstörningar), cerebrovaskulär sjukdom och tillstånd som skulle predisponera patienter för hypotoni (dehydrering, hypovolemi och behandling med antihypertensiva läkemedel ) där förekomsten av synkope eller hypotoni och/eller bradykardi kan utsätta patienten för en ökad medicinsk risk.
Försiktighet är nödvändig hos patienter som får behandling med andra läkemedel som har effekter som kan inducera hypotoni, bradykardi, andnings- eller centrala nervsystemets depression [se LÄKEMEDELSINTERAKTIONER ]. Samtidig administrering av intramuskulärt olanzapin och parenteralt bensodiazepin rekommenderas inte på grund av risken för överdriven sedering och kardiorespiratorisk depression.
Falls
ZYPREXA kan orsaka somnolens, postural hypotoni, motorisk och sensorisk instabilitet, vilket kan leda till fall och följaktligen frakturer eller andra skador. För patienter med sjukdomar, tillstånd eller mediciner som kan förvärra dessa effekter, slutföra fallriskbedömningar vid inledande av antipsykotisk behandling och återkommande för patienter på långvarig antipsykotisk behandling.
Leukopeni, Neutropeni och Agranulocytos
Klasseffekt
I kliniska prövningar och/eller erfarenheter efter marknadsföring har händelser av leukopeni/neutropeni rapporterats tidsmässigt relaterade till antipsykotiska medel, inklusive ZYPREXA. Agranulocytos har också rapporterats.
Möjliga riskfaktorer för leukopeni/neutropeni inkluderar redan existerande lågt antal vita blodkroppar (WBC) och historia av läkemedelsinducerad leukopeni/neutropeni. Patienter med en anamnes på kliniskt signifikant lågt WBC eller läkemedelsinducerad leukopeni/neutropeni bör få sitt fullständiga blodvärde (CBC) kontrollerat ofta under de första månaderna av behandlingen och utsättande av ZYPREXA bör övervägas vid första tecken på en kliniskt signifikant minskning i WBC i frånvaro av andra orsaksfaktorer.
Patienter med kliniskt signifikant neutropeni bör övervakas noggrant med avseende på feber eller andra symtom eller tecken på infektion och behandlas omedelbart om sådana symtom eller tecken uppstår. Patienter med svår neutropeni (absolut neutrofilantal
Dysfagi
Esofageal dysmotilitet och aspiration har associerats med användning av antipsykotiska läkemedel. Aspirationspneumoni är en vanlig orsak till sjuklighet och dödlighet hos patienter med avancerad Alzheimers sjukdom. Olanzapin är inte godkänt för behandling av patienter med Alzheimers sjukdom.
Anfall
Under premarketingtestning inträffade anfall hos 0,9 % (22/2500) av olanzapinbehandlade patienter. Det fanns förvirrande faktorer som kan ha bidragit till förekomsten av anfall i många av dessa fall. Olanzapin ska användas med försiktighet till patienter med anamnes på anfall eller med tillstånd som potentiellt sänker kramptröskeln, t.ex. Alzheimers demens. Olanzapin är inte godkänt för behandling av patienter med Alzheimers sjukdom. Tillstånd som sänker anfallströskeln kan vara vanligare i en befolkning på 65 år eller äldre.
Potential för kognitiv och motorisk funktionsnedsättning
Somnolens var en vanligen rapporterad biverkning i samband med behandling med olanzapin, som inträffade med en incidens på 26 % hos olanzapinpatienter jämfört med 15 % hos placebopatienter. Denna biverkning var också dosrelaterad. Somnolens ledde till utsättning av behandlingen hos 0,4 % (9/2500) av patienterna i premarketingdatabasen.
Eftersom olanzapin har potential att försämra omdöme, tänkande eller motorik, bör patienter varnas för att använda farliga maskiner, inklusive bilar, tills de är rimligt säkra på att olanzapinbehandling inte påverkar dem negativt [se Information om patientrådgivning ].
Reglering av kroppstemperatur
Störningar i kroppens förmåga att sänka kroppstemperaturen har tillskrivits antipsykotiska medel. Lämplig vård rekommenderas vid förskrivning av olanzapin till patienter som kommer att uppleva tillstånd som kan bidra till en höjning av kroppstemperaturen, t.ex. ansträngande träning, exponering för extrem värme, samtidig medicinering med antikolinerg aktivitet eller uttorkning [se PATIENTINFORMATION ].
Användning hos patienter med samtidig sjukdom
Klinisk erfarenhet av olanzapin hos patienter med vissa samtidiga systemiska sjukdomar är begränsad [se KLINISK FARMAKOLOGI ].
Olanzapin uppvisar in vitro muskarinreceptoraffinitet. I kliniska prövningar före marknadsföring med olanzapin var olanzapin associerat med förstoppning, muntorrhet och takykardi, alla biverkningar möjligen relaterade till kolinerg antagonism. Sådana biverkningar var inte ofta grunden för utsättningar av olanzapin, men olanzapin bör användas med försiktighet hos patienter med kliniskt signifikant prostatahypertrofi, trångvinkelglaukom eller en historia av paralytisk ileus eller relaterade tillstånd.
5 placebokontrollerade studier av olanzapin hos äldre patienter med demensrelaterad psykos (n=1184), rapporterades följande behandlingsuppkomna biverkningar hos olanzapinbehandlade patienter med en incidens på minst 2 % och signifikant högre än placebo- behandlade patienter: fall, somnolens, perifert ödem, onormal gång, urininkontinens, letargi, ökad vikt, asteni, pyrexi, lunginflammation, muntorrhet och synhallucinationer. Frekvensen av avbrott på grund av biverkningar var högre med olanzapin än placebo (13 % mot 7 %). Äldre patienter med demensrelaterad psykos som behandlas med olanzapin löper en ökad risk att dö jämfört med placebo. Olanzapin är inte godkänt för behandling av patienter med demensrelaterad psykos [se LÅDA VARNING , Äldre patienter med demensrelaterad psykos , och PATIENTINFORMATION ].
Olanzapin har inte utvärderats eller använts i någon nämnvärd omfattning hos patienter med en nyligen anamnes på hjärtinfarkt eller instabil hjärtsjukdom. Patienter med dessa diagnoser uteslöts från kliniska studier före marknadsföring. På grund av risken för ortostatisk hypotoni med olanzapin bör försiktighet iakttas hos hjärtpatienter [se Ortostatisk hypotension ].
Hyperprolaktinemi
Som med andra läkemedel som antagoniserar dopamin D2-receptorer, höjer olanzapin prolaktinnivåerna och höjningen kvarstår under kronisk administrering. Hyperprolaktinemi kan undertrycka hypotalamisk GnRH, vilket resulterar i minskad hypofysgonadotropinsekretion. Detta kan i sin tur hämma reproduktionsfunktionen genom att försämra gonadal steroidogenes hos både kvinnliga och manliga patienter. Galaktorré, amenorré, gynekomasti och impotens har rapporterats hos patienter som fått prolaktinhöjande substanser. Långvarig hyperprolaktinemi i samband med hypogonadism kan leda till minskad bentäthet hos både kvinnliga och manliga försökspersoner.
Vävnadsodlingsexperiment indikerar att ungefär en tredjedel av humana bröstcancer är prolaktinberoende in vitro, en faktor av potentiell betydelse om förskrivning av dessa läkemedel övervägs hos en patient med tidigare upptäckt bröstcancer. Som är vanligt med föreningar som ökar prolaktinfrisättningen observerades en ökning av bröstkörtelneoplasi i olanzapins karcinogenicitetsstudier på möss och råttor [se Icke-klinisk toxikologi ]. Varken kliniska studier eller epidemiologiska studier genomförda hittills har visat ett samband mellan kronisk administrering av denna klass av läkemedel och tumörbildning hos människor; den tillgängliga bevisningen anses vara för begränsad för att vara avgörande vid denna tidpunkt.
placebokontrollerade olanzapin kliniska studier (upp till 12 veckor) observerades förändringar från normala till höga i prolaktinkoncentrationer hos 30 % av de vuxna som behandlades med olanzapin jämfört med 10,5 % av de vuxna som behandlades med placebo. I en poolad analys från kliniska studier inklusive 8136 vuxna behandlade med olanzapin, inkluderade potentiellt associerade kliniska manifestationer menstruationsrelaterade händelser1 (2 % [49/3240] av kvinnorna), sexuella funktionsrelaterade händelser2 (2 % [150/8136] av kvinnorna) och män), och bröstrelaterade händelser3 (0,7 % [23/3240] av kvinnorna, 0,2 % [9/4896] av männen).
placebokontrollerade monoterapistudier med olanzapin på ungdomar (upp till 6 veckor) med schizofreni eller bipolär störning I (maniska eller blandade episoder) observerades förändringar från normala till höga prolaktinkoncentrationer hos 47 % av olanzapinbehandlade patienter jämfört med 7 % av placebobehandlade patienter. I en poolad analys från kliniska prövningar inkluderande 454 ungdomar behandlade med olanzapin, inkluderade potentiellt associerade kliniska manifestationer menstruationsrelaterade händelser1 (1 % [2/168] av kvinnorna), sexuella funktionsrelaterade händelser2 (0,7 % [3/454] av kvinnor och män ), och bröstrelaterade händelser3 (2 % [3/168] av kvinnorna, 2 % [7/286] av männen) [se Användning i specifika populationer ].
1 Baserat på en sökning av följande termer: amenorré, hypomenorré, försenad menstruation och oligomenorré.
2 Baserat på en sökning av följande termer: anorgasmi, försenad ejakulation, erektil dysfunktion, minskad libido, förlust av libido, onormal orgasm och sexuell dysfunktion.
Baserat på en sökning av följande termer: flytningar från brösten, förstoring eller svullnad, galaktorré, gynekomasti och amningsstörning.
Skillnader i dosgrupper med avseende på prolaktinhöjning har observerats. I en enda 8-veckors randomiserad, dubbelblind studie med fast dos som jämförde 10 (N=199), 20 (N=200) och 40 (N=200) mg/dag oralt olanzapin hos vuxna patienter med schizofreni eller schizoaffektiv störning, incidens av prolaktinhöjning >24,2 ng/ml (kvinna) eller >18,77 ng/ml (man) när som helst under försöket (10 mg/dag: 31,2 %; 20 mg/dag: 42,7 %; 40 mg/dag : 61,1 %) indikerade signifikanta skillnader mellan 10 vs 40 mg/dag och 20 vs 40 mg/dag.
Använd i kombination med fluoxetin, litium eller valproat
Vid användning av ZYPREXA och fluoxetin i kombination, ska förskrivaren även se avsnittet Varningar och försiktighet i bipacksedeln för Symbyax. När ZYPREXA används i kombination med litium eller valproat, ska förskrivaren hänvisa till avsnitten Varningar och försiktighet i bipacksedeln för litium eller valproat [se LÄKEMEDELSINTERAKTIONER ].
Laboratorietester
Fastande blodsockertest och lipidprofil i början av och periodvis under behandlingen rekommenderas [se Metaboliska förändringar och PATIENTINFORMATION ].
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide ) för de orala formuleringarna.
Patienter bör informeras om följande problem och uppmanas att varna sin förskrivare om dessa inträffar när de tar ZYPREXA 15 mg som monoterapi eller i kombination med fluoxetin. Om du inte tror att du blir bättre eller om du är orolig över ditt tillstånd när du tar ZYPREXA 2,5 mg, kontakta din läkare. Vid användning av ZYPREXA och fluoxetin i kombination, se även avsnittet Patientrådgivningsinformation i bipacksedeln för Symbyax.
Äldre patienter med demensrelaterad psykos: ökad dödlighet och cerebrovaskulära biverkningar (CVAE), inklusive stroke
Patienter och vårdgivare bör informeras om att äldre patienter med demensrelaterad psykos som behandlas med antipsykotiska läkemedel löper en ökad risk att dö. Patienter och vårdgivare bör informeras om att äldre patienter med demensrelaterad psykos som behandlats med ZYPREXA hade en signifikant högre incidens av cerebrovaskulära biverkningar (t.ex. stroke, övergående ischemisk attack) jämfört med placebo.
ZYPREXA är inte godkänt för äldre patienter med demensrelaterad psykos [se LÅDA VARNING och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Malignt neuroleptikasyndrom (NMS)
Patienter och vårdgivare bör informeras om att ett potentiellt dödligt symtomkomplex som ibland kallas NMS har rapporterats i samband med administrering av antipsykotiska läkemedel, inklusive ZYPREXA. Tecken och symtom på NMS inkluderar hyperpyrexi, muskelstelhet, förändrad mental status och tecken på autonom instabilitet (oregelbunden puls eller blodtryck, takykardi, diafores och hjärtrytmrubbningar) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS)
Patienter bör rådas att rapportera till sin vårdgivare vid tidigast debut av tecken och symtom som kan vara associerade med läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hyperglykemi och diabetes mellitus
Patienter bör informeras om den potentiella risken för hyperglykemirelaterade biverkningar. Patienter bör övervakas regelbundet med avseende på försämrad glukoskontroll. Patienter som har diabetes ska följa sin läkares instruktioner om hur ofta de ska kontrollera sitt blodsocker medan de tar ZYPREXA [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Dyslipidemi
Patienter bör informeras om att dyslipidemi har inträffat under behandling med ZYPREXA. Patienter bör få sin lipidprofil övervakad regelbundet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Viktökning
Patienter bör informeras om att viktökning har skett under behandling med ZYPREXA. Patienter bör få sin vikt övervakad regelbundet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Ortostatisk hypotension
Patienter bör informeras om risken för ortostatisk hypotoni, särskilt under perioden med initial dostitrering och i samband med samtidig användning av läkemedel som kan förstärka den ortostatiska effekten av ZYPREXA, t.ex. diazepam eller alkohol [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och LÄKEMEDELSINTERAKTIONER ]. Patienter bör rådas att byta position försiktigt för att förhindra ortostatisk hypotoni och att lägga sig ner om de känner sig yr eller svimmar tills de mår bättre. Patienter bör rådas att ringa sin läkare om de upplever något av följande tecken och symtom i samband med ortostatisk hypotoni: yrsel, snabba eller långsamma hjärtslag eller svimning.
Potential för kognitiv och motorisk funktionsnedsättning
Eftersom ZYPREXA har potential att försämra omdöme, tänkande eller motorik, bör patienter varnas för att använda farliga maskiner, inklusive bilar, tills de är rimligt säkra på att ZYPREXA-terapi inte påverkar dem negativt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Reglering av kroppstemperatur
Patienter bör informeras om lämplig vård för att undvika överhettning och uttorkning. Patienter bör rådas att omedelbart ringa sin läkare om de blir allvarligt sjuka och har några eller alla av dessa symtom på uttorkning: svettas för mycket eller inte alls, muntorrhet, känna sig mycket varm, känna sig törstig, inte kunna producera urin [ ser VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Samtidig medicinering
Patienter bör rådas att informera sin vårdgivare om de tar eller planerar att ta Symbyax. Patienter bör också rådas att informera sin vårdgivare om de tar, planerar att ta eller har slutat ta några receptbelagda eller receptfria läkemedel, inklusive växtbaserade kosttillskott, eftersom det finns risk för interaktioner [se LÄKEMEDELSINTERAKTIONER ].
Alkohol
Patienter bör rådas att undvika alkohol medan de tar ZYPREXA [se LÄKEMEDELSINTERAKTIONER ].
Fenylketonurik
ZYPREXA 10mg ZYDIS (olanzapin oralt sönderfallande tabletter) innehåller fenylalanin (0,34, 0,45, 0,67 eller 0,90 mg per 5, 10, 15 respektive 20 mg tablett) [se BESKRIVNING ].
Användning i specifika populationer
Graviditet
Rekommendera kvinnor att meddela sin vårdgivare om de blir gravida eller planerar att bli gravida under behandling med ZYPREXA. Informera patienter om att ZYPREXA kan orsaka extrapyramidala symtom och/eller abstinenssymtom (agitation, hypertoni, hypotoni, tremor, somnolens, andnöd och ätstörningar) hos en nyfödd. Informera patienter om att det finns ett graviditetsexponeringsregister som övervakar graviditetsresultat hos kvinnor som exponerats för ZYPREXA 7,5 mg under graviditeten [se Användning i specifika populationer ].
Laktation
Rekommendera ammande kvinnor som använder ZYPREXA 20 mg för att övervaka spädbarn för överdriven sedering, irritabilitet, dålig matning och extrapyramidala symtom (skakningar och onormala muskelrörelser) och att söka läkarvård om de märker dessa tecken. [ser Användning i specifika populationer ].
Infertilitet
Informera kvinnor med reproduktionspotential att ZYPREXA kan försämra fertiliteten på grund av en ökning av serumprolaktinnivåerna. Effekterna på fertiliteten är reversibla [se Användning i specifika populationer ].
Pediatrisk användning
ZYPREXA 15 mg är indicerat för behandling av schizofreni och maniska eller blandade episoder associerade med bipolär störning I hos ungdomar 13 till 17 år. Jämfört med patienter från kliniska prövningar för vuxna var det sannolikt att ungdomar gick upp mer i vikt, upplevde ökad sedering och hade större ökningar av totalkolesterol, triglycerider, LDL-kolesterol, prolaktin och leveraminotransferasnivåer. Patienter bör rådgöras om de potentiella långsiktiga riskerna förknippade med ZYPREXA och informeras om att dessa risker kan leda till att de överväger andra läkemedel först [se INDIKATIONER OCH ANVÄNDNING ]. Säkerhet och effektivitet för ZYPREXA 5 mg hos patienter under 13 år har inte fastställts. Säkerhet och effekt av ZYPREXA 15 mg och fluoxetin i kombination hos patienter 10 till 17 år har fastställts för akut behandling av depressiva episoder associerade med bipolär störning I. Säkerhet och effektivitet för ZYPREXA och fluoxetin i kombination hos patienter VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Behov av omfattande behandlingsprogram hos pediatriska patienter
ZYPREXA 20 mg är indicerat som en integrerad del av ett totalt behandlingsprogram för pediatriska patienter med schizofreni och bipolär sjukdom som kan innefatta andra åtgärder (psykologiska, pedagogiska, sociala) för patienter med sjukdomen. Effektivitet och säkerhet för ZYPREXA 7,5 mg har inte fastställts hos pediatriska patienter under 13 år. Atypiska antipsykotika är inte avsedda för användning på pediatriska patienter som uppvisar symtom sekundära till miljöfaktorer och/eller andra primära psykiatriska störningar. Lämplig utbildningsplacering är avgörande och psykosociala insatser är ofta till hjälp. Beslutet att förskriva atypiska antipsykotiska läkemedel kommer att bero på vårdgivarens bedömning av kroniska och svårighetsgraden av patientens symtom [se INDIKATIONER OCH ANVÄNDNING ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
Orala karcinogenicitetsstudier utfördes på möss och råttor. Olanzapin administrerades till möss i två 78-veckorsstudier i doser på 3, 10, 30/20 mg/kg/dag (motsvarande 0,8-5 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta) och 0,25, 2 , 8 mg/kg/dag (motsvarande 0,06-2 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta). Råttor doserades i 2 år i doser på 0,25, 1, 2,5, 4 mg/kg/dag (hanar) och 0,25, 1, 4, 8 mg/kg/dag (honor) (motsvarande 0,13-2 och 0,13-4 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta respektive). Incidensen av leverhemangiom och hemangiosarkom ökade signifikant i en musstudie på honmöss vid 2 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta. Dessa tumörer ökade inte i en annan musstudie på honor som doserades upp till 2-5 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta; i denna studie var det en hög förekomst av tidig dödlighet hos män i gruppen 30/20 mg/kg/dag. Incidensen av bröstkörteladenom och adenokarcinom ökade signifikant hos möss av honkön doserade ≥2 mg/kg/dag och honråttor doserade med ≥4 mg/kg/dag (0,5 och 2 gånger den dagliga orala MRHD baserat på mg/m²) kroppsyta, respektive). Antipsykotiska läkemedel har visat sig kroniskt höja prolaktinnivåerna hos gnagare. Serumprolaktinnivåer mättes inte under olanzapins karcinogenicitetsstudier; Mätningar under subkroniska toxicitetsstudier visade dock att olanzapin förhöjde serumprolaktinnivåerna upp till 4 gånger hos råttor vid samma doser som användes i karcinogenicitetsstudien. En ökning av bröstkörtelneoplasmer har hittats hos gnagare efter kronisk administrering av andra antipsykotiska läkemedel och anses vara prolaktinmedierad. Relevansen för mänsklig risk för att hitta prolaktinmedierade endokrina tumörer hos gnagare är okänd [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Mutagenes
Inga bevis för genotoxisk potential för olanzapin hittades i Ames omvänd mutationstest, in vivo mikrokärntest på möss, kromosomavvikelsetest i kinesisk hamster ovarieceller, oplanerat DNA-syntestest i råtthepatocyter, induktion av framåtmutationstest i muslymfomceller , eller in vivo systerkromatidutbytestest i benmärg hos kinesiska hamstrar.
Nedsättning av fertilitet
en oral fertilitets- och reproduktionsstudie på råttor försämrades hanars parningsprestanda, men inte fertiliteten, vid en dos på 22,4 mg/kg/dag och honans fertilitet minskade vid en dos på 3 mg/kg/dag (11 och 1,5). gånger den dagliga orala MRHD baserat på mg/m² kroppsyta respektive). Avbrytande av olanzapinbehandling vände effekterna på manlig parningsprestanda. Hos honråttor ökade precoitalperioden och parningsindexet minskade med 5 mg/kg/dag (2,5 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta). Diestrous var förlängd och brunst fördröjd med 1,1 mg/kg/dag (0,6 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta); därför kan olanzapin orsaka en fördröjning av ägglossningen.
Användning i specifika populationer
När du använder ZYPREXA och fluoxetin i kombination, se även avsnittet Användning i specifika populationer i bipacksedeln för Symbyax.
Graviditet
Registret för graviditetsexponering
Det finns ett graviditetsexponeringsregister som övervakar graviditetsutfall hos kvinnor som exponerats för atypiska antipsykotika, inklusive ZYPREXA, under graviditeten. Sjukvårdsleverantörer uppmuntras att registrera patienter genom att kontakta National Pregnancy Registry for Atypical Antipsychotics på 1-866-961-2388 eller besöka http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/.
Risksammanfattning
Nyfödda som exponerats för antipsykotiska läkemedel, inklusive ZYPREXA, under tredje trimestern löper risk för extrapyramidala och/eller abstinenssymtom efter förlossningen (se Kliniska överväganden ). Övergripande tillgängliga data från publicerade epidemiologiska studier av gravida kvinnor som exponerats för olanzapin har inte fastställt en läkemedelsrelaterad risk för allvarliga fosterskador, missfall eller ogynnsamma resultat hos modern eller foster (se Data ). Det finns risker för modern i samband med obehandlad schizofreni eller bipolär störning I och med exponering för antipsykotika, inklusive ZYPREXA 7,5 mg, under graviditet (se Kliniska överväganden ).
Olanzapin var inte teratogent när det administrerades oralt till gravida råttor och kaniner i doser som är 9 och 30 gånger den dagliga orala maximala rekommenderade humana dosen (MRHD), baserat på mg/m² kroppsyta; vissa fostertoxiciteter observerades vid dessa doser (se Data ).
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för de angivna populationerna är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för mödrar och embryon/foster
Det finns en risk för modern från obehandlad schizofreni eller bipolär störning I, inklusive ökad risk för återfall, sjukhusvistelse och självmord. Schizofreni och bipolär störning I är förknippade med ökade negativa perinatala utfall, inklusive för tidig födsel. Det är inte känt om detta är ett direkt resultat av sjukdomen eller andra komorbida faktorer.
Fetala/neonatala biverkningar
Extrapyramidala och/eller abstinenssymtom, inklusive agitation, hypertoni, hypotoni, tremor, somnolens, andningsbesvär och ätstörningar har rapporterats hos nyfödda som exponerats för antipsykotiska läkemedel, inklusive ZYPREXA 2,5 mg, under graviditetens tredje trimester. Dessa symtom har varierat i svårighetsgrad. Övervaka nyfödda för extrapyramidala och/eller abstinenssymtom och hantera symtomen på lämpligt sätt. Vissa nyfödda återhämtade sig inom timmar eller dagar utan specifik behandling; andra krävde långvarig sjukhusvistelse.
Data
Mänskliga data
Placentapassage har rapporterats i publicerade studierapporter; placentapassageförhållandet var dock mycket varierande mellan 7 % och 167 % vid födseln efter exponering under graviditeten. Den kliniska relevansen av detta fynd är okänd.
Publicerade data från observationsstudier, födelseregister och fallrapporter som har utvärderat användningen av atypiska antipsykotika under graviditeten visar inte någon ökad risk för större fosterskador. En retrospektiv kohortstudie från en Medicaid-databas med 9258 kvinnor som exponerats för antipsykotika under graviditeten indikerade inte en övergripande ökad risk för allvarliga fosterskador.
Djurdata
orala reproduktionsstudier på råttor vid doser upp till 18 mg/kg/dag och på kaniner vid doser upp till 30 mg/kg/dag (9 respektive 30 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta). inga tecken på teratogenicitet observerades. I en oral teratologisk studie på råtta observerades tidiga resorptioner och ökat antal icke-viabla foster vid en dos på 18 mg/kg/dag (9 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta), och dräktigheten förlängdes vid 10. mg/kg/dag (5 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta). I en oral teratologisk studie på kanin uppträdde fostertoxicitet som ökade resorptioner och minskad fostervikt vid en maternellt toxisk dos på 30 mg/kg/dag (30 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta).
Laktation
Risksammanfattning
Olanzapin finns i modersmjölk. Det finns rapporter om överdriven sedering, irritabilitet, dålig matning och extrapyramidala symtom (skakningar och onormala muskelrörelser) hos spädbarn som exponerats för olanzapin via bröstmjölk (se Kliniska överväganden ). Det finns ingen information om effekterna av olanzapin på mjölkproduktionen.
De utvecklingsmässiga och hälsomässiga fördelarna med amning bör beaktas tillsammans med moderns kliniska behov av ZYPREXA och eventuella negativa effekter på det ammade barnet från ZYPREXA eller från moderns underliggande tillstånd.
Kliniska överväganden
Spädbarn som exponerats för ZYPREXA 7,5 mg bör övervakas för överdriven sedering, irritabilitet, dålig matning och extrapyramidala symtom (skakningar och onormala muskelrörelser).
Kvinnor Och Hanar Av Reproduktionspotential
Infertilitet
Kvinnor
Baserat på den farmakologiska effekten av olanzapin (D2-receptorantagonism) kan behandling med ZYPREXA resultera i en ökning av serumprolaktinnivåerna, vilket kan leda till en reversibel minskning av fertiliteten hos kvinnor med reproduktionspotential [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Pediatrisk användning
Säkerheten och effektiviteten av oral ZYPREXA vid behandling av schizofreni och maniska eller blandade episoder associerade med bipolär störning I har fastställts i korttidsstudier på ungdomar (åldrar 13 till 17 år). Användning av ZYPREXA hos ungdomar stöds av bevis från adekvata och välkontrollerade studier av ZYPREXA 5 mg där 268 ungdomar fick ZYPREXA 20 mg i en mängd av 2,5 till 20 mg/dag [se Kliniska studier ]. Rekommenderad startdos för ungdomar är lägre än den för vuxna [se DOSERING OCH ADMINISTRERING ]. Jämfört med patienter från kliniska prövningar för vuxna, var det sannolikt att ungdomar gick upp mer i vikt, upplevde ökad sedering och hade större ökningar av totalkolesterol, triglycerider, LDL-kolesterol, prolaktin och leveraminotransferasnivåer [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och NEGATIVA REAKTIONER ]. När de bestämmer bland de alternativa behandlingar som är tillgängliga för ungdomar bör läkare överväga den ökade potentialen (hos ungdomar jämfört med vuxna) för viktökning och dyslipidemi. Läkare bör överväga de potentiella riskerna på lång sikt när de förskriver till ungdomar, och i många fall kan detta leda till att de överväger att förskriva andra läkemedel först till ungdomar [se INDIKATIONER OCH ANVÄNDNING ].
Säkerhet och effekt av olanzapin hos barn PATIENTINFORMATION ].
Säkerhet och effekt av ZYPREXA 7,5 mg och fluoxetin i kombination hos barn och ungdomar (10 till 17 år) har fastställts för akut behandling av depressiva episoder associerade med bipolär störning I.
Säkerhet och effektivitet för ZYPREXA och fluoxetin i kombination hos barn
Geriatrisk användning
Av de 2500 patienterna i premarketing kliniska studier med oralt olanzapin var 11 % (263) 65 år eller äldre. Hos patienter med schizofreni fanns det ingen indikation på någon annan tolerabilitet för olanzapin hos äldre jämfört med yngre patienter. Studier på äldre patienter med demensrelaterad psykos har antytt att det kan finnas en annan tolerabilitetsprofil i denna population jämfört med yngre patienter med schizofreni. Äldre patienter med demensrelaterad psykos som behandlas med olanzapin löper en ökad risk att dö jämfört med placebo. I placebokontrollerade studier av olanzapin hos äldre patienter med demensrelaterad psykos, fanns en högre incidens av cerebrovaskulära biverkningar (t.ex. stroke, övergående ischemisk attack) hos patienter som behandlades med olanzapin jämfört med patienter som behandlades med placebo. Olanzapin är inte godkänt för behandling av patienter med demensrelaterad psykos. Dessutom bör förekomsten av faktorer som kan minska farmakokinetisk clearance eller öka det farmakodynamiska svaret på olanzapin leda till övervägande av en lägre startdos för alla geriatriska patienter [se LÅDA VARNING , DOSERING OCH ADMINISTRERING , och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kliniska studier av ZYPREXA och fluoxetin i kombination inkluderade inte tillräckligt antal patienter ≥65 år för att avgöra om de svarar annorlunda än yngre patienter.
ÖVERDOS
Mänsklig erfarenhet
I premarketingstudier som involverade fler än 3100 patienter och/eller normala försökspersoner, identifierades oavsiktlig eller avsiktlig akut överdosering av olanzapin hos 67 patienter. Hos patienten som tog den största identifierade mängden, 300 mg, var de enda symptomen som rapporterades dåsighet och sluddrigt tal. Hos det begränsade antalet patienter som utvärderades på sjukhus, inklusive patienten som tog 300 mg, fanns inga observationer som tydde på en negativ förändring av laboratorieanalyter eller EKG. Vitala tecken var vanligtvis inom normala gränser efter överdoser.
rapporter efter marknadsföringen av överdosering med enbart olanzapin har symtom rapporterats i de flesta fall. Hos symtomatiska patienter inkluderade symtom med ≥10 % incidens agitation/aggressivitet, dysartri, takykardi, olika extrapyramidala symtom och minskad medvetandenivå från sedering till koma. Bland mindre vanliga rapporterade symtom var följande potentiellt medicinskt allvarliga reaktioner: aspiration, hjärt- och lungstillestånd, hjärtarytmier (såsom supraventrikulär takykardi och 1 patient som upplevde sinuspaus med spontant återupptagande av normal rytm), delirium, möjlig neuroleptisk respiratorisk depression/malignt respiratoriskt syndrom. , kramper, högt blodtryck och hypotoni. Eli Lilly and Company har fått rapporter om dödsfall i samband med överdosering av enbart olanzapin. I 1 fall av dödsfall rapporterades mängden akut intaget olanzapin möjligen vara så låg som 450 mg oralt olanzapin; Men i ett annat fall rapporterades en patient överleva ett akut olanzapin intag av cirka 2 g oralt olanzapin.
Hantering av överdosering
För aktuell information om hanteringen av ZYPREXA (olanzapin) överdosering, kontakta ett certifierat giftkontrollcenter (1-800-222-1222 eller www.poison.org). Möjligheten av flera droginblandning bör övervägas. Vid akut överdosering, etablera och underhåll en luftväg och säkerställ adekvat syresättning och ventilation, vilket kan innefatta intubation. Magsköljning (efter intubation, om patienten är medvetslös) och administrering av aktivt kol tillsammans med ett laxermedel bör övervägas. Administrering av aktivt kol (1 g) minskade Cmax och AUC för oralt olanzapin med cirka 60 %. Eftersom maximala olanzapinnivåer vanligtvis inte uppnås förrän cirka 6 timmar efter dosering, kan träkol vara en användbar behandling för överdosering av olanzapin.
Möjligheten för förtrubbning, kramper eller dystoniska reaktioner i huvud och hals efter överdosering kan skapa en risk för aspiration med inducerad emes. Kardiovaskulär övervakning bör påbörjas omedelbart och bör innefatta kontinuerlig elektrokardiografisk övervakning för att upptäcka möjliga arytmier.
Det finns ingen specifik motgift mot olanzapin. Därför bör lämpliga stödåtgärder vidtas. Hypotoni och cirkulationskollaps bör behandlas med lämpliga åtgärder såsom intravenösa vätskor och/eller sympatomimetiska medel. (Använd inte epinefrin, dopamin eller andra sympatomimetika med beta-agonistaktivitet, eftersom betastimulering kan förvärra hypotoni vid olanzapin-inducerad alfablockad.) Noggrann medicinsk övervakning och övervakning bör fortsätta tills patienten återhämtar sig.
För specifik information om överdosering med litium eller valproat, se avsnittet Överdosering i bipacksedeln för dessa produkter. För specifik information om överdosering med olanzapin och fluoxetin i kombination, se avsnittet Överdosering i Symbyax bipacksedel.
KONTRAINDIKATIONER
- Inga med ZYPREXA monoterapi.
- Vid användning av ZYPREXA och fluoxetin i kombination, se även avsnittet Kontraindikationer i bipacksedeln för Symbyax.
- För specifik information om kontraindikationerna för litium eller valproat, se avsnittet Kontraindikationer i bipacksedeln för dessa andra produkter.
KLINISK FARMAKOLOGI
Handlingsmekanism
Verkningsmekanismen för olanzapin i de listade indikationerna är oklar. Emellertid kan effekten av olanzapin vid schizofreni medieras genom en kombination av dopamin och serotonin typ 2 (5HT2) antagonism.
Farmakodynamik
Olanzapin binder med hög affinitet till följande receptorer: serotonin 5HT2A/2C, 5HT6 (Ki=4, 11 respektive 5 nM), dopamin D1-4 (Ki=11-31 nM), histamin H1 (Ki=7 nM) ) och adrenerga al-receptorer (Ki=19 nM). Olanzapin är en antagonist med måttlig affinitetsbindning för serotonin 5HT3 (Ki=57 nM) och muskarin M1-5 (Ki=73, 96, 132, 32 respektive 48 nM). Olanzapin binder med låg affinitet till GABAA, BZD och β-adrenerga receptorer (Ki>10 μM).
Farmakokinetik
Oral administrering, monoterapi
Olanzapin absorberas väl och når maximala koncentrationer inom cirka 6 timmar efter en oral dos. Det elimineras i stor utsträckning genom first pass-metabolism, varvid cirka 40 % av dosen metaboliseras innan det når den systemiska cirkulationen. Mat påverkar inte hastigheten eller omfattningen av olanzapinabsorptionen. Farmakokinetiska studier visade att ZYPREXA 5 mg tabletter och ZYPREXA ZYDIS (olanzapin oralt sönderfallande tabletter) doseringsformer av olanzapin är bioekvivalenta.
Olanzapin uppvisar linjär kinetik över det kliniska doseringsintervallet. Dess halveringstid sträcker sig från 21 till 54 timmar (5:e till 95:e percentilen; medelvärde av 30 timmar), och skenbar plasmaclearance varierar från 12 till 47 l/timme (5:e till 95:e percentilen; medelvärde av 25 l/timme).
Administrering av olanzapin en gång dagligen leder till steady-state-koncentrationer inom cirka 1 vecka som är ungefär två gånger högre än koncentrationerna efter engångsdoser. Plasmakoncentrationer, halveringstid och clearance av olanzapin kan variera mellan individer beroende på rökstatus, kön och ålder.
Olanzapin distribueras i stor utsträckning i hela kroppen, med en distributionsvolym på cirka 1000 L. Det är 93 % bundet till plasmaproteiner över koncentrationsintervallet 7 till 1100 ng/ml, binder främst till albumin och α1-syraglykoprotein.
Metabolism och eliminering
Efter en oral engångsdos av 14C-märkt olanzapin, återfanns 7 % av dosen av olanzapin i urinen som oförändrat läkemedel, vilket tyder på att olanzapin metaboliseras i hög grad. Cirka 57 % och 30 % av dosen återfanns i urinen respektive avföringen. I plasma utgjorde olanzapin endast 12 % av AUC för total radioaktivitet, vilket tyder på betydande exponering för metaboliter. Efter upprepad dosering var de huvudsakliga cirkulerande metaboliterna 10-N-glukuronid, närvarande vid steady state vid 44 % av koncentrationen av olanzapin, och 4´-N-desmetylolanzapin, närvarande vid steady state vid 31 % av koncentrationen av olanzapin . Båda metaboliterna saknar farmakologisk aktivitet vid de observerade koncentrationerna.
Direkt glukuronidering och cytokrom P450 (CYP)-medierad oxidation är de primära metaboliska vägarna för olanzapin. In vitro-studier tyder på att CYP 1A2 och 2D6 och det flavininnehållande monooxygenassystemet är involverade i olanzapinoxidation. CYP2D6-medierad oxidation tycks vara en mindre metabolisk väg in vivo, eftersom clearance av olanzapin inte reduceras hos patienter som har brist på detta enzym.
Intramuskulär administrering
ZYPREXA IntraMuscular resulterar i snabb absorption med maximala plasmakoncentrationer inom 15 till 45 minuter. Baserat på en farmakokinetisk studie på friska frivilliga ger en dos på 5 mg intramuskulärt olanzapin för injektion i genomsnitt en maximal plasmakoncentration som är cirka 5 gånger högre än den maximala plasmakoncentration som produceras av en dos på 5 mg oralt olanzapin. Arean under kurvan som uppnås efter en intramuskulär dos liknar den som uppnås efter oral administrering av samma dos. Halveringstiden som observeras efter intramuskulär administrering liknar den som observeras efter oral dosering. Farmakokinetiken är linjär över det kliniska doseringsintervallet. Metaboliska profiler efter intramuskulär administrering liknar kvalitativt de metabola profilerna efter oral administrering.
Specifika populationer
Nedsatt njurfunktion
Eftersom olanzapin i hög grad metaboliseras före utsöndring och endast 7 % av läkemedlet utsöndras oförändrat, är det osannolikt att enbart renal dysfunktion har någon större inverkan på olanzapins farmakokinetik. De farmakokinetiska egenskaperna för olanzapin var likartade hos patienter med gravt nedsatt njurfunktion och normala försökspersoner, vilket indikerar att dosjustering baserat på graden av nedsatt njurfunktion inte krävs. Dessutom avlägsnas inte olanzapin genom dialys. Effekten av nedsatt njurfunktion på metabolitelimineringen har inte studerats.
Nedsatt leverfunktion
Även om förekomsten av nedsatt leverfunktion kan förväntas minska clearance av olanzapin, visade en studie av effekten av nedsatt leverfunktion hos patienter (n=6) med kliniskt signifikant (Childs Pugh klassificering A och B) cirros liten effekt på farmakokinetiken. av olanzapin.
Geriatrisk
en studie som involverade 24 friska försökspersoner var den genomsnittliga eliminationshalveringstiden för olanzapin cirka 1,5 gånger högre hos äldre (≥65 år) än hos icke äldre försökspersoner ( DOSERING OCH ADMINISTRERING ].
Kön
Clearance av olanzapin är cirka 30 % lägre hos kvinnor än hos män. Det fanns dock inga uppenbara skillnader mellan män och kvinnor i effektivitet eller biverkningar. Dosjusteringar baserade på kön bör inte behövas.
Rökning status
Olanzapinclearance är cirka 40 % högre hos rökare än hos icke-rökare, även om dosjusteringar inte rekommenderas rutinmässigt.
Lopp
In vivo-studier har visat att exponeringen är likartad bland japaner, kineser och kaukasier, särskilt efter normalisering för kroppsviktsskillnader. Dosändringar för ras rekommenderas därför inte.
Kombinerade effekter
De kombinerade effekterna av ålder, rökning och kön kan leda till betydande farmakokinetiska skillnader i populationer. Clearance hos unga rökande män, till exempel, kan vara 3 gånger högre än hos äldre icke-rökare kvinnor. Dosjustering kan vara nödvändig hos patienter som uppvisar en kombination av faktorer som kan resultera i långsammare metabolism av olanzapin [se DOSERING OCH ADMINISTRERING ].
Ungdomar (åldrar 13 till 17 år)
I kliniska studier var de flesta ungdomar icke-rökare och denna population hade en lägre genomsnittlig kroppsvikt, vilket resulterade i högre genomsnittlig exponering för olanzapin jämfört med vuxna.
Djurtoxikologi och/eller farmakologi
djurstudier med olanzapin var de huvudsakliga hematologiska fynden reversibla perifera cytopenier hos enskilda hundar doserade med 10 mg/kg (17 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta), dosrelaterade minskningar av lymfocyter och neutrofiler hos möss och lymfopeni hos råttor. Ett fåtal hundar som behandlats med 10 mg/kg utvecklade reversibel neutropeni och/eller reversibel hemolytisk anemi mellan 1 och 10 månaders behandling. Dosrelaterade minskningar av lymfocyter och neutrofiler sågs hos möss som fick doser på 10 mg/kg (lika med 2 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta) i studier av 3 månaders varaktighet. Ospecifik lymfopeni, förenlig med minskad kroppsviktsökning, inträffade hos råttor som fick 22,5 mg/kg (11 gånger den dagliga orala MRHD baserat på mg/m² kroppsyta) under 3 månader eller 16 mg/kg (8 gånger den dagliga orala MRHD-baserade på mg/m² kroppsyta) i 6 eller 12 månader. Inga tecken på benmärgscytotoxicitet hittades hos någon av de undersökta arterna. Benmärg var normocellulär eller hypercellulär, vilket tyder på att minskningen av cirkulerande blodkroppar troligen berodde på perifera (icke-märg) faktorer.
Kliniska studier
När du använder ZYPREXA 7,5 mg och fluoxetin i kombination, se även avsnittet om kliniska studier i bipacksedeln för Symbyax.
Schizofreni
Vuxna
Effekten av oralt olanzapin vid behandling av schizofreni fastställdes i 2 kontrollerade korttidsstudier (6 veckor) med vuxna slutenvårdspatienter som uppfyllde DSM III-R-kriterierna för schizofreni. En enstaka haloperidolarm inkluderades som en jämförande behandling i 1 av de 2 prövningarna, men denna prövning jämförde inte dessa 2 läkemedel på hela området av kliniskt relevanta doser för båda.
Flera instrument användes för att bedöma psykiatriska tecken och symtom i dessa studier, bland dem Brief Psychiatric Rating Scale (BPRS), en multi-item inventering av allmän psykopatologi som traditionellt används för att utvärdera effekterna av läkemedelsbehandling vid schizofreni. BPRS-psykosklustret (konceptuell desorganisering, hallucinatoriskt beteende, misstänksamhet och ovanligt tankeinnehåll) anses vara en särskilt användbar undergrupp för att bedöma aktivt psykotiska schizofrena patienter. En andra traditionell bedömning, Clinical Global Impression (CGI), återspeglar intrycket av en skicklig observatör, fullt förtrogen med manifestationerna av schizofreni, om patientens övergripande kliniska tillstånd. Dessutom användes 2 mer nyligen utvecklade vågar; dessa inkluderade 30-punkters positiva och negativa symtomskalan (PANSS), i vilken de 18 artiklarna i BPRS är inbäddade, och skalan för att bedöma negativa symtom (SANS). Försökssammanfattningarna nedan fokuserar på följande resultat: PANSS total och/eller BPRS total; BPRS psykoskluster; PANSS negativ subskala eller SANS; och CGI Severity. Resultaten av försöken följer:
(1) I en 6-veckors, placebokontrollerad studie (n=149) som involverade 2 fasta olanzapindoser på 1 och 10 mg/dag (en gång dagligen), olanzapin, vid 10 mg/dag (men inte vid 1 mg/dag) dag), var överlägsen placebo på PANSS-totalpoängen (även på det extraherade BPRS-totalt), på BPRS-psykosklustret, på PANSS Negative-subskalan och på CGI-svårhet.
(2) I en 6-veckors, placebokontrollerad studie (n=253) som involverade 3 fasta dosintervall av olanzapin (5 ± 2,5 mg/dag, 10 ± 2,5 mg/dag och 15 ± 2,5 mg/dag) på en en gång dagligen var de två högsta dosgrupperna för olanzapin (faktiska medeldoser på 12 respektive 16 mg/dag) överlägsna placebo på BPRS-totalpoäng, BPRS-psykoskluster och CGI-allvarlighetspoäng; den högsta olanzapindosgruppen var överlägsen placebo på SANS. Det fanns ingen tydlig fördel för högdosgruppen jämfört med medeldosgruppen.
(3) I en långtidsstudie randomiserades vuxna öppenvårdspatienter (n=326) som övervägande uppfyllde DSM-IV-kriterierna för schizofreni och som förblev stabila på olanzapin under öppen behandling i minst 8 veckor till fortsatt behandling med sitt nuvarande olanzapin doser (från 10 till 20 mg/dag) eller till placebo. Uppföljningsperioden för att observera patienter för återfall, definierad i termer av ökningar av BPRS-positiva symtom eller sjukhusvistelse, var planerad för 12 månader, men kriterier uppfylldes för att avbryta studien tidigt på grund av ett överskott av placebo-återfall jämfört med olanzapin-återfall. , och olanzapin var överlägset placebo i tid för återfall, det primära resultatet för denna studie. Således var olanzapin effektivare än placebo för att bibehålla effekten hos patienter stabiliserad i cirka 8 veckor och följde under en observationsperiod på upp till 8 månader.
Undersökning av populationsundergrupper (ras och kön) avslöjade inte någon differentiell lyhördhet på basis av dessa undergrupper.
Tonåringar
Effekten av oralt olanzapin vid akut behandling av schizofreni hos ungdomar (åldrar 13 till 17 år) fastställdes i en 6-veckors dubbelblind, placebokontrollerad, randomiserad studie av slutenvårdspatienter och öppenvårdspatienter med schizofreni (n=107) som träffade diagnostiska kriterier enligt DSM-IV-TR och bekräftade av Kiddie Schedule for Affective Disorders and Schizophrenia for School Aged Children-Present and Lifetime Version (K-SADS-PL).
Det primära värderingsinstrumentet som användes för att bedöma psykiatriska tecken och symtom i denna studie var den förankrade versionen av den totala poängen för den korta psykiatriska betygsskalan för barn (BPRS-C).
denna flexibla dosprövning var olanzapin 2,5 till 20 mg/dag (modal medeldos 12,5 mg/dag, medeldos på 11,1 mg/dag) effektivare än placebo vid behandling av ungdomar med diagnosen schizofreni, vilket stöds av statistiskt sett signifikant större genomsnittlig minskning av BPRS-C totalpoäng för patienter i olanzapinbehandlingsgruppen än i placebogruppen.
Även om det inte finns några bevis tillgängliga för att besvara frågan om hur länge den tonårspatient som behandlas med ZYPREXA ska bibehållas, kan underhållseffekten extrapoleras från vuxendata tillsammans med jämförelser av olanzapins farmakokinetiska parametrar hos vuxna och ungdomar. Det rekommenderas generellt att patienter som svarar fortsätter efter det akuta svaret, men med den lägsta dos som behövs för att bibehålla remission. Patienter bör regelbundet utvärderas för att fastställa behovet av underhållsbehandling.
Bipolär störning I (maniska eller blandade avsnitt)
Vuxna
Monoterapi
Effekten av oralt olanzapin vid behandling av maniska eller blandade episoder fastställdes i 2 korttidsstudier (en 3-veckors och en 4-veckors) placebokontrollerade studier på vuxna patienter som uppfyllde DSM-IV-kriterierna för bipolär störning I med maniska eller blandade episoder. Dessa prövningar inkluderade patienter med eller utan psykotiska egenskaper och med eller utan en snabb cyklingskur.
Det primära betygsinstrumentet som användes för att bedöma maniska symtom i dessa prövningar var Young Mania Rating Scale (Y-MRS), en 11-punkts klinikerklassad skala som traditionellt används för att bedöma graden av manisk symptomatologi (irritabilitet, störande/aggressivt beteende, sömn). , förhöjt humör, tal, ökad aktivitet, sexuellt intresse, språk-/tankestörning, tankeinnehåll, utseende och insikt) inom ett intervall från 0 (inga maniska egenskaper) till 60 Â (maximal poäng). Det primära resultatet i dessa försök var förändring från baslinjen i Y-MRS totalpoäng. Resultaten av försöken följer:
(1) I en 3-veckors placebokontrollerad studie (n=67) som involverade ett dosintervall av olanzapin (5-20 mg/dag, en gång dagligen, med start vid 10 mg/dag), var olanzapin överlägset placebo i minskning av Y-MRS totalpoäng. I en identiskt utformad studie som genomfördes samtidigt med den första studien visade olanzapin en liknande behandlingsskillnad, men möjligen på grund av provstorlek och platsvariabilitet visade sig inte vara överlägsen placebo på detta resultat.
(2) I en 4-veckors placebokontrollerad studie (n=115) som involverade ett dosintervall av olanzapin (5-20 mg/dag, en gång dagligen, med start vid 15 mg/dag), var olanzapin överlägset placebo i minskning av Y-MRS totalpoäng.
(3) I en annan studie, 361 patienter som uppfyllde DSM-IV-kriterierna för en manisk eller blandad episod av bipolär störning I som hade svarat under en initial öppen behandlingsfas i cirka 2 veckor i genomsnitt på olanzapin 5 till 20 mg/ dag randomiserades till antingen fortsatt behandling med olanzapin i samma dos (n=225) eller till placebo (n=136), för observation av återfall. Ungefär 50 % av patienterna hade avbrutit behandlingen från olanzapingruppen dag 59 och 50 % av placebogruppen hade avbrutit behandlingen på dag 23 av dubbelblind behandling. Respons under den öppna fasen definierades genom att ha en minskning av Y-MRS totalpoäng till ≤12 och HAM-D 21 till ≤8. Återfall under den dubbelblinda fasen definierades som en ökning av Y-MRS eller HAM-D 21 totalpoäng till ≥15, eller att vara inlagd på sjukhus för antingen mani eller depression. I den randomiserade fasen upplevde patienter som fick fortsatt olanzapin en signifikant längre tid för återfall.
Tillägg till litium eller valproat
Effekten av oralt olanzapin med samtidig litium eller valproat vid behandling av maniska eller blandade episoder fastställdes i 2 kontrollerade studier på patienter som uppfyllde DSM-IV-kriterierna för bipolär störning I med maniska eller blandade episoder. Dessa prövningar inkluderade patienter med eller utan psykotiska egenskaper och med eller utan en snabb cyklingskur. Resultaten av försöken följer:
(1) I en 6-veckors placebokontrollerad kombinationsstudie randomiserades 175 polikliniska patienter på litium- eller valproatbehandling med otillräckligt kontrollerade maniska eller blandade symtom (Y-MRS ≥16) för att få antingen olanzapin eller placebo, i kombination med sin ursprungliga behandling . Olanzapin (i ett dosintervall på 5-20 mg/dag, en gång dagligen, med start vid 10 mg/dag) kombinerat med litium eller valproat (i ett terapeutiskt område av 0,6 mEq/L till 1,2 mEq/L eller 50 μg/ml till 125 μg/mL, respektive) var överlägsen litium eller valproat enbart i minskningen av Y-MRS totalpoäng.
(2) I en andra 6-veckors placebokontrollerad kombinationsstudie randomiserades 169 polikliniska patienter på litium- eller valproatbehandling med otillräckligt kontrollerade maniska eller blandade symtom (Y-MRS ≥16) till att få antingen olanzapin eller placebo, i kombination med deras ursprungliga terapi. Olanzapin (i ett dosintervall på 5-20 mg/dag, en gång dagligen, med start vid 10 mg/dag) kombinerat med litium eller valproat (i ett terapeutiskt område av 0,6 mEq/L till 1,2 mEq/L eller 50 μg/ml till 125 μg/mL, respektive) var överlägsen litium eller valproat enbart i minskningen av Y-MRS totalpoäng.
Tonåringar
Akut monoterapi
Effekten av oralt olanzapin vid behandling av akuta maniska eller blandade episoder hos ungdomar (åldrar 13 till 17 år) fastställdes i en 3-veckors, dubbelblind, placebokontrollerad, randomiserad studie av sluten och öppenvårdspatienter för ungdomar som uppfyllde diagnosen. kriterier för maniska eller blandade episoder associerade med bipolär störning I (med eller utan psykotiska egenskaper) enligt DSM-IV-TR (n=161). Diagnosen bekräftades av K-SADS-PL.
Det primära värderingsinstrumentet som användes för att bedöma maniska symtom i denna studie var totalpoängen för ungdomsstrukturerad Young-Mania Rating Scale (Y-MRS).
denna flexibla dosstudie var olanzapin 2,5 till 20 mg/dag (modal medeldos 10,7 mg/dag, medeldos på 8,9 mg/dag) effektivare än placebo vid behandling av ungdomar med maniska eller blandade episoder associerade med bipolär I. störning, vilket stöds av den statistiskt signifikant större genomsnittliga minskningen av Y-MRS totalpoäng för patienter i olanzapinbehandlingsgruppen än i placebogruppen.
Även om det inte finns några bevis tillgängliga för att besvara frågan om hur länge den tonårspatient som behandlas med ZYPREXA ska bibehållas, kan underhållseffekten extrapoleras från vuxendata tillsammans med jämförelser av olanzapins farmakokinetiska parametrar hos vuxna och ungdomar. Det rekommenderas generellt att patienter som svarar fortsätter efter det akuta svaret, men med den lägsta dos som behövs för att bibehålla remission. Patienter bör regelbundet utvärderas för att fastställa behovet av underhållsbehandling.
Agitation associerad med schizofreni och bipolär I-mani
Effekten av intramuskulärt olanzapin för injektion för behandling av agitation fastställdes i 3 kortvariga (24 timmars IM-behandling) placebokontrollerade studier på upprörda vuxna slutenvårdspatienter från 2 diagnostiska grupper: schizofreni och bipolär störning I (maniska eller blandade episoder) . Var och en av studierna inkluderade en enda aktiv jämförelsebehandlingsarm av antingen haloperidolinjektion (schizofrenistudier) eller lorazepaminjektion (bipolär I-manistudie). Patienter som inkluderades i prövningarna behövde: (1) bedömas av de kliniska utredarna som kliniskt upprörda och kliniskt lämpliga kandidater för behandling med intramuskulär medicin, och (2) uppvisa en nivå av agitation som nådde eller översteg ett tröskelvärde på ≥14 på de 5 objekten som består av positiv och negativ syndromskala (PANSS) exciterad komponent (dvs dålig impulskontroll, spänning, fientlighet, samarbetsförmåga och spänning) med minst 1 individuell punktpoäng ≥4 med ett 1-7 poängsystem (1= frånvarande, 4=måttlig, 7=extrem). I studierna var den genomsnittliga PANSS Excited Component-poängen 18,4, med poäng från 13 till 32 (av ett maximalt betyg på 35), vilket tyder på övervägande måttliga nivåer av agitation med vissa patienter som upplever milda eller svåra nivåer av agitation. Det primära effektmått som användes för att bedöma agitationstecken och symtom i dessa studier var förändringen från baslinjen i PANSS Excited Component 2 timmar efter injektionen. Patienterna kunde få upp till 3 injektioner under 24 timmars IM-behandlingsperioder; dock kunde patienter inte få den andra injektionen förrän efter den initiala 2-timmarsperioden då det primära effektmåttet utvärderades. Resultaten av försöken följer:
(1) I en placebokontrollerad studie på upprörda slutenvårdspatienter som uppfyller DSM-IV-kriterierna för schizofreni (n=270), utvärderades 4 fasta intramuskulära olanzapin för injektionsdoser på 2,5 mg, 5 mg, 7,5 mg och 10 mg. Alla doser var statistiskt överlägsna placebo på PANSS Excited Component 2 timmar efter injektionen. Effekten var dock större och mer konsekvent för de 3 högsta doserna. Det fanns inga signifikanta parvisa skillnader för doserna på 7,5 och 10 mg jämfört med dosen på 5 mg.
(2) I en andra placebokontrollerad studie på upprörda slutenvårdspatienter som uppfyller DSM-IV-kriterierna för schizofreni (n=311), utvärderades 1 fast intramuskulär olanzapin för injektionsdos på 10 mg. Olanzapin för injektion var statistiskt överlägsen placebo på PANSS Excited Component 2 timmar efter injektionen.
(3) I en placebokontrollerad studie på upprörda slutenvårdspatienter som uppfyller DSM-IV-kriterierna för bipolär störning I (och som för närvarande uppvisar en akut manisk eller blandad episod med eller utan psykotiska egenskaper) (n=201), 1 fast intramuskulär olanzapin för injektionsdos av 10 mg utvärderades. Olanzapin för injektion var statistiskt överlägsen placebo på PANSS Excited Component 2 timmar efter injektionen.
Undersökning av populationsundergrupper (ålder, ras och kön) avslöjade inte någon differentiell lyhördhet på basis av dessa undergrupper.
PATIENTINFORMATION
ZYPREXA® (zy-PREX-a) (olanzapin) tablett
ZYPREXA® ZYDIS® (zy-PREX-a ZY-dis) (olanzapin) Tablett, Oralt sönderfallande
Läs medicinguiden som medföljer ZYPREXA innan du börjar ta den och varje gång du får påfyllning. Det kan komma ny information. Denna medicinguide ersätter inte att prata med din läkare om ditt medicinska tillstånd eller din behandling. Tala med din läkare eller apotekspersonal om det är något du inte förstår eller om du vill lära dig mer om ZYPREXA.
Vilken är den viktigaste informationen jag borde veta om ZYPREXA?
ZYPREXA 20mg kan orsaka allvarliga biverkningar, inklusive:
Dessa allvarliga biverkningar beskrivs nedan.
1. Ökad dödsrisk hos äldre personer som är förvirrade, har minnesförlust och tappat kontakten med verkligheten (demensrelaterad psykos). ZYPREXA är inte godkänt för behandling av psykos hos äldre personer med demens.
2. Högt blodsocker (hyperglykemi). Högt blodsocker kan inträffa om du redan har diabetes eller om du aldrig har haft diabetes. Högt blodsocker kan leda till:
- en ansamling av syra i blodet på grund av ketoner (ketoacidos)
- koma
- död
Din läkare bör göra tester för att kontrollera ditt blodsocker innan du börjar ta ZYPREXA 7,5 mg och under behandlingen. Hos personer som inte har diabetes försvinner ibland högt blodsocker när ZYPREXA 7,5 mg stoppas. Personer med diabetes och vissa personer som inte hade diabetes innan de tog ZYPREXA måste ta medicin mot högt blodsocker även efter att de slutat ta ZYPREXA.
Om du har diabetes, följ din läkares instruktioner om hur ofta du ska kontrollera ditt blodsocker medan du tar ZYPREXA.
Ring din läkare om du har något av dessa symtom på högt blodsocker (hyperglykemi) medan du tar ZYPREXA:
- känner mig väldigt törstig
- behöver kissa mer än vanligt
- känner mig väldigt hungrig
- känna sig svag eller trött
- får ont i magen
- känner dig förvirrad eller din andedräkt luktar fruktig
3. Höga fettnivåer i ditt blod (kolesterol och triglycerider). Höga fettnivåer kan förekomma hos personer som behandlas med ZYPREXA 10 mg, särskilt hos tonåringar (13 till 17 år gamla), eller när de används i kombination med fluoxetin till barn (10 till 17 år). Du kanske inte har några symtom, så din läkare bör ta blodprover för att kontrollera dina kolesterol- och triglyceridnivåer innan du börjar ta ZYPREXA och under behandlingen.
4. Viktökning. Viktökning är mycket vanlig hos personer som tar ZYPREXA. Tonåringar (13 till 17 år) är mer benägna att gå upp i vikt och gå upp mer i vikt än vuxna. Barn (10 till 17 år) är också mer benägna att gå upp i vikt och gå upp mer än vuxna när ZYPREXA 7,5 mg används i kombination med fluoxetin. Vissa personer kan gå upp mycket i vikt när de tar ZYPREXA, så du och din läkare bör kontrollera din vikt regelbundet. Tala med din läkare om sätt att kontrollera viktökning, som att äta en hälsosam, balanserad kost och träna.
Vad är ZYPREXA?
ZYPREXA är ett receptbelagt läkemedel som används för att behandla:
- schizofreni hos personer 13 år eller äldre.
- bipolär sjukdom, inklusive:
- maniska eller blandade episoder som inträffar med bipolär störning I hos personer 13 år eller äldre.
- maniska eller blandade episoder som inträffar med bipolär sjukdom I, när de används tillsammans med läkemedlet litium eller valproat, hos vuxna.
- långtidsbehandling av bipolär störning I hos vuxna.
- episoder av depression som inträffar med bipolär sjukdom I, när det används tillsammans med läkemedlet fluoxetin (Prozac®) hos personer som är 10 år eller äldre.
- episoder av depression som inte blir bättre efter 2 andra läkemedel, även kallad behandlingsresistent depression, när de används tillsammans med läkemedlet fluoxetin (Prozac), hos vuxna.
ZYPREXA 7,5 mg har inte godkänts för användning till barn under 13 år. ZYPREXA 10 mg i kombination med fluoxetin har inte godkänts för användning hos barn under 10 år.
Symtomen på schizofreni inkluderar att höra röster, se saker som inte finns där, ha övertygelser som inte är sanna och att vara misstänksam eller tillbakadragen.
Symtomen på bipolär störning I inkluderar omväxlande perioder av depression och högt eller irriterat humör, ökad aktivitet och rastlöshet, rasande tankar, prata snabbt, impulsivt beteende och ett minskat behov av sömn.
Symptomen på behandlingsresistent depression inkluderar minskat humör, minskat intresse, ökade skuldkänslor, minskad energi, minskad koncentration, förändringar i aptit och självmordstankar eller självmordsbeteende.
Vissa av dina symtom kan förbättras med behandling. Om du inte tror att du blir bättre, ring din läkare.
Vad ska jag berätta för min läkare innan jag tar ZYPREXA?
ZYPREXA kanske inte är rätt för dig. Innan du börjar med ZYPREXA, berätta för din läkare om du har eller haft:
- hjärtproblem
- anfall
- diabetes eller höga blodsockernivåer (hyperglykemi)
- höga kolesterol- eller triglyceridnivåer i ditt blod
- leverproblem
- lågt eller högt blodtryck
- stroke eller "mini-stroke" även kallade transienta ischemiska attacker (TIA)
- Alzheimers sjukdom
- trångvinklat glaukom
- förstorad prostata hos män
- tarmobstruktion
- fenylketonuri, eftersom ZYPREXA 5mg ZYDIS innehåller fenylalanin
- bröstcancer
- tankar på självmord eller att skada dig själv
- något annat medicinskt tillstånd
- är gravid eller planerar att bli gravid. Det är inte känt om ZYPREXA 2,5 mg kommer att skada ditt ofödda barn.
- Om du blir gravid medan du får ZYPREXA 20 mg, prata med din vårdgivare om att registrera dig hos National Pregnancy Registry for Atypical Antipsychotics. Du kan registrera dig genom att ringa 1-866-961-2388 eller gå till http://womensmentalhealth.org/clinical-andresearch-programs/pregnancyregistry/.
- ammar eller planerar att amma. ZYPREXA passerar över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar ZYPREXA.
Tala om för din läkare om du tränar mycket eller ofta är på varma platser.
Symtomen på bipolär störning I, behandlingsresistent depression eller schizofreni kan inkludera tankar på självmord eller att skada dig själv eller andra. Om du har dessa tankar vid något tillfälle, tala om för din läkare eller gå till en akutmottagning omedelbart.
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. ZYPREXA 20 mg och vissa läkemedel kan interagera med varandra och kanske inte fungerar lika bra eller orsaka allvarliga biverkningar. Din läkare kan tala om för dig om det är säkert att ta ZYPREXA tillsammans med dina andra läkemedel. Starta eller sluta inte med någon medicin medan du tar ZYPREXA utan att först tala med din läkare.
Hur ska jag ta ZYPREXA 7,5 mg?
- Ta ZYPREXA exakt som ordinerats. Din läkare kan behöva ändra (justera) dosen av ZYPREXA 15 mg tills den är rätt för dig.
- Om du missar en dos av ZYPREXA 20 mg, ta den missade dosen så snart du kommer ihåg det. Om det nästan är dags för nästa dos, hoppa över den missade dosen och ta din nästa dos vid den vanliga tiden. Ta inte två doser ZYPREXA 10 mg samtidigt.
- För att förhindra allvarliga biverkningar, sluta inte ta ZYPREXA plötsligt. Om du behöver sluta ta ZYPREXA kan din läkare berätta för dig hur du säkert kan sluta ta det.
- Om du tar för mycket ZYPREXA, ring din läkare eller giftkontrollcentral på 1-800-222-1222 omedelbart, eller få akutvård.
- ZYPREXA 10 mg kan tas med eller utan mat.
- ZYPREXA tas vanligtvis en gång varje dag.
- Ta ZYPREXA 20 mg ZYDIS enligt följande:
- Se till att dina händer är torra.
- Öppna påsen och dra av folien på blistern. Tryck inte tabletten genom folien.
- Så snart du öppnar blistern, ta bort tabletten och stoppa in den i munnen.
- Tabletten sönderdelas snabbt i din saliv så att du lätt kan svälja den med eller utan att dricka vätska.
- Ring din läkare om du inte tror att du blir bättre eller om du är orolig över ditt tillstånd när du tar ZYPREXA.
Vad ska jag undvika när jag tar ZYPREXA?
- ZYPREXA kan orsaka sömnighet och kan påverka din förmåga att fatta beslut, tänka klart eller reagera snabbt. Du ska inte köra bil, använda tunga maskiner eller göra andra farliga aktiviteter förrän du vet hur ZYPREXA 7,5 mg påverkar dig.
- Undvik att dricka alkohol när du tar ZYPREXA. Att dricka alkohol medan du tar ZYPREXA kan göra dig sömnigare än om du tar ZYPREXA 15 mg enbart.
Vilka är de möjliga biverkningarna av ZYPREXA 5mg?
Allvarliga biverkningar kan inträffa när du tar ZYPREXA 5 mg, inklusive:
- Se ”Vilken är den viktigaste informationen jag bör veta om ZYPREXA?”, som beskriver den ökade risken för dödsfall hos äldre personer med demensrelaterad psykos och riskerna för högt blodsocker, höga kolesterol- och triglyceridnivåer samt viktökning.
- Ökad förekomst av stroke eller "mini-stroke" som kallas transienta ischemiska attacker (TIA) hos äldre personer med demensrelaterad psykos (äldre personer som tappat kontakten med verkligheten på grund av förvirring och minnesförlust). ZYPREXA är inte godkänt för dessa patienter.
- Malignt neuroleptikasyndrom (NMS): NMS är ett sällsynt men mycket allvarligt tillstånd som kan inträffa hos personer som tar antipsykotiska läkemedel, inklusive ZYPREXA. NMS kan orsaka dödsfall och måste behandlas på sjukhus. Ring din läkare omedelbart om du blir allvarligt sjuk och har något av dessa symtom:
- hög feber
- överdriven svettning
- stela muskler
- förvirring
- förändringar i din andning, hjärtslag och blodtryck.
- Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS): KLÄDNING kan förekomma med ZYPREXA. Funktioner hos DRESS kan vara hudutslag, feber, svullna körtlar och andra inre organpåverkan som lever, njure, lunga och hjärta. KLÄNNING är ibland ödesdigert; Tala därför omedelbart om för din läkare om du upplever något av dessa symtom.
- Tardiv dyskinesi: Detta tillstånd orsakar kroppsrörelser som fortsätter att hända och som du inte kan kontrollera. Dessa rörelser påverkar vanligtvis ansiktet och tungan. Tardiv dyskinesi kanske inte försvinner, även om du slutar ta ZYPREXA. Det kan också börja efter att du slutat ta ZYPREXA. Tala om för din läkare om du får några kroppsrörelser som du inte kan kontrollera.
- Sänkt blodtryck när du byter position, med symtom på yrsel, snabba eller långsamma hjärtslag eller svimning.
- Svårt att svälja, som kan göra att mat eller vätska kommer ner i lungorna.
- Kramper: Tala om för din läkare om du får ett anfall under behandling med ZYPREXA.
- Problem med kontroll av kroppstemperaturen: Du kan bli väldigt varm, till exempel när du tränar mycket eller vistas i ett område som är väldigt varmt. Det är viktigt för dig att dricka vatten för att undvika uttorkning. Ring din läkare omedelbart om du blir allvarligt sjuk och har något av dessa symtom på uttorkning:
- svettas för mycket eller inte alls
- torr mun
- känner sig väldigt varm
- känner sig törstig
- inte kan producera urin.
Vanliga biverkningar av ZYPREXA inkluderar: brist på energi, muntorrhet, ökad aptit, sömnighet, darrningar (skakningar), hård eller sällsynt avföring, yrsel, beteendeförändringar eller rastlöshet.
Andra vanliga biverkningar hos tonåringar (13-17 år) inkluderar: huvudvärk, magsmärtor (buksmärtor), smärta i armar eller ben eller trötthet. Tonåringar upplevde större ökningar av prolaktin, leverenzymer och sömnighet jämfört med vuxna.
Berätta för din läkare om alla biverkningar som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar med ZYPREXA. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara ZYPREXA?
- Förvara ZYPREXA i rumstemperatur, mellan 68°F till 77°F (20°C till 25°C).
- Håll ZYPREXA borta från ljus.
- Håll ZYPREXA 15 mg torrt och borta från fukt.
Förvara ZYPREXA 5mg och alla läkemedel utom räckhåll för barn.
Allmän information om ZYPREXA
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte ZYPREXA för ett tillstånd som det inte ordinerats för. Ge inte ZYPREXA 5 mg till andra personer, även om de har samma tillstånd. Det kan skada dem.
Den här medicineringsguiden sammanfattar den viktigaste informationen om ZYPREXA. Om du vill ha mer information, prata med din läkare. Du kan fråga din läkare eller apotekspersonal om information om ZYPREXA 20mg som är skriven för vårdpersonal. För mer information om ZYPREXA ring 1-800-Lilly-Rx (1-800-545-5979).
Vilka är ingredienserna i ZYPREXA?
Aktiv beståndsdel: olanzapin
Inaktiva Ingredienser:
karnaubavax, krospovidon, hydroxipropylcellulosa, hypromellos, laktos, magnesiumstearat, mikrokristallin cellulosa och andra inaktiva ingredienser. Färgbeläggningen innehåller: Titanium Dioxide, FD&C Blue No. 2 Aluminium Lake, eller Synthetic Red Iron Oxide.
ZYDIS - gelatin, mannitol, aspartam, natriummetylparaben och natriumpropylparaben.
Denna medicineringsguide har godkänts av US Food and Drug Administration.
