Paxil 10mg, 20mg, 30mg, 40mg Paroxetine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Paxil och hur används det?
Paxil 20mg är ett receptbelagt läkemedel som används för att behandla symtom på depression, tvångssyndrom (OCD), panikångest, social fobi, generaliserat ångestsyndrom, posttraumatiskt stressyndrom (PTSD) och premenstruella dysohoriska störningar (PMDD). Paxil kan användas ensamt eller tillsammans med andra läkemedel.
- Paxil 40mg tillhör en klass av läkemedel som kallas antidepressiva, SSRI.
- Det är inte känt om Paxil är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Paxil 30mg?
Paxil 10mg kan orsaka allvarliga biverkningar inklusive:
- racing tankar,
- minskat behov av sömn,
- ovanligt risktagande beteende,
- känslor av extrem lycka eller sorg,
- vara mer pratsam än vanligt,
- suddig syn,
- tunnelseende,
- ögonsmärta eller svullnad,
- ser glorier runt ljus,
- ovanlig skelettsmärta eller ömhet, svullnad eller blåmärken,
- förändringar i vikt,
- förändringar i aptit,
- lätt att få blåmärken,
- ovanlig blödning från näsan, munnen, slidan eller ändtarmen,
- hosta blod,
- mycket stela eller stela muskler,
- hög feber,
- svettas,
- förvirring,
- snabba eller ojämna hjärtslag,
- skakningar,
- svimning,
- huvudvärk,
- förvirring,
- sluddrigt tal,
- allvarlig svaghet,
- förlust av koordination, och
- känner sig ostadig
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Paxil 30mg inkluderar:
- synförändringar,
- svaghet,
- dåsighet,
- yrsel,
- trötthet,
- svettas,
- ångest,
- skakning,
- sömnproblem (sömnlöshet),
- aptitlöshet,
- illamående,
- kräkningar,
- diarre,
- förstoppning,
- torr mun,
- infektion,
- huvudvärk,
- minskad sexlust,
- impotens,
- onormal utlösning, och
- svårt att få orgasm
Suicidalitet och antidepressiva läkemedel
Antidepressiva läkemedel ökade risken jämfört med placebo för suicidtänkande och suicidalitet (suicidalitet) hos barn, ungdomar och unga vuxna i korttidsstudier av egentlig depression (MDD) och andra psykiatriska störningar. Alla som överväger att använda PAXIL 40mg eller något annat antidepressivt medel hos ett barn, ungdom eller ung vuxen måste balansera denna risk med det kliniska behovet. Korttidsstudier visade ingen ökning av risken för suicidalitet med antidepressiva läkemedel jämfört med placebo hos vuxna efter 24 års ålder; det fanns en minskning av risken med antidepressiva läkemedel jämfört med placebo hos vuxna 65 år och äldre. Depression och vissa andra psykiatriska störningar är i sig förknippade med ökad risk för självmord. Patienter i alla åldrar som påbörjas med antidepressiv behandling bör övervakas på lämpligt sätt och observeras noggrant med avseende på klinisk försämring, suicidalitet eller ovanliga beteendeförändringar. Familjer och vårdgivare bör informeras om behovet av noggrann observation och kommunikation med förskrivaren. PAXIL 30mg är inte godkänt för användning hos pediatriska patienter. (Se VARNINGAR: Klinisk försämring och självmordsrisk, PATIENTINFORMATION och FÖRSIKTIGHETSÅTGÄRDER: Pediatrisk användning.)
BESKRIVNING
PAXIL (paroxetinhydroklorid) är ett oralt administrerat psykofarmaka. Det är hydrokloridsaltet av en fenylpiperidinförening identifierad kemiskt som (-)-trans-4R-(4'fluorfenyl)-3S-[(3',4'-metylendioxifenoxi)-metyl]piperidinhydrokloridhemihydrat och har den empiriska formeln C19H20FNO3•HCl•½H2O. Molekylvikten är 374,8 (329,4 som fri bas). Strukturformeln för paroxetinhydroklorid är:
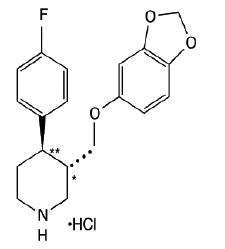
Paroxetinhydroklorid är ett luktfritt, benvitt pulver med ett smältpunktsintervall på 120° till 138°C och en löslighet på 5,4 mg/ml i vatten.
Varje filmdragerad tablett innehåller paroxetinhydroklorid ekvivalent med paroxetin enligt följande: 10 mg-gul (skårad); 20 mg-rosa (poängsatt); 30 mg-blå, 40 mg-grön. Inaktiva ingredienser består av dibasiskt kalciumfosfatdihydrat, hypromellos, magnesiumstearat, polyetylenglykoler, polysorbat 80, natriumstärkelseglykolat, titandioxid och 1 eller flera av följande: D&C Red No. 30 aluminium lake, D&C Yellow No. 10 aluminum lake , FD&C Blue No. 2 aluminiumsjö, FD&C Yellow No. 6 aluminiumsjö.
Suspension för oral administrering
Varje 5 ml apelsinfärgad vätska med apelsinsmak innehåller paroxetinhydroklorid motsvarande paroxetin, 10 mg. Inaktiva ingredienser består av polakrilinkalium, mikrokristallin cellulosa, propylenglykol, glycerin, sorbitol, metylparaben, propylparaben, natriumcitratdihydrat, vattenfri citronsyra, natriumsackarin, aromämnen, FD&C Yellow No. 6 aluminiumsjö, USP.
INDIKATIONER
PAXIL 20mg är indicerat för vuxna för behandling av:
- Major depressiv sjukdom (MDD)
- Tvångssyndrom (OCD)
- Panikångest (PD)
- Social ångestsyndrom (SAD)
- Generaliserat ångestsyndrom (GAD)
- Posttraumatiskt stressyndrom (PTSD)
DOSERING OCH ADMINISTRERING
Administrationsinformation
Administrera PAXIL som en daglig dos på morgonen, med eller utan mat.
Skaka den orala suspensionen väl före administrering.
Rekommenderad dosering för MDD, OCD, PD och PTSD
De rekommenderade startdoserna och maximala doserna av PAXIL 20 mg hos patienter med MDD, OCD, PD och PTSD presenteras i Tabell 1.
Hos patienter med otillräckligt svar, öka dosen i steg om 10 mg per dag med minst 1 veckas intervall, beroende på tolerabilitet.
Rekommenderad dosering för SAD och GAD
LEDSEN
Startdosen och den rekommenderade dosen för patienter med SAD är 20 mg dagligen. I kliniska prövningar har effekten av PAXIL 30 mg påvisats hos patienter som doserats inom ett intervall på 20 mg till 60 mg dagligen. Även om säkerheten för PAXIL har utvärderats hos patienter med SAD vid doser upp till 60 mg dagligen, tyder inte tillgänglig information på någon ytterligare fördel för doser över 20 mg dagligen [se Kliniska studier ].
GAD
Startdosen och den rekommenderade dosen för patienter med GAD är 20 mg dagligen. I kliniska prövningar har effekten av PAXIL 10 mg vid GAD påvisats hos patienter som doserats inom ett intervall av 20 mg till 50 mg dagligen. Det finns inte tillräckliga bevis för att antyda en större fördel för doser högre än 20 mg dagligen [se Kliniska studier ].
Hos patienter med otillräckligt svar, öka dosen i steg om 10 mg per dag med minst 1 veckas intervall, beroende på tolerabilitet.
Skärm för bipolär sjukdom innan PAXIL startas
Innan behandling med PAXIL 10 mg eller annat antidepressivt läkemedel påbörjas, screena patienter för personlig eller familjehistoria av bipolär sjukdom, mani eller hypomani [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Rekommenderad dosering för äldre patienter, patienter med gravt nedsatt njurfunktion och patienter med gravt nedsatt leverfunktion
Den rekommenderade initiala dosen är 10 mg per dag för äldre patienter, patienter med gravt nedsatt njurfunktion och patienter med gravt nedsatt leverfunktion. Doseringen bör inte överstiga 40 mg/dag.
Byta patienter till eller från en monoaminoxidashämmare (MAO-hämmare)
Minst 14 dagar måste förflyta mellan utsättande av en monoaminoxidashämmare (MAO-hämmare och initiering av PAXIL. Dessutom måste det gå minst 14 dagar efter avslutad PAXIL innan man påbörjar ett MAO-antidepressivt läkemedel [se KONTRAINDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Avbrytande av behandling med PAXIL
Biverkningar kan uppstå vid utsättande av PAXIL [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Minska gradvis dosen istället för att stoppa PAXIL abrupt när det är möjligt.
HUR LEVERERAS
Doseringsformer och styrkor
PAXIL tabletter finns som:
- 10 mg gul tablett med skåra graverad på framsidan med "PAXIL" och på baksidan med "10".
- 20 mg rosa tablett med skåra graverad på framsidan med "PAXIL" och på baksidan med "20".
- 30 mg blå tablett graverad på framsidan med "PAXIL" och på baksidan med "30".
- 40 mg grön tablett graverad på framsidan med "PAXIL" och på baksidan med "40".
PAXIL 20 mg oral suspension finns som:
- 10 mg/5 ml apelsinfärgad suspension med apelsinsmak i flaskor innehållande 250 ml.
Förvaring Och Hantering
PAXIL (paroxetin) tabletter är ovala tabletter som levereras som:
Förvara tabletter mellan 15° och 30°C (59° och 86°F).
PAXIL (paroxetin) oral suspension levereras som:
Förvara suspensionen vid eller under 25°C (77°F)
Tillverkad av: Apotex Inc., Toronto, Ontario, Kanada M9L 1T9. Reviderad: februari 2021
BIEFFEKTER
Följande biverkningar ingår mer i detalj i andra avsnitt av förskrivningsinformationen:
- Överkänslighetsreaktioner mot paroxetin [se KONTRAINDIKATIONER ]
- Suicidala tankar och beteenden [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Serotoninsyndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Embryofetal och neonatal toxicitet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Ökad risk för blödning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Aktivering av mani/hypomani [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Utsättningssyndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kramper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Stängningsvinkelglaukom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hyponatremi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Säkerhetsdata för PAXIL kommer från:
- 6-veckors kliniska prövningar på MDD-patienter som fick PAXIL 20 mg till 50 mg en gång dagligen
- 12-veckors kliniska prövningar på OCD-patienter som fick PAXIL 20 mg till 60 mg en gång dagligen
- 10- till 12-veckors kliniska prövningar på PD-patienter som fick PAXIL 10 mg till 60 mg en gång dagligen
- 12-veckors kliniska prövningar på SAD-patienter som fick PAXIL 20 mg till 50 mg en gång dagligen
- 8-veckors kliniska prövningar på GAD-patienter som fick PAXIL 10 mg till 50 mg en gång dagligen
- 12-veckors kliniska prövningar på PTSD-patienter som fick PAXIL 20 mg till 50 mg en gång dagligen
Biverkningar som leder till avbrytande
Tjugo procent (1 199/6 145) av patienterna som behandlades med PAXIL i kliniska prövningar vid MDD och 16,1% (84/522), 11,8% (64/542), 9,4% (44/469), 10,7% (79/735), och 11,7 % (79/676) av patienter som behandlats med PAXIL i kliniska prövningar i SAD, OCD, PD, GAD respektive PTSD, avbröt behandlingen på grund av en biverkning. De vanligaste biverkningarna (≥1 %) i samband med utsättning (dvs. de biverkningar som är förknippade med avhopp med en hastighet som är ungefär två gånger eller mer för PAXIL 10 mg jämfört med placebo) presenteras i Tabell 3:
De vanligaste biverkningarna
De vanligaste observerade biverkningarna i samband med användning av PAXIL (incidens på 5 % eller mer och minst dubbelt så hög som för placebo) var:
MDD
Asteni, svettning, illamående, minskad aptit, somnolens, yrsel, sömnlöshet, tremor, nervositet, utlösningsstörning och andra manliga könsorgan.
OCD
Illamående, muntorrhet, minskad aptit, förstoppning, yrsel, somnolens, tremor, svettning, impotens och onormal utlösning.
PD
Asteni, svettning, minskad aptit, minskad libido, tremor, onormal utlösning, kvinnliga könsorgan och impotens.
LEDSEN
Svettning, illamående, muntorrhet, förstoppning, minskad aptit, somnolens, tremor, minskad libido, gäspningar, onormal utlösning, kvinnliga könsorgan och impotens.
GAD
Asteni, infektion, förstoppning, minskad aptit, muntorrhet, illamående, minskad libido, somnolens, tremor, svettning och onormal utlösning.
PTSD
Asteni, svettning, illamående, muntorrhet, diarré, minskad aptit, somnolens, minskad libido, onormal utlösning, kvinnliga könsorgan och impotens.
Biverkningar hos patienter med MDD
Tabell 4 visar de biverkningar som inträffade med en incidens på 1 % eller mer och mer än placebo i kliniska prövningar av PAXIL-behandlade patienter med MDD.
Biverkningar hos patienter med OCD, PD och SAD
Tabell 5 visar biverkningar som inträffade med en frekvens på 2 % eller mer i kliniska prövningar på patienter med OCD, PD och SAD.
Biverkningar hos patienter med GAD och PTSD
Tabell 6 visar biverkningar som inträffade med en frekvens på 2 % eller mer i kliniska prövningar på patienter med GAD och PTSD.
Dosberoende biverkningar
MDD
En jämförelse av biverkningsfrekvensen i en studie med fast dos som jämförde PAXIL 10 mg, 20 mg, 30 mg och 40 mg en gång dagligen med placebo vid behandling av MDD avslöjade dosberoende biverkningar, som visas i Tabell 7:
OCD
I en studie med fast dos som jämförde placebo och PAXIL 20 mg, 40 mg och 60 mg vid behandling av OCD, fanns det inget tydligt samband mellan biverkningar och den dos av PAXIL 30 mg som patienterna tilldelats.
PD
en studie med fast dos som jämförde placebo och PAXIL 10 mg, 20 mg och 40 mg vid behandling av PD, visades följande biverkningar vara dosberoende: asteni, muntorrhet, ångest, minskad libido, tremor och onormal utlösning.
LEDSEN
I en studie med fast dos som jämförde placebo och PAXIL 20 mg, 40 mg och 60 mg vid behandling av SAD, för de flesta av biverkningarna, fanns det inget tydligt samband mellan biverkningar och den dos av PAXIL 10 mg som patienterna tilldelades .
GAD
I en studie med fast dos som jämförde placebo och PAXIL 20 mg och 40 mg vid behandling av GAD, visades följande biverkningar vara dosberoende: asteni, förstoppning och onormal utlösning.
PTSD
I en studie med fast dos som jämförde placebo och PAXIL 20 mg och 40 mg vid behandling av PTSD, visades följande biverkningar vara dosberoende: impotens och onormal utlösning.
Manlig och kvinnlig sexuell dysfunktion
Även om förändringar i sexuell lust, sexuell prestation och sexuell tillfredsställelse ofta förekommer som manifestationer av en psykiatrisk störning, kan de också vara en konsekvens av SSRI-behandling. Tillförlitliga uppskattningar av förekomsten och svårighetsgraden av ogynnsamma upplevelser som involverar sexuell lust, prestation och tillfredsställelse är dock svåra att få, delvis eftersom patienter och vårdgivare kan vara ovilliga att diskutera dem. Följaktligen kan uppskattningar av förekomsten av ogynnsam sexuell upplevelse och prestation som nämns i märkningen underskatta deras faktiska förekomst.
Andelen patienter som rapporterar symtom på sexuell dysfunktion hos män och kvinnor med MDD, OCD, PD, SAD, GAD och PTSD visas i Tabell 8.
Behandling med PAXIL 20 mg har associerats med flera fall av priapism. I de fall med känt utfall återhämtade sig patienterna utan följdsjukdomar.
Hallucinationer
poolade kliniska prövningar av PAXIL observerades hallucinationer hos 0,2 % av PAXIL-behandlade patienter jämfört med 0,1 % av patienterna som fick placebo.
Mindre vanliga biverkningar
Följande biverkningar inträffade under de kliniska studierna av PAXIL och är inte inkluderade någon annanstans i märkningen.
Biverkningar kategoriseras efter kroppssystem och listas i ordning efter minskande frekvens enligt följande definitioner: Frekventa biverkningar är de som inträffar vid 1 eller flera tillfällen hos minst 1/100 patienter; sällsynta biverkningar är de som inträffar hos 1/100 till 1/1 000 patienter; sällsynta biverkningar är de som inträffar hos färre än 1/1 000 patienter.
Kroppen som helhet
Sällsynt: Allergisk reaktion, frossa, ansiktsödem, sjukdomskänsla, nacksmärta; sällsynta: Adrenergt syndrom, cellulit, moniliasis, nackstelhet, bäckensmärta, peritonit, sepsis, sår.
Kardiovaskulära systemet
Vanliga: Hypertoni, takykardi; sällsynta: Bradykardi, hematom, hypotoni, migrän, postural hypotoni, synkope; sällsynta: Angina pectoris, arytmi nodal, förmaksflimmer, grenblock, cerebral ischemi, cerebrovaskulär olycka, kongestiv hjärtsvikt, hjärtblockering, lågt hjärtminutvolym, hjärtinfarkt, myokardischemi, blekhet, flebit, lungemboli, extrasyphlebitrikulär lungemboli, supra trombos, åderbråck, vaskulär huvudvärk, ventrikulära extrasystoler.
Matsmältningssystemet
Sällsynt: Bruxism, kolit, dysfagi, eruktion, gastrit, gastroenterit, gingivit, glossit, ökad salivutsöndring, onormala leverfunktionstester, rektal blödning, ulcerös stomatit; sällsynta: Aftös stomatit, blodig diarré, bulimi, kardiospasm, kolelitiasis, duodenit, enterit, esofagit, fekal inverkan, fekal inkontinens, tandköttsblödning, hematemes, hepatit, ileitis, ileus, intestinal obstruktion, gulsot, munslemhinne, melenticum, melenticum spottkörtelförstoring, sialadenit, magsår, stomatit, missfärgning av tungan, tungödem, tandkaries.
Endokrina systemet
Sällsynta: Diabetes mellitus, struma, hypertyreos, hypotyreos, tyreoidit.
Hemiska och lymfatiska system
Sällsynt: Anemi, leukopeni, lymfadenopati, purpura; sällsynta: Onormala erytrocyter, basofili, ökad blödningstid, eosinofili, hypokrom anemi, järnbristanemi, leukocytos, lymfödem, onormala lymfocyter, lymfocytos, mikrocytisk anemi, monocytos, normocytisk anemi, trombocytopeni, trombocytopeni.
Metaboliskt och näringsmässigt
Frekvent: Viktökning; sällsynt: Ödem, perifert ödem, ökad SGOT, ökad SGPT, törst, viktminskning; sällsynta: Förhöjt alkaliskt fosfatas, bilirubinemi, ökad BUN, ökad kreatininfosfokinas, uttorkning, ökad gammaglobuliner, gikt, hyperkalcemi, hyperkolesteremi, hyperglykemi, hyperkalemi, hyperfosfatemi, hypokalcemi, hypoglykemi, hyponatkalemi, hypoglykemi, hyponaositkalemi, icke-proteinkalemi, dehydroketas, kväve (NPN) ökade.
Muskuloskeletala systemet
Vanliga: Artralgi; sällsynt: Artrit, artros; sällsynta: Bursit, myosit, osteoporos, generaliserad spasm, tenosynovit, stelkramp.
Nervsystem
Frekvent: Känslomässig labilitet, svindel; sällan: Onormalt tänkande, alkoholmissbruk, ataxi, dystoni, dyskinesi, eufori, fientlighet, hypertoni, hypestesi, hypokinesi, inkoordination, brist på känslor, ökad libido, manisk reaktion, neuros, förlamning, paranoid reaktion; sällsynta: Onormal gång, akinesi, antisocial reaktion, afasi, koreoatetos, cirkumorala parestesier, konvulsioner, delirium, vanföreställningar, dubbelsidighet, drogberoende, dysartri, extrapyramidalt syndrom, fascikulationer, grand malkonvulsioner, hyperalgesi, hysteri, manic myelit, neuralgi, neuropati, nystagmus, perifer neurit, psykotisk depression, psykos, minskade reflexer, ökade reflexer, stupor, torticollis, trismus, abstinenssyndrom.
Andningssystem
Sällsynt: Astma, bronkit, dyspné, näsblod, hyperventilation, lunginflammation, andningsinfluensa; sällsynta: Emfysem, hemoptys, hicka, lungfibros, lungödem, ökat sputum, stridor, röstförändring.
Hud och bihang
Frekvent: Klåda; sällsynta: Akne, alopeci, kontaktdermatit, torr hud, ekkymos, eksem, herpes simplex, ljuskänslighet, urtikaria; sällsynta: Angioödem, erythema nodosum, erythema multiforme, exfoliativ dermatit, svampdermatit, furunkulos; herpes zoster, hirsutism, makulopapulära utslag, seborré, missfärgning av huden, hudhypertrofi, hudsår, minskad svettning, vesikulobulösa utslag.
Särskilda sinnen
Frekvent: Tinnitus; sällsynta: Avvikelser i logi, konjunktivit, öronvärk, ögonsmärta, keratokonjunktivit, mydriasis, otitis media; sällsynta: Amblyopi, anisokoria, blefarit, grå starr, konjunktivalt ödem, hornhinnesår, dövhet, exoftalmos, ögonblödning, glaukom, hyperakusis, nattblindhet, otitis externa, parosmi, fotofobi, ptos, retinal blödning, synfältsdefekt, smak.
Urogenitala systemet
Sällsynt: Amenorré, bröstsmärta, cystit, dysuri, hematuri, menorragi, natturi, polyuri, pyuri, urininkontinens, urinretention, urinträngning, vaginit; sällsynta: Abort, bröstatrofi, bröstförstoring, endometriesjukdom, epididymit, laktation hos kvinnor, fibrocystisk bröst, njursten, njursmärta, leukorré, mastit, metrorragi, nefrit, oliguri, salpingit, uretrit, urinvägssmärtor, urinvägssmärta blödning, vaginal moniliasis.
Erfarenhet efter marknadsföring
Följande reaktioner har identifierats under användning av PAXIL efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av okänd storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Akut pankreatit, förhöjda leverfunktionstester (de allvarligaste fallen var dödsfall på grund av levernekros och kraftigt förhöjda transaminaser associerade med allvarlig leverdysfunktion), Guillain-Barrés syndrom, Stevens-Johnsons syndrom, toxisk epidermal nekrolys, olämplig ADH-sekretionssyndrom, prolaktinemi och galaktorré; extrapyramidala symtom som har inkluderat akatisi, bradykinesi, kugghjulsstyvhet, okulologisk kris som har associerats med samtidig användning av pimozid; status epilepticus, akut njursvikt, pulmonell hypertoni, allergisk alveolit, anafylaxi, eklampsi, laryngis, optisk neurit, porfyri, restless legs syndrome (RLS), ventrikelflimmer, ventrikulär takykardi (inklusive torsade relaterade till anemi), hemorelaterade händelser hematopoiesis (inklusive aplastisk anemi, pancytopeni, benmärgsaplasi och agranulocytos), vaskulitiska syndrom (som Henoch-Schönlein purpura) och för tidig födsel hos gravida kvinnor. Det har förekommit en fallrapport av allvarlig hypotoni när PAXIL 20 mg lades till kronisk metoprololbehandling.
LÄKEMEDELSINTERAKTIONER
Tabell 9 visar kliniskt signifikanta läkemedelsinteraktioner med PAXIL.
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Självmordstankar och -beteenden hos ungdomar och unga vuxna
I poolade analyser av placebokontrollerade prövningar av antidepressiva läkemedel (SSRI och andra antidepressiva klasser) som inkluderade cirka 77 000 vuxna patienter och 4 500 pediatriska patienter, var förekomsten av självmordstankar och -beteenden hos patienter behandlade med antidepressiva medel i åldern 24 år och yngre högre än hos placebobehandlade patienter. Det fanns avsevärd variation i risk för självmordstankar och självmordsbeteenden bland droger, men det fanns en ökad risk hos unga patienter för de flesta studerade droger. Det fanns skillnader i absolut risk för självmordstankar och -beteenden över de olika indikationerna, med den högsta förekomsten hos patienter med MDD. Skillnaderna mellan läkemedel och placebo i antalet fall av självmordstankar och självmordsbeteenden per 1000 behandlade patienter anges i tabell 2.
PAXIL 30mg är inte godkänt för användning hos pediatriska patienter.
Det är okänt om risken för självmordstankar och självmordsbeteenden hos barn, ungdomar och unga vuxna sträcker sig till långvarig användning, dvs. längre än fyra månader. Det finns dock betydande bevis från placebokontrollerade underhållsstudier på vuxna med MDD för att antidepressiva läkemedel fördröjer återkommande depression och att depression i sig är en riskfaktor för självmordstankar och självmordsbeteenden.
Övervaka alla patienter som behandlas med antidepressivt läkemedel för indikationer på klinisk försämring och uppkomst av självmordstankar och -beteenden, särskilt under de första månaderna av läkemedelsbehandling och vid tidpunkter med dosförändringar. Rådgiv familjemedlemmar eller vårdgivare till patienter att övervaka beteendeförändringar och varna vårdgivaren. Överväg att ändra den terapeutiska regimen, inklusive eventuellt avbrytande av PAXIL, hos patienter vars depression är ihållande värre, eller som upplever framväxande självmordstankar eller -beteenden.
Serotonin syndrom
SSRI, inklusive PAXIL, kan utlösa serotonergt syndrom, ett potentiellt livshotande tillstånd. Risken ökar vid samtidig användning av andra serotonerga läkemedel (inklusive triptaner, tricykliska antidepressiva medel, fentanyl, litium, tramadol, tryptofan, buspiron, amfetamin och johannesört) och med läkemedel som försämrar metabolismen av serotonin, dvs MAO-hämmare [se MAO-hämmare [se] KONTRAINDIKATIONER , LÄKEMEDELSINTERAKTIONER ]. Serotonergt syndrom kan också uppstå när dessa läkemedel används ensamma.
Symtom på serotonergt syndrom kan inkludera förändringar i mental status (t.ex. agitation, hallucinationer, delirium och koma), autonom instabilitet (t.ex. takykardi, labilt blodtryck, yrsel, diafores, rodnad, hypertermi), neuromuskulära symtom (t.ex. tremor, stelhet, myoklonus, hyperreflexi, inkoordination), kramper och/eller gastrointestinala symtom (t.ex. illamående, kräkningar, diarré).
Samtidig användning av PAXIL och MAO-hämmare är kontraindicerad. Dessutom ska PAXIL 30 mg inte påbörjas hos en patient som behandlas med MAO-hämmare såsom linezolid eller intravenös metylenblått. Inga rapporter involverade administrering av metylenblått på andra sätt (såsom orala tabletter eller lokal vävnadsinjektion) eller vid lägre doser. Om det är nödvändigt att påbörja behandling med en MAO-hämmare såsom linezolid eller intravenös metylenblått hos en patient som tar PAXIL 10 mg, avbryt PAXIL 40 mg innan behandling med MAO-hämmaren påbörjas [se KONTRAINDIKATIONER , LÄKEMEDELSINTERAKTIONER ].
Övervaka alla patienter som tar PAXIL 20mg för uppkomsten av serotonergt syndrom. Avbryt behandlingen med PAXIL 20 mg och eventuella samtidiga serotonerga medel omedelbart om ovanstående symtom uppträder och påbörja stödjande symtomatisk behandling. Om samtidig användning av PAXIL med andra serotonerga läkemedel är kliniskt motiverad, informera patienterna om den ökade risken för serotonergt syndrom och övervaka symtomen.
Läkemedelsinteraktioner som leder till QT-förlängning
De CYP2D6-hämmande egenskaperna hos paroxetin kan höja plasmanivåerna av tioridazin och pimozid. Eftersom tioridazin och pimozid enbart ger förlängning av QTc-intervallet och ökar risken för allvarliga ventrikulära arytmier, är användning av PAXIL 40 mg kontraindicerat i kombination med tioridazin och pimozid [se KONTRAINDIKATIONER , LÄKEMEDELSINTERAKTIONER , KLINISK FARMAKOLOGI ].
Embryofetal Och Neonatal Toxicitet
PAXIL kan orsaka fosterskador när det ges till en gravid kvinna. Epidemiologiska studier har visat att spädbarn som exponerats för paroxetin under graviditetens första trimester har en ökad risk för kardiovaskulära missbildningar. Exponering för paroxetin i slutet av graviditeten kan leda till en ökad risk för ihållande pulmonell hypertoni hos nyfödda (PPNH) och/eller neonatala komplikationer som kräver långvarig sjukhusvistelse, andningsstöd och sondmatning.
Om PAXIL 20 mg används under graviditet, eller om patienten blir gravid medan du tar PAXIL 30 mg, ska patienten informeras om den potentiella faran för fostret [se Användning i specifika populationer ].
Ökad risk för blödning
Läkemedel som interfererar med hämning av serotoninåterupptag, inklusive PAXIL 40mg, ökar risken för blödningshändelser. Samtidig användning av acetylsalicylsyra, icke-steroida antiinflammatoriska läkemedel (NSAIDS), andra trombocythämmande läkemedel, warfarin och andra antikoagulantia kan öka denna risk. Fallrapporter och epidemiologiska studier (fallkontroll och kohortdesign) har visat ett samband mellan användning av läkemedel som stör serotoninåterupptaget och förekomsten av gastrointestinala blödningar. Blödningshändelser relaterade till läkemedel som stör serotoninåterupptaget har varierat från ekkymoser, hematom, näsblod och petekier till livshotande blödningar.
Informera patienter om den ökade risken för blödning i samband med samtidig användning av PAXIL 20 mg och trombocythämmande medel eller antikoagulantia. För patienter som tar warfarin, övervaka noggrant det internationella normaliserade förhållandet.
Aktivering av mani eller hypomani
Hos patienter med bipolär sjukdom kan behandling av en depressiv episod med PAXIL 30 mg eller annat antidepressivt medel utlösa en blandad/manisk episod. Under kontrollerade kliniska prövningar av PAXIL inträffade hypomani eller mani hos cirka 1 % av PAXIL-behandlade unipolära patienter jämfört med 1,1 % av aktiv kontroll och 0,3 % av placebobehandlade unipolära patienter. Innan behandling med PAXIL 20 mg påbörjas, screena patienterna för eventuell personlig eller familjehistoria av bipolär sjukdom, mani eller hypomani.
Utsättningssyndrom
Biverkningar efter utsättning av serotonerga antidepressiva läkemedel, särskilt efter abrupt utsättning, inkluderar: illamående, svettning, dysforiskt humör, irritabilitet, agitation, yrsel, känselrubbningar (t.ex. parestesi, såsom elektriska stötar), tremor, ångest, förvirring, huvudvärk, slöhet, emotionell labilitet, sömnlöshet, hypomani, tinnitus och anfall. En gradvis minskning av dosen snarare än abrupt utsättning rekommenderas när så är möjligt [se DOSERING OCH ADMINISTRERING ].
Under kliniska prövningar av GAD och PTSD användes gradvisa minskningar av den dagliga dosen med 10 mg/dag med veckointervall följt av 1 vecka med 20 mg/dag innan behandlingen avbröts. Följande biverkningar rapporterades med en incidens på 2 % eller mer för PAXIL 20 mg och var minst dubbelt så hög som rapporterad för placebo: Onormala drömmar, parestesi och yrsel Biverkningar har rapporterats vid utsättning av behandling med PAXIL hos pediatriska patienter. Säkerheten och effekten av PAXIL hos pediatriska patienter har inte fastställts [se LÅDA VARNING , Självmordstankar och -beteenden hos ungdomar och unga vuxna , Användning i specifika populationer ].
Anfall
PAXIL 10 mg tabletter och oral suspension har inte utvärderats systematiskt hos patienter med krampanfall. Patienter med anfallshistoria exkluderades från kliniska studier. Under kliniska studier inträffade anfall hos 0,1 % av patienterna som behandlades med PAXIL. PAXIL ska förskrivas med försiktighet till patienter med krampanfall. Avbryt PAXIL 30mg hos alla patienter som utvecklar anfall.
Stängningsvinkelglaukom
Pupillutvidgningen som uppstår efter användning av många antidepressiva läkemedel inklusive PAXIL kan utlösa en vinkelattack hos en patient med anatomiskt smala vinklar som inte har en patenterad iridektomi. Fall av stängningsvinkelglaukom i samband med användning av PAXIL 40 mg har rapporterats. Undvik användning av antidepressiva medel, inklusive PAXIL hos patienter med obehandlade anatomiskt smala vinklar.
Hyponatremi
Hyponatremi kan uppstå som ett resultat av behandling med SSRI, inklusive PAXIL. Fall med serumnatrium lägre än 110 mmol/L har rapporterats. Tecken och symtom på hyponatremi inkluderar huvudvärk, koncentrationssvårigheter, minnesstörning, förvirring, svaghet och ostadighet, vilket kan leda till fall. Tecken och symtom förknippade med mer allvarliga och/eller akuta fall har inkluderat hallucinationer, synkope, anfall, koma, andningsstopp och dödsfall. I många fall verkar denna hyponatremi vara resultatet av syndromet med olämplig antidiuretisk hormonsekretion (SIADH).
Hos patienter med symtomatisk hyponatremi, avbryt PAXIL och sätt in lämplig medicinsk intervention. Äldre patienter, patienter som tar diuretika och de som är utarmade kan löpa större risk att utveckla hyponatremi med SSRI [se Användning i specifika populationer ].
Minskning av effekten av Tamoxifen
Vissa studier har visat att effekten av tamoxifen, mätt som risken för återfall/dödlighet i bröstcancer, kan minska vid samtidig användning av PAXIL som ett resultat av paroxetins irreversibla hämning av CYP2D6 och lägre blodnivåer av tamoxifen [se LÄKEMEDELSINTERAKTIONER ]. En studie tyder på att risken kan öka med längre varaktighet av samtidig administrering. Men andra studier har misslyckats med att visa en sådan risk. När tamoxifen används för behandling eller förebyggande av bröstcancer bör förskrivare överväga att använda ett alternativt antidepressivt medel med liten eller ingen CYP2D6-hämning.
Benfraktur
Epidemiologiska studier om benfrakturrisk vid exponering för vissa antidepressiva läkemedel, inklusive SSRI, har rapporterat ett samband mellan antidepressiv behandling och frakturer. Det finns flera möjliga orsaker till denna observation och det är okänt i vilken utsträckning frakturrisken är direkt hänförlig till SSRI-behandling.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide ).
Självmordstankar och -beteenden
Råda patienter och vårdgivare att leta efter uppkomsten av suicidalitet, särskilt tidigt under behandlingen och när dosen justeras upp eller ner, och instruera dem att rapportera sådana symtom till vårdgivaren [se LÅDA VARNING och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Serotonin syndrom
Varna patienter för risken för serotonergt syndrom, särskilt vid samtidig användning av PAXIL med andra serotonerga läkemedel inklusive triptaner, tricykliska antidepressiva medel, fentanyl, litium, tramadol, tryptofan, buspiron, amfetamin, johannesört och med läkemedel som försämrar metabolismen av serotonin (särskilt MAO-hämmare, både de som är avsedda att behandla psykiatriska störningar och även andra, såsom linezolid). Instruera patienter att kontakta sin vårdgivare eller rapportera till akuten om de upplever tecken eller symtom på serotonergt syndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ].
Samtidig medicinering
Rekommendera patienter att informera sin läkare om de tar eller planerar att ta några receptbelagda eller receptfria läkemedel, eftersom det finns risk för läkemedelsinteraktioner [se VARNING OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ].
Ökad risk för blödning
Informera patienterna om samtidig användning av PAXIL och acetylsalicylsyra, NSAID, andra trombocythämmande läkemedel, warfarin eller andra antikoagulantia eftersom den kombinerade användningen har associerats med en ökad risk för blödning. Råda patienter att informera sin vårdgivare om de tar eller planerar att ta några receptbelagda eller receptfria läkemedel som ökar risken för blödning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Aktivering av mani/hypomani
Råda patienter och deras vårdgivare att observera efter tecken på aktivering av mani/hypomani och instruera dem att rapportera sådana symtom till vårdgivaren [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Utsättningssyndrom
Rekommendera patienter att inte abrupt avbryta behandlingen med PAXIL 40mg och att diskutera eventuell nedtrappning med sin vårdgivare. Informera patienter om att biverkningar kan uppstå när PAXIL sätts ut [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Administrationsinformation för oral suspension
Instruera patienterna att skaka den orala suspensionen väl före administrering [se DOSERING OCH ADMINISTRERING ].
Allergiska reaktioner
Rekommendera patienter att meddela sin vårdgivare om de utvecklar en allergisk reaktion som hudutslag, nässelfeber, svullnad eller andningssvårigheter [se NEGATIVA REAKTIONER ].
Embryo-fetal toxicitet
Informera kvinnor om den potentiella risken för fostret [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer ]. Rekommendera patienter att meddela sin vårdgivare om de blir gravida eller avser att bli gravida under behandlingen på grund av risken för fostret.
Amning
Råda kvinnor att meddela sin vårdgivare om de ammar ett spädbarn [se Användning i specifika populationer ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
Tvååriga karcinogenicitetsstudier utfördes på gnagare som fick paroxetin i kosten med 1, 5 och 25 mg/kg/dag (möss) och 1, 5 och 20 mg/kg/dag (råttor). Dessa doser är upp till 2,0 (mus) och 3,2 (råtta) gånger MRHD på 75 mg på mg/m2-basis. Det fanns ett signifikant större antal hanråttor i högdosgruppen med retikulumcellsarkom (1/100, 0/50, 0/50 och 4/50 för kontroll-, låg-, medel- och högdosgrupperna ) och en signifikant ökad linjär trend över dosgrupper för förekomsten av lymforetikulära tumörer hos hanråttor. Honråttor påverkades inte. Även om det fanns en dosrelaterad ökning av antalet tumörer hos möss, fanns det ingen läkemedelsrelaterad ökning av antalet möss med tumörer. Relevansen av dessa fynd för människor är okänd.

Mutagenes
Paroxetin gav inga genotoxiska effekter i ett batteri av 5 in vitro och 2 in vivo-analyser som inkluderade följande: bakteriell mutationsanalys, muslymfommutationsanalys, oplanerad DNA-syntesanalys och tester för cytogenetiska aberrationer in vivo i benmärg hos mus och in vitro i humana lymfocyter och i ett dominant dödligt test på råttor.
Nedsättning av fertilitet
Vissa kliniska studier har visat att SSRI (inklusive paroxetin) kan påverka spermiekvaliteten under SSRI-behandling, vilket kan påverka fertiliteten hos vissa män.
En minskad graviditetsfrekvens hittades i reproduktionsstudier på råttor vid en dos av paroxetin på 15 mg/kg/dag, vilket är 2,4 gånger MRHD på 75 mg på mg/m2-basis. Irreversibla lesioner inträffade i fortplantningsorganen hos råttor av hankön efter dosering i toxicitetsstudier under 2 till 52 veckor. Dessa lesioner bestod av vakuolering av epididymalt tubulärt epitel vid 50 mg/kg/dag och atrofiska förändringar i seminiferösa tubuli i testiklarna med stoppad spermatogenes vid 25 mg/kg/dag (8,2 och 4,1 gånger MRHD på 75 mg på en mg/dag). m2 bas).
Användning i specifika populationer
Graviditet
Graviditetskategori D [Se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Epidemiologiska studier har visat att spädbarn som exponerats för paroxetin under graviditetens första trimester har en ökad risk för medfödda missbildningar, särskilt kardiovaskulära missbildningar. Om paroxetin används under graviditet, eller om patienten blir gravid medan du tar paroxetin, informera patienten om den potentiella faran för fostret.
Kliniska överväganden
Om inte fördelarna med paroxetin för modern motiverar fortsatt behandling, bör man överväga att antingen avbryta paroxetinbehandlingen eller byta till ett annat antidepressivt läkemedel [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. För
- En studie baserad på svenska nationella registerdata visade att spädbarn som exponerats för paroxetin under graviditeten (n = 815) hade en ökad risk för kardiovaskulära missbildningar (risk på 2 % hos paroxetinexponerade spädbarn) jämfört med hela registerpopulationen (1 % risk), för en oddskvot (OR) på 1,8 (95 % konfidensintervall 1,1 till 2,8). Ingen ökning av risken för övergripande medfödda missbildningar sågs hos de paroxetinexponerade spädbarnen. Hjärtmissbildningarna hos de paroxetinexponerade spädbarnen var främst ventrikulära septumdefekter (VSD) och förmaksseptumdefekter (ASD). Septumdefekter varierar i svårighetsgrad från de som försvinner spontant till de som kräver operation.
- En separat retrospektiv kohortstudie från USA (United Healthcare-data) utvärderade 5 956 spädbarn till mödrar som gav antidepressiva läkemedel under den första trimestern (n = 815 för paroxetin). Denna studie visade en trend mot en ökad risk för kardiovaskulära missbildningar för paroxetin (risk på 1,5 %) jämfört med andra antidepressiva läkemedel (risk 1 %), för en OR på 1,5 (95 % konfidensintervall 0,8 till 2,9). Av de 12 paroxetinexponerade spädbarnen med kardiovaskulära missbildningar hade 9 VSD. Denna studie antydde också en ökad risk för övergripande allvarliga medfödda missbildningar inklusive kardiovaskulära defekter för paroxetin (4 % risk) jämfört med andra (2 % risk) antidepressiva läkemedel (OR 1,8; 95 % konfidensintervall 1,2 till 2,8).
- Två stora fall-kontrollstudier med separata databaser, var och en med >9 000 fall med fosterskador och >4 000 kontroller, fann att moderns användning av paroxetin under graviditetens första trimester var associerad med en 2- till 3-faldigt ökad risk för högerkammarutflöde obstruktioner i luftvägarna. I en studie var OR 2,5 (95 % konfidensintervall, 1,0 till 6,0, 7 exponerade spädbarn) och i den andra studien var OR 3,3 (95 % konfidensintervall, 1,3 till 8,8, 6 exponerade spädbarn).
Andra studier har funnit varierande resultat om det fanns en ökad risk för övergripande, kardiovaskulära eller specifika medfödda missbildningar. En metaanalys av epidemiologiska data under en 16-årsperiod (1992 till 2008) om användning av paroxetin i första trimestern under graviditet och medfödda missbildningar inkluderade de ovannämnda studierna förutom andra (n = 17 studier som inkluderade övergripande missbildningar och n = 14 studier som inkluderade kardiovaskulära missbildningar; n = 20 distinkta studier). Även om den var föremål för begränsningar antydde denna metaanalys en ökad förekomst av kardiovaskulära missbildningar (prevalensoddskvot [POR] 1,5; 95 % konfidensintervall 1,2 till 1,9) och övergripande missbildningar (POR 1,2; 95 % konfidensintervall 1,1 till 1,4) med paroxetin användning under första trimestern. Det var inte möjligt i denna metaanalys att fastställa i vilken utsträckning den observerade prevalensen av kardiovaskulära missbildningar kan ha bidragit till den för totala missbildningar, och det var inte heller möjligt att fastställa om några specifika typer av kardiovaskulära missbildningar kan ha bidragit till den observerade prevalensen av alla kardiovaskulära missbildningar.
Om inte fördelarna med paroxetin för modern motiverar fortsatt behandling, bör man överväga att antingen avbryta paroxetinbehandlingen eller byta till ett annat antidepressivt läkemedel [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. För kvinnor som planerar att bli gravida eller är i sin första trimester av graviditeten ska paroxetin endast påbörjas efter övervägande av andra tillgängliga behandlingsalternativ [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Behandling av gravida kvinnor under deras tredje trimester
Nyfödda som exponerats för SSRI eller serotonin- och noradrenalinåterupptagshämmare (SNRI), inklusive PAXIL 40mg, sent i tredje trimestern har utvecklat komplikationer som kräver långvarig sjukhusvistelse, andningsstöd och sondmatning. Sådana komplikationer kan uppstå omedelbart efter leverans. Rapporterade kliniska fynd har inkluderat andnöd, cyanos, apné, kramper, temperaturinstabilitet, ätsvårigheter, kräkningar, hypoglykemi, hypotoni, hypertoni, hyperreflexi, tremor, skakningar, irritabilitet och konstant gråt. Dessa egenskaper överensstämmer med antingen en direkt toxisk effekt av SSRI och SNRI eller, möjligen, ett läkemedelsavbrottssyndrom. Det bör noteras att den kliniska bilden i vissa fall överensstämmer med serotonergt syndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Exponering för SSRI i slutet av graviditeten kan ha en ökad risk för ihållande pulmonell hypertoni hos nyfödda (PPHN). PPHN förekommer hos 1 – 2 av 1 000 levande födda i den allmänna befolkningen och är associerat med betydande neonatal sjuklighet och mortalitet. I en retrospektiv fallkontrollstudie av 377 kvinnor vars spädbarn föddes med PPHN och 836 kvinnor vars spädbarn föddes friska, var risken för att utveckla PPHN ungefär sex gånger högre för spädbarn som exponerades för SSRI efter den 20:e graviditetsveckan jämfört med spädbarn som inte hade exponerats för antidepressiva medel under graviditeten.
Det har också förekommit rapporter efter marknadsföring om för tidigt födda barn hos gravida kvinnor som exponerats för paroxetin eller andra SSRI-preparat.
Vid behandling av en gravid kvinna med paroxetin under tredje trimestern bör läkaren noggrant överväga både de potentiella riskerna och fördelarna med behandlingen. En prospektiv longitudinell studie av 201 kvinnor med en historia av allvarlig depression som var euthymic i början av graviditeten. De kvinnor som avbröt antidepressiv medicinering under graviditeten var mer benägna att uppleva ett återfall av allvarlig depression än kvinnor som fortsatte med antidepressiv medicinering.
Djurfynd
Reproduktionsstudier utfördes vid doser upp till 50 mg/kg/dag på råttor och 6 mg/kg/dag på kaniner som administrerades under organogenesen. Dessa doser är cirka 6 (råtta) och mindre än 2 (kanin) gånger den maximala rekommenderade humandosen (MRHD – 75 mg) på mg/m2-basis. Dessa studier har inte visat några tecken på utvecklingseffekter. Hos råttor var det dock en ökning av valpdöden under de första 4 dagarna av laktationen när doseringen skedde under den sista trimestern av dräktigheten och fortsatte under hela laktationen. Denna effekt inträffade vid en dos på 1 mg/kg/dag, vilket är än MRHD på mg/m2-basis. Ingen effektdos för dödlighet av råttungar bestämdes inte. Orsaken till dessa dödsfall är inte känd.
Ammande mödrar
Liksom många andra läkemedel utsöndras paroxetin i bröstmjölk. På grund av risken för allvarliga biverkningar hos ammande spädbarn från PAXIL 20 mg, bör ett beslut fattas om att avbryta ammande spädbarn eller att avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Säkerheten och effekten av PAXIL hos pediatriska patienter har inte fastställts [se LÅDA VARNING ]. Effektivitet visades inte i tre placebokontrollerade studier på 752 PAXIL-behandlade pediatriska patienter med MDD.
Antidepressiva medel ökar risken för suicidtankar och självmordsbeteenden hos pediatriska patienter [se LÅDA VARNING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Minskad aptit och viktminskning har observerats i samband med användning av SSRI.
placebokontrollerade kliniska prövningar utförda med pediatriska patienter rapporterades följande biverkningar hos minst 2 % av de pediatriska patienterna som behandlades med PAXIL och inträffade i en frekvens som var minst dubbelt så hög som för pediatriska patienter som fick placebo: känslomässig labilitet (inklusive självskada) , självmordstankar, självmordsförsök, gråt och humörsvängningar), fientlighet, minskad aptit, tremor, svettning, hyperkinesi och agitation.
Biverkningar efter utsättning av behandling med PAXIL i de pediatriska kliniska prövningarna som inkluderade en nedskärningsfasregim, som inträffade hos minst 2 % av patienterna och i en frekvens som var minst dubbelt så stor som för placebo, var: emotionell labilitet (inklusive självmordstankar, självmord försök, humörsvängningar och tårkänsla), nervositet, yrsel, illamående och buksmärtor.
Geriatrisk användning
kliniska prövningar före marknadsföring med PAXIL 10 mg var 17 % av patienterna som behandlades med PAXIL (cirka 700) 65 år eller äldre. Farmakokinetiska studier visade ett minskat clearance hos äldre och en lägre startdos rekommenderas; dock observerades inga övergripande skillnader i säkerhet eller effektivitet mellan äldre och yngre patienter [se DOSERING OCH ADMINISTRERING , KLINISK FARMAKOLOGI ].
SSRI, inklusive PAXIL, har associerats med fall av kliniskt signifikant hyponatremi hos äldre patienter, som kan löpa större risk för denna biverkning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Nedsatt njur- och leverfunktion
Ökade plasmakoncentrationer av paroxetin förekommer hos patienter med nedsatt njur- och leverfunktion. Den initiala dosen av PAXIL bör reduceras hos patienter med gravt nedsatt njurfunktion och hos patienter med gravt nedsatt leverfunktion [se DOSERING OCH ADMINISTRERING , KLINISK FARMAKOLOGI ].
ÖVERDOS
Mänsklig erfarenhet
Sedan introduktionen av PAXIL 30 mg i USA har spontana fall av avsiktlig eller oavsiktlig överdosering under paroxetinbehandling rapporterats över hela världen. Dessa inkluderar överdoser med enbart paroxetin och i kombination med andra substanser. Det finns rapporter om dödsfall som verkar involvera enbart paroxetin.
Vanliga rapporterade biverkningar i samband med överdosering av paroxetin inkluderar somnolens, koma, illamående, tremor, takykardi, förvirring, kräkningar och yrsel. Andra anmärkningsvärda tecken och symtom som observerats vid överdoser som involverar paroxetin (enbart eller tillsammans med andra substanser) inkluderar mydriasis, kramper (inklusive status epilepticus), ventrikulära dysrytmier (inklusive torsade de pointes), hypertoni, aggressiva reaktioner, synkope, hypotoni, stupor, bradykard. rabdomyolys, symtom på leverdysfunktion (inklusive leversvikt, levernekros, gulsot, hepatit och leversteatos), serotonergt syndrom, maniska reaktioner, myoklonus, akut njursvikt och urinretention.
Överdosering
Inga specifika antidoter för PAXIL är kända. Om överdosering inträffar, ring ditt giftkontrollcenter på 1-800-222-1222 för de senaste rekommendationerna.
KONTRAINDIKATIONER
PAXIL är kontraindicerat hos patienter:
- Att ta, eller inom 14 dagar efter att man avslutat, MAO-hämmare (inklusive MAO-hämmare linezolid och intravenös metylenblått) på grund av en ökad risk för serotonergt syndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ].
- Tar tioridazin på grund av risken för QT-förlängning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och LÄKEMEDELSINTERAKTIONER ]
- Tar pimozid på grund av risken för QT-förlängning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ].
- Med känd överkänslighet (t.ex. anafylaxi, angioödem, Stevens-Johnsons syndrom) mot paroxetin eller någon av de inaktiva ingredienserna i PAXIL [se NEGATIVA REAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Verkningsmekanismen för PAXIL vid behandling av MDD, SAD, OCD\, PD, GAD och PTSD är okänd, men antas vara kopplad till förstärkning av serotonerg aktivitet i det centrala nervsystemet till följd av hämning av neuronalt återupptag av serotonin (5-hydroxi-tryptamin, 5-HT).
Farmakodynamik
Studier med kliniskt relevanta doser på människor har visat att paroxetin blockerar upptaget av serotonin i humana blodplättar. In vitro-studier på djur tyder också på att paroxetin är en potent och mycket selektiv hämmare av neuronalt serotoninåterupptag (SSRI) och har endast mycket svaga effekter på noradrenalin och dopamin neuronalt återupptag.
Farmakokinetik
Icke-linjäritet i farmakokinetiken observeras med ökande doser av PAXIL.
I en metaanalys av paroxetin från 4 studier gjorda på friska frivilliga efter upprepad dosering på 20 mg/dag till 40 mg/dag, uppvisade män inte en signifikant lägre Cmax eller AUC än kvinnor.
Absorption
Paroxetinhydroklorid absorberas fullständigt efter oral dosering av en lösning av hydrokloridsaltet. I en studie där normala manliga försökspersoner (n = 15) fick 30 mg tabletter dagligen i 30 dagar, uppnåddes steady-state paroxetinkoncentrationer med cirka 10 dagar för de flesta försökspersoner, även om det kan ta betydligt längre tid hos en enstaka patient. Vid steady state var medelvärdena för Cmax, Tmax, Cmin och T½ 61,7 ng/ml (CV 45%), 5,2 timmar. (CV 10%), 30,7 ng/ml (CV 67%), respektive 21,0 timmar (CV 32%). Cmax- och Cmin-värdena vid steady-state var cirka 6 och 14 gånger vad som skulle förutsägas från endosstudier. Läkemedelsexponering vid steady-state baserat på AUC0-24 var cirka 8 gånger större än vad som skulle ha förutsetts från singeldosdata hos dessa försökspersoner. Överskottsackumuleringen är en konsekvens av att ett av enzymerna som metaboliserar paroxetin är lätt mättbart.
Paroxetin är lika biotillgängligt från oral suspension och tablett.
Effekten av mat
Effekterna av föda på biotillgängligheten av paroxetin studerades hos försökspersoner som fick en engångsdos med och utan föda. AUC ökade endast något (6%) när läkemedlet administrerades med mat, men Cmax var 29% högre, medan tiden för att nå maximal plasmakoncentration minskade från 6,4 timmar efter dosering till 4,9 timmar.
Distribution
Paroxetin distribueras i hela kroppen, inklusive CNS, med endast 1 % kvar i plasman.
Cirka 95 % och 93 % av paroxetin är bundet till plasmaprotein vid 100 ng/ml respektive 400 ng/ml. Under kliniska förhållanden skulle paroxetinkoncentrationerna normalt vara mindre än 400 ng/ml. Paroxetin förändrar inte in vitro proteinbindningen av fenytoin eller warfarin.
Eliminering
Ämnesomsättning
Den genomsnittliga eliminationshalveringstiden är cirka 21 timmar (CV 32%) efter oral dosering av 30 mg tabletter dagligen under 30 dagar av PAXIL.
steady-state dosproportionalitetsstudier som involverade äldre och icke äldre patienter, vid doser på 20 mg till 40 mg dagligen för äldre och 20 mg till 50 mg dagligen för icke äldre, observerades viss olinjäritet i båda populationerna, vilket återigen speglar en mättbar metabolisk väg . Jämfört med Cmin-värden efter 20 mg dagligen var värdena efter 40 mg dagligen endast cirka 2 till 3 gånger större än fördubblats.
Paroxetin metaboliseras i stor utsträckning efter oral administrering. De huvudsakliga metaboliterna är polära och konjugerade produkter av oxidation och metylering, som lätt elimineras. Konjugat med glukuronsyra och sulfat dominerar, och huvudmetaboliter har isolerats och identifierats. Data indikerar att metaboliterna inte har mer än 1/50 av modersubstansens styrka att hämma serotoninupptaget. Metabolismen av paroxetin åstadkoms delvis av CYP2D6. Mättnad av detta enzym vid kliniska doser tycks förklara paroxetinkinetikens olinjäritet med ökande dos och ökande behandlingslängd. Rollen av detta enzym i paroxetinmetabolism antyder också potentiella läkemedelsinteraktioner [se LÄKEMEDELSINTERAKTIONER ]. Paroxetins farmakokinetiska beteende har inte utvärderats hos försökspersoner som har brist på CYP2D6 (dåliga metaboliserare).
Exkretion
Ungefär 64 % av en 30 mg oral lösningsdos av paroxetin utsöndrades i urinen med 2 % som modersubstans och 62 % som metaboliter under en 10-dagarsperiod efter dosering. Cirka 36 % utsöndrades i avföringen (troligen via gallan), mestadels som metaboliter och mindre än 1 % som modersubstans under 10-dagarsperioden efter dosering.
Läkemedelsinteraktionsstudier
Det finns kliniskt signifikanta, kända läkemedelsinteraktioner mellan paroxetin och andra läkemedel [se LÄKEMEDELSINTERAKTIONER ].
Figur 1. Paroxetins inverkan på farmakokinetiken för samtidigt administrerade läkemedel (log-skala)
Figur 2. Inverkan av samtidigt administrerade läkemedel på farmakokinetiken för paroxetin
Teofyllin
Rapporter om förhöjda teofyllinnivåer i samband med PAXIL-behandling har rapporterats. Även om denna interaktion inte har studerats formellt, rekommenderas att teofyllinnivåerna övervakas när dessa läkemedel administreras samtidigt.
Läkemedel som metaboliseras av Cytokrom CYP3A4
En interaktionsstudie in vivo som involverade samtidig administrering under steady-state-förhållanden av paroxetin och terfenadin, ett substrat för CYP3A4, visade ingen effekt av paroxetin på terfenadins farmakokinetik. Dessutom har in vitro-studier visat att ketokonazol, en potent hämmare av CYP3A4-aktivitet, är minst 100 gånger mer potent än paroxetin som en hämmare av metabolismen av flera substrat för detta enzym, inklusive terfenadin, astemizol, cisaprid, triazolam och cyklosporin. Paroxetins omfattning av hämning av CYP3A4-aktivitet förväntas inte vara av klinisk betydelse.
Specifika populationer
Effekten av specifika populationer på farmakokinetiken för paroxetin visas i figur 3.
Den rekommenderade startdosen och maximala dosen av PAXIL reduceras hos äldre patienter, patienter med gravt nedsatt njurfunktion och patienter med gravt nedsatt leverfunktion [se DOSERING OCH ADMINISTRERING ].
Figur 3. Inverkan av specifik population på farmakokinetiken för paroxetin (log-skala)
Kliniska studier
Major depressiv sjukdom
Effekten av PAXIL som behandling av egentlig depression (MDD) har fastställts i 6 placebokontrollerade studier av patienter med MDD (i åldern 18 till 73). I dessa studier har PAXIL visat sig vara statistiskt signifikant effektivare än placebo vid behandling av MDD med minst två av följande mått: Hamilton Depression Rating Scale (HDRS), Hamilton-deprimerad humör och Clinical Global Impression (CGI)- Sjukdomens svårighetsgrad. PAXIL var statistiskt signifikant bättre än placebo när det gällde förbättring av HDRS-subfaktorpoängen, inklusive det deprimerade humöret, sömnstörningsfaktorn och ångestfaktorn.
Långtidseffekt av PAXIL 10 mg för behandling av MDD hos polikliniska patienter visades i en randomiserad abstinensstudie. Patienter som svarade på PAXIL (HDRS totalpoäng
Tvångssyndrom
Effektiviteten av PAXIL vid behandling av tvångssyndrom (OCD) visades i två 12-veckors multicenter placebokontrollerade studier av vuxna öppenvårdspatienter (studierna 1 och 2). Patienterna hade måttlig till svår OCD (DSM-IIIR) med genomsnittliga baslinjevärden på Yale Brown Obsessive Compulsive Scale (YBOCS) totalpoäng som sträckte sig från 23 till 26. I studie 1, en studie för att hitta dosintervall, fick patienterna fasta dagliga doser av PAXIL 20 mg, 40 mg eller 60 mg. Studie 1 visade att dagliga doser av PAXIL 40 mg och 60 mg är effektiva vid behandling av OCD. Patienter som fick doser av PAXIL 40 mg och 60 mg upplevde en genomsnittlig minskning med cirka 6 respektive 7 poäng på YBOCS totalpoäng som var statistiskt signifikant högre än den ungefärliga 4-punktsreduktionen vid 20 mg och en minskning med 3 poäng i de placebobehandlade patienterna. Studie 2 var en studie med flexibel dos som jämförde PAXIL 20 mg till 60 mg dagligen med klomipramin 25 mg till 250 mg dagligen eller placebo). I denna studie upplevde patienter som fick PAXIL en genomsnittlig minskning på cirka 7 poäng på YBOCS totalpoäng, vilket var statistiskt signifikant större än medelminskningen på cirka 4 poäng hos placebobehandlade patienter.
Följande tabell ger resultatklassificeringen efter behandlingsgrupp på Global Improvement-objekt på Clinical Global Impression (CGI)-skalan för studie 1.
Subgruppsanalyser tydde inte på att det fanns några skillnader i behandlingsresultat som funktion av ålder eller kön.
Den långsiktiga effekten av PAXIL för behandling av OCD fastställdes i en långsiktig förlängning av studie 1. Patienter som svarade på PAXIL under den 3-månaders dubbelblinda fasen och en 6-månaders förlängning av öppen PAXIL 20 mg till 60 mg dagligen randomiserades till antingen PAXIL 10 mg eller placebo i en 6-månaders dubbelblind förebyggande fas av återfall. Patienter randomiserade till PAXIL var statistiskt signifikant mindre benägna att återfalla än placebobehandlade patienter.
Panikångest
Effektiviteten av PAXIL 20 mg vid behandling av panikångest (PD) visades i tre 10- till 12-veckors multicenter, placebokontrollerade studier av vuxna öppenvårdspatienter (Studier 1, 2 och 3). Patienterna hade PD (DSM-IIIR), med eller utan agorafobi. I dessa studier visades PAXIL vara statistiskt signifikant effektivare än placebo vid behandling av PD med minst 2 av 3 mått på panikattackerfrekvensen och på Clinical Global Impression Severity of Illness-poängen.
Studie 1 var en 10-veckors studie av dosintervall; patienter fick fasta doser av PAXIL 10 mg, 20 mg eller 40 mg dagligen eller placebo. En statistiskt signifikant skillnad från placebo observerades endast för gruppen PAXIL 40 mg dagligen. Vid endpoint var 76 % av patienterna som fick PAXIL 40 mg dagligen fria från panikattacker, jämfört med 44 % av placebobehandlade patienter.
Studie 2 var en 12-veckors studie med flexibel dos som jämförde PAXIL 10 mg med 60 mg dagligen och placebo. Vid endpoint var 51 % av de PAXIL-behandlade patienterna fria från panikattacker jämfört med 32 % av de placebobehandlade patienterna.
Studie 3 var en 12-veckors studie med flexibel dos som jämförde PAXIL 10 mg till 60 mg dagligen med placebo hos patienter som samtidigt fick standardiserad kognitiv beteendeterapi. Vid endpoint visade 33 % av de PAXIL-behandlade patienterna en minskning till 0 eller 1 panikattacker jämfört med 14 % av placebobehandlade patienter.
I studierna 2 och 3 var medeldosen av PAXIL för fullbordare vid endpoint cirka 40 mg dagligen.
Långtidseffekt av PAXIL 10 mg vid PD visades i en förlängning av studie 1. Patienter som svarade på PAXIL 20 mg under den 10 veckor långa dubbelblinda fasen och under en 3-månaders dubbelblind förlängningsfas randomiserades till antingen PAXIL 10 mg, 20 mg eller 40 mg dagligen eller placebo i en 3-månaders dubbelblind förebyggande fas av återfall. Patienter randomiserade till PAXIL 20 mg hade statistiskt signifikant mindre risk att återfalla än placebobehandlade patienter.
Subgruppsanalyser tydde inte på att det fanns några skillnader i behandlingsresultat som funktion av ålder eller kön.
Social fobi
Effektiviteten av PAXIL vid behandling av social ångeststörning (SAD) visades i tre 12-veckors multicenter, placebokontrollerade studier (Studier 1, 2 och 3) av vuxna öppenvårdspatienter med SAD (DSM-IV). I dessa studier utvärderades effektiviteten av PAXIL 30 mg jämfört med placebo på basis av (1) andelen svarande, enligt definitionen av en Clinical Global Impression (CGI) Improvement-poäng på 1 (mycket förbättrad) eller 2 (mycket förbättrad) ), och (2) förändring från baslinjen i Liebowitz Social Anxiety Scale (LSAS).
Studie 1 och 2 var studier med flexibel dos som jämförde PAXIL 20 mg med 50 mg dagligen och placebo. PAXIL visade statistiskt signifikant överlägsenhet gentemot placebo på både CGI Improvement responder-kriteriet och Liebowitz Social Anxiety Scale (LSAS). I studie 1, för patienter som avslutade till vecka 12, var 69 % av de PAXIL-behandlade patienterna jämfört med 29 % av placebobehandlade patienter som svarade på CGI Improvement. I studie 2 svarade CGI Improvement på 77 % och 42 % för PAXIL- respektive placebobehandlade patienter.
Studie 3 var en 12-veckors studie som jämförde fasta doser av PAXIL 20 mg, 40 mg eller 60 mg dagligen med placebo. PAXIL 20 mg var statistiskt signifikant överlägsen placebo på både LSAS Total Score och CGI Improvement responder-kriteriet; Det fanns trender för överlägsenhet gentemot placebo för PAXIL 40 mg och 60 mg dagliga dosgrupper. Det fanns ingen indikation i denna studie på någon ytterligare fördel för doser högre än 20 mg dagligen.
Undergruppsanalyser visade generellt inte skillnader i behandlingsresultat som en funktion av ålder, ras eller kön.
Generaliserat ångestsyndrom
Effektiviteten av PAXIL vid behandling av generaliserat ångestsyndrom (GAD) visades i två 8-veckors, multicenter, placebokontrollerade studier (studier 1 och 2) av vuxna öppenvårdspatienter med GAD (DSM-IV).
Studie 1 var en 8-veckors studie som jämförde fasta doser av PAXIL 20 mg eller 40 mg dagligen med placebo. Doser av PAXIL 20 mg eller 40 mg visades båda vara statistiskt signifikant överlägsna placebo på Hamilton Rating Scale for Anxiety (HAM-A) totalpoäng.
Det fanns inte tillräckliga bevis i denna studie för att föreslå en större fördel för PAXIL 40 mg daglig dos jämfört med 20 mg daglig dos.
Studie 2 var en studie med flexibel dos som jämförde PAXIL 20 mg med 50 mg dagligen och placebo. PAXIL visade statistiskt signifikant överlägsenhet gentemot placebo på Hamilton Rating Scale for Anxiety (HAM-A) totalpoäng.
En tredje studie, en studie med flexibel dos som jämförde PAXIL 20 mg till 50 mg dagligen med placebo, visade inte statistiskt signifikant överlägsenhet för PAXIL jämfört med placebo på Hamilton Rating Scale for Anxiety (HAM-A) totalpoäng, det primära resultatet.
Subgruppsanalyser indikerade inte skillnader i behandlingsresultat som en funktion av ras eller kön. Det fanns inte tillräckligt många äldre patienter för att göra subgruppsanalyser utifrån ålder.
en långtidsstudie randomiserades 566 patienter som uppfyllde DSM-IV-kriterierna för GAD, som hade svarat under en singelblind, 8-veckors akut behandlingsfas med PAXIL 20 mg till 50 mg dagligen, till fortsättning av PAXIL 30 mg. samma dos, eller placebo, i upp till 24 veckors observation för återfall. Respons under den enkelblinda fasen definierades genom att ha en minskning på ≥2 poäng jämfört med baslinjen på CGI-Severity of Illness-skalan, till en poäng på ≤3. Återfall under den dubbelblinda fasen definierades som en ökning med ≥2 poäng jämfört med baslinjen på CGI-Sverity of Illness-skalan till en poäng på ≥4, eller utsättning på grund av bristande effekt. Patienter som fortsatte att få PAXIL 40 mg upplevde en statistiskt signifikant lägre återfallsfrekvens under de efterföljande 24 veckorna jämfört med de som fick placebo.
Posttraumatisk stressyndrom
Effektiviteten av PAXIL 20 mg vid behandling av posttraumatiskt stressyndrom (PTSD) visades i två 12-veckors, multicenter, placebokontrollerade studier (studier 1 och 2) av vuxna öppenvårdspatienter som uppfyllde DSM-IV-kriterierna för PTSD. Den genomsnittliga varaktigheten av PTSD-symtom för de 2 studierna kombinerade var 13 år (från 0,1 år till 57 år). Andelen patienter med sekundär MDD eller icke-PTSD ångeststörningar i de kombinerade 2 studierna var 41 % (356 av 858 patienter) respektive 40 % (345 av 858 patienter). Studieresultatet bedömdes av (1) Clinician-Administered PTSD Scale Part 2 (CAPS-2) poäng och (2) Clinical Global Impression-Global Improvement Scale (CGI-I). CAPS-2 är ett instrument med flera artiklar som mäter tre aspekter av PTSD med följande symptomkluster: Återuppleva/intrång, undvikande/bedövande och hyperarousal. De två primära resultaten för varje studie var (1) förändring från baslinje till effektmått på CAPS-2 totalpoäng (17 poster) och (2) andel svarspersoner på CGI-I, där responders definierades som patienter med en poäng av 1 (mycket förbättrad) eller 2 (mycket förbättrad).
Studie 1 var en 12-veckors studie som jämförde fasta doser av PAXIL 20 mg eller 40 mg dagligen med placebo. Doser av PAXIL 20 mg och 40 mg visades vara statistiskt signifikant överlägsna placebo vid förändring från baslinjen för CAPS-2 totalpoäng och andelen responders på CGI-I. Det fanns inte tillräckliga bevis i denna studie för att antyda en större fördel för 40 mg daglig dos jämfört med 20 mg daglig dos.
Studie 2 var en 12-veckors studie med flexibel dos som jämförde PAXIL 20 mg och 50 mg dagligen med placebo. PAXIL 40 mg visades vara signifikant överlägsen placebo vid förändring från baslinjen för CAPS-2 totalpoäng och andelen svarande på CGI-I.
En tredje studie, en studie med flexibel dos som jämförde PAXIL 20 mg till 50 mg dagligen med placebo, visade att PAXIL 20 mg var statistiskt signifikant överlägsen placebo vid förändring från baslinjen för CAPS-2 totalpoäng, men inte på andelen svarande på CGI -Jag.
Majoriteten av patienterna i dessa studier var kvinnor (68 % kvinnor: 377 av 551 försökspersoner i studie 1 och 66 % kvinnor: 202 av 303 försökspersoner i studie 2). Subgruppsanalyser indikerade inte skillnader i behandlingsresultat som en funktion av kön. Det fanns ett otillräckligt antal patienter som var 65 år och äldre eller var icke-kaukasiska för att genomföra subgruppsanalyser på basis av ålder respektive ras.
PATIENTINFORMATION
PAXIL® (PAX-il)(paroxetin) tabletter & oral suspension
Vilken är den viktigaste informationen jag borde veta om PAXIL?
PAXIL kan orsaka allvarliga biverkningar, inklusive:
- Ökad risk för självmordstankar eller handlingar. PAXIL 10mg och andra antidepressiva läkemedel kan öka självmordstankar och -handlingar hos vissa personer 24 år och yngre, särskilt inom de första månaderna av behandlingen eller när dosen ändras. PAXIL är inte avsett för barn.
- Depression eller andra psykiska sjukdomar är de viktigaste orsakerna till självmordstankar och -handlingar.
Hur kan jag se efter och försöka förebygga självmordstankar och -handlingar?
- Var noga uppmärksam på alla förändringar, särskilt plötsliga förändringar i humör, beteende, tankar eller känslor eller om du utvecklar självmordstankar eller -handlingar. Detta är mycket viktigt när ett antidepressivt läkemedel påbörjas eller när dos byter.
- Ring din vårdgivare direkt för att rapportera nya eller plötsliga förändringar i humör, beteende, tankar eller känslor eller om du utvecklar självmordstankar eller -handlingar.
- Håll alla uppföljningsbesök hos din vårdgivare som planerat. Ring din vårdgivare mellan besöken vid behov, särskilt om du är orolig för symtom.
Ring din vårdgivare eller få akut medicinsk hjälp omedelbart om du har något av följande symtom, särskilt om de är nya, värre eller oroar dig:
- försök att begå självmord
- agerar aggressivt eller våldsamt
- ny eller värre depression
- känner sig upprörd, rastlös, arg eller irriterad
- ökad aktivitet och prata mer än vad som är normalt för dig
- agerar på farliga impulser
- tankar om självmord eller att dö
- ny eller värre ångest eller panikattacker
- sömnproblem
- andra ovanliga förändringar i beteende eller humör
Vad är PAXIL?
PAXIL 30mg är ett receptbelagt läkemedel som används av vuxna för att behandla:
- En viss typ av depression som kallas Major Depressive Disorder (MDD)
- Tvångssyndrom (OCD)
- Paniksyndrom (PD)
- Socialt ångestsyndrom (SAD)
- Generaliserat ångestsyndrom (GAD)
- Posttraumatiskt stressyndrom (PTSD)
Ta inte PAXIL om du:
- ta en monoaminoxidashämmare (MAO-hämmare)
- har slutat ta en MAO-hämmare under de senaste 14 dagarna
- behandlas med antibiotikum linezolid eller intravenöst metylenblått
- tar pimozid
- tar tioridazin
- är allergisk mot paroxetin eller något av innehållsämnena i PAXIL. Se slutet av denna medicineringsguide för en komplett lista över ingredienser i PAXIL.
Fråga din vårdgivare eller apotekspersonal om du är osäker på om du tar en MAO-hämmare eller något av dessa läkemedel, inklusive antibiotikumet linezolid eller intravenöst metylenblått.
Börja inte ta en MAO-hämmare på minst 14 dagar efter att du avslutat behandlingen med PAXIL.
Innan du tar PAXIL, berätta för din vårdgivare om alla dina medicinska tillstånd, inklusive om du:
- har hjärtproblem
- har eller haft blödningsproblem
- har, eller har en familjehistoria av, bipolär sjukdom, mani eller hypomani
- har eller haft kramper eller kramper
- har glaukom (högt tryck i ögat)
- har låga natriumnivåer i ditt blod
- har benproblem
- har njur- eller leverproblem
- är gravid eller planerar att bli gravid. PAXIL 40mg kan skada ditt ofödda barn. Tala med din vårdgivare om riskerna för ditt ofödda barn om du tar PAXIL under graviditeten. Berätta genast för din vårdgivare om du blir gravid eller tror att du är gravid under behandling med PAXIL.
- ammar eller planerar att amma. PAXIL passerar över i din bröstmjölk. Prata med din vårdgivare om det bästa sättet att mata ditt barn under behandlingen med PAXIL.
Berätta för din vårdgivare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott.
PAXIL och vissa andra läkemedel kan påverka varandra och orsaka allvarliga biverkningar. PAXIL 30 mg kan påverka hur andra läkemedel fungerar och andra läkemedel kan påverka hur PAXIL fungerar.
Berätta särskilt för din vårdgivare om du tar:
- läkemedel som används för att behandla migränhuvudvärk som kallas triptaner
- tricykliska antidepressiva medel
- fentanyl
- litium
- tramadol
- tryptofan
- buspiron
- amfetamin
- Johannesört
- läkemedel som kan påverka blodets koagulering såsom aspirin, icke-steroida antiinflammatoriska läkemedel (NSAID), warfarin
- diuretika
- tamoxifen
- läkemedel som används för att behandla humör, ångest, psykotiska störningar eller tankestörningar, inklusive selektivt serontoninåterupptag (SSRI) och serotonin-noradrenalinåterupptagshämmare (SNRI)
Fråga din vårdgivare om du inte är säker på om du tar något av dessa läkemedel. Din vårdgivare kan berätta för dig om det är säkert att ta PAXIL 10 mg tillsammans med dina andra läkemedel.
Starta eller sluta inte med andra läkemedel under behandling med PAXIL utan att först prata med din läkare. Om du plötsligt slutar med PAXIL kan du få allvarliga biverkningar. Ser, "Vilka är de möjliga biverkningarna av PAXIL 20mg?"
Vet vilka mediciner du tar. Håll en lista över dem att visa för din vårdgivare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag ta PAXIL?
- Ta PAXIL precis som ordinerats. Din vårdgivare kan behöva ändra dosen av PAXIL 30 mg tills det är rätt dos för dig.
- Ta PAXIL 1 gång varje dag på morgonen.
- PAXIL 30 mg kan tas med eller utan mat.
- Om du tar PAXIL oral suspension, skaka suspensionen väl innan du tar.
- Om du tar för mycket PAXIL, ring din giftcentral på 1-800-222-1222 eller gå till närmaste akutmottagning direkt.
Vilka är möjliga biverkningar av PAXIL 10mg?
PAXIL 40mg kan orsaka allvarliga biverkningar, inklusive:
- Ser, "Vad är den viktigaste informationen jag borde veta om PAXIL?"
- Serotonergt syndrom. Ett potentiellt livshotande problem som kallas serotonergt syndrom kan inträffa när du tar PAXIL 20 mg tillsammans med vissa andra läkemedel. Se, "Vem bör inte ta PAXIL?" Ring din vårdgivare eller gå till närmaste akutmottagning direkt om du har något av följande tecken och symtom på serotonergt syndrom:
- agitation
- se eller höra saker som inte är verkliga (hallucinationer)
- förvirring
- koma
- snabb hjärtslag
- förändringar i blodtrycket
- yrsel
- svettas
- spolning
- hög kroppstemperatur (hypertermi)
- skakningar (skakningar), stela muskler eller muskelryckningar
- förlust av koordination
- anfall
- illamående, kräkningar, diarré
- Ögonproblem (stängningsvinkelglaukom). PAXIL 10mg kan orsaka en typ av ögonproblem som kallas förslutningsvinkelglaukom hos personer med vissa andra ögonsjukdomar. Du kanske vill genomgå en synundersökning för att se om du är i riskzonen och få förebyggande behandling om du är det. Ring din vårdgivare om du har ögonsmärta, synförändringar eller svullnad eller rodnad i eller runt ögat.
- Medicininteraktioner. Att ta PAXIL 20 mg tillsammans med vissa andra läkemedel inklusive tioridazin och pimozid kan öka risken för att utveckla ett allvarligt hjärtproblem som kallas QT-förlängning.
- Kramper (kramper).
- Maniska episoder. Maniska episoder kan inträffa hos personer med bipolär sjukdom som tar PAXIL. Symtom kan inkludera:
- kraftigt ökad energi
- racing tankar
- ovanligt storslagna idéer
- prata mer eller snabbare än vanligt
- svåra sömnproblem
- hänsynslöst beteende
- överdriven lycka eller irritabilitet
- Utsättningssyndrom. Om du plötsligt stoppar PAXIL 20 mg kan du få allvarliga biverkningar. Din vårdgivare kanske vill minska din dos långsamt. Symtom kan inkludera:
- illamående
- svettas
- förändringar i ditt humör
- irritabilitet och agitation
- yrsel
- elektrisk stötkänsla (parestesi)
- darrning
- ångest
- förvirring
- huvudvärk
- trötthet
- problem med att sova
- hypomani
- ringningar i öronen (tinnitus)
- anfall
- Låga natriumnivåer i ditt blod (hyponatremi). Låga natriumnivåer i ditt blod som kan vara allvarliga och kan orsaka dödsfall kan inträffa under behandling med PAXIL. Äldre personer och personer som tar vissa läkemedel kan löpa en större risk att utveckla låga natriumnivåer i ditt blod. Tecken och symtom kan inkludera:
- huvudvärk
- koncentrationssvårigheter
- minnesförändringar
- förvirring
- svaghet och ostadighet på fötterna som kan leda till fall
mer allvarliga eller mer plötsliga fall inkluderar tecken och symtom:
- se eller höra saker som inte är verkliga (hallucinationer)
- svimning
- anfall
- koma
- andningsstopp (andningsstopp)
- Onormal blödning. Att ta PAXIL med acetylsalicylsyra, NSAID eller blodförtunnande medel kan öka denna risk. Berätta för din vårdgivare om eventuella ovanliga blödningar eller blåmärken.
- Benfrakturer.
De vanligaste biverkningarna av PAXIL 10mg inkluderar:
- manliga och kvinnliga sexuella funktionsproblem
- förstoppning
- diarre
- torr mun
- problem med att sova
- nervositet
- svettas
- gapande
- svaghet (asteni)
- minskad aptit
- yrsel
- infektion
- illamående
- sömnighet
- skakning (tremor)
Dessa är inte alla möjliga biverkningar av PAXIL.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara PAXIL?
- Förvara PAXIL-tabletter mellan 59°F till 86°F (15°C till 30°C).
- Förvara PAXIL 10 mg oral suspension vid eller under 77°F (25°C).
Förvara PAXIL och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av PAXIL.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Ta inte PAXIL för ett tillstånd som det inte ordinerats för. Ge inte PAXIL till andra personer, även om de har samma symtom som du har. Det kan skada dem. Du kan be din vårdgivare eller apotekspersonal om information om PAXIL som är skriven för vårdpersonal.
Vilka är ingredienserna i PAXIL 30mg?
Aktiv beståndsdel: paroxetinhydroklorid
Inaktiva Ingredienser:
dibasiskt kalciumfosfatdihydrat, hypromellos, magnesiumstearat, polyetylenglykoler, polysorbat 80, natriumstärkelseglykolat, titandioxid och 1 eller flera av följande: D&C Red No. 30 aluminium lake, D&C Yellow No. 10 aluminium lake, FD&C 2 aluminiumsjö, FD&C gul nr 6 aluminiumsjö
Oral suspension: citronsyra (vattenfri), FD&C gul nr. 6, aromämnen, glycerin, metylparaben, mikrokristallin cellulosa och karboximetylcellulosanatrium, polakrilinkalium, propylenglykol, propylparaben, renat vatten, sackarinatrium, simetikonemulsion och natriumcitrat (dihydrat)
Denna medicineringsguide har godkänts av US Food and Drug Administration.
