Seroquel 25mg, 50mg, 100mg, 200mg, 300mg Quetiapine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Seroquel 100mg och hur används det?
Seroquel 50mg är ett receptbelagt läkemedel som används för att behandla symptomen på schizofreni, bipolär störning I, mani; Bipolär sjukdom, depressiva episoder; Bipolär I sjukdom, underhåll; och allvarlig depressiv sjukdom. Seroquel 50mg kan användas ensamt eller tillsammans med andra läkemedel.
Seroquel tillhör en klass av läkemedel som kallas antipsykotika, 2:a generationen; Antimaniska medel.
Det är inte känt om Seroquel 200mg är säkert och effektivt för barn yngre än 12 år.
Vilka är de möjliga biverkningarna av Seroquel 50mg?
Seroquel kan orsaka allvarliga biverkningar inklusive:
- okontrollerade muskelrörelser i ansiktet (tugga, smälla på läpparna, rynka pannan, tungrörelser, blinka eller ögonrörelser),
- ansiktsmaskliknande utseende,
- problem med att svälja,
- problem med tal,
- yrsel,
- svår förstoppning,
- smärtsam eller svår urinering,
- suddig syn,
- tunnelseende,
- ögonsmärta,
- ser glorier runt ljus,
- mycket stela (styva) muskler,
- hög feber,
- svettas,
- förvirring,
- snabba eller ojämna hjärtslag,
- skakningar,
- svimning,
- ökad törst,
- ökad urinering,
- torr mun,
- fruktig andedräkt lukt,
- feber,
- frossa,
- munsår,
- hudsår,
- öm hals,
- hosta och
- problem att andas
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Seroquel inkluderar:
- talproblem,
- yrsel,
- dåsighet,
- trötthet,
- brist på energi,
- snabba hjärtslag,
- Täppt i näsan,
- ökad aptit,
- viktökning,
- orolig mage,
- kräkningar,
- förstoppning,
- muntorrhet och
- onormalt leverfunktionstest
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Seroquel. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
ÖKAD DÖDLIGHET HOS ÄLDRE PATIENTER MED DEMENSREATERAT PSYKOS; och SJÄLVmordstankar och -beteenden
Ökad dödlighet hos äldre patienter med demensrelaterad psykos
Äldre patienter med demensrelaterad psykos som behandlas med antipsykotiska läkemedel löper en ökad risk att dö [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER]. SEROQUEL är inte godkänt för behandling av patienter med demensrelaterad psykos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
Suicidala tankar och beteenden
Antidepressiva läkemedel ökade risken för självmordstankar och självmordsbeteende hos barn, ungdomar och unga vuxna i korttidsstudier. Dessa studier visade ingen ökning av risken för suicidtankar och självmordsbeteende vid användning av antidepressiva läkemedel hos patienter över 24 år; det fanns en minskning av risken med användning av antidepressiva läkemedel hos patienter i åldern 65 år och äldre [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
Hos patienter i alla åldrar som påbörjas med antidepressiv terapi, övervaka noga för försämring och uppkomst av självmordstankar och -beteenden. Informera familjer och vårdgivare om behovet av noggrann observation och kommunikation med förskrivaren [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
SEROQUEL 50mg är inte godkänt för användning hos pediatriska patienter under tio år [se Användning i specifika populationer].
BESKRIVNING
SEROQUEL® (quetiapinfumarat) är ett psykotropiskt medel som tillhör en kemisk klass, dibensotiazepinderivaten. Den kemiska beteckningen är 2-[2-(4-dibenso[b,f][1,4]tiazepin-11-yl-1-piperazinyl)etoxi]-etanolfumarat (2:1) (salt). Det finns i tabletter som fumaratsaltet. Alla doser och tablettstyrkor uttrycks som milligram bas, inte som fumaratsalt. Dess molekylformel är C42H50N6O4S2•C4H4O4 och den har en molekylvikt på 883,11 (fumaratsalt). Strukturformeln är:
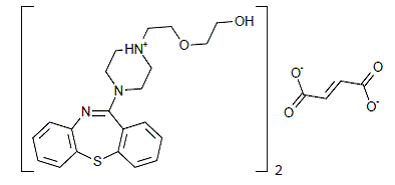
Quetiapinfumarat är ett vitt till benvitt kristallint pulver som är måttligt lösligt i vatten.
SEROQUEL tillhandahålls för oral administrering som 25 mg (rund, persika), 50 mg (rund, vit), 100 mg (rund, gul), 200 mg (rund, vit), 300 mg (kapselformad, vit) och 400 mg (kapselformade, gula) tabletter.
Inaktiva ingredienser är povidon, dibasiskt dikalciumfosfatdihydrat, mikrokristallin cellulosa, natriumstärkelseglykolat, laktosmonohydrat, magnesiumstearat, hypromellos, polyetylenglykol och titandioxid.
25 mg tabletterna innehåller röd järnoxid och gul järnoxid och 100 mg och 400 mg tabletterna innehåller endast gul järnoxid.
INDIKATIONER
Schizofreni
SEROQUEL XR är indicerat för behandling av schizofreni. Effekten av SEROQUEL XR vid schizofreni fastställdes i en 6-veckors och en underhållsstudie på vuxna med schizofreni. Effekten stöddes av tre 6-veckorsstudier på vuxna med schizofreni och en 6-veckorsstudie på ungdomar med schizofreni (13-17 år) behandlade med SEROQUEL [se Kliniska studier ].
Bipolär sjukdom
SEROQUEL 25 mg XR är indicerat för akut behandling av maniska eller blandade episoder associerade med bipolär störning I, både som monoterapi och som tillägg till litium eller divalproex. Effekten av SEROQUEL XR vid maniska eller blandade episoder av bipolär störning I fastställdes i en 3-veckors studie på vuxna med maniska eller blandade episoder associerade med bipolär störning I. Effekten stöddes av två 12-veckors monoterapistudier och en 3-veckors tilläggsprövning på vuxna med maniska episoder associerade med bipolär störning I samt en 3-veckors monoterapiprövning på barn och ungdomar (10 - 17 år) med maniska episoder associerade med bipolär sjukdom I behandlad med SEROQUEL [se Kliniska studier ].
SEROQUEL 100mg XR är indicerat för akut behandling av depressiva episoder i samband med bipolär sjukdom. Effekten av SEROQUEL XR fastställdes i en 8-veckors studie på vuxna med bipolär I- eller II-störning och stöddes av två 8-veckorsstudier på vuxna med bipolär I- eller II-störning behandlade med SEROQUEL [se Kliniska studier ].
SEROQUEL 100mg XR är indicerat för underhållsbehandling av bipolär sjukdom I, som ett komplement till litium eller divalproex. Effekten extrapolerades från två underhållsstudier på vuxna med bipolär störning I som behandlats med SEROQUEL. Effektiviteten av monoterapi för underhållsbehandling av bipolär störning I har inte utvärderats systematiskt i kontrollerade kliniska prövningar [se Kliniska studier ].
Tilläggsbehandling av allvarlig depressiv sjukdom (MDD)
SEROQUEL 100mg XR är indicerat för användning som tilläggsterapi till antidepressiva läkemedel för behandling av MDD. Effekten av SEROQUEL XR som tilläggsbehandling till antidepressiva läkemedel vid MDD fastställdes i två 6-veckorsstudier på vuxna med MDD som hade ett otillräckligt svar på antidepressiv behandling [se Kliniska studier ].
Särskilda överväganden vid behandling av pediatrisk schizofreni och bipolär störning I
Pediatrisk schizofreni och bipolär störning I är allvarliga psykiska störningar, men diagnos kan vara utmanande. För pediatrisk schizofreni kan symtomprofilerna variera, och för bipolär störning I kan patienter ha varierande mönster av periodicitet av maniska eller blandade symtom. Det rekommenderas att läkemedelsbehandling för pediatrisk schizofreni och bipolär störning I påbörjas först efter att en noggrann diagnostisk utvärdering har gjorts och noggrant övervägt riskerna förknippade med läkemedelsbehandling. Läkemedelsbehandling för både pediatrisk schizofreni och bipolär störning I är indicerad som en del av ett totalt behandlingsprogram som ofta inkluderar psykologiska, pedagogiska och sociala insatser.
DOSERING OCH ADMINISTRERING
Viktiga administrationsinstruktioner
SEROQUEL XR tabletter ska sväljas hela och inte delas, tuggas eller krossas.
Det rekommenderas att SEROQUEL 50mg XR tas utan mat eller med en lätt måltid (cirka 300 kalorier) [se KLINISK FARMAKOLOGI ].
SEROQUEL 25 mg XR ska administreras en gång dagligen, helst på kvällen.
Rekommenderad dosering
Den rekommenderade initialdosen, titreringen, dosintervallet och den maximala SEROQUEL 50 mg XR-dosen för varje godkänd indikation visas i Tabell 1 nedan. Efter initial dosering kan justeringar göras uppåt eller nedåt, om nödvändigt, beroende på patientens kliniska svar och tolerabilitet [se Kliniska studier ].
Underhållsbehandling för schizofreni och bipolär sjukdom I
Underhållsbehandling
Patienter bör regelbundet utvärderas för att fastställa behovet av underhållsbehandling och lämplig dos för sådan behandling [se Kliniska studier ].
Dosändringar hos äldre patienter
En långsammare dostitrering och en lägre måldos bör övervägas hos äldre och hos patienter som är försvagade eller som har en anlag för hypotensiva reaktioner [se Användning i specifika populationer , och KLINISK FARMAKOLOGI ]. Vid indikation bör dosökning utföras med försiktighet hos dessa patienter.
Äldre patienter bör inledas med SEROQUEL XR 50 mg/dag och dosen kan ökas i steg om 50 mg/dag beroende på den individuella patientens kliniska svar och tolerabilitet.
Dosändringar hos patienter med nedsatt leverfunktion
Patienter med nedsatt leverfunktion bör påbörjas med SEROQUEL XR 50 mg/dag. Dosen kan ökas dagligen i steg om 50 mg/dag till en effektiv dos, beroende på patientens kliniska svar och tolerabilitet.
Dosändringar vid användning med CYP3A4-hämmare
Seroquel XR-dosen ska reduceras till en sjättedel av den ursprungliga dosen när den samtidigt medicineras med en potent CYP3A4-hämmare (t.ex. ketokonazol, itrakonazol, indinavir, ritonavir, nefazodon, etc.). När CYP3A4-hämmaren sätts ut ska dosen av SEROQUEL XR ökas med 6 gånger [se KLINISK FARMAKOLOGI och LÄKEMEDELSINTERAKTIONER ].
Dosändringar vid användning med CYP3A4-inducerare
SeROQUEL XR-dosen bör ökas upp till 5 gånger den ursprungliga dosen när den används i kombination med en kronisk behandling (t.ex. mer än 7-14 dagar) av en potent CYP3A4-inducerare (t.ex. fenytoin, karbamazepin, rifampin, avasimibe, St. johannesört etc.). Dosen bör titreras baserat på den individuella patientens kliniska respons och tolerans. När CYP3A4-induceraren avbryts, bör dosen av SEROQUEL 100 mg XR reduceras till den ursprungliga nivån inom 7-14 dagar [se KLINISK FARMAKOLOGI och LÄKEMEDELSINTERAKTIONER ].
Återupptagande av behandling hos patienter som tidigare avbrutits
Även om det inte finns några data för att specifikt behandla återupptagande av behandling, rekommenderas att det initiala doseringsschemat ska följas vid återupptagande av behandlingen av patienter som har varit av med Seroquel 50 mg XR i mer än en vecka. Vid återstart av patienter som har varit av med Seroquel 300 mg XR i mindre än en vecka, kan det hända att gradvis dosökning inte behövs och underhållsdosen kan återupptas.
Byta patient från SEROQUEL 50mg tabletter till SEROQUEL 100mg XR tabletter
Patienter som för närvarande behandlas med SEROQUEL (formulering för omedelbar frisättning) kan bytas till SEROQUEL XR med motsvarande totala dagliga dos en gång dagligen. Individuella dosjusteringar kan vara nödvändiga.
Byte från antipsykotika
Det finns inga systematiskt insamlade data för att specifikt ta itu med byte av patienter från andra antipsykotika till SEROQUEL 200 mg XR, eller om samtidig administrering med andra antipsykotika. Även om omedelbart utsättande av den tidigare antipsykotiska behandlingen kan vara acceptabelt för vissa patienter, kan ett mer gradvis avbrott vara lämpligast för andra. I alla fall bör perioden med överlappande antipsykotisk administrering minimeras. När du byter patienter från depå antipsykotika, om det är medicinskt lämpligt, initiera SEROQUEL XR-behandling istället för nästa schemalagda injektion. Behovet av att fortsätta med befintlig medicinering av extrapyramidalt syndrom bör omvärderas med jämna mellanrum.
HUR LEVERERAS
Doseringsformer och styrkor
- 50 mg tabletter med förlängd frisättning är persika, filmdragerade, kapselformade, bikonvexa, intagliterade tabletter med ”XR 50” på ena sidan och slät på den andra sidan
- 150 mg tabletter med förlängd frisättning är vita, filmdragerade, kapselformade, bikonvexa, intagliterade tabletter med ”XR 150” på ena sidan och slät på den andra sidan
- 200 mg tabletter med förlängd frisättning är gula, filmdragerade, kapselformade, bikonvexa, intagliterade tabletter med ”XR 200” på ena sidan och släta på andra sidan
- 300 mg tabletter med förlängd frisättning är ljusgula, filmdragerade, kapselformade, bikonvexa, intagliterade tabletter med ”XR 300” på ena sidan och slät på den andra sidan
- 400 mg tabletter med förlängd frisättning är vita, filmdragerade, kapselformade, bikonvexa, intagliterade tabletter med ”XR 400” på ena sidan och slät på den andra sidan
Förvaring Och Hantering
50 mg tabletter ( NDC 0310-0280-60) persika, filmdragerad, kapselformad, bikonvex, intagliterad tablett med ”XR 50” på ena sidan och vanlig på den andra, levereras i burkar med 60 tabletter.
150 mg tabletter ( NDC 0310-0281-60) vit, filmdragerad, kapselformad, bikonvex, intagliterad tablett med ”XR 150” på ena sidan och slät på den andra, levereras i burkar med 60 tabletter.
200 mg tabletter ( NDC 0310-0282-60) gul, filmdragerad, kapselformad, bikonvex, intagliterad tablett med ”XR 200” på ena sidan och vanlig på den andra, levereras i burkar med 60 tabletter.
300 mg tabletter ( NDC 0310-0283-60) ljusgul, filmdragerad, kapselformad, bikonvex, intagliterad tablett med ”XR 300” på ena sidan och slät på den andra, levereras i burkar med 60 tabletter.
400 mg tabletter ( NDC 0310-0284-60) vit, filmdragerad, kapselformad, bikonvex, intagliterad tablett med ”XR 400” på ena sidan och slät på den andra, levereras i burkar med 60 tabletter.
Förvara SEROQUEL XR vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [Se USP ].
Distribuerat av: AstraZeneca Pharmaceuticals LP, Wilmington, DE 19850. Reviderad: Mar 2020
BIEFFEKTER
Följande biverkningar diskuteras mer i detalj i andra avsnitt av märkningen:
- Ökad dödlighet hos äldre patienter med demensrelaterad psykos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Självmordstankar och -beteenden hos ungdomar och unga vuxna [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Cerebrovaskulära biverkningar, inklusive stroke hos äldre patienter med demensrelaterad psykos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Malignt neuroleptikasyndrom (NMS) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Metaboliska förändringar (hyperglykemi, dyslipidemi, viktökning) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Tardiv dyskinesi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypotoni [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Faller [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Ökat blodtryck (barn och ungdomar) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Leukopeni, neutropeni och agranulocytos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Grå starr [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- QT-förlängning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kramper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypotyreos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hyperprolaktinemi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Potential för kognitiv och motorisk funktionsnedsättning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Reglering av kroppstemperatur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Dysfagi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Utsättningssyndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Antikolinerga (antimuskarina) effekter [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska studier
Eftersom kliniska studier utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska studierna av ett läkemedel inte direkt jämföras med frekvensen i de kliniska studierna av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Vuxna
Informationen nedan är hämtad från en databas för kliniska prövningar för SEROQUEL 200 mg som består av över 4300 patienter. Denna databas inkluderar 698 patienter exponerade för SEROQUEL för behandling av bipolär depression, 405 patienter exponerade för SEROQUEL 200 mg för behandling av akut bipolär mani (monoterapi och tilläggsterapi), 646 patienter exponerade för SEROQUEL för underhållsbehandling av bipolär I-sjukdom som tillägg behandling och cirka 2600 patienter och/eller normala försökspersoner som exponerats för 1 eller fler doser av SEROQUEL 200 mg för behandling av schizofreni.
Av dessa cirka 4 300 försökspersoner var cirka 4 000 (2 300 vid schizofreni, 405 vid akut bipolär mani, 698 vid bipolär depression och 646 för underhållsbehandling av bipolär störning I) patienter som deltog i effektivitetsstudier med flera doser, och deras erfarenhet motsvarade cirka 2400 patientår. Tillstånden och varaktigheten av behandlingen med SEROQUEL 200 mg varierade mycket och inkluderade (i överlappande kategorier) öppna och dubbelblinda faser av studier, slutenvård och öppenvård, studier med fasta doser och dostitrering samt korttids- eller långtidsstudier exponering. Biverkningar bedömdes genom att samla in biverkningar, resultat av fysiska undersökningar, vitala tecken, vikter, laboratorieanalyser, EKG och resultat av oftalmologiska undersökningar.
De angivna biverkningsfrekvenserna representerar andelen individer som minst en gång upplevt en biverkning av den listade typen.
Biverkningar associerade med avbrytande av behandling i kortvariga, placebokontrollerade prövningar
Schizofreni
Totalt sett var det liten skillnad i incidensen av utsättning på grund av biverkningar (4 % för SEROQUEL mot 3 % för placebo) i en pool av kontrollerade studier. Utsättningar på grund av somnolens (0,8 % SEROQUEL 100 mg vs. 0 % placebo) och hypotoni (0,4 % SEROQUEL 200 mg vs. 0 % placebo) ansågs dock vara läkemedelsrelaterade [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Bipolär sjukdom
Mani
Totalt sett var utsättningar på grund av biverkningar 5,7 % för SEROQUEL 25 mg vs. 5,1 % för placebo i monoterapi och 3,6 % för SEROQUEL mot 5,9 % för placebo i tilläggsbehandling.
Depression
Totalt sett var utsättningar på grund av biverkningar 12,3 % för SEROQUEL 300 mg jämfört med 19,0 % för SEROQUEL 600 mg och 5,2 % för placebo.
Vanligt observerade biverkningar i kortvariga, placebokontrollerade försök
studier med akut behandling av schizofreni (upp till 6 veckor) och bipolär mani (upp till 12 veckor), de vanligaste observerade biverkningarna förknippade med användning av SEROQUEL monoterapi (incidens på 5 % eller mer) och observerade i en takt på Seroquel minst dubbelt så stor som för placebo var somnolens (18 %), yrsel (11 %), muntorrhet (9 %), förstoppning (8 %), ökad ALAT (5 %), viktökning (5 %) och dyspepsi ( 5 %).
Biverkningar som inträffar med en incidens på 2 % eller mer bland SEROQUEL-behandlade patienter i kortvariga, placebokontrollerade prövningar
Förskrivaren bör vara medveten om att siffrorna i tabellerna och tabellerna inte kan användas för att förutsäga förekomsten av biverkningar under sedvanlig medicinsk praxis där patientegenskaper och andra faktorer skiljer sig från de som rådde i de kliniska prövningarna. På liknande sätt kan de angivna frekvenserna inte jämföras med siffror som erhållits från andra kliniska undersökningar som involverar olika behandlingar, användningar och utredare. De citerade siffrorna ger dock den förskrivande läkaren viss grund för att uppskatta det relativa bidraget av läkemedel och icke-läkemedelsfaktorer till biverkningsförekomsten i den studerade populationen.
Tabell 9 räknar upp förekomsten, avrundad till närmaste procent, av biverkningar som inträffade under akut behandling av schizofreni (upp till 6 veckor) och bipolär mani (upp till 12 veckor) hos 2 % eller fler av patienterna som behandlades med SEROQUEL (doser varierar). från 75 till 800 mg/dag) där incidensen hos patienter behandlade med SEROQUEL var högre än förekomsten hos placebobehandlade patienter.
I studier med akut tilläggsbehandling av bipolär mani (upp till 3 veckor) var de vanligast observerade biverkningarna förknippade med användningen av SEROQUEL (incidens på 5 % eller mer) och observerade i en frekvens av SEROQUEL minst dubbelt så stor som för placebo. somnolens (34 %), muntorrhet (19 %), asteni (10 %), förstoppning (10 %), buksmärtor (7 %), postural hypotoni (7 %), faryngit (6 %) och viktökning (6 %). %).
Tabell 10 räknar upp förekomsten, avrundad till närmaste procent, av biverkningar som inträffade under behandling (upp till 3 veckor) av akut mani hos 2 % eller fler av patienterna som behandlades med SEROQUEL (doser från 100 till 800 mg/dag) som används. som tilläggsbehandling till litium och divalproex där incidensen hos patienter behandlade med SEROQUEL var högre än förekomsten hos placebobehandlade patienter.
I studier av bipolär depression (upp till 8 veckor) var de vanligast observerade biverkningarna associerade med användning av SEROQUEL (incidens på 5 % eller mer) och observerade i en frekvens på Seroquel 200 mg minst dubbelt så hög som för placebo somnolens (57 % ), muntorrhet (44 %), yrsel (18 %), förstoppning (10 %) och slöhet (5 %).
Tabell 11 räknar upp förekomsten, avrundad till närmaste procent, av biverkningar som inträffade under behandling (upp till 8 veckor) av bipolär depression hos 2 % eller fler av patienterna som behandlades med SEROQUEL (doser på 300 och 600 mg/dag) där Incidensen hos patienter som behandlades med SEROQUEL var högre än förekomsten hos placebobehandlade patienter.
Utforskningar efter interaktioner på grundval av kön, ålder och ras avslöjade inga kliniskt betydelsefulla skillnader i förekomsten av biverkningar på grundval av dessa demografiska faktorer.
Dosberoende av biverkningar i kortsiktiga, placebokontrollerade försök
Dosrelaterade biverkningar
Spontant framkallade biverkningsdata från en studie av schizofreni där fem fasta doser av SEROQUEL (75 mg, 150 mg, 300 mg, 600 mg och 750 mg/dag) jämfördes med placebo undersöktes för dosrelaterade biverkningar. Logistiska regressionsanalyser visade ett positivt dossvar (p
Biverkningar i kliniska prövningar med quetiapin och inte listade någon annanstans på etiketten:
Följande biverkningar har också rapporterats med quetiapin: mardrömmar, överkänslighet och förhöjda serumkreatinfosfokinas (ej associerat med NMS), galaktorré, bradykardi (som kan uppstå vid eller nära behandlingsstart och vara associerad med hypotoni och/eller synkope ) minskade blodplättar, somnambulism (och andra relaterade händelser), förhöjda gamma-GT-nivåer, hypotermi, dyspné, eosinofili, urinretention, intestinal obstruktion och priapism.
Extrapyramidala symtom (EPS)
Dystoni
Klasseffekt
Symtom på dystoni, långvariga onormala sammandragningar av muskelgrupper, kan förekomma hos känsliga individer under de första dagarna av behandlingen. Dystoniska symtom inkluderar: spasmer i nackmusklerna, som ibland utvecklas till täthet i halsen, sväljsvårigheter, andningssvårigheter och/eller utskjutande tunga. Även om dessa symtom kan uppträda vid låga doser, förekommer de oftare och med större svårighetsgrad med hög styrka och vid högre doser av första generationens antipsykotiska läkemedel. En förhöjd risk för akut dystoni observeras hos män och yngre åldersgrupper.
Fyra metoder användes för att mäta EPS: (1) Simpson-Angus totalpoäng (medelförändring från baslinjen) som utvärderar Parkinsonism och akatisi, (2) Barnes Akathisia Rating Scale (BARS) Global Assessment Score, (3) förekomsten av spontana klagomål av EPS (akatisi, akinesi, kugghjulsstyvhet, extrapyramidalt syndrom, hypertoni, hypokinesi, nackstyvhet och tremor), och (4) användning av antikolinerga läkemedel för att behandla EPS.
Vuxna
Data från en 6-veckors klinisk studie av schizofreni som jämförde fem fasta doser av SEROQUEL (75, 150, 300, 600, 750 mg/dag) gav bevis för avsaknaden av extrapyramidala symtom (EPS) och dosrelaterad EPS förknippad med SEROQUEL 100mg behandling. Tre metoder användes för att mäta EPS: (1) Simpson-Angus totalpoäng (medelförändring från baslinjen) som utvärderar Parkinsonism och akatisi, (2) förekomst av spontana besvär av EPS (akatisi, akinesi, kugghjulsstyvhet, extrapyramidalt syndrom, hypertoni, hypokinesi, nackstelhet och tremor), och (3) användning av antikolinerga läkemedel mot EPS.
tabell 12 inkluderade dystoniska händelser nackstyvhet, hypertoni, dystoni, muskelstelhet, oculogyration; Parkinsonism inkluderade kugghjulsstyvhet, tremor, dregling, hypokinesi; akatisi innefattade akatisi, psykomotorisk agitation; dyskinetisk händelse inkluderade tardiv dyskinesi, dyskinesi, koreoatetos; och andra extrapyramidala händelser inkluderade rastlöshet, extrapyramidal störning, rörelsestörning.
Incidensfrekvenser för Parkinsonism mätt med Simpson-Angus totalpoäng för placebo och de fem fasta doserna (75, 150, 300, 600, 750 mg/dag) var: -0,6; -1,0, -1,2; -1,6; -1,8 och -1,8. Andelen antikolinerga läkemedel som användes för att behandla EPS för placebo och de fem fasta doserna var: 14 %; 11%; 10%; 8%; 12 % och 11 %.
ytterligare sex placebokontrollerade kliniska prövningar (3 vid akut mani och 3 vid schizofreni) med variabla doser av SEROQUEL, fanns det inga skillnader mellan behandlingsgrupperna för SEROQUEL och placebo i förekomsten av EPS, enligt Simpson-Angus totalpoäng, spontana besvär av EPS och användning av samtidig antikolinerga mediciner för att behandla EPS.
I två placebokontrollerade kliniska prövningar för behandling av bipolär depression med 300 mg och 600 mg SEROQUEL 100 mg, var förekomsten av biverkningar potentiellt relaterade till EPS 12 % i båda dosgrupperna och 6 % i placebogruppen. I dessa studier var incidensen av de individuella biverkningarna (akatisi, extrapyramidal störning, tremor, dyskinesi, dystoni, rastlöshet, ofrivilliga muskelsammandragningar, psykomotorisk hyperaktivitet och muskelstelhet) generellt låg och översteg inte 4 % i någon behandlingsgrupp.
De tre behandlingsgrupperna var lika i genomsnittlig förändring i SAS totalpoäng och BARS Global Assessment-poäng vid slutet av behandlingen. Användningen av samtidig antikolinerga läkemedel var sällsynt och liknade i de tre behandlingsgrupperna.
Barn Och Ungdomar
Informationen nedan är hämtad från en databas för kliniska prövningar för SEROQUEL 200 mg bestående av över 1 000 pediatriska patienter. Denna databas inkluderar 677 patienter som exponerats för SEROQUEL 200 mg för behandling av schizofreni och 393 barn och ungdomar (10-17 år gamla) som exponerats för SEROQUEL för behandling av akut bipolär mani.
Biverkningar associerade med avbrytande av behandling i kortvariga, placebokontrollerade försök
Schizofreni
Incidensen av avbrott på grund av biverkningar för quetiapinbehandlade och placebobehandlade patienter var 8,2 % respektive 2,7 %. Den biverkning som ledde till utsättning av behandlingen hos 1 % eller fler av patienterna som fick SEROQUEL och med en högre incidens än placebo var somnolens (2,7 % och 0 % för placebo).
Bipolär I Mania
Incidensen av avbrott på grund av biverkningar för quetiapinbehandlade och placebobehandlade patienter var 11,4 % respektive 4,4 %. De biverkningar som ledde till utsättning av behandlingen hos 2 % eller fler av patienterna på SEROQUEL och med en högre incidens än placebo var somnolens (4,1 % mot 1,1 %) och trötthet (2,1 % mot 0).
Vanligt observerade biverkningar i kortvariga, placebokontrollerade försök
Vid behandling för schizofreni (upp till 6 veckor) var de vanligaste observerade biverkningarna i samband med användning av quetiapin hos ungdomar (incidensen 5 % eller mer och quetiapinincidensen minst dubbelt så hög som för placebo) somnolens (34 %), yrsel (12%), muntorrhet (7%), takykardi (7%).
Vid bipolär manibehandling (upp till 3 veckor) var de vanligast observerade biverkningarna i samband med användning av quetiapin hos barn och ungdomar (incidens på 5 % eller mer och quetiapinincidens minst dubbelt så hög som för placebo) somnolens (53 %), yrsel (18 %), trötthet (11 %), ökad aptit (9 %), illamående (8 %), kräkningar (8 %), takykardi (7 %), muntorrhet (7 %) och viktökning (6 % ).
I en akut (8-veckors) SEROQUEL 100 mg XR-studie på barn och ungdomar (10-17 år) med bipolär depression, där effekt inte fastställdes, var de vanligast observerade biverkningarna i samband med användningen av SEROQUEL XR (incidens 5 % eller mer och minst dubbelt så mycket för placebo) var yrsel 7 %, diarré 5 %, trötthet 5 % och illamående 5 %.
Biverkningar som uppträder med en incidens på ≥ 2 % bland SEROQUEL 300 mg-behandlade patienter i kortvariga, placebokontrollerade studier
Schizofreni (ungdomar, 13-17 år gamla)
Följande fynd baserades på en 6-veckors placebokontrollerad studie där quetiapin administrerades antingen i doser på 400 eller 800 mg/dag.
Tabell 13 räknar upp incidensen, avrundad till närmaste procent, av biverkningar som inträffade under behandling (upp till 6 veckor) av schizofreni hos 2 % eller fler av patienterna som behandlats med SEROQUEL (doser på 400 eller 800 mg/dag) där incidensen hos patienter som behandlades med SEROQUEL var minst dubbelt så hög incidensen hos placebobehandlade patienter.
Biverkningar som potentiellt var dosrelaterade med högre frekvens i 800 mg-gruppen jämfört med 400 mg-gruppen inkluderade yrsel (8 % vs. 15 %), muntorrhet (4 % vs. 10 %) och takykardi (6 % vs. . 11 %).
Bipolär I-mani (barn och ungdomar 10-17 år gamla)
Följande fynd baserades på en 3-veckors placebokontrollerad studie där quetiapin administrerades i antingen doser på 400 eller 600 mg/dag.
Vanligt observerade biverkningar
Vid bipolär manibehandling (upp till 3 veckor) var de vanligast observerade biverkningarna i samband med användning av quetiapin hos barn och ungdomar (incidens på 5 % eller mer och quetiapinincidens minst dubbelt så hög som för placebo) somnolens (53 %), yrsel (18 %), trötthet (11 %), ökad aptit (9 %), illamående (8 %), kräkningar (8 %), takykardi (7 %), muntorrhet (7 %) och viktökning (6 % ).
Tabell 14 räknar upp förekomsten, avrundad till närmaste procent, av biverkningar som inträffade under behandling (upp till 3 veckor) av bipolär mani hos 2 % eller fler av patienterna som behandlats med SEROQUEL (doser på 400 eller 600 mg/dag) där Incidensen hos patienter som behandlades med SEROQUEL var högre än förekomsten hos placebobehandlade patienter.
Biverkningar som potentiellt var dosrelaterade med högre frekvens i 600 mg-gruppen jämfört med 400 mg-gruppen inkluderade somnolens (50 % vs. 57 %), illamående (6 % vs. 10 %) och takykardi (6 % vs. 9 %).
Extrapyramidala symtom
en korttidsstudie med placebokontrollerad monoterapi på ungdomar med schizofreni (6 veckors varaktighet) var den sammanlagda förekomsten av extrapyramidala symtom 12,9 % (19/147) för SEROQUEL 100 mg och 5,3 % (4/75) för placebo, även om incidensen av de individuella biverkningarna (akatisi, tremor, extrapyramidal störning, hypokinesi, rastlöshet, psykomotorisk hyperaktivitet, muskelstelhet, dyskinesi) inte översteg 4,1 % i någon behandlingsgrupp. I en korttidsstudie med placebokontrollerad monoterapi på barn och ungdomar med bipolär mani (3 veckors varaktighet) var den sammanlagda förekomsten av extrapyramidala symtom 3,6 % (7/193) eller SEROQUEL och 1,1 % (1/90) för placebo.
Tabell 15 visar en lista över patienter med biverkningar som potentiellt är associerade med extrapyramidala symtom i den kortsiktiga placebokontrollerade monoterapistudien hos ungdomar med schizofreni (6 veckors varaktighet).
tabellerna 15–16 inkluderade dystoniska händelser nackstyvhet, hypertoni och muskelstelhet; Parkinsonism inkluderade kugghjulsstyvhet och tremor; akatisi inkluderade endast akatisi; dyskinetisk händelse inkluderade tardiv dyskinesi, dyskinesi och koreoatetos; och andra extrapyramidala händelser inkluderade rastlöshet och extrapyramidal störning.
Tabell 16 visar en lista över patienter med biverkningar associerade med extrapyramidala symtom i en korttidsstudie med placebokontrollerad monoterapi hos barn och ungdomar med bipolär mani (3 veckors varaktighet).
Förändringar i laboratorier, EKG och vitala tecken som observerats i kliniska studier
Laboratorieförändringar
Antal neutrofiler
Vuxna
placebokontrollerade kliniska prövningar för monoterapi som involverade 3368 patienter på quetiapinfumarat och 1515 på placebo, förekomsten av minst en förekomst av neutrofilantal VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Transaminasförhöjningar
Vuxna
Asymtomatiska, övergående och reversibla förhöjningar av serumtransaminaser (främst ALAT) har rapporterats. I schizofrenistudier på vuxna var andelen patienter med transaminashöjningar på >3 gånger de övre gränserna för det normala referensintervallet i en pool av 3 till 6 veckors placebokontrollerade studier cirka 6 % (29/483) för SEROQUEL jämfört med 1 % (3/194) för placebo. I prövningar med akut bipolär mani hos vuxna var andelen patienter med transaminashöjningar på >3 gånger de övre gränserna för det normala referensintervallet i en pool av 3 till 12 veckors placebokontrollerade studier cirka 1 % för både SEROQUEL (3 /560) och placebo (3/294). Dessa leverenzymförhöjningar inträffade vanligtvis inom de första 3 veckorna av läkemedelsbehandlingen och återgick omedelbart till nivåerna före studien med pågående behandling med SEROQUEL. I studier med bipolär depression var andelen patienter med transaminashöjningar på >3 gånger de övre gränserna för det normala referensintervallet i två 8-veckors placebokontrollerade studier 1 % (5/698) för SEROQUEL 50 mg och 2 % (6/ 347) för placebo.
Sänkt hemoglobin
Vuxna
I korttids placebokontrollerade studier inträffade minskningar av hemoglobin till ≤13 g/dL män, ≤12 g/dL kvinnor vid minst ett tillfälle hos 8,3 % (594/7155) av quetiapinbehandlade patienter jämfört med 6,2 % ( 219/3536) av patienter som behandlats med placebo. I en databas med kontrollerade och okontrollerade kliniska prövningar inträffade minskningar av hemoglobin till ≤13 g/dL män, ≤12 g/dL kvinnor vid minst ett tillfälle hos 11 % (2277/20729) av quetiapinbehandlade patienter.
Interferens med urinläkemedelsskärmar
Det har förekommit litteraturrapporter som tyder på falskt positiva resultat i urinenzymimmunanalyser för metadon och tricykliska antidepressiva medel hos patienter som har tagit quetiapin. Försiktighet bör iakttas vid tolkningen av positiva urinläkemedelsscreeningsresultat för dessa läkemedel, och bekräftelse med alternativ analysteknik (t.ex. kromatografiska metoder) bör övervägas.
EKG-förändringar
Vuxna
Jämförelser mellan grupper för poolade placebokontrollerade studier visade inga statistiskt signifikanta SEROQUEL/placebo-skillnader i andelen patienter som upplever potentiellt viktiga förändringar i EKG-parametrar, inklusive QT, QTc och PR-intervall. Emellertid jämfördes andelen patienter som uppfyller kriterierna för takykardi i fyra 3- till 6-veckors placebokontrollerade kliniska prövningar för behandling av schizofreni, vilka visade en 1 % (4/399) incidens för SEROQUEL 100 mg jämfört med 0,6 % (1) /156) incidens för placebo. I prövningar med akut (monoterapi) bipolär mani var andelen patienter som uppfyller kriterierna för takykardi 0,5 % (1/192) för SEROQUEL 200 mg jämfört med 0 % (0/178) incidens för placebo. I akut bipolär mani (tilläggsstudier) var andelen patienter som uppfyller samma kriterier 0,6 % (1/166) för SEROQUEL 100 mg jämfört med 0 % (0/171) incidens för placebo. I försök med bipolär depression hade inga patienter hjärtfrekvensökningar till >120 slag per minut. Användning av SEROQUEL 50 mg associerades med en genomsnittlig ökning av hjärtfrekvensen, bedömd med EKG, på 7 slag per minut jämfört med en genomsnittlig ökning på 1 slag per minut bland placebopatienter. Denna lätta tendens till takykardi hos vuxna kan vara relaterad till SEROQUELs potential att inducera ortostatiska förändringar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Barn och ungdomar
I den akuta (6-veckors) schizofrenistudien hos ungdomar inträffade ökningar i hjärtfrekvens (>110 slag/min) hos 5,2 % (3/73) av patienterna som fick SEROQUEL 400 mg och 8,5 % (5/74) av patienterna som fick SEROQUEL 800 mg jämfört med 0 % (0/75) av patienterna som fick placebo. Den genomsnittliga ökningen av hjärtfrekvensen var 3,8 slag per minut och 11,2 slag per minut för SEROQUEL 400 mg respektive 800 mg grupper, jämfört med en minskning med 3,3 slag per minut i placebogruppen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
I den akuta (3-veckors) bipolär manistudien hos barn och ungdomar inträffade ökningar i hjärtfrekvens (>110 slag/min) hos 1,1 % (1/89) av patienterna som fick SEROQUEL 400 mg och 4,7 % (4/85) av patienterna får SEROQUEL 600 mg jämfört med 0 % (0/98) av patienterna som får placebo. Den genomsnittliga ökningen av hjärtfrekvensen var 12,8 slag/minut och 13,4 slag/minut för SEROQUEL 400 mg respektive 600 mg grupper, jämfört med en minskning med 1,7 slag/min i placebogruppen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
en akut (8-veckors) SEROQUEL XR-studie på barn och ungdomar (10-17 år) med bipolär depression, där effekt inte fastställdes, ökade hjärtfrekvensen (>110 slag/min 10-12 år och 13-17 år) år) förekom hos 0 % av patienterna som fick SEROQUEL XR och 1,2 % av patienterna som fick placebo. Den genomsnittliga ökningen av hjärtfrekvensen var 3,4 slag/min för SEROQUEL XR, jämfört med 0,3 slag/min i placebogruppen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Erfarenhet efter marknadsföring
Följande biverkningar identifierades efter godkännande av SEROQUEL. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Biverkningar som rapporterats sedan marknadsintroduktionen och som var temporärt relaterade till behandling med quetiapin inkluderar anafylaktisk reaktion, kardiomyopati, läkemedelsreaktion med eosinofili och systemiska symtom (DRESS), hyponatremi, myokardit, nattlig enures, pankreatit, retrograd amnesi, rhabdomediuretisk hormonsyndrom vid inappropritisk hormon, rabdomediolys. (SIADH), Stevens-Johnsons syndrom (SJS), toxisk epidermal nekrolys (TEN), minskat antal trombocyter, allvarliga leverreaktioner (inklusive hepatit, levernekros och leversvikt), agranulocytos, intestinal obstruktion, ileus, kolonischemi, urinretention sömnapné och akut generaliserad exantematös pustulos (AGEP).
LÄKEMEDELSINTERAKTIONER
Effekt av andra droger på Quetiapin
Riskerna med att använda SEROQUEL i kombination med andra läkemedel har inte utvärderats i större utsträckning i systematiska studier. Med tanke på de primära CNS-effekterna av SEROQUEL bör försiktighet iakttas när det tas i kombination med andra centralt verkande läkemedel. SEROQUEL 300 mg potentierade de kognitiva och motoriska effekterna av alkohol i en klinisk prövning på försökspersoner med utvalda psykotiska störningar, och alkoholhaltiga drycker bör begränsas när du tar quetiapin.
Exponeringen för quetiapin ökas av prototypen CYP3A4-hämmare (t.ex. ketokonazol, itrakonazol, indinavir, ritonavir, nefazodon, etc.) och minskas av prototypen av CYP3A4-inducerare (t.ex. fenytoin, karbamazepin, rifampin, johannesört, etc.) . Dosjustering av quetiapin kommer att vara nödvändig om det administreras samtidigt med potenta CYP3A4-inducerare eller -hämmare.
CYP3A4-hämmare
Samtidig administrering av ketokonazol, en potent hämmare av cytokrom CYP3A4, resulterade i signifikant ökning av exponeringen för quetiapin. Dosen av SEROQUEL 200 mg bör minskas till en sjättedel av den ursprungliga dosen om den administreras samtidigt med en stark CYP3A4-hämmare [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
CYP3A4-inducerare
Samtidig administrering av quetiapin och fenytoin, en CYP3A4-inducerare, ökade det genomsnittliga orala clearance av quetiapin med 5 gånger. Ökade doser av SEROQUEL 50 mg upp till 5 gånger kan behövas för att bibehålla kontroll över symtom på schizofreni hos patienter som får quetiapin och fenytoin eller andra kända potenta CYP3A4-inducerare [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ]. När CYP3A4-induceraren avbryts, bör dosen av SEROQUEL 25 mg reduceras till den ursprungliga nivån inom 7-14 dagar [se DOSERING OCH ADMINISTRERING ].
De potentiella effekterna av flera samtidiga läkemedel på quetiapins farmakokinetik studerades [se KLINISK FARMAKOLOGI ].
Effekt av Quetiapin på andra droger
På grund av dess potential att inducera hypotoni kan SEROQUEL 50 mg förstärka effekten av vissa antihypertensiva medel.
SEROQUEL 25 mg kan motverka effekterna av levodopa och dopaminagonister.
Det finns inga kliniskt relevanta farmakokinetiska interaktioner mellan Seroquel och andra läkemedel baserade på CYP-vägen. Seroquel 50 mg och dess metaboliter är icke-hämmare av huvudmetaboliserande CYP (1A2, 2C9, 2C19, 2D6 och 3A4).
Narkotikamissbruk och beroende
Kontrollerad substans
SEROQUEL är inte en kontrollerad substans.
Missbruk
SEROQUEL har inte systematiskt studerats, på djur eller människor, för dess potential för missbruk, tolerans eller fysiskt beroende. Även om de kliniska prövningarna inte avslöjade någon tendens till något läkemedelssökande beteende, var dessa observationer inte systematiska och det är inte möjligt att på basis av denna begränsade erfarenhet förutsäga i vilken utsträckning ett CNS-aktivt läkemedel kommer att missbrukas, avledas, och/eller missbrukas när den väl har marknadsförts. Följaktligen bör patienter utvärderas noggrant med avseende på en historia av drogmissbruk, och sådana patienter bör observeras noggrant med avseende på tecken på felaktig användning eller missbruk av SEROQUEL, t.ex. toleransutveckling, dosökningar, drogsökande beteende.
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Ökad dödlighet hos äldre patienter med demensrelaterad psykos
Äldre patienter med demensrelaterad psykos som behandlas med antipsykotiska läkemedel löper en ökad risk att dö. Analys av 17 placebokontrollerade studier (modal varaktighet på 10 veckor), till stor del på patienter som tog atypiska antipsykotiska läkemedel, visade en risk för död hos läkemedelsbehandlade patienter på mellan 1,6 till 1,7 gånger risken för död hos placebobehandlade patienter. Under loppet av en typisk 10-veckors kontrollerad studie var dödsfrekvensen hos läkemedelsbehandlade patienter cirka 4,5 %, jämfört med en frekvens på cirka 2,6 % i placebogruppen. Även om dödsorsakerna varierade, verkade de flesta av dödsfallen vara antingen kardiovaskulära (t.ex. hjärtsvikt, plötslig död) eller infektionssjukdomar (t.ex. lunginflammation). Observationsstudier tyder på att behandling med konventionella antipsykotiska läkemedel, i likhet med atypiska antipsykotiska läkemedel, kan öka dödligheten. I vilken utsträckning fynden av ökad mortalitet i observationsstudier kan tillskrivas det antipsykotiska läkemedlet i motsats till vissa egenskaper hos patienterna är inte klart. SEROQUEL är inte godkänt för behandling av patienter med demensrelaterad psykos [se LÅDA VARNING ].
Självmordstankar och -beteenden hos ungdomar och unga vuxna
Patienter med egentlig depression (MDD), både vuxna och barn, kan uppleva förvärring av sin depression och/eller uppkomsten av självmordstankar och självmordsbeteende (suicidalitet) eller ovanliga beteendeförändringar, oavsett om de tar antidepressiva mediciner eller inte, och detta risken kan kvarstå tills betydande remission inträffar. Självmord är en känd risk för depression och vissa andra psykiatriska störningar, och dessa störningar i sig är de starkaste prediktorerna för självmord. Det har dock funnits en långvarig oro för att antidepressiva medel kan ha en roll i att framkalla förvärring av depression och uppkomsten av suicidalitet hos vissa patienter under de tidiga faserna av behandlingen. Sammanslagna analyser av kortvariga placebokontrollerade studier av antidepressiva läkemedel (SSRI och andra) visade att dessa läkemedel ökar risken för suicidtänkande och självmordsbeteende (suicidalitet) hos barn, ungdomar och unga vuxna (18-24 år) med svår depression. störning (MDD) och andra psykiatriska störningar. Korttidsstudier visade ingen ökning av risken för suicidalitet med antidepressiva läkemedel jämfört med placebo hos vuxna efter 24 års ålder; det var en minskning med antidepressiva läkemedel jämfört med placebo hos vuxna 65 år och äldre.
De sammanslagna analyserna av placebokontrollerade studier på barn och ungdomar med MDD, tvångssyndrom (OCD) eller andra psykiatriska störningar inkluderade totalt 24 korttidsstudier av 9 antidepressiva läkemedel på över 4400 patienter. De sammanslagna analyserna av placebokontrollerade studier på vuxna med MDD eller andra psykiatriska störningar inkluderade totalt 295 korttidsstudier (medianlängd på 2 månader) av 11 antidepressiva läkemedel på över 77 000 patienter. Det fanns avsevärd variation i risk för suicidalitet bland droger, men en tendens till en ökning av de yngre patienterna för nästan alla studerade droger. Det fanns skillnader i absolut risk för suicidalitet mellan de olika indikationerna, med den högsta förekomsten av MDD. Riskskillnaderna (läkemedel kontra placebo) var dock relativt stabila inom åldersskikt och över indikationer. Dessa riskskillnader (skillnad mellan läkemedel och placebo i antalet fall av suicidalitet per 1000 behandlade patienter) anges i tabell 2.
Inga självmord inträffade i någon av de pediatriska prövningarna. Det förekom självmord i vuxenstudierna, men antalet var inte tillräckligt för att dra någon slutsats om läkemedelseffekt på självmord.
Det är okänt om suicidalitetsrisken sträcker sig till långvarig användning, dvs. längre än flera månader. Det finns dock betydande bevis från placebokontrollerade underhållsstudier på vuxna med depression att användning av antidepressiva medel kan fördröja återkommande depression.
Alla patienter som behandlas med antidepressiva medel för någon indikation bör övervakas på lämpligt sätt och observeras noggrant med avseende på klinisk försämring, suicidalitet och ovanliga beteendeförändringar, särskilt under de första månaderna av en läkemedelsbehandlingskur, eller vid tidpunkter med dosförändringar, antingen ökningar eller minskar.
Följande symtom, ångest, agitation, panikattacker, sömnlöshet, irritabilitet, fientlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastlöshet), hypomani och mani, har rapporterats hos vuxna och pediatriska patienter som behandlas med antidepressiva medel även för egentlig depression vad gäller andra indikationer, både psykiatriska och icke-psykiatriska. Även om ett orsakssamband mellan uppkomsten av sådana symtom och antingen försämringen av depression och/eller uppkomsten av självmordsimpulser inte har fastställts, finns det oro för att sådana symtom kan representera föregångare till framväxande suicidalitet.
Man bör överväga att ändra den terapeutiska kuren, inklusive eventuellt avbrytande av medicineringen, hos patienter vars depression är ihållande värre, eller som upplever framväxande suicidalitet eller symtom som kan vara prekursorer till förvärrad depression eller suicidalitet, särskilt om dessa symtom är allvarliga, plötsliga. i början eller inte var en del av patientens symptom.
Familjer och vårdgivare till patienter som behandlas med antidepressiva medel för allvarlig depressiv sjukdom eller andra indikationer, både psykiatriska och icke-psykiatriska, bör uppmärksammas om behovet av att övervaka patienter för uppkomsten av agitation, irritabilitet, ovanliga beteendeförändringar och andra symtom. som beskrivs ovan, liksom uppkomsten av suicidalitet, och att rapportera sådana symtom omedelbart till vårdgivare. Sådan övervakning bör innefatta daglig observation av familjer och vårdgivare. Recept för SEROQUEL bör skrivas ut för den minsta mängden tabletter som överensstämmer med god patienthantering, för att minska risken för överdosering.
Screening av patienter för bipolär sjukdom
En allvarlig depressiv episod kan vara den första presentationen av bipolär sjukdom. Det anses allmänt (även om det inte har fastställts i kontrollerade studier) att behandling av en sådan episod med enbart ett antidepressivt läkemedel kan öka sannolikheten för utfällning av en blandad/manisk episod hos patienter med risk för bipolär sjukdom. Huruvida något av de ovan beskrivna symptomen representerar en sådan omvandling är okänt. Innan behandling med ett antidepressivt läkemedel, inklusive SEROQUEL, påbörjas, bör dock patienter med depressiva symtom screenas på lämpligt sätt för att fastställa om de löper risk för bipolär sjukdom; sådan screening bör inkludera en detaljerad psykiatrisk historia, inklusive en familjehistoria av självmord, bipolär sjukdom och depression.
Cerebrovaskulära biverkningar, inklusive stroke, hos äldre patienter med demensrelaterad psykos
I placebokontrollerade studier med risperidon, aripiprazol och olanzapin hos äldre personer med demens, fanns en högre incidens av cerebrovaskulära biverkningar (cerebrovaskulära olyckor och övergående ischemiska attacker) inklusive dödsfall jämfört med placebobehandlade patienter. SEROQUEL är inte godkänt för behandling av patienter med demensrelaterad psykos [se även LÅDA VARNING och Ökad dödlighet hos äldre patienter med demensrelaterad psykos ].
Malignt neuroleptikasyndrom (NMS)
Ett potentiellt dödligt symtomkomplex som ibland kallas malignt neuroleptikasyndrom (NMS) har rapporterats i samband med administrering av antipsykotiska läkemedel, inklusive SEROQUEL. Sällsynta fall av NMS har rapporterats med SEROQUEL. Kliniska manifestationer av NMS är hyperpyrexi, muskelstelhet, förändrad mental status och tecken på autonom instabilitet (oregelbunden puls eller blodtryck, takykardi, diafores och hjärtrytmrubbningar). Ytterligare tecken kan vara förhöjt kreatininfosfokinas, myoglobinuri (rabdomyolys) och akut njursvikt.
Den diagnostiska utvärderingen av patienter med detta syndrom är komplicerad. För att komma fram till en diagnos är det viktigt att utesluta fall där den kliniska presentationen inkluderar både allvarlig medicinsk sjukdom (t.ex. lunginflammation, systemisk infektion etc.) och obehandlade eller otillräckligt behandlade extrapyramidala tecken och symtom (EPS). Andra viktiga överväganden i differentialdiagnosen inkluderar central antikolinerg toxicitet, värmeslag, läkemedelsfeber och primär patologi i centrala nervsystemet (CNS).
Hanteringen av NMS bör innefatta: 1) omedelbart utsättande av antipsykotiska läkemedel och andra läkemedel som inte är nödvändiga för samtidig behandling; 2) intensiv symtomatisk behandling och medicinsk övervakning; och 3) behandling av eventuella samtidiga allvarliga medicinska problem för vilka specifika behandlingar finns tillgängliga. Det finns ingen allmän enighet om specifika farmakologiska behandlingsregimer för NMS.
Om en patient behöver antipsykotisk läkemedelsbehandling efter återhämtning från NMS, bör det potentiella återinförandet av läkemedelsbehandling noggrant övervägas. Patienten bör övervakas noggrant eftersom återfall av NMS har rapporterats.
Metaboliska förändringar
Atypiska antipsykotiska läkemedel har associerats med metabola förändringar som inkluderar hyperglykemi/diabetes mellitus, dyslipidemi och kroppsviktsökning. Medan alla läkemedel i klassen har visat sig ge vissa metaboliska förändringar, har varje läkemedel sin egen specifika riskprofil. Hos vissa patienter observerades en försämring av mer än en av de metaboliska parametrarna vikt, blodsocker och lipider i kliniska studier. Förändringar i dessa metabola profiler bör hanteras som kliniskt lämpligt.
Hyperglykemi och diabetes mellitus
Hyperglykemi, i vissa fall extrem och förknippad med ketoacidos eller hyperosmolär koma eller död, har rapporterats hos patienter som behandlats med atypiska antipsykotika, inklusive quetiapin. Bedömning av sambandet mellan atypisk antipsykotisk användning och glukosavvikelser kompliceras av möjligheten av en ökad bakgrundsrisk för diabetes mellitus hos patienter med schizofreni och den ökande incidensen av diabetes mellitus i den allmänna befolkningen. Med tanke på dessa konfounders är förhållandet mellan atypisk antipsykotisk användning och hyperglykemirelaterade biverkningar inte helt klarlagt. Epidemiologiska studier tyder dock på en ökad risk för hyperglykemirelaterade biverkningar hos patienter som behandlas med de atypiska antipsykotika. Exakta riskuppskattningar för hyperglykemirelaterade biverkningar hos patienter som behandlas med atypiska antipsykotika finns inte tillgängliga.
Patienter med en fastställd diagnos av diabetes mellitus som påbörjas med atypiska antipsykotika bör övervakas regelbundet för försämrad glukoskontroll. Patienter med riskfaktorer för diabetes mellitus (t.ex. fetma, familjehistoria av diabetes) som påbörjar behandling med atypiska antipsykotika bör genomgå fastande blodsockertest i början av behandlingen och regelbundet under behandlingen. Alla patienter som behandlas med atypiska antipsykotika bör övervakas för symtom på hyperglykemi inklusive polydipsi, polyuri, polyfagi och svaghet. Patienter som utvecklar symtom på hyperglykemi under behandling med atypiska antipsykotika bör genomgå fasteblodsockertest. I vissa fall har hyperglykemi försvunnit när det atypiska antipsykotiska medlet avbröts; vissa patienter krävde dock fortsatt antidiabetisk behandling trots att det misstänkta läkemedlet avbröts.
Vuxna
en 24-veckors studie (aktivkontrollerad, 115 patienter behandlade med SEROQUEL) utformad för att utvärdera glykemisk status med oral glukostoleranstestning av alla patienter, vid vecka 24 var incidensen av en glukosnivå efter glukosutmaning ≥200 mg/dL 1,7 % och förekomsten av en fastande blodsockernivå ≥126 mg/dL var 2,6 %. Den genomsnittliga förändringen i fasteglukos från baslinjen var 3,2 mg/dL och genomsnittlig förändring i 2-timmarsglukos från baslinjen var -1,8 mg/dL för quetiapin.
2 långtidsplacebokontrollerade, randomiserade kliniska utsättningsstudier för bipolär sjukdom I, medelexponering på 213 dagar för SEROQUEL (646 patienter) och 152 dagar för placebo (680 patienter), var den genomsnittliga förändringen i glukos från baslinjen +5,0 mg /dL för SEROQUEL 100 mg och –0,05 mg/dL för placebo. Den exponeringsjusterade frekvensen av eventuell ökad blodsockernivå (≥126 mg/dL) för patienter mer än 8 timmar efter en måltid (dock kan vissa patienter inte ha varit uteslutna från kaloriintag från vätska under fasta) var 18,0 per 100 patientår för SEROQUEL (10,7 % av patienterna; n=556) och 9,5 för placebo per 100 patientår (4,6 % av patienterna; n=581).
Barn och ungdomar
en placebokontrollerad SEROQUEL 25 mg monoterapistudie av tonårspatienter (13-17 år) med schizofreni (6 veckors varaktighet), den genomsnittliga förändringen i fasteglukosnivåer för SEROQUEL (n=138) jämfört med placebo (n=67) var – 0,75 mg/dL mot –1,70 mg/dL. I en placebokontrollerad SEROQUEL 300 mg monoterapistudie av barn och ungdomar (10-17 år) med bipolär mani (3 veckors varaktighet), den genomsnittliga förändringen av fasteglukosnivån för SEROQUEL (n=170) jämfört med placebo (n) =81) var 3,62 mg/dL mot –1,17 mg/dL. Ingen patient i någon av studien med en normal fasteglukosnivå vid utgångsläget (
en placebokontrollerad SEROQUEL XR-monoterapistudie (8 veckors varaktighet) av barn och ungdomar (1017 år) med bipolär depression, där effekt inte fastställdes, var den genomsnittliga förändringen i fasteglukosnivåer för SEROQUEL 300mg XR (n= 60) jämfört med placebo (n=62) var 1,8 mg/dL jämfört med 1,6 mg/dL. I den här studien fanns det inga patienter i gruppen med SEROQUEL XR eller placebobehandlade med en normal fasteglukosnivå vid baslinjen (126 mg/dL. Det fanns en patient i SEROQUEL 25 mg XR-gruppen med en gränsvärde fasteglukosnivå (>100 mg/dL och 126 mg/dL jämfört med noll patienter i placebogruppen.
Dyslipidemi
Vuxna
Tabell 4 visar procentandelen vuxna patienter med förändringar i totalt kolesterol, triglycerider, LDL-kolesterol och HDL-kolesterol från baslinjen efter indikation i kliniska prövningar med SEROQUEL.
Barn och ungdomar
Tabell 5 visar andelen barn och ungdomar med förändringar i totalkolesterol, triglycerider, LDL-kolesterol och HDL-kolesterol från baslinjen i kliniska prövningar med SEROQUEL.
I en placebokontrollerad SEROQUEL XR-monoterapistudie (8 veckors varaktighet) på barn och ungdomar (1017 år) med bipolär depression, där effekt inte fastställdes, var andelen barn och ungdomar med förändringar i totalkolesterol (≥200) mg/dL), triglycerider (≥150 mg/dL), LDL-kolesterol (≥ 130 mg/dL) och HDL-kolesterol (≤40 mg/dL) från baslinjen till kliniskt signifikanta nivåer var: totalkolesterol 8% (7) /83) för SEROQUEL 50 mg XR vs. 6 % (5/84) för placebo; triglycerider 28 % (22/80) för SEROQUEL 100 mg XR vs. 9 % (7/82) för placebo; LDL-kolesterol 2% (2/86) för SEROQUEL XR vs. 4% (3/85) för placebo och HDL-kolesterol 20% (13/65) för SEROQUEL XR vs. 15% (11/74) för placebo.
Viktökning
Viktökningar har observerats i kliniska prövningar. Patienter som får quetiapin bör få regelbunden kontroll av vikten.
Vuxna
I kliniska prövningar med SEROQUEL 50 mg har följande viktökningar rapporterats.
Barn och ungdomar
I två kliniska prövningar med SEROQUEL 25 mg, en vid bipolär mani och en vid schizofreni, är rapporterade viktökningar inkluderade i Tabell 7.
Den genomsnittliga förändringen i kroppsvikt i schizofrenistudien var 2,0 kg i SEROQUEL 25 mg-gruppen och -0,4 kg i placebogruppen och i bipolär manistudien var den 1,7 kg i SEROQUEL 200 mg-gruppen och 0,4 kg i placebogruppen.
en öppen studie som inkluderade patienter från ovanstående två pediatriska studier, fullföljde 63 % av patienterna (241/380) 26 veckors behandling med SEROQUEL. Efter 26 veckors behandling var den genomsnittliga ökningen av kroppsvikten 4,4 kg. Fyrtiofem procent av patienterna gick upp ≥7 % av sin kroppsvikt, inte justerat för normal tillväxt. För att justera för normal tillväxt under 26 veckor användes en ökning med minst 0,5 standardavvikelse från baslinjen i BMI som ett mått på en kliniskt signifikant förändring; 18,3 % av patienterna på SEROQUEL uppfyllde detta kriterium efter 26 veckors behandling.
I en klinisk prövning av SEROQUEL XR hos barn och ungdomar (10-17 år) med bipolär depression, där effekt inte fastställdes, var andelen patienter med viktökning ≥7 % av kroppsvikten vid något tillfälle 15 % ( 14/92) för SEROQUEL 25 mg XR vs. 10 % (10/100) för placebo. Den genomsnittliga förändringen i kroppsvikt var 1,4 kg i SEROQUEL 50 mg XR-gruppen jämfört med 0,6 kg i placebogruppen.
Vid behandling av pediatriska patienter med SEROQUEL 50 mg för alla indikationer, bör viktökning bedömas mot vad som förväntas för normal tillväxt.
Tardiv dyskinesi
Ett syndrom med potentiellt irreversibla, ofrivilliga, dyskinetiska rörelser kan utvecklas hos patienter som behandlas med antipsykotiska läkemedel, inklusive quetiapin. Även om prevalensen av syndromet verkar vara högst bland äldre, särskilt äldre kvinnor, är det omöjligt att förlita sig på prevalensuppskattningar för att förutsäga, vid inledningen av antipsykotisk behandling, vilka patienter som sannolikt kommer att utveckla syndromet. Huruvida antipsykotiska läkemedel skiljer sig i deras potential att orsaka tardiv dyskinesi är okänt.
Risken för att utveckla tardiv dyskinesi och sannolikheten att den blir irreversibel tros öka när behandlingstiden och den totala kumulativa dosen av antipsykotiska läkemedel som ges till patienten ökar. Syndromet kan dock utvecklas, även om det är mycket mindre vanligt, efter relativt korta behandlingsperioder vid låga doser eller kan till och med uppstå efter avslutad behandling.
Tardiv dyskinesi kan försvinna, delvis eller helt, om antipsykotisk behandling avbryts. Antipsykotisk behandling i sig kan dock undertrycka (eller delvis undertrycka) tecknen och symtomen på syndromet och kan därigenom eventuellt maskera den underliggande processen. Effekten som symtomatisk suppression har på det långvariga förloppet av syndromet är okänd.
Mot bakgrund av dessa överväganden bör SEROQUEL 50 mg förskrivas på ett sätt som med största sannolikhet minimerar förekomsten av tardiv dyskinesi. Kronisk antipsykotisk behandling bör i allmänhet reserveras för patienter som verkar lida av en kronisk sjukdom som (1) är känd för att svara på antipsykotiska läkemedel, och (2) för vilka alternativa, lika effektiva men potentiellt mindre skadliga behandlingar inte är tillgängliga eller lämpliga. . Hos patienter som behöver kronisk behandling bör den minsta dosen och den kortaste behandlingstiden som ger ett tillfredsställande kliniskt svar eftersträvas. Behovet av fortsatt behandling bör omprövas med jämna mellanrum.

Om tecken och symtom på tardiv dyskinesi uppträder hos en patient som behandlas med SEROQUEL 200 mg, bör utsättning av läkemedel övervägas. Vissa patienter kan dock behöva behandling med SEROQUEL 200 mg trots förekomsten av syndromet.
Hypotoni
Quetiapin kan inducera ortostatisk hypotoni associerad med yrsel, takykardi och, hos vissa patienter, synkope, särskilt under den initiala dostitreringsperioden, vilket troligen återspeglar dess α1-adrenerga antagonistegenskaper. Synkope rapporterades hos 1 % (28/3265) av patienterna som behandlades med SEROQUEL, jämfört med 0,2 % (2/954) på placebo och cirka 0,4 % (2/527) på aktiva kontrollläkemedel. Ortostatisk hypotoni, yrsel och synkope kan leda till fall.
SEROQUEL 25 mg ska användas med särskild försiktighet till patienter med känd kardiovaskulär sjukdom (historia av hjärtinfarkt eller ischemisk hjärtsjukdom, hjärtsvikt eller överledningsstörningar), cerebrovaskulär sjukdom eller tillstånd som skulle kunna predisponera patienter för hypotoni (dehydrering, hypovolemi och behandling med antihypertensiva läkemedel). Risken för ortostatisk hypotoni och synkope kan minimeras genom att begränsa initialdosen till 25 mg två gånger dagligen [se DOSERING OCH ADMINISTRERING ]. Om hypotoni inträffar under titrering till måldosen är en återgång till föregående dos i titreringsschemat lämplig.
Falls
Atypiska antipsykotiska läkemedel, inklusive SEROQUEL, kan orsaka somnolens, postural hypotoni, motorisk och sensorisk instabilitet, vilket kan leda till fall och följaktligen frakturer eller andra skador. För patienter med sjukdomar, tillstånd eller mediciner som kan förvärra dessa effekter, slutföra fallriskbedömningar vid inledande av antipsykotisk behandling och återkommande för patienter på långvarig antipsykotisk behandling.
Ökat blodtryck (barn och ungdomar)
placebokontrollerade studier på barn och ungdomar med schizofreni (6 veckors varaktighet) eller bipolär mani (3 veckors varaktighet) var incidensen av ökningar av systoliskt blodtryck (≥20 mmHg) 15,2 % (51/335) ) för SEROQUEL 50 mg och 5,5 % (9/163) för placebo; Incidensen av ökningar av diastoliskt blodtryck (≥10 mmHg) var 40,6 % (136/335) för SEROQUEL och 24,5 % (40/163) för placebo. I den 26-veckors öppna kliniska prövningen upplevde ett barn med en rapporterad historia av hypertoni en hypertensiv kris. Blodtrycket hos barn och ungdomar bör mätas i början av och regelbundet under behandlingen.
en placebokontrollerad SEROQUEL XR klinisk prövning (8 veckors varaktighet) på barn och ungdomar (10-17 år) med bipolär depression, där effekt inte fastställdes, förekom incidensen av ökningar av systoliskt blodtryck när som helst (≥ 20 mmHg) var 6,5 % (6/92) för SEROQUEL XR och 6,0 % (6/100) för placebo; Incidensen av ökningar av diastoliskt blodtryck (≥10 mmHg) var 46,7 % (43/92) för SEROQUEL 25 mg XR och 36,0 % (36/100) för placebo.
Leukopeni, Neutropeni och Agranulocytos
I kliniska prövningar och erfarenheter efter marknadsföring har händelser av leukopeni/neutropeni rapporterats tidsmässigt relaterade till atypiska antipsykotiska medel, inklusive SEROQUEL. Agranulocytos har rapporterats.
Agranulocytos (definierat som absolut neutrofilantal
Möjliga riskfaktorer för leukopeni/neutropeni inkluderar redan existerande lågt antal vita blodkroppar (WBC) och historia av läkemedelsinducerad leukopeni/neutropeni. Patienter med redan existerande lågt WBC eller en historia av läkemedelsinducerad leukopeni/neutropeni bör få sitt fullständiga blodvärde (CBC) övervakat ofta under de första månaderna av behandlingen och bör avbryta behandlingen med SEROQUEL 50 mg vid första tecken på en minskning av WBC i frånvaro av andra orsaksfaktorer.
Patienter med neutropeni bör övervakas noggrant med avseende på feber eller andra symtom eller tecken på infektion och behandlas omedelbart om sådana symtom eller tecken uppstår. Patienter med svår neutropeni (absolut neutrofilantal
Grå starr
Utvecklingen av grå starr observerades i samband med behandling med quetiapin i kroniska hundstudier [se Icke-klinisk toxikologi ]. Linsförändringar har också observerats hos vuxna, barn och ungdomar under långvarig behandling med SEROQUEL 100 mg, men ett orsakssamband till användning av SEROQUEL 200 mg har inte fastställts. Ändå kan möjligheten till linsformiga förändringar inte uteslutas för närvarande. Därför rekommenderas undersökning av linsen med metoder som är lämpliga för att upptäcka kataraktbildning, såsom spaltlampsundersökning eller andra lämpligt känsliga metoder, vid behandlingsstart eller kort därefter, och med 6-månadersintervaller under kronisk behandling.
QT-förlängning
kliniska prövningar var quetiapin inte associerat med en ihållande ökning av QT-intervall. QT-effekten utvärderades dock inte systematiskt i en grundlig QT-studie. Efter marknadsföring har det rapporterats fall av QT-förlängning hos patienter som överdoserat quetiapin [se ÖVERDOS ], hos patienter med samtidig sjukdom och hos patienter som tar läkemedel som är kända för att orsaka elektrolytobalans eller öka QT-intervallet [se LÄKEMEDELSINTERAKTIONER ].
Användning av quetiapin bör undvikas i kombination med andra läkemedel som är kända för att förlänga QTc inklusive klass 1A antiarytmika (t.ex. kinidin, prokainamid) eller klass III antiarytmika (t.ex. amiodaron, sotalol), antipsykotiska läkemedel (t.ex. ziprasidon, klorpromazin, tioridazin), antibiotika (t.ex. gatifloxacin, moxifloxacin) eller någon annan klass av mediciner som är kända för att förlänga QTc-intervallet (t.ex. pentamidin, levometadylacetat, metadon).
Quetiapin bör också undvikas under omständigheter som kan öka risken för uppkomsten av torsade de pointes och/eller plötslig död, inklusive (1) en historia av hjärtarytmier såsom bradykardi; (2) hypokalemi eller hypomagnesemi; (3) samtidig användning av andra läkemedel som förlänger QTc-intervallet; och (4) förekomst av medfödd förlängning av QT-intervallet.
Försiktighet bör också iakttas när quetiapin förskrivs till patienter med ökad risk för QT-förlängning (t.ex. kardiovaskulär sjukdom, familjehistoria med QT-förlängning, äldre, kronisk hjärtsvikt och hjärthypertrofi).
Anfall
Under kliniska prövningar inträffade anfall hos 0,5 % (20/3490) av patienterna som behandlades med SEROQUEL jämfört med 0,2 % (2/954) på placebo och 0,7 % (4/527) på aktiva kontrollläkemedel. Som med andra antipsykotika ska SEROQUEL 25 mg användas med försiktighet till patienter med anamnes på anfall eller med tillstånd som potentiellt sänker kramptröskeln, t.ex. Alzheimers demens. Tillstånd som sänker anfallströskeln kan vara vanligare i en befolkning på 65 år eller äldre.
Hypotyreos
Vuxna
Kliniska prövningar med quetiapin visade dosrelaterade minskningar av sköldkörtelhormonnivåer. Minskningen av totalt och fritt tyroxin (T4) med cirka 20 % vid den övre delen av det terapeutiska dosintervallet var maximal under de första sex veckorna av behandlingen och bibehölls utan anpassning eller progression under mer kronisk behandling. I nästan alla fall var ett upphörande av behandling med quetiapin förknippat med en reversering av effekterna på totalt och fritt T4, oberoende av behandlingens varaktighet. Mekanismen genom vilken quetiapin påverkar sköldkörtelaxeln är oklar. Om det finns en effekt på hypotalamus-hypofysaxeln, kanske enbart mätning av TSH inte exakt återspeglar patientens sköldkörtelstatus. Därför bör både TSH och fritt T4, förutom klinisk bedömning, mätas vid baslinjen och vid uppföljning.
tilläggsstudierna för mani, där SEROQUEL 50 mg lades till litium eller divalproex, hade 12 % (24/196) av patienterna behandlade med SEROQUEL 200 mg jämfört med 7 % (15/203) av placebobehandlade patienterna förhöjda TSH-nivåer. Av de SEROQUEL 300 mg-behandlade patienterna med förhöjda TSH-nivåer hade 3 samtidiga låga nivåer av fritt T4 (fritt T4
Cirka 0,7 % (26/3489) av SEROQUEL-patienterna upplevde TSH-ökningar i monoterapistudier. Vissa patienter med TSH-ökningar behövde ersättningsbehandling med sköldkörteln.
I alla quetiapinstudier var incidensen av förändringar i sköldkörtelhormoner och TSH 1: minskning av fritt T4 (5 mIU/L), 4,9 % (956/19412). Hos åtta patienter, där TBG mättes, var nivåerna av TBG oförändrade.
Tabell 8 visar förekomsten av dessa förändringar i korttids placebokontrollerade kliniska prövningar.
I korttidsstudier med placebokontrollerad monoterapi var incidensen av reciproka förändringar i T3 och TSH 0,0 % för både quetiapin (1/4800) och placebo (0/2190) och för T4 och TSH var förändringarna 0,1 % (7) /6154) för quetiapin mot 0,0 % (1/3007) för placebo.
Barn Och Ungdomar
I akuta placebokontrollerade studier på barn och ungdomar med schizofreni (6 veckors varaktighet) eller bipolär mani (3 veckors varaktighet), förekomsten av förändringar i sköldkörtelfunktionsvärdena när som helst för SEROQUEL 100 mg-behandlade patienter och placebobehandlade patienter för förhöjt TSH var 2,9% (8/280) respektive 0,7% (1/138), och för minskat total tyroxin var 2,8% (8/289) respektive 0% (0/145). Av de SEROQUEL-behandlade patienterna med förhöjda TSH-nivåer hade en samtidig låg nivå av fritt T4 vid slutet av behandlingen.
Hyperprolaktinemi
Vuxna
Under kliniska prövningar med quetiapin inträffade incidensen av förskjutningar i prolaktinnivåer till ett kliniskt signifikant värde hos 3,6 % (158/4416) av patienterna som behandlades med quetiapin jämfört med 2,6 % (51/1968) på placebo.
Barn Och Ungdomar
I akuta placebokontrollerade studier på barn och ungdomar med bipolär mani (3 veckors varaktighet) eller schizofreni (6 veckors varaktighet), förekomsten av förändringar i prolaktinnivåer till ett värde (>20 μg/L män; >26 μg /L kvinnor när som helst) var 13,4 % (18/134) för SEROQUEL jämfört med 4 % (3/75) för placebo hos män och 8,7 % (9/104) för SEROQUEL 25 mg jämfört med 0 % (0/39) för placebo hos kvinnor.
Liksom andra läkemedel som motverkar dopamin D2-receptorer, höjer SEROQUEL 300 mg prolaktinnivåerna hos vissa patienter och höjningen kan kvarstå under kronisk administrering. Hyperprolaktinemi, oavsett etiologi, kan undertrycka hypotalamisk GnRH, vilket resulterar i minskad hypofysgonadotropinutsöndring. Detta kan i sin tur hämma reproduktionsfunktionen genom att försämra gonadal steroidogenes hos både kvinnliga och manliga patienter. Galaktorré, amenorré, gynekomasti och impotens har rapporterats hos patienter som fått prolaktinhöjande substanser. Långvarig hyperprolaktinemi i samband med hypogonadism kan leda till minskad bentäthet hos både kvinnliga och manliga försökspersoner.
Vävnadsodlingsexperiment indikerar att ungefär en tredjedel av human bröstcancer är prolaktinberoende in vitro, en faktor av potentiell betydelse om förskrivning av dessa läkemedel övervägs hos en patient med tidigare upptäckt bröstcancer. Liksom är vanligt med föreningar som ökar frisättningen av prolaktin, observerades bröstkörtel- och pankreasöcellsneoplasi (adenokarcinom i bröst, hypofys och pankreas) i karcinogenicitetsstudier utförda på möss och råttor. Varken kliniska studier eller epidemiologiska studier genomförda hittills har visat ett samband mellan kronisk administrering av denna klass av läkemedel och tumörbildning hos människor, men de tillgängliga bevisen är för begränsade för att vara avgörande [se Icke-klinisk toxikologi ].
Potential för kognitiv och motorisk funktionsnedsättning
Somnolens var en vanligt rapporterad biverkning som rapporterades hos patienter som behandlades med SEROQUEL, särskilt under den 3-5 dagar långa initiala dostitreringen. I schizofrenistudier rapporterades somnolens hos 18 % (89/510) av patienterna som fick SEROQUEL 200 mg jämfört med 11 % (22/206) av placebopatienterna. I prövningar med akut bipolär mani med SEROQUEL 200 mg som monoterapi rapporterades somnolens hos 16 % (34/209) av patienterna som fick SEROQUEL 300 mg jämfört med 4 % av placebopatienterna. I prövningar med akut bipolär mani med SEROQUEL som tilläggsbehandling rapporterades somnolens hos 34 % (66/196) av patienterna på SEROQUEL jämfört med 9 % (19/203) av placebopatienterna. I prövningar av bipolär depression rapporterades somnolens hos 57 % (398/698) av patienterna som fick SEROQUEL 50 mg jämfört med 15 % (51/347) av placebopatienterna. Eftersom SEROQUEL 25 mg har potential att försämra omdöme, tänkande eller motorik, bör patienterna varnas för att utföra aktiviteter som kräver mental vakenhet, såsom att köra ett motorfordon (inklusive bilar) eller använda farliga maskiner tills de är rimligt säkra på att SEROQUEL-terapin gör det. inte påverka dem negativt. Somnolens kan leda till fall.
Reglering av kroppstemperatur
Även om det inte rapporterats med SEROQUEL 100mg, har störningar i kroppens förmåga att sänka kroppstemperaturen tillskrivits antipsykotiska medel. Lämplig vård rekommenderas vid förskrivning av SEROQUEL 300 mg till patienter som kommer att uppleva tillstånd som kan bidra till en höjning av kroppstemperaturen, t.ex. ansträngande träning, exponering för extrem värme, samtidig medicinering med antikolinerg aktivitet eller uttorkning.
Dysfagi
Esofageal dysmotilitet och aspiration har associerats med användning av antipsykotiska läkemedel. Aspirationspneumoni är en vanlig orsak till sjuklighet och dödlighet hos äldre patienter, särskilt de med avancerad Alzheimers demens. SEROQUEL 100 mg och andra antipsykotiska läkemedel ska användas med försiktighet hos patienter med risk för aspirationspneumoni.
Utsättningssyndrom
Akuta abstinenssymtom, såsom sömnlöshet, illamående och kräkningar har beskrivits efter abrupt utsättande av atypiska antipsykotiska läkemedel, inklusive SEROQUEL. I korttids placebokontrollerade, kliniska monoterapistudier med SEROQUEL 25 mg XR som inkluderade en utsättningsfas som utvärderade utsättningssymtom, var den sammanlagda förekomsten av patienter som upplevde ett eller flera utsättningssymtom efter abrupt utsättande 12,1 % (241/1993) för SEROQUEL XR. och 6,7 % (71/1065) för placebo. Incidensen av de individuella biverkningarna (dvs. sömnlöshet, illamående, huvudvärk, diarré, kräkningar, yrsel och irritabilitet) översteg inte 5,3 % i någon behandlingsgrupp och försvann vanligtvis efter 1 vecka efter avslutad behandling. Gradvis tillbakadragande rekommenderas. [ser Användning i specifika populationer ]
Antikolinerga (antimuskarina) effekter
Norquetiapin, en aktiv metabolit av quetiapin, har måttlig till stark affinitet för flera muskarinreceptorsubtyper. Detta bidrar till antikolinerga biverkningar när SEROQUEL 25 mg används i terapeutiska doser, tas samtidigt med andra antikolinerga läkemedel eller tas i överdos. SEROQUEL ska användas med försiktighet till patienter som får mediciner som har antikolinerga (antimuskarina) effekter [se ÖVERDOS och KLINISK FARMAKOLOGI ].
Förstoppning var en vanligt rapporterad biverkning hos patienter som behandlades med quetiapin och utgör en riskfaktor för tarmobstruktion. Tarmobstruktion har rapporterats med quetiapin, inklusive dödsfall hos patienter som fick flera samtidiga läkemedel som minskar tarmens motilitet.
SEROQUEL 300 mg ska användas med försiktighet till patienter med en aktuell diagnos eller tidigare anamnes på urinretention, kliniskt signifikant prostatahypertrofi, förstoppning eller ökat intraokulärt tryck.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen (läkemedelsguiden).
Patienter bör informeras om följande problem och uppmanas att varna sin förskrivare om dessa inträffar när de tar SEROQUEL.
Ökad dödlighet hos äldre patienter med demensrelaterad psykos Patienter och vårdgivare bör informeras om att äldre patienter med demensrelaterad psykos som behandlas med atypiska antipsykotiska läkemedel löper ökad risk att dö jämfört med placebo. Quetiapin är inte godkänt för äldre patienter med demensrelaterad psykos [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Självmordstankar och -beteenden
Patienter, deras familjer och deras vårdgivare bör uppmuntras att vara uppmärksamma på uppkomsten av ångest, agitation, panikattacker, sömnlöshet, irritabilitet, fientlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastlöshet), hypomani, mani, andra ovanliga beteendeförändringar , försämring av depression och självmordstankar, särskilt tidigt under antidepressiv behandling och när dosen justeras upp eller ner. Familjer och vårdgivare till patienter bör rådas att leta efter uppkomsten av sådana symtom på en daglig basis, eftersom förändringar kan vara abrupta. Sådana symtom bör rapporteras till patientens förskrivare eller hälso- och sjukvårdspersonal, särskilt om de är allvarliga, plötsliga debuterande eller inte var en del av patientens symtom. Symtom som dessa kan vara förknippade med en ökad risk för suicidtänkande och självmordsbeteende och indikerar behov av mycket noggrann övervakning och eventuellt förändringar i medicineringen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Malignt neuroleptikasyndrom (NMS)
Patienter bör rådas att rapportera till sin läkare alla tecken eller symtom som kan vara relaterade till NMS. Dessa kan inkludera muskelstelhet och hög feber [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hyperglykemi och diabetes mellitus
Patienter bör vara medvetna om symtomen på hyperglykemi (högt blodsocker) och diabetes mellitus. Patienter som diagnostiseras med diabetes, de med riskfaktorer för diabetes eller de som utvecklar dessa symtom under behandlingen bör få sitt blodsocker övervakat i början av och regelbundet under behandlingen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hyperlipidemi
Patienter bör informeras om att förhöjda totalkolesterol, LDL-kolesterol och triglycerider och minskningar av HDL-kolesterol kan förekomma. Patienter bör få sin lipidprofil övervakad i början av och regelbundet under behandlingen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Viktökning
Patienter bör informeras om att de kan uppleva viktökning. Patienter bör få sin vikt övervakad regelbundet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Ortostatisk hypotension
Patienter bör informeras om risken för ortostatisk hypotoni (symtom inkluderar yrsel eller yrsel när man står upp, vilket kan leda till fall), särskilt under perioden med initial dostitrering och även vid återupptagande av behandling eller dosökningar [ ser VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Ökat blodtryck hos barn och ungdomar
Barn och ungdomar bör få sitt blodtryck mätt i början av och med jämna mellanrum under behandlingen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Leukopeni/Neutropeni
Patienter med redan existerande lågt WBC eller en historia av läkemedelsinducerad leukopeni/neutropeni bör informeras om att de bör övervaka sin CBC medan de tar SEROQUEL. Patienter bör rådas att prata med sin läkare så snart som möjligt om de har feber, influensaliknande symtom, halsont eller någon annan infektion eftersom detta kan vara ett resultat av ett mycket lågt WBC, vilket kan kräva att Seroquel 100 mg stoppas och/eller behandling som ska ges [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Interferens med kognitiva och motoriska prestanda
Patienter bör informeras om risken för somnolens eller sedering (vilket kan leda till fall), särskilt under perioden med initial dostitrering. Patienter bör varnas för att utföra någon aktivitet som kräver mental vakenhet, såsom att köra ett motorfordon (inklusive bilar) eller använda maskiner, tills de är rimligt säkra på att quetiapinbehandling inte påverkar dem negativt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Värmeexponering och uttorkning
Patienter bör informeras om lämplig vård för att undvika överhettning och uttorkning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Samtidig medicinering
Som med andra mediciner bör patienter rådas att meddela sin läkare om de tar eller planerar att ta några receptbelagda eller receptfria läkemedel [se LÄKEMEDELSINTERAKTIONER ].
Graviditet
Rekommendera gravida kvinnor att meddela sin vårdgivare om de blir gravida eller avser att bli gravida under behandling med SEROQUEL. Informera patienter om att SEROQUEL kan orsaka extrapyramidala symtom och/eller abstinenssymtom (agitation, hypertoni, hypotoni, tremor, somnolens, andnöd och ätstörningar) hos en nyfödd. Informera patienter om att det finns ett graviditetsregister som övervakar graviditetsutfall hos kvinnor som exponerats för Seroquel 25 mg under graviditeten [se Användning i specifika populationer ].
Infertilitet
Informera kvinnor med reproduktionspotential att SEROQUEL kan försämra fertiliteten på grund av en ökning av serumprolaktinnivåerna. Effekterna på fertiliteten är reversibla [se Användning i specifika populationer ].
Behov av omfattande behandlingsprogram
SEROQUEL är indicerat som en integrerad del av ett totalt behandlingsprogram för ungdomar med schizofreni och pediatrisk bipolär sjukdom som kan innefatta andra åtgärder (psykologiska, pedagogiska och sociala). Effekten och säkerheten för SEROQUEL 100 mg har inte fastställts hos pediatriska patienter yngre än 13 år för schizofreni eller yngre än 10 år för bipolär mani. Lämplig utbildningsplacering är avgörande och psykosociala insatser är ofta till hjälp. Beslutet att förskriva atypiska antipsykotiska läkemedel kommer att bero på läkarens bedömning av kroniska och svårighetsgraden av patientens symtom [se INDIKATIONER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
Carcinogenicitetsstudier utfördes på C57BL-möss och Wistar-råttor. Quetiapin administrerades i kosten till möss i doser på 20, 75, 250 och 750 mg/kg och till råttor genom sondmatning i doser på 25, 75 och 250 mg/kg under två år. Dessa doser motsvarar 0,1, 0,5, 1,5 och 4,5 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta (möss) eller 0,3, 1 och 3 gånger MRHD baserat på mg/m2 kroppsyta. (råttor). Det fanns statistiskt signifikanta ökningar av follikulära adenom i sköldkörteln hos hanmöss vid doser 1,5 och 4,5 gånger MRHD baserat på mg/m2 kroppsyta och hos hanråttor vid en dos av 3 gånger MRHD på mg/m2 kroppsyta. Bröstkörteladenokarcinom ökade statistiskt signifikant hos honråttor vid alla testade doser (0,3, 1 och 3 gånger MRHD baserat på mg/m2 kroppsyta).
Sköldkörtelfollikulära celladenom kan ha orsakats av kronisk stimulering av sköldkörteln med sköldkörtelstimulerande hormon (TSH) till följd av ökad metabolism och clearance av tyroxin av gnagarlever. Förändringar i TSH, tyroxin och tyroxinclearance i överensstämmelse med denna mekanism observerades i subkroniska toxicitetsstudier på råtta och mus och i en 1-årig toxicitetsstudie på råtta; dock var resultaten av dessa studier inte definitiva. Relevansen av ökningen av follikelcelladenom i sköldkörteln för mänsklig risk, oavsett mekanism, är okänd.
Antipsykotiska läkemedel har visat sig kroniskt höja prolaktinnivåerna hos gnagare. Serummätningar i en 1-årig toxicitetsstudie visade att quetiapin ökade medianprolaktinnivåerna i serum med maximalt 32 och 13 gånger hos han- respektive honråttor. Ökning av bröstneoplasmer har hittats hos gnagare efter kronisk administrering av andra antipsykotiska läkemedel och anses vara prolaktinmedierad. Relevansen av denna ökade incidens av prolaktin-medierade bröstkörteltumörer hos råttor för mänsklig risk är okänd [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Mutagenes
Quetiapin var inte mutagent eller klastogent i standardgentoxicitetstester. Den mutagena potentialen för quetiapin testades i Ames bakteriell genmutationsanalysen in vitro och i in vitro analysen av däggdjursgenmutationer i kinesisk hamster ovarieceller. Den klastogena potentialen för quetiapin testades i in vitro kromosomavvikelseanalysen i odlade humana lymfocyter och i in vivo benmärgsmikronkärntest på råttor upp till 500 mg/kg, vilket är 6 gånger den maximala rekommenderade humandosen baserat på mg/m2 kroppsyta.
Nedsättning av fertilitet
Quetiapin minskade parning och fertilitet hos Sprague-Dawley-hanråttor vid orala doser på 50 och 150 mg/kg eller cirka 1 och 3 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. Läkemedelsrelaterade effekter inkluderade ökningar i intervall till parning och i antalet parningar som krävs för framgångsrik impregnering. Dessa effekter fortsatte att observeras vid 3 gånger MRHD även efter en tvåveckorsperiod utan behandling. Ingen effektdos för nedsatt parning och fertilitet hos hanråttor var 25 mg/kg, eller 0,3 gånger MRHD-dosen baserat på mg/m2 kroppsyta. Quetiapin påverkade parning och fertilitet negativt hos Sprague-Dawley-honråttor vid en oral dos cirka 1 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. Läkemedelsrelaterade effekter inkluderade minskningar av parningar och i parningar som resulterade i graviditet och en ökning av intervallet för att para sig. En ökning av oregelbundna brunstcykler observerades vid doser på 10 och 50 mg/kg, eller cirka 0,1 och 1 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. Ingen effektdos hos honråttor var 1 mg/kg, eller 0,01 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta.
Användning i specifika populationer
Graviditet
Registret för graviditetsexponering
Det finns ett graviditetsexponeringsregister som övervakar graviditetsresultat hos kvinnor som exponerats för atypiska antipsykotika, inklusive SEROQUEL 50 mg, under graviditeten. Sjukvårdsleverantörer uppmuntras att registrera patienter genom att kontakta National Pregnancy Registry for Atypical Antipsychotics på 1-866-961-2388 eller online på http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
Risksammanfattning
Nyfödda som exponerats för antipsykotiska läkemedel (inklusive SEROQUEL) under tredje trimestern löper risk för extrapyramidala och/eller abstinenssymtom efter förlossningen (se Kliniska överväganden ). Övergripande tillgängliga data från publicerade epidemiologiska studier av gravida kvinnor som exponerats för quetiapin har inte fastställt en läkemedelsrelaterad risk för allvarliga fosterskador, missfall eller ogynnsamma resultat hos modern eller foster (se Data ). Det finns risker för mamman i samband med obehandlad schizofreni, bipolär I eller egentlig depression, och med exponering för antipsykotika, inklusive SEROQUEL 200 mg, under graviditet (se Kliniska överväganden ).
I djurstudier inträffade embryo-fetal toxicitet inklusive fördröjningar i skelettets förbening vid cirka 1 och 2 gånger den maximala rekommenderade humandosen (MRHD) på 800 mg/dag hos både råttor och kaniner, och en ökad förekomst av karpal/tarsal flexur (mindre) mjukvävnadsavvikelse) hos kaninfoster vid ungefär 2 gånger MRHD. Dessutom minskade fostervikten hos båda arterna. Maternell toxicitet (observerad som minskad kroppsvikt och/eller död) inträffade vid 2 gånger MRHD hos råttor och ungefär 1-2 gånger MRHD hos kaniner.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för de angivna populationerna är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 till 4 % respektive 15 till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för mödrar och/eller foster
Det finns en risk för modern från obehandlad schizofreni eller bipolär sjukdom I, inklusive ökad risk för återfall, sjukhusvistelse och självmord. Schizofreni och bipolär störning I är förknippade med ökade negativa perinatala utfall, inklusive för tidig födsel. Det är inte känt om detta är ett direkt resultat av sjukdomen eller andra komorbida faktorer.
En prospektiv, longitudinell studie följde 201 gravida kvinnor med en historia av allvarlig depressiv sjukdom som var euthymic och tog antidepressiva i början av graviditeten. De kvinnor som avbröt antidepressiva läkemedel under graviditeten hade större risk att uppleva ett återfall av allvarlig depression än kvinnor som fortsatte med antidepressiva. Tänk på risken för obehandlad depression när du avbryter eller byter behandling med antidepressiv medicin under graviditet och efter förlossningen.
Fetala/neonatala biverkningar
Extrapyramidala och/eller abstinenssymtom, inklusive agitation, hypertoni, hypotoni, tremor, somnolens, andningsbesvär och ätstörningar har rapporterats hos nyfödda som exponerats för antipsykotiska läkemedel, inklusive SEROQUEL 50 mg, under graviditetens tredje trimester. Dessa symtom varierade i svårighetsgrad. Övervaka nyfödda för extrapyramidala och/eller abstinenssymtom och hantera symtomen på lämpligt sätt. Vissa nyfödda återhämtade sig inom timmar eller dagar utan specifik behandling; andra krävde långvarig sjukhusvistelse.
Data
Mänskliga data
Publicerade data från observationsstudier, födelseregister och fallrapporter om användning av atypiska antipsykotika under graviditeten visar inte ett tydligt samband med antipsykotika och större fosterskador. En retrospektiv kohortstudie från en Medicaid-databas med 9258 kvinnor som exponerats för antipsykotika under graviditeten indikerade inte en övergripande ökad risk för allvarliga fosterskador.
Djurdata
När dräktiga råttor och kaniner exponerades för quetiapin under organogenesen fanns ingen teratogen effekt på foster. Doserna var 25, 50 och 200 mg/kg hos råttor och 25, 50 och 100 mg/kg hos kaniner, vilket är ungefär 0,3, 0,6 och 2 gånger (råttor) och 0,6, 1 och 2 gånger (kaniner) MRHD för schizofreni på 800 mg/dag baserat på mg/m2 kroppsyta. Det fanns dock tecken på embryo-fetal toxicitet inklusive förseningar i skelettförbening vid cirka 1 och 2 gånger MRHD på 800 mg/dag hos både råttor och kaniner, och en ökad förekomst av karpal/tarsal böjning (mindre mjukvävnadsavvikelse) i kaninfoster vid ungefär 2 gånger MRHD. Dessutom minskade fostervikten hos båda arterna. Maternell toxicitet (observerad som minskad kroppsvikt och/eller död) inträffade vid 2 gånger MRHD hos råttor och ungefär 1-2 gånger MRHD (alla testade doser) hos kaniner.
en peri/postnatal reproduktionsstudie på råttor observerades inga läkemedelsrelaterade effekter när gravida mödrar behandlades med quetiapin i doser 0,01, 0,1 och 0,2 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. I en preliminär peri/postnatal studie förekom dock ökningar av foster- och valpdöd, och minskningar i medelvikt för kull vid 3 gånger MRHD.
Laktation
Risksammanfattning
Begränsade data från publicerad litteratur rapporterar förekomst av quetiapin i human bröstmjölk vid relativ spädbarnsdos på
Kvinnor Och Hanar Av Reproduktionspotential
Infertilitet
Kvinnor
Baserat på den farmakologiska effekten av quetiapin (D2-antagonism), kan behandling med SEROQUEL resultera i en ökning av serumprolaktinnivåerna, vilket kan leda till en reversibel minskning av fertiliteten hos kvinnor med reproduktionspotential [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Pediatrisk användning
I allmänhet liknade de biverkningar som observerades hos barn och ungdomar under de kliniska prövningarna de hos den vuxna befolkningen med få undantag. Ökning av systoliskt och diastoliskt blodtryck förekom hos barn och ungdomar och förekom inte hos vuxna. Ortostatisk hypotoni förekom oftare hos vuxna (4-7 %) jämfört med barn och ungdomar ( VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och NEGATIVA REAKTIONER ].
Schizofreni
Effekten och säkerheten av SEROQUEL 50 mg vid behandling av schizofreni hos ungdomar i åldrarna 13-17 år visades i en 6 veckor lång, dubbelblind, placebokontrollerad studie [se INDIKATIONER , DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER , och Kliniska studier ].
Säkerhet och effektivitet för SEROQUEL 300 mg hos pediatriska patienter yngre än 13 år med schizofreni har inte fastställts.
Underhåll
Säkerheten och effektiviteten av SEROQUEL vid underhållsbehandling av bipolär sjukdom har inte fastställts hos pediatriska patienter under 18 år. Säkerheten och effektiviteten av SEROQUEL vid underhållsbehandling av schizofreni har inte fastställts hos någon patientpopulation, inklusive pediatriska patienter.
Bipolär mani
Effekten och säkerheten av SEROQUEL vid behandling av mani hos barn och ungdomar i åldrarna 10-17 år med bipolär störning I visades i en 3-veckors, dubbelblind, placebokontrollerad, multicenterstudie [se INDIKATIONER , DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER , och Kliniska studier ]. Säkerhet och effektivitet för SEROQUEL hos pediatriska patienter yngre än 10 år med bipolär mani har inte fastställts.
Bipolär depression
Säkerhet och effektivitet för SEROQUEL 300 mg hos pediatriska patienter yngre än 18 år med bipolär depression har inte fastställts. En klinisk prövning med SEROQUEL XR utfördes på barn och ungdomar (10-17 år) med bipolär depression, effekt fastställdes inte.
Vissa skillnader i farmakokinetiken för quetiapin noterades mellan barn/ungdomar (10-17 år) och vuxna. Justerat för vikt var AUC och Cmax för quetiapin 41 % respektive 39 % lägre hos barn och ungdomar jämfört med vuxna. Farmakokinetiken för den aktiva metaboliten, norquetiapin, var likartad mellan barn/ungdomar och vuxna efter justering för vikt [se KLINISK FARMAKOLOGI ].
Geriatrisk användning
Av de cirka 3700 patienterna i kliniska studier med SEROQUEL 300 mg var 7 % (232) 65 år eller äldre. I allmänhet fanns det ingen indikation på någon annan tolerabilitet av SEROQUEL hos äldre jämfört med yngre vuxna. Icke desto mindre bör närvaron av faktorer som kan minska farmakokinetisk clearance, öka det farmakodynamiska svaret på SEROQUEL 200 mg eller orsaka sämre tolerans eller ortostas leda till övervägande av en lägre startdos, långsammare titrering och noggrann övervakning under den initiala doseringsperioden i äldre. Det genomsnittliga plasmaclearancen för SEROQUEL 25 mg minskade med 30 % till 50 % hos äldre patienter jämfört med yngre patienter [se KLINISK FARMAKOLOGI och DOSERING OCH ADMINISTRERING ].
Nedsatt njurfunktion
Klinisk erfarenhet av SEROQUEL hos patienter med nedsatt njurfunktion är begränsad [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Eftersom quetiapin i stor utsträckning metaboliseras av levern förväntas högre plasmanivåer hos patienter med nedsatt leverfunktion. I denna population rekommenderas en låg startdos på 25 mg/dag och dosen kan ökas i steg om 25 mg/dag-50 mg/dag [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
ÖVERDOS
Mänsklig erfarenhet
I kliniska prövningar har överlevnad rapporterats vid akuta överdoser på upp till 30 gram quetiapin. De flesta patienter som överdoserade upplevde inga biverkningar eller återhämtade sig helt från de rapporterade händelserna. Död har rapporterats i en klinisk prövning efter en överdos på 13,6 gram enbart quetiapin. I allmänhet var rapporterade tecken och symtom de som härrörde från en överdrift av läkemedlets kända farmakologiska effekter, dvs dåsighet, sedering, takykardi, hypotoni och antikolinerg toxicitet inklusive koma och delirium. Patienter med redan existerande allvarlig kardiovaskulär sjukdom kan löpa en ökad risk för effekterna av överdosering [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Ett fall, som involverade en uppskattad överdos på 9600 mg, var associerat med hypokalemi och första gradens hjärtblock. Efter marknadsintroduktion har det rapporterats fall av QT-förlängning med överdosering.
Hantering av överdosering
Upprätta och underhålla en luftväg och säkerställa tillräcklig syresättning och ventilation. Kardiovaskulär övervakning bör påbörjas omedelbart och bör innefatta kontinuerlig elektrokardiografisk övervakning för att upptäcka möjliga arytmier.
Lämpliga stödåtgärder är ledningens grundpelare. För den senaste informationen om hantering av Seroquel XR-överdosering, kontakta ett certifierat regionalt giftkontrollcenter (1-800-222-1222).
KONTRAINDIKATIONER
Överkänslighet mot quetiapin eller mot något hjälpämne i SEROQUEL XR-formuleringen. Anafylaktiska reaktioner har rapporterats hos patienter som behandlats med SEROQUEL XR.
KLINISK FARMAKOLOGI
Handlingsmekanism
Verkningsmekanismen för quetiapin vid de listade indikationerna är oklar. Emellertid kan effekten av quetiapin vid dessa indikationer medieras genom en kombination av dopamin typ 2 (D2) och serotonin typ 2 (5HT2) antagonism. Den aktiva metaboliten, N-desalkylquetiapin (norquetiapin), har liknande aktivitet vid D2, men större aktivitet vid 5HT2A-receptorer, än moderläkemedlet (quetiapin).
Farmakodynamik
Quetiapin och dess metabolit, norquetiapin, har affinitet för flera neurotransmittorreceptorer med norquetiapinbindning med högre affinitet än quetiapin i allmänhet. Ki-värdena för quetiapin och norquetiapin vid dopamin D1 är 428/99,8 nM, vid D2 626/489 nM, vid serotonin 5HT1A 1040/191 nM vid 5HT2A 38/2,9 nM, vid histamin H1,1 . 38,3 nM, och vid adrenerg alb 14,6/46,4 nM respektive, vid a2-receptorer 617/1290 nM. Quetiapin och norquetiapin saknar märkbar affinitet till bensodiazepinreceptorerna.
Effekt på QT-intervall
kliniska prövningar var quetiapin inte associerat med en ihållande ökning av QT-intervall. QT-effekten utvärderades dock inte systematiskt i en grundlig QT-studie. Efter marknadsföring har det rapporterats fall av QT-förlängning hos patienter som överdoserat quetiapin [se ÖVERDOS ], hos patienter med samtidig sjukdom och hos patienter som tar läkemedel som är kända för att orsaka elektrolytobalans eller öka QT-intervallet.
Farmakokinetik
Vuxna
Quetiapinfumarataktiviteten beror främst på moderläkemedlet. Flerdosfarmakokinetiken för quetiapin är dosproportionell inom det föreslagna kliniska dosintervallet, och quetiapinackumulering är förutsägbar vid upprepad dosering. Eliminering av quetiapin sker huvudsakligen via levermetabolism med en genomsnittlig terminal halveringstid på cirka 6 timmar inom det föreslagna kliniska dosintervallet. Steady-state-koncentrationer förväntas uppnås inom två dagar efter dosering. Quetiapin kommer sannolikt inte att störa metabolismen av läkemedel som metaboliseras av cytokrom P450-enzymer.
Barn Och Ungdomar
Vid steady state var modersubstansens farmakokinetik, hos barn och ungdomar (10-17 år), liknande den hos vuxna. Justerat för dos och vikt var dock AUC och Cmax för modersubstansen 41 % respektive 39 % lägre hos barn och ungdomar än hos vuxna. För den aktiva metaboliten, norquetiapin, var AUC och Cmax 45 % respektive 31 % högre hos barn och ungdomar än hos vuxna. Justerat för dos och vikt var farmakokinetiken för metaboliten norquetiapin likartad mellan barn och ungdomar och vuxna [se Användning i specifika populationer ].
Absorption
Quetiapinfumarat absorberas snabbt efter oral administrering och når maximala plasmakoncentrationer inom 1,5 timmar. Tablettformuleringen är 100 % biotillgänglig i förhållande till lösningen. Biotillgängligheten av quetiapin påverkas marginellt av administrering med föda, med Cmax- och AUC-värden ökade med 25 % respektive 15 %.
Distribution
Quetiapin distribueras brett i hela kroppen med en skenbar distributionsvolym på 10±4 l/kg. Det är 83 % bundet till plasmaproteiner vid terapeutiska koncentrationer. In vitro påverkade inte quetiapin bindningen av warfarin eller diazepam till humant serumalbumin. I sin tur förändrade varken warfarin eller diazepam bindningen av quetiapin.
Metabolism och eliminering
Efter en oral engångsdos av 14C-quetiapin utsöndrades mindre än 1 % av den administrerade dosen som oförändrat läkemedel, vilket tyder på att quetiapin metaboliseras i hög grad. Cirka 73 % och 20 % av dosen återfanns i urinen respektive avföringen.
Quetiapin metaboliseras i stor utsträckning av levern. De huvudsakliga metaboliska vägarna är sulfoxidation till sulfoxidmetaboliten och oxidation till modersyrametaboliten; båda metaboliterna är farmakologiskt inaktiva. In vitro-studier med humana levermikrosomer visade att cytokrom P450 3A4 isoenzymet är involverat i metabolismen av quetiapin till dess huvudsakliga men inaktiva sulfoxidmetabolit och i metabolismen av dess aktiva metabolit N-desalkylquetiapin.
Ålder
Oralt clearance av quetiapin minskade med 40 % hos äldre patienter (≥ 65 år, n=9) jämfört med unga patienter (n=12), och dosjustering kan vara nödvändig [se DOSERING OCH ADMINISTRERING ].
Kön
Det finns ingen könseffekt på farmakokinetiken för quetiapin.
Lopp
Det finns ingen raseffekt på quetiapins farmakokinetik.
Rökning
Rökning har ingen effekt på det orala clearance av quetiapin.
Njurinsufficiens
Patienter med gravt nedsatt njurfunktion (Clcr=10-30 mL/min/1,73 m2, n=8) hade ett 25 % lägre genomsnittligt oralt clearance än normala försökspersoner (Clcr > 80 mL/min/1,73 m2, n=8), men plasmakoncentrationer av quetiapin hos patienter med njurinsufficiens var inom koncentrationsintervallet hos normala försökspersoner som fick samma dos. Dosjustering behövs därför inte hos dessa patienter [se Användning i specifika populationer ].
Leverinsufficiens
Patienter med nedsatt leverfunktion (n=8) hade en 30 % lägre genomsnittlig oral clearance av quetiapin än normala försökspersoner. Hos två av de 8 patienterna med nedsatt leverfunktion var AUC och Cmax 3 gånger högre än de som normalt observerats hos friska försökspersoner. Eftersom quetiapin i stor utsträckning metaboliseras av levern förväntas högre plasmanivåer hos patienter med nedsatt leverfunktion och dosjustering kan behövas [se DOSERING OCH ADMINISTRERING och ANVÄND I SPECIFIKA POPULATIONER ].
Läkemedel-läkemedelsinteraktionsstudier
Bedömningarna in vivo av effekten av andra läkemedel på quetiapins farmakokinetik sammanfattas i tabell 17 [se DOSERING OCH ADMINISTRERING och LÄKEMEDELSINTERAKTIONER ].
In vitro-enzymhämningsdata tyder på att quetiapin och 9 av dess metaboliter skulle ha liten hämmande effekt på in vivo-metabolism medierad av cytokromerna CYP 1A2, 2C9, 2C19, 2D6 och 3A4. Quetiapin i doser på 750 mg/dag påverkade inte farmakokinetiken för enkeldos av antipyrin, litium eller lorazepam (tabell 18) [se LÄKEMEDELSINTERAKTIONER ].
Djurtoxikologi och/eller farmakologi
Quetiapin orsakade en dosrelaterad ökning av pigmentdeposition i sköldkörteln i toxicitetsstudier på råtta som varade 4 veckor eller längre och i en 2-årig karcinogenicitetsstudie på mus. Doserna var 10, 25, 50, 75, 150 och 250 mg/kg i råttstudier som är ungefär 0,1, 0,3, 0,6, 1, 2 och 3 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. , respektive. Doserna i musens karcinogenicitetsstudie var 20, 75, 250 och 750 mg/kg, vilket är cirka 0,1, 0,5, 1,5 och 4,5 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. Pigmentavlagring visade sig vara irreversibel hos råttor. Pigmentets identitet kunde inte fastställas, men visade sig vara samlokaliserad med quetiapin i follikulära epitelceller i sköldkörteln. De funktionella effekterna och relevansen av detta fynd för mänsklig risk är okända.
Hos hundar som fick quetiapin i 6 eller 12 månader, men inte under 1 månad, uppträdde fokal triangulär grå starr vid korsningen av bakre suturer i linsens yttre cortex i en dos på 100 mg/kg, eller 4 gånger MRHD på 800 mg/dag baserat på mg/m2 kroppsyta. Detta fynd kan bero på hämning av kolesterolbiosyntesen av quetiapin. Quetiapin orsakade en dosrelaterad minskning av plasmakolesterolnivåerna i studier med upprepade doser på hund och apa; dock fanns det inget samband mellan plasmakolesterol och förekomsten av grå starr hos enskilda hundar. Uppkomsten av delta-8kolestanol i plasma överensstämmer med hämning av ett sent stadium i kolesterolbiosyntesen hos dessa arter. En minskning med 25 % av kolesterolhalten i linsens yttre cortex observerades också i en speciell studie på quetiapinbehandlade honhundar. Läkemedelsrelaterad grå starr har inte setts hos någon annan art; i en 1-årig studie på apor detekterades dock ett tvärstrimmigt utseende av den främre linsens yta hos 2/7 honor vid en dos på 225 mg/kg eller 5,5 gånger MRHD på 800 mg/dag baserat på mg/m2 kropp ytarea.
Kliniska studier
Schizofreni
Korttidsförsök-Vuxna
Effekten av SEROQUEL 50 mg vid behandling av schizofreni fastställdes i 3 kontrollerade korttidsstudier (6 veckor) med slutenvårdspatienter med schizofreni som uppfyllde DSM III-R-kriterierna för schizofreni. Även om en engångsarm med fast dos av haloperidol inkluderades som en jämförande behandling i en av de tre studierna, var denna enkeldosgrupp för haloperidol otillräcklig för att ge en tillförlitlig och giltig jämförelse mellan SEROQUEL 200 mg och haloperidol.
Flera instrument användes för att bedöma psykiatriska tecken och symtom i dessa studier, bland dem Brief Psychiatric Rating Scale (BPRS), en multi-item inventering av allmän psykopatologi som traditionellt används för att utvärdera effekterna av läkemedelsbehandling vid schizofreni. BPRS-psykosklustret (konceptuell desorganisering, hallucinatoriskt beteende, misstänksamhet och ovanligt tankeinnehåll) anses vara en särskilt användbar undergrupp för att bedöma aktivt psykotiska schizofrena patienter. En andra traditionell bedömning, Clinical Global Impression (CGI), återspeglar intrycket av en skicklig observatör, fullt förtrogen med manifestationerna av schizofreni, om patientens övergripande kliniska tillstånd.
Resultaten av försöken följer:
De primära effektresultaten av dessa tre studier vid behandling av schizofreni hos vuxna presenteras i Tabell 19.
Undersökning av populationsundergrupper (ras, kön och ålder) avslöjade inte någon differentiell respons på grund av ras eller kön, med en uppenbarligen större effekt hos patienter under 40 år jämfört med de äldre än 40. Den kliniska betydelsen av detta fynd är okänt.
Ungdomar (13–17 år)
Effekten av SEROQUEL 300 mg vid behandling av schizofreni hos ungdomar (13-17 år) visades i en 6 veckor lång, dubbelblind, placebokontrollerad studie (studie 4). Patienter som uppfyllde DSM-IV diagnostiska kriterier för schizofreni randomiserades till en av tre behandlingsgrupper: SEROQUEL 400 mg/dag (n=73), SEROQUEL 800 mg/dag (n=74) eller placebo (n=75). Studiemedicinering påbörjades med 50 mg/dag och på dag 2 ökades till 100 mg/per dag (delat och givet två eller tre gånger per dag). Därefter titrerades dosen till måldosen 400 mg/dag eller 800 mg/dag med steg om 100 mg/dag, delades upp och gavs två eller tre gånger dagligen. Den primära effektvariabeln var den genomsnittliga förändringen från baslinjen i total positiv och negativ syndromskala (PANSS).
SEROQUEL vid 400 mg/dag och 800 mg/dag var överlägsen placebo vad gäller minskningen av PANSS totalpoäng. De primära effektresultaten av denna studie vid behandling av schizofreni hos ungdomar presenteras i Tabell 19.
Bipolär sjukdom
Bipolär I-störning, maniska eller blandade episoder
Vuxna
Effekten av SEROQUEL vid akut behandling av maniska episoder fastställdes i 3 placebokontrollerade studier på patienter som uppfyllde DSM-IV-kriterierna för bipolär störning I med maniska episoder. Dessa studier inkluderade patienter med eller utan psykotiska egenskaper och exkluderade patienter med snabb cykling och blandade episoder. Av dessa studier var 2 monoterapi (12 veckor) och 1 var tilläggsterapi (3 veckor) till antingen litium eller divalproex. Nyckelresultat i dessa studier var förändring från baslinjen i Young Mania Rating Scale (YMRS)-poäng vid 3 och 12 veckor för monoterapi och efter 3 veckor för tilläggsbehandling. Tilläggsbehandling definieras som samtidig initiering eller efterföljande administrering av SEROQUEL 100 mg med litium eller divalproex.
Det primära värderingsinstrumentet som användes för att bedöma maniska symtom i dessa försök var YMRS, en 11-punkts klinikerklassad skala som traditionellt används för att bedöma graden av manisk symptomatologi (irritabilitet, störande/aggressivt beteende, sömn, förhöjt humör, tal, ökad aktivitet, sexuellt intresse, språk-/tankestörning, tankeinnehåll, utseende och insikt) inom ett intervall från 0 (inga maniska drag) till 60 (maxpoäng).
Resultaten av försöken följer:
Monoterapi
Effekten av SEROQUEL vid akut behandling av bipolär mani fastställdes i 2 placebokontrollerade studier. I två 12-veckorsstudier (n=300, n=299) som jämförde SEROQUEL med placebo, var SEROQUEL 300 mg överlägsen placebo när det gäller minskningen av YMRS-totalpoängen vid vecka 3 och 12. Majoriteten av patienterna i dessa studier som tog SEROQUEL 100 mg doserades i ett intervall mellan 400 mg/dag och 800 mg per dag (studierna 1 och 2 i tabell 20).
Tilläggsterapi
denna 3-veckors placebokontrollerade studie randomiserades 170 patienter med bipolär mani (YMRS ≥20) till att få SEROQUEL 100 mg eller placebo som tilläggsbehandling till litium eller divalproex. Patienter kan ha fått en adekvat behandlingskur med litium eller divalproex före randomiseringen. SEROQUEL 50 mg var överlägset placebo när det lades till endast litium eller divalproex i minskningen av YMRS totalpoäng (studie 3 i tabell 20).
Majoriteten av patienterna i denna studie som tog SEROQUEL 25 mg doserades i ett intervall mellan 400 mg/dag och 800 mg per dag. I en liknande designad studie (n=200) var SEROQUEL associerad med en förbättring av YMRS-poäng men visade inte överlägsenhet gentemot placebo, möjligen på grund av en högre placeboeffekt.
De primära effektresultaten av dessa studier vid behandling av mani hos vuxna presenteras i Tabell 20.
Barn och ungdomar (10-17 år)
Effekten av SEROQUEL vid akut behandling av maniska episoder associerade med bipolär störning I hos barn och ungdomar (10-17 år) visades i en 3-veckors dubbelblind, placebokontrollerad multicenterstudie (studie 4 i Tabell 20). Patienter som uppfyllde DSM-IV diagnostiska kriterier för en manisk episod randomiserades till en av tre behandlingsgrupper: SEROQUEL 400 mg/dag (n=95), SEROQUEL 600 mg/dag (n=98) eller placebo (n=91) . Studiemedicinering påbörjades med 50 mg/dag och på dag 2 ökade till 100 mg/dag (delade doser gavs två eller tre gånger dagligen). Därefter titrerades dosen till en måldos på 400 mg/dag eller 600 mg/dag med steg om 100 mg/dag, givet i uppdelade doser två eller tre gånger dagligen. Den primära effektvariabeln var den genomsnittliga förändringen från baslinjen i total YMRS-poäng.
SEROQUEL 400 mg/dag och 600 mg/dag var överlägsna placebo i minskningen av YMRS totalpoäng (tabell 20).
Bipolär sjukdom, depressiva episoder
Vuxna
Effekten av SEROQUEL 25 mg för akut behandling av depressiva episoder associerade med bipolär sjukdom fastställdes i två identiskt utformade 8-veckors, randomiserade, dubbelblinda, placebokontrollerade studier (N=1045) (studierna 5 och 6 i tabell 21) . Dessa studier inkluderade patienter med antingen bipolär sjukdom I eller II och de med eller utan ett snabbt cykelförlopp. Patienter randomiserade till SEROQUEL 200 mg gavs fasta doser på antingen 300 mg eller 600 mg en gång dagligen.
Det primära värderingsinstrumentet som användes för att bedöma depressiva symtom i dessa studier var Montgomery-Asberg Depression Rating Scale (MADRS), en 10-punkts klinikbedömd skala med poäng från 0 till 60. Det primära effektmåttet i båda studierna var förändringen från baslinje i MADRS-poäng vid vecka 8. I båda studierna var SEROQUEL 50 mg överlägsen placebo vad gäller minskning av MADRS-poäng. Förbättring av symtom, mätt som förändring i MADRS-poäng jämfört med placebo, sågs i båda studierna på dag 8 (vecka 1) och framåt. I dessa studier sågs ingen ytterligare fördel med dosen 600 mg. För 300 mg-dosgruppen sågs statistiskt signifikanta förbättringar jämfört med placebo i övergripande livskvalitet och tillfredsställelse relaterad till olika funktionsområden, mätt med Q-LES-Q(SF).
De primära effektresultaten av dessa studier vid akut behandling av depressiva episoder associerade med bipolär sjukdom hos vuxna presenteras i Tabell 21.
Underhållsbehandling som komplement till litium eller divalproex
Effekten av SEROQUEL 100 mg vid underhållsbehandling av bipolär I-sjukdom fastställdes i 2 placebokontrollerade studier på patienter (n=1326) som uppfyllde DSM-IV-kriterierna för bipolär I-sjukdom (studierna 7 och 8 i figurerna 1 och 2). Studierna inkluderade patienter vars senaste episod var manisk, deprimerad eller blandad, med eller utan psykotiska egenskaper. I den öppna fasen krävdes det att patienterna var stabila på SEROQUEL plus litium eller divalproex i minst 12 veckor för att kunna randomiseras. I genomsnitt stabiliserades patienterna i 15 veckor. I randomiseringsfasen fortsatte patienterna behandlingen med litium eller divalproex och randomiserades till att få antingen SEROQUEL (administrerat två gånger dagligen totalt 400 mg/dag till 800 mg/dag) eller placebo. Cirka 50 % av patienterna hade avbrutit behandlingen med SEROQUEL-gruppen dag 280 och 50 % av placebogruppen hade avbrutit behandlingen med dubbelblind behandling dag 117. Det primära effektmåttet i dessa studier var tiden innan en humörhändelse återkommer (manisk, blandad eller deprimerad episod). En humörhändelse definierades som behandlingsstart eller sjukhusvistelse för en humörepisod; YMRS-poäng≥20 eller MADRS-poäng≥20 vid 2 på varandra följande bedömningar; eller studieavbrott på grund av en humörhändelse (Figur 1 och Figur 2).
båda studierna var SEROQUEL överlägsen placebo när det gällde att öka tiden till återkommande humörhändelser. Behandlingseffekten var närvarande för ökande tid till återfall av både maniska och deprimerade episoder. Effekten av SEROQUEL var oberoende av någon specifik undergrupp (tilldelad humörstabilisator, kön, ålder, ras, senaste bipolär episod eller snabb cykling).
Figur 1: Kaplan-Meier-kurvor över tid till återkommande humörhändelser (Studie 7)
Figur 2: Kaplan-Meier-kurvor över tid till återkommande humörhändelser (Studie 8)
PATIENTINFORMATION
SEROQUEL (SER-oh-kwell)(quetiapinfumarat) Tabletter
Läs denna medicineringsguide innan du börjar ta SEROQUEL och varje gång du får påfyllning. Det kan komma ny information. Denna information ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling.
Vilken är den viktigaste informationen jag borde veta om SEROQUEL?
SEROQUEL 100mg kan orsaka allvarliga biverkningar, inklusive:
- Prata med din eller din familjemedlems vårdgivare om:
- alla risker och fördelar med behandling med antidepressiva läkemedel.
- alla behandlingsval för depression eller annan allvarlig psykisk sjukdom
- Antidepressiva läkemedel kan öka självmordstankar eller -handlingar hos vissa barn, tonåringar och unga vuxna inom de första månaderna av behandlingen.
- Depression och andra allvarliga psykiska sjukdomar är de viktigaste orsakerna till självmordstankar och -handlingar. Vissa människor kan ha en särskilt hög risk att få självmordstankar eller -handlingar. Dessa inkluderar personer som har (eller har en familjehistoria av) depression, bipolär sjukdom (även kallad manodepressiv sjukdom) eller självmordstankar eller -handlingar.
- Hur kan jag se efter och försöka förebygga självmordstankar och -handlingar hos mig själv eller en familjemedlem?
- Var uppmärksam på alla förändringar, särskilt plötsliga förändringar, i humör, beteenden, tankar eller känslor. Detta är mycket viktigt när ett antidepressivt läkemedel påbörjas eller när dosen ändras.
- Ring genast vårdgivaren för att rapportera nya eller plötsliga förändringar i humör, beteende, tankar eller känslor.
- Håll alla uppföljningsbesök hos vårdgivaren enligt schemat. Ring vårdgivaren mellan besöken vid behov, särskilt om du är orolig för symtom.
Ring en vårdgivare omedelbart om du eller din familjemedlem har något av följande symtom, särskilt om de är nya, värre eller oroar dig:
- tankar om självmord eller att dö
- försök att begå självmord
- ny eller värre depression
- ny eller värre ångest
- känner sig väldigt upprörd eller rastlös
- panikattacker
- sömnsvårigheter (sömnlöshet)
- ny eller värre irritabilitet
- agerar aggressivt, är arg eller våldsam
- agerar på farliga impulser
- en extrem ökning av aktivitet och prat (mani)
- andra ovanliga förändringar i beteende eller humör
Vad mer behöver jag veta om antidepressiva läkemedel?
- Sluta aldrig med ett antidepressivt läkemedel utan att först prata med din vårdgivare. Att plötsligt stoppa ett antidepressivt läkemedel kan orsaka andra symtom.
- Antidepressiva medel är läkemedel som används för att behandla depression och andra sjukdomar. Det är viktigt att diskutera alla risker med att behandla depression, och även riskerna med att inte behandla den. Patienter och deras familjer eller andra vårdgivare bör diskutera alla behandlingsval med vårdgivaren, inte bara användningen av antidepressiva medel.
- Antidepressiva läkemedel har andra biverkningar. Prata med vårdgivaren om biverkningarna av det läkemedel som ordinerats till dig eller din familjemedlem.
- Antidepressiva läkemedel kan interagera med andra läkemedel. Känn till alla läkemedel som du eller din familjemedlem tar. Håll en lista över alla läkemedel för att visa vårdgivaren. Börja inte med nya läkemedel utan att först kontrollera med din vårdgivare.
- Inte alla antidepressiva läkemedel som skrivs ut för barn är FDA-godkända för användning till barn. Prata med ditt barns vårdgivare för mer information.
Vad är SEROQUEL 300mg?
SEROQUEL 100mg är ett receptbelagt läkemedel som används för att behandla:
- schizofreni hos personer 13 år eller äldre
- bipolär sjukdom hos vuxna, inklusive:
- depressiva episoder i samband med bipolär sjukdom
- maniska episoder associerade med bipolär sjukdom I enbart eller med litium eller divalproex
- långtidsbehandling av bipolär sjukdom I med litium eller divalproex
- maniska episoder associerade med bipolär störning I hos barn i åldrarna 10-17 år
Det är inte känt om SEROQUEL 100 mg är säkert och effektivt för barn under 10 år.
Vad ska jag berätta för min vårdgivare innan jag tar SEROQUEL 100mg?
Innan du tar SEROQUEL 200 mg, berätta för din läkare om du har eller har haft:
- diabetes eller högt blodsocker hos dig eller din familj. Din vårdgivare bör kontrollera ditt blodsocker innan du börjar med SEROQUEL 300mg och även under behandlingen
- höga nivåer av totalt kolesterol, triglycerider eller LDL-kolesterol, eller låga nivåer av HDL-kolesterol
- lågt eller högt blodtryck
- lågt antal vita blodkroppar
- grå starr
- anfall
- onormala sköldkörtelprov
- höga prolaktinnivåer
- hjärtproblem
- leverproblem
- något annat medicinskt tillstånd
- graviditet eller planerar att bli gravid. Det är inte känt om SEROQUEL 100 mg kommer att skada ditt ofödda barn.
- Om du blir gravid medan du får SEROQUEL, prata med din vårdgivare om att registrera dig hos National Pregnancy Registry for Atypical Antipsychotics. Du kan registrera dig genom att ringa 1-866-961-2388 eller gå till http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
- ammar eller planerar att amma. SEROQUEL kan passera över i din bröstmjölk. Prata med din vårdgivare om det bästa sättet att mata ditt barn om du får SEROQUEL.
- om du har eller har haft ett tillstånd där du inte kan tömma urinblåsan helt (urinretention), har en förstorad prostata eller förstoppning eller ökat tryck i ögonen.
Berätta för vårdgivaren om alla läkemedel du tar eller nyligen har tagit inklusive receptbelagda läkemedel, receptfria läkemedel, växtbaserade kosttillskott och vitaminer.
SEROQUEL 300mg och andra läkemedel kan påverka varandra och orsaka allvarliga biverkningar. SEROQUEL 200 mg kan påverka hur andra läkemedel fungerar, och andra läkemedel kan påverka hur SEROQUEL 200 mg fungerar.
Berätta för din vårdgivare om du har en urinläkemedelsscreening eftersom SEROQUEL kan påverka dina testresultat. Berätta för dem som gör testet att du tar SEROQUEL.
Hur ska jag ta Seroquel?
- Ta SEROQUEL exakt som din läkare säger åt dig att ta det. Ändra inte dosen själv.
- Ta SEROQUEL 25 mg genom munnen, med eller utan mat.
- Om du känner att du behöver sluta med SEROQUEL 25 mg, prata med din läkare först. Om du plötsligt slutar att ta SEROQUEL kan du få biverkningar som sömnsvårigheter eller problem med att sova (sömnlöshet), illamående och kräkningar.
- Om du missar en dos av SEROQUEL 25 mg, ta den så snart du kommer ihåg det. Om du är nära din nästa dos, hoppa över den missade dosen. Ta bara nästa dos vid din vanliga tid. Ta inte 2 doser samtidigt om inte din läkare säger åt dig att göra det. Om du är osäker på din dosering, ring din vårdgivare.
Vad ska jag undvika när jag tar SEROQUEL 100mg?
- Kör inte bil, använd inte maskiner eller gör andra farliga aktiviteter förrän du vet hur SEROQUEL påverkar dig. SEROQUEL kan göra dig dåsig.
- Undvik att bli överhettad eller uttorkad.
- Överträna inte.
- Vid varmt väder, håll dig inne på en sval plats om möjligt.
- Håll dig borta från solen. Bär inte för mycket eller tunga kläder.
- Drick mycket vatten.
- Drick inte alkohol medan du tar Seroquel. Det kan förvärra vissa biverkningar av SEROQUEL.
Vilka är möjliga biverkningar av SEROQUEL 300mg?
SEROQUEL 200mg kan orsaka allvarliga biverkningar, inklusive:
- Se "Vad är den viktigaste informationen jag borde veta om SEROQUEL 200mg?"
- stroke som kan leda till döden kan inträffa hos äldre personer med demens som tar mediciner som SEROQUEL
- malignt neuroleptikasyndrom (NMS). NMS är ett sällsynt men mycket allvarligt tillstånd som kan inträffa hos personer som tar antipsykotiska läkemedel, inklusive SEROQUEL. NMS kan orsaka dödsfall och måste behandlas på sjukhus. Ring din vårdgivare omedelbart om du blir allvarligt sjuk och har några eller alla av dessa symtom:
- hög feber
- överdriven svettning
- stela muskler
- förvirring
- förändringar i din andning, hjärtslag och blodtryck
- faller kan hända hos vissa personer som tar Seroquel. Dessa fall kan orsaka allvarliga skador.
- högt blodsocker (hyperglykemi). Högt blodsocker kan inträffa om du redan har diabetes eller om du aldrig har haft diabetes. Högt blodsocker kan leda till:
- ansamling av syra i blodet på grund av ketoner (ketoacidos)
- koma
- död
Blodsockerhöjningar kan inträffa hos vissa personer som tar SEROQUEL. Extremt högt blodsocker kan leda till koma eller dödsfall. Om du har diabetes eller riskfaktorer för diabetes (som övervikt eller diabetes i familjen) bör din läkare kontrollera ditt blodsocker innan du börjar med Seroquel 50 mg och under behandlingen. Ring din vårdgivare om du har något av dessa symtom på högt blodsocker (hyperglykemi) när du tar SEROQUEL:
- känner mig väldigt törstig
- behöver kissa mer än vanligt
- känner mig väldigt hungrig
- känna sig svag eller trött
- får ont i magen
- känna dig förvirrad, eller så luktar din andedräkt fruktig
- höga fettnivåer i ditt blod (ökat kolesterol och triglycerider). Höga fettnivåer kan förekomma hos personer som behandlas med SEROQUEL. Du kanske inte har några symtom, så din läkare kan besluta att kontrollera ditt kolesterol och triglycerider under din behandling med SEROQUEL.
- viktökning (viktökning). Viktuppgång är vanligt hos personer som tar SEROQUEL så du och din läkare bör kontrollera din vikt regelbundet. Prata med din vårdgivare om sätt att kontrollera viktökning, som att äta en hälsosam, balanserad kost och träna.
- rörelser som du inte kan kontrollera i ansiktet, tungan eller andra kroppsdelar (tardiv dyskinesi). Dessa kan vara tecken på ett allvarligt tillstånd. Tardiv dyskinesi kanske inte försvinner, även om du slutar ta SEROQUEL. Tardiv dyskinesi kan också börja efter att du slutat ta Seroquel.
- sänkt blodtryck (ortostatisk hypotoni), inklusive yrsel eller svimning orsakad av en plötslig förändring i hjärtfrekvens och blodtryck när man stiger för snabbt från sittande eller liggande läge.
- förhöjt blodtryck hos barn och tonåringar. Din vårdgivare bör kontrollera blodtrycket hos barn och ungdomar innan du börjar med SEROQUEL och under behandlingen.
- lågt antal vita blodkroppar. Berätta för din vårdgivare så snart som möjligt om du har feber, influensaliknande symtom eller någon annan infektion, eftersom detta kan vara ett resultat av ett mycket lågt antal vita blodkroppar. Din vårdgivare kan kontrollera din nivå av vita blodkroppar för att avgöra om ytterligare behandling eller andra åtgärder behövs.
- grå starr
- anfall
- onormala sköldkörtelprov. Din vårdgivare kan göra blodprover för att kontrollera din sköldkörtelhormonnivå.
- ökningar av prolaktinnivåer
- sömnighet, dåsighet, trötthet, svårt att tänka och göra normala aktiviteter
- ökad kroppstemperatur
- svårt att svälja
- sömnsvårigheter eller problem med att sova (sömnlöshet), illamående eller kräkningar om du plötsligt slutar ta SEROQUEL. Dessa symtom blir vanligtvis bättre 1 vecka efter att du börjar ha dem.
De vanligaste biverkningarna av SEROQUEL 50 mg inkluderar:
Hos vuxna:
- dåsighet
- plötsligt blodtrycksfall när man står upp
- viktökning
- tröghet
- onormala leverprover
- orolig mage
- torr mun
- yrsel
- svaghet
- buksmärtor
- förstoppning
- öm hals
Hos barn och ungdomar:
- dåsighet
- yrsel
- Trötthet
- illamående
- torr mun
- viktökning
- ökad aptit
- kräkningar
- snabba hjärtslag
Dessa är inte alla möjliga biverkningar av SEROQUEL. För mer information, fråga din vårdgivare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara SEROQUEL 100mg?
- Förvara SEROQUEL 100 mg i rumstemperatur, mellan 68°F till 77°F (20°C till 25°C).
- Förvara SEROQUEL och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av SEROQUEL
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte Seroquel för ett tillstånd som det inte har ordinerats för. Ge inte SEROQUEL till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Den här medicineringsguiden sammanfattar den viktigaste informationen om SEROQUEL. Om du vill ha mer information, prata med din vårdgivare. Du kan fråga din apotekspersonal eller vårdgivare om information om SEROQUEL 100mg som är skriven för vårdpersonal.
För mer information, gå till www.SEROQUEL.com , eller ring 1-800-236-9933.
Vilka är ingredienserna i SEROQUEL 200mg?
Aktiv beståndsdel: quetiapinfumarat
Inaktiva Ingredienser: povidon, dibasiskt dikalciumfosfatdihydrat, mikrokristallin cellulosa, natriumstärkelseglykolat, laktosmonohydrat, magnesiumstearat, hypromellos, polyetylenglykol och titandioxid. 25 mg tabletterna innehåller röd och gul järnoxid. Tabletterna 100 mg och 400 mg innehåller endast gul järnoxid.
Denna medicineringsguide har godkänts av US Food and Drug Administration.
