Lexapro 10mg, 20mg, 5mg Escitalopram Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Lexapro och hur används det?
Lexapro är ett receptbelagt läkemedel som används för att behandla symtom på egentlig depression och generaliserat ångestsyndrom. Lexapro kan användas ensamt eller tillsammans med andra läkemedel.
- Lexapro tillhör en klass av läkemedel som kallas antidepressiva, SSRI.
- Det är inte känt om Lexapro 10 mg är säkert och effektivt för barn yngre än 12 år.
Vilka är de möjliga biverkningarna av Lexapro?
Lexapro kan orsaka allvarliga biverkningar inklusive:
- Buksmärtor,
- onormal blödning,
- Onormala drömmar,
- Allergi,
- suddig syn,
- tunnelseende,
- bröstsmärta,
- minskad koncentration,
- hemostas,
- ögonsmärta eller svullnad,
- ser glorier runt ljus,
- racing tankar,
- ovanligt risktagande beteende,
- känslor av extrem lycka eller sorg,
- huvudvärk,
- halsbränna,
- värmevallningar,
- förvirring,
- sluddrigt tal,
- allvarlig svaghet,
- kräkningar,
- förlust av koordination,
- känner sig ostadig,
- mycket stela (styva) muskler,
- hög feber,
- svettas,
- förvirring,
- snabba eller ojämna hjärtslag,
- skakningar och
- yrsel
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Lexapro inkluderar:
- yrsel,
- dåsighet,
- svaghet,
- svettas,
- känner sig skakig eller orolig,
- sömnproblem (sömnlöshet),
- torr mun,
- aptitlöshet,
- illamående,
- förstoppning,
- gapande,
- viktförändringar,
- minskad sexlust,
- impotens och
- svårt att få orgasm
VARNING
SUICIDALITET OCH ANTIDEPRESSIVA DROGER
Antidepressiva läkemedel ökade risken jämfört med placebo för suicidtänkande och suicidalitet (suicidalitet) hos barn, ungdomar och unga vuxna i korttidsstudier av egentlig depression (MDD) och andra psykiatriska störningar. Alla som överväger att använda Lexapro eller något annat antidepressivt medel hos ett barn, tonåring eller ung vuxen måste balansera denna risk med det kliniska behovet. Korttidsstudier visade ingen ökning av risken för suicidalitet med antidepressiva läkemedel jämfört med placebo hos vuxna efter 24 års ålder; det fanns en minskning av risken med antidepressiva läkemedel jämfört med placebo hos vuxna 65 år och äldre. Depression och vissa andra psykiatriska störningar är i sig förknippade med ökad risk för självmord. Patienter i alla åldrar som påbörjas med antidepressiv behandling bör övervakas på lämpligt sätt och observeras noggrant med avseende på klinisk försämring, suicidalitet eller ovanliga beteendeförändringar. Familjer och vårdgivare bör informeras om behovet av noggrann observation och kommunikation med förskrivaren. Lexapro 5mg är inte godkänt för användning hos pediatriska patienter under 12 år. [Ser VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER Klinisk försämring och självmordsrisk, PATIENTINFORMATION , och Användning i specifika populationer : Pediatrisk användning].
BESKRIVNING
Lexapro® (escitalopramoxalat) är en oralt administrerad selektiv serotoninåterupptagshämmare (SSRI). Escitalopram är den rena senantiomeren (enkel isomer) av det racemiska bicykliska ftalanderivatet citalopram. Escitalopramoxalat betecknas S-(+)-1-[3(dimetylamino)propyl]-1-(p-fluorfenyl)-5-ftalankarbonitriloxalat med följande strukturformel:
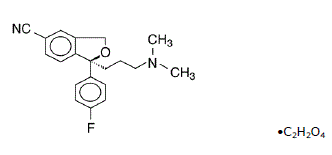
Molekylformeln är C20H21FN2O • C2H2O4 och molekylvikten är 414,40.
Escitalopramoxalat förekommer som ett fint, vitt till svagt gult pulver och är fritt lösligt i metanol och dimetylsulfoxid (DMSO), lösligt i isoton saltlösning, svårlösligt i vatten och etanol, lätt lösligt i etylacetat och olösligt i heptan.
Lexapro (escitalopramoxalat) finns som tabletter eller som oral lösning.
Lexapro tabletter är filmdragerade, runda tabletter som innehåller escitalopramoxalat i styrkor motsvarande 5 mg, 10 mg och 20 mg escitaloprambas. Tabletterna på 10 och 20 mg är skårade. Tabletterna innehåller även följande inaktiva ingredienser: talk, kroskarmellosnatrium, mikrokristallin cellulosa/kolloidal kiseldioxid och magnesiumstearat. Filmbeläggningen innehåller hypromellos, titandioxid och polyetylenglykol.
Lexapro 5 mg oral lösning innehåller escitalopramoxalat motsvarande 1 mg/ml escitaloprambas. Den innehåller även följande inaktiva ingredienser: sorbitol, renat vatten, citronsyra, natriumcitrat, äppelsyra, glycerin, propylenglykol, metylparaben, propylparaben och naturlig pepparmintsmak.
INDIKATIONER
Major depressiv sjukdom
Lexapro (escitalopram) är indicerat för akut och underhållsbehandling av egentlig depression hos vuxna och ungdomar i åldern 12 till 17 år [se Kliniska studier ].
En stor depressiv episod (DSM-IV) innebär ett framträdande och relativt ihållande (nästan varje dag i minst 2 veckor) deprimerat eller dysforiskt humör som vanligtvis stör den dagliga funktionen, och inkluderar minst fem av följande nio symtom: nedstämdhet, förlust av intresse för vanliga aktiviteter, betydande förändring i vikt och/eller aptit, sömnlöshet eller hypersomni, psykomotorisk agitation eller retardation, ökad trötthet, skuldkänslor eller värdelöshet, långsammare tänkande eller nedsatt koncentrationsförmåga, ett självmordsförsök eller självmordstankar.
Generaliserat ångestsyndrom
Lexapro 20mg är indicerat för akut behandling av generaliserat ångestsyndrom (GAD) hos vuxna [se Kliniska studier ].
Generaliserat ångestsyndrom (DSM-IV) kännetecknas av överdriven ångest och oro (orolig förväntan) som är bestående i minst 6 månader och som personen har svårt att kontrollera. Det måste vara associerat med minst 3 av följande symtom: rastlöshet eller känsla av att vara uppskruvad eller på kant, lätt trötthet, koncentrationssvårigheter eller att sinnet blir tomt, irritabilitet, muskelspänningar och sömnstörningar.
DOSERING OCH ADMINISTRERING
Lexapro 5mg ska administreras en gång dagligen, på morgonen eller kvällen, med eller utan mat.
Major depressiv sjukdom
Inledande behandling
Tonåringar
Den rekommenderade dosen av Lexapro är 10 mg en gång dagligen. En prövning med flexibel dos av Lexapro (10 till 20 mg/dag) visade effektiviteten av Lexapro [se Kliniska studier ]. Om dosen höjs till 20 mg bör detta ske efter minst tre veckor.
Vuxna
Den rekommenderade dosen av Lexapro 10 mg är 10 mg en gång dagligen. En prövning med fast dos av Lexapro visade effektiviteten av både 10 mg och 20 mg Lexapro 5 mg, men lyckades inte visa en större fördel med 20 mg över 10 mg [se Kliniska studier ]. Om dosen höjs till 20 mg bör detta ske efter minst en vecka.
Underhållsbehandling
Det är allmänt överens om att akuta episoder av egentlig depression kräver flera månader eller längre av långvarig farmakologisk terapi utöver svaret på den akuta episoden. Systematisk utvärdering av fortsatt Lexapro 10 eller 20 mg/dag hos vuxna patienter med egentlig depression som svarade när de tog Lexapro under en 8-veckors akut behandlingsfas visade en fördel med sådan underhållsbehandling [se Kliniska studier ]. Icke desto mindre bör den läkare som väljer att använda Lexapro 5 mg under längre perioder med jämna mellanrum omvärdera läkemedlets långsiktiga användbarhet för den enskilda patienten. Patienter bör regelbundet utvärderas för att fastställa behovet av underhållsbehandling.
Generaliserat ångestsyndrom
Inledande behandling
Vuxna
Den rekommenderade startdosen av Lexapro är 10 mg en gång dagligen. Om dosen höjs till 20 mg bör detta ske efter minst en vecka.
Underhållsbehandling
Generaliserat ångestsyndrom anses vara ett kroniskt tillstånd. Effekten av Lexapro vid behandling av GAD efter 8 veckor har inte studerats systematiskt. Den läkare som väljer att använda Lexapro under längre perioder bör med jämna mellanrum omvärdera läkemedlets långsiktiga användbarhet för den enskilda patienten.
Skärm för bipolär sjukdom innan du startar Lexapro
Innan behandling med Lexapro eller annat antidepressivt läkemedel påbörjas, screena patienterna för en personlig familjehistoria av bipolär sjukdom, mani eller hypomani [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Särskilda populationer
10 mg/dag är den rekommenderade dosen för de flesta äldre patienter och patienter med nedsatt leverfunktion.
Ingen dosjustering är nödvändig för patienter med lätt eller måttligt nedsatt njurfunktion. Lexapro ska användas med försiktighet till patienter med gravt nedsatt njurfunktion.
Avbrytande av behandling med Lexapro
Symtom i samband med utsättning av Lexapro 5 mg och andra SSRI och SNRI har rapporterats [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Patienter bör övervakas med avseende på dessa symtom när behandlingen avbryts. En gradvis minskning av dosen snarare än abrupt utsättning rekommenderas när så är möjligt. Om oacceptabla symtom uppstår efter en minskning av dosen eller efter avslutad behandling, kan återuppta den tidigare ordinerade dosen övervägas. Därefter kan läkaren fortsätta att minska dosen men i en mer gradvis takt.
Byta en patient till eller från en monoaminoxidashämmare (MAO-hämmare) avsedd att behandla psykiatriska störningar
Minst 14 dagar bör förflyta mellan utsättande av en MAO-hämmare avsedd för behandling av psykiatriska störningar och påbörjande av behandling med Lexapro. Omvänt bör minst 14 dagar tillåtas efter avslutad Lexapro 20 mg innan man påbörjar en MAO-hämmare avsedd att behandla psykiatriska störningar [se KONTRAINDIKATIONER ].
Användning av Lexapro med andra MAO-hämmare såsom linezolid eller metylenblått
Starta inte Lexapro 5mg hos en patient som behandlas med linezolid eller intravenöst metylenblått eftersom det finns en ökad risk för serotonergt syndrom. Hos en patient som behöver mer akut behandling av ett psykiatriskt tillstånd bör andra insatser, inklusive sjukhusvistelse, övervägas [se KONTRAINDIKATIONER ].
vissa fall kan en patient som redan får Lexapro 10 mg-behandling behöva akut behandling med linezolid eller intravenöst metylenblått. Om acceptabla alternativ till linezolid eller intravenös behandling med metylenblått inte finns tillgängliga och de potentiella fördelarna med behandling med linezolid eller intravenös metylenblått bedöms uppväga riskerna för serotonergt syndrom hos en viss patient, ska Lexapro stoppas omedelbart och linezolid eller intravenös metylenblått kan administreras. Patienten ska övervakas med avseende på symtom på serotonergt syndrom i 2 veckor eller fram till 24 timmar efter den sista dosen av linezolid eller intravenöst metylenblått, beroende på vilket som inträffar först. Behandling med Lexapro kan återupptas 24 timmar efter den sista dosen av linezolid eller intravenös metylenblått [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Risken med att administrera metylenblått på icke-intravenös väg (som orala tabletter eller genom lokal injektion) eller i intravenösa doser mycket lägre än 1 mg/kg med Lexapro 10 mg är oklar. Läkaren bör dock vara medveten om möjligheten av uppkommande symtom på serotonergt syndrom vid sådan användning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
HUR LEVERERAS
Doseringsformer och styrkor
Tabletter
Lexapro 10 mg tabletter är filmdragerade, runda tabletter som innehåller escitalopramoxalat i styrkor motsvarande 5 mg, 10 mg och 20 mg escitaloprambas. Tabletterna på 10 och 20 mg är skårade. Stämplad med "FL" på ena sidan och antingen "5", "10" eller "20" på andra sidan beroende på deras respektive styrkor.
Oral lösning
Lexapro oral lösning innehåller escitalopramoxalat motsvarande 1 mg/ml escitaloprambas (säljs inte för närvarande).
Förvaring Och Hantering
Tabletter
5 mg tabletter
Flaska med 100 - NDC # 0456-2005-01
Vita till benvita, runda, icke-skårade, filmbelagda. Tryck "FL" på ena sidan av tabletten och "5" på den andra sidan.
10 mg tabletter
Flaska med 100 - NDC 0456-2010-01 10 x 10 enhetsdos - NDC # 0456-2010-63
Vit till benvit, rund, skårad, filmbelagd. Avtryck på den skårade sidan med "F" på vänster sida och "L" på höger sida. Stämpel på sidan utan poäng med "10".
20 mg tabletter
Flaska med 100 - NDC # 0456-2020-01 10 x 10 enhetsdos - NDC # 0456-2020-63
Vit till benvit, rund, skårad, filmbelagd. Avtryck på den skårade sidan med "F" på vänster sida och "L" på höger sida. Stämpel på sidan utan poäng med "20".
Oral lösning
5 mg/5 ml, pepparmintsmak (240 ml) - NDC # 0456-2101-08. Den orala lösningen marknadsförs för närvarande inte.
Förvaring Och Hantering
Förvara vid 20°C till 25°C (68°F till 77°F); utflykter tillåtna till 15 till 30°C (59° till 86°F).
Distribuerat av: Allergan USA, Inc. Madison, NJ 07940. Reviderad: sep 2021
BIEFFEKTER
Erfarenhet av kliniska prövningar
Eftersom kliniska studier utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska studierna av ett läkemedel inte direkt jämföras med frekvensen i de kliniska studierna av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Datakällor för kliniska prövningar
Pediatrik (6-17 år)
Biverkningar samlades in hos 576 pediatriska patienter (286 Lexapro 5 mg, 290 placebo) med egentlig depression i dubbelblinda placebokontrollerade studier. Säkerhet och effektivitet för Lexapro 5mg hos pediatriska patienter under 12 år har inte fastställts.
Vuxna
Biverkningsinformation för Lexapro 5 mg samlades in från 715 patienter med egentlig depression som exponerades för escitalopram och från 592 patienter som exponerades för placebo i dubbelblinda, placebokontrollerade studier. Ytterligare 284 patienter med egentlig depression exponerades nyligen för escitalopram i öppna prövningar. Biverkningsinformationen för Lexapro hos patienter med GAD samlades in från 429 patienter som exponerats för escitalopram och från 427 patienter som exponerats för placebo i dubbelblinda, placebokontrollerade studier.
Biverkningar under exponering erhölls i första hand genom allmän förfrågan och registrerades av kliniska utredare med hjälp av terminologi som de själva valt. Följaktligen är det inte möjligt att ge en meningsfull uppskattning av andelen individer som upplever biverkningar utan att först gruppera liknande typer av händelser i ett mindre antal standardiserade händelsekategorier. I tabellerna och tabellerna som följer har Världshälsoorganisationens (WHO) standardterminologi använts för att klassificera rapporterade biverkningar.
De angivna frekvenserna av biverkningar representerar andelen individer som åtminstone en gång upplevt en behandlingsuppkomnande biverkning av den listade typen. En händelse ansågs vara upphov till behandling om den inträffade för första gången eller förvärrades under behandling efter baslinjeutvärdering.
Biverkningar i samband med avbrytande av behandling
Major depressiv sjukdom
Pediatrik (6-17 år)
Biverkningar var associerade med utsättning av 3,5 % av 286 patienter som fick Lexapro och 1 % av 290 patienter som fick placebo. Den vanligaste biverkningen (incidens minst 1 % för Lexapro 10 mg och mer än placebo) i samband med utsättande av behandlingen var sömnlöshet (1 % Lexapro, 0 % placebo).
Vuxna
Bland de 715 deprimerade patienter som fick Lexapro i placebokontrollerade studier avbröt 6 % behandlingen på grund av en biverkning, jämfört med 2 % av 592 patienter som fick placebo. I två studier med fasta doser skilde sig inte frekvensen av avbrott på grund av biverkningar hos patienter som fick 10 mg/dag Lexapro 20 mg signifikant från frekvensen av utsättning på grund av biverkningar hos patienter som fick placebo. Frekvensen av avbrott på grund av biverkningar hos patienter som tilldelats en fast dos på 20 mg/dag Lexapro var 10 %, vilket var signifikant skild från frekvensen av utsättning för biverkningar hos patienter som fick 10 mg/dag Lexapro (4 %) och placebo (3%). Biverkningar som var förknippade med utsättningen av minst 1 % av patienterna som behandlades med Lexapro 5 mg, och för vilka frekvensen var minst dubbelt så hög som för placebo, var illamående (2 %) och ejakulationsstörning (2 % av manliga patienter).
Generaliserat ångestsyndrom
Vuxna
Bland de 429 GAD-patienter som fick Lexapro 10-20 mg/dag i placebokontrollerade studier, avbröt 8 % behandlingen på grund av en biverkning, jämfört med 4 % av 427 patienter som fick placebo. Biverkningar som var associerade med utsättningen av minst 1 % av patienterna som behandlades med Lexapro 20 mg, och för vilka frekvensen var minst dubbelt så hög som placebofrekvensen, var illamående (2 %), sömnlöshet (1 %) och trötthet (1 %). %).
Förekomst av biverkningar i placebokontrollerade kliniska prövningar
Major depressiv sjukdom
Pediatrik (6-17 år)
Den övergripande profilen av biverkningar hos pediatriska patienter liknade i allmänhet den som sågs i vuxna studier, som visas i tabell 2. Följande biverkningar (exklusive de som visas i tabell 2 och de för vilka de kodade termerna var oinformativa eller missvisande) ) rapporterades med en incidens på minst 2 % för Lexapro och mer än placebo: ryggsmärtor, urinvägsinfektion, kräkningar och nästäppa.
Vuxna
De vanligast observerade biverkningarna hos Lexapro 10 mg-patienter (incidens på cirka 5 % eller mer och cirka dubbelt så stor incidens hos placebopatienter) var sömnlöshet, ejakulationsstörning (främst utlösningsfördröjning), illamående, ökad svettning, trötthet och somnolens.
Tabell 2 räknar upp incidensen, avrundad till närmaste procent, av behandlingsuppkomna biverkningar som inträffade bland 715 deprimerade patienter som fick Lexapro 20 mg i doser från 10 till 20 mg/dag i placebokontrollerade studier. Händelser som ingår är de som inträffade hos 2 % eller fler av patienterna som behandlades med Lexapro 20 mg och för vilka incidensen hos patienter behandlade med Lexapro 10 mg var högre än förekomsten hos placebobehandlade patienter.
TABELL 2 Behandlingsuppkomna biverkningar observerade med en frekvens på ≥ 2 % och mer än placebo för allvarlig depressiv sjukdom
Generaliserat ångestsyndrom
Vuxna
De vanligast observerade biverkningarna hos Lexapro-patienter (incidens av cirka 5 % eller mer och cirka dubbelt så stor incidens hos placebopatienter) var illamående, ejakulationsstörning (främst utlösningsfördröjning), sömnlöshet, trötthet, minskad libido och anorgasmi.
räknar upp incidensen, avrundad till närmaste procent av behandlingsuppkomna biverkningar som inträffade bland 429 GAD-patienter som fick Lexapro 10 till 20 mg/dag i placebokontrollerade studier. Händelser som ingår är de som inträffade hos 2 % eller fler av patienterna som behandlades med Lexapro och för vilka incidensen hos patienter behandlade med Lexapro var högre än förekomsten hos placebobehandlade patienter.
TABELL 3 Behandlingsuppkomna biverkningar observerade med en frekvens på ≥ 2 % och mer än placebo för generaliserat ångestsyndrom
Dosberoende av biverkningar
Det potentiella dosberoendet av vanliga biverkningar (definierad som en incidens på ≥5 % i antingen 10 mg eller 20 mg Lexapro-grupperna) undersöktes på basis av den kombinerade förekomsten av biverkningar i två prövningar med fasta doser. Den totala incidensen av biverkningar hos 10 mg Lexapro-behandlade patienter (66 %) liknade den för placebobehandlade patienter (61 %), medan incidensen hos 20 mg/dag Lexapro-behandlade patienter var högre (86 %). Tabell 4 visar vanliga biverkningar som inträffade i 20 mg/dag Lexapro-gruppen med en incidens som var ungefär dubbelt så stor som för 10 mg/dag Lexapro 10 mg-gruppen och ungefär två gånger den för placebogruppen.
TABELL 4 Incidens av vanliga biverkningar hos patienter med allvarlig depressiv sjukdom
Manlig och kvinnlig sexuell dysfunktion med SSRI
Även om förändringar i sexuell lust, sexuell prestation och sexuell tillfredsställelse ofta förekommer som manifestationer av en psykiatrisk störning, kan de också vara en konsekvens av farmakologisk behandling. I synnerhet tyder vissa bevis på att SSRI kan orsaka sådana ogynnsamma sexuella upplevelser.
Tillförlitliga uppskattningar av förekomsten och svårighetsgraden av ogynnsamma upplevelser som involverar sexuell lust, prestation och tillfredsställelse är dock svåra att få, delvis på grund av att patienter och läkare kan vara ovilliga att diskutera dem. Följaktligen kommer uppskattningar av förekomsten av ogynnsam sexuell upplevelse och prestanda som nämns i produktmärkning sannolikt att underskatta deras faktiska förekomst.
TABELL 5 Förekomst av sexuella biverkningar i placebokontrollerade kliniska prövningar
Det finns inga tillräckligt utformade studier som undersöker sexuell dysfunktion med escitaloprambehandling.
Priapism har rapporterats med alla SSRI-preparat.
Även om det är svårt att veta den exakta risken för sexuell dysfunktion i samband med användning av SSRI, bör läkare rutinmässigt fråga om sådana möjliga biverkningar.
Vital Sign Changes
Lexapro 5 mg och placebogrupper jämfördes med avseende på (1) genomsnittlig förändring från baslinjen i vitala tecken (puls, systoliskt blodtryck och diastoliskt blodtryck) och (2) incidensen av patienter som uppfyller kriterierna för potentiellt kliniskt signifikanta förändringar från baslinjen i dessa variabler. Dessa analyser avslöjade inga kliniskt viktiga förändringar i vitala tecken associerade med Lexapro 20 mg behandling. Dessutom indikerade en jämförelse av mätningar av liggande och stående vitala tecken hos patienter som fick Lexapro 20 mg att Lexapro-behandling inte är associerad med ortostatiska förändringar.
Viktförändringar
Patienter som behandlats med Lexapro i kontrollerade studier skilde sig inte från placebobehandlade patienter med avseende på kliniskt viktig förändring i kroppsvikt.
Laboratorieförändringar
Lexapro 5 mg och placebogrupper jämfördes med avseende på (1) genomsnittlig förändring från baslinjen i olika serumkemi-, hematologi- och urinanalysvariabler, och (2) förekomsten av patienter som uppfyller kriterierna för potentiellt kliniskt signifikanta förändringar från baslinjen i dessa variabler. Dessa analyser avslöjade inga kliniskt viktiga förändringar i laboratorietestparametrar associerade med Lexapro-behandling.
EKG-förändringar
Elektrokardiogram från grupperna Lexapro (N=625) och placebo (N=527) jämfördes med avseende på extremvärden definierade som försökspersoner med QTc-förändringar över 60 msek från baslinjen eller absoluta värden över 500 msek efter dos, och försökspersoner med hjärtfrekvensökningar till över 100 slag per minut eller minskar till mindre än 50 slag per minut med en förändring på 25 % från baslinjen (takykardisk respektive bradykardisk extremvärde). Ingen av patienterna i Lexapro 20 mg-gruppen hade ett QTcF-intervall >500 msek eller en förlängning >60 msek jämfört med 0,2 % av patienterna i placebogruppen. Incidensen av takykardiska extremvärden var 0,2 % i Lexapro 5 mg och placebogruppen. Incidensen av bradykardiska extremvärden var 0,5 % i Lexapro 10 mg-gruppen och 0,2 % i placebogruppen.
QTcF-intervallet utvärderades i en randomiserad, placebo- och aktiv (moxifloxacin 400 mg) kontrollerad cross-over, eskalerande multipeldosstudie på 113 friska försökspersoner. Den maximala medelskillnaden (95 % övre konfidensgräns) från placeboarmen var 4,5 (6,4) respektive 10,7 (12,7) msek för 10 mg respektive supraterapeutiskt 30 mg escitalopram givet en gång dagligen. Baserat på det etablerade exponerings-responssambandet är den förväntade QTcF-förändringen från placeboarmen (95 % konfidensintervall) under Cmax för dosen 20 mg 6,6 (7,9) msek. Escitalopram 30 mg givet en gång dagligen resulterade i medel-Cmax 1,7 gånger högre än medel-Cmax för den maximalt rekommenderade terapeutiska dosen vid steady state (20 mg). Exponeringen under supraterapeutisk 30 mg dos liknar de steady state-koncentrationer som förväntas hos CYP2C19-fattiga metaboliserare efter en terapeutisk dos på 20 mg.
Andra reaktioner som observerats under premarketingutvärderingen av Lexapro
Följande är en lista över behandlingsuppkomna biverkningar, enligt definitionen i introduktionen till NEGATIVA REAKTIONER avsnitt, rapporterat av de 1428 patienter som behandlats med Lexapro under perioder på upp till ett år i dubbelblinda eller öppna kliniska prövningar under utvärderingen före marknadsföringen. Listan inkluderar inte de händelser som redan är listade i de händelser för vilka en drogorsak var avlägsen och med en frekvens som är mindre än 1 % eller lägre än placebo, de händelser som var så allmänna att de inte var informativa, och de händelser som rapporterats endast en gång som inte hade någon betydande sannolikhet att vara akut livshotande. Händelser är kategoriserade efter kroppssystem. Händelser av stor klinisk betydelse beskrivs i VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER sektion.
Kardiovaskulär -hypertoni, hjärtklappning.
Störningar i centrala och perifera nervsystemet - yrsel i huvudet, migrän.
Gastrointestinala störningar -bukkramper, halsbränna, gastroenterit.
Allmän - allergi, bröstsmärtor, feber, värmevallningar, smärta i armar och ben.
Metaboliska och näringsmässiga störningar -ökad vikt.
Muskuloskeletala systemet - artralgi, myalgi käkstelhet.
Psykiatriska störningar ökad aptit, försämrad koncentration, irritabilitet.
Reproduktionsstörningar/Kvinna - mensvärk, menstruationsstörning.
Störningar i andningsorganen - bronkit, hosta, nästäppa, sinustäppa, sinushuvudvärk.
Hud- och bihangsstörningar - utslag.
Särskilda sinnen - suddig syn, tinnitus.
Störningar i urinvägarna -urinfrekvens, urinvägsinfektion.
Erfarenhet efter marknadsföring
Biverkningar rapporterade efter marknadsföringen av Escitalopram
Följande biverkningar har identifierats efter användning av Lexapro efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Blod- och lymfsystemet: anemi, agranulocyt, aplastisk anemi, hemolytisk anemi, idiopatisk trombocytopeni purpura, leukopeni, trombocytopeni.
Hjärtsjukdomar: förmaksflimmer, bradykardi, hjärtsvikt, hjärtinfarkt, takykardi, torsade de pointes, ventrikulär arytmi, ventrikulär takykardi.
Öron- och labyrintsjukdomar: vertigo
Endokrina störningar: diabetes mellitus, hyperprolaktinemi, SIADH.
Ögonstörningar: stängningsvinkelglaukom, diplopi, mydriasis, synstörning.
Gastrointestinala störningar: dysfagi, gastrointestinal blödning, gastroesofageal reflux, pankreatit, rektal blödning.
Allmänna störningar och villkor för administrationsplatsen: onormal gång, asteni, ödem, fall, onormal känsla, sjukdomskänsla.
Lever och gallvägar: fulminant hepatit, leversvikt, levernekros, hepatit.
Immunsystemets störningar: allergisk reaktion, anafylaxi.
Undersökningar: bilirubin ökat, minskad vikt, elektrokardiogram QT-förlängning, leverenzymer ökade, hyperkolesterolemi, INR ökade, protrombin minskade.
Metabolism och näringsstörningar: hyperglykemi, hypoglykemi, hypokalemi, hyponatremi.
Muskuloskeletala och bindvävssjukdomar: muskelkramp, muskelstelhet, muskelsvaghet, rabdomyolys.
Störningar i nervsystemet: akatisi, amnesi, ataxi, koreoatetos, cerebrovaskulär olycka, dysartri, dyskinesi, dystoni, extrapyramidala störningar, grand mal-anfall (eller kramper), hypoestesi, myoklonus, nystagmus, Parkinsonism, restless legs, anfall, tremordyskinesi, synkope.
Graviditet, Puerperium och perinatala tillstånd: spontan abort.
Psykiatriska störningar: akut psykos, aggression, agitation, ilska, ångest, apati, fullbordat självmord, förvirring, depersonalisering, förvärrad depression, delirium, vanföreställning, desorientering, overklig känsla, hallucinationer (visuella och auditiva), humörsvängningar, nervositet, mardröm, panikreaktion, paranoia rastlöshet, självskadebeteende eller tankar på självskada, självmordsförsök, självmordstankar, självmordsbenägenhet.
Njur- och urinvägsstörningar: akut njursvikt, dysuri, urinretention.
Reproduktionssystemet och bröststörningar: menorragi, priapism.
Andningsvägar, bröstkorg och mediastinum: dyspné, näsblod, lungemboli, pulmonell hypertoni hos den nyfödda. Hud och subkutan vävnad: alopeci, angioödem, dermatit, ekkymos, erythema multiforme, ljuskänslighetsreaktion, Stevens Johnsons syndrom, toxisk epidermal nekrolys, urtikaria.
Vaskulära sjukdomar: djup ventrombos, rodnad, hypertensiv kris, hypotoni, ortostatisk hypotoni, flebit, trombos.
LÄKEMEDELSINTERAKTIONER
Monoaminoxidashämmare (MAO-hämmare)
[Ser DOSERING OCH ADMINISTRERING och , KONTRAINDIKATIONER och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Serotonerga läkemedel
[Ser DOSERING OCH ADMINISTRERING och , KONTRAINDIKATIONER och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Triptaner
Det har förekommit sällsynta rapporter om serotonergt syndrom efter marknadsföring med användning av en SSRI och en triptan. Om samtidig behandling av Lexapro 10 mg och en triptan är kliniskt motiverad, rekommenderas noggrann observation av patienten, särskilt under behandlingsstart och dosökningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
CNS-läkemedel
Med tanke på de primära CNS-effekterna av escitalopram bör försiktighet iakttas när det tas i kombination med andra centralt verkande läkemedel.
Alkohol
Även om Lexapro inte förstärkte de kognitiva och motoriska effekterna av alkohol i en klinisk prövning, som med andra psykotropa läkemedel, rekommenderas inte användning av alkohol av patienter som tar Lexapro.
Läkemedel som stör hemostas (NSAID, aspirin, warfarin, etc.)
Serotoninfrisättning av blodplättar spelar en viktig roll vid hemostas. Epidemiologiska studier av fall-kontroll och kohortdesign som har visat ett samband mellan användning av psykotropa läkemedel som stör serotoninåterupptag och förekomsten av övre gastrointestinala blödningar har också visat att samtidig användning av ett NSAID eller acetylsalicylsyra kan potentiera risken för blödning. Förändrade antikoagulantiaeffekter, inklusive ökad blödning, har rapporterats när SSRI och SNRI administreras samtidigt med warfarin. Patienter som får warfarinbehandling bör övervakas noggrant när Lexapro påbörjas eller avbryts.
Cimetidin
Hos försökspersoner som hade fått 21 dagar med 40 mg/dag racemisk citalopram, resulterade kombinerad administrering av 400 mg cimetidin två gånger dagligen under 8 dagar i en ökning av citaloprams AUC och Cmax med 43 % respektive 39 %. Den kliniska betydelsen av dessa fynd är okänd.
Digoxin
Hos försökspersoner som hade fått 21 dagar med 40 mg/dag racemiskt citalopram, påverkade kombinerad administrering av citalopram och digoxin (engångsdos på 1 mg) inte signifikant farmakokinetiken för varken citalopram eller digoxin.
Litium
Samtidig administrering av racemiskt citalopram (40 mg/dag i 10 dagar) och litium (30 mmol/dag i 5 dagar) hade ingen signifikant effekt på farmakokinetiken för citalopram eller litium. Likväl bör plasmalitiumnivåerna övervakas med lämplig justering av litiumdosen i enlighet med klinisk standardpraxis. Eftersom litium kan förstärka de serotonerga effekterna av escitalopram, bör försiktighet iakttas när Lexapro 5 mg och litium administreras samtidigt.
Pimozide och Celexa
en kontrollerad studie var en engångsdos av pimozid 2 mg administrerad samtidigt med racemisk citalopram 40 mg givet en gång dagligen i 11 dagar associerad med en genomsnittlig ökning av QTc-värden på cirka 10 msek jämfört med pimozid givet ensamt. Racemisk citalopram förändrade inte medel-AUC eller Cmax för pimozid. Mekanismen för denna farmakodynamiska interaktion är inte känd.
Sumatriptan
Det har förekommit sällsynta rapporter efter marknadsföring som beskriver patienter med svaghet, hyperreflexi och inkoordination efter användning av SSRI och sumatriptan. Om samtidig behandling med sumatriptan och en SSRI (t.ex. fluoxetin, fluvoxamin, paroxetin, sertralin, citalopram, escitalopram) är kliniskt motiverad, rekommenderas lämplig observation av patienten.
Teofyllin
Kombinerad administrering av racemiskt citalopram (40 mg/dag i 21 dagar) och CYP1A2-substratet teofyllin (engångsdos på 300 mg) påverkade inte farmakokinetiken för teofyllin. Effekten av teofyllin på farmakokinetiken för citalopram har inte utvärderats.
Warfarin
Administrering av 40 mg racemiskt citalopram/dag under 21 dagar påverkade inte farmakokinetiken för warfarin, ett CYP3A4-substrat. Protrombintiden ökade med 5 %, vars kliniska betydelse är okänd.
Karbamazepin
Kombinerad administrering av racemisk citalopram (40 mg/dag i 14 dagar) och karbamazepin (titrerat till 400 mg/dag i 35 dagar) påverkade inte signifikant farmakokinetiken för karbamazepin, ett CYP3A4-substrat. Även om bottennivåerna av citalopram i plasma var opåverkade, med tanke på karbamazepins enzyminducerande egenskaper, bör möjligheten att karbamazepin kan öka clearance av escitalopram övervägas om de två läkemedlen ges samtidigt.
Triazolam
Kombinerad administrering av racemiskt citalopram (titrerat till 40 mg/dag i 28 dagar) och CYP3A4-substratet triazolam (engångsdos på 0,25 mg) påverkade inte farmakokinetiken för varken citalopram eller triazolam signifikant.
Ketokonazol
Kombinerad administrering av racemisk citalopram (40 mg) och ketokonazol (200 mg), en potent CYP3A4-hämmare, minskade Cmax och AUC för ketokonazol med 21 % respektive 10 % och påverkade inte farmakokinetiken för citalopram signifikant.
Ritonavir
Kombinerad administrering av en singeldos ritonavir (600 mg), både ett CYP3A4-substrat och en potent hämmare av CYP3A4, och escitalopram (20 mg) påverkade inte farmakokinetiken för vare sig ritonavir eller escitalopram.
CYP3A4- och -2C19-hämmare
In vitro-studier visade att CYP3A4 och -2C19 är de primära enzymerna involverade i metabolismen av escitalopram. Samtidig administrering av escitalopram (20 mg) och ritonavir (600 mg), en potent hämmare av CYP3A4, påverkade dock inte escitaloprams farmakokinetik signifikant. Eftersom escitalopram metaboliseras av flera enzymsystem, kan hämning av ett enda enzym inte nämnvärt minska escitalopramclearance.
Läkemedel som metaboliseras av Cytokrom P4502D6
In vitro-studier visade ingen hämmande effekt av escitalopram på CYP2D6. Dessutom var steady state-nivåerna av racemiskt citalopram inte signifikant olika hos låga metaboliserare och omfattande CYP2D6-metaboliserare efter administrering av flera doser av citalopram, vilket tyder på att samtidig administrering, med escitalopram, av ett läkemedel som hämmar CYP2D6, sannolikt inte kommer att ha kliniskt signifikanta effekter på escitalopram metabolism. Det finns dock begränsade in vivo-data som tyder på en måttlig CYP2D6-hämmande effekt för escitalopram, dvs. samtidig administrering av escitalopram (20 mg/dag i 21 dagar) med det tricykliska antidepressiva medlet desipramin (engångsdos på 50 mg), ett substrat för CYP2D6, resulterade i i en 40% ökning av Cmax och en 100% ökning av AUC för desipramin. Den kliniska betydelsen av detta fynd är okänd. Ändå är försiktighet indicerad vid samtidig administrering av escitalopram och läkemedel som metaboliseras av CYP2D6.
Metoprolol
Administrering av 20 mg/dag Lexapro 20 mg under 21 dagar hos friska frivilliga resulterade i en 50 % ökning av Cmax och 82 % ökning av AUC för den beta-adrenerga blockeraren metoprolol (given i en engångsdos på 100 mg). Ökade plasmanivåer av metoprolol har associerats med minskad kardioselektivitet. Samtidig administrering av Lexapro 5 mg och metoprolol hade inga kliniskt signifikanta effekter på blodtryck eller hjärtfrekvens.
Elektrokonvulsiv terapi (ECT)
Det finns inga kliniska studier av kombinerad användning av ECT och escitalopram.
Narkotikamissbruk och beroende
Missbruk och beroende
Fysiskt och psykologiskt beroende
Djurstudier tyder på att risken för missbruk av racemiskt citalopram är låg. Lexapro 10mg har inte systematiskt studerats på människor för dess potential för missbruk, tolerans eller fysiskt beroende. Den kliniska erfarenheten av Lexapro före marknadsföringen avslöjade inte något läkemedelssökande beteende. Dessa observationer var dock inte systematiska och det är inte möjligt att utifrån denna begränsade erfarenhet förutsäga i vilken utsträckning ett CNS-aktivt läkemedel kommer att missbrukas, avledas och/eller missbrukas när det väl marknadsförts. Följaktligen bör läkare noggrant utvärdera Lexapro-patienter med avseende på drogmissbruk och följa dessa patienter noggrant och observera dem för tecken på missbruk eller missbruk (t.ex. utveckling av tolerans, ökningar av dosen, drogsökande beteende).
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Självmordstankar och -beteenden hos ungdomar och unga vuxna
poolade analyser av placebokontrollerade prövningar av antidepressiva läkemedel (SSRI och andra antidepressiva klasser) som inkluderade cirka 77 000 vuxna patienter och 4 500 pediatriska patienter, var förekomsten av självmordstankar och självmordsbeteenden hos de antidepressiva patienter i åldern 24 år och yngre högre än hos placebobehandlade patienter. Det fanns avsevärd variation i risk för självmordstankar och självmordsbeteenden bland droger, men det fanns en ökad risk hos unga patienter för de flesta studerade droger. Det fanns skillnader i absolut risk för självmordstankar och -beteenden över de olika indikationerna, med den högsta förekomsten hos patienter med MDD. Skillnaderna mellan läkemedel och placebo i antalet fall av självmordstankar och självmordsbeteenden per 1 000 behandlade patienter anges i
Det är okänt om risken för självmordstankar och självmordsbeteenden hos barn, ungdomar och unga vuxna sträcker sig till långvarig användning, dvs. längre än fyra månader. Det finns dock betydande bevis från placebokontrollerade underhållsstudier på vuxna med MDD för att antidepressiva läkemedel fördröjer återkommande depression och att depression i sig är en riskfaktor för självmordstankar och självmordsbeteenden.
Övervaka alla patienter som behandlas med antidepressivt läkemedel för indikationer på klinisk försämring och uppkomst av självmordstankar och -beteenden, särskilt under de första månaderna av läkemedelsbehandling och vid tidpunkter med dosförändringar. Rådgiv familjemedlemmar eller vårdgivare till patienter att övervaka beteendeförändringar och varna vårdgivaren. Överväg att ändra den terapeutiska regimen, inklusive eventuellt avbrytande av Lexapro, hos patienter vars depression är ihållande värre eller som upplever framväxande självmordstankar eller -beteenden.
Serotonin syndrom
Utveckling av ett potentiellt livshotande serotonergt syndrom har rapporterats med SNRI och SSRI, inklusive Lexapro, enbart men särskilt vid samtidig användning av andra serotonerga läkemedel (inklusive triptaner, tricykliska antidepressiva medel, fentanyl, litium, tramadol, tryptofan, buspiron, och johannesört) och med läkemedel som försämrar metabolismen av serotonin (särskilt MAO-hämmare, både de som är avsedda att behandla psykiatriska störningar och även andra, såsom linezolid och intravenöst metylenblått).
Symtom på serotonergt syndrom kan inkludera förändringar i mental status (t.ex. agitation, hallucinationer, delirium och koma), autonom instabilitet (t.ex. takykardi, labilt blodtryck, yrsel, diafores, rodnad, hypertermi), neuromuskulära symtom (t.ex. tremor, stelhet, myoklonus, hyperreflexi, inkoordination) kramper och/eller gastrointestinala symtom (t.ex. illamående, kräkningar, diarré). Patienter bör övervakas med avseende på uppkomsten av serotonergt syndrom.
Samtidig användning av Lexapro 10 mg och MAO-hämmare avsedda att behandla psykiatriska störningar är kontraindicerad. Lexapro 5mg ska inte heller påbörjas hos en patient som behandlas med MAO-hämmare som linezolid eller intravenös metylenblått. Alla rapporter med metylenblått som gav information om administreringssättet involverade intravenös administrering i dosintervallet 1 mg/kg till 8 mg/kg. Inga rapporter involverade administrering av metylenblått på andra sätt (såsom orala tabletter eller lokal vävnadsinjektion) eller vid lägre doser. Det kan finnas omständigheter då det är nödvändigt att påbörja behandling med en MAO-hämmare såsom linezolid eller intravenös metylenblått hos en patient som tar Lexapro. Lexapro bör avbrytas innan behandling med MAO-hämmaren påbörjas [se KONTRAINDIKATIONER och DOSERING OCH ADMINISTRERING ].
Om samtidig användning av Lexapro 5mg med andra serotonerga läkemedel inklusive triptaner, tricykliska antidepressiva medel, fentanyl, litium, tramadol, buspiron, tryptofan, amfetamin och johannesört är kliniskt motiverad, bör patienterna göras medvetna om en potentiell ökad risk för serotonergt syndrom. , särskilt under behandlingsstart och dosökningar.
Behandling med Lexapro och eventuella samtidiga serotonerga medel ska avbrytas omedelbart om ovanstående händelser inträffar och stödjande symtomatisk behandling bör inledas.
Avbrytande av behandling med Lexapro
Under marknadsföringen av Lexapro och andra SSRI och SNRI (serotonin- och noradrenalinåterupptagshämmare) har det förekommit spontana rapporter om biverkningar som inträffat vid utsättande av dessa läkemedel, särskilt vid abrupt behandling, inklusive följande: dysforiskt humör, irritabilitet, agitation, yrsel, sensorisk störningar (t.ex. parestesier såsom elektriska stötar), ångest, förvirring, huvudvärk, letargi, emotionell labilitet, sömnlöshet och hypomani. Även om dessa händelser i allmänhet är självbegränsande, har det förekommit rapporter om allvarliga utsättningssymtom.
Patienter bör övervakas för dessa symtom när behandlingen med Lexapro avbryts. En gradvis minskning av dosen snarare än abrupt utsättning rekommenderas när så är möjligt. Om oacceptabla symtom uppstår efter en minskning av dosen eller efter avslutad behandling, kan återuppta den tidigare ordinerade dosen övervägas. Därefter kan läkaren fortsätta att minska dosen men i en mer gradvis takt [se DOSERING OCH ADMINISTRERING ].
Anfall
Även om antikonvulsiva effekter av racemiskt citalopram har observerats i djurstudier, har Lexapro inte systematiskt utvärderats hos patienter med krampanfall. Dessa patienter uteslöts från kliniska studier under produktens premarketingtestning. I kliniska prövningar av Lexapro 5 mg har fall av kramper rapporterats i samband med behandling med Lexapro. Liksom andra läkemedel som är effektiva vid behandling av egentlig depression, bör Lexapro 20 mg introduceras med försiktighet hos patienter med anamnes på anfallsstörning.
Aktivering av mani eller hypomani
Hos patienter med bipolär sjukdom kan behandling av en depressiv episod med Lexapro eller annat antidepressivt medel utlösa en blandad/manisk episod. I placebokontrollerade studier av Lexapro 20 mg vid egentlig depression rapporterades aktivering av mani/hypomani hos en (0,1 %) av 715 patienter som behandlades med Lexapro 20 mg och hos ingen av de 592 patienter som behandlades med placebo. Ytterligare ett fall av hypomani har rapporterats i samband med behandling med Lexapro 10 mg. Aktivering av mani/hypomani har också rapporterats hos en liten del av patienterna med allvarliga affektiva störningar som behandlats med racemiskt citalopram och andra marknadsförda läkemedel som är effektiva vid behandling av egentlig depression. Innan behandling med Lexapro påbörjas, screena patienter för eventuell personlig eller familjehistoria av bipolär sjukdom, mani eller hypomani [se DOSERING OCH ADMINISTRERING ].
Hyponatremi
Hyponatremi kan uppstå som ett resultat av behandling med SSRI och SNRI, inklusive Lexapro. I många fall verkar denna hyponatremi vara resultatet av syndromet med olämplig antidiuretisk hormonsekretion (SIADH), och var reversibel när Lexapro 20 mg avbröts. Fall med serumnatrium lägre än 110 mmol/L har rapporterats. Äldre patienter kan löpa större risk att utveckla hyponatremi med SSRI och SNRI. Dessutom kan patienter som tar diuretika eller som på annat sätt är utarmade i volym löpa större risk [se Geriatrisk användning ]. Utsättning av Lexapro bör övervägas hos patienter med symtomatisk hyponatremi och lämplig medicinsk intervention bör sättas in.
Tecken och symtom på hyponatremi inkluderar huvudvärk, koncentrationssvårigheter, minnesstörning, förvirring, svaghet och ostadighet, vilket kan leda till fall. Tecken och symtom förknippade med mer allvarliga och/eller akuta fall har inkluderat hallucinationer, synkope, anfall, koma, andningsstopp och dödsfall.
Onormal blödning
SSRI och SNRI, inklusive Lexapro 20 mg, kan öka risken för blödningar. Samtidig användning av aspirin, icke-steroida antiinflammatoriska läkemedel, warfarin och andra antikoagulantia kan öka risken. Fallrapporter och epidemiologiska studier (fallkontroll och kohortdesign) har visat ett samband mellan användning av läkemedel som stör serotoninåterupptaget och förekomsten av gastrointestinala blödningar. Blödningshändelser relaterade till användning av SSRI och SNRI har varierat från ekkymoser, hematom, näsblod och petekier till livshotande blödningar.
Patienter bör varnas för risken för blödning i samband med samtidig användning av Lexapro 20 mg och NSAID, acetylsalicylsyra eller andra läkemedel som påverkar koagulationen.
Interferens med kognitiva och motoriska prestanda
en studie på normala frivilliga gav Lexapro 10 mg/dag ingen försämring av intellektuell funktion eller psykomotorisk prestation. Eftersom alla psykoaktiva droger kan försämra omdömet, tänkandet eller motoriken, bör dock patienter varnas för att använda farliga maskiner, inklusive bilar, tills de är rimligt säkra på att Lexapro-terapi inte påverkar deras förmåga att delta i sådana aktiviteter.
Vinkelstängning glaukom
Vinkelstängningsglaukom: Pupillvidgningen som uppstår efter användning av många antidepressiva läkemedel inklusive Lexapro 20 mg kan utlösa en vinkelattack hos en patient med anatomiskt smala vinklar som inte har en patenterad iridektomi.
Användning hos patienter med samtidig sjukdom
Klinisk erfarenhet av Lexapro hos patienter med vissa samtidiga systemiska sjukdomar är begränsad. Försiktighet rekommenderas vid användning av Lexapro 5 mg till patienter med sjukdomar eller tillstånd som orsakar förändrad metabolism eller hemodynamiska svar.
Lexapro har inte utvärderats systematiskt hos patienter med en nyligen anamnes på hjärtinfarkt eller instabil hjärtsjukdom. Patienter med dessa diagnoser uteslöts i allmänhet från kliniska studier under produktens premarketingtestning.
Hos patienter med nedsatt leverfunktion minskade clearance av racemiskt citalopram och plasmakoncentrationerna ökade. Den rekommenderade dosen av Lexapro till patienter med nedsatt leverfunktion är 10 mg/dag [se DOSERING OCH ADMINISTRERING ].
Eftersom escitalopram metaboliseras i stor utsträckning, är utsöndring av oförändrat läkemedel i urinen en mindre elimineringsväg. Tills ett tillräckligt antal patienter med gravt nedsatt njurfunktion har utvärderats under kronisk behandling med Lexapro 20 mg, bör det dock användas med försiktighet hos sådana patienter [se DOSERING OCH ADMINISTRERING ].
Sexuell dysfunktion
Användning av SSRI, inklusive Lexapro, kan orsaka symtom på sexuell dysfunktion [se NEGATIVA REAKTIONER ]. Hos manliga patienter kan SSRI-användning resultera i försening eller ejakulationssvikt, minskad libido och erektil dysfunktion. Hos kvinnliga patienter kan användning av SSRI resultera i minskad libido och försenad eller utebliven orgasm.
Det är viktigt för förskrivare att fråga sig om sexuell funktion innan Lexapro påbörjas och att fråga specifikt om förändringar i sexuell funktion under behandlingen, eftersom sexuell funktion kanske inte spontant rapporteras. När man utvärderar förändringar i sexuell funktion är det viktigt att få en detaljerad historia (inklusive tidpunkten för symtomdebut) eftersom sexuella symtom kan ha andra orsaker, inklusive den underliggande psykiatriska störningen. Diskutera potentiella hanteringsstrategier för att stödja patienter i att fatta välgrundade beslut om behandling.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide ).
Självmordstankar och -beteenden
Råda patienter, deras familjer och vårdgivare att leta efter uppkomsten av självmordstankar och självmordsbeteende, särskilt under behandling och när dosen justeras upp eller ner, och instruera dem att rapportera sådana symtom till sin vårdgivare [se LÅDA VARNING och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Serotonin syndrom
Patienter bör varnas för risken för serotonergt syndrom vid samtidig användning av Lexapro med andra serotonerga läkemedel inklusive triptaner, tricykliska antidepressiva medel, fentanyl, litium, tramadol, tryptofan, buspiron, amfetamin och johannesört, och med läkemedel som försämrar ämnesomsättningen av serotonin (särskilt MAO-hämmare, både de som är avsedda att behandla psykiatriska störningar och även andra, såsom linezolid) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Aktivering av mani eller hypomani
Råda patienter och deras vårdgivare att observera efter tecken på aktivering av mani/hypomani och instruera dem att rapportera sådana symtom till vårdgivaren [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Onormal blödning
Patienter bör varnas för samtidig användning av Lexapro 5mg och NSAID, acetylsalicylsyra, warfarin eller andra läkemedel som påverkar koagulationen eftersom kombinerad användning av psykotropa läkemedel som stör serotoninåterupptaget och dessa medel har associerats med en ökad risk för blödning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Vinkelstängning glaukom
Patienter bör informeras om att intag av Lexapro 5 mg kan orsaka mild pupillvidgning, vilket hos känsliga individer kan leda till en episod av glaukom med vinkelstängning. Redan existerande glaukom är nästan alltid glaukom med öppen vinkel eftersom stängningsvinkelglaukom, när det diagnostiseras, kan behandlas definitivt med iridektomi. Öppenvinkelglaukom är inte en riskfaktor för stängningsvinkelglaukom. Patienter kan vilja undersökas för att avgöra om de är mottagliga för vinkelstängning och genomgå en profylaktisk procedur (t.ex. iridektomi), om de är mottagliga [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Sexuell dysfunktion
Informera patienter om att användning av Lexapro kan orsaka symtom på sexuell dysfunktion hos både manliga och kvinnliga patienter. Informera patienter om att de bör diskutera eventuella förändringar i sexuell funktion och potentiella hanteringsstrategier med sin vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Samtidig medicinering
Eftersom escitalopram är den aktiva isomeren av racemiskt citalopram (Celexa), bör de två medlen inte administreras samtidigt. Patienter bör rådas att informera sin läkare om de tar eller planerar att ta några receptbelagda eller receptfria läkemedel, eftersom det finns risk för interaktioner.
Fortsätter den föreskrivna terapin
Även om patienter kan märka förbättring med Lexapro 10 mg-behandling inom 1 till 4 veckor, bör de rådas att fortsätta behandlingen enligt anvisningarna.
Interferens med psykomotorisk prestanda
Eftersom psykoaktiva droger kan försämra omdöme, tänkande eller motorik, bör patienter varnas för att använda farliga maskiner, inklusive bilar, tills de är rimligtvis säkra på att Lexapro-terapi inte påverkar deras förmåga att delta i sådana aktiviteter.
Alkohol
Patienter bör informeras om att även om Lexapro 5 mg inte har visats i experiment med normala försökspersoner öka de mentala och motoriska försämringar som orsakas av alkohol, rekommenderas inte samtidig användning av Lexapro 20 mg och alkohol hos deprimerade patienter.
Graviditet
Råda gravida kvinnor att meddela sin vårdgivare om de blir gravida eller avser att bli gravida under behandling med LEXAPRO. Informera patienterna om att användning av LEXAPRO 10 mg senare under graviditeten kan leda till ökad risk för neonatala komplikationer som kräver långvarig sjukhusvistelse, andningsstöd, sondmatning och/eller ihållande pulmonell hypertoni (PPHN) hos det nyfödda barnet [se Användning i specifika populationer ].
Informera kvinnor om att det finns ett graviditetsexponeringsregister som övervakar graviditetsresultat hos kvinnor som exponerats för LEXAPRO under graviditeten [se Användning i specifika populationer ].
Laktation
Rekommendera ammande kvinnor som använder LEXAPRO att övervaka spädbarn med avseende på överdriven sedering, rastlöshet, agitation, dålig matning och dålig viktökning och att söka läkarvård om de märker dessa tecken [se Användning i specifika populationer ].
Behov av omfattande behandlingsprogram
Lexapro 20mg är indicerat som en integrerad del av ett totalt behandlingsprogram för MDD som kan innefatta andra åtgärder (psykologiska, pedagogiska, sociala) för patienter med detta syndrom. Läkemedelsbehandling kanske inte är indicerad för alla ungdomar med detta syndrom. Säkerhet och effektivitet för Lexapro 10 mg vid MDD har inte fastställts hos pediatriska patienter under 12 år. Antidepressiva medel är inte avsedda för användning hos ungdomar som uppvisar symtom som är sekundära till miljöfaktorer och/eller andra primära psykiatriska störningar. Lämplig utbildningsplacering är avgörande och psykosociala insatser är ofta till hjälp. När enbart avhjälpande åtgärder är otillräckliga, kommer beslutet att förskriva antidepressiv medicin bero på läkarens bedömning av kroniska och svårighetsgraden av patientens symtom.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
Racemiskt citalopram administrerades i kosten till NMRI/BOM-stammöss och COBS WI-stamråttor under 18 respektive 24 månader. Det fanns inga bevis för carcinogenicitet av racemiskt citalopram hos möss som fick upp till 240 mg/kg/dag. Det fanns en ökad incidens av tunntarmscancer hos råttor som fick 8 eller 24 mg/kg/dag racemiskt citalopram. En dos utan effekt för detta fynd fastställdes inte. Relevansen av dessa fynd för människor är okänd.
Mutagenes
Racemiskt citalopram var mutagent i in vitro bakteriell omvänd mutationsanalys (Ames-test) i 2 av 5 bakteriestammar (Salmonella TA98 och TA1537) i frånvaro av metabolisk aktivering. Det var klastogent i in vitro lungcellsanalysen av kinesisk hamster för kromosomavvikelser i närvaro och frånvaro av metabolisk aktivering. Racemiskt citalopram var inte mutagent i in vitro däggdjursframåtgenmutationsanalysen (HPRT) i muslymfomceller eller i en kopplad in vitro/in vivo analys av oplanerad DNA-syntes (UDS) i råttlever. Det var inte klastogent i in vitro-kromosomavvikelseanalysen i humana lymfocyter eller i två in vivo-musmikronukleusanalyser.
Nedsättning av fertilitet
När racemiskt citalopram administrerades oralt till 16 hanråttor och 24 honråttor före och under parning och dräktighet i doser på 32, 48 och 72 mg/kg/dag, minskade parningen vid alla doser och fertiliteten minskade vid doser ≥ 32 mg/kg/dag. Dräktighetstiden ökade med 48 mg/kg/dag.
Användning i specifika populationer
Graviditet
Registret för graviditetsexponering
Det finns ett graviditetsexponeringsregister som övervakar graviditetsutfall hos kvinnor som exponerats för antidepressiva läkemedel under graviditeten. Sjukvårdsleverantörer uppmuntras att registrera patienter genom att ringa National Pregnancy Registry for Antidepressants på 1-844-405-6185 eller besöka online på https://womensmentalhealth.org/clnical-and-research-programs/pregnancyregistry/antidepressants/
Risksammanfattning
Tillgängliga data från publicerade epidemiologiska studier och rapporter efter marknadsföring har inte fastställt en ökad risk för allvarliga fosterskador eller missfall. Det finns risker för ihållande pulmonell hypertoni hos nyfödda (PPHN) (se Data ) och dålig neonatal anpassning (se Kliniska överväganden ) med exponering för selektiva serotoninåterupptagshämmare (SSRI), inklusive LEXAPRO 5 mg, under graviditet. Det finns risker förknippade med obehandlad depression under graviditet (se Kliniska överväganden ).
reproduktionsstudier på djur har både escitalopram och racemiskt citalopram visat sig ha negativa effekter på embryo/foster och postnatal utveckling, inklusive fosterstrukturella abnormiteter, när de administreras i doser som är högre än humana terapeutiska doser (se Data ).
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i de kliniskt erkända graviditeterna 2 till 4 % respektive 15 till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för modern och/eller embryo/foster risk
Kvinnor som slutar använda antidepressiva är mer benägna att uppleva ett återfall av allvarlig depression än kvinnor som fortsätter med antidepressiva. Detta fynd är från en prospektiv longitudinell studie av 201 gravida kvinnor med en historia av allvarlig depression, som var euthymic och tog antidepressiva i början av graviditeten. Tänk på risken för obehandlad depression när du avbryter eller byter behandling med antidepressiv medicin under graviditet och efter förlossningen.
Fetala/neonatala biverkningar
Nyfödda som exponerats för SSRI eller SNRI, inklusive Lexapro 5mg, sent i tredje trimestern har utvecklat komplikationer som kräver långvarig sjukhusvistelse, andningsstöd och sondmatning. Sådana komplikationer kan uppstå omedelbart efter leverans. Rapporterade kliniska fynd har inkluderat andnöd, cyanos, apné, kramper, temperaturinstabilitet, ätsvårigheter, kräkningar, hypoglykemi, hypotoni, hypertoni, hyperreflexi, tremor, skakningar, irritabilitet och konstant gråt. Dessa egenskaper överensstämmer med antingen en direkt toxisk effekt av SSRI och SNRI eller, möjligen, ett läkemedelsavbrottssyndrom. Det bör noteras att den kliniska bilden i vissa fall överensstämmer med serotonergt syndrom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Data
Mänskliga data
Exponering för SSRI, särskilt senare under graviditeten, kan öka risken för PPHN. PPHN förekommer hos 1-2 av 1000 levande födda i den allmänna populationen och är associerat med betydande neonatal sjuklighet och mortalitet.
Djurdata
en utvecklingsstudie på råtta embryo/foster resulterade oral administrering av escitalopram (56, 112 eller 150 mg/kg/dag) till dräktiga djur under organogenesperioden i minskad fostrets kroppsvikt och tillhörande förseningar i förbening vid de två högre doserna [ungefär ≥ 55 gånger den maximala rekommenderade humandosen (MRHD) på 20 mg/dag på mg/m2-basis]. Maternell toxicitet (kliniska tecken och minskad kroppsviktsökning och matkonsumtion), mild vid 56 mg/kg/dag, var närvarande vid alla dosnivåer. Utvecklingsdosen utan effekt på 56 mg/kg/dag är cirka 27 gånger MRHD på 20 mg på mg/m2-basis. Inga missbildningar observerades vid någon av de testade doserna (så höga som 73 gånger MRHD på mg/m2-basis).
När honråttor behandlades med escitalopram (6, 12, 24 eller 48 mg/kg/dag) under dräktighet och vid avvänjning, noterades något ökad avkommamortalitet och tillväxthämning vid 48 mg/kg/dag, vilket är ungefär 23 gånger högre än MRHD på 20 mg på mg/m2-basis. Lätt maternell toxicitet (kliniska tecken och minskad kroppsviktsökning och matkonsumtion) sågs vid denna dos. Något ökad avkommamortalitet sågs också vid 24 mg/kg/dag. Dosen utan effekt var 12 mg/kg/dag, vilket är ungefär 6 gånger MRHD på 20 mg på mg/m2-basis.
två studier på utvecklingen av embryo/foster på råtta, resulterade oral administrering av racemiskt citalopram (32, 56 eller 112 mg/kg/dag) till dräktiga djur under organogenesperioden i minskad embryo/fostertillväxt och överlevnad och en ökad förekomst av foster. abnormiteter (inklusive kardiovaskulära och skelettdefekter) vid den höga dosen, som är cirka 18 gånger MRHD på 60 mg/dag på mg/m2-basis. Denna dos var också associerad med maternell toxicitet (kliniska tecken, minskad kroppsviktsökning). Utvecklingsdosen utan effekt var 56 mg/kg/dag är cirka 9 gånger MRHD på mg/m2-basis. I en kaninstudie observerades inga negativa effekter på embryo-/fosterutveckling vid doser av racemiskt citalopram på upp till 16 mg/kg/dag, eller cirka 5 gånger MRHD på mg/m2-basis. Således observerades utvecklingseffekter av racemiskt citalopram vid en maternellt toxisk dos hos råtta och observerades inte hos kanin.
När honråttor behandlades med racemiskt citalopram (4,8, 12,8 eller 32 mg/kg/dag) från sen dräktighet till avvänjning, observerades ökad avkommamortalitet under de första 4 dagarna efter födseln och ihållande avkommans tillväxthämning vid den högsta dosen, vilket är cirka 5 gånger MRHD på 60 mg på mg/m2-basis. Dosen utan effekt var 12,8 mg/kg/dag är cirka 2 gånger MRHD på mg/m2-basis. Liknande effekter på avkommans dödlighet och tillväxt sågs när moderdjur behandlades under hela dräktigheten och tidig laktation med doser ≥ 24 mg/kg/dag, cirka 4 gånger MRHD på mg/m2-basis. En dos utan effekt fastställdes inte i den studien.
Laktation
Risksammanfattning
Data från den publicerade litteraturen rapporterar förekomsten av escitalopram och desmetylescitalopram i bröstmjölk (se Data ). Det finns rapporter om överdriven sedering, rastlöshet, agitation, dålig matning och dålig viktökning hos spädbarn som exponerats för escitalopram via bröstmjölk (se Kliniska överväganden ),. Det finns inga data om effekterna av escitalopram eller dess metaboliter på mjölkproduktionen. De utvecklingsmässiga och hälsomässiga fördelarna med amning bör beaktas tillsammans med moderns kliniska behov av LEXAPRO 5 mg och eventuella negativa effekter på det ammade barnet från LEXAPRO eller från det underliggande moderns tillståndet.
Kliniska överväganden
Spädbarn som exponerats för LEXAPRO 20 mg bör övervakas för överdriven sedering, rastlöshet, agitation, dålig mat och dålig viktökning.
Data
En studie av 8 ammande mödrar på escitalopram med dagliga doser på 10-20 mg/dag visade att enbart ammade spädbarn får cirka 3,9 % av moderns viktjusterade dos av escitalopram och 1,7 % av moderns viktjusterade dos av desmetylcitalopram .
Pediatrisk användning
Säkerheten och effektiviteten av Lexapro 10 mg har fastställts hos ungdomar (12 till 17 år) för behandling av egentlig depression [se Kliniska studier ]. Även om underhållseffekten hos ungdomar med egentlig depression inte har utvärderats systematiskt, kan underhållseffekten extrapoleras från vuxendata tillsammans med jämförelser av escitaloprams farmakokinetiska parametrar hos vuxna och ungdomar.
Säkerheten och effektiviteten av Lexapro har inte fastställts hos pediatriska (yngre än 12 års ålder) patienter med egentlig depression. I en 24 veckor lång, öppen säkerhetsstudie på 118 barn (i åldern 7 till 11 år) som hade allvarlig depressiv sjukdom, överensstämde säkerhetsfynden med den kända säkerhets- och tolerabilitetsprofilen för Lexapro.
Säkerhet och effektivitet för Lexapro har inte fastställts hos pediatriska patienter yngre än 18 år med generaliserat ångestsyndrom.
Minskad aptit och viktminskning har observerats i samband med användning av SSRI. Följaktligen bör regelbunden övervakning av vikt och tillväxt utföras hos barn och ungdomar som behandlas med ett SSRI såsom Lexapro.
Geriatrisk användning
Ungefär 6 % av de 1144 patienter som fick escitalopram i kontrollerade studier med Lexapro 10 mg vid egentlig depression och GAD var 60 år eller äldre; äldre patienter i dessa studier fick dagliga doser av Lexapro mellan 10 och 20 mg. Antalet äldre patienter i dessa prövningar var otillräckligt för att adekvat bedöma möjliga skillnader i effekt och säkerhetsåtgärder på grundval av ålder. Ändå kan en större känslighet hos vissa äldre individer för effekter av Lexapro inte uteslutas.
SSRI och SNRI, inklusive Lexapro 5mg, har associerats med fall av kliniskt signifikant hyponatremi hos äldre patienter, som kan löpa större risk för denna biverkning [se Hyponatremi ].
två farmakokinetiska studier ökade escitaloprams halveringstid med cirka 50 % hos äldre försökspersoner jämfört med unga försökspersoner och Cmax var oförändrat [se KLINISK FARMAKOLOGI ]. 10 mg/dag är den rekommenderade dosen för äldre patienter [se DOSERING OCH ADMINISTRERING ].
Av 4422 patienter i kliniska studier av racemiskt citalopram var 1357 60 och över, 1034 var 65 och över och 457 var 75 och över. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre försökspersoner, och annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter, men återigen, större känslighet hos vissa äldre individer kan inte uteslutas.
ÖVERDOS
Följande har rapporterats vid överdosering av Lexapro tabletter:
- Kramper, som kan vara försenade, och förändrad mental status inklusive koma.
- Kardiovaskulär toxicitet, som kan vara fördröjd, inklusive QRS- och QTc-intervallförlängning, omfattande komplexa takyarytmier och torsade de pointes. Hypertoni ses vanligast, men kan sällan se hypotoni ensam eller tillsammans med alkohol.
- Serotonergt syndrom (patienter med en överdosering av flera läkemedel med andra proserotonerga läkemedel kan ha en högre risk).
Långvarig hjärtövervakning rekommenderas vid intag av överdosering av Lexapro på grund av risken för arytmier.
Gastrointestinal dekontaminering med aktivt kol bör övervägas hos patienter som uppträder tidigt efter en överdos av Lexapro.
Överväg att kontakta ett giftcenter (1-800-221-2222) eller en medicinsk toxikolog för rekommendationer för överdosering.
KONTRAINDIKATIONER
Monoaminoxidashämmare (MAO-hämmare)
Användning av MAO-hämmare avsedda att behandla psykiatriska störningar med Lexapro eller inom 14 dagar efter avslutad behandling med Lexapro 5 mg är kontraindicerat på grund av en ökad risk för serotonergt syndrom. Användning av Lexapro 20 mg inom 14 dagar efter avslutad MAO-hämmare avsedd att behandla psykiatriska störningar är också kontraindicerat [se DOSERING OCH ADMINISTRERING , och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Att börja med Lexapro 20 mg hos en patient som behandlas med MAO-hämmare som linezolid eller intravenös metylenblått är också kontraindicerat på grund av en ökad risk för serotonergt syndrom [se DOSERING OCH ADMINISTRERING , och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Pimozide
Samtidig användning hos patienter som tar pimozid är kontraindicerad [se LÄKEMEDELSINTERAKTIONER ].
Överkänslighet mot Escitalopram eller Citalopram
Lexapro 20mg är kontraindicerat för patienter med överkänslighet mot escitalopram eller citalopram eller någon av de inaktiva ingredienserna i Lexapro.
KLINISK FARMAKOLOGI
Handlingsmekanism
Mekanismen för antidepressiv verkan av escitalopram, S-enantiomeren av racemiskt citalopram, antas vara kopplad till förstärkning av serotonerg aktivitet i det centrala nervsystemet (CNS) till följd av dess hämning av CNS-neuronalt återupptag av serotonin (5-HT).
Farmakodynamik
In vitro- och in vivo-studier på djur tyder på att escitalopram är en mycket selektiv serotoninåterupptagshämmare (SSRI) med minimal effekt på noradrenalin och neuronalt återupptag av dopamin. Escitalopram är minst 100 gånger mer potent än R-enantiomeren med avseende på hämning av 5-HT-återupptag och hämning av 5-HT-neuronavfyrningshastighet. Tolerans mot en modell av antidepressiv effekt hos råttor inducerades inte av långtidsbehandling (upp till 5 veckor) med escitalopram. Escitalopram har ingen eller mycket låg affinitet för serotonerga (5-HT1-7) eller andra receptorer inklusive alfa- och beta-adrenerga, dopamin (D1-5), histamin (H1-3), muskarin (M1-5) och bensodiazepin receptorer. Escitalopram binder inte heller till, eller har låg affinitet för, olika jonkanaler inklusive Na+, K+, Cl- och Ca++ kanaler. Antagonism av muskarina, histaminerga och adrenerga receptorer har antagits vara associerad med olika antikolinerga, sedativa och kardiovaskulära biverkningar av andra psykotropa läkemedel.
Farmakokinetik
Escitaloprams farmakokinetik för enkel- och flerdos är linjär och dosproportionell i ett dosintervall på 10 till 30 mg/dag. Biotransformation av escitalopram är huvudsakligen lever, med en genomsnittlig terminal halveringstid på cirka 27-32 timmar. Med dosering en gång dagligen uppnås steady state plasmakoncentrationer inom cirka en vecka. Vid steady state var graden av ackumulering av escitalopram i plasma hos unga friska försökspersoner 2,2-2,5 gånger de plasmakoncentrationer som observerades efter en engångsdos. Tabletten och doseringsformerna för oral lösning av escitalopramoxalat är bioekvivalenta.
Absorption och distribution
Efter en oral engångsdos (20 mg tablett eller lösning) av escitalopram uppnås toppnivåer i blodet efter cirka 5 timmar. Absorptionen av escitalopram påverkas inte av mat.
Den absoluta biotillgängligheten för citalopram är cirka 80 % i förhållande till en intravenös dos, och distributionsvolymen för citalopram är cirka 12 L/kg. Specifika data för escitalopram är inte tillgängliga.
Bindningen av escitalopram till humana plasmaproteiner är cirka 56 %.
Metabolism och eliminering
Efter oral administrering av escitalopram är andelen läkemedel som återvinns i urinen som escitalopram och S-demetylcitalopram (S-DCT) cirka 8 % respektive 10 %. Det orala clearance av escitalopram är 600 ml/min, varav cirka 7 % beror på renalt clearance.
Escitalopram metaboliseras till S-DCT och S-didemetylcitalopram (S-DDCT). Hos människor är oförändrad escitalopram den dominerande föreningen i plasma. Vid steady state är koncentrationen av escitaloprammetaboliten S-DCT i plasma ungefär en tredjedel av escitaloprams. Nivån av S-DDCT var inte detekterbar i de flesta försökspersoner. In vitro-studier visar att escitalopram är minst 7 och 27 gånger mer potent än S-DCT respektive S-DDCT i hämningen av serotoninåterupptag, vilket tyder på att metaboliterna av escitalopram inte bidrar signifikant till de antidepressiva effekterna av escitalopram. S-DCT och SDDCT har också ingen eller mycket låg affinitet för serotonerga (5-HT1-7) eller andra receptorer inklusive alfa- och beta-adrenerga, dopamin (D1-5), histamin (H1-3), muskarin (M1- 5), och bensodiazepinreceptorer. S-DCT och S-DDCT binder inte heller till olika jonkanaler inklusive Na+, K+, Cl- och Ca++ kanaler.
In vitro-studier med humana levermikrosomer visade att CYP3A4 och CYP2C19 är de primära isozymerna som är involverade i N-demetyleringen av escitalopram.
Populationsundergrupper
Ålder
Tonåringar
I en singeldosstudie med 10 mg escitalopram minskade AUC för escitalopram med 19 % och Cmax ökade med 26 % hos friska ungdomar (12 till 17 år) jämfört med vuxna. Efter upprepad dosering av 40 mg/dag citalopram, var escitaloprams eliminationshalveringstid, steady-state Cmax och AUC liknande hos patienter med MDD (12 till 17 år) jämfört med vuxna patienter. Ingen dosjustering behövs hos ungdomar.
Äldre
Escitaloprams farmakokinetik hos försökspersoner ≥ 65 år jämfördes med yngre försökspersoner i en endos- och en multipeldosstudie. Escitalopram AUC och halveringstid ökade med cirka 50 % hos äldre försökspersoner och Cmax var oförändrat. 10 mg är den rekommenderade dosen för äldre patienter [se DOSERING OCH ADMINISTRERING ].
Kön
Baserat på data från engångs- och flerdosstudier som mäter escitalopram hos äldre, unga vuxna och ungdomar, behövs ingen dosjustering på grundval av kön.
Nedsatt leverfunktion
Citaloprams orala clearance minskade med 37 % och halveringstiden fördubblades hos patienter med nedsatt leverfunktion jämfört med normala försökspersoner. 10 mg är den rekommenderade dosen av escitalopram för de flesta patienter med nedsatt leverfunktion [se DOSERING OCH ADMINISTRERING ].
Nedsatt njurfunktion
Hos patienter med lätt till måttligt nedsatt njurfunktion minskade oralt clearance av citalopram med 17 % jämfört med normala försökspersoner. Ingen dosjustering rekommenderas för sådana patienter. Ingen information finns tillgänglig om farmakokinetiken för escitalopram hos patienter med kraftigt nedsatt njurfunktion (kreatininclearance
Läkemedelsinteraktioner
In vitro-enzymhämningsdata avslöjade ingen hämmande effekt av escitalopram på CYP3A4, -1A2, -2C9, -2C19 och -2E1. Baserat på in vitro-data skulle escitalopram förväntas ha liten hämmande effekt på in vivo-metabolism medierad av dessa cytokromer. Även om in vivo-data för att lösa denna fråga är begränsade, tyder resultat från läkemedelsinteraktionsstudier på att escitalopram, i en dos på 20 mg, inte har någon 3A4-hämmande effekt och en blygsam 2D6-hämmande effekt. Ser LÄKEMEDELSINTERAKTIONER för mer detaljerad information om tillgängliga läkemedelsinteraktionsdata.
Djurtoxikologi och/eller farmakologi
Näthinneförändringar hos råttor
Patologiska förändringar (degeneration/atrofi) observerades i näthinnan hos albinoråttor i den 2-åriga karcinogenicitetsstudien med racemiskt citalopram. Det fanns en ökning av både incidensen och svårighetsgraden av retinal patologi hos både han- och honråttor som fick 80 mg/kg/dag. Liknande fynd fanns inte hos råttor som fick 24 mg/kg/dag av racemiskt citalopram under två år, hos möss som fick upp till 240 mg/kg/dag av racemiskt citalopram under 18 månader, eller hos hundar som fick upp till 20 mg/kg/ dag av racemiskt citalopram i ett år.
Ytterligare studier för att undersöka mekanismen för denna patologi har inte utförts, och den potentiella betydelsen av denna effekt hos människor har inte fastställts.
Kardiovaskulära förändringar hos hundar
en ettårig toxikologisk studie dog 5 av 10 beaglehundar som fick orala racemiska citalopramdoser på 8 mg/kg/dag plötsligt mellan veckorna 17 och 31 efter påbörjad behandling. Plötsliga dödsfall observerades inte hos råttor vid doser av racemiskt citalopram upp till 120 mg/kg/dag, vilket gav plasmanivåer av citalopram och dess metaboliter demetylcitalopram och didemetylcitalopram (DDCT) liknande de som observerats hos hundar vid 8 mg/kg/dag. En efterföljande intravenös doseringsstudie visade att racemisk DDCT hos beaglehundar orsakade QT-förlängning, en känd riskfaktor för det observerade resultatet hos hundar.
Kliniska studier
Major depressiv sjukdom
Tonåringar
Effekten av Lexapro som en akut behandling av egentlig depression hos tonårspatienter fastställdes i en 8 veckor lång, flexibel dos, placebokontrollerad studie som jämförde Lexapro 10-20 mg/dag med placebo hos öppenvårdspatienter i åldern 12 till 17 år. inklusive som uppfyllde DSM-IV-kriterierna för egentlig depression. Det primära resultatet var förändring från baslinje till effektmått i Children's Depression Rating Scale - Revised (CDRS-R). I denna studie visade Lexapro 5mg en statistiskt signifikant större genomsnittlig förbättring jämfört med placebo på CDRS-R.
Effekten av Lexapro vid akut behandling av egentlig depression hos ungdomar fastställdes delvis på basis av extrapolering från den 8 veckor långa placebokontrollerade studien med flexibla doser med racemisk citalopram 20-40 mg/dag. I denna polikliniska studie på barn och ungdomar i åldern 7 till 17 år som uppfyllde DSM-IV-kriterierna för allvarlig depressiv sjukdom, visade citaloprambehandling statistiskt signifikant större genomsnittlig förbättring från baslinjen, jämfört med placebo, på CDRS-R; de positiva resultaten för denna studie kom till stor del från ungdomsundergruppen.
Ytterligare två placebokontrollerade MDD-studier med flexibel dos (en Lexapro-studie på patienter i åldrarna 7 till 17 och en citalopram-studie på ungdomar) visade inte effekt.
Även om underhållseffekten hos ungdomar inte har utvärderats systematiskt, kan underhållseffekten extrapoleras från vuxendata tillsammans med jämförelser av escitaloprams farmakokinetiska parametrar hos vuxna och ungdomar.
Vuxna
Effekten av Lexapro 5mg som behandling för egentlig depression fastställdes i tre, 8-veckors, placebokontrollerade studier utförda på öppenvårdspatienter mellan 18 och 65 år som uppfyllde DSM-IV-kriterierna för egentlig depression. Det primära resultatet i alla tre studierna var förändring från baslinje till effektmått i Montgomery Asberg Depression Rating Scale (MADRS).
En studie med fast dos jämförde 10 mg/dag Lexapro och 20 mg/dag Lexapro med placebo och 40 mg/dag citalopram. Behandlingsgrupperna med 10 mg/dag och 20 mg/dag Lexapro 5 mg visade statistiskt signifikant större genomsnittlig förbättring jämfört med placebo på MADRS. 10 mg och 20 mg Lexapro-grupperna var likartade i detta resultatmått.
I en andra studie med fast dos av 10 mg/dag Lexapro och placebo, visade 10 mg/dag Lexapro-behandlingsgruppen statistiskt signifikant större medelförbättring jämfört med placebo på MADRS.
en studie med flexibel dos, som jämförde Lexapro 20 mg, titrerad mellan 10 och 20 mg/dag, med placebo och citalopram, titrerad mellan 20 och 40 mg/dag, visade Lexapro 5 mg-behandlingsgruppen statistiskt signifikant större genomsnittlig förbättring jämfört med placebo på MADRS.
Analyser av sambandet mellan behandlingsresultat och ålder, kön och ras antydde inte någon differentiell respons på basis av dessa patientegenskaper.
I en långtidsstudie randomiserades 274 patienter som uppfyllde (DSM-IV) kriterier för allvarlig depressiv sjukdom, som hade svarat under en första 8 veckors öppen behandlingsfas med Lexapro 10 eller 20 mg/dag, till fortsatt behandling med Lexapro i samma dos, eller placebo, under upp till 36 veckors observation för återfall. Svar under den öppna fasen definierades genom att ha en minskning av MADRS totalpoäng till ≤ 12. Återfall under den dubbelblinda fasen definierades som en ökning av MADRS totalpoäng till ≥ 22, eller utsättning på grund av otillräckligt kliniskt svar . Patienter som fick fortsatt Lexapro fick en statistiskt signifikant längre tid till återfall jämfört med de som fick placebo.
Generaliserat ångestsyndrom
Effekten av Lexapro 5 mg vid akut behandling av generaliserat ångestsyndrom (GAD) visades i tre, 8-veckors, multicenter, flexibla doser, placebokontrollerade studier som jämförde Lexapro 10-20 mg/dag med placebo hos vuxna öppenvårdspatienter mellan kl. 18 och 80 år som uppfyllde DSM-IV-kriterierna för GAD. I alla tre studierna visade Lexapro en statistiskt signifikant större medelförbättring jämfört med placebo på Hamilton Anxiety Scale (HAM-A).
Det fanns för få patienter i olika etniska grupper och åldersgrupper för att kunna bedöma om Lexapro har olika effekter i dessa grupper eller inte. Det fanns ingen skillnad i svaret på Lexapro mellan män och kvinnor.
PATIENTINFORMATION
Lexapro® (leks-a-pro) (escitalopram) Tabletter/oral lösning
Läs medicinguiden som följer med Lexapro innan du börjar ta den och varje gång du får en påfyllning. Det kan komma ny information. Denna medicineringsguide ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling. Prata med din vårdgivare om det är något du inte förstår eller vill veta mer om.
Vilken är den viktigaste informationen jag borde veta om Lexapro 20mg?
Lexapro 10mg och andra antidepressiva läkemedel kan orsaka allvarliga biverkningar, inklusive:
Håll alla uppföljningsbesök hos din vårdgivare och ring mellan besöken om du är orolig för symtom.
Ring din vårdgivare omedelbart om du har något av följande symtom, eller ring 911 om en nödsituation, särskilt om de är nya, värre eller oroar dig:
Ring din vårdgivare omedelbart om du har något av följande symtom, eller ring 911 om en nödsituation. Lexapro kan förknippas med dessa allvarliga biverkningar:
Symtom hos män kan inkludera:
Symtom hos kvinnor kan inkludera:
Tala med din vårdgivare om du utvecklar några förändringar i din sexuella funktion eller om du har några frågor eller funderingar kring sexuella problem under behandling med Lexapro. Det kan finnas behandlingar som din vårdgivare kan föreslå.
- Lexapro 5mg och andra antidepressiva läkemedel kan öka självmordstankar eller -handlingar hos vissa barn, tonåringar eller unga vuxna inom de första månaderna av behandlingen eller när dosen ändras.
- Depression eller andra allvarliga psykiska sjukdomar är de viktigaste orsakerna till självmordstankar eller -handlingar.
- Se upp för dessa förändringar och ring din vårdgivare omedelbart om du märker:
- Nya eller plötsliga förändringar i humör, beteende, handlingar, tankar eller känslor, särskilt om det är allvarligt.
- Var särskilt uppmärksam på sådana förändringar när Lexapro 5 mg påbörjas eller när dosen ändras.
- försök att begå självmord
- agerar på farliga impulser
- agerar aggressivt eller våldsamt
- tankar om självmord eller att dö
- ny eller värre depression
- ny eller värre ångest eller panikattacker
- känner sig upprörd, rastlös, arg eller irriterad
- sömnproblem
- ökad aktivitet eller prata mer än vad som är normalt för dig
- andra ovanliga förändringar i beteende eller humör
- agitation, hallucinationer, koma eller andra förändringar i mental status
- koordinationsproblem eller muskelryckningar (överaktiva reflexer)
- snabba hjärtslag, högt eller lågt blodtryck
- svettningar eller feber
- illamående, kräkningar eller diarré
- muskelstelhet
- problem att andas
- svullnad i ansikte, tunga, ögon eller mun
- utslag, kliande nässelutslag eller blåsor, ensamma eller med feber eller ledvärk
- kraftigt ökad energi
- svåra sömnproblem
- racing tankar
- hänsynslöst beteende
- ovanligt storslagna idéer
- överdriven lycka eller irritabilitet
- prata mer eller snabbare än vanligt
- huvudvärk
- svaghet eller att känna sig ostadig
- förvirring, problem med att koncentrera sig eller tänka eller minnesproblem
Endast vissa människor är i riskzonen för dessa problem. Du kanske vill genomgå en synundersökning för att se om du är i riskzonen och få förebyggande behandling om du är det.
- ögonsmärta
- förändringar i synen
- svullnad eller rodnad i eller runt ögat
- Försenad utlösning eller oförmåga att få utlösning
- Minskad sexlust
- Problem att få eller behålla erektion
- Minskad sexlust
- Försenad orgasm eller oförmåga att få orgasm
Sluta inte med Lexapro utan att först prata med din läkare. Att stoppa Lexapro 5mg för snabbt kan orsaka allvarliga symtom inklusive:
- ångest, irritabilitet, högt eller lågt humör, rastlöshet eller förändringar i sömnvanor
- huvudvärk, svettning, illamående, yrsel
- elektriska stötar, skakningar, förvirring
Vad är Lexapro?
Lexapro 20mg är ett receptbelagt läkemedel som används för att behandla depression. Det är viktigt att prata med din vårdgivare om riskerna med att behandla depression och även riskerna med att inte behandla den. Du bör diskutera alla behandlingsval med din vårdgivare. Lexapro används också för att behandla:
- Major depressiv sjukdom (MDD)
- Generaliserat ångestsyndrom (GAD)
Prata med din vårdgivare om du inte tror att ditt tillstånd blir bättre med Lexapro-behandling.
Vem bör inte ta Lexapro 5mg?
Ta inte Lexapro 10 mg om du:
Personer som tar Lexapro 20 mg nära en MAO-hämmare kan ha allvarliga eller till och med livshotande biverkningar. Få medicinsk hjälp omedelbart om du har något av dessa symtom:
- är allergisk mot escitalopram eller citalopram eller något av innehållsämnena i Lexapro. Se slutet av denna medicinguide för en komplett lista över ingredienser i Lexapro.
- Ta en monoaminoxidashämmare (MAO-hämmare). Fråga din läkare eller apotekspersonal om du är osäker på om du tar en MAO-hämmare, inklusive linezolid.
- Ta inte en MAO-hämmare inom 2 veckor efter att du avslutat Lexapro 10mg om inte din läkare har ordinerat det
- Börja inte med Lexapro 20 mg om du slutat ta en MAO-hämmare under de senaste 2 veckorna såvida inte din läkare har beordrat det.
- hög feber
- okontrollerade muskelspasmer
- stela muskler
- snabba förändringar i hjärtfrekvens eller blodtryck
- förvirring
- förlust av medvetande (svimma)
- Ta inte Lexapro med Orap® (pimozid) eftersom att ta dessa två läkemedel tillsammans kan orsaka allvarliga hjärtproblem.
Vad ska jag berätta för min vårdgivare innan jag tar Lexapro 20mg? Fråga om du är osäker.
Innan du börjar med Lexapro 20mg, berätta för din läkare om du:
- Tar vissa droger som:
- Triptaner används för att behandla migränhuvudvärk
- Läkemedel som används för att behandla humör, ångest, psykotiska störningar eller tankestörningar, inklusive tricykliska läkemedel, litium, SSRI, SNRI, amfetamin eller antipsykotika
- Tramadol
- Receptfria kosttillskott som tryptofan eller johannesört
- har leverproblem
- har njurproblem
- har hjärtproblem
- har eller haft kramper eller kramper
- har bipolär sjukdom eller mani
- har låga natriumnivåer i ditt blod
- har en historia av stroke
- har högt blodtryck
- har eller haft blödningsproblem
- är gravid eller planerar att bli gravid. Att ta LEXAPRO sent under graviditeten kan leda till en ökad risk för vissa problem hos din nyfödda. Prata med din vårdgivare om fördelarna och riskerna med att behandla depression under graviditeten
- Om du blir gravid medan du tar LEXAPRO, prata med din vårdgivare om att registrera dig hos National Pregnancy Registry for Antidepressants. Du kan registrera dig genom att ringa 1-844-405-6185 eller gå till https://womensmentalhealth.org/clinicaland- researchprograms/ pregnancyregistry/antidepressants/
- ammar eller planerar att amma. Lexapro kan passera över i din bröstmjölk. Prata med din vårdgivare om det bästa sättet att mata ditt barn om du tar Lexapro.
Berätta för din vårdgivare om alla läkemedel du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Lexapro 10mg och vissa läkemedel kan interagera med varandra, kanske inte fungera lika bra eller kan orsaka allvarliga biverkningar.
Din vårdgivare eller apotekspersonal kan berätta för dig om det är säkert att ta Lexapro 20 mg tillsammans med dina andra läkemedel. Starta eller sluta inte med någon medicin medan du tar Lexapro 10 mg utan att först prata med din läkare.
Om du tar Lexapro ska du inte ta några andra läkemedel som innehåller escitalopram eller citalopram inklusive: Celexa.
Hur ska jag ta Lexapro?
- Ta Lexapro precis som ordinerats. Din vårdgivare kan behöva ändra dosen av Lexapro tills det är rätt dos för dig.
- Lexapro 5 mg kan tas med eller utan mat.
- Om du missar en dos av Lexapro, ta den missade dosen så snart du kommer ihåg det. Om det nästan är dags för nästa dos, hoppa över den missade dosen och ta din nästa dos vid ordinarie tidpunkt. Ta inte två doser av Lexapro samtidigt.
- Om du tar för mycket Lexapro, ring din vårdgivare eller giftcentral direkt eller få akut behandling.
Vad ska jag undvika när jag tar Lexapro?
Lexapro 5mg kan orsaka sömnighet eller kan påverka din förmåga att fatta beslut, tänka klart eller reagera snabbt. Du bör inte köra bil, använda tunga maskiner eller göra andra farliga aktiviteter förrän du vet hur Lexapro påverkar dig. Drick inte alkohol när du använder Lexapro.
Vilka är de möjliga biverkningarna av Lexapro 20mg?
Lexapro 10mg kan orsaka allvarliga biverkningar, inklusive alla av de som beskrivs i avsnittet "Vilken är den viktigaste informationen jag borde veta om Lexapro?"
Vanliga möjliga biverkningar hos personer som tar Lexapro 5mg inkluderar:
- Illamående
- Sömnighet
- Svaghet
- Yrsel
- Känner mig orolig
- Sömnproblem
- Sexuella problem
- Svettas
- Skakning
- Känner mig inte hungrig
- Torr mun
- Förstoppning
- Infektion
- Gapande
Andra biverkningar hos barn och ungdomar inkluderar:
- ökad törst
- onormal ökning av muskelrörelser eller agitation
- näsblod
- svår urinering
- kraftiga menstruationer
- eventuellt minskad tillväxthastighet och viktförändring. Ditt barns längd och vikt bör övervakas under behandling med Lexapro.
Berätta för din vårdgivare om du har någon biverkning som stör dig eller som inte försvinner. Dessa är inte alla möjliga biverkningar av Lexapro. För mer information, fråga din vårdgivare eller apotekspersonal.
RING DIN LÄKARE FÖR MEDICINSK RÅD OM BIVERKNINGAR. DU KAN RAPPORTERA BIVERKNINGAR TILL FDA PÅ 1-800-FDA-1088.
Hur ska jag förvara Lexapro 20mg?
- Förvara Lexapro vid 68°F till 77°F (20°C till 25°C); utflykter tillåtna till 59°F till 86°F (15°C till 30°C).
- Håll Lexapro-flaskan tätt stängd.
Förvara Lexapro 10mg och alla läkemedel utom räckhåll för barn.
Allmän information om Lexapro
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte Lexapro för ett tillstånd som det inte har ordinerats för. Ge inte Lexapro 10 mg till andra personer, även om de har samma tillstånd. Det kan skada dem.
Denna medicinguide sammanfattar den viktigaste informationen om Lexapro. Om du vill ha mer information, prata med din vårdgivare. Du kan be din vårdgivare eller apotekspersonal om information om Lexapro som är skriven för vårdpersonal.
För mer information om Lexapro 20mg ring 1-800-678-1605 eller gå till www.Lexapro.com.
Vilka är ingredienserna i Lexapro 20mg?
Aktiv ingrediens: escitalopramoxalat Inaktiva ingredienser:
- talk, kroskarmellosnatrium, mikrokristallin cellulosa/kolloidal kiseldioxid och magnesiumstearat. Filmbeläggningen innehåller hypromellos, titandioxid och polyetylenglykol.
- Oral lösning: sorbitol, renat vatten, citronsyra, natriumcitrat, äppelsyra, glycerin, propylenglykol, metylparaben, propylparaben och naturlig pepparmintsmak (oral lösning marknadsförs för närvarande inte).
Denna medicineringsguide har godkänts av US Food and Drug Administration.
