Naprelan 250mg, 500mg Naproxen Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Naprelan och hur används det?
Naprelan är ett receptbelagt läkemedel som används för att behandla symptomen på reumatoid artrit, artros, ankylosinspondylit, dysmenorré, akut gikt och smärta. Naprelan kan användas ensamt eller tillsammans med andra läkemedel.
Naprelan tillhör en klass av läkemedel som kallas NSAID.
Det är inte känt om Naprelan 250 mg är säkert och effektivt för barn yngre än 2 år.
Vilka är de möjliga biverkningarna av Naprelan 500mg?
Naprelan kan orsaka allvarliga biverkningar inklusive:
- nässelfeber,
- svårt att andas,
- svullnad av ansikte, läppar, tunga eller svalg,
- lätt att få blåmärken eller blödningar,
- svår eller smärtsam sväljning,
- ringer i öronen,
- humörförändringar,
- förändringar i mängden urin,
- oförklarlig stel nacke,
- synförändringar,
- svullnad av anklar och fötter,
- ovanlig trötthet,
- ovanlig och plötslig viktökning,
- mörk urin,
- ihållande illamående eller kräkningar,
- aptitlöshet,
- buksmärtor,
- gulfärgning av ögon eller hud (gulsot), och
- svår yrsel
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Naprelan inkluderar:
- orolig mage,
- illamående,
- halsbränna,
- huvudvärk,
- förhöjt blodtryck
- dåsighet och
- yrsel
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Naprelan. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
RISK FÖR ALLVARLIGA HJÄRT- OCH Gastrointestinala HÄNDELSER
Kardiovaskulära trombotiska händelser
- Icke-steroida antiinflammatoriska läkemedel (NSAID) orsakar en ökad risk för allvarliga kardiovaskulära trombotiska händelser, inklusive hjärtinfarkt och stroke, som kan vara dödlig. Denna risk kan uppstå tidigt i behandlingen och kan öka med användningstiden [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
- NAPRELAN är kontraindicerat vid kranskärlsbypassoperationer (CABG) [se KONTRAINDIKATIONER och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
Gastrointestinal blödning, sårbildning och perforering
- NSAID orsakar en ökad risk för allvarliga gastrointestinala (GI) biverkningar inklusive blödning, sårbildning och perforering av magen eller tarmarna, vilket kan vara dödligt. Dessa händelser kan inträffa när som helst under användning och utan varningssymptom. Äldre patienter och patienter med en anamnes på magsår och/eller GI-blödning löper större risk för allvarliga GI-händelser [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
BESKRIVNING
NAPRELAN (naproxennatrium) tabletter med kontrollerad frisättning är ett icke-steroid antiinflammatoriskt läkemedel, tillgängligt som tabletter med kontrollerad frisättning i styrkorna 375 mg, 500 mg och 750 mg för oral administrering. Det kemiska namnet är 2-naftalenättiksyra, 6-metoxi-α-metyl-natriumsalt, (S)-. Molekylvikten är 252,24. Dess molekylformel är C14H13NaO3, och den har följande kemiska struktur.
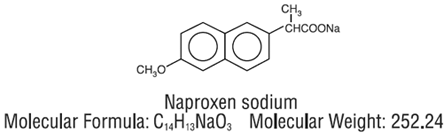
Naproxennatrium är ett luktfritt kristallint pulver, vit till krämig till färgen. Det är lösligt i metanol och vatten. NAPRELAN 250 mg tabletter innehåller 412,5 mg, 550 mg eller 825 mg naproxennatrium, motsvarande 375 mg, 500 mg och 750 mg naproxen och 37,5 mg, 50 mg respektive 75 mg natrium. Varje NAPRELAN 250 mg tablett innehåller även följande inaktiva ingredienser: ammoniometakrylatsampolymer typ A, ammoniometakrylatsampolymer typ B, citronsyra, krospovidon, magnesiumstearat, metakrylsyrasampolymer typ A, mikrokristallin cellulosa, povidon och talk. Tablettbeläggningen innehåller hydroxipropylmetylcellulosa, polyetylenglykol och titandioxid.
INDIKATIONER
NAPRELAN 250 mg tabletter är indicerade för behandling av:
- reumatoid artrit (RA)
- artros (OA)
- ankyloserande spondylit (AS)
- tendinit, bursit
- akut gikt
- primär dysmenorré (PD)
- lindring av mild till måttlig smärta
 [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
DOSERING OCH ADMINISTRERING
Allmänna doseringsanvisningar
Överväg noga de potentiella fördelarna och riskerna med NAPRELAN och andra behandlingsalternativ innan du bestämmer dig för att använda NAPRELAN. Använd den lägsta effektiva dosen för den kortaste varaktigheten förenlig med individuella patientbehandlingsmål [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Efter att ha observerat svaret på initial behandling med NAPRELAN, bör dosen och frekvensen justeras för att passa en individuell patients behov.
Reumatoid artrit, artros och ankyloserande spondylit
Den rekommenderade startdosen av NAPRELAN tabletter för vuxna är två NAPRELAN 375 mg tabletter (750 mg) en gång dagligen, en NAPRELAN 750 mg (750 mg) en gång dagligen eller två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen. Patienter som redan tar naproxen 250 mg, 375 mg eller 500 mg två gånger dagligen (morgon och kväll) kan få sin totala dagliga dos ersatt med NAPRELAN 500 mg tabletter som en enstaka daglig dos.
Under långtidsadministrering kan dosen av NAPRELAN 250 mg tabletter justeras upp eller ner beroende på patientens kliniska svar. Hos patienter som tolererar lägre doser av NAPRELAN tabletter väl, kan dosen ökas till två NAPRELAN 750 mg tabletter (1 500 mg) eller tre NAPRELAN 500 mg tabletter (1 500 mg) en gång dagligen under begränsade perioder när en högre nivå av antiinflammatorisk effekt. /analgetisk aktivitet krävs. Vid behandling av patienter, särskilt vid högre dosnivåer, bör läkaren observera tillräcklig ökad klinisk nytta för att kompensera för den potentiella ökade risken [se KLINISK FARMAKOLOGI ]. Den lägsta effektiva dosen bör eftersträvas och användas till varje patient. Symtomatisk förbättring av artrit börjar vanligtvis inom en vecka; behandling i två veckor kan dock krävas för att uppnå en terapeutisk fördel.
Hantering av smärta, primär dysmenorré och akut tendinit och bursit
Den rekommenderade startdosen är två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen. För patienter som behöver större analgetisk nytta kan två NAPRELAN 750 mg tabletter (1 500 mg) eller tre NAPRELAN 500 mg tabletter (1 500 mg) användas under en begränsad period. Därefter bör den totala dagliga dosen inte överstiga två NAPRELAN 500 mg tabletter (1 000 mg).
Akut gikt
Den rekommenderade dosen den första dagen är två till tre NAPRELAN 500 mg tabletter (1 000 till 1 500 mg) en gång dagligen, följt av två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen, tills attacken har avtagit.
Dosjusteringar hos patienter med nedsatt leverfunktion
En lägre dos bör övervägas hos patienter med nedsatt njur- eller leverfunktion eller hos äldre patienter [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Studier indikerar att även om den totala plasmakoncentrationen av naproxen är oförändrad, ökar den obundna plasmafraktionen av naproxen hos äldre. Försiktighet tillråds när höga doser krävs och viss dosjustering kan behövas hos äldre patienter. Som med andra läkemedel som används till äldre är det klokt att använda den lägsta effektiva dosen.
HUR LEVERERAS
Doseringsformer och styrkor
NAPRELAN (naproxennatrium) tabletter med kontrollerad frisättning finns tillgängliga enligt följande:
- NAPRELAN 375: vit, kapselformad tablett med ”N” på ena sidan och ”375” på baksidan. Varje tablett innehåller 412,5 mg naproxennatrium motsvarande 375 mg naproxen.
- NAPRELAN 500: vit, kapselformad tablett med ”N” på ena sidan och ”500” på baksidan. Varje tablett innehåller 550 mg naproxennatrium motsvarande 500 mg naproxen.
- NAPRELAN 750: vit, kapselformad tablett med ”N” på ena sidan och ”750” på baksidan. Varje tablett innehåller 825 mg naproxennatrium motsvarande 750 mg naproxen.
Förvaring Och Hantering
NAPRELAN (naproxennatrium) 375 mg, 500 mg och 750 mg är tabletter med kontrollerad frisättning som levereras som:
NAPRELAN 375 : vit, kapselformad tablett med ”N” på ena sidan och ”375” på baksidan; i flaskor om 100; NDC 52427-272-01. Varje tablett innehåller 412,5 mg naproxennatrium motsvarande 375 mg naproxen.
NAPRELAN 500 : vit, kapselformad tablett med ”N” på ena sidan och ”500” på baksidan; i flaskor om 75; NDC 52427-273-75. Varje tablett innehåller 550 mg naproxennatrium motsvarande 500 mg naproxen.
NAPRELAN 750 : vit, kapselformad tablett med ”N” på ena sidan och ”750” på baksidan; i flaskor om 30; NDC 52427-274-30. Varje tablett innehåller 825 mg naproxennatrium motsvarande 750 mg naproxen.
Lagring
Förvara i rumstemperatur, 20° till 25°C (68° till 77°F), utflykter tillåtna 15° till 30°C (59° till 86°F) [se USP kontrollerad rumstemperatur]. Apoteker: Fördela i en väl tillsluten behållare.
Distribueras av: Almatica Pharma, Inc. Morristown, NJ 07960 USA. Reviderad: april 2021
BIEFFEKTER
Följande biverkningar diskuteras mer i detalj i andra avsnitt av märkningen:
- Kardiovaskulära trombotiska händelser [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- GI-blödning, sårbildning och perforering [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hepatotoxicitet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypertoni [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hjärtsvikt och ödem [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Njurtoxicitet och hyperkalemi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Anafylaktiska reaktioner [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Allvarliga hudreaktioner [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hematologisk toxicitet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Som med alla läkemedel i denna klass beror frekvensen och svårighetsgraden av biverkningar på flera faktorer: läkemedlets dos och behandlingens varaktighet; patientens ålder, kön, fysiska tillstånd; eventuella samtidiga medicinska diagnoser eller individuella riskfaktorer. Följande biverkningar är indelade i tre delar baserat på frekvens och huruvida möjligheten finns för ett orsakssamband mellan läkemedelsanvändning och dessa biverkningar. I de reaktioner som anges som "troligt orsakssamband" finns det minst ett fall för varje biverkning där det finns bevis som tyder på att det finns ett orsakssamband mellan droganvändning och den rapporterade händelsen. De rapporterade biverkningarna baserades på resultaten från två dubbelblinda kontrollerade kliniska prövningar på tre månader med ytterligare nio månaders öppen förlängning. Totalt 542 patienter fick NAPRELAN-tabletter antingen i den dubbelblinda perioden eller i den nio månaders öppna förlängningen. Av dessa 542 patienter fick 232 NAPRELAN-tabletter, 167 behandlades initialt med Naprosyn® och 143 behandlades initialt med placebo. Biverkningar som rapporterats av patienter som fått NAPRELAN 500 mg tabletter visas per kroppssystem. De biverkningar som observerats med naproxen men som inte rapporterats i kontrollerade studier med NAPRELAN tabletter är kursiverade.
De vanligaste biverkningarna från de dubbelblinda och öppna kliniska prövningarna var huvudvärk (15 %), följt av dyspepsi (14 %) och influensasyndrom (10 %). Incidensen av andra biverkningar som inträffar hos 3 % till 9 % av patienterna är markerade med en asterisk.
De reaktioner som förekommer hos mindre än 3 % av patienterna är omärkta.
Incidens större än 1 % (troligt orsakssamband)
Kroppen som helhet - Smärta (rygg)*, smärta*, infektion*, feber, skada (olycka), asteni, smärta i bröstet, huvudvärk (15%), influensasyndrom (10%).
Gastrointestinala - Illamående*, diarré*, förstoppning*, buksmärtor*, flatulens, gastrit, kräkningar, dysfagi, dyspepsi (14%), halsbränna*, stomatit.
Hematologiska - Anemi, ekkymos.
Andningsorgan - Faryngit*, rinit*, bihåleinflammation*, bronkit, ökad hosta.
Renal - Urinvägsinfektion*, cystit.
Dermatologiska - Hudutslag*, hudutslag*, ekkymos*, purpura.
Metabolism och nutrition - Perifert ödem, hyperglykemi.
Centrala nervsystemet - Yrsel, parestesi, sömnlöshet, dåsighet*, yrsel.
Kardiovaskulär - Hypertoni, ödem*, dyspné*, hjärtklappning.
Muskuloskeletala - Kramper (ben), myalgi, artralgi, ledsjukdom, sensjukdom.
Särskilda sinnen - Tinnitus*, hörselstörningar, synstörningar.
Allmänt - Törst.
Incidens Mindre än 1 % (troligt orsakssamband)
Kroppen som helhet - Böld, monilia, nacken stel, smärta i nacken, buken förstorad, karcinom, cellulit, ödem allmänt, LE-syndrom, sjukdomskänsla, slemhinnor, allergisk reaktion, smärta i bäckenet.
Gastrointestinala - Anorexi, kolecystit, kolelithiasis, utslag, GI-blödning, rektalblödning, stomatit aftös, stomatit sår, sår i munnen, magsår, parodontala abscess, kardiospasm, kolit, esofagit, gastroenterit, GI-funktion, livospat, GI abnormitet, melena, sår i matstrupen, hematemes, gulsot, pankreatit, nekros.
Renal - Dysmenorré, dysuri, njurfunktionsavvikelse, natturi, prostatasjukdom, pyelonefrit, bröstkarcinom, urininkontinens, njursten, njursvikt, menorragi, metrorragi, neoplasmabröst, nefroskleros, urinavvikelse, urinfrekvens, urinsmärta, urinfrekvens, normal smärta retention, livmoderspasm, vaginit, glomerulär nefrit, hyperkalemi, interstitiell nefrit, nefrotiskt syndrom, njursjukdom, njursvikt, njurpapillär nekros.
Hematologiska - Leukopeni, ökad blödningstid, eosinofili, onormal RBC, onormal WBC, trombocytopeni, agranulocytos, granulocytopeni.
Centrala nervsystemet - Depression, ångest, hypertoni, nervositet, neuralgi, neurit, yrsel, minnesförlust, förvirring, koordination, onormal dubbelsidighet, emotionell labilitet, hematom subdural, förlamning, drömavvikelser, oförmåga att koncentrera sig, muskelsvaghet.
Dermatologiska: Angiodermatit, herpes simplex, torr hud, svettning, hudsår, akne, alopeci, dermatitkontakt, eksem, herpes zoster, nagelstörning, hudnekros, subkutan knöl, klåda, urtikaria, neoplasmahud, ljuskänslig dermatit, ljuskänslighetsreaktioner som liknar tarporfyri , epidermolysis bullosa.
Särskilda sinnen - Amblyopi, sklerit, grå starr, konjunktivit, döva, öronsjukdom, keratokonjunktivit, tårbildningsstörning, otitis media, smärta i ögat.
Kardiovaskulär - Angina pectoris, kranskärlssjukdom, hjärtinfarkt, djup tromboflebit, vasodilatation, vaskulär anomali, arytmi, grenblock, onormalt EKG, hjärtsvikt höger, blödning, migrän, aortastenos, synkope, takykardi, kongestiv hjärtsvikt.
Andningsorgan - Astma, dyspné, lungödem, laryngit, lungsjukdom, näsblod, lunginflammation, andnöd, andningsstörning, eosinofil pneumonit.
Muskuloskeletala - Myasteni, benstörning, spontan benfraktur, fibrotendinit, skelettsmärta, ptos, allmän spasm, bursit.
Metabolism och nutrition - Kreatininökning, glukosuri, hyperkolesteremi, albuminuri, alkalos, BUN ökad, uttorkning, ödem, sänkning av glukostolerans, hyperurikemi, hypokalemi, SGOT-ökning, SGPT-ökning, viktminskning.
Allmänt - Anafylaktoida reaktioner, angioneurotiskt ödem, menstruationsrubbningar, hypoglykemi, pyrexi (frossa och feber).
Incidens Mindre än 1 % (orsakssamband okänt)
Andra biverkningar listade på naproxenförpackningens etikett, men som inte rapporterats av dem som fått NAPRELAN-tabletter, visas i kursiv stil. Dessa observationer listas som varningsinformation till läkaren.
Hematologiska - Aplastisk anemi, hemolytisk anemi.
Centrala nervsystemet - Aseptisk meningit, kognitiv dysfunktion.
Dermatologiska - Epidermal nekrolys, erythema multiforme, Stevens-Johnsons syndrom.
Gastrointestinala - Icke-peptisk GI-ulceration, ulcerös stomatit.
Kardiovaskulär - Vaskulit.
LÄKEMEDELSINTERAKTIONER
Se tabell 1 för kliniskt signifikanta läkemedelsinteraktioner med naproxen.
Interaktioner med läkemedel/laboratorietest
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Kardiovaskulära trombotiska händelser
Kliniska prövningar av flera COX-2 selektiva och icke-selektiva NSAID med upp till tre års varaktighet har visat en ökad risk för allvarliga kardiovaskulära (CV) trombotiska händelser, inklusive hjärtinfarkt (MI) och stroke, som kan vara dödlig. Baserat på tillgängliga data är det oklart att risken för CV-trombotiska händelser är liknande för alla NSAID. Den relativa ökningen av allvarliga CV-trombotiska händelser jämfört med baslinjen till följd av NSAID-användning tycks vara liknande hos de med och utan känd CV-sjukdom eller riskfaktorer för CV-sjukdom. Patienter med känd CV-sjukdom eller riskfaktorer hade dock en högre absolut incidens av alltför allvarliga CV-trombotiska händelser, på grund av deras ökade baslinjefrekvens. Vissa observationsstudier fann att denna ökade risk för allvarliga CV-trombotiska händelser började redan under de första veckorna av behandlingen. Ökningen av CV-trombotisk risk har observerats mest konsekvent vid högre doser.
För att minimera den potentiella risken för en negativ CV-händelse hos NSAID-behandlade patienter, använd den lägsta effektiva dosen under kortast möjliga varaktighet. Läkare och patienter bör vara uppmärksamma på utvecklingen av sådana händelser, under hela behandlingsförloppet, även i frånvaro av tidigare CV-symtom. Patienter bör informeras om symtomen på allvarliga CV-händelser och de åtgärder som ska vidtas om de inträffar.
Det finns inga konsekventa bevis för att samtidig användning av aspirin minskar den ökade risken för allvarliga CV-trombotiska händelser i samband med NSAID-användning. Samtidig användning av aspirin och ett NSAID, såsom naproxen, ökar risken för allvarliga gastrointestinala (GI) händelser [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Status efter kranskärlsbypassoperation (CABG).
Två stora, kontrollerade kliniska prövningar av ett COX-2 selektivt NSAID för behandling av smärta under de första 10–14 dagarna efter CABG-operation fann en ökad incidens av hjärtinfarkt och stroke. NSAID är kontraindicerade vid CABG [se KONTRAINDIKATIONER ].
Patienter efter MI
Observationsstudier utförda i det danska nationella registret har visat att patienter som behandlats med NSAID under perioden efter MI löpte ökad risk för reinfarkt, CV-relaterad död och dödlighet av alla orsaker med början under den första behandlingsveckan. I samma kohort var incidensen av dödsfall under det första året efter MI 20 per 100 personår hos NSAID-behandlade patienter jämfört med 12 per 100 personår hos icke-NSAID-exponerade patienter. Även om den absoluta dödsfrekvensen minskade något efter det första året efter MI, kvarstod den ökade relativa risken för död hos NSAID-användare under åtminstone de kommande fyra åren av uppföljning.
Undvik användningen av NAPRELAN 250 mg till patienter med nyligen hjärtinfarkt såvida inte fördelarna förväntas uppväga risken för återkommande CV-trombotiska händelser. Om NAPRELAN används till patienter med nyligen hjärtinfarkt, övervaka patienterna för tecken på hjärtischemi.
Gastrointestinal blödning, sårbildning och perforering
NSAID, inklusive naproxen, orsakar allvarliga gastrointestinala (GI) biverkningar inklusive inflammation, blödning, sårbildning och perforering av matstrupen, magen, tunntarmen eller tjocktarmen, vilket kan vara dödligt. Dessa allvarliga biverkningar kan inträffa när som helst, med eller utan varningssymtom, hos patienter som behandlas med NSAID. Endast en av fem patienter som utvecklar en allvarlig övre GI-biverkning på NSAID-behandling är symtomatisk. Övre gastrointestinala sår, grov blödning eller perforation orsakad av NSAID förekom hos cirka 1 % av patienterna som behandlades under 3 till 6 månader och hos cirka 2 % till 4 % av patienterna som behandlades under ett år. Men även kortvarig NSAID-behandling är inte utan risk.
Riskfaktorer för GI-blödning, sårbildning och perforering
Patienter med magsår i anamnesen och/eller gastrointestinala blödningar som använde NSAID hade en mer än 10 gånger ökad risk för att utveckla en gastrointestinala blödning jämfört med patienter utan dessa riskfaktorer. Andra faktorer som ökar risken för GI-blödning hos patienter som behandlas med NSAID inkluderar längre varaktighet av NSAID-behandling; samtidig användning av orala kortikosteroider, aspirin, antikoagulantia eller selektiva serotoninåterupptagshämmare (SSRI); rökning; användning av alkohol; äldre ålder; och dåligt allmänt hälsotillstånd. De flesta rapporter om dödliga gastrointestinala händelser efter marknadsföring inträffade hos äldre eller försvagade patienter. Dessutom löper patienter med avancerad leversjukdom och/eller koagulopati en ökad risk för GI-blödning.
Strategier för att minimera GI-riskerna hos NSAID-behandlade patienter
- Använd den lägsta effektiva dosen under kortast möjliga varaktighet.
- Undvik administrering av mer än ett NSAID åt gången.
- Undvik användning till patienter med högre risk om inte fördelarna förväntas uppväga den ökade risken för blödning. För sådana patienter, såväl som de med aktiv GI-blödning, överväg alternativa terapier än NSAID.
- Var uppmärksam på tecken och symtom på magsår och blödning under NSAID-behandling.
- Om en allvarlig GI-biverkning misstänks, initiera omedelbart utvärdering och behandling och avbryt NAPRELAN 250 mg tills en allvarlig GI-biverkning är utesluten.
- Vid samtidig användning av lågdos acetylsalicylsyra för hjärtprofylax, övervaka patienterna noggrannare för tecken på GI-blödning [se LÄKEMEDELSINTERAKTIONER ].
Hepatotoxicitet
Förhöjningar av ALAT eller ASAT (tre eller fler gånger den övre normalgränsen [ULN]) har rapporterats hos cirka 1 % av NSAID-behandlade patienter i kliniska prövningar. Dessutom har sällsynta, ibland dödliga, fall av allvarlig leverskada, inklusive fulminant hepatit, levernekros och leversvikt rapporterats.
Förhöjningar av ALAT eller ASAT (mindre än tre gånger ULN) kan förekomma hos upp till 15 % av patienterna som behandlas med NSAID inklusive naproxen.
Informera patienterna om varningstecken och symtom på levertoxicitet (t.ex. illamående, trötthet, letargi, diarré, klåda, gulsot, ömhet i den övre högra kvadranten och "influensaliknande" symtom). Om kliniska tecken och symtom som överensstämmer med leversjukdom utvecklas, eller om systemiska manifestationer uppstår (t.ex. eosinofili, hudutslag, etc.), avbryt NAPRELAN 500 mg omedelbart och utför en klinisk utvärdering av patienten.
Hypertoni
NSAID, inklusive NAPRELAN, kan leda till nystart eller försämring av redan existerande hypertoni, vilka båda kan bidra till den ökade incidensen av CV-händelser. Patienter som tar angiotensinomvandlande enzym (ACE)-hämmare, tiaziddiuretika eller loopdiuretika kan ha försämrat svar på dessa behandlingar när de tar NSAID [se LÄKEMEDELSINTERAKTIONER ].
Övervaka blodtrycket (BP) under inledning av NSAID-behandling och under hela behandlingen.
Hjärtsvikt och ödem
Coxib och traditionella NSAID Trialists' Collaboration-metaanalys av randomiserade kontrollerade studier visade en ungefär tvåfaldig ökning av sjukhusvistelser för hjärtsvikt hos COX-2 selektivt behandlade patienter och icke-selektiva NSAID-behandlade patienter jämfört med placebobehandlade patienter. I en dansk National Register-studie av patienter med hjärtsvikt ökade NSAID-användning risken för hjärtinfarkt, sjukhusvistelse för hjärtsvikt och död.
Dessutom har vätskeretention och ödem observerats hos vissa patienter som behandlats med NSAID. Användning av naproxen kan dämpa CV-effekterna av flera terapeutiska medel som används för att behandla dessa medicinska tillstånd (t.ex. diuretika, ACE-hämmare eller angiotensinreceptorblockerare [ARB]) [se LÄKEMEDELSINTERAKTIONER ].
Undvik användning av NAPRELAN 250 mg till patienter med svår hjärtsvikt om inte fördelarna förväntas uppväga risken för förvärrad hjärtsvikt. Om NAPRELAN används till patienter med allvarlig hjärtsvikt, övervaka patienterna för tecken på förvärrad hjärtsvikt.
Njurtoxicitet och hyperkalemi
Njurtoxicitet
Långvarig administrering av NSAID har resulterat i njurpapillär nekros och annan njurskada.
Njurtoxicitet har också setts hos patienter hos vilka njurprostaglandiner har en kompensatorisk roll i upprätthållandet av njurperfusion. Hos dessa patienter kan administrering av ett NSAID orsaka en dosberoende minskning av prostaglandinbildningen och, i andra hand, i njurblodflödet, vilket kan utlösa tydlig njurdekompensation. Patienter med störst risk för denna reaktion är de med nedsatt njurfunktion, uttorkning, hypovolemi, hjärtsvikt, leverdysfunktion, de som tar diuretika och ACE-hämmare eller ARB och äldre. Avbrytande av NSAID-behandling följs vanligtvis av återhämtning till förbehandlingstillstånd.
Ingen information finns tillgänglig från kontrollerade kliniska studier angående användning av NAPRELAN hos patienter med avancerad njursjukdom. Njureffekterna av NAPRELAN 250 mg kan påskynda utvecklingen av njurdysfunktion hos patienter med redan existerande njursjukdom.
Korrigera volymstatus hos dehydrerade eller hypovolemiska patienter innan NAPRELAN påbörjas. Övervaka njurfunktionen hos patienter med nedsatt njur- eller leverfunktion, hjärtsvikt, uttorkning eller hypovolemi under användning av NAPRELAN [se LÄKEMEDELSINTERAKTIONER ]. Undvik användning av NAPRELAN 500 mg till patienter med avancerad njursjukdom såvida inte fördelarna förväntas uppväga risken för försämrad njurfunktion. Om NAPRELAN används till patienter med avancerad njursjukdom, övervaka patienterna för tecken på försämrad njurfunktion.
Hyperkalemi
Ökning av serumkaliumkoncentrationen, inklusive hyperkalemi, har rapporterats vid användning av NSAID, även hos vissa patienter utan nedsatt njurfunktion. Hos patienter med normal njurfunktion har dessa effekter tillskrivits ett tillstånd av hyporeninemisk-hypoaldosteronism.
Anafylaktiska reaktioner
Naproxen har associerats med anafylaktiska reaktioner hos patienter med och utan känd överkänslighet mot naproxen och hos patienter med aspirinkänslig astma [se KONTRAINDIKATIONER och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Sök akut hjälp om en anafylaktisk reaktion inträffar.
Förvärring av astma relaterad till aspirinkänslighet
En subpopulation av patienter med astma kan ha aspirinkänslig astma som kan innefatta kronisk rhinosinusit komplicerad av näspolyper; allvarlig, potentiellt dödlig bronkospasm; och/eller intolerans mot aspirin och andra NSAID. Eftersom korsreaktivitet mellan acetylsalicylsyra och andra NSAID har rapporterats hos sådana aspirinkänsliga patienter, är NAPRELAN 250 mg kontraindicerat hos patienter med denna form av acetylsalicylsyrakänslighet [se KONTRAINDIKATIONER ]. När NAPRELAN används till patienter med redan existerande astma (utan känd acetylsalicylsyrakänslighet), övervaka patienterna med avseende på förändringar i tecken och symtom på astma.
Allvarliga hudreaktioner
NSAID, inklusive naproxen, kan orsaka allvarliga hudbiverkningar som exfoliativ dermatit, Stevens-Johnsons syndrom (SJS) och toxisk epidermal nekrolys (TEN), som kan vara dödlig. Dessa allvarliga händelser kan inträffa utan förvarning. Informera patienter om tecken och symtom på allvarliga hudreaktioner och att avbryta användningen av NAPRELAN 500 mg vid första uppkomsten av hudutslag eller andra tecken på överkänslighet.
NAPRELAN är kontraindicerat hos patienter med tidigare allvarliga hudreaktioner på NSAID [se KONTRAINDIKATIONER ].
Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS)
Läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) har rapporterats hos patienter som tar NSAID såsom NAPRELAN. Några av dessa händelser har varit dödliga eller livshotande. DRESS ger vanligtvis, men inte uteslutande, feber, hudutslag, lymfadenopati och/eller svullnad i ansiktet. Andra kliniska manifestationer kan inkludera hepatit, nefrit, hematologiska abnormiteter, myokardit eller myosit. Ibland kan symtom på DRESS likna en akut virusinfektion. Eosinofili är ofta närvarande. Eftersom denna störning är variabel i sin presentation, kan andra organsystem som inte noteras här vara inblandade. Det är viktigt att notera att tidiga manifestationer av överkänslighet, såsom feber eller lymfadenopati, kan förekomma även om utslag inte är uppenbara. Om sådana tecken eller symtom finns, avbryt NAPRELAN och utvärdera patienten omedelbart.
Fostertoxicitet
För tidig stängning av Fetal Ductus Arteriosus
Undvik användning av NSAID, inklusive NAPRELAN, hos gravida kvinnor vid cirka 30 veckors graviditet och senare. NSAID, inklusive NAPRELAN, ökar risken för för tidig stängning av fetal ductus arteriosus vid ungefär denna graviditetsålder.
Oligohydramnios/neonatal njurfunktionsnedsättning
Användning av NSAID, inklusive NAPRELAN 500 mg, vid cirka 20 veckors graviditet eller senare under graviditeten kan orsaka fosterns njurfunktion som leder till oligohydramnios och i vissa fall neonatal njurfunktionsnedsättning. Dessa negativa utfall ses i genomsnitt efter dagar till veckors behandling, även om oligohydramnios sällan har rapporterats så snart som 48 timmar efter NSAID-start. Oligohydramnios är ofta, men inte alltid, reversibel när behandlingen avbryts. Komplikationer av långvariga oligohydramnios kan till exempel inkludera lemkontrakturer och försenad lungmognad. I vissa fall av nedsatt neonatal njurfunktion efter marknadsföringen krävdes invasiva procedurer såsom utbytestransfusion eller dialys.
Om NSAID-behandling är nödvändig mellan cirka 20 veckor och 30 veckors graviditet, begränsa användningen av NAPRELAN 500 mg till lägsta effektiva dos och kortast möjliga varaktighet. Överväg ultraljudsövervakning av fostervatten om behandlingen med NAPRELAN sträcker sig längre än 48 timmar. Avbryt NAPRELAN om oligohydramnios uppstår och följ upp enligt klinisk praxis [se Användning i specifika populationer ].
Hematologisk toxicitet
Anemi har förekommit hos NSAID-behandlade patienter. Detta kan bero på ockult eller grov blodförlust, vätskeretention eller en ofullständigt beskriven effekt på erytropoes. Om en patient som behandlas med NAPRELAN 500 mg har några tecken eller symtom på anemi, övervaka hemoglobin eller hematokrit.
NSAID, inklusive NAPRELAN, kan öka risken för blödningar. Samorbida tillstånd som koagulationsrubbningar, samtidig användning av warfarin, andra antikoagulantia, trombocythämmande medel (t.ex. aspirin), serotoninåterupptagshämmare (SSRI) och serotonin noradrenalinåterupptagshämmare (SNRI) kan öka denna risk. Övervaka dessa patienter för tecken på blödning [se LÄKEMEDELSINTERAKTIONER ].
Maskering av inflammation och feber
Den farmakologiska aktiviteten av NAPRELAN 250 mg för att minska inflammation och eventuellt feber kan minska användbarheten av diagnostiska tecken för att upptäcka infektioner.
Laboratorieövervakning
Eftersom allvarlig GI-blödning, levertoxicitet och njurskada kan uppstå utan varningssymtom eller tecken, överväg att övervaka patienter på långvarig NSAID-behandling med en CBC och en kemiprofil regelbundet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide ) som medföljer varje utskrivet recept. Informera patienter, familjer eller deras vårdgivare om följande information innan behandling med NAPRELAN 500 mg påbörjas och med jämna mellanrum under pågående behandling.
Kardiovaskulära trombotiska händelser
Rekommendera patienter att vara uppmärksamma på symtom på kardiovaskulära trombotiska händelser, inklusive bröstsmärtor, andnöd, svaghet eller sluddrigt tal, och att omedelbart rapportera något av dessa symtom till sin vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Gastrointestinal blödning, sårbildning och perforering
NAPRELAN 500mg, liksom andra NSAID, kan orsaka GI-besvär och, sällan, allvarliga GI-biverkningar, såsom sår och blödningar, vilket kan leda till sjukhusvistelse och till och med dödsfall. Råda patienter att rapportera symtom på sår och blödningar, inklusive epigastrisk smärta, dyspepsi, melena och hematemes till sin vårdgivare. Vid samtidig användning av lågdos aspirin för hjärtprofylax, informera patienterna om den ökade risken för och tecknen och symtomen på gastrointestinala blödningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hepatotoxicitet
Informera patienterna om varningstecken och symtom på levertoxicitet (t.ex. illamående, trötthet, letargi, klåda, diarré, gulsot, ömhet i den övre högra kvadranten och "influensaliknande" symtom). Om dessa inträffar, instruera patienterna att sluta med NAPRELAN och omedelbart söka medicinsk behandling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hjärtsvikt och ödem
Rekommendera patienter att vara uppmärksamma på symtom på kronisk hjärtsvikt inklusive andnöd, oförklarlig viktökning eller ödem och att kontakta sin vårdgivare om sådana symtom uppstår [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Anafylaktiska reaktioner
Informera patienterna om tecknen på en anafylaktisk reaktion (t.ex. andningssvårigheter, svullnad i ansikte eller hals). Instruera patienter att söka omedelbar akut hjälp om dessa inträffar [se KONTRAINDIKATIONER och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Allvarliga hudreaktioner, inklusive KLÄNNING
NAPRELAN 500mg, liksom andra NSAID, kan orsaka allvarliga hudbiverkningar som exfoliativ dermatit, SJS och TEN, vilket kan leda till sjukhusvistelse och till och med dödsfall. Råda patienter att sluta ta NAPRELAN omedelbart om de utvecklar någon typ av hudutslag eller feber och att kontakta sin vårdgivare så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kvinnlig fertilitet
Informera kvinnor med reproduktionspotential som önskar graviditet att NSAID, inklusive NAPRELAN 250 mg, kan vara associerade med en reversibel försening av ägglossningen [se Användning i specifika populationer ].
Fostertoxicitet
Informera gravida kvinnor att undvika användning av NAPRELAN 500 mg och andra NSAID-preparat från och med 30 veckors graviditet på grund av risken för för tidig stängning av fetal ductus arteriosus. Om behandling med NAPRELAN 500 mg behövs för en gravid kvinna mellan cirka 20 till 30 veckors graviditet, informera henne om att hon kan behöva övervakas för oligohydramnios, om behandlingen fortsätter längre än 48 timmar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Undvik samtidig användning av NSAID
Informera patienterna om att samtidig användning av NAPRELAN och andra NSAID eller salicylater (t.ex. diflunisal, salsalat) inte rekommenderas på grund av den ökade risken för gastrointestinal toxicitet och liten eller ingen ökning av effekt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och LÄKEMEDELSINTERAKTIONER ]. Varna patienter om att NSAID kan finnas i "receptfria" läkemedel för behandling av förkylningar, feber eller sömnlöshet.
Användning av NSAID och lågdos aspirin
Informera patienterna att inte använda lågdos acetylsalicylsyra samtidigt med NAPRELAN 250 mg tills de pratat med sin vårdgivare [se LÄKEMEDELSINTERAKTIONER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
En tvåårig studie utfördes på råttor för att utvärdera naproxens cancerframkallande potential vid doser på 8 mg/kg/dag, 16 mg/kg/dag och 24 mg/kg/dag (0,05, 0,1 och 0,16 gånger det maximala rekommenderade mänsklig daglig dos på 1 500 mg/dag baserat på en jämförelse av kroppsytan). Inga tecken på tumörframkallande egenskaper hittades.
Mutagenes
Studier för att utvärdera den mutagena potentialen hos Naprosyn Suspension har inte slutförts.
Nedsättning av fertilitet
Studier för att utvärdera effekten av naproxen på manlig eller kvinnlig fertilitet har inte slutförts.
Användning i specifika populationer
Graviditet
Risksammanfattning
Användning av NSAID, inklusive NAPRELAN 500 mg, kan orsaka för tidig stängning av fetal ductus arteriosus och fosterns njurfunktion som leder till oligohydramnios och, i vissa fall, neonatal njurfunktionsnedsättning. På grund av dessa risker, begränsa dosen och varaktigheten av NAPRELAN 500 mg mellan cirka 20 och 30 veckors graviditet, och undvik användning av NAPRELAN 500 mg vid cirka 30 veckors graviditet och senare under graviditeten (se Kliniska överväganden , Data ).
För tidig stängning av Fetal Ductus Arteriosus
Användning av NSAID, inklusive NAPRELAN 500 mg, vid cirka 30 veckors graviditet eller senare under graviditeten ökar risken för för tidig stängning av fostergången arteriosus.
Oligohydramnios/neonatal njurfunktionsnedsättning
Användning av NSAID vid ungefär 20 veckors graviditet eller senare under graviditeten har associerats med fall av fosterns njurfunktion som leder till oligohydramnios och i vissa fall neonatal njurfunktionsnedsättning.
Data från observationsstudier angående andra potentiella embryofetala risker med användning av NSAID hos kvinnor under graviditetens första eller andra trimester är inte övertygande. I reproduktionsstudier på djur på råttor, kaniner och möss inga tecken på teratogenicitet eller fosterskada när naproxen administrerades under organogenesperioden i doser 0,13, 0,26 respektive 0,6 gånger den maximala rekommenderade dagliga dosen för människor på 1 500 mg/dag. Baserat på djurdata har prostaglandiner visat sig ha en viktig roll i endometrievaskulär permeabilitet, blastocystimplantation och decidualisering. I djurstudier resulterade administrering av prostaglandinsynteshämmare såsom naproxen i ökad förlust före och efter implantation. Prostaglandiner har också visat sig ha en viktig roll i fostrets njurutveckling. I publicerade djurstudier har prostaglandinsynteshämmare rapporterats försämra njurutvecklingen när de administreras i kliniskt relevanta doser.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den eller de indikerade populationerna är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Kliniska överväganden
Fetala/neonatala biverkningar
För tidig stängning av Fetal Ductus Arteriosus: Undvik användning av NSAID hos kvinnor vid cirka 30 veckors graviditet och senare under graviditeten, eftersom NSAID, inklusive NAPRELAN, kan orsaka för tidig stängning av fetal ductus arteriosus (se Data ).
Oligohydramnios/neonatal njurfunktionsnedsättning: Om ett NSAID är nödvändigt vid ungefär 20 veckors graviditet eller senare under graviditeten, begränsa användningen till den lägsta effektiva dosen och kortast möjliga varaktighet. Om behandlingen med NAPRELAN 500 mg sträcker sig längre än 48 timmar, överväg att övervaka med ultraljud för oligohydramnios. Om oligohydramnios uppstår, avbryt behandlingen med NAPRELAN 500 mg och följ upp enligt klinisk praxis (se Data ).
Arbetskraft eller leverans
Det finns inga studier på effekterna av NAPRELAN 500mg under förlossningen eller förlossningen. I djurstudier hämmar NSAID, inklusive naproxennatrium, prostaglandinsyntesen, orsakar försenad förlossning, ökar förekomsten av dystoci och ökar förekomsten av dödfödsel.
Data
Mänskliga data
Det finns vissa bevis som tyder på att när hämmare av prostaglandinsyntes används för att fördröja för tidig förlossning, finns det en ökad risk för neonatala komplikationer såsom nekrotiserande enterokolit, patent ductus arteriosus och intrakraniell blödning. Naproxenbehandling som ges i slutet av graviditeten för att fördröja förlossningen har associerats med ihållande pulmonell hypertoni, njurdysfunktion och onormala prostaglandin E-nivåer hos för tidigt födda barn. På grund av den kända effekten av läkemedel av denna klass på det mänskliga fostrets kardiovaskulära system (stängning av ductus arteriosus), bör användning under tredje trimestern undvikas.
För tidig stängning av Fetal Ductus Arteriosus
Publicerad litteratur rapporterar att användning av NSAID vid cirka 30 veckors graviditet och senare i graviditeten kan orsaka för tidig stängning av fostergången arteriosus.
Oligohydramnios/neonatal njurfunktionsnedsättning
Publicerade studier och rapporter efter marknadsföring beskriver moderns NSAID-användning vid cirka 20 veckors graviditet eller senare under graviditeten i samband med fosterns njurfunktion som leder till oligohydramnios och i vissa fall neonatal njurfunktionsnedsättning. Dessa negativa utfall ses i genomsnitt efter dagar till veckors behandling, även om oligohydramnios sällan har rapporterats så snart som 48 timmar efter NSAID-start. I många fall, men inte alla, var minskningen av fostervatten övergående och reversibel när läkemedlet upphörde. Det har förekommit ett begränsat antal fallrapporter av maternell NSAID-användning och neonatal njurfunktion utan oligohydramnios, av vilka några var irreversibla. Vissa fall av neonatal njurdysfunktion krävde behandling med invasiva procedurer, såsom utbytestransfusion eller dialys.
Metodologiska begränsningar av dessa eftermarknadsföringsstudier och rapporter inkluderar bristen på en kontrollgrupp; begränsad information om dos, varaktighet och tidpunkt för läkemedelsexponering; och samtidig användning av andra läkemedel. Dessa begränsningar utesluter upprättande av en tillförlitlig uppskattning av risken för ogynnsamma foster- och neonatala utfall vid användning av moders NSAID. Eftersom de publicerade säkerhetsdata om neonatala resultat mestadels involverade prematura spädbarn, är generaliserbarheten av vissa rapporterade risker för fullgångna spädbarn som exponerats för NSAID genom modern användning osäker.
Djurdata
Reproduktionsstudier har utförts på råttor med 20 mg/kg/dag (0,13 gånger den maximala rekommenderade dagliga dosen för människor på 1 500 mg/dag baserat på jämförelse av kroppsytan) kaniner med 20 mg/kg/dag (0,26 gånger den maximala rekommenderade humana dosen) daglig dos, baserat på jämförelse av kroppsytan), och möss med 170 mg/kg/dag (0,6 gånger den maximala rekommenderade dagliga dosen för människor baserat på jämförelse av kroppsytan) utan tecken på nedsatt fertilitet eller skada på fostret på grund av läkemedel. Baserat på djurdata har prostaglandiner visat sig ha en viktig roll i endometrievaskulär permeabilitet, blastocystimplantation och decidualisering. I djurstudier resulterade administrering av prostaglandinsynteshämmare såsom naproxennatrium i ökad förlust före och efter implantation.
Laktation
Risksammanfattning
Naproxenanjonen har hittats i mjölken hos ammande kvinnor i en koncentration av cirka 1 % av den som finns i plasma. De utvecklingsmässiga och hälsomässiga fördelarna med amning bör beaktas tillsammans med moderns kliniska behov av NAPRELAN och eventuella negativa effekter på det ammade barnet från NAPRELAN eller från det underliggande moderns tillståndet.
Kvinnor Och Hanar Av Reproduktionspotential
Infertilitet
Kvinnor
Baserat på verkningsmekanismen kan användningen av prostaglandinmedierade NSAID, inklusive NAPRELAN, fördröja eller förhindra bristning av äggstocksfolliklar, vilket har associerats med reversibel infertilitet hos vissa kvinnor. Publicerade djurstudier har visat att administrering av prostaglandinsynteshämmare har potential att störa prostaglandinmedierad follikelruptur som krävs för ägglossning. Små studier på kvinnor som behandlats med NSAID har också visat en reversibel försening av ägglossningen. Överväg utsättande av NSAID, inklusive NAPRELAN 250 mg, hos kvinnor som har svårt att bli gravida eller som genomgår utredning av infertilitet.
Pediatrisk användning
Säkerheten och effektiviteten av NAPRELAN 500 mg i pediatriska populationer har inte fastställts.
Geriatrisk användning
Äldre patienter, jämfört med yngre patienter, löper större risk för NSAID-relaterade allvarliga kardiovaskulära, gastrointestinala och/eller renala biverkningar. Om den förväntade fördelen för den äldre patienten uppväger dessa potentiella risker, börja doseringen i den nedre delen av doseringsintervallet och övervaka patienterna för biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Naproxen och dess metaboliter är kända för att väsentligen utsöndras via njurarna, och risken för biverkningar av detta läkemedel kan vara större hos patienter med nedsatt njurfunktion. Eftersom äldre patienter är mer benägna att ha nedsatt njurfunktion, var försiktig i denna patientpopulation, och det kan vara användbart att övervaka njurfunktionen [se KLINISK FARMAKOLOGI ].
ÖVERDOS
Symtom efter akuta NSAID-överdoseringar har vanligtvis begränsats till slöhet, dåsighet, illamående, kräkningar och epigastrisk smärta, som i allmänhet har varit reversibla med stödbehandling. Gastrointestinal blödning har inträffat. Hypertoni, akut njursvikt, andningsdepression och koma har förekommit, men var sällsynta [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Ett fåtal patienter har upplevt anfall, men det är inte klart om dessa var drogrelaterade eller inte. Det är inte känt vilken dos av drogen som skulle vara livshotande.
Hantera patienter med symtomatisk och stödjande vård efter en överdosering av NSAID. Det finns inga specifika motgift. Hemodialys minskar inte plasmakoncentrationen av naproxen på grund av den höga graden av dess proteinbindning. Överväg kräkning och/eller aktivt kol (60 till 100 gram hos vuxna, 1 till 2 gram per kg kroppsvikt hos pediatriska patienter) och/eller osmotisk katartisk hos symtomatiska patienter som ses inom fyra timmar efter intag eller hos patienter med en stor överdosering ( 5 till 10 gånger den rekommenderade dosen). Påtvingad diures, alkalinisering av urin, hemodialys eller hemoperfusion kanske inte är användbara på grund av hög proteinbindning.
För ytterligare information om överdoseringsbehandling kontakta en giftkontrollcentral (1-800-222-1222).
KONTRAINDIKATIONER
NAPRELAN 500mg är kontraindicerat för följande patienter:
Känd överkänslighet (t.ex. anafylaktiska reaktioner och allvarliga hudreaktioner) mot naproxen eller någon del av läkemedelsprodukten [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Anamnes med astma, urtikaria eller andra reaktioner av allergisk typ efter att ha tagit acetylsalicylsyra eller andra NSAID. Allvarliga, ibland dödliga, anafylaktiska reaktioner på NSAID har rapporterats hos sådana patienter [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
samband med kranskärlsbypassoperation (CABG) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
KLINISK FARMAKOLOGI
Handlingsmekanism
Naproxen har smärtstillande, antiinflammatoriska och febernedsättande egenskaper.
Verkningsmekanismen för NAPRELAN, liksom andra NSAID, är inte helt klarlagd men involverar hämning av cyklooxygenas (COX-1 och COX-2).
Naproxennatrium är en potent hämmare av prostaglandinsyntes in vitro. Koncentrationer av natriumnaproxen som uppnåtts under behandlingen har gett in vivo-effekter. Prostaglandiner sensibiliserar afferenta nerver och potentierar verkan av bradykinin för att inducera smärta i djurmodeller.
Prostaglandiner är mediatorer av inflammation. Eftersom naproxennatrium är en hämmare av prostaglandinsyntes, kan dess verkningsmekanism bero på en minskning av prostaglandiner i perifera vävnader.
Farmakodynamik
en studie med friska frivilliga visade 10 dagars samtidig administrering av naproxen 220 mg en gång dagligen med lågdos acetylsalicylsyra med omedelbar frisättning (81 mg) en interaktion med den trombocythämmande aktiviteten hos aspirin mätt som % serumtromboxan B2-hämning efter 24 timmar efter dag 10-dosen [98,7 % (enbart acetylsalicylsyra) mot 93,1 % (naproxen och aspirin)]. Interaktionen observerades även efter utsättning av naproxen på dag 11 (medan aspirindosen fortsatte) men normaliserades till dag 13. I samma studie var interaktionen större när naproxen administrerades 30 minuter före aspirin [98,7% vs 87,7%] och minimal när acetylsalicylsyra administrerades 30 minuter före naproxen [98,7 % vs 95,4 %].
Efter administrering av naproxen 220 mg två gånger dagligen med lågdos acetylsalicylsyra med omedelbar frisättning (första dosen av naproxen gavs 30 minuter före aspirin), var interaktionen minimal 24 timmar efter dos dag 10 [98,7 % vs 95,7 %]. Interaktionen var dock mer framträdande efter utsättning av naproxen (uttvättning) på dag 11 [98,7 % vs 84,3 %] och normaliserades inte helt på dag 13 [98,5 % vs 90,7 %]. [ser LÄKEMEDELSINTERAKTIONER ].
Farmakokinetik
Även om naproxen självt absorberas väl, absorberas natriumsaltformen snabbare, vilket resulterar i högre maximala plasmanivåer för en given dos. Cirka 30 % av den totala naproxennatriumdosen i NAPRELAN 500 mg tabletter finns i doseringsformen som en komponent med omedelbar frisättning. Återstående naproxennatrium beläggs som mikropartiklar för att ge fördröjda frisättningsegenskaper. Efter oral administrering detekteras plasmanivåer av naproxen inom 30 minuter efter dosering, med maximala plasmanivåer cirka 5 timmar efter dosering. Den observerade terminala eliminationshalveringstiden för naproxen från både naproxennatrium med omedelbar frisättning och NAPRELAN-tabletter är cirka 15 timmar. Steady state-nivåer av naproxen uppnås på 3 dagar och graden av naproxenackumulering i blodet överensstämmer med detta.
Plasma Naproxen-koncentrationer Genomsnitt av 24 försökspersoner (+/-2SD) (Steady State, dag 5)
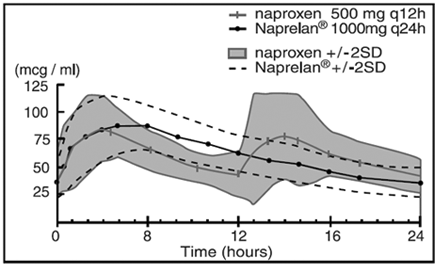
Farmakokinetiska parametrar vid steady state dag 5 (medelvärde av 24 försökspersoner)
Absorption
Naproxen i sig absorberas snabbt och fullständigt från mag-tarmkanalen med en biotillgänglighet in vivo på 95 %. Baserat på den farmakokinetiska profilen sker absorptionsfasen för NAPRELAN 250 mg tabletter under de första 4 till 6 timmarna efter administrering. Detta sammanfaller med sönderfall av tabletten i magen, transiteringen av mikropartiklarna med fördröjd frisättning genom tunntarmen och in i den proximala tjocktarmen. En in vivo avbildningsstudie har utförts på friska frivilliga som bekräftar snabb sönderdelning av tablettmatrisen och dispergering av mikropartiklarna.
Absorptionshastigheten från partikelkomponenten med fördröjd frisättning i NAPRELAN tabletter är långsammare än för konventionella naproxennatriumtabletter. Det är denna förlängning av läkemedelsabsorptionsprocesser som upprätthåller plasmanivåerna och möjliggör dosering en gång dagligen.
Mateffekter
Inga signifikanta födoeffekter observerades när tjugofyra försökspersoner fick en engångsdos av NAPRELAN 500 mg tabletter 500 mg antingen efter en natts fasta eller 30 minuter efter en måltid. I likhet med konventionella naproxen- och naproxennatriumformuleringar orsakar mat en lätt minskning av absorptionshastigheten för naproxen efter administrering av NAPRELAN 250 mg tabletter.
Distribution
Naproxen har en distributionsvolym på 0,16 l/kg. Vid terapeutiska nivåer är naproxen mer än 99 % albuminbundet. Vid doser av naproxen som är större än 500 mg/dag finns en mindre än proportionell ökning av plasmanivåerna på grund av en ökning av clearance orsakad av mättnad av plasmaproteinbindningen vid högre doser. Koncentrationen av obundet naproxen fortsätter dock att öka proportionellt mot dosen. NAPRELAN tabletter uppvisar liknande dosproportionella egenskaper.
Eliminering
Ämnesomsättning
Naproxen metaboliseras i stor utsträckning till 6-0-desmetylnaproxen och både förälder och metaboliter inducerar inte metaboliserande enzymer.
Exkretion
Elimineringshalveringstiden för NAPRELAN 500 mg tabletter och konventionella naproxen är cirka 15 timmar. Steady state-tillstånd uppnås efter 2 till 3 doser av NAPRELAN-tabletter. Det mesta av läkemedlet utsöndras i urinen, främst som oförändrad naproxen (mindre än 1%), 6-0-desmetylnaproxen (mindre än 1%) och deras glukuronid eller andra konjugat (66 till 92%). En liten mängd (
Specifika populationer
Pediatrisk
Inga pediatriska studier har utförts med NAPRELAN 500 mg tabletter, varför säkerheten för NAPRELAN 500 mg tabletter i pediatriska populationer inte har fastställts.
Nedsatt leverfunktion
Kronisk alkoholisk leversjukdom och troligen andra sjukdomar med minskade eller onormala plasmaproteiner (albumin) minskar den totala plasmakoncentrationen av naproxen, men plasmakoncentrationen av obundet naproxen ökar. Försiktighet tillråds när höga doser krävs och viss dosjustering kan behövas hos dessa patienter. Det är klokt att använda den lägsta effektiva dosen.
Nedsatt njurfunktion
Naproxens farmakokinetik har inte fastställts hos patienter med njurinsufficiens. Med tanke på att naproxen metaboliseras och konjugat primärt utsöndras via njurarna, finns det en potential för naproxenmetaboliter att ackumuleras i närvaro av njurinsufficiens. Eliminationen av naproxen minskar hos patienter med gravt nedsatt njurfunktion. Naproxen-innehållande produkter rekommenderas inte för användning till patienter med måttligt till svårt och gravt nedsatt njurfunktion (kreatininclearance VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Läkemedelsinteraktionsstudier
Aspirin
När NSAID administrerades med acetylsalicylsyra reducerades proteinbindningen av NSAID, även om clearance av fritt NSAID inte förändrades. Den kliniska betydelsen av denna interaktion är inte känd. Se tabell 1 för kliniskt signifikanta läkemedelsinteraktioner mellan NSAID och acetylsalicylsyra [se LÄKEMEDELSINTERAKTIONER ].
Kliniska studier
Reumatoid artrit
Användningen av NAPRELAN 500 mg tabletter för att hantera tecken och symtom på reumatoid artrit utvärderades i en 12 veckor lång dubbelblind, randomiserad, placebo- och aktivt kontrollerad studie på 348 patienter. Två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen och naproxen 500 mg tabletter två gånger dagligen (1 000 mg) var effektivare än placebo. Klinisk effektivitet visades efter en vecka och fortsatte under hela studien.
Artros
Användningen av NAPRELAN-tabletter för att hantera tecknen och symtomen på knäartros utvärderades i en 12 veckor lång dubbelblind, placebo- och aktivt kontrollerad studie på 347 patienter. Två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen och naproxen 500 mg tabletter två gånger dagligen (1 000 mg) var effektivare än placebo. Klinisk effektivitet visades efter en vecka och fortsatte under hela studien.
Analgesi
Debut av den smärtstillande effekten av NAPRELAN tabletter sågs inom 30 minuter i en farmakokinetisk/farmakodynamisk studie av patienter med smärta efter oral kirurgi. I kontrollerade kliniska prövningar har naproxen använts i kombination med guld, D-penicillamin, metotrexat och kortikosteroider. Dess användning i kombination med salicylat rekommenderas inte eftersom det finns bevis för att acetylsalicylsyra ökar utsöndringshastigheten av naproxen och data är otillräckliga för att visa att naproxen och acetylsalicylsyra ger en större förbättring jämfört med den som uppnås med enbart aspirin. Dessutom, som med andra NSAID-preparat, kan kombinationen resultera i högre frekvens av biverkningar än vad som visats för endera produkten ensam.
Specialstudier
en dubbelblind randomiserad parallellgruppsstudie fick 19 försökspersoner antingen två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen eller naproxen 500 mg tabletter (1 000 mg) två gånger dagligen i 7 dagar. Slemhinnebiopsipoäng och endoskopiska poäng var lägre hos försökspersonerna som fick NAPRELAN-tabletter. I en annan dubbelblind, randomiserad crossover-studie fick 23 försökspersoner två NAPRELAN 500 mg tabletter (1 000 mg) en gång dagligen, naproxen 500 mg tabletter (1 000 mg) två gånger dagligen och aspirin 650 mg fyra gånger dagligen (2 600 mg) i 7 dagar varje. Det sågs signifikant färre erosioner i tolvfingertarmen med NAPRELAN-tabletter än med antingen naproxen eller aspirin. Det var signifikant färre magerosioner med både NAPRELAN-tabletter och naproxen än med acetylsalicylsyra. Den kliniska betydelsen av dessa fynd är okänd.
PATIENTINFORMATION
Läkemedelsguide för icke-steroida antiinflammatoriska läkemedel (NSAID)
Vilken är den viktigaste informationen jag borde veta om läkemedel som kallas icke-steroida antiinflammatoriska läkemedel (NSAID)?
NSAID kan orsaka allvarliga biverkningar, inklusive:
- Ökad risk för hjärtinfarkt eller stroke som kan leda till döden. Denna risk kan inträffa tidigt i behandlingen och kan öka:
- med ökande doser av NSAID
- med längre användning av NSAID
Ta inte NSAID precis före eller efter en hjärtoperation som kallas "kransartär bypassgraft (CABG)." Undvik att ta NSAID efter en nyligen inträffad hjärtinfarkt, såvida inte din läkare säger åt dig att göra det. Du kan ha en ökad risk för en ny hjärtinfarkt om du tar NSAID-preparat efter en nyligen genomförd hjärtinfarkt.
- Ökad risk för blödningar, sår och revor (perforering) i matstrupen (slangen som leder från munnen till magen), magen och tarmarna:
- när som helst under användning
- utan varningssymtom
- som kan orsaka dödsfall
Risken för att få ett sår eller blödning ökar med:
- tidigare anamnes på magsår, eller blödning från magen eller tarmen vid användning av NSAID
- tar läkemedel som kallas "kortikosteroider", "antikoagulantia", "SSRI" eller "SNRI"
- ökande doser av NSAID
- äldre ålder
- längre användning av NSAID
- dålig hälsa
- rökning
- avancerad leversjukdom
- dricker alkohol
- blödningsproblem
NSAID bör endast användas:
- precis som föreskrivet
- vid lägsta möjliga dos för din behandling
- för den kortaste tiden som behövs
Vad är NSAID?
NSAID används för att behandla smärta och rodnad, svullnad och värme (inflammation) från medicinska tillstånd som olika typer av artrit, mensvärk och andra typer av kortvarig smärta.
Vem bör inte ta NSAID?
Ta inte NSAID:
- om du har haft en astmaanfall, nässelfeber eller annan allergisk reaktion med acetylsalicylsyra eller andra NSAID-preparat.
- precis före eller efter bypassoperation.
Innan du tar NSAID, berätta för din vårdgivare om alla dina medicinska tillstånd, inklusive om du:
- har lever- eller njurproblem
- har högt blodtryck
- har astma
- är gravid eller planerar att bli gravid. Om du tar NSAID vid ungefär 20 veckors graviditet eller senare kan det skada ditt ofödda barn. Om du behöver ta NSAID i mer än 2 dagar när du är mellan 20 och 30 veckor av graviditeten, kan din läkare behöva övervaka mängden vätska i livmodern runt ditt barn. Du ska inte ta NSAID efter ca 30 veckors graviditet.
- ammar eller planerar att amma.
Berätta för din vårdgivare om alla läkemedel du tar, inklusive receptbelagda eller receptfria läkemedel, vitaminer eller växtbaserade kosttillskott. NSAID och vissa andra läkemedel kan interagera med varandra och orsaka allvarliga biverkningar. Börja inte ta något nytt läkemedel utan att först prata med din läkare.
Vilka är de möjliga biverkningarna av NSAID?
NSAID kan orsaka allvarliga biverkningar, inklusive:
Se "Vilken är den viktigaste informationen jag bör veta om läkemedel som kallas icke-steroida antiinflammatoriska läkemedel (NSAID)?
- nytt eller värre högt blodtryck
- hjärtsvikt
- leverproblem inklusive leversvikt
- njurproblem inklusive njursvikt
- låga röda blodkroppar (anemi)
- livshotande hudreaktioner
- livshotande allergiska reaktioner
Andra biverkningar av NSAID inkluderar: magsmärtor, förstoppning, diarré, gaser, halsbränna, illamående, kräkningar och yrsel.
Få akut hjälp omedelbart om du får något av följande symtom:
- andnöd eller andningssvårigheter
- sluddrigt tal
- bröstsmärta
- svullnad i ansikte eller hals
- svaghet i en del eller sida av din kropp
Sluta ta ditt NSAID och ring din vårdgivare omedelbart om du får något av följande symtom:
- illamående
- spy blod
- tröttare eller svagare än vanligt
- det finns blod i din tarmrörelse eller så är det svart och klibbigt som tjära
- diarre
- klåda
- ovanlig viktökning
- din hud eller ögon ser gula ut
- hudutslag eller blåsor med feber
- matsmältningsbesvär eller magsmärtor
- svullnad av armar, ben, händer och fötter
- influensaliknande symtom
Om du tar för mycket av ditt NSAID, ring din vårdgivare eller få medicinsk hjälp omedelbart.
Dessa är inte alla möjliga biverkningar av NSAID. För mer information, fråga din vårdgivare eller apotekspersonal om NSAID.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Annan information om NSAID
- Aspirin är ett NSAID men det ökar inte risken för hjärtinfarkt. Aspirin kan orsaka blödningar i hjärnan, magen och tarmarna. Aspirin kan också orsaka sår i magen och tarmarna.
- Vissa NSAID-preparat säljs i lägre doser utan recept (receptfria). Prata med din vårdgivare innan du använder receptfria NSAIDs i mer än 10 dagar.
Allmän information om säker och effektiv användning av NSAID
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte NSAID för ett tillstånd som det inte ordinerats för. Ge inte NSAID till andra människor, även om de har samma symtom som du har. Det kan skada dem.
Om du vill ha mer information om NSAID, prata med din vårdgivare. Du kan fråga din apotekspersonal eller vårdgivare om information om NSAID som är skriven för vårdpersonal.
Denna medicineringsguide har godkänts av US Food and Drug Administration.
