Provera 5mg, 10mg Medroxyprogesterone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Provera och hur används det?
Provera 10mg är ett receptbelagt läkemedel som används för att behandla symtomen kraftiga menstruationsblödningar, frånvarande eller oregelbundna menstruationsblödningar och som preventivmedel. Provera 10mg kan användas ensamt eller tillsammans med andra läkemedel.
Provera 5mg tillhör en klass av läkemedel som kallas antineoplastika, hormoner, gestagen.
Det är inte känt om Provera är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Provera 10mg?
Provera 5mg kan orsaka allvarliga biverkningar inklusive:
- vaginal blödning (om du redan har gått igenom klimakteriet),
- yrsel,
- bröstknöl,
- depression,
- sömnproblem (sömnlöshet),
- yrsel,
- humörförändringar,
- huvudvärk,
- feber,
- gulfärgning av huden eller ögonen (gulsot),
- svullnad i dina händer, vrister eller fötter,
- bröstsmärtor eller tryck,
- smärta sprider sig till din käke eller axel,
- illamående,
- svettas,
- plötslig domningar eller svaghet,
- plötslig svår huvudvärk,
- sluddrigt tal,
- synproblem,
- problem med din balans,
- plötslig hosta,
- väsande andning,
- snabb andning,
- hosta upp blod, och
- smärta i benet (eller båda) med svullnad, värme och rodnad
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Provera 10mg inkluderar:
- stänkblödning eller genombrottsblödning,
- förändringar i din menstruation,
- vaginal klåda eller flytningar,
- ömhet eller flytningar i brösten,
- huvudvärk,
- yrsel,
- känner dig nervös eller deprimerad,
- blåmärken eller svullnad av dina vener,
- uppblåsthet,
- vätskeretention,
- humörförändringar,
- sömnproblem (sömnlöshet),
- klåda,
- utslag,
- acne,
- hårväxt,
- förlust av hår på hårbotten,
- obehag i magen,
- uppblåsthet,
- illamående,
- viktökning och
- synförändringar eller svårigheter att använda kontaktlinser
VARNING
Hjärt- och kärlsjukdomar, BRÖSTCANCER OCH TROLIG DEMENS FÖR ÖTROGEN PLUS PROGESTINBEHANDLING
Kardiovaskulära störningar och trolig demens
Behandling med östrogen plus gestagen bör inte användas för att förebygga hjärt-kärlsjukdom eller demens. (Ser Kliniska studier och VARNINGAR , Kardiovaskulära störningar och trolig demens .)
Women's Health Initiative (WHI) östrogen plus gestagen delstudie rapporterade en ökad risk för djup ventrombos (DVT), lungemboli (PE), stroke och hjärtinfarkt (MI) hos postmenopausala kvinnor (50 till 79 år gamla) ) under 5,6 års behandling med dagliga orala konjugerade östrogener (CE) [0,625 mg] kombinerat med medroxiprogesteronacetat (MPA) [2,5 mg], jämfört med placebo. (Ser Kliniska studier och VARNINGAR , Kardiovaskulära sjukdomar .)
WHI Memory Study (WHIMS) östrogen plus progestin kompletterande studie rapporterade en ökad risk för att utveckla trolig demens hos postmenopausala kvinnor 65 år eller äldre under 4 års behandling med daglig CE (0,625 mg) kombinerat med MPA (2,5 mg), relativt till placebo. Det är okänt om detta fynd gäller yngre postmenopausala kvinnor. (Ser Kliniska studier och VARNINGAR , Trolig demens och FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning .)
Bröstcancer
WHI östrogen plus gestagen delstudie visade en ökad risk för invasiv bröstcancer. (Ser Kliniska studier och VARNINGAR , Malign neoplasm , Bröstcancer .)
I avsaknad av jämförbara data bör dessa risker antas vara likartade för andra doser av CE och MPA, och andra kombinationer och beredningsformer av östrogener och progestiner.
Progestiner med östrogener bör förskrivas i de lägsta effektiva doserna och för den kortaste varaktigheten som överensstämmer med behandlingens mål och risker för den enskilda kvinnan.
BESKRIVNING
PROVERA® tabletter innehåller medroxiprogesteronacetat, som är ett derivat av progesteron. Det är ett vitt till benvitt, luktfritt kristallint pulver, stabilt i luft, smälter mellan 200 och 210°C. Den är lättlöslig i kloroform, löslig i aceton och dioxan, svårlöslig i alkohol och metanol, lättlöslig i eter och olöslig i vatten.
Det kemiska namnet för medroxiprogesteronacetat är pregn-4-en-3, 20-dion, 17-(acetyloxi)-6-metyl-, (6α)-. Strukturformeln är:
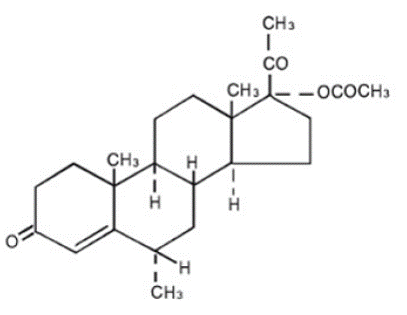
Varje PROVERA 5 mg tablett för oral administrering innehåller 2,5 mg, 5 mg eller 10 mg medroxiprogesteronacetat och följande inaktiva ingredienser: kalciumstearat, majsstärkelse, laktos, mineralolja, sorbinsyra, sackaros och talk. 2,5 mg tabletten innehåller FD&C Yellow No. 6.
INDIKATIONER
PROVERA 5 mg tabletter är indicerade för behandling av sekundär amenorré och onormal livmoderblödning på grund av hormonell obalans i frånvaro av organisk patologi, såsom myom eller livmodercancer. De är också indicerade för användning för att förebygga endometriehyperplasi hos icke-hysterektomiserade postmenopausala kvinnor som dagligen får orala konjugerade östrogener 0,625 mg tabletter.
DOSERING OCH ADMINISTRERING
Sekundär amenorré
PROVERA 10 mg tabletter kan ges i doser på 5 eller 10 mg dagligen i 5 till 10 dagar. En dos för att inducera en optimal sekretorisk transformation av ett endometrium som har förberetts adekvat med antingen endogent eller exogent östrogen är 10 mg PROVERA 10 mg dagligen i 10 dagar. I fall av sekundär amenorré kan behandlingen påbörjas när som helst. Progestinabstinensblödning inträffar vanligtvis inom tre till sju dagar efter att behandlingen med PROVERA 10 mg avslutats.
Onormal livmoderblödning på grund av hormonell obalans i avsaknad av organisk patologi
Från och med den beräknade 16:e eller 21:a dagen i menstruationscykeln kan 5 eller 10 mg PROVERA 10 mg ges dagligen i 5 till 10 dagar. För att åstadkomma en optimal sekretorisk transformation av ett endometrium som har förberetts adekvat med antingen endogent eller exogent östrogen, föreslås 10 mg PROVERA 10 mg dagligen i 10 dagar med början på den 16:e dagen av cykeln. Progestinabstinensblödning inträffar vanligtvis inom tre till sju dagar efter avslutad behandling med PROVERA. Patienter med en tidigare historia av återkommande episoder av onormal livmoderblödning kan ha nytta av planerad menstruationscykel med PROVERA.
Minskning av endometriehyperplasi hos postmenopausala kvinnor som dagligen får 0,625 mg konjugerade östrogener
När östrogen ordineras till en postmenopausal kvinna med livmoder bör ett gestagen initieras för att minska risken för endometriecancer. En kvinna utan livmoder behöver inte progestin. Användning av östrogen, ensamt eller i kombination med ett gestagen, bör ske med den lägsta effektiva dosen och för den kortaste varaktigheten förenlig med behandlingsmål och risker för den enskilda kvinnan. Patienter bör utvärderas på nytt med jämna mellanrum om det är kliniskt lämpligt (till exempel med 3 till 6 månaders intervall) för att avgöra om behandling fortfarande är nödvändig (se VARNINGAR ). För kvinnor som har en livmoder bör adekvata diagnostiska åtgärder, såsom endometrieprovtagning, när så är indicerat, vidtas för att utesluta malignitet i fall av odiagnostiserad ihållande eller återkommande onormal vaginal blödning.
PROVERA tabletter kan ges i doser om 5 eller 10 mg dagligen under 12 till 14 dagar i följd per månad, till postmenopausala kvinnor som dagligen får 0,625 mg konjugerade östrogener, antingen med början på cykelns första dag eller cykelns 16:e dag.
Patienter bör startas med den lägsta dosen.
Den lägsta effektiva dosen av PROVERA har inte fastställts.
HUR LEVERERAS
PROVERA 10mg tabletter finns i följande styrkor och förpackningsstorlekar:
2,5 mg (poängsatt, rund, orange)
30 flaskor NDC 0009-0064-06 Flaskor med 100 st NDC 0009-0064-04
5 mg (poängsatt, sexkantigt, vitt)
100 flaskor NDC 0009-0286-03
10 mg (poängsatt, rund, vit)
100 flaskor NDC 0009-0050-02 Flaskor med 500 st NDC 0009-0050-11
Förvara i kontrollerad rumstemperatur 20° till 25°C (68° till 77°F) [se USP ].
"Förvara utom räckhåll för barn"
Distribueras av: Pharmacia & Upjohn Company, Division of Pfizer Inc., NY, NY 10017. Reviderad: Aug 2015
BIEFFEKTER
Ser LÅDA VARNINGAR , VARNINGAR , och FÖRSIKTIGHETSÅTGÄRDER .
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Följande biverkningar har rapporterats hos kvinnor som tar PROVERA 10 mg tabletter utan samtidig östrogenbehandling:
Genitourinary System
Onormal livmoderblödning (oregelbunden, ökning, minskning), förändring i menstruationsflöde, genombrottsblödning, stänkblödning, amenorré, förändringar i cervikal erosion och cervikala sekret.
Bröst
Bröstömhet, mastodyni eller galaktorré har rapporterats.
Kardiovaskulär
Tromboemboliska störningar inklusive tromboflebit och lungemboli har rapporterats.
Gastrointestinala
Illamående, kolestatisk gulsot.
Hud
Känslighetsreaktioner bestående av urtikaria, klåda, ödem och generaliserade utslag har förekommit. Akne, känslighetsreaktioner bestående av urtikaria, klåda, ödem och generaliserade utslag har förekommit. Akne, alopeci och hirsutism har rapporterats.
Ögon
Neuro-okulära lesioner, till exempel retinal trombos och optisk neurit.
Centrala nervsystemet
Psykisk depression, sömnlöshet, somnolens, yrsel, huvudvärk, nervositet.
Diverse
Överkänslighetsreaktioner (till exempel anafylaxi och anafylaktoida reaktioner, angioödem), hudutslag (allergiskt) med och utan klåda, förändring i vikt (ökning eller minskning), pyrexi, ödem/vätskeretention, trötthet, minskad glukostolerans.
Följande biverkningar har rapporterats med östrogen plus gestagenbehandling.
Genitourinary System
Onormal livmoderblödning/fläckar, eller flöde; genombrottsblödning; spotting; dysmenorré/bäckensmärta; ökning av storleken på livmoderleiomyomata; vaginit, inklusive vaginal candidiasis; förändring i mängden cervikal sekretion; förändringar i cervikal ektropion; äggstockscancer; endometriehyperplasi; endometriecancer.
Bröst
Ömhet, förstoring, smärta, flytningar från bröstvårtan, galaktorré; fibrocystiska bröstförändringar; bröstcancer.
Kardiovaskulär
Djup och ytlig venös trombos; lungemboli; tromboflebit; hjärtinfarkt; stroke; ökning av blodtrycket.
Gastrointestinala
Illamående, kräkningar; magkramper, uppblåsthet; kolestatisk gulsot; ökad förekomst av sjukdom i gallblåsan; pankreatit; förstoring av hepatiska hemangiom.
Hud
Kloasma eller melasma som kan kvarstå när läkemedlet avbryts; erythema multiforme; erythema nodosum; hemorragisk utbrott; förlust av hår på hårbotten; hirsutism; klåda, utslag.
Ögon
Retinal vaskulär trombos, intolerans mot kontaktlinser.
Centrala nervsystemet
Huvudvärk; migrän; yrsel; mental depression; chorea; nervositet; humörstörningar; irritabilitet; exacerbation av epilepsi, demens.
Diverse
Öka eller minska i vikt; minskad kolhydrattolerans; förvärring av porfyri; ödem; arthalgier; benkramper; förändringar i libido; urtikaria, angioödem, anafylaktoida/anafylaktiska reaktioner; hypokalcemi; exacerbation av astma; ökade triglycerider.
LÄKEMEDELSINTERAKTIONER
Interaktioner mellan läkemedel och laboratorietest
Följande laboratorieresultat kan förändras genom användning av östrogen plus gestagenbehandling:
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
Ser LÅDA VARNINGAR .
Kardiovaskulära sjukdomar
En ökad risk för PE, DVT, stroke och MI har rapporterats med östrogen plus gestagenbehandling. Om någon av dessa händelser inträffar eller misstänks ska behandlingen med östrogen plus gestagen avbrytas omedelbart.
Riskfaktorer för arteriell kärlsjukdom (till exempel hypertoni, diabetes mellitus, tobaksanvändning, hyperkolesterolemi och fetma) och/eller venös tromboembolism (VTE) (till exempel personlig historia eller familjehistoria av VTE, fetma och systemisk lupus erythematosus) bör hanteras på lämpligt sätt.
Stroke
WHI östrogen plus gestagen substudie rapporterades en statistiskt signifikant ökad risk för stroke hos kvinnor 50 till 79 år som fick CE (0,625 mg) plus MPA (2,5 mg) jämfört med kvinnor i samma åldersgrupp som fick placebo (33 jämfört med 25 per 10 000 kvinnoår). (Ser Kliniska studier .) Riskökningen påvisades efter det första året och kvarstod. Om en stroke inträffar eller misstänks, ska behandlingen med östrogen plus gestagen avbrytas omedelbart.
Kranskärlssjukdom
I WHI-substudien östrogen plus gestagen, fanns det en statistiskt icke-signifikant ökad risk för CHD-händelser som rapporterades hos kvinnor som fick daglig CE (0,625 mg) plus MPA (2,5 mg) jämfört med kvinnor som fick placebo (41 mot 34 per 10 000 kvinnoår) ). En ökning av den relativa risken påvisades år 1, och en trend mot minskande relativ risk rapporterades år 2 till 5.
Hos postmenopausala kvinnor med dokumenterad hjärtsjukdom (n = 2 763, i genomsnitt 66,7 års ålder), i en kontrollerad klinisk prövning av sekundär prevention av hjärt-kärlsjukdom (hjärt- och östrogen/progestinersättningsstudie [HERS]), behandling med daglig CE (0,625 mg) ) plus MPA (2,5 mg) visade ingen kardiovaskulär fördel. Under en genomsnittlig uppföljning på 4,1 år minskade inte behandling med CE plus MPA den totala frekvensen av CHD-händelser hos postmenopausala kvinnor med etablerad kranskärlssjukdom. Det förekom fler CHD-händelser i den CE plus MPA-behandlade gruppen än i placebogruppen år 1, men inte under de efterföljande åren. Två tusen trehundratjugoen (2 321) kvinnor från det ursprungliga HERS-försöket gick med på att delta i en öppen förlängning av HERS, HERS II. Genomsnittlig uppföljning i HERS II var ytterligare 2,7 år, totalt 6,8 år totalt. Frekvensen av CHD-händelser var jämförbara bland kvinnor i CE plus MPA-gruppen och placebogruppen i HERS, HERS II och totalt sett.
Venös tromboembolism
WHI östrogen plus gestagen substudie rapporterades en statistiskt signifikant 2 gånger högre frekvens av VTE (DVT och PE) hos kvinnor som fick daglig CE (0,625 mg) plus MPA (2,5 mg) jämfört med kvinnor som fick placebo (35 mot 17 per dag) 10 000 kvinnoår). Statistiskt signifikanta riskökningar för både DVT (26 mot 13 per 10 000 kvinnoår) och PE (18 mot 8 per 10 000 kvinnoår) visades också. Ökningen av VTE-risken påvisades under det första året och kvarstod. (Ser Kliniska studier .) Om en VTE uppstår eller misstänks, bör östrogen plus gestagenbehandling avbrytas omedelbart.
Om möjligt bör östrogener plus gestagen avbrytas minst 4 till 6 veckor före operation av den typ som är förknippad med en ökad risk för tromboembolism, eller under perioder av långvarig immobilisering.
Maligna neoplasmer
Bröstcancer
Den viktigaste randomiserade kliniska studien som ger information om bröstcancer hos användare av östrogen plus gestagen är WHI-substudien av daglig CE (0,625 mg) plus MPA (2,5 mg). Efter en genomsnittlig uppföljning på 5,6 år rapporterade substudien med östrogen plus gestagen en ökad risk för invasiv bröstcancer hos kvinnor som tog dagligen CE plus MPA.
denna delstudie rapporterades tidigare användning av enbart östrogen eller östrogen plus gestagenbehandling av 26 procent av kvinnorna. Den relativa risken för invasiv bröstcancer var 1,24, och den absoluta risken var 41 mot 33 fall per 10 000 kvinnoår, för CE plus MPA jämfört med placebo. Bland kvinnor som rapporterade tidigare användning av hormonbehandling var den relativa risken för invasiv bröstcancer 1,86, och den absoluta risken var 46 mot 25 fall per 10 000 kvinnoår, för CE plus MPA jämfört med placebo. Bland kvinnor som inte rapporterade någon tidigare användning av hormonbehandling var den relativa risken för invasiv bröstcancer 1,09, och den absoluta risken var 40 mot 36 fall per 10 000 kvinnoår, för CE plus MPA jämfört med placebo. I samma delstudie var invasiva bröstcancer större, var mer benägna att vara nodpositiva och diagnostiserades i ett mer framskridet stadium i gruppen CE (0,625 mg) plus MPA (2,5 mg) jämfört med placebogruppen. Metastaserande sjukdom var sällsynt utan någon uppenbar skillnad mellan de två grupperna. Andra prognostiska faktorer såsom histologisk subtyp, grad och hormonreceptorstatus skilde sig inte mellan grupperna. (Ser Kliniska studier .)
enlighet med WHI-studien har observationsstudier också rapporterat en ökad risk för bröstcancer för behandling med östrogen plus gestagen, och en mindre risk för enbart östrogenbehandling, efter flera års användning. Risken ökade med användningens varaktighet och verkade återgå till baslinjen under cirka 5 år efter avslutad behandling (endast observationsstudierna har betydande data om risken efter avslutad behandling). Observationsstudier tyder också på att risken för bröstcancer var större, och blev uppenbar tidigare, med östrogen plus gestagenbehandling jämfört med enbart östrogenbehandling. Dessa studier har dock inte funnit signifikant variation i risken för bröstcancer mellan olika kombinationer av östrogen plus gestagen, eller administreringsvägar.
Användning av östrogen plus gestagen har rapporterats resultera i en ökning av onormala mammografi som kräver ytterligare utvärdering. Alla kvinnor bör få årliga bröstundersökningar av en vårdgivare och utföra månatliga bröstsjälvundersökningar. Dessutom bör mammografiundersökningar schemaläggas baserat på patientens ålder, riskfaktorer och tidigare mammografiresultat.
Endometriecancer
En ökad risk för endometriecancer har rapporterats vid användning av oöverträffad östrogenbehandling hos kvinnor med livmoder. Den rapporterade risken för endometriecancer bland icke-opponerade östrogenanvändare är cirka 2 till 12 gånger större än hos icke-användare, och verkar vara beroende av behandlingens varaktighet och östrogendosen. De flesta studier visar ingen signifikant ökad risk förknippad med användning av östrogener under mindre än 1 år. Den största risken verkar vara associerad med långvarig användning, med ökade risker på 15 till 24 gånger under 5 till 10 år eller mer. Denna risk har visats kvarstå i minst 8 till 15 år efter att östrogenbehandlingen avbrutits.
Klinisk övervakning av alla kvinnor som använder östrogen plus gestagenbehandling är viktig. Adekvata diagnostiska åtgärder, inklusive endometrieprovtagning när så är indicerat, bör vidtas för att utesluta malignitet i alla fall av odiagnostiserad ihållande eller återkommande onormal genital blödning. Det finns inga bevis för att användningen av naturliga östrogener resulterar i en annan endometrial riskprofil än syntetiska östrogener med motsvarande östrogendos. Att lägga till ett gestagen till östrogenbehandling har visat sig minska risken för endometriehyperplasi, som kan vara en föregångare till endometriecancer.
Äggstockscancer
WHI östrogen plus gestagen delstudie rapporterade en statistiskt icke-signifikant ökad risk för äggstockscancer. Efter en genomsnittlig uppföljning på 5,6 år var den relativa risken för äggstockscancer för CE plus MPA jämfört med placebo 1,58 (95 procent CI, 0,77–3,24). Den absoluta risken för CE plus MPA var 4 mot 3 fall per 10 000 kvinnoår. I vissa epidemiologiska studier har användningen av östrogen plus gestagen och endast östrogenprodukter, i synnerhet under 5 eller fler år, associerats med ökad risk för äggstockscancer. Varaktigheten av exponeringen förknippad med ökad risk är dock inte konsekvent i alla epidemiologiska studier och vissa rapporterar inget samband.
Trolig demens
WHIMS-studien med östrogen plus progestin av WHI randomiserades en population av 4 532 postmenopausala kvinnor i åldern 65 till 79 år till daglig CE (0,625 mg) plus MPA (2,5 mg) eller placebo. Efter en genomsnittlig uppföljning på 4 år diagnostiserades 40 kvinnor i CE plus MPA-gruppen och 21 kvinnor i placebogruppen med sannolik demens. Den relativa risken för trolig demens för CE plus MPA jämfört med placebo var 2,05 (95 procent KI, 1,21–3,48). Den absoluta risken för trolig demens för CE plus MPA jämfört med placebo var 45 mot 22 fall per 10 000 kvinnoår. Det är okänt om dessa fynd gäller yngre postmenopausala kvinnor. (Ser Kliniska studier och FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning .)
Synavvikelser
Avbryt behandlingen med östrogen plus gestagen i avvaktan på undersökning om det finns plötslig partiell eller fullständig synförlust, eller en plötslig uppkomst av proptos, dubbelsidighet eller migrän. Om undersökning avslöjar papillödem eller retinala vaskulära lesioner, bör östrogen plus gestagenbehandling avbrytas permanent.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Tillägg av ett gestagen när en kvinna inte har genomgått en hysterektomi
Studier av tillsats av ett progestin under 10 eller fler dagar av en cykel av östrogenadministrering, eller dagligen med östrogen i en kontinuerlig regim, har rapporterat en lägre incidens av endometriehyperplasi än vad som skulle induceras av enbart östrogenbehandling. Endometriehyperplasi kan vara en föregångare till endometriecancer.
Det finns dock möjliga risker som kan vara förknippade med användning av gestagen med östrogener jämfört med enbart östrogen. Dessa inkluderar en ökad risk för bröstcancer.
Oväntad onormal vaginal blödning
I fall av oväntad onormal vaginal blödning är adekvata diagnostiska åtgärder indikerade.
Förhöjt blodtryck
Blodtrycket bör övervakas med jämna mellanrum med östrogen plus gestagenbehandling.
Hypertriglyceridemi
Hos kvinnor med redan existerande hypertriglyceridemi kan behandling med östrogen plus gestagen vara associerad med förhöjda plasmatriglycerider som leder till pankreatit. Överväg att avbryta behandlingen om pankreatit uppstår.
Nedsatt leverfunktion och/eller tidigare historia av kolestatisk gulsot
Östrogener plus gestagen kan vara dåligt metaboliserad hos kvinnor med nedsatt leverfunktion. För kvinnor med en historia av kolestatisk gulsot i samband med tidigare östrogenanvändning eller med graviditet, bör försiktighet iakttas, och vid återfall bör medicinering avbrytas.
Vätskeretention
Progestiner kan orsaka en viss grad av vätskeretention. Kvinnor som har tillstånd som kan påverkas av denna faktor, såsom hjärt- eller njurfunktionsnedsättning, kräver noggrann observation när östrogen plus gestagen ordineras.
Hypokalcemi
Behandling med östrogen plus gestagen bör användas med försiktighet hos kvinnor med hypoparatyreos eftersom östrogeninducerad hypokalcemi kan förekomma.
Förvärring av andra tillstånd
Behandling med östrogen plus gestagen kan orsaka en förvärring av astma, diabetes mellitus, epilepsi, migrän, porfyri, systemisk lupus erythematosus och hepatiska hemangiom och bör användas med försiktighet hos kvinnor med dessa tillstånd.
Patientinformation
Läkare rekommenderas att diskutera PATIENTINFORMATION broschyr med kvinnor som de ordinerar PROVERA till.
Det kan finnas en ökad risk för mindre fosterskador hos barn vars mödrar exponeras för gestagen under graviditetens första trimester. Den möjliga risken för det manliga barnet är hypospadi, ett tillstånd där öppningen av penis är på undersidan snarare än spetsen av penis. Detta tillstånd förekommer naturligt i cirka 5 till 8 av 1000 manliga födslar. Risken kan öka vid exponering för PROVERA. Förstoring av klitoris och sammansmältning av blygdläpparna kan förekomma hos kvinnliga barn. Ett tydligt samband mellan hypospadi, klitorisförstoring och labial fusion med användning av PROVERA har dock inte fastställts.
Informera patienten om vikten av att rapportera exponering för PROVERA 5 mg under tidig graviditet.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Cancerframkallande egenskaper
Långvarig intramuskulär administrering av medroxiprogesteronacetat har visat sig ge brösttumörer hos beaglehundar. Det fanns inga tecken på en karcinogen effekt associerad med oral administrering av medroxiprogesteronacetat till råttor och möss.
Långvarig kontinuerlig administrering av östrogen plus gestagenbehandling har visat en ökad risk för bröstcancer och äggstockscancer. (Ser VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER .)
Genotoxicitet
Medroxiprogesteronacetat var inte mutagent i en rad genetiska toxicitetsanalyser in vitro eller in vivo.
Fertilitet
Medroxiprogesteronacetat i höga doser är ett antifertilitetsläkemedel och höga doser kan förväntas försämra fertiliteten tills behandlingen upphör.
Graviditet
Graviditetskategori X
PROVERA ska inte användas under graviditet. (Ser KONTRAINDIKATIONER .)
Det kan finnas ökade risker för hypospadi, klitorisförstoring och blygdläppsfusion hos barn vars mödrar exponeras för PROVERA 10 mg under graviditetens första trimester. Ett tydligt samband mellan dessa tillstånd med användning av PROVERA har dock inte fastställts.
Ammande mödrar
PROVERA ska inte användas under amning. Detekterbara mängder gestagen har identifierats i bröstmjölken hos ammande mödrar som får gestagen.
Pediatrisk användning
PROVERA 10 mg tabletter är inte indicerade för barn. Kliniska studier har inte utförts på den pediatriska populationen.
Geriatrisk användning
Det har inte varit tillräckligt många geriatriska kvinnor involverade i kliniska studier med endast PROVERA för att avgöra om de över 65 år skiljer sig från yngre försökspersoner i deras svar på enbart PROVERA.
The Women's Health Initiative Studies
I WHI-delstudien med östrogen plus gestagen (daglig CE [0,625 mg] plus MPA [2,5 mg] jämfört med placebo), fanns det en högre relativ risk för icke-fatal stroke och invasiv bröstcancer hos kvinnor äldre än 65 år. (Ser Kliniska studier .)
The Women's Health Initiative Memory Study
I WHIMS sidostudier av postmenopausala kvinnor i åldern 65 till 79 år fanns det en ökad risk att utveckla trolig demens hos kvinnor som fick enbart östrogen eller östrogen plus gestagen jämfört med placebo. (Ser VARNINGAR , Trolig demens .)
Eftersom båda kompletterande studierna utfördes på kvinnor i åldern 65 till 79 år är det okänt om dessa fynd gäller yngre postmenopausala kvinnor. (Ser VARNINGAR , Trolig demens .)
ÖVERDOS
Överdosering av östrogen plus gestagenbehandling kan orsaka illamående och kräkningar, ömma bröst, yrsel, buksmärtor, dåsighet/trötthet och abstinensblödningar kan förekomma hos kvinnor. Behandling av överdosering består av utsättande av CE plus MPA tillsammans med inrättande av lämplig symtomatisk vård.
KONTRAINDIKATIONER
PROVERA 10mg är kontraindicerat för kvinnor med något av följande tillstånd:
KLINISK FARMAKOLOGI
Medroxiprogesteronacetat (MPA) administrerat oralt eller parenteralt i rekommenderade doser till kvinnor med adekvat endogent östrogen, omvandlar proliferativt till sekretoriskt endometrium. Androgena och anabola effekter har noterats, men läkemedlet saknar tydligen betydande östrogen aktivitet. Medan parenteralt administrerat MPA hämmar produktionen av gonadotropin, vilket i sin tur förhindrar follikelmognad och ägglossning, indikerar tillgängliga data att detta inte inträffar när den vanligtvis rekommenderade orala dosen ges som enstaka dagliga doser.
Farmakokinetik
Farmakokinetiken för MPA bestämdes hos 20 postmenopausala kvinnor efter en endosadministrering av åtta PROVERA 2,5 mg tabletter eller en enkel administrering av två PROVERA 10 mg tabletter under fasta. I en annan studie bestämdes steady-state farmakokinetiken för MPA under fastande förhållanden hos 30 postmenopausala kvinnor efter daglig administrering av en PROVERA 10 mg tablett i 7 dagar. I båda studierna kvantifierades MPA i serum med en validerad gaskromatografi-masspektrometrimetod (GC-MS). Uppskattningar av de farmakokinetiska parametrarna för MPA efter enstaka och multipla doser av PROVERA-tabletter var mycket varierande och sammanfattas i tabell 1.
Absorption
Ingen specifik undersökning av den absoluta biotillgängligheten av MPA hos människor har utförts. MPA absorberas snabbt från mag-tarmkanalen och maximala MPA-koncentrationer erhålls mellan 2 till 4 timmar efter oral administrering.
Administrering av PROVERA med mat ökar biotillgängligheten av MPA. En 10 mg dos av PROVERA 10 mg, intagen omedelbart före eller efter en måltid, ökade MPA Cmax (50 till 70 %) och AUC (18 till 33 %). Halveringstiden för MPA ändrades inte med mat.
Distribution
MPA är till cirka 90 % proteinbundet, primärt till albumin; ingen MPA-bindning sker med könshormonbindande globulin.
Ämnesomsättning
Efter oral dosering metaboliseras MPA i stor utsträckning i levern via hydroxylering, med efterföljande konjugering och eliminering i urinen.
Exkretion
De flesta MPA-metaboliter utsöndras i urinen som glukuronidkonjugat med endast mindre mängder som utsöndras som sulfater.
Specifika populationer
Leverinsufficiens
MPA elimineras nästan uteslutande via levermetabolism. Hos 14 patienter med avancerad leversjukdom var MPA-dispositionen signifikant förändrad (minskad eliminering). Hos patienter med fettlever var den genomsnittliga procentuella dosen som utsöndrades i 24-timmarsurinen som intakt MPA efter en dos på 10 mg eller 100 mg 7,3 % respektive 6,4 %.
Njurinsufficiens
Effekten av nedsatt njurfunktion på farmakokinetiken för PROVERA 5 mg har inte studerats.
Läkemedelsinteraktioner
Medroxiprogesteronacetat (MPA) metaboliseras in vitro främst genom hydroxylering via CYP3A4. Specifika läkemedelsinteraktionsstudier som utvärderar de kliniska effekterna med CYP3A4-inducerare eller -hämmare på MPA har inte utförts. Inducerare och/eller hämmare av CYP3A4 kan påverka metabolismen av MPA.
Kliniska studier
Effekter På Endometriet
I en 3-årig, dubbelblind, placebokontrollerad studie av 356 icke-hysterektomiserade, postmenopausala kvinnor mellan 45 och 64 år randomiserade att få placebo (n=119), endast 0,625 mg konjugerat östrogen (n=119), eller 0,625 mg konjugerat östrogen plus cyklisk PROVERA (n=118), resultat visade en minskad risk för endometriehyperplasi i behandlingsgruppen som fick 10 mg PROVERA 5 mg plus 0,625 mg konjugerade östrogener jämfört med gruppen som endast fick 0,625 mg konjugerade östrogener. Se tabell 2.
en andra 1-årsstudie behandlades 832 postmenopausala kvinnor mellan 45 och 65 år med dagligen 0,625 mg konjugerat östrogen (dag 1–28), plus antingen 5 mg cyklisk PROVERA eller 10 mg cyklisk PROVERA (dag 15–28), eller endast 0,625 mg konjugerat östrogen dagligen. Behandlingsgrupperna som fick 5 eller 10 mg cyklisk PROVERA (dagar 15–28) plus dagliga konjugerade östrogener visade en signifikant lägre frekvens av hyperplasi jämfört med gruppen med endast konjugerade östrogener. Se tabell 3.
Studier av initiativ för kvinnors hälsa
WHI registrerade cirka 27 000 övervägande friska postmenopausala kvinnor i två delstudier för att bedöma riskerna och fördelarna med daglig oral CE (0,625 mg) ensam eller i kombination med MPA (2,5 mg) jämfört med placebo för att förebygga vissa kroniska sjukdomar. Det primära effektmåttet var förekomsten av koronar hjärtsjukdom (CHD) (definierad som icke-dödlig hjärtinfarkt, tyst hjärtinfarkt och dödsfall), med invasiv bröstcancer som det primära negativa resultatet. Ett "globalt index" inkluderade den tidigaste förekomsten av CHD, invasiv bröstcancer, stroke, PE, endometriecancer (endast i CE plus MPA-substudien), kolorektal cancer, höftfraktur eller död på grund av annan orsak. Dessa delstudier utvärderade inte effekterna av CE-ensamt eller CE plus MPA på klimakteriebesvär.
WHI Estrogen Plus Progestin Substudie
WHI östrogen plus gestagen delstudien stoppades tidigt. Enligt den fördefinierade stoppregeln, efter en genomsnittlig uppföljning av 5,6 års behandling, översteg den ökade risken för invasiv bröstcancer och kardiovaskulära händelser de specificerade fördelarna som ingår i det "globala indexet". Den absoluta överrisken för händelser som ingår i det "globala indexet" var 19 per 10 000 kvinnoår.
För de utfall som ingår i WHI "globala index" som nådde statistisk signifikans efter 5,6 års uppföljning, var de absoluta överriskerna per 10 000 kvinnoår i gruppen som behandlades med CE plus MPA 7 fler CHD-händelser, 8 fler stroke, 10 fler PEs och 8 fler invasiva bröstcancer, medan den absoluta riskminskningen per 10 000 kvinnoår var 6 färre kolorektal cancer och 5 färre höftfrakturer.
Resultaten från CE plus MPA-delstudien, som inkluderade 16 608 kvinnor (genomsnitt 63 år, intervall 50 till 79; 83,9 procent vita, 6,8 procent svarta, 5,4 procent latinamerikanska, 3,9 procent övriga) presenteras i tabell 4. Dessa resultat återspeglas centralt. bedömd data efter en genomsnittlig uppföljning på 5,6 år.
Tidpunkten för initiering av östrogen plus gestagenbehandling i förhållande till början av klimakteriet kan påverka den övergripande risk-nyttoprofilen. WHI östrogen plus gestagen delstudie stratifierad efter ålder visade hos kvinnor 50 till 59 år en icke-signifikant trend mot minskad risk för total dödlighet [hazard ration (HR) 0,69 (95 procent CI, 0,44–1,07)].
Women's Health Initiative Memory Study
WHIMS-studien med östrogen plus progestin av WHI inkluderade 4 532 övervägande friska postmenopausala kvinnor 65 år och äldre (47 procent var i åldern 65 till 69 år, 35 procent var 70 till 74 år och 18 procent var 75 år gamla. ålder och äldre) för att utvärdera effekterna av daglig CE (0,625 mg) plus MPA (2,5 mg) på förekomsten av trolig demens (primärt utfall) jämfört med placebo.
Efter en genomsnittlig uppföljning på 4 år var den relativa risken för trolig demens för CE plus MPA kontra placebo 2,05 (95 procent KI, 1,21–3,48). Den absoluta risken för trolig demens för CE plus MPA jämfört med placebo var 45 mot 33 per 10 000 kvinnoår. Trolig demens som definieras i denna studie inkluderade Alzheimers sjukdom (AD), vaskulär demens (VaD) och blandad typ (med egenskaper av både AD och VaD). Den vanligaste klassificeringen av sannolik demens i behandlingsgruppen och placebogruppen var AD. Eftersom den kompletterande studien genomfördes på kvinnor i åldern 65 till 79 år är det okänt om dessa fynd gäller yngre postmenopausala kvinnor. (Ser VARNINGAR , Trolig demens och FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning ).
PATIENTINFORMATION
PROVERA (pro-VE-rah) (medroxiprogesteronacetat) tabletter , USP
Läs denna patientinformation innan du börjar ta PROVERA och läs vad du får varje gång du fyller på ditt PROVERA-recept. Det kan komma ny information. Denna information ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling.
Vilken är den viktigaste informationen jag borde veta om PROVERA (ett progestinhormon)?
- Använd inte östrogener med gestagen för att förhindra hjärtsjukdomar, hjärtinfarkter, stroke eller demens (nedgång i hjärnans funktion).
- Att använda östrogener med gestagen kan öka din chans att få hjärtinfarkt, stroke, bröstcancer och blodproppar.
- Att använda östrogener med gestagen kan öka din chans att få demens, baserat på en studie av kvinnor som är 65 år eller äldre.
- Du och din vårdgivare bör prata regelbundet om huruvida du fortfarande behöver behandling med PROVERA.
Vad är PROVERA 10mg?
PROVERA är ett läkemedel som innehåller medroxiprogesteronacetat, ett gestagenhormon.
Vad används PROVERA 5mg för?
PROVERA används för att:
- Behandla menstruationer som har upphört eller för att behandla onormal livmoderblödning. Kvinnor med livmoder som inte är gravida, som slutar ha regelbundna menstruationer eller som börjar få oregelbundna menstruationer kan få en sänkning av sin progesteronnivå. Prata med din vårdgivare om PROVERA 10mg är rätt för dig.
- Minska dina chanser att få cancer i livmodern (livmodern). Hos postmenopausala kvinnor med en livmoder som använder östrogener, kommer att ta gestagen i kombination med östrogen minska risken att få livmodercancer.
Vem bör inte ta PROVERA?
Börja inte ta PROVERA om du:
- har ovanlig vaginal blödning
- för närvarande har eller har haft vissa cancerformer Östrogen plus gestagen kan öka din chans att få vissa typer av cancer, inklusive bröstcancer. Om du har eller har haft cancer, prata med din vårdgivare om du ska använda PROVERA.
- haft en stroke eller hjärtinfarkt
- för närvarande har eller har haft blodproppar
- för närvarande har eller har haft leverproblem
- är allergiska mot PROVERA 10mg eller någon av dess ingredienser Se listan över ingredienser i PROVERA i slutet av denna bipacksedel.
- tror att du kan vara gravid PROVERA är inte för gravida kvinnor. Om du tror att du kan vara gravid bör du göra ett graviditetstest och veta resultatet. Använd inte PROVERA om testet är positivt och prata med din vårdgivare. Det kan finnas en ökad risk för mindre fosterskador hos barn vars mödrar tar PROVERA under de första 4 månaderna av graviditeten. PROVERA ska inte användas som ett graviditetstest.
Vad ska jag berätta för min vårdgivare innan jag tar PROVERA 10mg? Innan du tar PROVERA 5mg, berätta för din läkare om du:
- har andra medicinska problem Din vårdgivare kan behöva kontrollera dig mer noggrant om du har vissa tillstånd som astma (väsande andning), epilepsi (kramper), diabetes, migrän, endometrios (svår bäckensmärta), lupus eller problem med ditt hjärta, lever, sköldkörtel, njurar eller har högt kalcium i blodet.
- ska opereras eller ligga i sängläge Din vårdgivare kommer att meddela dig om du behöver sluta ta PROVERA.
- ammar Hormonet i PROVERA kan passera över i din bröstmjölk.
Berätta för din vårdgivare om alla läkemedel du tar inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Vissa läkemedel kan påverka hur PROVERA verkar. PROVERA kan också påverka hur andra läkemedel fungerar.
Hur ska jag ta PROVERA 10mg?
Börja med den lägsta dosen och prata med din vårdgivare om hur väl den dosen fungerar för dig. Den lägsta effektiva dosen av PROVERA har inte fastställts. Du och din vårdgivare bör prata regelbundet (var tredje till var sjätte månad) om dosen du tar och om du fortfarande behöver behandling med PROVERA.
Vilka är de möjliga biverkningarna av PROVERA?
Följande biverkningar har rapporterats vid användning av PROVERA 10 mg enbart:
- ömhet i brösten
- bröstmjölksutsöndring
- genombrottsblödning
- stänkblödning (mindre vaginal blödning)
- oregelbundna mens
- amenorré (avsaknad av menstruationer)
- vaginala sekret
- huvudvärk
- nervositet
- yrsel
- depression
- sömnlöshet, sömnighet, trötthet
- premenstruella syndromliknande symtom
- tromboflebit (inflammerade vener)
- blodpropp
- klåda, nässelutslag, hudutslag
- acne
- håravfall, hårväxt
- Abdominalt obehag
- illamående
- uppblåsthet
- feber
- viktökning
- svullnad
- förändringar i syn och känslighet för kontaktlinser
Ring din vårdgivare omedelbart om du får nässelfeber, andningsproblem, svullnad i ansikte, mun, tunga eller hals
Följande biverkningar har rapporterats vid användning av PROVERA 5mg med ett östrogen.
Biverkningar grupperas efter hur allvarliga de är och hur ofta de inträffar när du behandlas.
Allvarliga men mindre vanliga biverkningar inkluderar:
- hjärtattack
- stroke
- blodproppar
- demens
- bröstcancer
- cancer i livmodern
- cancer i äggstockarna
- högt blodtryck
- högt blodsocker
- gallblåsan sjukdom
- leverproblem
- förändringar i dina sköldkörtelhormonnivåer
- förstoringar av godartade tumörer ("fibroider")
Ring din vårdgivare omedelbart om du får något av följande varningstecken eller andra ovanliga symtom som berör dig:
- nya bröstklumpar
- ovanlig vaginal blödning
- förändringar i syn och tal
- plötslig ny kraftig huvudvärk
- svår smärta i bröstet eller benen med eller utan andnöd, svaghet och trötthet
- minnesförlust eller förvirring
Mindre allvarliga, men vanliga biverkningar inkluderar:
- huvudvärk
- bröstsmärtor
- oregelbunden vaginal blödning eller stänkblödning
- mag- eller bukkramper, uppblåsthet
- illamående och kräkningar
- håravfall
- vätskeretention
- vaginal svampinfektion
Dessa är inte alla möjliga biverkningar av PROVERA med eller utan östrogen. För mer information, fråga din vårdgivare eller apotekspersonal om råd om biverkningar. Berätta för din vårdgivare om du har biverkningar som stör dig eller inte försvinner. Du kan rapportera biverkningar till Pfizer på 1-800-438-1985 eller FDA på 1-800-FDA-1088.
Vad kan jag göra för att minska risken för en allvarlig biverkning med PROVERA 10mg?
- Prata med din vårdgivare regelbundet om huruvida du ska fortsätta att ta PROVERA. Tillsats av ett gestagen rekommenderas generellt för kvinnor med livmoder för att minska risken för att få cancer i livmodern (livmodern).
- Kontakta din läkare omedelbart om du får vaginal blödning när du tar PROVERA.
- Gör en bäckenundersökning, bröstundersökning och mammografi (bröströntgen) varje år om inte din vårdgivare säger något annat till dig. Om medlemmar av din familj har haft bröstcancer eller om du någonsin har haft bröstklumpar eller en onormal mammografi, kan du behöva genomgå bröstundersökningar oftare.
- Om du har högt blodtryck, högt kolesterol (fett i blodet), diabetes, är överviktig eller om du använder tobak kan du ha större chans att få hjärtsjukdom. Fråga din vårdgivare om sätt att minska din chans att få hjärtsjukdom.
Allmän information om säker och effektiv användning av PROVERA
- Läkemedel skrivs ibland ut för tillstånd som inte nämns i patientinformationsblad.
- Ta inte PROVERA för tillstånd som det inte ordinerats för.
- Ge inte PROVERA till andra människor, även om de har samma symtom som du har. Det kan skada dem.
Förvara PROVERA 10mg utom räckhåll för barn.
Denna broschyr ger en sammanfattning av den viktigaste informationen om PROVERA. Om du vill ha mer information, prata med din vårdgivare eller apotekspersonal. Du kan be om information om PROVERA 10mg som är skriven för vårdpersonal. Du kan få mer information genom att ringa det avgiftsfria numret, 1-800-438-1985.
Vilka är ingredienserna i PROVERA?
Varje PROVERA 5 mg tablett för oral administrering innehåller 2,5 mg, 5 mg eller 10 mg medroxiprogesteronacetat.
Inaktiva ingredienser: kalciumstearat, majsstärkelse, laktos, mineralolja, sorbinsyra, sackaros, talk. 2,5 mg tabletten innehåller FD&C Yellow No. 6.
Denna produkts etikett kan ha uppdaterats. För aktuell fullständig förskrivningsinformation, besök www.pfizer.com
