Diflucan 50mg, 100mg, 150mg, 200mg Fluconazole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Diflucan och hur används det?
Diflucan är ett receptbelagt läkemedel som används för att behandla symtom på svampinfektioner. Diflucan 50 mg kan användas ensamt eller tillsammans med andra läkemedel.
Diflucan 100mg tillhör en klass av läkemedel som kallas antimykotika.
Vilka är biverkningarna av Diflucan 150mg?
Diflucan 100mg kan orsaka allvarliga biverkningar inklusive:
- snabba eller bultande hjärtslag,
- fladdra i ditt bröst,
- andnöd,
- plötslig yrsel,
- feber,
- frossa,
- kroppssmärtor,
- influensa symptom,
- lätta blåmärken eller blödningar,
- ovanlig svaghet,
- anfall (kramper),
- hudutslag eller skador,
- aptitlöshet,
- ont i övre magen,
- mörk urin,
- lerfärgad pall, och
- gulfärgning av ögon eller hud (gulsot)
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Diflucan inkluderar:
- illamående,
- magont,
- diarre,
- orolig mage,
- huvudvärk,
- yrsel och
- förändringar i ditt smaksinne
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Diflucan. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
DIFLUCAN® (flukonazol), den första i en ny underklass av syntetiska triazol-svampmedel, finns tillgänglig som tabletter för oral administrering, som pulver för oral suspension.
Flukonazol betecknas kemiskt som 2,4-difluoro-a,α1-bis(1H-1,2,4-triazol-1-ylmetyl)bensylalkohol med en empirisk formel av C13H12F2N6O och molekylvikt på 306,3. Strukturformeln är:
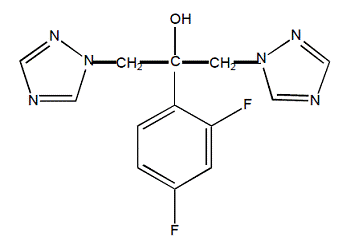
Flukonazol är ett vitt kristallint fast ämne som är lätt lösligt i vatten och koksaltlösning.
DIFLUCAN tabletter innehåller 50, 100, 150 eller 200 mg flukonazol och följande inaktiva ingredienser: mikrokristallin cellulosa, vattenfri dibasisk kalciumfosfat, povidon, kroskarmellosnatrium, FD&C Red No. 40 aluminiumsjöstearat och magnesium.
DIFLUCAN för oral suspension innehåller 350 mg eller 1400 mg flukonazol och följande inaktiva ingredienser: sackaros, natriumcitratdihydrat, vattenfri citronsyra, natriumbensoat, titandioxid, kolloidal kiseldioxid, xantangummi och naturlig apelsinsmak. Efter beredning med 24 ml destillerat vatten eller renat vatten (USP), innehåller varje ml rekonstituerad suspension 10 mg eller 40 mg flukonazol.
INDIKATIONER
DIFLUCAN (flukonazol) är indicerat för behandling av:
- Vaginal candidiasis (vaginal svampinfektion på grund av Candida).
- Orofaryngeal och esofagus candidiasis. I öppna icke-jämförande studier av ett relativt litet antal patienter var DIFLUCAN också effektivt för behandling av Candida urinvägsinfektioner, peritonit och systemiska Candida-infektioner inklusive candidemi, spridd candidiasis och lunginflammation.
- Kryptokock meningit. Innan du förskriver DIFLUCAN (flukonazol) till AIDS-patienter med kryptokockmeningit, se Kliniska studier sektion. Studier som jämförde DIFLUCAN 150 mg med amfotericin B på icke-hiv-infekterade patienter har inte utförts.
Profylax
DIFLUCAN är också indicerat för att minska incidensen av candidiasis hos patienter som genomgår benmärgstransplantation och som får cytotoxisk kemoterapi och/eller strålbehandling.
Prover för svampodling och andra relevanta laboratoriestudier (serologi, histopatologi) bör tas före behandling för att isolera och identifiera orsakande organismer. Terapi kan sättas in innan resultaten av odlingarna och andra laboratoriestudier är kända; men när dessa resultat blir tillgängliga bör antiinfektionsterapin justeras därefter.
DOSERING OCH ADMINISTRERING
Dosering och administrering hos vuxna
En dos
Vaginal candidiasis
Den rekommenderade dosen av DIFLUCAN för vaginal candidiasis är 150 mg som en oral engångsdos.
Flera doser
DÅ ORAL ABSORPTION ÄR SNABB OCH NÄSTAN FULLSTÄNDIG, ÄR DEN DAGLIGA DOSEN AV DIFLUCAN (FLUCONAZOL) SAMMA FÖR ORAL (TABLETTER OCH SUSPENSION) OCH INTRAVENÖS ADMINISTRERING. I allmänhet rekommenderas en laddningsdos på två gånger den dagliga dosen den första behandlingsdagen för att resultera i plasmakoncentrationer nära steady-state den andra dagen av behandlingen.
Den dagliga dosen av DIFLUCAN 100 mg för behandling av andra infektioner än vaginal candidiasis bör baseras på den infekterande organismen och patientens svar på behandlingen. Behandlingen ska fortsätta tills kliniska parametrar eller laboratorietester indikerar att aktiv svampinfektion har avtagit. En otillräcklig behandlingsperiod kan leda till att den aktiva infektionen återkommer. Patienter med AIDS och kryptokockmeningit eller återkommande orofaryngeal candidiasis kräver vanligtvis underhållsbehandling för att förhindra återfall.
Orofaryngeal candidiasis
Den rekommenderade dosen av DIFLUCAN för orofaryngeal candidiasis är 200 mg den första dagen, följt av 100 mg en gång dagligen. Kliniska tecken på orofaryngeal candidiasis försvinner i allmänhet inom flera dagar, men behandlingen bör fortsätta i minst 2 veckor för att minska sannolikheten för återfall.
Esophageal Candidiasis
Den rekommenderade dosen av DIFLUCAN 200 mg för esofagus candidiasis är 200 mg den första dagen, följt av 100 mg en gång dagligen. Doser upp till 400 mg/dag kan användas, baserat på medicinsk bedömning av patientens svar på behandlingen. Patienter med esofagus candidiasis bör behandlas i minst tre veckor och i minst två veckor efter att symtomen försvunnit.
Systemiska Candida-infektioner
För systemiska Candida-infektioner inklusive candidemia, spridd candidiasis och lunginflammation har optimal terapeutisk dosering och behandlingslängd inte fastställts. I öppna, icke-jämförande studier av ett litet antal patienter har doser på upp till 400 mg dagligen använts.
Urinvägsinfektioner och peritonit
För behandling av Candida urinvägsinfektioner och peritonit har dagliga doser på 50 till 200 mg använts i öppna, icke-jämförande studier av ett litet antal patienter.
Cryptococcal meningit
Den rekommenderade dosen för behandling av akut kryptokockmeningit är 400 mg den första dagen, följt av 200 mg en gång dagligen. En dos på 400 mg en gång dagligen kan användas, baserat på medicinsk bedömning av patientens svar på behandlingen. Den rekommenderade behandlingstiden för initial behandling av kryptokockmeningit är 10 till 12 veckor efter att cerebrospinalvätskan blivit odlingsnegativ. Den rekommenderade dosen av DIFLUCAN 150 mg för undertryckande av återfall av kryptokockmeningit hos patienter med AIDS är 200 mg en gång dagligen.
Profylax hos patienter som genomgår benmärgstransplantation
Den rekommenderade dagliga dosen DIFLUCAN för att förebygga candidiasis hos patienter som genomgår benmärgstransplantation är 400 mg en gång dagligen. Patienter som förväntas ha svår granulocytopeni (mindre än 500 neutrofila celler/mm³) bör påbörja DIFLUCAN-profylax flera dagar före den förväntade starten av neutropeni och fortsätta i 7 dagar efter att neutrofilantalet stiger över 1000 celler/mm³.
Dosering och administrering hos barn
Följande dosekvivalensschema bör generellt ge likvärdig exponering hos pediatriska och vuxna patienter:
Erfarenhet av DIFLUCAN hos nyfödda är begränsad till farmakokinetiska studier på prematura nyfödda. (Ser KLINISK FARMAKOLOGI .) Baserat på den förlängda halveringstiden hos prematura nyfödda (gestationsålder 26 till 29 veckor), bör dessa barn, under de två första levnadsveckorna, få samma dos (mg/kg) som hos äldre barn, men ges var 72:e timme. Efter de första två veckorna ska dessa barn doseras en gång dagligen. Ingen information om DIFLUCANs farmakokinetik hos fullgångna nyfödda är tillgänglig.
Orofaryngeal candidiasis
Den rekommenderade dosen av DIFLUCAN 150 mg för orofaryngeal candidiasis hos barn är 6 mg/kg den första dagen, följt av 3 mg/kg en gång dagligen. Behandling bör ges i minst 2 veckor för att minska sannolikheten för återfall.
Esophageal Candidiasis
För behandling av esofageal candidiasis är den rekommenderade dosen av DIFLUCAN till barn 6 mg/kg den första dagen, följt av 3 mg/kg en gång dagligen. Doser upp till 12 mg/kg/dag kan användas, baserat på medicinsk bedömning av patientens svar på behandlingen. Patienter med esofagus candidiasis bör behandlas i minst tre veckor och i minst 2 veckor efter att symtomen försvunnit.
Systemiska Candida-infektioner
För behandling av candidemia och spridda Candida-infektioner har dagliga doser på 6 till 12 mg/kg/dag använts i en öppen, icke-jämförande studie av ett litet antal barn.
Cryptococcal meningit
För behandling av akut kryptokockmeningit är den rekommenderade dosen 12 mg/kg den första dagen, följt av 6 mg/kg en gång dagligen. En dos på 12 mg/kg en gång dagligen kan användas, baserat på medicinsk bedömning av patientens svar på behandlingen. Den rekommenderade behandlingstiden för initial behandling av kryptokockmeningit är 10 till 12 veckor efter att cerebrospinalvätskan blivit odlingsnegativ. För suppression av återfall av kryptokockmeningit hos barn med AIDS är den rekommenderade dosen av DIFLUCAN 6 mg/kg en gång dagligen.
Dosering hos patienter med nedsatt njurfunktion
Flukonazol elimineras primärt genom renal utsöndring som oförändrat läkemedel. Det finns inget behov av att justera singeldosbehandling för vaginal candidiasis på grund av nedsatt njurfunktion. Till patienter med nedsatt njurfunktion som kommer att få flera doser av DIFLUCAN, bör en initial laddningsdos på 50 mg till 400 mg ges. Efter laddningsdosen ska den dagliga dosen (enligt indikation) baseras på följande tabell:
Patienter i hemodialys bör få 100 % av den rekommenderade dosen efter varje hemodialys; på dagar utan dialys bör patienterna få en reducerad dos beroende på deras kreatininclearance.
Dessa är föreslagna dosjusteringar baserade på farmakokinetik efter administrering av flera doser. Ytterligare justering kan behövas beroende på kliniskt tillstånd.
När serumkreatinin är det enda tillgängliga måttet på njurfunktion, bör följande formel (baserad på patientens kön, vikt och ålder) användas för att uppskatta kreatininclearance hos vuxna:
Män: Vikt (kg) × (140 – ålder)/ 72 × serumkreatinin (mg/100 ml)
Kvinnor: 0,85 × över värde
Även om farmakokinetiken för flukonazol inte har studerats hos barn med njurinsufficiens, bör dosreduktionen hos barn med njurinsufficiens vara parallell med den som rekommenderas för vuxna. Följande formel kan användas för att uppskatta kreatininclearance hos barn:
× linjär längd eller höjd (cm)/ serumkreatinin (mg/100 mL)
(Där K=0,55 för barn äldre än 1 år och 0,45 för spädbarn.)
Administrering
DIFLUCAN 100 mg administreras oralt. DIFLUCAN kan tas med eller utan mat.
Anvisningar för att blanda den orala suspensionen
Förbered en suspension vid tidpunkten för dispensering enligt följande: knacka på flaskan tills allt pulver flyter fritt. För att rekonstituera, tillsätt 24 ml destillerat vatten eller renat vatten (USP) till flukonazolflaskan och skaka kraftigt för att suspendera pulvret. Varje flaska kommer att leverera 35 ml suspension. Koncentrationerna av de rekonstituerade suspensionerna är följande:
Obs: Skaka oral suspension väl före användning. Förvara beredd suspension mellan 86°F (30°C) och 41°F (5°C) och kassera oanvänd del efter 2 veckor. Skydda mot frysning.
HUR LEVERERAS
DIFLUCAN 100mg tabletter Rosa trapetsformade tabletter innehållande 50, 100 eller 200 mg flukonazol är förpackade i flaskor eller endosblister. 150 mg flukonazoltabletterna är rosa och ovala, förpackade i en endosenhetsblister.
DIFLUCAN tabletter levereras enligt följande:
DIFLUCAN 50 mg tabletter : Graverad med "DIFLUCAN" och "50" på framsidan och "ROERIG" på baksidan.
NDC 0049-3410-30 Flaskor med 30 st
DIFLUCAN 100 mg tabletter : Graverad med "DIFLUCAN" och "100" på framsidan och "ROERIG" på baksidan.
NDC 0049-3420-30 Flaskor med 30 st NDC 0049-3420-41 Endosförpackning om 100 st
DIFLUCAN 150 mg tabletter : Graverad med "DIFLUCAN" och "150" på framsidan och "ROERIG" på baksidan.
NDC 0049-3500-79 Endosförpackning om 1
DIFLUCAN 200 mg tabletter : Graverad med "DIFLUCAN" och "200" på framsidan och "ROERIG" på baksidan.
NDC 0049-3430-30 Flaskor med 30 st NDC 0049-3430-41 Endosförpackning om 100 st
Lagring
Förvara tabletter under 30°C (86°F).
DIFLUCAN 100mg för oral suspension : DIFLUCAN för oral suspension tillhandahålls som ett pulver med apelsinsmak för att ge 35 ml per flaska enligt följande:
NDC 0049-3440-19 Flukonazol 350 mg per flaska NDC 0049-3450-19 Flukonazol 1400 mg per flaska
Lagring
Förvara torrt pulver under 86°F (30°C). Förvara beredd suspension mellan 86°F (30°C) och 41°F (5°C) och kassera oanvänd del efter 2 veckor. Skydda mot frysning.
Distribuerat av: Roerig Division of Pfizer Inc., NY, NY 10017. Reviderad: okt 2021
BIEFFEKTER
DIFLUCAN tolereras i allmänhet väl.
Hos vissa patienter, särskilt de med allvarliga underliggande sjukdomar som AIDS och cancer, har förändringar i njur- och hematologiska funktionstestresultat och leveravvikelser observerats under behandling med flukonazol och jämförande medel, men den kliniska betydelsen och sambandet med behandlingen är osäker.
Hos patienter som får en enstaka dos för vaginal candidiasis
Under jämförande kliniska studier utförda i USA, behandlades 448 patienter med vaginal candidiasis med DIFLUCAN, 150 mg engångsdos. Den totala förekomsten av biverkningar möjligen relaterade till DIFLUCAN var 26 %. Hos 422 patienter som fick aktiva jämförelsemedel var incidensen 16 %. De vanligaste behandlingsrelaterade biverkningarna som rapporterades hos patienter som fick 150 mg engångsdos av flukonazol mot vaginit var huvudvärk (13 %), illamående (7 %) och buksmärtor (6 %). Andra biverkningar som rapporterats med en incidens lika med eller större än 1 % inkluderade diarré (3 %), dyspepsi (1 %), yrsel (1 %) och smakperversion (1 %). De flesta av de rapporterade biverkningarna var milda till måttliga i svårighetsgrad. I sällsynta fall har angioödem och anafylaktiska reaktioner rapporterats i marknadsföringserfarenheter.
Hos patienter som får flera doser för andra infektioner
Sexton procent av över 4000 patienter som behandlats med DIFLUCAN (flukonazol) i kliniska prövningar på 7 dagar eller mer upplevde biverkningar. Behandlingen avbröts hos 1,5 % av patienterna på grund av biverkningar och hos 1,3 % av patienterna på grund av abnormiteter i laboratorietester.
Kliniska biverkningar rapporterades oftare hos HIV-infekterade patienter (21 %) än hos icke-HIV-infekterade patienter (13 %). mönstren hos HIV-infekterade och icke-HIV-infekterade patienter var dock liknande. Andelen patienter som avbröt behandlingen på grund av kliniska biverkningar var likartade i de två grupperna (1,5%).
Följande behandlingsrelaterade kliniska biverkningar inträffade med en incidens på 1 % eller mer hos 4048 patienter som fick DIFLUCAN 50 mg i 7 eller fler dagar i kliniska prövningar: illamående 3,7 %, huvudvärk 1,9 %, hudutslag 1,8 %, kräkningar 1,7 %, buk. smärta 1,7 % och diarré 1,5 %.
Hepato-Gallväg
kombinerade kliniska prövningar och marknadsföringserfarenhet har det förekommit sällsynta fall av allvarliga leverreaktioner under behandling med DIFLUCAN. (Ser VARNINGAR .) Spektrumet av dessa leverreaktioner har varierat från milda övergående förhöjningar av transaminaser till klinisk hepatit, kolestas och fulminant leversvikt, inklusive dödsfall. Fall av fatala leverreaktioner noterades främst hos patienter med allvarliga underliggande medicinska tillstånd (främst AIDS eller malignitet) och ofta när de tog flera samtidiga läkemedel. Övergående leverreaktioner, inklusive hepatit och gulsot, har förekommit hos patienter utan andra identifierbara riskfaktorer. I vart och ett av dessa fall återgick leverfunktionen till utgångsvärdet när behandlingen med DIFLUCAN avbröts.
två jämförande studier som utvärderade effekten av DIFLUCAN för att dämpa återfall av kryptokockmeningit, observerades en statistiskt signifikant ökning av median AST (SGOT) nivåer från ett baslinjevärde på 30 IE/L till 41 IE/L i en studie och 34 IU/L till 66 IU/L i den andra. Den totala frekvensen av serumtransaminashöjningar på mer än 8 gånger den övre normalgränsen var cirka 1 % hos flukonazolbehandlade patienter i kliniska prövningar. Dessa förhöjningar inträffade hos patienter med allvarlig underliggande sjukdom, övervägande AIDS eller maligniteter, av vilka de flesta fick flera samtidiga läkemedel, inklusive många kända för att vara hepatotoxiska. Incidensen av onormalt förhöjda serumtransaminaser var högre hos patienter som tog DIFLUCAN samtidigt med en eller flera av följande mediciner: rifampin, fenytoin, isoniazid, valproinsyra eller orala sulfonylurea hypoglykemiska medel.
Erfarenhet efter marknadsföring
Dessutom har följande biverkningar inträffat efter marknadsföring.
Immunologiska: I sällsynta fall har anafylaxi (inklusive angioödem, ansiktsödem och klåda) rapporterats.
Kroppen som helhet: Asteni, trötthet, feber, sjukdomskänsla.
Kardiovaskulär: QT-förlängning, torsade de pointes. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Centrala nervsystemet: Kramper, yrsel.
Hematopoetisk och lymfatisk: Leukopeni, inklusive neutropeni och agranulocytos, trombocytopeni.
Metaboliskt: Hyperkolesterolemi, hypertriglyceridemi, hypokalemi.
Gastrointestinala: Kolestas, muntorrhet, hepatocellulär skada, dyspepsi, kräkningar.
Andra sinnen: Smakperversion.
Muskuloskeletala systemet: muskelvärk.
Nervsystem: Sömnlöshet, parestesi, somnolens, tremor, svindel.
Hud och bihang: Akut generaliserad exantematös pustulos, läkemedelsutbrott inklusive fast läkemedelsutbrott, ökad svettning, exfoliativa hudsjukdomar inklusive Stevens-Johnsons syndrom och toxisk epidermal nekrolys, läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) (se VARNINGAR ), alopeci.
Biverkningar hos barn
Mönstret och förekomsten av biverkningar och laboratorieavvikelser som registrerats under pediatriska kliniska prövningar är jämförbara med de som ses hos vuxna.
I kliniska fas II/III-prövningar utförda i USA och i Europa behandlades 577 pediatriska patienter i åldrarna 1 dag till 17 år med DIFLUCAN i doser upp till 15 mg/kg/dag i upp till 1 616 dagar. Tretton procent av barnen upplevde behandlingsrelaterade biverkningar. De vanligaste rapporterade händelserna var kräkningar (5 %), buksmärtor (3 %), illamående (2 %) och diarré (2 %). Behandlingen avbröts hos 2,3 % av patienterna på grund av biverkningar och hos 1,4 % av patienterna på grund av abnormiteter i laboratorietester. Majoriteten av behandlingsrelaterade laboratorieavvikelser var förhöjda transaminaser eller alkaliskt fosfatas.
Andel patienter med behandlingsrelaterade biverkningar
LÄKEMEDELSINTERAKTIONER
(Ser KONTRAINDIKATIONER .) Flukonazol är en måttlig CYP2C9- och CYP3A4-hämmare. Flukonazol är också en stark hämmare av CYP2C19. Patienter som behandlas med DIFLUCAN, som också samtidigt behandlas med läkemedel med ett snävt terapeutiskt fönster som metaboliseras genom CYP2C9 och CYP3A4, bör övervakas för biverkningar associerade med de samtidigt administrerade läkemedlen. Utöver de observerade/dokumenterade interaktionerna som nämns nedan, finns det en risk för ökad plasmakoncentration av andra substanser som metaboliseras av CYP2C9, CYP2C19 och CYP3A4 tillsammans med flukonazol. Därför bör försiktighet iakttas vid användning av dessa kombinationer och patienterna bör övervakas noggrant. Den enzymhämmande effekten av flukonazol kvarstår 4 till 5 dagar efter avslutad flukonazolbehandling på grund av den långa halveringstiden för flukonazol. Kliniskt eller potentiellt signifikanta läkemedelsinteraktioner mellan DIFLUCAN 200 mg och följande medel/klasser har observerats och beskrivs mer detaljerat nedan:
Alfentanil
En studie observerade en minskning av clearance och distributionsvolym samt förlängning av t½ av alfentanil efter samtidig behandling med flukonazol. En möjlig verkningsmekanism är flukonazols hämning av CYP3A4. Dosjustering av alfentanil kan vara nödvändig.
Amiodaron
Samtidig administrering av flukonazol och amiodaron kan öka QT-förlängningen. Försiktighet måste iakttas om samtidig användning av flukonazol och amiodaron är nödvändig, särskilt med högdos flukonazol (800 mg).
Amitriptylin, Nortriptylin
Flukonazol ökar effekten av amitriptylin och nortriptylin. 5-Nortriptylin och/eller S-amitriptylin kan mätas vid start av kombinationsbehandlingen och efter 1 vecka. Doseringen av amitriptylin/nortriptylin bör justeras vid behov.
Amfotericin B
Samtidig administrering av flukonazol och amfotericin B i infekterade normala och immunsupprimerade möss visade följande resultat: en liten additiv svampdödande effekt vid systemisk infektion med Candida albicans, ingen interaktion vid intrakraniell infektion med Cryptococcus neoformans och antagonism av de två läkemedlen vid systemisk infektion med A fumigatus. Den kliniska betydelsen av resultat som erhållits i dessa studier är okänd.
Azitromycin
En öppen, randomiserad, trevägsöverkorsningsstudie på 18 friska försökspersoner utvärderade effekten av en enstaka 1200 mg oral dos av azitromycin på farmakokinetiken för en enstaka 800 mg oral dos av flukonazol samt effekterna av flukonazol på farmakokinetiken. av azitromycin. Det fanns ingen signifikant farmakokinetisk interaktion mellan flukonazol och azitromycin.
Kalciumkanalblockerare
Vissa kalciumkanalantagonister (nifedipin, isradipin, amlodipin, verapamil och felodipin) metaboliseras av CYP3A4. Flukonazol har potential att öka den systemiska exponeringen av kalciumkanalantagonisterna. Frekvent övervakning av biverkningar rekommenderas.
Karbamazepin
Flukonazol hämmar metabolismen av karbamazepin och en ökning av serumkarbamazepin på 30 % har observerats. Det finns en risk att utveckla karbamazepintoxicitet. Dosjustering av karbamazepin kan vara nödvändig beroende på koncentrationsmätningar/effekt.
Celecoxib
Under samtidig behandling med flukonazol (200 mg dagligen) och celecoxib (200 mg), ökade celecoxibs Cmax och AUC med 68 % respektive 134 %. Hälften av celecoxibdosen kan vara nödvändig i kombination med flukonazol.
Antikoagulantia av kumarintyp
Protrombintiden kan öka hos patienter som samtidigt får DIFLUCAN 150 mg och antikoagulantia av kumarintyp. Efter marknadsintroduktionen har blödningshändelser (blåmärken, näsblod, gastrointestinal blödning, hematuri och melena) rapporterats i samband med ökad protrombintid hos patienter som får flukonazol samtidigt med warfarin, liksom med andra azol-antimykotika. Noggrann övervakning av protrombintiden hos patienter som får DIFLUCAN 50 mg och antikoagulantia av kumarintyp rekommenderas. Dosjustering av warfarin kan vara nödvändig. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Cyklofosfamid
Kombinationsbehandling med cyklofosfamid och flukonazol resulterar i en ökning av serumbilirubin och serumkreatinin. Kombinationen kan användas samtidigt som man tar ökad hänsyn till risken för ökat serumbilirubin och serumkreatinin.
Cyklosporin
DIFLUCAN 100 mg ökar signifikant ciklosporinnivåerna hos njurtransplanterade patienter med eller utan nedsatt njurfunktion. Noggrann övervakning av ciklosporinkoncentrationer och serumkreatinin rekommenderas hos patienter som får DIFLUCAN och ciklosporin. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .) Denna kombination kan användas genom att reducera dosen av ciklosporin beroende på ciklosporinkoncentrationen.
Fentanyl
Ett dödsfall av möjlig fentanyl-flukonazol-interaktion rapporterades. Författaren bedömde att patienten dog av fentanylförgiftning. I en randomiserad crossover-studie med 12 friska frivilliga visades det dessutom att flukonazol fördröjde elimineringen av fentanyl signifikant. Förhöjda fentanylkoncentrationer kan leda till andningsdepression.
HMG-CoA-reduktashämmare
Risken för myopati och rabdomyolys ökar när flukonazol administreras samtidigt med HMG-CoA-reduktashämmare som metaboliseras genom CYP3A4, såsom atorvastatin och simvastatin, eller genom CYP2C9, såsom fluvastatin. Om samtidig behandling är nödvändig ska patienten observeras med avseende på symtom på myopati och rabdomyolys och kreatininkinas bör övervakas. HMG-CoA-reduktashämmare ska avbrytas om en markant ökning av kreatininkinas observeras eller myopati/rabdomyolys diagnostiseras eller misstänks.
Hydroklortiazid
I en farmakokinetisk interaktionsstudie ökade samtidig administrering av multipeldos hydroklortiazid till friska frivilliga som fick flukonazol plasmakoncentrationerna av flukonazol med 40 %. En effekt av denna storleksordning bör inte kräva en förändring av flukonazoldosregimen hos patienter som samtidigt får diuretika.
Ibrutinib
Måttliga hämmare av CYP3A4 såsom flukonazol kan öka plasmakoncentrationen av ibrutinib och öka risken för biverkningar associerade med ibrutinib. Om ibrutinib och flukonazol administreras samtidigt, reducera dosen av ibrutinib enligt anvisningarna i förskrivningsinformationen för ibrutinib och patienten bör övervakas regelbundet för eventuella biverkningar associerade med ibrutinib.
Lemborexant
Samtidig administrering av flukonazol ökade lemborexant Cmax och AUC med cirka 1,6 respektive 4,2 gånger, vilket förväntas öka risken för biverkningar, såsom somnolens. Undvik samtidig användning av DIFLUCAN och lemborexant.
Losartan
Flukonazol hämmar metabolismen av losartan till dess aktiva metabolit (E-31 74) som är ansvarig för det mesta av angiotensin Il-receptorantagonismen som uppstår under behandling med losartan. Patienter bör få sitt blodtryck övervakat kontinuerligt.
Metadon
Flukonazol kan öka serumkoncentrationen av metadon. Dosjustering av metadon kan vara nödvändig.
Icke-steroida antiinflammatoriska läkemedel
Cmax och AUC för flurbiprofen ökade med 23 % respektive 81 % vid samtidig administrering med flukonazol jämfört med administrering av enbart flurbiprofen. På liknande sätt ökade Cmax och AUC för den farmakologiskt aktiva isomeren [S-(+)-ibuprofen] med 15 % respektive 82 % när flukonazol gavs samtidigt med racemiskt ibuprofen (400 mg) jämfört med administrering av enbart racemiskt ibuprofen.
Även om det inte har studerats specifikt, har flukonazol potential att öka den systemiska exponeringen av andra icke-steroida antiinflammatoriska läkemedel (NSAID) som metaboliseras av CYP2C9 (t.ex. naproxen, lornoxikam, meloxikam, diklofenak). Frekvent övervakning av biverkningar och toxicitet relaterade till NSAID rekommenderas. Justering av dosen av NSAID kan behövas.
Olaparib
Måttliga hämmare av CYP3A4 såsom flukonazol ökar plasmakoncentrationerna av olaparib; samtidig användning rekommenderas inte. Om kombinationen inte kan undvikas, minska dosen av olaparib enligt instruktionerna i LYNPARZA® (Olaparib) förskrivningsinformation.
Orala preventivmedel
Två farmakokinetiska studier med ett kombinerat oralt preventivmedel har utförts med multipla doser av flukonazol. Det fanns inga relevanta effekter på hormonnivån i 50 mg flukonazolstudien, medan vid 200 mg dagligen ökade AUC för etinylöstradiol och levonorgestrel med 40 % respektive 24 %. Det är därför osannolikt att flerdosanvändning av flukonazol i dessa doser har någon effekt på effekten av det kombinerade orala preventivmedlet.
Oral hypoglykemi
Kliniskt signifikant hypoglykemi kan utlösas genom användning av DIFLUCAN med orala hypoglykemiska medel; en dödlighet har rapporterats från hypoglykemi i samband med kombinerad användning av DIFLUCAN 150 mg och glyburid. DIFLUCAN minskar metabolismen av tolbutamid, glyburid och glipizid och ökar plasmakoncentrationen av dessa medel. När DIFLUCAN 100 mg används samtidigt med dessa eller andra orala hypoglykemiska medel av sulfonylurea, bör blodsockerkoncentrationerna övervakas noggrant och dosen av sulfonylureid bör justeras vid behov. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
fenytoin
DIFLUCAN ökar plasmakoncentrationerna av fenytoin. Noggrann övervakning av fenytoinkoncentrationer hos patienter som får DIFLUCAN 50 mg och fenytoin rekommenderas. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Pimozide
Även om det inte har studerats in vitro eller in vivo, kan samtidig administrering av flukonazol och pimozid resultera i hämning av pimozidmetabolismen. Ökade plasmakoncentrationer av pimozid kan leda till QT-förlängning och sällsynta förekomster av torsade de pointes. Samtidig administrering av flukonazol och pimozid är kontraindicerat.
Prednison
Det fanns en fallrapport om att en levertransplanterad patient som behandlades med prednison utvecklade akut binjurebarkinsufficiens när en 3 månaders behandling med flukonazol avbröts. Utsättningen av flukonazol orsakade förmodligen en ökad CYP3A4-aktivitet som ledde till ökad metabolism av prednison. Patienter på långtidsbehandling med flukonazol och prednison bör noggrant övervakas med avseende på binjurebarksinsufficiens när flukonazol sätts ut.
Kinidin
Även om det inte har studerats in vitro eller in vivo, kan samtidig administrering av flukonazol och kinidin resultera i hämning av kinidinmetabolismen. Användning av kinidin har associerats med QT-förlängning och sällsynta förekomster av torsade de pointes. Samtidig administrering av flukonazol och kinidin är kontraindicerat. (Ser KONTRAINDIKATIONER .)
Rifabutin
Det har förekommit rapporter om att en interaktion förekommer när flukonazol administreras samtidigt med rifabutin, vilket leder till ökade serumnivåer av rifabutin upp till 80 %. Det har rapporterats om uveit hos patienter till vilka flukonazol och rifabutin administrerats samtidigt. Patienter som får rifabutin och flukonazol samtidigt bör övervakas noggrant. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Rifampin
Rifampin ökar metabolismen av samtidigt administrerad DIFLUCAN. Beroende på kliniska omständigheter bör man överväga att öka dosen av DIFLUCAN 200 mg när det administreras med rifampin. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Saquinavir
Flukonazol ökar AUC för saquinavir med cirka 50 %, Cmax med cirka 55 %, och minskar clearance av saquinavir med cirka 50 % på grund av hämning av saquinavirs levermetabolism av CYP3A4 och hämning av P-glykoprotein. Dosjustering av saquinavir kan vara nödvändig.
Kortverkande bensodiazepiner
Efter oral administrering av midazolam resulterade flukonazol i betydande ökningar av midazolamkoncentrationer och psykomotoriska effekter. Denna effekt på midazolam verkar vara mer uttalad efter oral administrering av flukonazol än med flukonazol administrerat intravenöst. Om kortverkande bensodiazepiner, som metaboliseras av cytokrom P450-systemet, administreras samtidigt med flukonazol, bör man överväga att minska bensodiazepindosen och patienterna bör övervakas på lämpligt sätt. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Sirolimus
Flukonazol ökar plasmakoncentrationerna av sirolimus förmodligen genom att hämma metabolismen av sirolimus via CYP3A4 och P-glykoprotein. Denna kombination kan användas med en dosjustering av sirolimus beroende på effekt/koncentrationsmätningar.
Takrolimus
Flukonazol kan öka serumkoncentrationerna av oralt administrerad takrolimus upp till 5 gånger på grund av hämning av takrolimus metabolism genom CYP3A4 i tarmarna. Inga signifikanta farmakokinetiska förändringar har observerats när takrolimus ges intravenöst. Ökade takrolimusnivåer har associerats med nefrotoxicitet. Doseringen av oralt administrerad takrolimus bör minskas beroende på takrolimuskoncentrationen. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Teofyllin
DIFLUCAN 50mg ökar serumkoncentrationerna av teofyllin. Noggrann övervakning av serumkoncentrationen av teofyllin hos patienter som får DIFLUCAN 100 mg och teofyllin rekommenderas. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Tofacitinib
Systemisk exponering för tofacitinib ökar när tofacitinib administreras samtidigt med flukonazol. Minska dosen av tofacitinib när det ges samtidigt med flukonazol (dvs från 5 mg två gånger dagligen till 5 mg en gång dagligen enligt anvisningarna på XELJANZ [tofacitinib]-etiketten). (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Tolvaptan
Plasmaexponering för tolvaptan ökar signifikant (200 % i AUC; 80 % i Cmax) när tolvaptan, ett CYP3A4-substrat, administreras samtidigt med flukonazol, en måttlig CYP3A4-hämmare. Denna interaktion kan resultera i risken för en signifikant ökning av biverkningar associerade med tolvaptan, särskilt signifikant diures, uttorkning och akut njursvikt. Om tolvaptan och flukonazol administreras samtidigt, ska tolvaptandosen minskas enligt anvisningarna i tolvaptanförskrivningsinformationen och patienten ska övervakas regelbundet för eventuella biverkningar associerade med tolvaptan.
Triazolam
Flukonazol ökar AUC för triazolam (engångsdos) med cirka 50 %, Cmax med 20 % till 32 % och ökar t½ med 25 % till 50 % på grund av hämningen av metabolismen av triazolam. Dosjusteringar av triazolam kan vara nödvändiga.
Vinca Alkaloider
Även om det inte studerats kan flukonazol öka plasmanivåerna av vinca-alkaloiderna (t.ex. vinkristin och vinblastin) och leda till neurotoxicitet, vilket möjligen beror på en hämmande effekt på CYP3A4.
Vitamin A
Baserat på en fallrapport hos en patient som fick kombinationsbehandling med all-trans-retinoidsyra (en sur form av vitamin A) och flukonazol, har biverkningar relaterade till centrala nervsystemet (CNS) utvecklats i form av pseudotumor cerebri, som försvann efter avbrytande av flukonazolbehandling. Denna kombination kan användas men förekomsten av CNS-relaterade biverkningar bör beaktas.
Vorikonazol
Undvik samtidig administrering av vorikonazol och flukonazol. Övervakning av biverkningar och toxicitet relaterade till vorikonazol rekommenderas; speciellt om vorikonazol påbörjas inom 24 timmar efter den sista dosen av flukonazol. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier .)
Zidovudin
Flukonazol ökar Cmax och AUC för zidovudin med 84 % respektive 74 % på grund av en cirka 45 % minskning av oralt zidovudinclearance. Halveringstiden för zidovudin förlängdes likaså med cirka 128 % efter kombinationsbehandling med flukonazol. Patienter som får denna kombination bör övervakas med avseende på utveckling av zidovudinrelaterade biverkningar. Dosminskning av zidovudin kan övervägas.

Läkare bör vara medvetna om att interaktionsstudier med andra läkemedel än de som anges i avsnittet KLINISK FARMAKOLOGI inte har utförts, men sådana interaktioner kan förekomma.
VARNINGAR
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Vissa azoler, inklusive flukonazol, har associerats med förlängning av QT-intervallet på elektrokardiogrammet. Flukonazol orsakar QT-förlängning via hämning av Rectifier Potassium Channel-ström (Ikr). QT-förlängningen orsakad av andra läkemedel (såsom amiodaron) kan förstärkas genom hämning av cytokrom P450 (CYP) 3A4. (Ser FÖRSIKTIGHETSÅTGÄRDER : Läkemedelsinteraktioner .) Under övervakning efter marknadsföring har det förekommit sällsynta fall av QT-förlängning och torsade de pointes hos patienter som tagit flukonazol. De flesta av dessa rapporter involverade allvarligt sjuka patienter med flera förvirrande riskfaktorer, såsom strukturell hjärtsjukdom, elektrolytavvikelser och samtidig medicinering som kan ha varit bidragande. Patienter med hypokalemi och avancerad hjärtsvikt löper en ökad risk för uppkomsten av livshotande ventrikulära arytmier och torsade de pointes.
Flukonazol bör administreras med försiktighet till patienter med dessa potentiellt proarytmiska tillstånd.
Samtidig användning av flukonazol och erytromycin kan öka risken för kardiotoxicitet (förlängt QT-intervall, torsade de pointes) och följaktligen plötslig hjärtdöd. Denna kombination bör undvikas.
Flukonazol bör administreras med försiktighet till patienter med nedsatt njurfunktion.
Binjurebarksvikt har rapporterats hos patienter som får azoler, inklusive flukonazol. Reversibla fall av binjurebarksvikt har rapporterats hos patienter som får flukonazol.
DIFLUCAN 100 mg pulver för oral suspension innehåller sackaros och ska inte användas till patienter med ärftlig fruktos, glukos/galaktosmalabsorption och sukras-isomaltasbrist.
Vid bilkörning eller användning av maskiner bör man ta hänsyn till att yrsel eller kramper ibland kan förekomma.
En dos
Bekvämligheten och effekten av den orala singeldabletten av flukonazol för behandling av vaginala svampinfektioner bör vägas mot acceptansen av en högre förekomst av läkemedelsrelaterade biverkningar med DIFLUCAN (26 %) jämfört med intravaginala medel (16 %) i USA jämförande kliniska studier. (Ser NEGATIVA REAKTIONER och Kliniska studier .)
Icke-klinisk toxikologi
Karcinogenes, mutagenes och försämring av fertilitet
Flukonazol visade inga tecken på cancerframkallande potential hos möss och råttor som behandlades oralt i 24 månader med doser på 2,5 mg/kg/dag, 5 mg/kg/dag eller 10 mg/kg/dag (ungefär 2 till 7 gånger den rekommenderade dosen för människor ). Hanråttor behandlade med 5 mg/kg/dag och 10 mg/kg/dag hade en ökad förekomst av hepatocellulära adenom.
Flukonazol, med eller utan metabolisk aktivering, var negativ i tester för mutagenicitet i fyra stammar av S. typhimurium och i muslymfom L5178Y-systemet. Cytogenetiska studier in vivo (murina benmärgsceller, efter oral administrering av flukonazol) och in vitro (humana lymfocyter exponerade för flukonazol vid 1000 mcg/ml) visade inga tecken på kromosomala mutationer.
Flukonazol påverkade inte fertiliteten hos han- eller honråttor som behandlades oralt med dagliga doser på 5 mg/kg, 10 mg/kg eller 20 mg/kg eller med parenterala doser på 5 mg/kg, 25 mg/kg eller 75 mg /kg, även om förlossningens början var något försenad vid 20 mg/kg PO. I en intravenös perinatal studie på råttor vid 5 mg/kg, 20 mg/kg och 40 mg/kg observerades dystoki och förlängning av förlossningen hos några få mödrar vid 20 mg/kg (ungefär 5 till 15 gånger den rekommenderade dosen för människor ) och 40 mg/kg, men inte vid 5 mg/kg. Förlossningsstörningarna återspeglades av en liten ökning av antalet dödfödda ungar och minskning av neonatal överlevnad vid dessa dosnivåer. Effekterna på förlossningen hos råttor överensstämmer med den artspecifika östrogen-sänkande egenskapen som produceras av höga doser av flukonazol. En sådan hormonförändring har inte observerats hos kvinnor som behandlats med flukonazol. (Ser KLINISK FARMAKOLOGI .)
Graviditet
Teratogena effekter
Potentiell för fosterskada
Användning under graviditet bör undvikas förutom hos patienter med allvarliga eller potentiellt livshotande svampinfektioner där flukonazol kan användas om den förväntade fördelen uppväger den möjliga risken för fostret. Ett fåtal publicerade fallrapporter beskriver ett mönster av distinkta medfödda anomalier hos spädbarn som exponerats i livmodern för högdos flukonazol hos modern (400 till 800 mg/dag) under större delen av eller hela den första trimestern. Dessa rapporterade anomalier liknar de som setts i djurstudier. Effektiva preventivmedel bör övervägas hos kvinnor i fertil ålder som behandlas med DIFLUCAN 400 till 800 mg/dag och bör fortsätta under hela behandlingsperioden och i cirka 1 vecka (5 till 6 halveringstider) efter den sista dosen. Om DIFLUCAN används under graviditet, eller om patienten blir gravid medan du tar läkemedlet, ska patienten informeras om den potentiella faran för fostret. Spontana aborter och medfödda abnormiteter har föreslagits som potentiella risker förknippade med 150 mg flukonazol som engångsdos eller upprepad dos under graviditetens första trimester baserat på retrospektiva epidemiologiska studier. Det finns inga adekvata och välkontrollerade studier av DIFLUCAN 150 mg på gravida kvinnor. (Ser VARNINGAR : Potential för fosterskada .)
Mänskliga data
Fallrapporter beskriver ett distinkt och sällsynt mönster av fosterskador bland spädbarn vars mödrar fick höga doser (400 till 800 mg/dag) flukonazol under större delen av eller hela graviditetens första trimester. De egenskaper som ses hos dessa spädbarn inkluderar brachycephaly, onormal ansiktsuttryck, onormal utveckling av calvarial, gomspalt, lårbensböjning, tunna revben och långa ben, arthrogryposis och medfödd hjärtsjukdom. Dessa effekter liknar de som setts i djurstudier.
Epidemiologiska studier tyder på en potentiell risk för spontan abort och medfödda abnormiteter hos spädbarn vars mödrar behandlades med 150 mg flukonazol som engångsdos eller upprepad dos under första trimestern, men dessa epidemiologiska studier har begränsningar och dessa fynd har inte bekräftats i kontrollerade kliniska studier prövningar.
Djurdata
Flukonazol administrerades oralt till dräktiga kaniner under organogenesen i två studier i doser på 5 mg/kg, 10 mg/kg och 20 mg/kg och vid 5 mg/kg, 25 mg/kg respektive 75 mg/kg. Moderns viktökning försämrades vid alla dosnivåer (ungefär 0,25 till 4 gånger den kliniska dosen på 400 mg baserat på kroppsyta [BSA] jämförelse), och aborter inträffade vid 75 mg/kg (ungefär 4 gånger den kliniska dosen på 400 mg baserat på BSA); inga negativa fostereffekter observerades.
flera studier där gravida råttor fick flukonazol oralt under organogenesen, försämrades moderns viktökning och placentans vikt ökade med 25 mg/kg. Det fanns inga fostereffekter vid 5 mg/kg eller 10 mg/kg; ökningar av fostrets anatomiska varianter (överflödiga revben, utvidgning av njurbäckenet) och förseningar i förbening observerades vid 25 mg/kg och 50 mg/kg och högre doser. Vid doser från 80 till 320 mg/kg (ungefär 2 till 8 gånger den kliniska dosen på 400 mg baserat på BSA), ökade embryodödligheten hos råttor och fosteravvikelser inkluderade vågiga revben, gomspalt och onormal kraniofacial förbening. Dessa effekter överensstämmer med hämningen av östrogensyntes hos råttor och kan vara ett resultat av kända effekter av sänkt östrogen på graviditet, organogenes och förlossning.
Ammande mödrar
Flukonazol fanns i låga nivåer i bröstmjölk efter administrering av en engångsdos på 150 mg, baserat på data från en studie på 10 ammande kvinnor som tillfälligt eller permanent avbröt amningen 5 dagar till 19 månader efter förlossningen. Den uppskattade dagliga spädbarnsdosen av flukonazol från bröstmjölk (med antagande av en genomsnittlig mjölkkonsumtion på 150 mL/kg/dag) baserad på den genomsnittliga maximala mjölkkoncentrationen (2,61 mcg/ml [intervall: 1,57 till 3,65 mcg/ml] 5,2 timmar efter dos) var 0,39 mg/kg/dag, vilket är cirka 13 % av den rekommenderade pediatriska dosen för orofaryngeal candidiasis. (Märkt pediatrisk dos är 6 mg/kg/dag den första dagen följt av 3 mg/kg/dag; uppskattad spädbarnsdos är 13 % av 3 mg/kg/dag underhållsdos). Det finns inga data om flukonazolnivåer i mjölk efter upprepad användning eller efter högdos flukonazol. En publicerad undersökning av 96 ammande kvinnor som behandlades med flukonazol 150 mg varannan dag (i genomsnitt 7,3 kapslar [intervall 1 till 29 kapslar]) för amningsrelaterad candida i brösten rapporterade inga allvarliga biverkningar hos spädbarn. Försiktighet bör iakttas när DIFLUCAN ges till en ammande kvinna.
Pediatrisk användning
En öppen, randomiserad, kontrollerad studie har visat att DIFLUCAN 100 mg är effektivt vid behandling av orofaryngeal candidiasis hos barn mellan 6 månader och 13 år. (Ser Kliniska studier .)
Användningen av DIFLUCAN 200 mg till barn med kryptokockmeningit, Candida-esofagit eller systemiska Candida-infektioner stöds av den effekt som visas för dessa indikationer hos vuxna och av resultaten från flera små icke-jämförande pediatriska kliniska studier. Dessutom farmakokinetiska studier på barn (se KLINISK FARMAKOLOGI ) har fastställt en dosproportionalitet mellan barn och vuxna. (Ser DOSERING OCH ADMINISTRERING .)
en icke-jämförande studie av barn med allvarliga systemiska svampinfektioner, varav de flesta var candidemia, var effekten av DIFLUCAN liknande den som rapporterats för behandling av candidemia hos vuxna. Av 17 försökspersoner med odlingsbekräftad candidemia, hade 11 av 14 (79 %) med baslinjesymtom (3 var asymtomatiska) ett kliniskt botemedel; 13/15 (87%) av de utvärderbara patienterna hade ett mykologiskt botemedel i slutet av behandlingen, men två av dessa patienter fick återfall 10 respektive 18 dagar efter avslutad behandling.
Effekten av DIFLUCAN för att undertrycka kryptokock-meningit var framgångsrik hos 4 av 5 barn som behandlades i en studie av flukonazol för behandling av livshotande eller allvarlig mykos. Det finns ingen information om effekten av flukonazol för primär behandling av kryptokock meningit hos barn.
Säkerhetsprofilen för DIFLUCAN 200 mg hos barn har studerats hos 577 barn i åldrarna 1 dag till 17 år som fick doser från 1 till 15 mg/kg/dag under 1 till 1 616 dagar. (Ser NEGATIVA REAKTIONER .)
Effekten av DIFLUCAN har inte fastställts hos spädbarn yngre än 6 månader. (Ser KLINISK FARMAKOLOGI .) Ett litet antal patienter (29) i åldern från 1 dag till 6 månader har behandlats säkert med DIFLUCAN.
Geriatrisk användning
Hos icke-AIDS-patienter rapporterades biverkningar möjligen relaterade till flukonazolbehandling hos färre patienter i åldern 65 år och äldre (9%, n =339) än för yngre patienter (14%, n=2240). Det fanns dock ingen konsekvent skillnad mellan de äldre och yngre patienterna med avseende på individuella biverkningar. Av de vanligast rapporterade (>1 %) biverkningarna förekom hudutslag, kräkningar och diarré i större andelar av äldre patienter. Liknande andelar äldre patienter (2,4 %) och yngre patienter (1,5 %) avbröt behandlingen med flukonazol på grund av biverkningar. Efter godkännandet för försäljning var spontana rapporter om anemi och akut njursvikt vanligare bland patienter 65 år eller äldre än hos patienter mellan 12 och 65 år. På grund av rapporternas frivilliga natur och den naturliga ökningen av förekomsten av anemi och njursvikt hos äldre är det dock inte möjligt att fastställa ett orsakssamband till läkemedelsexponering.
Kontrollerade kliniska prövningar av flukonazol inkluderade inte tillräckligt många patienter i åldern 65 år och äldre för att utvärdera om de svarar annorlunda än yngre patienter vid varje indikation. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter.
Flukonazol elimineras primärt genom renal utsöndring som oförändrat läkemedel. Eftersom äldre patienter är mer benägna att ha nedsatt njurfunktion, bör försiktighet iakttas för att justera dosen baserat på kreatininclearance. Det kan vara användbart att övervaka njurfunktionen. (Ser KLINISK FARMAKOLOGI och DOSERING OCH ADMINISTRERING .)
ÖVERDOS
Det har förekommit rapporter om överdosering av flukonazol åtföljd av hallucinationer och paranoid beteende.
I händelse av överdosering bör symtomatisk behandling (med stödjande åtgärder och magsköljning om det är kliniskt indicerat) sättas in.
Flukonazol utsöndras till stor del i urinen. En 3-timmars hemodialyssession minskar plasmanivåerna med cirka 50 %.
Hos möss och råttor som fick mycket höga doser av flukonazol inkluderade kliniska effekter hos båda arterna minskad motilitet och andning, ptos, tårbildning, salivutsöndring, urininkontinens, förlust av upprättande reflex och cyanos; döden föregicks ibland av kloniska kramper.
KONTRAINDIKATIONER
DIFLUCAN (flukonazol) är kontraindicerat till patienter som har visat överkänslighet mot flukonazol eller mot något av dess hjälpämnen. Det finns ingen information om korsöverkänslighet mellan flukonazol och andra antimykotisk azolmedel. Försiktighet bör iakttas vid förskrivning av DIFLUCAN till patienter med överkänslighet mot andra azoler. Samtidig administrering av andra läkemedel som är kända för att förlänga QT-intervallet och som metaboliseras via enzymet CYP3A4 såsom erytromycin, pimozid och kinidin är kontraindicerat hos patienter som får flukonazol. (Ser KLINISK FARMAKOLOGI : Läkemedelsinteraktionsstudier och FÖRSIKTIGHETSÅTGÄRDER .)
KLINISK FARMAKOLOGI
Farmakokinetik och metabolism
De farmakokinetiska egenskaperna för flukonazol är liknande efter administrering via intravenös eller oral administrering. Hos normala frivilliga är biotillgängligheten för oralt administrerat flukonazol över 90 % jämfört med intravenös administrering. Bioekvivalens fastställdes mellan 100 mg tabletten och båda suspensionsstyrkorna när de administrerades som en engångsdos på 200 mg.
Maximala plasmakoncentrationer (Cmax) hos fastande normala frivilliga inträffar mellan 1 och 2 timmar med en terminal plasmaelimineringshalveringstid på cirka 30 timmar (intervall: 20 till 50 timmar) efter oral administrering.
Hos fastande normala frivilliga leder administrering av en oral engångsdos på 400 mg DIFLUCAN (flukonazol) till ett genomsnittligt Cmax på 6,72 mcg/ml (intervall: 4,12 till 8,08 mcg/ml) och efter orala engångsdoser på 50 till 400 mg, flukonazol plasmakoncentrationer och area under plasmakoncentration-tidkurvan (AUC) är dosproportionella.
Cmax- och AUC-data från en mat-effektstudie som involverade administrering av DIFLUCAN (flukonazol) tabletter till friska frivilliga under fastande förhållanden och med en måltid med hög fetthalt indikerade att exponering för läkemedlet inte påverkas av mat. Därför kan DIFLUCAN tas utan hänsyn till måltider. (Ser DOSERING OCH ADMINISTRERING .)
Steady-state-koncentrationer uppnås inom 5 till 10 dagar efter orala doser på 50 till 400 mg som ges en gång dagligen. Administrering av en laddningsdos (på dag 1) på två gånger den vanliga dagliga dosen resulterar i plasmakoncentrationer nära steady-state den andra dagen. Den skenbara distributionsvolymen för flukonazol är ungefär den för totalt kroppsvatten. Plasmaproteinbindningen är låg (11 till 12%). Efter antingen enstaka eller flera orala doser i upp till 14 dagar tränger flukonazol in i alla studerade kroppsvätskor (se Bordet nedanför ). Hos normala frivilliga var salivkoncentrationerna av flukonazol lika med eller något högre än plasmakoncentrationerna oavsett dos, doseringsväg eller doseringslängd. Hos patienter med bronkiektasi var sputumkoncentrationerna av flukonazol efter en engångsdos på 150 mg lika med plasmakoncentrationerna både 4 och 24 timmar efter dosering. Hos patienter med svampmeningit är flukonazolkoncentrationerna i cerebrospinalvätskan (CSF) cirka 80 % av motsvarande plasmakoncentrationer.
En enstaka oral 150 mg dos av flukonazol administrerad till 27 patienter penetrerade in i vaginal vävnad, vilket resulterade i vävnad: plasmakvoter som sträckte sig från 0,94 till 1,14 under de första 48 timmarna efter dosering.
En oral engångsdos på 150 mg flukonazol administrerad till 14 patienter penetrerade in i vaginalvätskan, vilket resulterade i vätske: plasmakvoter som sträckte sig från 0,36 till 0,71 under de första 72 timmarna efter dosering.
Hos normala frivilliga elimineras flukonazol primärt genom renal utsöndring, med cirka 80 % av den administrerade dosen som oförändrat läkemedel i urinen. Cirka 11 % av dosen utsöndras i urinen som metaboliter.
Flukonazols farmakokinetik påverkas markant av reducerad njurfunktion. Det finns ett omvänt samband mellan eliminationshalveringstiden och kreatininclearance. Dosen av DIFLUCAN kan behöva minskas hos patienter med nedsatt njurfunktion. (Ser DOSERING OCH ADMINISTRERING .) En 3-timmars hemodialyssession minskar plasmakoncentrationerna med cirka 50 %.
Hos normala frivilliga associerades administrering av DIFLUCAN (doser från 200 mg till 400 mg en gång dagligen i upp till 14 dagar) med små och inkonsekventa effekter på testosteronkoncentrationer, endogena kortikosteroidkoncentrationer och det adrenokortikotropa hormonet (ACTH)-stimulerade kortisolsvaret.
Farmakokinetik hos barn
Hos barn har följande farmakokinetiska data {Mean (%cv)} rapporterats:
Clearance korrigerat för kroppsvikt påverkades inte av ålder i dessa studier. Genomsnittlig kroppsclearance hos vuxna rapporteras vara 0,23 (17 %) ml/min/kg.
Hos prematura nyfödda (gestationsålder 26 till 29 veckor) var medelvärdet (%cv) clearance inom 36 timmar efter födseln 0,180 (35 %, N=7) mL/min/kg, vilket ökade med tiden till ett medelvärde av 0,218 ( 31 %, N=9) mL/min/kg sex dagar senare och 0,333 (56 %, N=4) mL/min/kg 12 dagar senare. På liknande sätt var halveringstiden 73,6 timmar, vilket minskade med tiden till i genomsnitt 53,2 timmar sex dagar senare och 46,6 timmar 12 dagar senare.
Farmakokinetik hos äldre
En farmakokinetisk studie utfördes på 22 försökspersoner, 65 år eller äldre, som fick en engångsdos på 50 mg flukonazol. Tio av dessa patienter fick diuretika samtidigt. Cmax var 1,54 mcg/ml och inträffade 1,3 timmar efter dosering. Medel-AUC var 76,4 ± 20,3 mcg•h/ml, och den genomsnittliga terminala halveringstiden var 46,2 timmar. Dessa farmakokinetiska parametervärden är högre än analoga värden som rapporterats för normala unga frivilliga män. Samtidig administrering av diuretika förändrade inte signifikant AUC eller Cmax. Dessutom var kreatininclearance (74 ml/min), procenten av läkemedlet som återfanns oförändrat i urinen (0 till 24 timmar, 22%) och uppskattningarna av njurclearance för flukonazol (0,124 ml/min/kg) för äldre generellt sett lägre än yngre volontärer. Således tycks förändringen av flukonazoldispositionen hos äldre vara relaterad till nedsatt njurfunktion som är karakteristisk för denna grupp. En kurva över varje individs terminala eliminationshalveringstid kontra kreatininclearance jämfört med den förutsagda halveringstiden – kreatininclearance-kurvan härledd från normala försökspersoner och försökspersoner med olika grader av njurinsufficiens indikerade att 21 av 22 försökspersoner föll inom 95 % konfidensgräns för de förväntade halveringstiden-kreatininclearance-kurvorna. Dessa resultat överensstämmer med hypotesen att högre värden för de farmakokinetiska parametrarna som observerats hos äldre försökspersoner jämfört med normala unga frivilliga män beror på den minskade njurfunktionen som förväntas hos äldre.
Läkemedelsinteraktionsstudier
(Ser LÄKEMEDELSINTERAKTIONER )
Orala preventivmedel
Orala preventivmedel gavs som en engångsdos både före och efter oral administrering av DIFLUCAN 50 mg en gång dagligen i 10 dagar hos 10 friska kvinnor. Det fanns ingen signifikant skillnad i etinylöstradiol eller levonorgestrel AUC efter administrering av 50 mg DIFLUCAN. Den genomsnittliga ökningen av etinylöstradiol AUC var 6 % (intervall: –47 till 108 %) och levonorgestrel AUC ökade med 17 % (intervall: –33 till 141 %).
en andra studie fick tjugofem normala kvinnor dagliga doser av både 200 mg DIFLUCAN 150 mg tabletter eller placebo under två, tio dagar långa perioder. Behandlingscyklerna skilde sig med en månads mellanrum med alla försökspersoner som fick DIFLUCAN under en cykel och placebo under den andra. Ordningen för studiebehandlingen var slumpmässig. Enstaka doser av en p-piller innehållande levonorgestrel och etinylestradiol administrerades på den sista behandlingsdagen (dag 10) i båda cyklerna. Efter administrering av 200 mg DIFLUCAN var den genomsnittliga procentuella ökningen av AUC för levonorgestrel jämfört med placebo 25 % (intervall: – 12 till 82 %) och den genomsnittliga procentuella ökningen för etinylestradiol jämfört med placebo var 38 % (intervall: –11 till 101 %). Båda dessa ökningar skilde sig statistiskt signifikant från placebo.
En tredje studie utvärderade den potentiella interaktionen av en dosering av flukonazol 300 mg en gång i veckan till 21 normala kvinnor som tog ett oralt preventivmedel innehållande etinylestradiol och noretindron. I denna placebokontrollerade, dubbelblinda, randomiserade, tvåvägs överkorsningsstudie utförd under tre cykler av oral preventivmedelsbehandling, resulterade flukonazoldosering i små ökningar av medel-AUC för etinylöstradiol och noretindron jämfört med liknande placebodosering. Medel-AUC för etinylöstradiol och noretindron ökade med 24 % (95 % KI-intervall: 18 till 31 %) respektive 13 % (95 % KI-intervall: 8 till 18 %), jämfört med placebo. Behandling med flukonazol orsakade inte en minskning av etinylöstradiol AUC för någon enskild individ i denna studie jämfört med placebodosering. De individuella AUC-värdena för noretindron minskade mycket något (
Cimetidin
DIFLUCAN 100 mg administrerades som en enstaka oral dos enbart och två timmar efter en engångsdos av cimetidin 400 mg till sex friska frivilliga män. Efter administrering av cimetidin skedde en signifikant minskning av flukonazols AUC och Cmax. Det var en genomsnittlig ± SD-minskning av flukonazols AUC på 13 % ± 11 % (intervall: -3,4 till -31%) och Cmax minskade 19% ± 14% (intervall: -5 till -40) %). Administrering av cimetidin 600 mg till 900 mg intravenöst under en fyratimmarsperiod (från en timme före till 3 timmar efter en oral engångsdos av DIFLUCAN 200 mg) påverkade dock inte biotillgängligheten eller farmakokinetiken för flukonazol hos 24 friska manliga frivilliga. .
Antacida
Administrering av Maalox® (20 ml) till 14 normala frivilliga manliga försökspersoner omedelbart före en engångsdos av DIFLUCAN 100 mg hade ingen effekt på absorptionen eller elimineringen av flukonazol.
Hydroklortiazid
Samtidig oral administrering av 100 mg DIFLUCAN och 50 mg hydroklortiazid under 10 dagar hos 13 normala frivilliga resulterade i en signifikant ökning av flukonazols AUC och Cmax jämfört med DIFLUCAN givet ensamt. Det var en genomsnittlig ± SD-ökning av flukonazols AUC och Cmax på 45 % ± 31 % (intervall: 19 till 114 %) respektive 43 % ± 31 % (intervall: 19 till 122 %). Dessa förändringar tillskrivs en genomsnittlig ± SD-minskning i renalt clearance på 30 % ± 12 % (intervall: -10 till -50%).
Rifampin
Administrering av en oral engångsdos på 200 mg av DIFLUCAN 200 mg efter 15 dagars rifampin administrerat som 600 mg dagligen till åtta friska frivilliga manliga försökspersoner resulterade i en signifikant minskning av flukonazols AUC och en signifikant ökning av uppenbar oral clearance av flukonazol. Det var en genomsnittlig ± SD-reduktion av flukonazol AUC på 23 % ± 9 % (intervall: -13 till -42%). Synbar oral clearance av flukonazol ökade med 32 % ± 17 % (intervall: 16 till 72 %). Flukonazols halveringstid minskade från 33,4 ± 4,4 timmar till 26,8 ± 3,9 timmar. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Warfarin
Det var en signifikant ökning av protrombintidssvar (area under protrombintid-tid-kurvan) efter en singeldos warfarin (15 mg) administrerad till 13 normala manliga frivilliga efter oral DIFLUCAN 200 mg administrerad dagligen i 14 dagar jämfört med administreringen av enbart warfarin. Det fanns en genomsnittlig ± SD-ökning i protrombintidssvaret (area under protrombintid-tid-kurvan) på 7 % ± 4 % (intervall: – 2 till 13 %). (Ser FÖRSIKTIGHETSÅTGÄRDER .) Medelvärdet baseras på data från 12 försökspersoner eftersom en av 13 försökspersoner upplevde en 2-faldig ökning av sitt protrombintidssvar.
fenytoin
AUC för fenytoin bestämdes efter 4 dagars fenytoindosering (200 mg dagligen, oralt i 3 dagar följt av 250 mg intravenöst för en dos) både med och utan administrering av flukonazol (oral DIFLUCAN 200 mg dagligen i 16 dagar) hos 10 normala män frivilliga. Det fanns en signifikant ökning av fenytoins AUC. Den genomsnittliga ± SD-ökningen i fenytoin AUC var 88 % ± 68 % (intervall: 16 till 247 %). Den absoluta omfattningen av denna interaktion är okänd på grund av fenytoins inneboende olinjära disposition. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Cyklosporin
Cyklosporin AUC och Cmax bestämdes före och efter administrering av flukonazol 200 mg dagligen i 14 dagar hos åtta njurtransplanterade patienter som hade cyklosporinbehandling i minst 6 månader och på en stabil ciklosporindos i minst 6 veckor. Det fanns en signifikant ökning av ciklosporin AUC, Cmax, Cmin (24-timmarskoncentration) och en signifikant minskning av skenbart oralt clearance efter administrering av flukonazol. Den genomsnittliga ± SD-ökningen i AUC var 92 % ± 43 % (intervall: 18 till 147 %). Cmax ökade med 60 % ± 48 % (intervall: – 5 till 133 %). C ökade 157 % ± 96 % (intervall: 33 till 360 %). Det skenbara orala clearance minskade med 45 % ± 15 % (intervall: -15 till -60%). (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Zidovudin
Plasmakoncentrationer av zidovudin bestämdes vid två tillfällen (före och efter flukonazol 200 mg dagligen i 15 dagar) hos 13 frivilliga med AIDS eller ARC som fick en stabil zidovudindos i minst två veckor. Det fanns en signifikant ökning av zidovudin AUC efter administrering av flukonazol. Den genomsnittliga ± SD-ökningen i AUC var 20 % ± 32 % (intervall: – 27 till 104 %). Förhållandet mellan metaboliten, GZDV, och moderläkemedlet minskade signifikant efter administrering av flukonazol, från 7,6 ± 3,6 till 5,7 ± 2,2.
Teofyllin
Farmakokinetiken för teofyllin bestämdes från en intravenös engångsdos av aminofyllin (6 mg/kg) före och efter oral administrering av flukonazol 200 mg dagligen i 14 dagar hos 16 normala manliga frivilliga. Det fanns signifikanta ökningar av AUC, Cmax och halveringstid för teofyllin med en motsvarande minskning av clearance. Medelvärdet ± SD teofyllin AUC ökade med 21 % ± 16 % (intervall: – 5 till 48 %). Cmax ökade med 13 % ± 17 % (intervall: –13 till 40 %). Teofyllinclearance minskade med 16 % ± 11 % (intervall: –32 till 5%). Halveringstiden för teofyllin ökade från 6,6 ± 1,7 timmar till 7,9 ± 1,5 timmar. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Kinidin
Även om det inte har studerats in vitro eller in vivo, kan samtidig administrering av flukonazol och kinidin resultera i hämning av kinidinmetabolismen. Användning av kinidin har associerats med QT-förlängning och sällsynta förekomster av torsade de pointes. Samtidig administrering av flukonazol och kinidin är kontraindicerat. (Ser KONTRAINDIKATIONER och FÖRSIKTIGHETSÅTGÄRDER .)
Oral hypoglykemi
Effekterna av flukonazol på farmakokinetiken för de orala hypoglykemiska sulfonylureamedlen tolbutamid, glipizid och glyburid utvärderades i tre placebokontrollerade studier på normala frivilliga. Alla försökspersoner fick enbart sulfonylurean som en enstaka dos och igen som en engångsdos efter administrering av DIFLUCAN 100 mg dagligen i 7 dagar. I dessa tre studier upplevde 22/46 (47,8 %) av DIFLUCAN-behandlade patienter och 9/22 (40,1 %) av placebobehandlade patienter symtom som överensstämde med hypoglykemi. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Tolbutamid
Hos 13 normala frivilliga manliga försökspersoner fanns en signifikant ökning av AUC och Cmax för tolbutamid (500 mg engångsdos) efter administrering av flukonazol. Det var en genomsnittlig ± SD-ökning i tolbutamid AUC på 26 % ± 9 % (intervall: 12 till 39 %). Tolbutamid Cmax ökade med 11 % ± 9 % (intervall: -6 till 27%). (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Glipizid
AUC och Cmax för glipizid (2,5 mg engångsdos) ökade signifikant efter administrering av flukonazol hos 13 normala manliga frivilliga. Det var en genomsnittlig ± SD-ökning i AUC på 49 % ± 13 % (intervall: 27 till 73 %) och en ökning av Cmax på 19 % ± 23 % (intervall: – 11 till 79 %). (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Glyburide
AUC och Cmax för glyburid (5 mg enkeldos) ökade signifikant efter administrering av flukonazol hos 20 normala manliga frivilliga. Det var en genomsnittlig ± SD-ökning i AUC på 44 % ± 29 % (intervall: –13 till 115 %) och Cmax ökade med 19 % ± 19 % (intervall: –23 till 62 %). Fem försökspersoner behövde oral glukos efter intag av glyburid efter 7 dagars administrering av flukonazol. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Rifabutin
Det har publicerats rapporter om att en interaktion föreligger när flukonazol administreras samtidigt med rifabutin, vilket leder till ökade serumnivåer av rifabutin. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Takrolimus
Det har publicerats rapporter om att en interaktion föreligger när flukonazol administreras samtidigt med takrolimus, vilket leder till ökade serumnivåer av takrolimus. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Midazolam
Effekten av flukonazol på farmakokinetiken och farmakodynamiken för midazolam undersöktes i en randomiserad cross-over-studie på 12 frivilliga. I studien intog försökspersoner placebo eller 400 mg flukonazol på dag 1 följt av 200 mg dagligen från dag 2 till dag 6. Dessutom intogs en dos på 7,5 mg midazolam oralt den första dagen, 0,05 mg/kg administrerades intravenöst den fjärde dagen och 7,5 mg oralt den sjätte dagen. Flukonazol minskade clearance av IV midazolam med 51 %. På den första doseringsdagen ökade flukonazol AUC och C för midazolam med 259 % respektive 150 %. På den sjätte doseringsdagen ökade flukonazol AUC och C för midazolam med 259 % respektive 74 %. De psykomotoriska effekterna av midazolam ökade signifikant efter oral administrering av midazolam men påverkades inte signifikant efter intravenös midazolam.
En andra randomiserad, dubbeldummy, placebokontrollerad, överkorsningsstudie i tre faser utfördes för att fastställa effekten av administreringssätt för flukonazol på interaktionen mellan flukonazol och midazolam. I varje fas fick försökspersonerna oral flukonazol 400 mg och intravenös koksaltlösning; oral placebo och intravenös flukonazol 400 mg; och oral placebo och IV saltlösning. En oral dos på 7,5 mg midazolam intogs efter flukonazol/placebo. AUC och Cmax för midazolam var signifikant högre efter oral än IV administrering av flukonazol. Oralt flukonazol ökade midazolams AUC och Cmax med 272 % respektive 129 %. IV flukonazol ökade midazolams AUC och Cmax med 244 % respektive 79 %. Både oralt och IV flukonazol ökade de farmakodynamiska effekterna av midazolam. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Azitromycin
En öppen, randomiserad, trevägs crossover-studie på 18 friska försökspersoner utvärderade effekten av en enstaka 800 mg oral dos av flukonazol på farmakokinetiken för en enstaka 1200 mg oral dos av azitromycin samt effekterna av azitromycin på farmakokinetiken. av flukonazol. Det fanns ingen signifikant farmakokinetisk interaktion mellan flukonazol och azitromycin.
Vorikonazol
Vorikonazol är ett substrat för både CYP2C9 och CYP3A4 isoenzymer. Samtidig administrering av oral Voriconazol (400 mg Q12h under 1 dag, sedan 200 mg Q12h i 2,5 dagar) och oral flukonazol (400 mg på Dag 1, sedan 200 mg Q24h under 4 dagar) till 6 friska manliga försökspersoner resulterade i en ökning av Cmax och AUCτ för vorikonazol med i genomsnitt 57 % (90 % KI: 20 % till 107 %) respektive 79 % (90 % KI: 40 % till 128 %). I en uppföljande klinisk studie med 8 friska manliga försökspersoner eliminerade eller minskade inte reducerad dosering och/eller frekvens av vorikonazol och flukonazol denna effekt. Samtidig administrering av vorikonazol och flukonazol i alla doser rekommenderas inte. Noggrann övervakning av biverkningar relaterade till vorikonazol rekommenderas om vorikonazol används sekventiellt efter flukonazol, särskilt inom 24 timmar efter den sista dosen av flukonazol. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Tofacitinib
Samtidig administrering av flukonazol (400 mg på dag 1 och 200 mg en gång dagligen i 6 dagar [dagar 2–7]) och tofacitinib (30 mg engångsdos på dag 5) till friska försökspersoner resulterade i ökade genomsnittliga AUC- och Cmax-värden för tofacitinib på ca. 79 % (90 % KI: 64 % till 96 %) respektive 27 % (90 % KI: 12 % till 44 %) jämfört med administrering av enbart tofacitinib. (Ser FÖRSIKTIGHETSÅTGÄRDER .)
Mikrobiologi
Handlingsmekanism
Flukonazol är en mycket selektiv hämmare av svampcytokrom P450-beroende enzym lanosterol 14-α-demetylas. Detta enzym fungerar för att omvandla lanosterol till ergosterol. Den efterföljande förlusten av normala steroler korrelerar med ackumuleringen av 14-a-metylsteroler i svampar och kan vara ansvarig för den fungistatiska aktiviteten av flukonazol. Demetylering av däggdjursceller är mycket mindre känslig för flukonazolhämning.
Motstånd
En potential för utveckling av resistens mot flukonazol är välkänd. Svampisolat som uppvisar minskad känslighet för andra azoler kan också visa minskad känslighet för flukonazol. Frekvensen av läkemedelsresistensutveckling för de olika svampar som detta läkemedel är indicerat för är inte känd.
Flukonazolresistens kan uppstå från en modifiering av kvaliteten eller kvantiteten av målenzymet (lanosterol 14-α-demetylas), minskad tillgång till läkemedelsmålet eller någon kombination av dessa mekanismer.
Punktmutationer i genen (ERG11) som kodar för målenzymet leder till ett förändrat mål med minskad affinitet för azoler. Överuttryck av ERG11 resulterar i produktion av höga koncentrationer av målenzymet, vilket skapar behovet av högre intracellulära läkemedelskoncentrationer för att hämma alla enzymmolekyler i cellen.
Den andra huvudmekanismen för läkemedelsresistens involverar aktivt utflöde av flukonazol ut ur cellen genom aktivering av två typer av multiläkemedelsutflödestransportörer; de viktigaste facilitatorerna (kodade av MDR-gener) och de i den ATP-bindande kassettsuperfamiljen (kodas av CDR-gener). Uppreglering av MDR-genen leder till flukonazolresistens, medan uppreglering av CDR-gener kan leda till resistens mot flera azoler.
Resistens i Candida glabrata inkluderar vanligtvis uppreglering av CDR-gener vilket resulterar i resistens mot flera azoler. För ett isolat där den lägsta hämmande koncentrationen (MIC) är kategoriserad som Intermediär (16 till 32 mcg/ml), rekommenderas den högsta flukonazoldosen.
Candida krusei bör anses vara resistent mot flukonazol. Resistens hos C. krusei verkar förmedlas av reducerad känslighet hos målenzymet för hämning av medlet.
Det har förekommit rapporter om fall av superinfektion med andra Candida-arter än C. albicans, som ofta i sig inte är mottagliga för DIFLUCAN (t.ex. Candida krusei). Sådana fall kan kräva alternativ antimykotisk behandling.
Antimikrobiell aktivitet
Flukonazol har visat sig vara aktivt mot de flesta isolat av följande mikroorganismer både in vitro och vid kliniska infektioner.
Candida albicans Candida glabrata (Många isolat är medelkänsliga) Candida parapsilos Candida tropicalis Cryptococcus neoformans
Följande in vitro-data finns tillgängliga, men deras kliniska betydelse är okänd. Minst 90 % av följande svampar uppvisar en MIC in vitro som är mindre än eller lika med den känsliga brytpunkten för flukonazol (https://www.fda.gov/STIC) mot isolat av liknande släkte eller organismgrupp. Effektiviteten av flukonazol vid behandling av kliniska infektioner på grund av dessa svampar har dock inte fastställts i adekvata och välkontrollerade kliniska prövningar.
Candida dubliniensis Candida guilliermondii Candida kefyr Candida lusitaniae
Candida krusei bör anses vara resistent mot flukonazol. Resistens hos C. krusei verkar förmedlas av reducerad känslighet hos målenzymet för hämning av medlet.
Det har förekommit rapporter om fall av superinfektion med andra Candida-arter än C. albicans, som ofta i sig inte är mottagliga för DIFLUCAN (t.ex. Candida krusei). Sådana fall kan kräva alternativ antimykotisk behandling.
Känslighetstestning
För specifik information om tolkningskriterier för känslighetstest och tillhörande testmetoder och kvalitetskontrollstandarder som erkänns av FDA för detta läkemedel, se: https://www.fda.gov/STIC.
Kliniska studier
Cryptococcal meningit
I en multicenterstudie som jämförde DIFLUCAN (200 mg/dag) med amfotericin B (0,3 mg/kg/dag) för behandling av kryptokockmeningit hos patienter med AIDS, avslöjade en multivariat analys tre förbehandlingsfaktorer som förutspådde dödsfall under behandlingens gång: onormalt mental status, cerebrospinalvätskans kryptokockantigentiter högre än 1:1024 och cerebrospinalvätskans antal vita blodkroppar på mindre än 20 celler/mm³. Dödligheten bland högriskpatienter var 33 % och 40 % för amfotericin B- respektive DIFLUCAN-patienter (p=0,58), med totala dödsfall 14 % (9 av 63 försökspersoner) och 18 % (24 av 131 försökspersoner) för de två armarna av studien (p=0,48). Optimala doser och regimer för patienter med akut kryptokockmeningit och med hög risk för behandlingsmisslyckande återstår att fastställa. (Saag, et al. N Engl J Med 1992; 326:83-9.)
Vaginal candidiasis
Två adekvata och välkontrollerade studier utfördes i USA med 150 mg tabletten. I båda var resultaten av flukonazolregimen jämförbara med kontrollregimen (klotrimazol eller mikonazol intravaginalt i 7 dagar) både kliniskt och statistiskt vid utvärderingen en månad efter behandling.
Den terapeutiska botningsfrekvensen, definierad som en fullständig upplösning av tecken och symtom på vaginal candidiasis (klinisk bot), tillsammans med en negativ KOH-undersökning och negativ odling för Candida (mikrobiologisk utrotning), var 55 % i både flukonazolgruppen och de vaginala produkterna grupp.
Ungefär tre fjärdedelar av de inskrivna patienterna hade akut vaginit (
Avsevärt fler gastrointestinala händelser rapporterades i flukonazolgruppen jämfört med den vaginala produktgruppen. De flesta av händelserna var milda till måttliga. Eftersom flukonazol gavs som engångsdos inträffade inga utsättningar.
Pediatriska studier
Orofaryngeal candidiasis
En öppen, jämförande studie av effekten och säkerheten av DIFLUCAN (2 till 3 mg/kg/dag) och oralt nystatin (400 000 IE 4 gånger dagligen) på immunförsvagade barn med orofaryngeal candidiasis genomfördes. Kliniska och mykologiska svarsfrekvenser var högre hos barn som behandlades med flukonazol.
Klinisk bot i slutet av behandlingen rapporterades för 86 % av de flukonazolbehandlade patienterna jämfört med 46 % av de nystatinbehandlade patienterna. Mykologiskt hade 76 % av flukonazolbehandlade patienter den infekterande organismen utrotad jämfört med 11 % för nystatinbehandlade patienter.
Andelen patienter med kliniskt återfall 2 veckor efter avslutad behandling var 14 % för patienter som fick DIFLUCAN och 16 % för patienter som fick nystatin. Vid 4 veckor efter avslutad behandling var andelen patienter med kliniskt återfall 22 % för DIFLUCAN 150 mg och 23 % för nystatin.
PATIENTINFORMATION
DIFLUCAN® (färgämne-FLEW-kan) (flukonazol) Tabletter
Denna bipacksedel innehåller viktig information om DIFLUCAN. Det är inte menat att ersätta din vårdgivares instruktioner. Läs denna information noggrant innan du tar DIFLUCAN. Fråga din vårdgivare om du inte förstår någon av denna information eller om du vill veta mer om DIFLUCAN.
Vad är DIFLUCAN 100mg?
DIFLUCAN är ett receptbelagt läkemedel som används för att behandla vaginala svampinfektioner orsakade av en svamp som kallas Candida. DIFLUCAN 150mg hjälper till att stoppa för mycket jäst från att växa i slidan så att jästinfektionen försvinner.
DIFLUCAN 150mg skiljer sig från andra behandlingar för vaginal svampinfektion eftersom det är en tablett som tas genom munnen. DIFLUCAN används även för andra tillstånd. Den här broschyren handlar dock bara om att använda DIFLUCAN 50 mg för vaginal svampinfektion. För information om hur du använder DIFLUCAN 200mg av andra skäl, fråga din vårdgivare. Se avsnittet i denna broschyr för information om vaginal svampinfektion.
Vad är en vaginal svampinfektion?
Det är normalt att en viss mängd jäst finns i slidan. Ibland börjar för mycket jäst att växa i slidan och detta kan orsaka en svampinfektion. Vaginala svampinfektioner är vanliga. Ungefär tre av fyra vuxna kvinnor kommer att ha minst en vaginal svampinfektion under sitt liv.
Vissa mediciner och medicinska tillstånd kan öka din chans att få en svampinfektion. Om du är gravid, har diabetes, använder p-piller eller tar antibiotika kan du få svampinfektioner oftare än andra kvinnor. Personlig hygien och vissa typer av kläder kan öka dina chanser att få en svampinfektion. Fråga din vårdgivare om tips om vad du kan göra för att förhindra vaginal svampinfektion. Om du får en vaginal svampinfektion kan du ha något av följande symtom:
- klåda
- en brännande känsla när du kissar
- rodnad
- ömhet
- en tjock vit flytning från slidan som ser ut som keso
Ta inte DIFLUCAN om du.
- ta följande mediciner:
- kinidin
- erytromycin
- pimozid
- är allergisk mot flukonazol, den aktiva ingrediensen i DIFLUCAN 50 mg eller något av innehållsämnena i DIFLUCAN. Se slutet av denna patientinformationsbroschyr för en komplett lista över ingredienser i DIFLUCAN.
Innan du tar DIFLUCAN, berätta för din vårdgivare om alla dina medicinska tillstånd, om du:
- har leverproblem
- har njurproblem
- har hjärtproblem inklusive hjärtarytmier
- har hypokalemi (lågt kalium)
- är gravid eller planerar att bli gravid. Berätta omedelbart för din läkare om du blir gravid medan du tar DIFLUCAN. Du och din vårdgivare kommer att bestämma om DIFLUCAN 100mg är rätt för dig. Om du kan bli gravid bör du använda en preventivmetod (preventivmedel) medan du tar DIFLUCAN och i 1 vecka efter din sista dos.
- ammar eller planerar att amma. DIFLUCAN kan passera över i din bröstmjölk. Prata med din vårdgivare om det bästa sättet att mata ditt barn medan du tar DIFLUCAN.
Innan du börjar ta DIFLUCAN, berätta för din läkare om alla läkemedel du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Berätta särskilt för din vårdgivare om du tar:
- diabetesläkemedel som glyburid, tolbutamid, glipizid
- blodtrycksläkemedel som hydroklortiazid, losartan, amlodipin, verapamilnifedipin eller felodipin
- blodförtunnande medel som warfarin
- ciklosporin, takrolimus eller sirolimus (används för att förhindra avstötning av organtransplantationer)
- rifampin eller rifabutin för tuberkulos
- fenytoin eller karbamazepin för att kontrollera anfall
- teofyllin för att kontrollera astma
- kinidin (används för att korrigera störningar i hjärtrytmen)
- amiodaron (används för att behandla ojämna hjärtslag 'arytmier')
- amitriptylin eller nortriptylin för depression
- pimozid för psykiatrisk sjukdom
- amfotericin B eller vorikonazol för svampinfektioner
- erytromycin för bakteriella infektioner
- olaparib, cyklofosfamid eller vinca alkaloider såsom vinkristin eller vinblastin för behandling av cancer
- fentanyl, alfentanil eller metadon vid kronisk smärta
- ibrutinib används för att behandla blodcancer
- lemborexant, används för behandling av sömnlöshet
- lipidsänkande läkemedel såsom atorvastatin, simvastatin och fluvastatin
- icke-steroida antiinflammatoriska läkemedel inklusive celecoxib, ibuprofen och naproxen
- prednison, en steroid som används för att behandla hud-, gastrointestinala, hematologiska eller andningssjukdomar
- antivirala läkemedel som används för att behandla HIV som saquinavir eller zidovudin
- tofacitinib för reumatoid artrit
- vitamin A näringstillskott
- tolvaptan används för att behandla hyponatremi (låga nivåer av natrium i ditt blod) eller för att bromsa nedgången av njurfunktionen
Eftersom det finns många varumärken för dessa läkemedel, kontakta din vårdgivare eller apotekspersonal om du har några frågor.
Hur ska jag ta DIFLUCAN?
- Ta DIFLUCAN precis som din läkare säger åt dig.
- Ta DIFLUCAN 100 mg genom munnen med eller utan mat.
- Om du tar för mycket DIFLUCAN 50 mg, ring din vårdgivare eller gå till närmaste akutmottagning direkt.
Vad ska jag undvika när jag tar DIFLUCAN 150mg?
DIFLUCAN kan orsaka yrsel och kramper. Kör inte bil eller använd maskiner förrän du vet hur DIFLUCAN påverkar dig.
Vilka är de möjliga biverkningarna av DIFLUCAN 150mg?
DIFLUCAN 50mg kan orsaka allvarliga biverkningar inklusive:
- allvarliga leverproblem. Vissa personer med allvarliga medicinska problem har utvecklat allvarliga leverproblem som blev livshotande eller orsakade döden när de tog DIFLUCAN. Ibland kan dessa leverproblem vändas när du slutar ta DIFLUCAN. Berätta omedelbart för din vårdgivare om du har symtom på allvarliga leverproblem inklusive:
- mörkfärgad urin
- kraftig hudklåda
- gulfärgning av hud och ögon (gulsot)
- ljusa avföring
- trötthet
- kräkningar
- aptitlöshet
- allvarliga allergiska reaktioner: I sällsynta fall har allvarliga allergiska reaktioner (anafylaxi) inträffat när du tagit DIFLUCAN. Sluta ta DIFLUCAN 50mg, ring din vårdgivare eller gå till närmaste akutmottagning omedelbart om du får några tecken eller symtom på en allergisk reaktion inklusive:
- andnöd
- feber
- svullnad av ögonlocken
- hosta
- hudutslag, nässelutslag, blåsor eller hudflossning
- ansikte, mun, hals eller någon annan del av kroppen
- väsande andning
- bultande i hjärtat eller öronen
- frossa
- allvarliga hudproblem. Vissa personer med allvarliga medicinska problem har utvecklat allvarliga hudproblem som har orsakat döden när de tagit DIFLUCAN. Berätta genast för din läkare om du får utslag när du tar DIFLUCAN.
De vanligaste biverkningarna av DIFLUCAN 200mg inkluderar:
- huvudvärk
- yrsel
- diarre
- magont
- illamående eller orolig mage
- förändringar i hur maten smakar
Andra biverkningar inkluderar:
- binjurebarksvikt: Vissa personer som har tagit DIFLUCAN utvecklade binjurebarksvikt som var reversibel. Berätta genast för din vårdgivare om du har symtom på binjurebarksvikt inklusive:
- långvarig trötthet
- muskelsvaghet
- aptitlöshet
- viktminskning
- magont
- yrsel
- illamående
- kräkningar
- yrsel eller kramper.
Dessa är inte alla möjliga biverkningar av DIFLUCAN.
Ring din vårdgivare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara DIFLUCAN?
Förvara DIFLUCAN tabletter under 86°F (30°C).
Förvara DIFLUCAN 50 mg och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av DIFLUCAN.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en patientinformationsbroschyr. Använd inte DIFLUCAN 50 mg för ett tillstånd som det inte har ordinerats för. Ge inte DIFLUCAN till andra personer, även om de har samma symtom som du har. Det kan skada dem. Du kan be din vårdgivare om information om DIFLUCAN 200mg som är skriven för vårdpersonal.
Vilka är ingredienserna i DIFLUCAN 150mg?
Aktiv beståndsdel: flukonazol
Inaktiva Ingredienser: mikrokristallin cellulosa, vattenfritt dibasiskt kalciumfosfat, povidon, kroskarmellosnatrium, FD&C Red No. 40 aluminiumsjöfärgämne och magnesiumstearat.
Denna patientinformation har godkänts av US Food and Drug Administration
