Prometrium 100mg, 200mg Progesterone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Prometrium 100mg och hur används det?
Prometrium 200mg är ett receptbelagt läkemedel som används för att förebygga behandling av symtom på endometriehyperplasi och symtom på sekundär amenorré (avsaknad av mens eller mens). Prometrium kan användas ensamt eller tillsammans med andra läkemedel.
Prometrium tillhör en klass av läkemedel som kallas progestiner.
Det är inte känt om Prometrium 200mg är säkert och effektivt för barn.
Vilka är möjliga biverkningar av Prometrium?
Prometrium kan orsaka allvarliga biverkningar, inklusive:
- ovanlig vaginal blödning,
- smärta eller sveda vid urinering,
- bröstknöl,
- plötsliga synproblem,
- svår huvudvärk,
- smärta bakom ögonen,
- depression,
- sömnproblem,
- svaghet,
- humörförändringar,
- svår yrsel,
- dåsighet,
- snurrande känsla,
- förvirring,
- andnöd,
- bröstsmärtor eller tryck,
- smärta som sprider sig till käken eller axeln,
- illamående,
- svettas,
- ont i övre magen,
- klåda,
- trötthet,
- aptitlöshet,
- mörkfärgad urin,
- lerfärgad avföring,
- gulfärgning av huden eller ögonen (gulsot),
- plötslig domningar eller svaghet,
- plötslig svår huvudvärk,
- sluddrigt tal ,
- svårt att prata eller balansera,
- plötslig hosta,
- väsande andning,
- snabb andning,
- hosta blod,
- bensmärta,
- svullnad i benet, och
- värme eller rodnad i ett eller båda benen
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Prometrium 100mg inkluderar:
- dåsighet,
- yrsel,
- bröstsmärtor,
- humörförändringar,
- huvudvärk,
- förstoppning,
- diarre,
- halsbränna,
- uppblåsthet,
- svullnad i händer eller fötter,
- ledvärk,
- värmevallningar och
- flytningar från slidan
Tala om för din läkare om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Prometrium. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
Hjärt- och kärlsjukdomar, BRÖSTCANCER och TROLIG DEMENS FÖR ÖTROGEN PLUS PROGESTINTERAPI
Kardiovaskulära störningar och trolig demens
Östrogener plus gestagenbehandling bör inte användas för att förebygga hjärt-kärlsjukdom eller demens. (Ser Kliniska studier och VARNINGAR , Kardiovaskulära störningar och sannolik demens. )
Women's Health Initiative (WHI) östrogen plus gestagen delstudie rapporterade ökade risker för djup ventrombos, lungemboli, stroke och hjärtinfarkt hos postmenopausala kvinnor (50 till 79 år) under 5,6 års behandling med daglig oral konjugerad östrogener (CE) [0,625 mg] i kombination med medroxiprogesteronacetat (MPA) [2,5 mg], jämfört med placebo. (Ser Kliniska studier och VARNINGAR , Kardiovaskulära störningar. )
WHI Memory Study (WHIMS) östrogen plus progestin-undersökande studie av WHI rapporterade en ökad risk för att utveckla trolig demens hos postmenopausala kvinnor 65 år eller äldre under 4 års behandling med daglig CE (0,625 mg) kombinerat med MPA (2,5 mg) ), i förhållande till placebo. Det är okänt om detta fynd gäller yngre postmenopausala kvinnor. (Ser Kliniska studier och VARNINGAR , Trolig demens och FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning .)
Bröstcancer
WHI östrogen plus gestagen delstudie visade också en ökad risk för invasiv bröstcancer. (Ser Kliniska studier och VARNINGAR , Maligna neoplasmer, bröstcancer .)
I avsaknad av jämförbara data bör dessa risker antas vara likartade för andra doser av CE och MPA, och andra kombinationer och beredningsformer av östrogener och progestiner.
Progestiner med östrogener bör förskrivas i de lägsta effektiva doserna och för den kortaste varaktigheten som överensstämmer med behandlingens mål och risker för den enskilda kvinnan.
BESKRIVNING
PROMETRIUM (progesteron, USP) Kapslar innehåller mikroniserat progesteron för oral administrering. Progesteron har en molekylvikt på 314,47 och en molekylformel på C21H30O2. Progesteron (pregn-4-en-3, 20-dion) är ett vitt eller gräddvitt, luktfritt, kristallint pulver praktiskt taget olösligt i vatten, lösligt i alkohol, aceton och dioxan och svårlösligt i vegetabiliska oljor, stabilt i luft, smälter mellan kl. 126° och 131°C. Strukturformeln är:
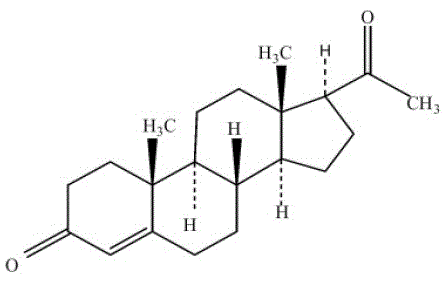
Progesteron syntetiseras från ett utgångsmaterial från en växtkälla och är kemiskt identisk med progesteron av mänskligt äggstocksursprung. PROMETRIUM kapslar finns i flera styrkor för att ge doseringsflexibilitet för optimal hantering. PROMETRIUM kapslar innehåller 100 mg eller 200 mg mikroniserat progesteron.
De inaktiva ingredienserna för PROMETRIUM Kapslar 100 mg inkluderar: jordnötsolja NF, gelatin NF, glycerin USP, lecitin NF, titandioxid USP, FD&C Red No. 40 och D&C Yellow No. 10. De inaktiva ingredienserna för PROMETRIUM 100 mg Capsules inkluderar 200 mg Capsules : jordnötsolja NF, gelatin NF, glycerin USP, lecitin NF, titandioxid USP, D&C Yellow No. 10 och FD&C Yellow No. 6.
INDIKATIONER
PROMETRIUM 200 mg kapslar är indicerade för användning för att förebygga endometriehyperplasi hos icke-hysterektomiserade postmenopausala kvinnor som får konjugerade östrogentabletter. De är också indikerade för användning vid sekundär amenorré.
DOSERING OCH ADMINISTRERING
Förebyggande av endometriehyperplasi
PROMETRIUM 100 mg kapslar ska ges som en engångsdos vid sänggåendet, 200 mg oralt i 12 dagar i följd per 28-dagarscykel, till en postmenopausal kvinna med livmoder som får dagliga konjugerade östrogentabletter.
Behandling av sekundär amenorré
PROMETRIUM 100 mg kapslar kan ges som en engångsdos på 400 mg vid sänggåendet i 10 dagar.
Vissa kvinnor kan uppleva svårigheter att svälja PROMETRIUM kapslar. För dessa kvinnor ska PROMETRIUM Capsules tas med ett glas vatten i stående position.
HUR LEVERERAS
PROMETRIUM (progesteron, USP) Kapslar 100 mg är runda, persikofärgade kapslar märkta med svart tryck "SV".
NDC 0032-1708-01 (flaska med 100)
PROMETRIUM (progesteron, USP) Kapslar 200 mg är ovala, blekt gulfärgade kapslar märkta med svart tryck "SV2".
NDC 0032-1711-01 (flaska med 100)
Förvara vid 25°C (77°F); utflykter tillåtna till 15° till 30°C (59° till 86°F) [Se USP kontrollerad rumstemperatur].
Skydda mot överdriven fukt.
Dispensera i tät, ljusbeständig behållare enligt definitionen i USP/NF, åtföljd av en patientinsats.
Förvara utom räckhåll för barn.
Tillverkad av: Catalent Pharma Solutions, St. Petersburg, FL 33716. Reviderad: sep 2013
BIEFFEKTER
Ser LÅDA VARNING , VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER .
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
I en multicenter, randomiserad, dubbelblind, placebokontrollerad klinisk studie studerades effekterna av PROMETRIUM 100 mg kapslar på endometriet hos totalt 875 postmenopausala kvinnor. Tabell 6 listar biverkningar större än eller lika med 2 procent av kvinnorna som fick cykliska PROMETRIUM-kapslar 200 mg dagligen (12 dagar per kalendermånadscykel) med 0,625 mg konjugerade östrogener eller placebo.
TABELL 6. Biverkningar (≥ 2 %) rapporterade i en placebokontrollerad studie med 875 patienter på postmenopausala kvinnor under en 3-årsperiod [Procentandel (%) av patienter som rapporterade]
Effekter på sekundär amenorré
I en multicenter, randomiserad, dubbelblind, placebokontrollerad klinisk studie studerades effekten av PROMETRIUM Capsules på sekundär amenorré hos 49 östrogenprimerade postmenopausala kvinnor. Tabell 7 listar biverkningar större än eller lika med 5 procent av kvinnorna som fick PROMETRIUM 100 mg kapslar eller placebo.
TABELL 7. Biverkningar (≥ 5 %) rapporterade hos patienter som använder 400 mg/dag i en placebokontrollerad studie på östrogenprimerade postmenopausala kvinnor
en multicenter, parallellgruppsöppen doseringsstudie efter marknadsföring bestående av tre på varandra följande 28-dagars behandlingscykler, randomiserades 220 premenopausala kvinnor med sekundär amenorré till att få daglig konjugerad östrogenbehandling (0,625 mg konjugerade östrogener) och PROMETRIUM3 mg,0mg,0mg,0mg,0mg. per dag (n=113) eller PROMETRIUM-kapslar, 400 mg per/dag (n=107) under 10 dagar av varje behandlingscykel. Sammantaget var de mest frekvent rapporterade behandlingsuppkomna biverkningarna, rapporterade hos mer än eller lika med 5 procent av försökspersonerna, illamående, trötthet, vaginal mykos, nasofaryngit, övre luftvägsinfektion, huvudvärk, yrsel, ömhet i brösten, utspänd buk, akne , dysmenorré, humörsvängningar och urinvägsinfektion.
Erfarenhet efter marknadsföring
Följande ytterligare biverkningar har rapporterats med PROMETRIUM 200 mg kapslar. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att tillförlitligt uppskatta frekvensen eller fastställa ett orsakssamband till läkemedelsexponering.
Genitourinary System
endometriekarcinom, hypospadi, intrauterin död, menorragi, menstruationsstörning, metrorragi, ovariecysta, spontan abort.
Kardiovaskulär
cirkulationskollaps, medfödd hjärtsjukdom (inklusive ventrikulär septumdefekt och patent ductus arteriosus), hypertoni, hypotoni, takykardi.
Gastrointestinala
akut pankreatit, kolestas, kolestatisk hepatit, dysfagi, leversvikt, levernekros, hepatit, ökade leverfunktionstester (inklusive ökat alaninaminotransferas, ökat aspartataminotransferas, ökat gamma-glutamyltransferas), gulsot, svullen tunga.
Hud
alopeci, klåda, urtikaria.
Ögon
dimsyn, dubbelsyn, synstörningar.
Centrala nervsystemet
aggression, kramper, depersonalisering, deprimerad medvetenhet, desorientering, dysartri, medvetslöshet, parestesi, sedering, stupor, synkope (med och utan hypotoni), övergående ischemisk attack, självmordstankar.
Under den första behandlingen har ett fåtal kvinnor upplevt en konstellation av många eller alla av följande symtom: extrem yrsel och/eller dåsighet, suddig syn, sluddrigt tal, svårigheter att gå, medvetslöshet, yrsel, förvirring, desorientering, berusningskänsla och andnöd.
Diverse
onormal gång, anafylaktisk reaktion, artralgi, ökat blodsocker, kvävning, läppspalt, gomspalt, gångsvårigheter, dyspné, ansiktsödem, onormal känsla av berusning, överkänslighet, astma, muskelkramper, stram hals, tinnitus, svindel, viktminskning , ökade vikten.
LÄKEMEDELSINTERAKTIONER
Interaktioner mellan läkemedel och laboratorietest
Följande laboratorieresultat kan förändras genom användning av östrogen plus gestagenbehandling:
- Ökad sulfobromoftaleinretention och andra leverfunktionstester.
- Koagulationstester: ökning av protrombinfaktorerna VII, VIII, IX och X.
- Pregnandiol bestämning.
- Sköldkörtelfunktion: ökning av PBI och butanol extraherbart proteinbundet jod och minskning av T3 upptagsvärden.
VARNINGAR
Ser LÅDA VARNING .
Kardiovaskulära störningar
En ökad risk för lungemboli, djup ventrombos (DVT), stroke och hjärtinfarkt har rapporterats med östrogen plus gestagenbehandling. Om något av dessa inträffar eller misstänks, bör östrogen med gestagenbehandling avbrytas omedelbart.
Riskfaktorer för arteriell kärlsjukdom (till exempel hypertoni, diabetes mellitus, tobaksanvändning, hyperkolesterolemi och fetma) och/eller venös tromboembolism (till exempel personlig historia eller familjehistoria av venös tromboembolism [VTE], fetma och systemisk lupus erythematosus ) bör hanteras på lämpligt sätt.
Stroke
I Women's Health Initiative (WHI) östrogen plus progestin-substudie rapporterades en statistiskt signifikant ökad risk för stroke hos kvinnor i åldern 50 till 79 år som fick daglig CE (0,625 mg) plus MPA (2,5 mg) jämfört med kvinnor i samma ålder grupp som fick placebo (33 mot 25 per 10 000 kvinnoår). Riskökningen påvisades efter det första året och fortsatte. (Ser Kliniska studier .) Om en stroke inträffar eller misstänks, bör östrogen plus gestagenbehandling avbrytas omedelbart.
Kranskärlssjukdom
WHI östrogen plus progestin-substudien rapporterades en statistiskt icke-signifikant ökad risk för koronar hjärtsjukdom (definierad som icke-fatal hjärtinfarkt [MI], tyst MI eller CHD-död) hos kvinnor som fick daglig CE (0,625) mg) plus MPA (2,5 mg) jämfört med kvinnor som får placebo (41 mot 34 per 10 000 kvinnoår). En ökning av relativ risk visades år 1 och en trend mot minskande relativ risk rapporterades år 2 till 5. (Se Kliniska studier .)
Hos postmenopausala kvinnor med dokumenterad hjärtsjukdom (n = 2 763, medelålder 66,7 år), i en kontrollerad klinisk prövning av sekundär prevention av hjärt-kärlsjukdom (Hjärta och östrogen/progestinersättningsstudie [HERS]), behandling med daglig CE (0,625 mg) plus MPA (2,5 mg) visade ingen kardiovaskulär fördel. Under en genomsnittlig uppföljning på 4,1 år minskade inte behandling med CE plus MPA den totala frekvensen av CHD-händelser hos postmenopausala kvinnor med etablerad kranskärlssjukdom. Det förekom fler CHD-händelser i den CE plus MPA-behandlade gruppen än i placebogruppen år 1, men inte under de efterföljande åren. Två tusen, tre hundra och tjugoen (2 321) kvinnor från den ursprungliga HERS-prövningen gick med på att delta i en öppen utökning av HERS, HERS II. Genomsnittlig uppföljning i HERS II var ytterligare 2,7 år, totalt 6,8 år totalt. Frekvensen av CHD-händelser var jämförbara bland kvinnor i CE plus MPA-gruppen och placebogruppen i HERS, HERS II och totalt sett.
Venös tromboembolism
I WHI östrogen plus gestagen substudie rapporterades en statistiskt signifikant 2 gånger högre frekvens av VTE (DVT och lungemboli [PE]) hos kvinnor som fick daglig CE (0,625 mg) plus MPA (2,5 mg) jämfört med kvinnor som fick placebo ( 35 mot 17 per 10 000 kvinnoår). Statistiskt signifikanta riskökningar för både DVT (26 mot 13 per 10 000 kvinnoår) och PE (18 mot 8 per 10 000 kvinnoår) visades också. Ökningen av VTE-risken påvisades under det första året och kvarstod. (Ser Kliniska studier .) Om en VTE uppstår eller misstänks, bör östrogen plus gestagenbehandling avbrytas omedelbart.
Om möjligt bör östrogener med gestagen avbrytas minst 4 till 6 veckor före operation av den typ som förknippas med en ökad risk för tromboembolism, eller under perioder av långvarig immobilisering.
Maligna neoplasmer
Bröstcancer
Den viktigaste randomiserade kliniska studien som ger information om bröstcancer hos användare av östrogen plus gestagen är Women's Health Initiative (WHI) delstudie av daglig CE (0,625 mg) plus MPA (2,5 mg). Efter en genomsnittlig uppföljning på 5,6 år rapporterade substudien med östrogen plus gestagen en ökad risk för invasiv bröstcancer hos kvinnor som tog dagligen CE plus MPA. I denna delstudie rapporterades tidigare användning av enbart östrogen eller östrogen plus gestagenbehandling av 26 procent av kvinnorna. Den relativa risken för invasiv bröstcancer var 1,24 (95 procent nCI, 1,01-1,54), och den absoluta risken var 41 mot 33 fall per 10 000 kvinnoår, för CE plus MPA jämfört med placebo. Bland kvinnor som rapporterade tidigare användning av hormonbehandling var den relativa risken för invasiv bröstcancer 1,86, och den absoluta risken var 46 mot 25 fall per 10 000 kvinnoår, för östrogen plus gestagen jämfört med placebo. Bland kvinnor som inte rapporterade någon tidigare användning av hormonbehandling var den relativa risken för invasiv bröstcancer 1,09, och den absoluta risken var 40 mot 36 fall per 10 000 kvinnoår för CE plus MPA jämfört med placebo. I samma delstudie var invasiva bröstcancer större, var mer benägna att vara nodpositiva och diagnostiserades i ett mer framskridet stadium i gruppen CE (0,625 mg) plus MPA (2,5 mg) jämfört med placebogruppen. Metastaserande sjukdom var sällsynt, utan någon uppenbar skillnad mellan de två grupperna. Andra prognostiska faktorer såsom histologisk subtyp, grad och hormonreceptorstatus skilde sig inte mellan grupperna. (Ser Kliniska studier .)
enlighet med WHI kliniska prövningar har observationsstudier också rapporterat en ökad risk för bröstcancer för behandling med östrogen plus gestagen, och en mindre ökad risk för enbart östrogenbehandling, efter flera års användning. Risken ökade med användningens varaktighet och verkade återgå till baslinjen under cirka 5 år efter avslutad behandling (endast observationsstudierna har betydande data om risken efter avslutad behandling). Observationsstudier tyder också på att risken för bröstcancer var större, och blev uppenbar tidigare, med östrogen plus gestagenbehandling jämfört med enbart östrogenbehandling. Dessa studier har emellertid i allmänhet inte funnit signifikant variation i risken för bröstcancer bland olika kombinationer, doser eller administreringssätt av östrogen plus gestagen.
Användning av östrogen plus gestagen har rapporterats resultera i en ökning av onormala mammografi som kräver ytterligare utvärdering. Alla kvinnor bör få årliga bröstundersökningar av en vårdgivare och utföra månatliga bröstsjälvundersökningar. Dessutom bör mammografiundersökningar schemaläggas baserat på patientens ålder, riskfaktorer och tidigare mammografiresultat.
Endometriecancer
En ökad risk för endometriecancer har rapporterats vid användning av oväntad östrogenbehandling hos en kvinna med livmoder. Den rapporterade risken för endometriecancer bland icke-opponerade östrogenanvändare är cirka 2 till 12 gånger större än hos icke-användare, och verkar vara beroende av behandlingens varaktighet och östrogendosen. De flesta studier visar ingen signifikant ökad risk förknippad med användning av östrogener under mindre än 1 år. Den största risken verkar vara förknippad med långvarig användning, med ökade risker på 15 till 24 gånger under 5 till 10 år eller mer och denna risk har visats kvarstå i minst 8 till 15 år efter att östrogenbehandlingen avbrutits.
Klinisk övervakning av alla kvinnor som använder östrogen plus gestagenbehandling är viktig. Adekvata diagnostiska åtgärder, inklusive riktad eller slumpmässig endometrieprovtagning när så är indicerat, bör vidtas för att utesluta malignitet i alla fall av odiagnostiserad ihållande eller återkommande onormal genital blödning. Det finns inga bevis för att användningen av naturliga östrogener resulterar i en annan endometrial riskprofil än syntetiska östrogener med motsvarande östrogendos. Att lägga till ett gestagen till östrogenbehandling hos postmenopausala kvinnor har visat sig minska risken för endometriehyperplasi, som kan vara en föregångare till endometriecancer.
Äggstockscancer
WHI östrogen plus gestagen delstudie rapporterade en statistiskt icke-signifikant ökad risk för äggstockscancer. Efter en genomsnittlig uppföljning på 5,6 år var den relativa risken för äggstockscancer för CE plus MPA jämfört med placebo 1,58 (95 procent nCI, 0,77 – 3,24). Den absoluta risken för CE plus MPA jämfört med placebo var 4 mot 3 fall per 10 000 kvinnoår. I vissa epidemiologiska studier har användningen av östrogen plus gestagen och endast östrogenprodukter, i synnerhet under 5 eller fler år, associerats med en ökad risk för äggstockscancer. Varaktigheten av exponeringen förknippad med ökad risk är dock inte konsekvent i alla epidemiologiska studier och vissa rapporterar inget samband.
Trolig demens
I östrogen plus progestin Women's Health Initiative Memory Study (WHIMS), en kompletterande studie av WHI, randomiserades en population av 4 532 postmenopausala kvinnor i åldern 65 till 79 år till daglig CE (0,625 mg) plus MPA (2,5 mg) eller placebo.
WHIMS-studien med östrogen plus gestagen, efter en genomsnittlig uppföljning på 4 år, diagnostiserades 40 kvinnor i CE plus MPA-gruppen och 21 kvinnor i placebogruppen med trolig demens. Den relativa risken för trolig demens för östrogen plus gestagen kontra placebo var 2,05 (95 procent KI, 1,21-3,48). Den absoluta risken för trolig demens för CE plus MPA jämfört med placebo var 45 mot 22 fall per 10 000 kvinnoår. Det är okänt om dessa fynd gäller yngre postmenopausala kvinnor. (Ser Kliniska studier och FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning .)
Synavvikelser
Retinal vaskulär trombos har rapporterats hos patienter som får östrogen. Avbryt behandlingen med östrogen plus gestagen i avvaktan på undersökning om det finns plötslig partiell eller fullständig synförlust eller om det plötsligt uppstår proptos, dubbelsidighet eller migrän. Om undersökning avslöjar papillödem eller retinala vaskulära lesioner, bör östrogen plus gestagenbehandling avbrytas permanent.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Tillägg av ett gestagen när en kvinna inte har genomgått en hysterektomi
Studier av tillsats av ett progestin under 10 eller fler dagar av en cykel av östrogenadministrering, eller dagligen med östrogen i en kontinuerlig regim, har rapporterat en lägre incidens av endometriehyperplasi än vad som skulle induceras av enbart östrogenbehandling. Endometriehyperplasi kan vara en föregångare till endometriecancer.
Det finns dock möjliga risker som kan vara förknippade med användning av gestagen med östrogener jämfört med enbart östrogen. Dessa inkluderar en ökad risk för bröstcancer.
Vätskeretention
Progesteron kan orsaka en viss grad av vätskeretention. Kvinnor med tillstånd som kan påverkas av denna faktor, såsom hjärt- eller njurdysfunktion, kräver noggrann observation.
Yrsel Och Dåsighet
PROMETRIUM Kapslar kan orsaka övergående yrsel och dåsighet och bör användas med försiktighet när du kör ett motorfordon eller använder maskiner. PROMETRIUM Kapslar ska tas som en daglig dos vid sänggåendet.
Patientinformation
Allmän
Denna produkt innehåller jordnötsolja och ska inte användas om du är allergisk mot jordnötter.
Läkare rekommenderas att diskutera innehållet i patientinformationsbroschyren med patienter som de förskriver PROMETRIUM 100 mg kapslar.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Progesteron har inte testats för cancerogenicitet hos djur via oral administreringsväg. När det implanterades i honmöss producerade progesteron bröstkarcinom, ovariegranulosacelltumörer och endometriestromala sarkom. Hos hundar gav långvariga intramuskulära injektioner nodulär hyperplasi och benigna och maligna brösttumörer. Subkutana eller intramuskulära injektioner av progesteron minskade latensperioden och ökade förekomsten av brösttumörer hos råttor som tidigare behandlats med ett kemiskt cancerframkallande ämne.
Progesteron visade inga tecken på genotoxicitet i in vitro-studier för punktmutationer eller för kromosomskador. In vivo-studier för kromosomskador har gett positiva resultat på möss vid orala doser på 1000 mg/kg och 2000 mg/kg. Exogent administrerat progesteron har visat sig hämma ägglossningen hos ett antal arter och det förväntas att höga doser som ges under en längre tid skulle försämra fertiliteten tills behandlingen upphör.
Graviditet
PROMETRIUM kapslar ska inte användas under graviditet. (Ser KONTRAINDIKATIONER ).
Graviditetskategori B
Reproduktionsstudier har utförts på möss i doser upp till 9 gånger den orala dosen för människor, på råttor i doser upp till 44 gånger den orala dosen för människor, på kaniner i en dos på 10 mikrogram/dag tillfört lokalt i livmodern med en implanterad enhet , hos marsvin i doser på ungefär hälften av den orala dosen för människor och hos rhesusapor vid doser ungefär den mänskliga dosen, allt baserat på kroppsyta, och har visat få eller inga tecken på nedsatt fertilitet eller fosterskada p.g.a. progesteron.
Vårdande kvinnor
Detekterbara mängder gestagen har identifierats i mjölken hos ammande kvinnor som får gestagen. Försiktighet bör iakttas när PROMETRIUM 100 mg kapslar administreras till en ammande kvinna.
Pediatrisk användning
PROMETRIUM kapslar är inte indicerat för barn. Kliniska studier har inte utförts på den pediatriska populationen.
Geriatrisk användning
Det har inte varit tillräckligt många geriatriska kvinnor involverade i kliniska studier med PROMETRIUM kapslar för att avgöra om de över 65 år skiljer sig från yngre försökspersoner i deras svar på PROMETRIUM 200 mg kapslar.
The Women's Health Initiative Study
I Women's Health Initiative (WHI) östrogen plus gestagen substudie (daglig CE [0,625 mg] plus MPA [2,5 mg] jämfört med placebo), fanns det en högre relativ risk för icke-fatal stroke och invasiv bröstcancer hos kvinnor äldre än 65 år . (Ser Kliniska studier och VARNINGAR , Kardiovaskulära störningar och Maligna neoplasmer. )
The Women's Health Initiative Memory Study
I Women's Health Initiative Memory Study (WHIMS) av postmenopausala kvinnor i åldern 65 till 79 år, fanns det en ökad risk för att utveckla trolig demens i östrogen plus gestagen understudie jämfört med placebo. (Ser Kliniska studier och VARNINGAR , Trolig demens. )
ÖVERDOS
Inga studier på överdosering har utförts på människor. Vid överdosering ska PROMETRIUM kapslar sättas ut och patienten behandlas symtomatiskt.
KONTRAINDIKATIONER
PROMETRIUM Kapslar ska inte användas till kvinnor med något av följande tillstånd:
KLINISK FARMAKOLOGI
PROMETRIUM 200mg kapslar är en oral doseringsform av mikroniserat progesteron som är kemiskt identiskt med progesteron av äggstocksursprung. Den orala biotillgängligheten av progesteron ökar genom mikronisering.
Farmakokinetik
Absorption
Efter oral administrering av progesteron som en mikroniserad mjukgelatinkapselformulering uppnåddes maximala serumkoncentrationer inom 3 timmar. Den absoluta biotillgängligheten för mikroniserat progesteron är inte känd. Tabell 1 sammanfattar de genomsnittliga farmakokinetiska parametrarna hos postmenopausala kvinnor efter fem orala dagliga doser av PROMETRIUM Kapslar 100 mg som en mikroniserad mjukgelatinkapselformulering.
TABELL 1. Farmakokinetiska parametrar för PROMETRIUM 200 mg kapslar
Serumprogesteronkoncentrationerna verkade linjära och dosproportionella efter administrering av flera doser av PROMETRIUM 200 mg kapslar 100 mg över dosintervallet 100 mg per dag till 300 mg per dag hos postmenopausala kvinnor. Även om doser över 300 mg per dag inte studerades hos kvinnor, verkade serumkoncentrationer från en studie på frivilliga manliga försökspersoner linjära och dosproportionella mellan 100 mg per dag och 400 mg per dag. De farmakokinetiska parametrarna hos frivilliga manliga försökspersoner överensstämde generellt med de som sågs hos postmenopausala kvinnor.
Distribution
Progesteron är cirka 96 procent till 99 procent bundet till serumproteiner, främst till serumalbumin (50 till 54 procent) och transkortin (43 till 48 procent).
Ämnesomsättning
Progesteron metaboliseras huvudsakligen av levern till pregnandioler och pregnanoloner. Pregnandioler och pregnanoloner konjugeras i levern till glukuronid- och sulfatmetaboliter. Progesteronmetaboliter som utsöndras i gallan kan dekonjugeras och kan metaboliseras ytterligare i tarmen via reduktion, dehydroxylering och epimerisering.
Exkretion
Glukuronid- och sulfatkonjugaten av pregnandiol och pregnanolon utsöndras i gallan och urinen. Progesteronmetaboliter elimineras huvudsakligen via njurarna. Progesteronmetaboliter som utsöndras i gallan kan genomgå enterohepatisk återvinning eller kan utsöndras i avföringen.
Särskilda populationer
Farmakokinetiken för PROMETRIUM kapslar har inte utvärderats hos patienter med låg kroppsvikt eller fetma.
Leverinsufficiens
Effekten av nedsatt leverfunktion på farmakokinetiken för PROMETRIUM 100 mg kapslar har inte studerats.
Njurinsufficiens
Effekten av nedsatt njurfunktion på farmakokinetiken för PROMETRIUM kapslar har inte studerats.
Interaktion mellan mat och läkemedel
Samtidigt intag av föda ökade biotillgängligheten av PROMETRIUM 100 mg kapslar i förhållande till ett fastande tillstånd när det administrerades till postmenopausala kvinnor i en dos på 200 mg.
Läkemedelsinteraktioner
Metabolismen av progesteron av humana levermikrosomer hämmades av ketokonazol (IC50
Samtidig administrering av konjugerade östrogener och PROMETRIUM 200 mg kapslar till 29 postmenopausala kvinnor under en 12-dagarsperiod resulterade i en ökning av totala östronkoncentrationer (Cmax 3,68 ng/mL till 4,93 ng/ml) och totala ekvilinkoncentrationer (Cmax 32,2 mL till 7 ng/2 mL) ng/ml) och en minskning av cirkulerande 17β-östradiolkoncentrationer (Cmax 0,037 ng/ml till 0,030 ng/ml). Halveringstiden för de konjugerade östrogenerna var liknande vid samtidig administrering av PROMETRIUM-kapslar. Tabell 2 sammanfattar de farmakokinetiska parametrarna.
TABELL 2. Farmakokinetiska medelparametrar (± SD) för östradiol, östron och ekvilin efter samtidig administrering av konjugerade östrogener 0,625 mg och PROMETRIUM-kapslar 200 mg under 12 dagar till postmenopausala kvinnor
Kliniska studier
Effekter På Endometriet
en randomiserad, dubbelblind klinisk prövning fick 358 postmenopausala kvinnor, var och en med en intakt livmoder, behandling i upp till 36 månader. Behandlingsgrupperna var: PROMETRIUM-kapslar i dosen 200 mg per dag under 12 dagar per 28-dagarscykel i kombination med konjugerade östrogener 0,625 mg per dag (n=120); konjugerade östrogener endast 0,625 mg per dag (n=119); eller placebo (n=119). Försökspersonerna i alla tre behandlingsgrupperna var främst kaukasiska kvinnor (87 procent eller mer av varje grupp). Resultaten för incidensen av endometriehyperplasi hos kvinnor som får upp till 3 års behandling visas i tabell 3. En jämförelse mellan behandlingsgruppen PROMETRIUM Capsules plus konjugerade östrogener med gruppen endast med konjugerade östrogener visade en signifikant lägre frekvens av hyperplasi (6 procent) kombinationsprodukt kontra 64 procent enbart östrogen) i behandlingsgruppen PROMETRIUM Capsules plus konjugerade östrogener under 36 månaders behandling.
TABELL 3. Incidens av endometriehyperplasi hos kvinnor som får 3 års behandling
Tiderna till diagnos av endometriehyperplasi under 36 månaders behandling visas i figur 1. Denna figur illustrerar grafiskt att andelen patienter med hyperplasi var signifikant större för gruppen konjugerade östrogener (64 procent) jämfört med gruppen konjugerade östrogener plus PROMETRIUM Capsules (6 procent).
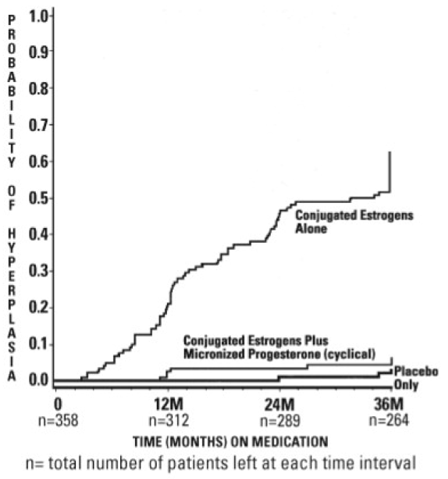
Figur 1. Tid till hyperplasi hos kvinnor som får upp till 36 månaders behandling
Avbrottsfrekvensen på grund av hyperplasi under de 36 månaderna av behandling visas i tabell 4. För alla grader av hyperplasi var avbrottsfrekvensen för patienter som fick konjugerade östrogener plus PROMETRIUM 100 mg kapslar liknande den för placebogruppen, medan Avbrottsfrekvensen för patienter som fick enbart konjugerade östrogener var signifikant högre. Kvinnor som permanent avbröt behandlingen på grund av hyperplasi liknade demografin som den totala studiepopulationen.
TABELL 4. Avbrottsfrekvens på grund av hyperplasi under 36 månaders behandling
Effekter på sekundär amenorré
en enkelcenter, randomiserad, dubbelblind klinisk studie som inkluderade premenopausala kvinnor med sekundär amenorré under minst 90 dagar, resulterade administrering av 10 dagars behandling med PROMETRIUM 200 mg kapslar i att 80 procent av kvinnorna fick abstinensblödningar inom 7 dagar efter den senaste dos PROMETRIUM 100 mg kapslar, 300 mg per dag (n=20), jämfört med 10 procent av kvinnorna som fick abstinensblödning i placebogruppen (n=21).
I en multicenter, parallellgruppsöppen, postmarketingdoseringsstudie som inkluderade premenopausala kvinnor med sekundär amenorré under minst 90 dagar, administrering av 10 dagars PROMETRIUM 100 mg kapslar under två 28-dagars behandlingscykler, 300 mg per dag (n= 107) eller 400 mg per dag (n=99), resulterade i att 73,8 procent respektive 76,8 procent av kvinnorna fick abstinensblödningar.
Hastigheten av sekretorisk transformation utvärderades i en multicenter, randomiserad, dubbelblind klinisk studie på östrogen-primade postmenopausala kvinnor. PROMETRIUM 100 mg kapslar administrerade oralt i 10 dagar med 400 mg per dag (n=22) inducerade fullständiga sekretoriska förändringar i endometriet hos 45 procent av kvinnorna jämfört med 0 procent i placebogruppen (n=23).
En andra multicenter, parallell-grupp, öppen doseringsstudie efter marknadsföring på premenopausala kvinnor med sekundär amenorré under minst 90 dagar utvärderade också graden av sekretorisk transformation. Alla försökspersoner fick dagliga orala konjugerade östrogener under 3 på varandra följande 28-dagars behandlingscykler och PROMETRIUM-kapslar, 300 mg per dag (n=107) eller 400 mg per dag (n=99) under 10 dagar av varje behandlingscykel. Graden av fullständig sekretorisk transformation var 21,5 procent respektive 28,3 procent.
Studier av initiativ för kvinnors hälsa
Women's Health Initiative (WHI) registrerade cirka 27 000 övervägande friska postmenopausala kvinnor i två delstudier för att bedöma riskerna och fördelarna med dagliga orala konjugerade östrogener (CE) [0,625 mg] - ensamma eller i kombination med medroxiprogesteronacetat (MPA) [2,5 mg] jämfört med placebo för att förebygga vissa kroniska sjukdomar. Det primära effektmåttet var incidensen av kranskärlssjukdom [(CHD) definierad som icke-fatal hjärtinfarkt (MI), tyst hjärtinfarkt och CHD-död], med invasiv bröstcancer som det primära negativa resultatet. Ett "globalt index" inkluderade den tidigaste förekomsten av CHD, invasiv bröstcancer, stroke, lungemboli (PE), endometriecancer (endast i CE plus MPA-substudien), kolorektal cancer, höftfraktur eller död på grund av annan orsak. Dessa delstudier utvärderade inte effekterna av CE-ensamt eller CE plus MPA på klimakteriebesvär.
WHI Estrogen Plus Progestin Substudie
WHI östrogen plus gestagen delstudien stoppades tidigt. Enligt den fördefinierade stoppregeln, efter en genomsnittlig uppföljning av 5,6 års behandling, översteg den ökade risken för bröstcancer och kardiovaskulära händelser de specificerade fördelarna som ingår i det "globala indexet". Den absoluta överrisken för händelser i det ”globala indexet” var 19 per 10 000 kvinnoår.
För de utfall som ingår i WHI "globala index" som nådde statistisk signifikans efter 5,6 års uppföljning, var de absoluta överriskerna per 10 000 kvinnoår i gruppen som behandlades med CE plus MPA 7 fler CHD-händelser, 8 fler stroke, 10 fler PEs och 8 fler invasiva bröstcancer, medan de absoluta riskminskningarna per 10 000 kvinnoår var 6 färre kolorektalcancer och 5 färre höftfrakturer.
Resultaten av östrogen plus gestagen-substudien, som inkluderade 16 608 kvinnor (genomsnitt 63 år, intervall 50 till 79; 83,9 procent vita, 6,8 procent svarta, 5,4 procent latinamerikanska, 3,9 procent övriga) presenteras i tabell 5. Dessa resultat återspeglas centralt. bedömd data efter en genomsnittlig uppföljning på 5,6 år.
TABELL 5. Relativ och absolut risk sett i Estrogen Plus Progestin-substudien av WHI vid ett genomsnitt på 5,6 år a, b
Tidpunkten för initiering av östrogen plus gestagenbehandling i förhållande till början av klimakteriet kan påverka den övergripande risk-nyttoprofilen. WHI östrogen plus gestagen delstudie stratifierad för ålder visade hos kvinnor 50 till 59 år en icke-signifikant trend mot att minska risken för total dödlighet [hazard ratio (HR) 0,69 (95 procent CI, 0,44-1,07)].
Women's Health Initiative Memory Study
The estrogen plus progestin Women's Health Initiative Memory Study (WHIMS), en kompletterande studie av WHI, inkluderade 4 532 övervägande friska postmenopausala kvinnor 65 år och äldre (47 procent var 65 till 69 år gamla; 35 procent var 70 till 74 år gamla) ålder, och 18 procent var 75 år och äldre) för att utvärdera effekterna av daglig CE (0,625 mg) plus MPA (2,5 mg) på förekomsten av trolig demens (primärt utfall) jämfört med placebo.
Efter en genomsnittlig uppföljning på 4 år var den relativa risken för trolig demens för CE plus MPA kontra placebo 2,05 (95 procent KI, 1,21 – 3,48). Den absoluta risken för trolig demens för CE plus MPA jämfört med placebo var 45 mot 22 per 10 000 kvinnoår. Trolig demens som definieras i denna studie inkluderade Alzheimers sjukdom (AD), vaskulär demens (VaD) och blandad typ (med egenskaper av både AD och VaD). Den vanligaste klassificeringen av sannolik demens i behandlingsgruppen och placebogruppen var AD. Eftersom den kompletterande studien genomfördes på kvinnor i åldern 65 till 79 år är det okänt om dessa fynd gäller yngre postmenopausala kvinnor. (Ser VARNINGAR , Trolig demens och FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning .)
PATIENTINFORMATION
PROMETRIUM® (progesteron, USP) Kapslar 100 mg & 200 mg
Läs denna PATIENTINFORMATION innan du börjar ta PROMETRIUM 200 mg kapslar och läs vad du får varje gång du fyller på ditt recept på PROMETRIUM 100 mg kapslar. Det kan komma ny information. Denna information ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling.
VILKEN ÄR DEN VIKTIGASTE INFORMATIONEN JAG BÖR VETA OM PROMETRIUM 100mg KAPSLAR (ett progesteronhormon)?
- Progestiner med östrogener bör inte användas för att förhindra hjärtsjukdomar, hjärtinfarkter, stroke eller demens.
- Att använda progestiner med östrogener kan öka din chans att få hjärtinfarkt, stroke, bröstcancer och blodproppar.
- Att använda progestiner med östrogener kan öka din chans att få demens, baserat på en studie av kvinnor 65 år och äldre.
- Du och din vårdgivare bör prata regelbundet om huruvida du fortfarande behöver behandling med PROMETRIUM 100 mg kapslar.
DENNA PRODUKT INNEHÅLLER JORDNÖTOLJA OCH BÖR INTE ANVÄNDAS OM DU ÄR ALLERGISK MOT JORDNÖTTER.
Vad är PROMETRIUM 200mg kapslar?
PROMETRIUM 100mg kapslar innehåller det kvinnliga hormonet progesteron.
Vad används PROMETRIUM 100mg kapslar till?
Behandling av menstruationsrubbningar
PROMETRIUM 200 mg kapslar används för behandling av sekundär amenorré (avsaknad av menstruation hos kvinnor som tidigare haft menstruation) på grund av en minskning av progesteron. När du inte producerar tillräckligt med progesteron kan menstruationsrubbningar uppstå. Om din vårdgivare har fastställt att din kropp inte producerar tillräckligt med progesteron på egen hand, kan PROMETRIUM 200 mg kapslar ordineras för att ge det progesteron du behöver.
Skydd av endometrium (slemhinnan i livmodern)
PROMETRIUM 200mg kapslar används i kombination med östrogenhaltiga mediciner hos en postmenopausal kvinna med livmoder (livmoder). Att ta östrogen ensamt ökar chansen att utveckla ett tillstånd som kallas endometriehyperplasi som kan leda till cancer i livmoderns slemhinna (livmodern). Tillsats av ett gestagen rekommenderas generellt för en kvinna med livmoder för att minska risken för att få cancer i livmodern (livmodern).
Vem bör inte ta PROMETRIUM kapslar?
Börja inte ta PROMETRIUM kapslar om du:
- Är allergisk mot jordnötter
- Har ovanlig vaginal blödning
- Har för närvarande eller har haft vissa cancerformer Behandling med östrogen plus gestagen kan öka risken för att få vissa typer av cancer, inklusive cancer i bröstet eller livmodern. Om du har eller har haft cancer, prata med din vårdgivare om huruvida du ska ta PROMETRIUM Capsules.
- Fick en stroke eller hjärtinfarkt
- Har för närvarande eller har haft blodproppar
- Har för närvarande eller har haft leverproblem
- Är allergisk mot PROMETRIUM-kapslar eller någon av dess ingredienser Se listan över ingredienser i PROMETRIUM 200 mg kapslar i slutet av denna bipacksedel.
- Tror du kan vara gravid
Berätta för din vårdgivare:
- Om du ammar. Hormonet i PROMETRIUM 100 mg kapslar kan passera över i din bröstmjölk.
- Om alla dina medicinska problem. Din vårdgivare kan behöva kontrollera dig mer noggrant om du har vissa tillstånd, såsom astma (väsande andning), epilepsi (kramper), diabetes, migrän, endometrios, lupus, problem med ditt hjärta, lever, sköldkörtel eller njurar, eller har höga kalciumnivåer i ditt blod.
- Om alla mediciner du tar. Detta inkluderar receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Vissa läkemedel kan påverka hur PROMETRIUM 100 mg kapslar fungerar. PROMETRIUM Kapslar kan också påverka hur dina andra läkemedel fungerar.
Hur ska jag ta PROMETRIUM 200mg kapslar?
Vilka är de möjliga biverkningarna av PROMETRIUM kapslar?
Biverkningar är grupperade efter hur allvarliga de är och hur ofta de inträffar när du behandlas:
Allvarliga men mindre vanliga biverkningar inkluderar:
- Risk för fostret: Fall av gomspalt, läppspalt, hypospadi, ventrikulär septumdefekt, patenterad ductus arteriosus och andra medfödda hjärtfel.
- Onormal blodpropp: Stroke, hjärtinfarkt, lungemboli, synförlust eller blindhet.
Några av varningstecknen på allvarliga biverkningar inkluderar:
- Förändringar i syn eller tal
- Plötsligt ny kraftig huvudvärk
- Svår smärta i bröstet eller benen med eller utan andnöd, svaghet och trötthet
- Yrsel och matthet
- Kräkningar
Ring din vårdgivare omedelbart om du får något av dessa varningstecken eller andra ovanliga symtom som berör dig.
Mindre allvarliga, men vanliga biverkningar inkluderar:
- Huvudvärk
- Bröstsmärtor
- Oregelbunden vaginal blödning eller stänkblödning
- Mag- eller bukkramper, uppblåsthet
- Illamående och kräkningar
- Håravfall
- Vätskeretention
- Vaginal svampinfektion
Dessa är inte alla möjliga biverkningar av PROMETRIUM 200 mg kapslar. För mer information, fråga din vårdgivare eller apotekspersonal om råd om biverkningar. Du kan rapportera biverkningar till AbbVie Inc. på 1-800-633-9110 eller till FDA på 1-800-FDA-1088.
Vad kan jag göra för att minska mina chanser att få en allvarlig biverkning med PROMETRIUM 100mg kapslar?
- Prata med din vårdgivare regelbundet om huruvida du ska fortsätta att ta PROMETRIUM 100 mg kapslar.
- Kontakta din läkare omedelbart om du får ovanlig vaginal blödning när du tar PROMETRIUM Capsules.
- Gör en bäckenundersökning, bröstundersökning och mammografi (bröströntgen) varje år om inte din vårdgivare säger något annat till dig. Om medlemmar av din familj har haft bröstcancer eller om du någonsin har haft bröstklumpar eller en onormal mammografi, kan du behöva genomgå bröstundersökningar oftare.
- Om du har högt blodtryck, högt kolesterol (fett i blodet), diabetes, är överviktig, eller om du använder tobak, kan du ha högre chans att få hjärtsjukdom. Fråga din vårdgivare om sätt att minska dina chanser att få hjärtsjukdom.
Allmän information om säker och effektiv användning av PROMETRIUM kapslar
- Läkemedel skrivs ibland ut för tillstånd som inte nämns i patientinformationsblad. Ta inte PROMETRIUM kapslar för tillstånd som det inte ordinerats för.
- Din vårdgivare har ordinerat detta läkemedel för dig och dig ensam. Ge inte PROMETRIUM kapslar till andra personer, även om de har samma symtom som du har. Det kan skada dem.
- PROMETRIUM 200 mg kapslar ska tas som en daglig dos vid sänggåendet. Vissa kvinnor kan uppleva extrem yrsel och/eller dåsighet under den första behandlingen. I några få fall kan symtom inkludera dimsyn, svårt att tala, svårigheter att gå och att känna sig onormal. Om du upplever dessa symtom, diskutera dem med din läkare omedelbart.
- Var försiktig när du kör ett motorfordon eller använder maskiner eftersom yrsel eller dåsighet kan uppstå.
Förvara PROMETRIUM kapslar utom räckhåll för barn.
Denna broschyr ger en sammanfattning av den viktigaste informationen om PROMETRIUM 100 mg kapslar. Om du vill ha mer information, prata med din vårdgivare eller apotekspersonal. Du kan be om information om PROMETRIUM 100mg kapslar som är skriven för vårdpersonal. Du kan få mer information genom att ringa det avgiftsfria numret 1-800-633-9110.
Vilka är ingredienserna i PROMETRIUM kapslar?
Aktiv ingrediens: 100 mg eller 200 mg mikroniserat progesteron
De inaktiva ingredienserna i PROMETRIUM Kapslar 100 mg inkluderar: jordnötsolja NF, gelatin NF, glycerin USP, lecitin NF, titandioxid USP, FD&C Red No. 40 och D&C Yellow No. 10.
De inaktiva ingredienserna i PROMETRIUM Kapslar 200 mg inkluderar: jordnötsolja NF, gelatin NF, glycerin USP, lecitin NF, titandioxid USP, D&C Yellow No. 10 och FD&C Yellow No. 6.
HUR LEVERERAS
PROMETRIUM 200mg Kapslar 100 mg är runda, persikofärgade kapslar märkta med svart tryck "SV".
PROMETRIUM 100 mg kapslar 200 mg är ovala, blekt gulfärgade kapslar märkta med svart tryck "SV2".
Förvara vid 25°C (77°F); utflykter tillåtna till 15° till 30°C (59° till 86°F) [Se USP kontrollerad rumstemperatur].
