Parlodel 2.5mg Bromocriptine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Parlodel och hur används det?
Parlodel 2,5 mg är ett receptbelagt läkemedel som används för att behandla symtom på hyperprolaktinemi-associerade dysfunktioner, Parkinsons sjukdom, akromegali. Parlodel 2,5 mg kan användas ensamt eller tillsammans med andra läkemedel.
Parlodel 2,5 mg tillhör en klass av läkemedel som kallas antiparkinsonmedel, dopaminagonister; Hyperprolaktinemi; Metaboliska och endokrina, Övriga.
Det är inte känt om Parlodel 2,5 mg är säkert och effektivt för barn yngre än 10 år.
Vilka är de möjliga biverkningarna av Parlodel?
Parlodel kan orsaka allvarliga biverkningar inklusive:
- nässelfeber,
- svårt att andas,
- svullnad av ansikte, läppar, tunga eller svalg,
- synproblem,
- konstant rinnande näsa,
- bröstsmärta,
- smärta när du andas,
- snabb puls,
- snabb andning,
- andnöd,
- ryggont,
- svullnad i anklar eller fötter,
- kissa mindre eller inte alls,
- förvirring,
- hallucinationer,
- yrsel,
- huvudvärk,
- hunger,
- svaghet,
- svettas,
- skakningar,
- irritabilitet,
- koncentrationssvårigheter,
- ofrivilliga muskelrörelser,
- förlust av balans eller koordination,
- blodig eller tjäraktig avföring,
- hosta blod,
- kräks som ser ut som kaffesump,
- svår huvudvärk,
- suddig syn,
- surrar i dina öron,
- ångest,
- förvirring,
- bröstsmärta,
- andnöd,
- ojämna hjärtslag, och
- anfall
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Parlodel 2,5 mg inkluderar:
- yrsel,
- snurrande känsla,
- lätt dåsighet,
- trötthet,
- lätt huvudvärk,
- deppigt humör,
- sömnproblem (sömnlöshet),
- torr mun,
- Täppt i näsan,
- orolig mage,
- illamående,
- kräkningar,
- magont,
- aptitlöshet,
- diarre,
- förstoppning och
- kall känsla eller domningar i fingrarna
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Parlodel. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
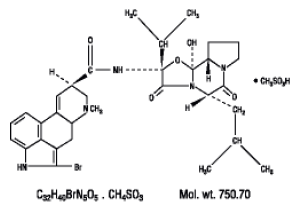
BESKRIVNING
Parlodel® (bromokriptinmesylat) är ett ergotderivat med potent dopaminreceptoragonistaktivitet. Varje Parlodel® (bromokriptinmesylat) SnapTabs® tablett för oral administrering innehåller 2½ mg och varje kapsel innehåller 5 mg bromokriptin (som mesylat). Bromokriptinmesylat är kemiskt betecknat som Ergotaman-3',6',18-trion, 2-bromo-12'-hydroxi-2'-(1-methylethyl)-5'-( 2-metylpropyl)-, (5'a)-monometansulfonat (salt).
Strukturformeln är:
2½ mg SnapTabs®
Aktiv beståndsdel: bromokriptinmesylat, USP
Inaktiva Ingredienser: kolloidal kiseldioxid, laktos, magnesiumstearat, povidon, stärkelse och en annan ingrediens
5 mg kapslar
Aktiv beståndsdel: bromokriptinmesylat, USP
Inaktiva Ingredienser: kolloidal kiseldioxid, gelatin, laktos, magnesiumstearat, röd järnoxid, kiseldioxid, natriumlaurylsulfat, stärkelse, titandioxid, gul järnoxid och en annan ingrediens
INDIKATIONER
Hyperprolaktinemi-associerade dysfunktioner
Parlodel (bromokriptinmesylat) är indicerat för behandling av dysfunktioner i samband med hyperprolaktinemi Inklusive amenorré med eller utan galaktorré, infertilitet eller hypogonadism . Parlodel 2,5 mg behandling är indicerad till patienter med prolaktinutsöndrande adenom , vilket kan vara den grundläggande underliggande endokrinopatin som bidrar till ovanstående kliniska presentationer. Minskning i tumörstorlek har visats hos både manliga och kvinnliga patienter med makroadenom. I fall där adenektomi väljs kan en behandlingskur med Parlodel 2,5 mg användas för att minska tumörmassan före operation.
Akromegali
Parlodel 2,5 mg terapi är indicerat för behandling av akromegali. Parlodelterapi, ensam eller som tilläggsbehandling med bestrålning av hypofysen eller kirurgi, minskar serumtillväxthormonet med 50 % eller mer hos cirka ½ av de behandlade patienterna, men vanligtvis inte till normala nivåer.
Eftersom effekterna av extern hypofysstrålning kanske inte blir maximal på flera år, erbjuder tilläggsbehandling med Parlodel 2,5 mg potentiella fördelar innan effekterna av bestrålning visar sig.
Parkinsons sjukdom
Parlodel 2,5 mg SnapTabs eller kapslar är indicerade för behandling av tecken och symtom på idiopatisk eller postencefalitisk Parkinsons sjukdom. Som tilläggsbehandling till levodopa (enbart eller tillsammans med en perifer dekarboxylashämmare), kan Parlodel-behandling ge ytterligare terapeutiska fördelar för de patienter som för närvarande hålls på optimala doser av levodopa, de som börjar försämras (utvecklar tolerans) mot levodopabehandling, och de som upplever "slut på dossvikt" på levodopabehandling. Parlodel 2,5 mg-behandling kan tillåta en minskning av underhållsdosen av levodopa och kan således lindra förekomsten och/eller svårighetsgraden av biverkningar i samband med långvarig levodopabehandling såsom onormala ofrivilliga rörelser (t.ex. dyskinesier) och de markanta svängningarna i motorfunktion ("on-off"-fenomen). Fortsatt effekt av Parlodel 2,5 mg-behandling under behandling på mer än 2 år har inte fastställts.
Data är otillräckliga för att utvärdera potentiell nytta av att behandla nydiagnostiserad Parkinsons sjukdom med Parlodel. Studier har dock visat signifikant fler biverkningar (särskilt illamående, hallucinationer, förvirring och hypotoni) hos Parlodel-behandlade patienter än hos levodopa/karbidopa-behandlade patienter. Patienter som inte svarar på levodopa är dåliga kandidater för Parlodel-behandling.
DOSERING OCH ADMINISTRERING
Allmän
Det rekommenderas att Parlodel (bromokriptinmesylat) tas med mat. Patienter bör utvärderas ofta under dosökning för att fastställa den lägsta dos som ger ett terapeutiskt svar.
Hyperprolaktinemiska indikationer
Den initiala dosen av Parlodel SnapTabs till vuxna är en ½ till en 2½ mg tablett med skåror dagligen. Ytterligare en 2½ mg tablett kan läggas till behandlingsregimen som tolereras var 2:e till 7:e dag tills ett optimalt terapeutiskt svar uppnås. Den terapeutiska dosen varierade från 2,5-15 mg dagligen hos vuxna studerade kliniskt.
Baserat på begränsade data från barn i åldern 11 till 15, (se Pediatrisk användning ) startdosen är en ½ till en 2½ mg skårad tablett dagligen. Doseringen kan behöva ökas när den tolereras tills ett terapeutiskt svar uppnås. Den terapeutiska dosen varierade från 2,5-10 mg dagligen till barn med prolaktinutsöndrande hypofysadenom.
För att minska sannolikheten för långvarig exponering för Parlodels om en oförtänkt graviditet inträffar, ska ett mekaniskt preventivmedel användas tillsammans med Parlodel 2,5 mg-behandling tills normala ägglossningsmenstruationscykler har återställts. Preventivmedel kan sedan avbrytas hos patienter som önskar graviditet.
Därefter, om menstruationen inte inträffar inom 3 dagar efter det förväntade datumet, bör behandlingen med Parlodel 2,5 mg avbrytas och ett graviditetstest utföras.
Akromegali
Praktiskt taget alla akromegala patienter som får terapeutisk nytta av Parlodel 2,5 mg har också minskningar i cirkulerande nivåer av tillväxthormon. Därför kommer periodisk bedömning av cirkulerande nivåer av tillväxthormon i de flesta fall att fungera som en vägledning för att fastställa den terapeutiska potentialen för Parlodel. Om, efter en kort prövning med Parlodel-behandling, ingen signifikant minskning av tillväxthormonnivåerna har skett, bör noggrann bedömning av sjukdomens kliniska egenskaper göras, och om ingen förändring har skett, bör dosjustering eller avbrytande av behandlingen övervägas. .
Den initiala rekommenderade dosen är en ½ till en 2½ mg Parlodel SnapTabs tablett vid pensionering (med mat) i 3 dagar. Ytterligare en ½ till 1 SnapTabs-tablett ska läggas till behandlingsregimen som tolereras var 3:e till 7:e dag tills patienten får optimal terapeutisk nytta. Patienterna bör omvärderas varje månad och dosen justeras baserat på minskningar av tillväxthormon eller kliniskt svar. Det vanliga optimala terapeutiska dosintervallet för Parlodel varierar från 20-30 mg/dag hos de flesta patienter. Den maximala dosen bör inte överstiga 100 mg/dag.
Patienter som behandlas med bestrålning av hypofysen bör avbrytas från Parlodel 2,5 mg-behandling på årsbasis för att bedöma både de kliniska effekterna av strålning på sjukdomsprocessen och effekterna av Parlodel-behandlingen. Vanligtvis är en 4 till 8 veckors karensperiod tillräcklig för detta ändamål. Återkommande tecken/symtom eller ökningar av tillväxthormon tyder på att sjukdomsprocessen fortfarande är aktiv och ytterligare kurer med Parlodel bör övervägas.
Parkinsons sjukdom
Grundprincipen för Parlodel 2,5 mg-behandling är att initiera behandling med en låg dos och, på individuell basis, öka den dagliga dosen långsamt tills maximalt terapeutiskt svar uppnås. Doseringen av levodopa under denna introduktionsperiod bör bibehållas om möjligt. Initialdosen av Parlodel 2,5 mg är en ½ av en 2½ mg SnapTabs tablett två gånger dagligen i samband med måltid. Bedömningar rekommenderas med 2 veckors intervall under dostitrering för att säkerställa att den lägsta dosen som ger ett optimalt terapeutiskt svar inte överskrids. Om nödvändigt kan dosen ökas var 14:e till 28:e dag med 2½ mg/dag i samband med måltid. Om det skulle vara tillrådligt att minska dosen av levodopa på grund av biverkningar, bör den dagliga dosen av Parlodel, om den ökas, utföras gradvis i små (2½ mg) steg.
Säkerheten för Parlodel har inte visats i doser som överstiger 100 mg/dag.
HUR LEVERERAS
Parlodel (Bromocriptine Mesylate) SnapTabs
2½ mg
Parlodel finns i flaskor innehållande 30 och 100 tabletter à 2 ½ mg, varje flaska innehåller ett torkmedel.
Runda, benvita SnapTabs med fasad kant, som var och en innehåller 2½ mg bromokriptin (som mesylatet). Graverad "PARLODEL 2½" på ena sidan och "017" på den skårade sidan. Uppfyller USP-upplösningstest 1.
Paket om 30 - NDC 30698-202-30 Paket om 100 - NDC 30698-202-01
Parlodel (Bromocriptine Mesylate) Kapslar
5 mg
Karamell och vita kapslar, som var och en innehåller 5 mg bromokriptin (som mesylatet). Tryckt med rött bläck "PARLODEL 5 mg" på ena halvan och "102" på andra halvan.
Paket om 30 - NDC 30698-201-30 Paket om 100 - NDC 30698-201-01
Förvara Och Dispensera
Förvara vid 68° till 77°F (20° till 25°C); utflykter tillåtna till 59° till 86°F (15° till 30°C) [Se USP Controlled Room Temperature].
Dispensera i en tät, ljusbeständig behållare.
Tillverkad för och distribuerad av: Validus Pharmaceuticals LLC Parsippany, NJ 07054. Reviderad: juli 2021
BIEFFEKTER
Biverkningar från kliniska prövningar
Hyperprolaktinemiska indikationer
Förekomsten av biverkningar är ganska hög (69 %) men dessa är i allmänhet milda till måttliga. Behandlingen avbröts hos cirka 5 % av patienterna på grund av biverkningar. Dessa i fallande frekvens är: illamående (49%), huvudvärk (19%), yrsel (17%), trötthet (7%), yrsel (5%), kräkningar (5%), magkramper (4%) , nästäppa (3%), förstoppning (3%), diarré (3%) och dåsighet (3%).
En lätt hypotensiv effekt kan åtfölja behandling med Parlodel (bromokriptinmesylat). Förekomsten av biverkningar kan minskas genom att tillfälligt minska dosen till ½ SnapTabs tablett 2 eller 3 gånger dagligen. Ett fåtal fall av cerebrospinalvätska-rinorré har rapporterats hos patienter som fått Parlodel 2,5 mg för behandling av stora prolaktinom. Detta har inträffat i sällsynta fall, vanligtvis endast hos patienter som tidigare har genomgått transsfenoidal kirurgi, hypofysstrålning eller båda och som fått Parlodel 2,5 mg för återfall av tumör. Det kan också förekomma hos tidigare obehandlade patienter vars tumör sträcker sig in i sinus sphenoid.
Akromegali
De vanligaste biverkningarna hos akromegala patienter som behandlades med Parlodel 2,5 mg var: illamående (18 %), förstoppning (14 %), postural/ortostatisk hypotoni (6 %), anorexi (4 %), muntorrhet/nästäppa (4 %). %), matsmältningsbesvär/dyspepsi (4%), digital vasospasm (3%), dåsighet/trötthet (3%) och kräkningar (2%).
Mindre frekventa biverkningar (mindre än 2%) var: gastrointestinala blödningar, yrsel, exacerbation av Raynauds syndrom, huvudvärk och synkope. I sällsynta fall (mindre än 1%) håravfall, alkoholpotentiering, svimning, yrsel, arytmi, ventrikulär takykardi, minskat sömnbehov, synhallucinationer, trötthet, andnöd, bradykardi, svindel, parestesi, tröghet, vasovagal attack, vanföreställningspsykos, paranoid , sömnlöshet, tung huvudenhet, minskad tolerans mot kyla, stickningar i öron, blekhet i ansiktet och muskelkramper har rapporterats.
Parkinsons sjukdom
kliniska prövningar där Parlodel 2,5 mg administrerades med samtidig minskning av dosen levodopa/karbidopa, var de vanligaste nytillkomna biverkningarna: illamående, onormala ofrivilliga rörelser, hallucinationer, förvirring, "on-off"-fenomen, yrsel, dåsighet, svimning/svimning, kräkningar, asteni, bukbesvär, synstörningar, ataxi, sömnlöshet, depression, hypotoni, andnöd, förstoppning och svindel.
Mindre vanliga biverkningar som kan uppstå inkluderar: anorexi, ångest, blefarospasm, muntorrhet, dysfagi, ödem i fötter och vrister, erytromelalgi, epileptiforma anfall, trötthet, huvudvärk, letargi, fläckar i huden, nästäppa mardrömmar, nervositet, parestesi, hudutslag, urinfrekvens, urininkontinens, urinretention och i sällsynta fall tecken och symtom på ergotism såsom stickningar i fingrar, kalla fötter, domningar, muskelkramper i fötter och ben eller förvärring av Raynauds syndrom.
Avvikelser i laboratorietester kan innefatta förhöjda ureakväve i blodet, SGOT, SGPT, GGPT, CPK, alkaliskt fosfatas och urinsyra, som vanligtvis är övergående och inte av klinisk betydelse.
Biverkningar från eftermarknadsföring
Följande biverkningar har rapporterats under användning av Parlodel efter godkännande (alla indikationer kombinerade). Eftersom biverkningar från spontana rapporter rapporteras frivilligt från en population av osäker storlek är det i allmänhet inte möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Psykiatriska störningar: Förvirring, psykomotorisk agitation/excitation, hallucinationer, psykotiska störningar, sömnlöshet, ökning av libido, hypersexualitet och impulskontroll/tvångsmässiga beteenden (inklusive spel, utgifter och andra intensiva drifter).
Störningar i nervsystemet: Huvudvärk, dåsighet, yrsel, dyskinesi, somnolens, parestesi, överdriven somnolens dagtid, plötslig sömn.
Ögonbesvär: Synstörning, suddig syn.
Öron- och labyrintsjukdomar: Tinnitus.
Hjärtsjukdomar: Perikardiell effusion, sammandragande perikardit, takykardi, bradykardi, arytmi, hjärtklafffibros.
Vaskulära störningar: Hypotension, ortostatisk hypotoni (vilkar mycket sällan till synkope), reversibel blekhet hos fingrar och tår inducerad av kyla (särskilt hos patienter med Raynauds fenomen i anamnesen).
Andningsvägar, bröstkorg och mediastinum: Nästäppa, pleurautgjutning, pleural fibros, pleurit, lungfibros, dyspné.
Gastrointestinala störningar: Illamående, förstoppning, kräkningar, muntorrhet, diarré, buksmärtor, retroperitoneal fibros, gastrointestinala sår, gastrointestinala blödningar.
Hud och subkutan vävnad: Allergiska hudreaktioner, håravfall.
Muskuloskeletala och bindvävssjukdomar: Benkramper.
Allmänna symtom och tillstånd på administreringsstället: Trötthet, perifert ödem, ett syndrom som liknar malignt neuroleptikasyndrom vid plötsligt utsättande av Parlodel, abstinenssymtom (inklusive apati, ångest, depression, trötthet, sömnlöshet, svettning och smärta) med nedtrappning eller efter utsättning (se FÖRSIKTIGHETSÅTGÄRDER ).
Biverkningar observerade under andra förhållanden
Postpartumpatienter (se ovan VARNINGAR )
postpartumstudier med Parlodel 2,5 mg hade 23 procent av de behandlade postpartumpatienterna minst 1 biverkning, men de var i allmänhet milda till måttliga i graden. Behandlingen avbröts hos cirka 3 % av patienterna. De vanligast förekommande biverkningarna var: huvudvärk (10 %), yrsel (8 %), illamående (7 %), kräkningar (3 %), trötthet (1,0 %), synkope (0,7 %), diarré (0,4 %) och kramper (0,4%). Blodtryckssänkningar (≥ 20 mm Hg systoliskt och ≥ 10 mm Hg diastoliskt) förekom hos 28 % av patienterna minst en gång under de första 3 dagarna efter förlossningen; dessa var vanligtvis av övergående karaktär. Rapporter om svimning under puerperiet kan möjligen vara relaterade till denna effekt. Enligt erfarenheter efter marknadsföring i USA inkluderar allvarliga biverkningar rapporterade 72 fall av anfall (inklusive 4 fall av status epilepticus), 30 fall av stroke och 9 fall av hjärtinfarkt bland postpartumpatienter. Anfallsfall åtföljdes inte nödvändigtvis av utveckling av hypertoni. En outtröttlig och ofta progressivt svår huvudvärk, ibland åtföljd av synstörningar, ofta föregås av timmar till dagar många fall av anfall och/eller stroke. De flesta patienter hade inte visat några tecken på någon av de hypertensiva störningarna under graviditeten inklusive eklampsi, preeklampsi eller graviditetsinducerad hypertoni. Ett fall av stroke var associerat med sagittal sinustrombos och ett annat var associerat med cerebral och cerebellär vaskulit. Ett fall av hjärtinfarkt var associerat med oförklarlig disseminerad intravaskulär koagulation och ett andra inträffade i samband med användning av en annan ergotalkaloid. Sambandet mellan dessa biverkningar och administrering av Parlodel har inte fastställts.
sällsynta fall har allvarliga biverkningar, inklusive hypertoni, hjärtinfarkt, anfall, stroke eller psykiska störningar rapporterats hos kvinnor efter förlossningen som behandlats med Parlodel. Hos vissa patienter föregicks utvecklingen av anfall eller stroke av svår huvudvärk och/eller övergående synstörningar. Även om orsakssambandet mellan dessa händelser och läkemedlet är osäkert, är periodisk övervakning av blodtrycket tillrådligt hos kvinnor efter förlossningen som får Parlodel. Om hypertoni, svår, progressiv eller oupphörlig huvudvärk (med eller utan synstörningar) eller tecken på CNS-toxicitet utvecklas, ska administreringen av Parlodel 2,5 mg avbrytas och patienten ska utvärderas omedelbart.
Särskild försiktighet krävs hos patienter som nyligen har behandlats eller samtidigt behandlas med läkemedel som kan förändra blodtrycket, t.ex. vasokonstriktorer såsom sympatomimetika eller ergotalkaloider inklusive ergometrin eller metylergometrin och deras samtidiga användning under puerperium rekommenderas inte.
För att rapportera MISSTÄNKTA BIVERKNINGAR, kontakta Validus Pharmaceuticals LLC på 1-866-982-5438 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
LÄKEMEDELSINTERAKTIONER
Risken med att använda Parlodel i kombination med andra läkemedel har inte utvärderats systematiskt, men alkohol kan förstärka biverkningarna av Parlodel. Parlodel 2,5 mg kan interagera med dopaminantagonister, butyrofenoner och vissa andra medel. Föreningar i dessa kategorier resulterar i en minskad effekt av Parlodel: fenotiaziner, haloperidol, metoklopramid och pimozid. Bromokriptin är ett substrat för CYP3A4. Försiktighet bör därför iakttas vid samtidig administrering av läkemedel som är starka hämmare av detta enzym (såsom azolantimykotika, HIV-proteashämmare). Samtidig användning av makrolidantibiotika som erytromycin visades öka plasmanivåerna av bromokriptin (medelvärden för AUC och Cmax ökade 3,7 gånger respektive 4,6 gånger).1 Samtidig behandling av akromegala patienter med bromokriptin och oktreotid ledde till ökad plasmaoktreotid nivåer av bromokriptin (bromokriptins AUC ökade med cirka 38%).4 Samtidig användning av Parlodel och andra ergotalkaloider rekommenderas inte. Dosjustering kan vara nödvändig i de fall där höga doser bromokriptin används (som Parkinsons sjukdom).
VARNINGAR
Eftersom hyperprolaktinemi med amenorré/galaktorré och infertilitet har hittats hos patienter med hypofystumörer, är en fullständig utvärdering av hypofysen indicerad före behandling med Parlodel (bromokriptinmesylat).
Om graviditet inträffar under administrering av Parlodel är noggrann observation av dessa patienter obligatorisk. Prolaktinutsöndrande adenom kan expandera och kompression av optiken eller andra kranialnerver kan uppstå, akut hypofyskirurgi blir nödvändig. I de flesta fall försvinner kompressionen efter leverans. Återinitiering av Parlodel 2,5 mg-behandling har rapporterats ge förbättring av synfältet hos patienter hos vilka nervkompression har inträffat under graviditeten. Säkerheten för Parlodel 2,5 mg-behandling under graviditet för modern och fostret har inte fastställts.
Parlodel 2,5 mg har associerats med somnolens och episoder av plötslig sömn, särskilt hos patienter med Parkinsons sjukdom. Plötsligt insättande sömn under dagliga aktiviteter, i vissa fall utan medvetenhet eller varningssignaler, har rapporterats. Patienterna måste informeras om detta och rådas att inte köra bil eller använda maskiner under behandling med bromokriptin. Patienter som har upplevt somnolens och/eller en episod av plötslig sömn får inte köra bil eller använda maskiner. Dessutom kan en minskning av dosen eller avbrytande av behandlingen övervägas.
Symtomatisk hypotoni kan förekomma hos patienter som behandlas med Parlodel för alla indikationer. I postpartumstudier med Parlodel har minskningar av systoliskt och diastoliskt tryck i liggande på mer än 20 mm respektive 10 mm Hg observerats hos nästan 30 % av patienterna som fått Parlodel. Ibland var sänkningen av systoliskt tryck i ryggläge så mycket som 50-59 mm Hg.
Eftersom, särskilt under de första dagarna av behandlingen, hypotensiva reaktioner ibland kan uppstå och resultera i minskad vakenhet, bör särskild försiktighet iakttas när du kör fordon eller använder maskiner.
Även om hypotoni under starten av behandlingen med Parlodel 2,5 mg förekommer hos vissa patienter, har i sällsynta fall allvarliga biverkningar, inklusive hypertoni, hjärtinfarkt, kramper, stroke, rapporterats hos kvinnor efter förlossningen som behandlats med Parlodel 2,5 mg för hämning av amning. Hypertoni har rapporterats, ibland i början av behandlingen, men utvecklas ofta under den andra behandlingens vecka; anfall har också rapporterats både med och utan föregående utveckling av hypertoni; stroke har främst rapporterats hos postpartumpatienter vars prenatala och obstetriska förlopp hade varit okomplicerade. Många av dessa patienter som upplevde anfall (inklusive fall av status epilepticus) och/eller stroke rapporterade att de utvecklade en konstant och ofta progressivt svår huvudvärk timmar till dagar före den akuta händelsen. Vissa fall av stroke och anfall föregicks också av synstörningar (suddig syn och övergående kortikal blindhet). Fall av akut hjärtinfarkt har också rapporterats.
Även om ett orsakssamband mellan administrering av Parlodel och hypertoni, anfall, stroke och hjärtinfarkt hos kvinnor efter förlossningen inte har fastställts, rekommenderas inte användning av läkemedlet för att förebygga fysiologisk amning eller hos patienter med okontrollerad hypertoni. Hos patienter som behandlas för hyperprolaktinemi ska Parlodel 2,5 mg sättas ut när graviditet diagnostiseras (se FÖRSIKTIGHETSÅTGÄRDER , Hyperprolaktinemiska tillstånd ). I händelse av att Parlodel 2,5 mg återinsätts för att kontrollera ett snabbt expanderande makroadenom (se FÖRSIKTIGHETSÅTGÄRDER , Hyperprolaktinemiska tillstånd och en patient upplever en hypertensiv sjukdom under graviditeten, måste fördelen med att fortsätta med Parlodel vägas mot den möjliga risken med användningen under en hypertensiv sjukdom under graviditeten. När Parlodel används för att behandla akromegali eller Parkinsons sjukdom hos patienter som senare blir gravida, bör ett beslut fattas om behandlingen fortsätter att vara medicinskt nödvändig eller kan avbrytas. Om det fortsätter ska läkemedlet sättas ut hos personer som kan uppleva hypertensiva störningar under graviditeten (inklusive eklampsi, preeklampsi eller graviditetsinducerad hypertoni) såvida inte utsättande av Parlodel anses vara medicinskt kontraindicerat. På grund av risken för en interaktion mellan Parlodel och andra ergotalkaloider, rekommenderas inte samtidig användning av dessa läkemedel. Regelbunden övervakning av blodtrycket, särskilt under de första veckorna av behandlingen, är försiktig. Om hypertoni, svår, progressiv eller oupphörlig huvudvärk (med eller utan synstörningar) eller tecken på CNS-toxicitet utvecklas, ska läkemedelsbehandlingen avbrytas och patienten utvärderas omgående. Särskild uppmärksamhet bör ägnas patienter som nyligen har behandlats eller som samtidigt behandlas med läkemedel som kan förändra blodtrycket. Samtidig användning under barnsängen rekommenderas inte.
Bland patienter på Parlodel, särskilt på långtids- och högdosbehandling, har pleurala och perikardiella utgjutningar, såväl som pleural och pulmonell fibros och konstriktiv perikardit, rapporterats. Patienter med oförklarliga pleuropulmonella störningar bör undersökas noggrant och avbrytande av behandlingen med Parlodel 2,5 mg bör övervägas. I de fall då behandlingen med Parlodel 2,5 mg avslutades, återgick förändringarna långsamt till det normala.
Hos ett fåtal patienter på Parlodel, särskilt på långtidsbehandling och högdosbehandling, har retroperitoneal fibros rapporterats. För att säkerställa igenkänning av retroperitoneal fibros i ett tidigt reversibelt skede rekommenderas att dess manifestationer (t.ex. ryggsmärtor, ödem i de nedre extremiteterna, nedsatt njurfunktion) övervakas hos denna patientkategori. Parlodel-läkemedel bör avbrytas om fibrotiska förändringar i retroperitoneum diagnostiseras eller misstänks.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Det har förekommit rapporter om patienter som upplevt intensiva spelbehov, ökade sexuella drifter, intensiva behov av att spendera pengar okontrollerat och/eller andra intensiva drifter, och oförmåga att kontrollera dessa drifter medan de tar en eller flera av medicinerna, inklusive Parlodel 2,5 mg , som ökar den centrala dopaminerga tonen. I vissa fall, även om inte alla, rapporterades dessa drifter ha upphört när dosen reducerades eller medicineringen avbröts. Eftersom patienter kanske inte känner igen dessa beteenden som onormala, är det viktigt för förskrivare att specifikt fråga patienter eller deras vårdgivare om utvecklingen av nya eller ökade spelbehov, sexuella drifter, okontrollerade utgifter eller andra drifter medan de behandlas med Parlodel 2,5 mg för Parkinsons sjukdom eller hyperprolaktinemi-associerade dysfunktioner. Läkare bör överväga att minska dosen eller att avbryta medicineringen om en patient utvecklar sådana trängningar när de tar Parlodel.
Säkerhet och effekt av Parlodel (bromokriptinmesylat) har inte fastställts hos patienter med njur- eller leversjukdom. Försiktighet bör iakttas när Parlodel-behandling ges samtidigt med andra läkemedel som är kända för att sänka blodtrycket.
Läkemedlet bör användas med försiktighet till patienter med en historia av psykos eller hjärt-kärlsjukdom. Om akromegala patienter eller patienter med prolaktinom eller Parkinsons sjukdom behandlas med Parlodel 2,5 mg under graviditet, bör de observeras försiktigt, särskilt under postpartumperioden om de har en historia av hjärt-kärlsjukdom.
Patienter med sällsynta ärftliga problem med galaktosintolerans, allvarlig laktasbrist eller glukos-galaktosmalabsorption bör inte ta detta läkemedel.
Hyperprolaktinemiska tillstånd
Synfältsnedsättning är en känd komplikation av makroprolaktinom. Effektiv behandling med Parlodel 2,5 mg leder till en minskning av hyperprolaktinemi och ofta till en upplösning av synnedsättningen. Hos vissa patienter kan dock en sekundär försämring av synfälten senare utvecklas trots normaliserade prolaktinnivåer och tumörkrympning, vilket kan bli följden av drag på den optiska chiasmen som dras ner i den nu delvis tomma sella. I dessa fall kan synfältsdefekten förbättras vid minskning av bromokriptindosen medan det finns en viss höjning av prolaktin och viss tumöråterexpansion. Övervakning av synfält hos patienter med makroprolaktinom rekommenderas därför för tidig upptäckt av sekundärt fältförlust på grund av chiasmalt herniering och anpassning av läkemedelsdosen.
Den relativa effekten av Parlodel kontra kirurgi för att bevara synfält är inte känd. Patienter med snabbt progressivt synfältsförlust bör utvärderas av en neurokirurg för att hjälpa till att besluta om den mest lämpliga behandlingen.
Eftersom graviditet ofta är det terapeutiska målet hos många hyperprolaktinemiska patienter med amenorré/galaktorré och hypogonadism (infertilitet), är en noggrann bedömning av hypofysen avgörande för att upptäcka närvaron av ett prolaktinutsöndrande adenom. Patienter som inte söker graviditet, eller de som har stora adenom, bör rådas att använda andra preventivmedel än orala preventivmedel under behandling med Parlodel. Eftersom graviditet kan inträffa innan menstruationen återupptas, rekommenderas ett graviditetstest minst var 4:e vecka under amenorroperioden och, när menstruationen väl har återupptagits, varje gång en patient missar en menstruation. Behandling med Parlodel SnapTabs eller kapslar ska avbrytas så snart graviditet har konstaterats. Patienter måste övervakas noga under hela graviditeten för tecken och symtom som kan signalera förstoring av en tidigare oupptäckt eller existerande prolaktinutsöndrande tumör. Utsättning av Parlodel-behandling hos patienter med kända makroadenom har i de flesta fall associerats med snabb återväxt av tumören och ökning av serumprolaktin.
Rinorré i cerebrospinalvätska har observerats hos vissa patienter med prolaktinutsöndrande adenom som behandlats med Parlodel.
Akromegali
Kylkänslig digital vasospasm har observerats hos vissa akromegala patienter som behandlats med Parlodel. Svaret, om det skulle inträffa, kan vändas genom att minska dosen av Parlodel 2,5 mg och kan förhindras genom att hålla fingrarna varma. Fall av svår gastrointestinal blödning från magsår har rapporterats, några med dödlig utgång. Även om det inte finns några bevis för att Parlodel 2,5 mg ökar förekomsten av magsår hos akromegala patienter, bör symtom som tyder på magsår undersökas noggrant och behandlas på lämpligt sätt. Patienter med anamnes på magsår eller gastrointestinala blödningar bör observeras noggrant under behandling med Parlodel.
Möjlig tumörexpansion under behandling med Parlodel har rapporterats hos ett fåtal patienter. Eftersom den naturliga historien för tillväxthormonutsöndrande tumörer är okänd, bör alla patienter övervakas noggrant och, om tecken på tumörexpansion utvecklas, avbrytande av behandlingen och alternativa procedurer övervägas.
Parkinsons sjukdom
Säkerhet vid långvarig användning i mer än 2 år vid de doser som krävs för parkinsonism har inte fastställts.
Som med all kronisk behandling rekommenderas periodisk utvärdering av lever-, hematopoetisk, kardiovaskulär och njurfunktion. Symtomatisk hypotoni kan uppstå och därför bör försiktighet iakttas vid behandling av patienter som får antihypertensiva läkemedel.
Höga doser av Parlodel 2,5 mg kan vara förknippade med förvirring och psykiska störningar. Eftersom parkinsonpatienter kan uppvisa milda grader av demens, bör försiktighet iakttas vid behandling av sådana patienter.
Parlodel administrerat ensamt eller samtidigt med levodopa kan orsaka hallucinationer (visuella eller auditiva). Hallucinationer försvinner vanligtvis med dosreduktion; ibland krävs utsättning av Parlodel 2,5 mg. I sällsynta fall, efter höga doser, har hallucinationer kvarstått i flera veckor efter avslutad behandling med Parlodel.
Liksom med levodopa bör försiktighet iakttas vid administrering av Parlodel till patienter med en historia av hjärtinfarkt som har en kvarvarande förmaks-, nodal- eller ventrikulär arytmi.
Retroperitoneal fibros har rapporterats hos ett fåtal patienter som får långtidsbehandling (2 till 10 år) med Parlodel 2,5 mg i doser från 30-140 mg dagligen.
Epidemiologiska studier har visat att patienter med Parkinsons sjukdom har en högre risk (2ca 6 gånger högre) att utveckla melanom än den allmänna befolkningen. Huruvida den ökade risken som observerades berodde på Parkinsons sjukdom eller andra faktorer, såsom läkemedel som används för att behandla Parkinsons sjukdom, är oklart. Av de skäl som anges ovan, rekommenderas patienter och vårdgivare att övervaka melanom ofta och regelbundet när de använder Parlodel för alla indikationer. Helst bör periodiska hudundersökningar utföras av lämpligt kvalificerade personer (t.ex. hudläkare).
Avbrytande av Parlodel bör göras gradvis när så är möjligt, även om patienten ska fortsätta på levodopa. Ett symtomkomplex som liknar malignt neuroleptikasyndrom (kännetecknat av förhöjd temperatur, muskelstelhet, förändrat medvetande och autonom instabilitet), utan någon annan uppenbar etiologi, har rapporterats i samband med snabb dosreduktion, utsättande av eller förändringar i antiparkinsonbehandling.
Symtom inklusive apati, ångest, depression, trötthet, sömnlöshet, svettning och smärta har rapporterats under nedtrappning eller efter utsättning av dopaminagonister, inklusive Parlodel. Dessa symtom svarar i allmänhet inte på levodopa. Innan behandlingen med Parlodel sätts ut ska patienterna informeras om potentiella abstinenssymtom och övervakas noggrant under och efter utsättning av Parlodel. Vid svåra abstinenssymtom kan återadministrering av en dopaminagonist med den lägsta effektiva dosen övervägas.
Karcinogenes, Mutagenes, Nedsatt fertilitet
En 74-veckors studie utfördes på möss som använde dietnivåer av bromokriptinmesylat motsvarande orala doser på 10 och 50 mg/kg/dag. En 100-veckors studie på råttor genomfördes med kostnivåer motsvarande orala doser på 1,7, 9,8 och 44 mg/kg/dag. De högsta doserna som testades på möss och råttor var cirka 2,5 respektive 4,4 gånger den maximala humana dosen som administrerades i kontrollerade kliniska prövningar (100 mg/dag) baserat på kroppsyta. Maligna livmodertumörer, endometriella och myometriella, hittades hos råttor enligt följande: 0/50 kontrollhonor, 2/50 honor som fick 1,7 mg/kg dagligen, 7/49 honor fick 9,8 mg/kg dagligen och 9/50 honor fick 44 mg/kg dagligen. Förekomsten av dessa neoplasmer kan troligen tillskrivas det höga östrogen/progesteronförhållandet som uppträder hos råttor som ett resultat av den prolaktininhiberande verkan av bromokriptinmesylat. De endokrina mekanismerna som tros vara inblandade i råttorna finns inte hos människor. Det finns ingen känd korrelation mellan uterina maligniteter som förekommer hos bromokriptinbehandlade råttor och risken för människor. I motsats till fynden hos råttor visade livmodern från möss som dödats efter 74 veckors behandling inga tecken på läkemedelsrelaterade förändringar.
Bromokriptinmesylat utvärderades med avseende på mutagen potential i serien av tester som inkluderade Ames bakteriell mutationsanalys, mutagen aktivitet in vitro på V79 kinesisk hamsterfibroblaster, cytogenetisk analys av benmärgsceller från kinesisk hamster efter in vivo-behandling och ett in vivo mikrokärntest för mutagena potential hos möss.
Inga mutagena effekter erhölls i något av dessa tester.
Fertilitet och reproduktionsförmåga hos råttor av honkön påverkades inte negativt av behandling med bromokriptin utöver den förväntade viktminskningen hos valpar på grund av undertryckande av laktation. Hos män som behandlats med 50 mg/kg av detta läkemedel var parning och fertilitet inom det normala intervallet. Ökad perinatal förlust producerades i undergrupperna av moderdjur, som avlivades på dag 21 postpartum (pp) efter parning med hanar som behandlats med den högsta dosen (50 mg/kg).
Graviditet
Kategori B
Administrering av 10-30 mg/kg bromokriptin till 2 råttstammar dag 6 till 15 postcoitum (pc) samt en enkeldos på 10 mg/kg dag 5 st störde nideringen. Tre mg/kg gav på dagarna 6 till 15 hade ingen effekt på nideringen och gav inga anomalier. Hos djur behandlade från dag 8-15 pc, dvs efter implantation, gav 30 mg/kg ökad prenatal mortalitet i form av ökad förekomst av embryonal resorption. En anomali, aplasi av ryggkotor och revben, hittades i gruppen av 262 foster som härrörde från moderdjuren behandlade med 30 mg/kg bromokriptin. Inga fostertoxiska effekter hittades hos avkommor till moderdjur som behandlats under den peri- eller postnatala perioden.
Två studier utfördes på kaniner (2 stammar) för att fastställa risken för att störa nideringen. Dosnivåer på 100 eller 300 mg/kg/dag från dag 1 till dag 6 st påverkade inte nideringen negativt. Den höga dosen var cirka 63 gånger den maximala humana dosen som administrerades i kontrollerade kliniska prövningar (100 mg/dag), baserat på kroppsyta. Hos vita kaniner från Nya Zeeland inträffade viss embryodödlighet vid 300 mg/kg, vilket var en återspegling av öppen maternell toxicitet. Tre studier utfördes på 2 kaninstammar för att bestämma den teratologiska potentialen hos bromokriptin vid dosnivåer på 3, 10, 30, 100 och 300 mg/kg givet från dag 6 till dag 18 st. I 2 studier med Yellow-silver-stammen , gomspalt hittades hos 3 och 2 foster vid maternellt toxiska doser på 100 respektive 300 mg/kg. Ett kontrollfoster uppvisade också denna anomali. I den tredje studien som genomfördes med vita kaniner från Nya Zeeland med ett identiskt protokoll, producerades inga gomspalter.
Inga teratologiska eller embryotoxiska effekter av bromokriptin producerades hos någon av 6 avkommor från 6 apor vid en dosnivå på 2 mg/kg.
Information om 1276 graviditeter hos kvinnor som tar Parlodel har samlats in. I de flesta fall avbröts Parlodel inom 8 veckor in i graviditeten (medelvärde 28,7 dagar), men 8 patienter fick läkemedlet kontinuerligt under hela graviditeten. Den genomsnittliga dagliga dosen för alla patienter var 5,8 mg (intervall 1-40 mg).
Av dessa 1276 graviditeter var det 1088 fullgångna förlossningar (4 dödfödda), 145 spontana aborter (11,4%) och 28 framkallade aborter (2,2%). Dessutom orsakade 12 extrauterinegraviditeter och 3 hydatidiforma födelsemärken (två gånger hos samma patient) tidigt graviditetsavbrott. Dessa data jämförs positivt med abortfrekvensen (11 % -25 %) som anges för graviditeter inducerade av klomifencitrat, menopausalt gonadotropin och koriongonadotropin.
Även om spontana aborter ofta inte rapporteras, särskilt före 20 veckors graviditet, har deras frekvens uppskattats till 15 %.
Förekomsten av fosterskador i befolkningen i stort varierar från 2% -4,5%. Incidensen i 1109 levande födda från patienter som får bromokriptin är 3,3 %.
Det finns inget som tyder på att Parlodel 2,5 mg bidrog till typen eller förekomsten av fosterskador hos denna grupp av spädbarn.
Ammande mödrar
Parlodel 2,5 mg ska inte användas under amning hos kvinnor efter förlossningen.
Pediatrisk användning
Säkerheten och effektiviteten av bromokriptin för behandling av prolaktinutsöndrande hypofysadenom har fastställts hos patienter i åldern 16 till vuxna. Inga data finns tillgängliga för användning av bromokriptin hos pediatriska patienter under 8 år. En enda 8-årig patient som behandlats med bromokriptin för ett prolaktinutsöndrande hypofysmakroadenom har rapporterats utan terapeutiskt svar.
Användningen av bromokriptin för behandling av prolaktinutsöndrande adenom hos pediatriska patienter i åldersgruppen 11 till under 16 år stöds av bevis från välkontrollerade studier på vuxna, med ytterligare data för ett begränsat antal (n=14) barn och ungdomar i åldern 11 till 15 år med prolaktinutsöndrande hypofysmakro- och mikroadenom som har behandlats med bromokriptin. Av de 14 rapporterade patienterna hade 9 framgångsrika resultat, 3 partiella svar och 2 svarade inte på bromokriptinbehandling. Kronisk hypopituitarism komplicerade makroadenombehandling hos 5 av patienterna som svarade, både hos patienter som fick bromokriptin enbart och hos dem som fick bromokriptin i kombination med kirurgisk behandling och/eller hypofysstrålning.
Säkerhet och effektivitet för bromokriptin hos pediatriska patienter har inte fastställts för någon annan indikation som anges i avsnittet INDIKATIONER OCH ANVÄNDNING.
Geriatrisk användning
Kliniska studier för Parlodel 2,5 mg inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om äldre svarar annorlunda än yngre försökspersoner. Andra rapporterade kliniska erfarenheter, inklusive rapportering efter marknadsföring av biverkningar, har dock inte identifierat skillnader i svar eller tolerabilitet mellan äldre och yngre patienter. Även om ingen variation i effekt eller biverkningsprofil har observerats hos geriatriska patienter som tar Parlodel 2,5 mg, kan större känslighet hos vissa äldre personer inte kategoriskt uteslutas. I allmänhet bör dosval för en äldre patient vara försiktigt, med början i den nedre änden av dosintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling i denna population.
ÖVERDOS
De vanligast rapporterade tecknen och symtomen förknippade med akut överdos av Parlodel (bromokriptinmesylat) är: illamående, kräkningar, förstoppning, diafores, yrsel, blekhet, allvarlig hypotoni, sjukdomskänsla, förvirring, slöhet, dåsighet, vanföreställningar, hallucinationer och upprepade förvirringar. Den dödliga dosen har inte fastställts och läkemedlet har en mycket bred säkerhetsmarginal. Ett dödsfall inträffade dock hos en patient som begick självmord med en okänd mängd Parlodel 2,5 mg och klorokin.
Behandling av överdosering består av avlägsnande av läkemedlet genom kräkning (om man är vid medvetande), magsköljning, aktivt kol eller koksaltlösning. Noggrann övervakning och registrering av vätskeintag och utflöde är viktigt. Hypotension bör behandlas genom att placera patienten i Trendelenburg-position och administrera IV-vätskor. Om tillfredsställande lindring av hypotoni inte kan uppnås genom att använda ovanstående åtgärder till fullo, bör vasopressorer övervägas.
Det har förekommit enstaka rapporter om barn som av misstag fått i sig Parlodel. Kräkningar, somnolens och feber rapporterades som biverkningar. Patienterna återhämtade sig antingen spontant inom några timmar eller efter lämplig behandling.
KONTRAINDIKATIONER
Överkänslighet mot bromokriptin eller mot något av hjälpämnena i Parlodel (bromokriptinmesylat), okontrollerad hypertoni och känslighet för eventuella ergotalkaloider. Hos patienter som behandlas för hyperprolaktinemi ska Parlodel 2,5 mg sättas ut när graviditet diagnostiseras (se FÖRSIKTIGHETSÅTGÄRDER , Hyperprolaktinemiska tillstånd ). I händelse av att Parlodel 2,5 mg återupptas för att kontrollera ett snabbt expanderande makroadenom (se FÖRSIKTIGHETSÅTGÄRDER , Hyperprolaktinemiska tillstånd och en patient upplever en hypertensiv sjukdom under graviditeten, måste fördelen med att fortsätta med Parlodel vägas mot den möjliga risken med användningen under en hypertensiv sjukdom under graviditeten. När Parlodel används för att behandla akromegali, prolaktinom eller Parkinsons sjukdom hos patienter som senare blir gravida, bör ett beslut fattas om behandlingen fortsätter att vara medicinskt nödvändig eller kan avbrytas. Om det fortsätter ska läkemedlet sättas ut hos personer som kan uppleva hypertensiva störningar under graviditeten (inklusive eklampsi, preeklampsi eller graviditetsinducerad hypertoni) såvida inte utsättande av Parlodel anses vara medicinskt kontraindicerat.
Läkemedlet bör inte användas under postpartumperioden till kvinnor med en historia av kranskärlssjukdom och andra allvarliga kardiovaskulära tillstånd om inte abstinens anses vara medicinskt kontraindicerat. Om läkemedlet används under postpartumperioden bör patienten observeras med försiktighet.
KLINISK FARMAKOLOGI
Parlodel (bromokriptinmesylat) är en dopaminreceptoragonist, som aktiverar postsynaptiska dopaminreceptorer. De dopaminerga neuronerna i den tuberoinfundibulära processen modulerar utsöndringen av prolaktin från den främre hypofysen genom att utsöndra en prolaktinhämmande faktor (tros vara dopamin); i corpus striatum är de dopaminerga neuronerna involverade i kontrollen av motorisk funktion. Kliniskt minskar Parlodel 2,5 mg signifikant plasmanivåerna av prolaktin hos patienter med fysiologiskt förhöjt prolaktin såväl som hos patienter med hyperprolaktinemi. Hämningen av fysiologisk laktation såväl som galaktorré i patologiska hyperprolaktinemiska tillstånd erhålls vid dosnivåer som inte påverkar utsöndringen av andra tropiska hormoner från hypofysen. Experiment har visat att bromokriptin inducerar långvarigt stereotypt beteende hos gnagare och vändningsbeteende hos råttor med unilaterala lesioner i substantia nigra. Dessa effekter, som är karakteristiska för de som produceras av dopamin, hämmas av dopaminantagonister och antyder en direkt verkan av bromokriptin på striatala dopaminreceptorer.
Bromokriptinmesylat är ett icke-hormonellt, icke-östrogent medel som hämmar utsöndringen av prolaktin hos människor, med liten eller ingen effekt på andra hypofyshormoner, förutom hos patienter med akromegali, där det sänker förhöjda blodnivåer av tillväxthormon hos majoriteten av patienterna.
Bromokriptinmesylat producerar sin terapeutiska effekt vid behandling av Parkinsons sjukdom, ett kliniskt tillstånd som kännetecknas av en progressiv brist på dopaminsyntes i substantia nigra, genom att direkt stimulera dopaminreceptorerna i corpus striatum. Däremot utövar levodopa sin terapeutiska effekt först efter omvandling till dopamin av neuronerna i substantia nigra, vilka är kända för att vara numeriskt minskade i denna patientpopulation.
Farmakokinetik
Absorption
Efter administrering av en engångsdos av Parlodel 2,5 mg tabletter, 2 x 2,5 mg till 5 friska frivilliga under fastande förhållanden, var de genomsnittliga maximala plasmanivåerna av bromokriptin, tiden för att nå maximala plasmakoncentrationer och eliminationshalveringstid 465 pg/ml ± 226, 2,5 timmar ± 2 respektive 4,85 timmar.1 Linjärt samband hittades mellan engångsdoser av Parlodel 2,5 mg och Cmax och AUC i dosintervallet 1 till 7,5 mg.2 Farmakokinetiken för bromokriptinmetaboliter har inte rapporterats.
Mat påverkade inte signifikant den systemiska exponeringen av bromokriptin efter administrering av Parlodel tabletter, 2,5 mg.3 Det rekommenderas att Parlodel 2,5 mg tas tillsammans med mat på grund av den höga andelen försökspersoner som kräks när de får bromokriptin under fasta.
Efter Parlodel 5 mg administrerat två gånger dagligen i 14 dagar var bromokriptinets Cmax och AUC vid steady-state 628 ± 375 pg/ml respektive 2377 ± 1186 pg*tim/ml.4
Distribution
In vitro-experiment visade att bromokriptin var 90% -96% bundet till serumalbumin.
Ämnesomsättning
Bromokriptin genomgår omfattande first-pass biotransformation, vilket återspeglas av komplexa metabolitprofiler och av nästan fullständig frånvaro av moderläkemedel i urin och avföring.
In vitro-studier med humana levermikrosomer visade att bromokriptin har hög affinitet för CYP3A och hydroxyleringar vid prolinringen av cyklopeptiddelen utgjorde en huvudsaklig metabolisk väg.5 Hämmare och/eller potenta substrat för CYP3A4 kan därför hämma clearance av bromokriptin och bly till ökade nivåer. (ser FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER sektion). Deltagandet av andra viktiga CYP-enzymer såsom 2D6, 2C8 och 2C19 på metabolismen av bromokriptin har inte utvärderats. Bromokriptin är också en hämmare av CYP3A4 med ett beräknat IC50-värde på 1,69 μM.6 Givet de låga terapeutiska koncentrationerna av bromokriptin hos patienter (Cmax=0,82 nM), bör en signifikant förändring av metabolismen av ett andra läkemedel vars clearance medieras av inte CYP3A4 väntas. Den potentiella effekten av bromokriptin och dess metaboliter att fungera som inducerare av CYP-enzymer har inte rapporterats.
Exkretion
Cirka 82 % och 5,6 % av den oralt administrerade radioaktiva dosen återfanns i avföring respektive urin. Bromolysergic acid och bromoisolysergic acid stod för hälften av radioaktiviteten i urinen.5
Specifika populationer
Effekt av nedsatt njurfunktion
Effekten av njurfunktionen på bromokriptins farmakokinetik har inte utvärderats.
Eftersom moderläkemedlet och metaboliter nästan fullständigt utsöndras via metabolism, och endast 6 % elimineras via njurarna, kan njurfunktionsnedsättning inte ha någon signifikant inverkan på farmakokinetiken för bromokriptin och dess metaboliter (se FÖRSIKTIGHETSÅTGÄRDER , Allmän ).
Effekt av nedsatt leverfunktion
Effekten av nedsatt leverfunktion på PK av Parlodel och dess metaboliter har inte utvärderats. Eftersom Parlodel huvudsakligen elimineras genom metabolism, kan nedsatt leverfunktion öka plasmanivåerna av bromokriptin, därför kan försiktighet vara nödvändig (se FÖRSIKTIGHETSÅTGÄRDER , Allmän ).
Effekten av ålder, ras och kön på farmakokinetiken för bromokriptin och dess metaboliter har inte utvärderats.
Kliniska studier
I cirka 75 % av fallen av amenorré och galaktorré undertrycker Parlodel 2,5 mg terapi galaktorrén helt eller nästan helt och återupptar normala ägglossningsmenstruationscykler.
Mensen återupptas vanligtvis före fullständig suppression av galaktorré; tiden för detta är i genomsnitt 6 till 8 veckor. Vissa patienter svarar dock inom några dagar och andra kan ta upp till 8 månader.
Galaktorré kan ta längre tid att kontrollera beroende på graden av stimulering av bröstvävnaden före behandlingen. Minst 75 % minskning av sekretionen observeras vanligtvis efter 8 till 12 veckor. Vissa patienter kan misslyckas med att svara även efter 12 månaders behandling.
Hos många akromegala patienter ger Parlodel 2,5 mg en snabb och varaktig minskning av cirkulerande nivåer av serumtillväxthormon.
1 Nelson, M. et. al. (1990). Farmakokinetisk utvärdering av erytromycin och koffein administrerat med bromokriptin. Clin Pharmacol Ther; 47(6):694-7.
Schran, HF, Bhuta, SI, Schwartz, et al. (1980). Farmakokinetiken för bromokriptin hos människa. I: Golstein, M. Calne, DB, et. Al (red.). Ergotförening och hjärnfunktion: Neuroendokrina och neuropsykiatriska aspekter, s. 125-139, New York, Rave Press.
3 Kopitar, Z., Vrhovac, B., Povsic, L., Plavsic, F., Francetic, I., Urbancic, J. (1991). Effekten av mat och metoklopramid på farmakokinetiken och biverkningarna av bromokriptin. Eur J Drug Metab Pharmacokinet; 16(3):177-81
4 Flogstad, AK, Halse, J., Grass, P., Abisch, E., Djoseland, O., Kutz, K., Bodd, E., and Jervell, J., (1994). En jämförelse av oktreotid, bromokriptin eller en kombination av båda läkemedlen vid akromegali. Journal of Clinical Endocrinology & Metabolism; Vol 79, 461-465
5 Peyronneau MA, Delaforge M, Riviere R et al. 1994. Hög affinitet av ergopeptider för CYP P450 3A. Betydelsen av deras peptiddel för P450-igenkänning och hydroxylering av bromokriptin. Eur J Biochem 223:947-56.
Wynalda, MA, Wienkers, LC (1997). Bedömning av potentiella interaktioner mellan dopaminreceptoragonister och olika humana cytokrom P450-enzymer med hjälp av en enkel in vitro-inhiberingsscreening. Läkemedel Metab Dispos; 25:1211-14.
PATIENTINFORMATION
Under kliniska prövningar har yrsel, dåsighet, svimning, svimning och synkope rapporterats tidigt under behandlingen med Parlodel 2,5 mg. I rapporter efter marknadsföring har Parlodel associerats med somnolens och episoder av plötslig sömn, särskilt hos patienter med Parkinsons sjukdom. Plötsligt insättande sömn under dagliga aktiviteter, i vissa fall utan medvetenhet eller varningssignaler, har rapporterats mycket sällan. Alla patienter som får Parlodel bör varnas med avseende på att delta i aktiviteter som kräver snabba och exakta svar, såsom att köra bil eller använda maskiner. Patienter som behandlas med Parlodel 2,5 mg och som uppvisar somnolens och/eller plötsliga sömnepisoder måste rådas att inte köra bil eller delta i aktiviteter där nedsatt vakenhet kan utsätta sig själva eller andra för risk för allvarlig skada eller dödsfall (t.ex. att använda maskiner).
Patienter som får Parlodel 2,5 mg för hyperprolaktinemiska tillstånd associerade med makroadenom eller de som tidigare har genomgått transsfenoidal kirurgi bör uppmanas att rapportera eventuella ihållande vattniga näsflytningar till sin läkare. Patienter som får Parlodel 2,5 mg för behandling av ett makroadenom bör informeras om att utsättande av läkemedlet kan vara förknippat med snabb återväxt av tumören och återkommande symtom.
Patienter och deras vårdgivare bör uppmärksammas på möjligheten att patienter kan uppleva intensiva drifter att spendera pengar okontrollerat, intensiva spelbehov, ökade sexuella drifter och andra intensiva drifter och oförmåga att kontrollera dessa drifter medan de tar Parlodel. Råda patienter och deras vårdgivare att informera sin vårdgivare om de utvecklar nya eller ökade okontrollerade utgifter, spelbehov, sexuella drifter eller andra drifter medan de behandlas med Parlodel [se FÖRSIKTIGHETSÅTGÄRDER ].
Särskilt under de första dagarna av behandlingen kan hypotensiva reaktioner ibland uppstå och resultera i minskad vakenhet, särskild försiktighet bör iakttas när du kör fordon eller använder maskiner.
Rekommendera patienter att kontakta sin vårdgivare om de vill avbryta behandlingen med Parlodel eller minska dosen av Parlodel. Rekommendera patienter som har ordinerats en lägre dos eller som har tagit slut från läkemedlet att meddela sin vårdgivare om de har abstinenssymtom som feber, muskelstelhet, förändrat medvetande, apati, ångest, depression, trötthet, sömnlöshet, svettning eller smärta (se FÖRSIKTIGHETSÅTGÄRDER ).
