Arimidex 1mg Anastrozole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Arimidex och hur används det?
Arimidex 1mg är ett receptbelagt läkemedel som används för att behandla symtom på bröstcancer hos postmenopausala kvinnor. Arimidex kan användas ensamt eller tillsammans med andra läkemedel.
Arimidex tillhör en klass av läkemedel som kallas Antineoplastics, Aromatashämmare.
Det är inte känt om Arimidex är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Arimidex?
Arimidex kan orsaka allvarliga biverkningar inklusive:
- andnöd,
- benfraktur,
- svullna körtlar,
- illamående,
- ont i övre magen,
- klåda,
- trötthet,
- aptitlöshet,
- mörk urin,
- lerfärgad avföring,
- gulfärgning av huden eller ögonen (gulsot),
- plötslig domningar eller svaghet (särskilt på ena sidan av kroppen),
- plötslig svår huvudvärk,
- sluddrigt tal,
- problem med syn eller balans,
- feber,
- öm hals,
- svullnad i ansiktet eller tungan,
- brännande i dina ögon,
- hudsmärta och
- röda eller lila hudutslag som sprider sig (särskilt i ansiktet eller överkroppen) med blåsor och fjällning
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Arimidex inkluderar:
- svaghet,
- värmevallningar,
- domningar eller stickningar i huden,
- svullnad i anklar eller fötter,
- ledvärk eller stelhet,
- problem med fingrarna när du greppar,
- öm hals,
- huvudvärk,
- ryggont,
- skelettsmärta,
- depression,
- humörförändringar,
- sömnproblem (sömnlöshet),
- högt blodtryck,
- svår huvudvärk,
- suddig syn,
- dunkar i nacken eller öronen,
- illamående,
- kräkningar och
- milda utslag
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Arimidex. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
ARIMIDEX (anastrozol) tabletter för oral administrering innehåller 1 mg anastrozol, en icke-steroid aromatashämmare. Det beskrivs kemiskt som 1,3-bensendiacetonitril, a, a, a', a'-tetrametyl-5-(1H-1,2,4-triazol-1-ylmetyl). Dess molekylformel är C17H19N5 och dess strukturformel är:
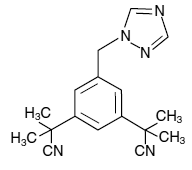
Anastrozol är ett benvitt pulver med en molekylvikt på 293,4. Anastrozol har måttlig vattenlöslighet (0,5 mg/ml vid 25°C); lösligheten är oberoende av pH i det fysiologiska området. Anastrozol är fritt lösligt i metanol, aceton, etanol och tetrahydrofuran och mycket lösligt i acetonitril.
Varje tablett innehåller som inaktiva ingredienser: laktos, magnesiumstearat, hydroxipropylmetylcellulosa, polyetylenglykol, povidon, natriumstärkelseglykolat och titandioxid.
INDIKATIONER
Adjuvansbehandling
ARIMIDEX är indicerat för adjuvant behandling av postmenopausala kvinnor med hormonreceptorpositiv tidig bröstcancer.
Första linjens behandling
ARIMIDEX 1mg är indicerat för förstahandsbehandling av postmenopausala kvinnor med hormonreceptorpositiv eller hormonreceptor okänd lokalt avancerad eller metastaserad bröstcancer.
Andra linjens behandling
ARIMIDEX 1mg är indicerat för behandling av avancerad bröstcancer hos postmenopausala kvinnor med sjukdomsprogression efter tamoxifenbehandling. Patienter med ER-negativ sjukdom och patienter som inte svarat på tidigare tamoxifenbehandling svarade sällan på ARIMIDEX.
DOSERING OCH ADMINISTRERING
Rekommenderad dos
Dosen av ARIMIDEX är en 1 mg tablett en gång om dagen. För patienter med avancerad bröstcancer ska ARIMIDEX 1 mg fortsätta tills tumörprogression. ARIMIDEX kan tas med eller utan mat.
För adjuvant behandling av tidig bröstcancer hos postmenopausala kvinnor är den optimala behandlingstiden okänd. I ATAC-studien administrerades ARIMIDEX 1 mg under fem år [se Kliniska studier ].
Ingen dosjustering är nödvändig för patienter med nedsatt njurfunktion eller för äldre patienter [se Användning i specifika populationer ].
Patienter med nedsatt leverfunktion
Inga dosförändringar rekommenderas för patienter med lätt till måttligt nedsatt leverfunktion. ARIMIDEX har inte studerats på patienter med gravt nedsatt leverfunktion [se Användning i specifika populationer ].
HUR LEVERERAS
Doseringsformer och styrkor
Tabletterna är vita, bikonvexa, filmdragerade och innehåller 1 mg anastrozol. Tabletterna är präglade på ena sidan med en logotyp som består av bokstaven "A" (versal) med en pilspets fäst vid foten av det förlängda högra benet på "A" och på baksidan med tablettstyrkan "Adx 1" ”.
Förvaring Och Hantering
Dessa tabletter levereras i burkar med 30 tabletter ( NDC 0310-0201-30).
Lagring
Förvara i kontrollerad rumstemperatur, 20-25°C (68-77°F) [se USP ].
Distribuerat av: AstraZeneca Pharmaceuticals LP Wilmington, DE 19850. Reviderad: maj 2014
BIEFFEKTER
Allvarliga biverkningar med ARIMIDEX som inträffar hos färre än 1 av 10 000 patienter är: 1) hudreaktioner såsom lesioner, sår eller blåsor; 2) allergiska reaktioner med svullnad av ansikte, läppar, tunga och/eller svalg. Detta kan orsaka svårigheter att svälja och/eller andas; och 3) förändringar i blodprov av leverfunktionen, inklusive inflammation i levern med symtom som kan innefatta en allmän känsla av att inte må bra, med eller utan gulsot, leversmärta eller leversvullnad.
Vanliga biverkningar (förekommer med en incidens på ≥ 10%) hos kvinnor som tar ARIMIDEX 1 mg inkluderade: värmevallningar, asteni, artrit, smärta, artralgi, högt blodtryck, depression, illamående och kräkningar, hudutslag, osteoporos, frakturer, ryggsmärtor, sömnlöshet, huvudvärk, skelettsmärta, perifert ödem, ökad hosta, dyspné, faryngit och lymfödem.
ATAC-studien var den vanligaste rapporterade biverkningen (> 0,1 %) som ledde till att behandlingen avbröts för båda behandlingsgrupperna värmevallningar, även om det fanns färre patienter som avbröt behandlingen till följd av värmevallningar i ARIMIDEX 1 mg-gruppen.
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Erfarenhet av kliniska prövningar
Adjuvant terapi
Biverkningsdata för adjuvant terapi baseras på ATAC-studien [se Kliniska studier ]. Mediandurationen av adjuvant behandling för säkerhetsutvärdering var 59,8 månader och 59,6 månader för patienter som fick ARIMIDEX 1 mg respektive tamoxifen 20 mg.
Biverkningar som inträffar med en incidens på minst 5 % i endera behandlingsgruppen under behandlingen eller inom 14 dagar efter avslutad behandling presenteras i Tabell 1.
Vissa biverkningar och kombinationer av biverkningar specificerades prospektivt för analys, baserat på kända farmakologiska egenskaper och biverkningsprofiler för de två läkemedlen (se tabell 2).
Ischemiska kardiovaskulära händelser
Mellan behandlingsarmarna i den totala populationen på 6186 patienter fanns ingen statistisk skillnad i ischemiska kardiovaskulära händelser (4 % ARIMIDEX vs. 3 % tamoxifen).
I den totala populationen rapporterades angina pectoris hos 71/3092 (2,3 %) patienter i ARIMIDEX 1 mg-armen och 51/3094 (1,6 %) patienter i tamoxifen-armen; hjärtinfarkt rapporterades hos 37/3092 (1,2%) patienter i ARIMIDEX 1 mg-armen och 34/3094 (1,1%) patienter i tamoxifen-armen.
Hos kvinnor med redan existerande ischemisk hjärtsjukdom 465/6186 (7,5 %) var incidensen av ischemiska kardiovaskulära händelser 17 % hos patienter på ARIMIDEX och 10 % hos patienter på tamoxifen. I denna patientpopulation rapporterades angina pectoris hos 25/216 (11,6 %) patienter som fick ARIMIDEX och 13/249 (5,2 %) patienter som fick tamoxifen; hjärtinfarkt rapporterades hos 2/216 (0,9 %) patienter som fick ARIMIDEX och 8/249 (3,2 %) patienter som fick tamoxifen.
Fynd av benmineraldensitet
Resultat från ATAC-provbenssubstudien vid 12 och 24 månader visade att patienter som fick ARIMIDEX 1 mg hade en genomsnittlig minskning av både ländryggen och total höftbensmineraldensitet (BMD) jämfört med baslinjen. Patienter som fick tamoxifen hade en genomsnittlig ökning av både ländryggen och total BMD i höften jämfört med baslinjen.
Eftersom ARIMIDEX sänker cirkulerande östrogennivåer kan det orsaka en minskning av bentätheten.
En post-marketingstudie utvärderade de kombinerade effekterna av ARIMIDEX 1 mg och bisfosfonatrisedronat på förändringar från baslinjen i BMD och markörer för benresorption och bildning hos postmenopausala kvinnor med hormonreceptorpositiv tidig bröstcancer. Alla patienter fick kalcium- och D-vitamintillskott. Efter 12 månader noterades små minskningar av benmineraldensiteten i ländryggen hos patienter som inte fick bisfosfonater. Bisfosfonatbehandling bevarade bentätheten hos de flesta patienter med risk för frakturer.
Postmenopausala kvinnor med tidig bröstcancer som planeras att behandlas med ARIMIDEX 1 mg bör få sin benstatus hanterad enligt behandlingsriktlinjer som redan finns tillgängliga för postmenopausala kvinnor med liknande risk för skörhetsfraktur.
Kolesterol
Under ATAC-studien rapporterades fler patienter som fick ARIMIDEX 1 mg ha ett förhöjt serumkolesterol jämfört med patienter som fick tamoxifen (9 % respektive 3,5 %).
En studie efter marknadsföringen utvärderade också eventuella effekter av ARIMIDEX på lipidprofilen. I den primära analyspopulationen för lipider (enbart ARIMIDEX 1 mg) fanns det ingen kliniskt signifikant förändring av LDL-C från baslinjen till 12 månader och HDL-C från baslinjen till 12 månader.
I sekundär population för lipider (ARIMIDEX+risedronat) fanns det heller ingen kliniskt signifikant förändring av LDL-C och HDL-C från baslinjen till 12 månader.
båda populationerna för lipider fanns det ingen kliniskt signifikant skillnad i totalt kolesterol (TC) eller serumtriglycerider (TG) efter 12 månader jämfört med baslinjen.
I denna studie hade behandling under 12 månader med enbart ARIMIDEX 1 mg en neutral effekt på lipidprofilen. Kombinationsbehandling med ARIMIDEX och risedronat hade också en neutral effekt på lipidprofilen.
Studien ger bevis för att postmenopausala kvinnor med tidig bröstcancer som är planerad att behandlas med ARIMIDEX 1 mg bör hanteras med hjälp av de nuvarande riktlinjerna för National Cholesterol Education Program för kardiovaskulär riskbaserad behandling av enskilda patienter med LDL-förhöjningar.
Andra biverkningar
Patienter som fick ARIMIDEX hade en ökning av ledbesvär (inklusive artrit, artros och artralgi) jämfört med patienter som fick tamoxifen. Patienter som fick ARIMIDEX hade en ökning av incidensen av alla frakturer (särskilt frakturer i ryggraden, höften och handleden) [315 (10 %)] jämfört med patienter som fick tamoxifen [209 (7 %)].
Patienter som fick ARIMIDEX 1 mg hade en högre incidens av karpaltunnelsyndrom [78 (2,5 %)] jämfört med patienter som fick tamoxifen [22 (0,7 %)].
Vaginal blödning förekom oftare hos de tamoxifenbehandlade patienterna jämfört med de ARIMIDEX-behandlade patienterna 317 (10 %) respektive 167 (5 %).
Patienter som fick ARIMIDEX hade en lägre incidens av värmevallningar, vaginal blödning, vaginal flytning, endometriecancer, venösa tromboemboliska händelser och ischemiska cerebrovaskulära händelser jämfört med patienter som fick tamoxifen.
10-års medianuppföljningssäkerhetsresultat från ATAC-försöket
Resultaten överensstämmer med tidigare analyser.
Allvarliga biverkningar var likartade mellan ARIMIDEX (50 %) och tamoxifen (51 %).
- Kardiovaskulära händelser överensstämde med de kända säkerhetsprofilerna för ARIMIDEX och tamoxifen.
- Den kumulativa incidensen av alla första frakturer (både allvarliga och icke-allvarliga, uppträdande antingen under eller efter behandling) var högre i ARIMIDEX-gruppen (15 %) jämfört med tamoxifen-gruppen (11 %). Denna ökade andel första frakturer under behandlingen fortsatte inte under uppföljningsperioden efter behandlingen.
- Den kumulativa incidensen av nya primära cancerformer var liknande i ARIMIDEX 1 mg-gruppen (13,7 %) jämfört med tamoxifengruppen (13,9 %). I enlighet med tidigare analyser var endometriecancer högre i tamoxifengruppen (0,8 %) jämfört med ARIMIDEX-gruppen (0,2 %).
- Det totala antalet dödsfall (under eller utanför behandling) var likartat mellan behandlingsgrupperna. Det fanns fler dödsfall relaterade till bröstcancer i tamoxifen än i ARIMIDEX 1 mg-behandlingsgruppen.
Första linjens terapi
Biverkningar som inträffar med en incidens på minst 5 % i endera behandlingsgruppen av prövningar 0030 och 0027 under eller inom 2 veckor efter behandlingens slut visas i Tabell 3.
Mindre frekventa biverkningar som rapporterats hos patienter som fick ARIMIDEX 1 mg l mg i antingen försök 0030 eller försök 0027 liknade de som rapporterats för andrahandsbehandling.
Baserat på resultat från andrahandsbehandling och den etablerade säkerhetsprofilen för tamoxifen, analyserades incidensen av 9 fördefinierade biverkningskategorier som potentiellt var orsaksmässigt relaterade till en eller båda behandlingarna på grund av deras farmakologi statistiskt. Inga signifikanta skillnader sågs mellan behandlingsgrupperna.
Andra linjens terapi
ARIMIDEX 1 mg tolererades i två kontrollerade kliniska prövningar (dvs. prövningar 0004 och 0005), där mindre än 3,3 % av de ARIMIDEX-behandlade patienterna och 4,0 % av de megestrolacetatbehandlade patienterna drog ut på grund av en biverkning.
Den huvudsakliga biverkningen som var vanligare med ARIMIDEX än med megestrolacetat var diarré. Biverkningar som rapporterats hos mer än 5 % av patienterna i någon av behandlingsgrupperna i dessa två kontrollerade kliniska prövningar, oavsett orsakssamband, presenteras nedan:
Kroppen som helhet: Influensasyndrom; feber; nacksmärta; obehag; oavsiktlig skada; infektion
Kardiovaskulär: hypertoni; tromboflebit
Lever: Gamma GT ökade; SGOT ökade; SGPT ökad Hematologisk: Anemi; leukopeni
Metaboliskt och näringsmässigt: Alkaliskt fosfatas ökat; viktminskning
Den genomsnittliga totalkolesterolnivån i serum ökade med 0,5 mmol/L bland patienter som fick ARIMIDEX. Ökning av LDL-kolesterol har visat sig bidra till dessa förändringar.
Muskuloskeletala: Muskelvärk; artralgi; patologisk fraktur
Nervös: Sömnighet; förvirring; sömnlöshet; ångest; nervositet
Andningsvägar: Bihåleinflammation; bronkit; rinit
Hud och bihang: Hårförtunning (alopeci); klåda
Urogenital: Urinvägsinfektion; bröstsmärtor
Incidensen av följande biverkningsgrupper som potentiellt är kausalt relaterade till en eller båda behandlingarna på grund av deras farmakologi analyserades statistiskt: viktökning, ödem, tromboembolisk sjukdom, gastrointestinala störningar, värmevallningar och vaginal torrhet. Dessa sex grupper, och de biverkningar som fångats i grupperna, definierades prospektivt. Resultaten visas i tabellen nedan.
Erfarenhet efter marknadsföring
Dessa biverkningar rapporteras frivilligt från en population av osäker storlek. Därför är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering. Följande har rapporterats vid användning av Arimidex efter godkännande:
- Lever och gallvägar inklusive ökningar av alkaliskt fosfatas, alaninaminotransferas, aspartataminotransferas, gamma-GT och bilirubin; hepatit
- Utslag inklusive fall av mukokutana sjukdomar som erythema multiforme och Stevens-Johnsons syndrom
- Fall av allergiska reaktioner inklusive angioödem, urtikaria och anafylaxi [se KONTRAINDIKATIONER ]
- Myalgi, triggerfinger och hyperkalcemi (med eller utan en ökning av bisköldkörtelhormon)
LÄKEMEDELSINTERAKTIONER
Tamoxifen
Samtidig administrering av anastrozol och tamoxifen till bröstcancerpatienter minskade plasmakoncentrationen av anastrozol med 27 %. Samtidig administrering av anastrozol och tamoxifen påverkade dock inte farmakokinetiken för tamoxifen eller N-desmetyltamoxifen. Vid en medianuppföljning på 33 månader visade kombinationen av ARIMIDEX och tamoxifen ingen effektfördel jämfört med tamoxifen hos alla patienter såväl som i den hormonreceptorpositiva subpopulationen. Denna behandlingsarm avbröts från försöket [se Kliniska studier ]. Baserat på kliniska och farmakokinetiska resultat från ATAC-studien ska tamoxifen inte administreras tillsammans med anastrozol.
Östrogen
Östrogeninnehållande terapier ska inte användas tillsammans med ARIMIDEX 1 mg eftersom de kan minska dess farmakologiska verkan.
Warfarin
en studie utförd på 16 frivilliga manliga försökspersoner förändrade inte anastrozol exponeringen (mätt som Cmax och AUC) och antikoagulerande aktivitet (mätt som protrombintid, aktiverad partiell tromboplastintid och trombintid) för både R- och S- warfarin.
Cytokrom P450 Baserat på resultat in vitro och in vivo är det osannolikt att samtidig administrering av ARIMIDEX 1 mg kommer att påverka andra läkemedel som ett resultat av hämning av cytokrom P450 [se KLINISK FARMAKOLOGI ].
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Ischemiska kardiovaskulära händelser
Hos kvinnor med redan existerande ischemisk hjärtsjukdom observerades en ökad incidens av ischemiska kardiovaskulära händelser med ARIMIDEX i ATAC-studien (17 % av patienterna som fick ARIMIDEX 1 mg och 10 % av patienterna på tamoxifen). Överväg riskerna och fördelarna med ARIMIDEX-behandling hos patienter med redan existerande ischemisk hjärtsjukdom [se NEGATIVA REAKTIONER ]
Beneffekter
Resultat från ATAC-provbenssubstudien vid 12 och 24 månader visade att patienter som fick ARIMIDEX hade en genomsnittlig minskning av både ländryggen och total höftbensmineraldensitet (BMD) jämfört med baslinjen. Patienter som fick tamoxifen hade en genomsnittlig ökning av både ländryggen och total BMD i höften jämfört med baslinjen. Överväg övervakning av bentäthet hos patienter som behandlas med ARIMIDEX [se NEGATIVA REAKTIONER ].
Kolesterol
Under ATAC-studien rapporterades fler patienter som fick ARIMIDEX 1 mg ha förhöjt serumkolesterol jämfört med patienter som fick tamoxifen (9 % respektive 3,5 %) [se NEGATIVA REAKTIONER ].
Information om patientrådgivning
Ser FDA godkänd patientmärkning (PATIENTINFORMATION).
Graviditet
Patienter bör informeras om att ARIMIDEX 1 mg kan orsaka fosterskador. De bör också informeras om att ARIMIDEX 1 mg inte är avsett för premenopausala kvinnor; därför, om de blir gravida, ska de sluta ta ARIMIDEX och omedelbart kontakta sin läkare.
Allergiska (överkänslighets) reaktioner
Patienter bör informeras om risken för allvarliga allergiska reaktioner med svullnad av ansikte, läppar, tunga och/eller svalg (angioödem) som kan orsaka svårigheter att svälja och/eller andas och att omedelbart uppsöka läkare.
Ischemiska kardiovaskulära händelser
Patienter med redan existerande ischemisk hjärtsjukdom bör informeras om att en ökad incidens av kardiovaskulära händelser har observerats vid användning av ARIMIDEX 1 mg jämfört med användning av tamoxifen. Om patienter har nya eller förvärrade bröstsmärtor eller andnöd ska de omedelbart uppsöka läkare.
Beneffekter
Patienterna ska informeras om att ARIMIDEX sänker nivån av östrogen. Detta kan leda till en förlust av mineralinnehållet i ben, vilket kan minska benstyrkan. En möjlig konsekvens av minskat mineralinnehåll i ben är en ökad risk för frakturer.
Kolesterol
Patienterna ska informeras om att en förhöjd kolesterolnivå kan ses när de får ARIMIDEX.
Kittling, stickningar eller domningar
Patienter bör informeras om att om de upplever kittling, stickningar eller domningar ska de meddela sin vårdgivare.
Tamoxifen
Patienter bör rådas att inte ta ARIMIDEX med Tamoxifen.
Missade doser
Informera patienterna om att om de missar en dos, ta den så snart de kommer ihåg. Om det nästan är dags för nästa dos, hoppa över den missade dosen och ta nästa regelbundna dos. Patienter ska inte ta två doser samtidigt.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
En konventionell karcinogenesstudie på råttor vid doser på 1,0 till 25 mg/kg/dag (cirka 10 till 243 gånger den dagliga maximala rekommenderade humandosen på mg/m²-basis) administrerad genom oral sondmatning i upp till 2 år visade en ökning av förekomst av hepatocellulärt adenom och karcinom och livmoderstromapolyper hos kvinnor och sköldkörteladenom hos män vid den höga dosen. En dosrelaterad ökning observerades i incidensen av ovarie- och livmoderhyperplasi hos kvinnor. Vid 25 mg/kg/dag var AUC0-24 timmars plasmanivåer hos råttor 110 till 125 gånger högre än nivån som uppvisades hos postmenopausala frivilliga vid den rekommenderade dosen. En separat karcinogenicitetsstudie på möss vid orala doser på 5 till 50 mg/kg/dag (cirka 24 till 243 gånger den dagliga maximala rekommenderade humandosen på mg/m²-basis) under upp till 2 år gav en ökning av incidensen av benigna ovariestroma-, epitel- och granulosacelltumörer vid alla dosnivåer. En dosrelaterad ökning av incidensen av ovariell hyperplasi observerades också hos honmöss. Dessa äggstocksförändringar anses vara gnagarspecifika effekter av aromatasinhibering och är av tvivelaktig betydelse för människor. Incidensen av lymfosarkom ökade hos män och kvinnor vid den höga dosen. Vid 50 mg/kg/dag var AUC-nivåerna i plasma hos möss 35 till 40 gånger högre än nivån hos postmenopausala frivilliga vid den rekommenderade dosen.
ARIMIDEX 1mg har inte visats vara mutagent i in vitro-tester (Ames och E. coli bakteriella tester, CHO-K1 genmutationsanalys) eller klastogena varken in vitro (kromosomavvikelser i humana lymfocyter) eller in vivo (mikronukleustest på råttor) .
Oral administrering av anastrozol till honråttor (från 2 veckor före parning till dräktighet dag 7) gav signifikant incidens av infertilitet och minskade antalet livsdugliga graviditeter vid 1 mg/kg/dag (cirka 10 gånger den rekommenderade dosen för människa på mg/m²-basis och 9 gånger högre än AUC0-24 timmar som hittats hos postmenopausala frivilliga vid den rekommenderade dosen). Förlust av ägg eller foster före implantation ökade vid doser lika med eller högre än 0,02 mg/kg/dag (cirka en femtedel av den rekommenderade dosen för människa på mg/m²-basis). Återhämtning av fertiliteten observerades efter en 5-veckors icke-doseringsperiod som följde efter 3 veckors dosering. Det är inte känt om dessa effekter som observerats hos honråttor tyder på nedsatt fertilitet hos människor.
Flerdosstudier på råttor som administrerades anastrozol i 6 månader i doser lika med eller större än 1 mg/kg/dag (som gav plasmaanastrozol Cssmax och AUC 0-24 timmar som var 19 och 9 gånger högre än de respektive värdena som hittades i postmenopausal frivilliga vid den rekommenderade dosen) resulterade i hypertrofi av äggstockarna och förekomsten av follikulära cystor. Dessutom observerades hyperplastiska livmoder i 6-månadersstudier på honhundar med doser lika med eller större än 1 mg/kg/dag (som producerade plasmaanastrozol Cssmax och AUC0-24 timmar som var 22 gånger och 16 gånger högre än respektive värden hos postmenopausala kvinnor vid den rekommenderade dosen). Det är inte känt om dessa effekter på djurs reproduktionsorgan är associerade med nedsatt fertilitet hos premenopausala kvinnor.
Användning i specifika populationer
Graviditet
Graviditetskategori X [ser KONTRAINDIKATIONER ]
ARIMIDEX kan orsaka fosterskador när det administreras till en gravid kvinna och ger ingen klinisk fördel för premenopausala kvinnor med bröstcancer. ARIMIDEX är kontraindicerat för kvinnor som är eller kan bli gravida. I djurstudier orsakade anastrozol graviditetssvikt, ökad graviditetsförlust och tecken på försenad fosterutveckling. Det finns inga studier på användning av ARIMIDEX 1 mg hos gravida kvinnor. Om ARIMIDEX 1 mg används under graviditet, eller om patienten blir gravid under behandling med detta läkemedel, ska patienten informeras om den potentiella faran för fostret och den potentiella risken för graviditetsförlust.
reproduktionsstudier på djur fick dräktiga råttor och kaniner anastrozol under organogenesen i doser lika med eller större än 1 (råtta) och 1/3 (kaniner) av den rekommenderade dosen för människor på mg/m² basis. Hos båda arterna korsade anastrozol placentan och det fanns ökad graviditetsförlust (ökad förlust före och/eller efter implantation, ökad resorption och minskat antal levande foster). Hos råttor var dessa effekter dosrelaterade och placentavikten ökade signifikant. Fostertoxicitet, inklusive försenad fosterutveckling (dvs ofullständig förbening och sänkt fosterkroppsvikt), inträffade hos råttor vid anastrozoldoser som gav maximala plasmanivåer 19 gånger högre än serumnivåer hos människor vid den terapeutiska dosen (AUC 0-24 timmar 9 gånger högre) . Hos kaniner orsakade anastrozol graviditetssvikt vid doser lika med eller större än 16 gånger den rekommenderade humandosen på mg/m² basis [se Djurtoxikologi och/eller farmakologi ].
Ammande mödrar
Det är inte känt om anastrozol utsöndras i modersmjölk. Eftersom många läkemedel utsöndras i bröstmjölk och på grund av den tumörframkallande egenskapen som visats för anastrozol i djurstudier, eller risken för allvarliga biverkningar hos ammande spädbarn, bör ett beslut fattas om att avbryta amningen eller att avbryta läkemedlet, med hänsyn tagen till drogens betydelse för modern.
Pediatrisk användning
Kliniska studier på pediatriska patienter inkluderade en placebokontrollerad studie på pojkar i puberteten i ungdomsåldern med gynekomasti och en enarmad studie på flickor med McCune-Albrights syndrom och progressiv tidig pubertet. Effekten av ARIMIDEX 1 mg vid behandling av pubertetsgynekomasti hos ungdomar och vid behandling av tidig pubertet hos flickor med McCune-Albrights syndrom har inte visats.
Gynekomastistudie
En randomiserad, dubbelblind, placebokontrollerad, multicenterstudie inkluderade 80 pojkar med pubertalgynekomasti i åldern 11 till 18 år. Patienterna randomiserades till en daglig regim av antingen ARIMIDEX 1 mg eller placebo. Efter 6 månaders behandling fanns det ingen statistiskt signifikant skillnad i andelen patienter som upplevde en ≥ 50 % minskning av gynekomasti (primär effektanalys). Sekundära effektanalyser (absolut förändring i bröstvolym, procentandelen patienter som hade någon minskning av den beräknade volymen av gynekomasti, bröstsmärtaupplösning) överensstämde med den primära effektanalysen. Serumkoncentrationerna av östradiol vid behandlingsmånad 6 minskade med 15,4 % i ARIMIDEX-gruppen och 4,5 % i placebogruppen.
Biverkningar som bedömdes som behandlingsrelaterade av utredarna inträffade hos 16,3 % av de ARIMIDEX-behandlade patienterna och 8,1 % av de placebobehandlade patienterna, varav de vanligaste var akne (7 % ARIMIDEX och 2,7 % placebo) och huvudvärk (7 % ARIMIDEX 1 mg och 0 % placebo); alla andra biverkningar visade små skillnader mellan behandlingsgrupperna. En patient som behandlades med ARIMIDEX 1 mg avbröt studien på grund av testikelförstoring. Den genomsnittliga baseline-subtraherade förändringen i testikelvolymen efter 6 månaders behandling var + 6,6 ± 7,9 cm³ hos de ARIMIDEX-behandlade patienterna och + 5,2 ± 8,0 cm³ i placebogruppen.
McCune-Albrights syndromstudie
En multicenter, enarmad, öppen studie genomfördes på 28 flickor med McCune-Albrights syndrom och progressiv tidig pubertet i åldern 2 till
Fem patienter (18%) upplevde biverkningar som ansågs möjligen relaterade till ARIMIDEX. Dessa var illamående, akne, smärta i en extremitet, ökat alanintransaminas och aspartattransaminas och allergisk dermatit.
Farmakokinetik hos pediatriska patienter
Efter multipel administrering av 1 mg en gång dagligen till pediatriska patienter var medeltiden för att nå maximal anastrozolkoncentration 1 timme. De genomsnittliga (intervall) dispositionsparametrarna för anastrozol hos pediatriska patienter beskrevs av en CL/F på 1,54 L/h (0,77-4,53 L/h) och V/F på 98,4 L (50,7-330,0 L). Den terminala eliminationshalveringstiden var 46,8 timmar, vilket liknade det som observerats hos postmenopausala kvinnor som behandlats med anastrozol för bröstcancer. Baserat på en populationsfarmakokinetisk analys var farmakokinetiken för anastrozol likartad hos pojkar med pubertetsgynekomasti och flickor med McCune-Albrights syndrom.
Geriatrisk användning
studierna 0030 och 0027 var cirka 50 % av patienterna 65 år eller äldre. Patienter ≥ 65 år hade måttligt bättre tumörsvar och tid till tumörprogression än patienter
I ATAC-studien var 45 % av patienterna 65 år eller äldre. Effekten av ARIMIDEX 1 mg jämfört med tamoxifen hos patienter som var 65 år eller äldre (N=1413 för ARIMIDEX och N=1410 för tamoxifen, riskkvoten för sjukdomsfri överlevnad var 0,93 [95 % KI: 0,80, 1,08]) mindre än effekt observerades hos patienter som var yngre än 65 år (N=1712 för ARIMIDEX och N=1706 för tamoxifen, riskkvoten för sjukdomsfri överlevnad var 0,79 [95 % KI: 0,67, 0,94]).
Farmakokinetiken för anastrozol påverkas inte av ålder.
Nedsatt njurfunktion
Eftersom endast cirka 10 % av anastrozol utsöndras oförändrat i urinen, påverkar inte njurfunktionsnedsättningen det totala kroppsclearancen. Dosjustering hos patienter med nedsatt njurfunktion är inte nödvändig [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Plasmakoncentrationerna av anastrozol hos patienter med levercirros låg inom det koncentrationsintervall som sågs hos normala försökspersoner i alla kliniska prövningar. Därför är dosjustering inte heller nödvändig hos patienter med stabil levercirros. ARIMIDEX har inte studerats på patienter med gravt nedsatt leverfunktion [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
ÖVERDOS
Kliniska prövningar har utförts med ARIMIDEX, upp till 60 mg i en engångsdos till friska manliga frivilliga och upp till 10 mg dagligen till postmenopausala kvinnor med avancerad bröstcancer; dessa doser tolererades. En engångsdos av ARIMIDEX 1 mg som resulterar i livshotande symtom har inte fastställts. Det finns ingen specifik motgift mot överdosering och behandlingen måste vara symptomatisk. Vid hantering av en överdos, tänk på att flera medel kan ha tagits. Kräkningar kan framkallas om patienten är uppmärksam. Dialys kan vara till hjälp eftersom ARIMIDEX inte är starkt proteinbundet. Allmän stödjande vård, inklusive frekvent övervakning av vitala tecken och noggrann observation av patienten, är indicerat.
KONTRAINDIKATIONER
Graviditet och premenopausala kvinnor
ARIMIDEX 1mg kan orsaka fosterskador när det administreras till en gravid kvinna och ger ingen klinisk fördel för premenopausala kvinnor med bröstcancer. ARIMIDEX 1mg är kontraindicerat för kvinnor som är eller kan bli gravida. Det finns inga adekvata och välkontrollerade studier på gravida kvinnor som använder ARIMIDEX. Om ARIMIDEX 1 mg används under graviditet, eller om patienten blir gravid medan du tar detta läkemedel, ska patienten informeras om den potentiella faran för ett foster eller potentiell risk för att förlora graviditeten [se Användning i specifika populationer ].
Överkänslighet
ARIMIDEX 1 mg är kontraindicerat för alla patienter som har visat en överkänslighetsreaktion mot läkemedlet eller mot något av hjälpämnena. Observerade reaktioner inkluderar anafylaxi, angioödem och urtikaria [se NEGATIVA REAKTIONER ]
KLINISK FARMAKOLOGI
Handlingsmekanism
Tillväxten av många bröstcancer stimuleras eller upprätthålls av östrogener.
Hos postmenopausala kvinnor härrör östrogener huvudsakligen från verkan av aromatasenzymet, som omvandlar binjure androgener (främst androstenedion och testosteron) till östron och estradiol. Undertryckandet av östrogenbiosyntesen i perifera vävnader och i själva cancervävnaden kan därför uppnås genom att specifikt hämma aromatasenzymet.
Anastrozol är en selektiv icke-steroid aromatashämmare. Det sänker avsevärt serumöstradiolkoncentrationerna och har ingen detekterbar effekt på bildandet av binjurekortikosteroider eller aldosteron.
Farmakodynamik
Effekt på Estradiol
Genomsnittliga serumkoncentrationer av östradiol utvärderades i flera dagliga doseringsstudier med 0,5, 1, 3, 5 och 10 mg ARIMIDEX hos postmenopausala kvinnor med avancerad bröstcancer. Kliniskt signifikant suppression av serumöstradiol sågs med alla doser. Doser på 1 mg och högre resulterade i undertryckande av medelserumkoncentrationer av östradiol till den nedre detektionsgränsen (3,7 pmol/L). Den rekommenderade dagliga dosen, ARIMIDEX 1 mg, minskade östradiol med cirka 70 % inom 24 timmar och med cirka 80 % efter 14 dagars daglig dosering. Undertryckandet av serumöstradiol bibehölls i upp till 6 dagar efter upphörande av daglig dosering med ARIMIDEX 1 mg.
Effekten av ARIMIDEX 1 mg hos premenopausala kvinnor med tidig eller avancerad bröstcancer har inte studerats. Eftersom aromatisering av binjure androgener inte är en signifikant källa till östradiol hos premenopausala kvinnor, förväntas ARIMIDEX inte sänka östradiolnivåerna hos premenopausala kvinnor.
Effekt på kortikosteroider
multipla dagliga doseringsförsök med 3, 5 och 10 mg utvärderades anastrozols selektivitet genom att undersöka effekter på kortikosteroidsyntes. För alla doser påverkade inte anastrozol kortisol- eller aldosteronsekretion vid baslinjen eller som svar på ACTH. Ingen ersättningsbehandling med glukokortikoid eller mineralkortikoid är nödvändig med anastrozol.
Andra endokrina effekter
I flera dagliga doseringsförsök med 5 och 10 mg, mättes sköldkörtelstimulerande hormon (TSH); det fanns ingen ökning av TSH under administrering av ARIMIDEX. ARIMIDEX har inte direkt gestagen, androgen eller östrogen aktivitet hos djur, men stör de cirkulerande nivåerna av progesteron, androgener och östrogener.
Farmakokinetik
Absorption
Hämning av aromatasaktivitet beror främst på anastrozol, moderläkemedlet. Absorptionen av anastrozol är snabb och maximala plasmakoncentrationer inträffar vanligtvis inom 2 timmar efter dosering under fasta. Studier med radioaktivt märkt läkemedel har visat att oralt administrerat anastrozol absorberas väl i den systemiska cirkulationen. Mat minskar hastigheten men inte den totala omfattningen av anastrozolabsorptionen. Medelvärdet för Cmax för anastrozol minskade med 16 % och medianvärdet för Tmax fördröjdes från 2 till 5 timmar när anastrozol administrerades 30 minuter efter mat. Farmakokinetiken för anastrozol är linjär över dosintervallet 1 till 20 mg och ändras inte vid upprepad dosering. Farmakokinetiken för anastrozol var likartad hos patienter och friska frivilliga.
Distribution
Steady-state plasmanivåer är cirka 3 till 4 gånger högre än nivåerna som observerats efter en engångsdos av ARIMIDEX. Plasmakoncentrationer närmar sig steady-state-nivåer vid cirka 7 dagar med dosering en gång dagligen. Anastrozol är till 40 % bundet till plasmaproteiner inom det terapeutiska området.
Ämnesomsättning
Metabolism av anastrozol sker genom N-dealkylering, hydroxylering och glukuronidering. Tre metaboliter av anastrozol (triazol, ett glukuronidkonjugat av hydroxianastrozol och ett glukuronidkonjugat av anastrozol i sig) har identifierats i human plasma och urin. Den huvudsakliga cirkulerande metaboliten av anastrozol, triazol, saknar farmakologisk aktivitet.
Anastrozol hämmade reaktioner katalyserade av cytokrom P450 1A2, 2C8/9 och 3A4 in vitro med Ki-värden som var ungefär 30 gånger högre än de genomsnittliga steady-state Cmax-värdena som observerades efter en daglig dos på 1 mg. Anastrozol hade ingen hämmande effekt på reaktioner katalyserade av cytokrom P450 2A6 eller 2D6 in vitro. Administrering av en enstaka 30 mg/kg eller flera 10 mg/kg doser av anastrozol till friska försökspersoner hade ingen effekt på clearance av antipyrin eller urinåtervinning av antipyrinmetaboliter.
Exkretion
Åttiofem procent av radiomärkt anastrozol återfanns i avföring och urin. Levermetabolismen står för cirka 85 % av elimineringen av anastrozol. Renal elimination svarar för cirka 10 % av det totala clearance. Den genomsnittliga eliminationshalveringstiden för anastrozol är 50 timmar.
Effekt av kön och ålder
Anastrozols farmakokinetik har undersökts hos postmenopausala kvinnliga frivilliga och patienter med bröstcancer. Inga åldersrelaterade effekter sågs över intervallet 80 år.
Effekt av ras
Serumnivåerna av östradiol och östronsulfat var likartade mellan japanska och kaukasiska postmenopausala kvinnor som fick 1 mg anastrozol dagligen i 16 dagar. Anastrozols genomsnittliga steady-state minsta plasmakoncentration hos kaukasiska och japanska postmenopausala kvinnor var 25,7 respektive 30,4 ng/ml.
Effekt av nedsatt njurfunktion
Anastrozols farmakokinetik har undersökts hos personer med nedsatt njurfunktion. Anastrozols njurclearance minskade proportionellt med kreatininclearance och var cirka 50 % lägre hos frivilliga med gravt nedsatt njurfunktion (kreatininclearance DOSERING OCH ADMINISTRERING och Användning i specifika populationer ].
Effekt av nedsatt leverfunktion
Anastrozols farmakokinetik har undersökts hos patienter med levercirros relaterad till alkoholmissbruk. Det skenbara orala clearance (CL/F) av anastrozol var cirka 30 % lägre hos patienter med stabil levercirros än hos kontrollpersoner med normal leverfunktion. Dessa plasmakoncentrationer var dock fortfarande med det värdeintervall som observerades hos normala försökspersoner. Effekten av gravt nedsatt leverfunktion har inte studerats. Ingen dosjustering är nödvändig för stabil levercirros [se DOSERING OCH ADMINISTRERING och Användning i specifika populationer ].
Djurtoxikologi och/eller farmakologi
Reproduktiv toxikologi
Anastrozol har visat sig passera placentan efter oral administrering av 0,1 mg/kg till råttor och kaniner (cirka 1 respektive 1,9 gånger den rekommenderade dosen för människor, på mg/m²-basis). Studier på både råttor och kaniner vid doser lika med eller högre än 0,1 respektive 0,02 mg/kg/dag (cirka 1 respektive 1/3, den rekommenderade dosen för människor på mg/m²-basis), administrerade under perioden med organogenes visade att anastrozol ökade graviditetsförlusten (ökad förlust före och/eller efter implantation, ökad resorption och minskat antal levande foster); effekterna var dosrelaterade hos råttor. Placentalvikten ökade signifikant hos råttor vid doser på 0,1 mg/kg/dag eller mer.
Bevis på fostertoxicitet, inklusive försenad fosterutveckling (dvs ofullständig förbening och sänkt fosterkroppsvikt), observerades hos råttor som fick doser på 1 mg/kg/dag (som producerade plasmaanastrozol Cssmax och AUC 0-24 timmar som var 19 gånger och 9 gånger högre än de respektive värden som hittades hos postmenopausala frivilliga vid den rekommenderade dosen). Det fanns inga tecken på teratogenicitet hos råttor som fick doser upp till 1,0 mg/kg/dag. Hos kaniner orsakade anastrozol dräktighetssvikt vid doser lika med eller större än 1,0 mg/kg/dag (cirka 16 gånger den rekommenderade humandosen på mg/m²-basis); det fanns inga tecken på teratogenicitet hos kaniner som administrerades 0,2 mg/kg/dag (cirka 3 gånger den rekommenderade humandosen på mg/m²-basis).
Kliniska studier
Adjuvansbehandling av bröstcancer hos postmenopausala kvinnor
En multicenter, dubbelblind studie (ATAC) randomiserade 9 366 postmenopausala kvinnor med operabel bröstcancer till adjuvant behandling med ARIMIDEX 1 mg dagligen, tamoxifen 20 mg dagligen eller en kombination av de två behandlingarna under fem år eller tills sjukdomen återkommer.
Studiens primära effektmått var sjukdomsfri överlevnad (dvs. tid till inträffande av ett avlägsna eller lokalt återfall, eller kontralateral bröstcancer eller död av någon orsak). Sekundära effektmått för studien inkluderade sjukdomsfri överlevnad på avstånd, förekomsten av kontralateral bröstcancer och total överlevnad. Vid en medianuppföljning på 33 månader visade kombinationen av ARIMIDEX och tamoxifen ingen effektfördel jämfört med tamoxifen hos alla patienter såväl som i den hormonreceptorpositiva subpopulationen. Denna behandlingsarm avbröts från försöket. Baserat på kliniska och farmakokinetiska resultat från ATAC-studien ska tamoxifen inte administreras tillsammans med anastrozol [se LÄKEMEDELSINTERAKTIONER ].
Demografiska och andra baslinjeegenskaper var likartade bland de tre behandlingsgrupperna (se tabell 7).
Patienter i de två monoterapiarmarna i ATAC-studien behandlades i median 60 månader (5 år) och följdes i median 68 månader. Sjukdomsfri överlevnad i den intention-to-treat-populationen var statistiskt signifikant förbättrad [Hazard Ratio (HR) = 0,87, 95 % CI: 0,78, 0,97, p=0,0127] i ARIMIDEX-armen jämfört med tamoxifen-armen. I den hormonreceptorpositiva subpopulationen som representerade cirka 84 % av försökspatienterna var sjukdomsfri överlevnad också statistiskt signifikant förbättrad (HR = 0,83, 95 % KI: 0,73, 0,94, p=0,0049) i ARIMIDEX 1 mg-armen jämfört med tamoxifen arm.
Figur 1: Sjukdomsfri överlevnad Kaplan Meier överlevnadskurva för alla patienter randomiserade till ARIMIDEX 1 mg eller Tamoxifen Monoterapi i ATAC-studien (Intent-to-Treat) 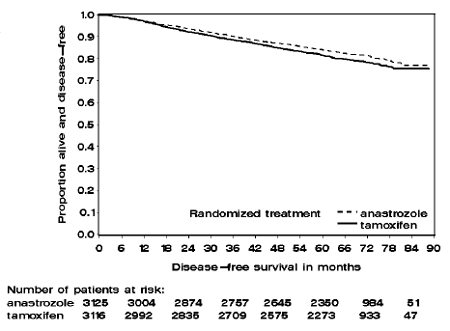
Figur 2: Sjukdomsfri överlevnad för hormonreceptorpositiv subpopulation av patienter randomiserade till ARIMIDEX eller Tamoxifen monoterapi i ATAC-studien 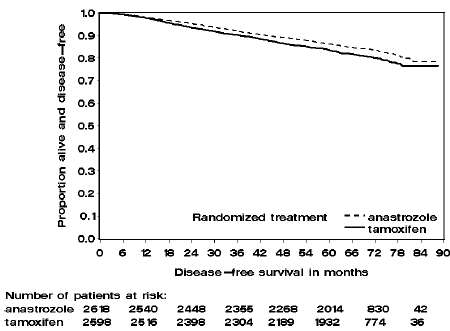
Överlevnadsdata med 68 månaders uppföljning presenteras i tabell 9.
I gruppen patienter som tidigare haft adjuvant kemoterapi (N=698 för ARIMIDEX 1 mg och N=647 för tamoxifen) var riskkvoten för sjukdomsfri överlevnad 0,91 (95 % KI: 0,73 till 1,13) i ARIMIDEX-armen jämfört med tamoxifenarmen.
Frekvensen av individuella händelser i den avsikt att behandla populationen och den hormonreceptorpositiva subpopulationen beskrivs i Tabell 8.
En sammanfattning av studiens effektivitetsresultat finns i Tabell 9.
10-års medianuppföljning Effektresultat från ATAC-studien
I en efterföljande analys av ATAC-studien följdes patienter i de två monoterapiarmarna i median 120 månader (10 år). Patienterna fick studiebehandling i median 60 månader (5 år) (se tabell 10).
Figur 3: Sjukdomsfri överlevnad Kaplan Meier överlevnadskurva för alla patienter randomiserade till ARIMIDEX eller Tamoxifen monoterapi i ATAC-prövningen (Intent-to-Treat)a 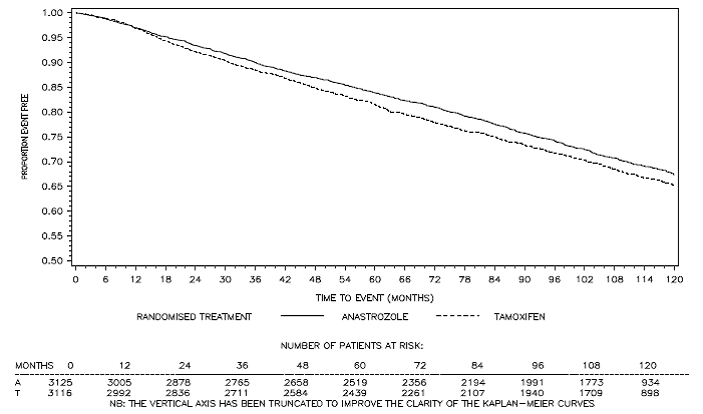
a Andelen patienter med 120 månaders uppföljning var 29,4 %.
Figur 4: Sjukdomsfri överlevnad för hormonreceptorpositiv subpopulation av patienter randomiserade till ARIMIDEX 1 mg eller tamoxifen monoterapi i ATAC-studien 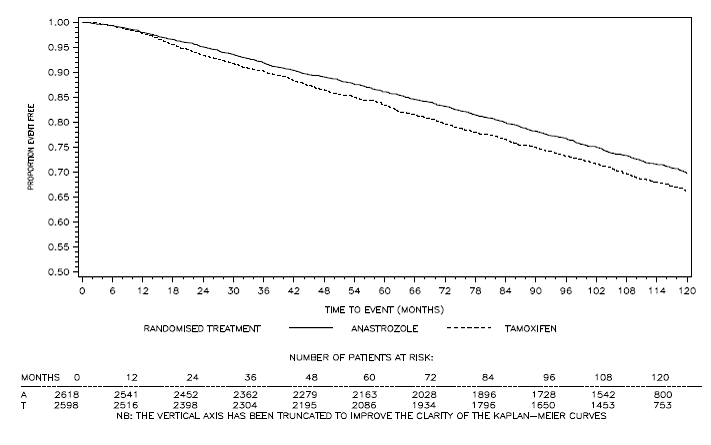
bAndelen patienter med 120 månaders uppföljning var 29,8 %.
Första linjens terapi hos postmenopausala kvinnor med avancerad bröstcancer
Två dubbelblinda, kontrollerade kliniska studier av liknande design (0030, en nordamerikansk studie och 0027, en övervägande europeisk studie) utfördes för att bedöma effekten av ARIMIDEX 1 mg jämfört med tamoxifen som förstahandsbehandling för hormonreceptorpositiv eller hormonreceptor okänd lokalt avancerad eller metastaserad bröstcancer hos postmenopausala kvinnor. Totalt 1021 patienter mellan 30 och 92 år randomiserades för att få provbehandling. Patienterna randomiserades till att få 1 mg ARIMIDEX 1 mg en gång dagligen eller 20 mg tamoxifen en gång dagligen. De primära effektmåtten för båda studierna var tid till tumörprogression, objektiv tumörsvarsfrekvens och säkerhet.
Demografi och andra baslinjeegenskaper, inklusive patienter som hade mätbar och ingen mätbar sjukdom, patienter som fått tidigare adjuvansbehandling, platsen för metastaserande sjukdom och etniskt ursprung var likartade för de två behandlingsgrupperna för båda studierna. Följande tabell sammanfattar hormonreceptorstatusen vid inträde för alla randomiserade patienter i försök 0030 och 0027.
För de primära effektmåtten visade studie 0030 att ARIMIDEX hade en statistiskt signifikant fördel jämfört med tamoxifen (p=0,006) för tiden till tumörprogression; objektiva tumörsvarsfrekvenser var liknande för ARIMIDEX 1 mg och tamoxifen. Försök 0027 visade att ARIMIDEX 1 mg och tamoxifen hade liknande objektiva tumörsvarsfrekvenser och tid till tumörprogression (se tabell 12 och figurerna 5 och 6).
Tabell 12 nedan sammanfattar resultaten från studie 0030 och studie 0027 för de primära effektmåtten.
Figur 5: Kaplan-Meier sannolikhet för tid till sjukdomsprogression för alla randomiserade patienter (intent-to-treat) i försök 0030 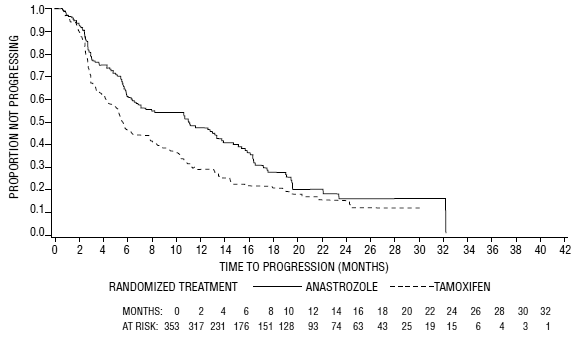
Figur 6: Kaplan-Meier sannolikhet för tid till progression för alla randomiserade patienter (intent-to-treat) i försök 0027 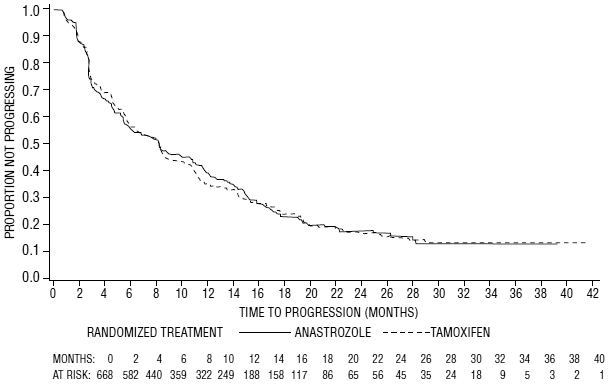
Resultat från de sekundära effektmåtten stödde resultaten från de primära effektmåtten. Det förekom för få dödsfall i behandlingsgrupperna i båda studierna för att dra slutsatser om övergripande överlevnadsskillnader.
Andra linjens terapi hos postmenopausala kvinnor med avancerad bröstcancer som hade sjukdomsprogression efter tamoxifenterapi
Anastrozol studerades i två kontrollerade kliniska prövningar (0004, en nordamerikansk studie; 0005, en övervägande europeisk studie) på postmenopausala kvinnor med avancerad bröstcancer som hade sjukdomsprogression efter tamoxifenbehandling för antingen avancerad eller tidig bröstcancer. Några av patienterna hade också fått tidigare cellgiftsbehandling. De flesta patienter var ER-positiva; en mindre del var ER-okända eller ER-negativa; de ER-negativa patienterna var berättigade endast om de hade haft ett positivt svar på tamoxifen. Kvalificerade patienter med mätbar och icke-mätbar sjukdom randomiserades till att få antingen en engångsdos på 1 mg eller 10 mg ARIMIDEX eller megestrolacetat 40 mg fyra gånger om dagen. Studierna var dubbelblinda med avseende på ARIMIDEX. Tid till progression och objektiv respons (endast patienter med mätbar sjukdom kunde betraktas som partiell respons) var de primära effektvariablerna. Objektiva svarsfrekvenser beräknades utifrån kriterierna för Union Internationale Contre le Cancer (UICC). Frekvensen av förlängd (mer än 24 veckor) stabil sjukdom, progressionshastigheten och överlevnaden beräknades också.
Båda studierna inkluderade över 375 patienter; demografi och andra baslinjeegenskaper var likartade för de tre behandlingsgrupperna i varje studie. Patienter i 0005-studien hade svarat bättre på tidigare tamoxifenbehandling. Av de patienter som deltog som tidigare hade tamoxifenbehandling för avancerad sjukdom (58 % i försök 0004; 57 % i försök 0005), rapporterades 18 % av dessa patienter i försök 0004 och 42 % i försök 0005 av den primära prövaren ha svarat. I försök 0004 var 81 % av patienterna ER-positiva, 13 % var ER-okända och 6 % var ER-negativa. I försök 0005 var 58 % av patienterna ER-positiva, 37 % var ER-okända och 5 % var ER-negativa. I försök 0004 hade 62 % av patienterna mätbar sjukdom jämfört med 79 % i försök 0005. Platserna för metastaserande sjukdom var likartade bland behandlingsgrupperna för varje försök. I genomsnitt hade 40 % av patienterna mjukdelsmetastaser; 60 % hade benmetastaser; och 40 % hade viscerala (15 % lever) metastaser.
Effektresultaten från de två studierna var liknande de som presenteras i Tabell 13. I båda studierna fanns inga signifikanta skillnader mellan behandlingsarmarna med avseende på någon av effektparametrarna som anges i tabellen nedan.
När data från de två kontrollerade studierna slås samman, var de objektiva svarsfrekvenserna och mediantiderna till progression och död liknande för patienter randomiserade till ARIMIDEX 1 mg och megestrolacetat. Det finns, i dessa data, inga indikationer på att ARIMIDEX 10 mg är överlägset ARIMIDEX 1 mg.
PATIENTINFORMATION
ARIMIDEX® A-rim-eh-dex (anastrozol) tabletter för oral administrering
Vilken är den viktigaste informationen jag borde veta om ARIMIDEX?
ARIMIDEX kan orsaka allvarliga biverkningar inklusive:
- hjärtsjukdom. Kvinnor med tidig bröstcancer, som har en historia av blockering i sina hjärtartärer (ischemisk hjärtsjukdom) och som tar ARIMIDEX 1 mg, kan ha en ökning av symtom på minskat blodflöde till hjärtat jämfört med liknande kvinnor som tar tamoxifen.
Få medicinsk hjälp omedelbart om du får ny eller förvärrad bröstsmärta eller andnöd under behandling med ARIMIDEX.
Vad är ARIMIDEX?
ARIMIDEX 1mg är ett receptbelagt läkemedel som används av kvinnor efter klimakteriet ("livsförändringen") för:
- behandling av tidig bröstcancer
- efter operationen
- hos kvinnor vars bröstcancer är hormonreceptorpositiv
- den första behandlingen av bröstcancer som har spridit sig till närliggande vävnader eller lymfkörtlar (lokalt avancerade) eller har spridit sig till andra delar av kroppen (metastaserande), hos kvinnor vars bröstcancer är hormonreceptorpositiv eller hormonreceptorerna inte är kända
- behandling av avancerad bröstcancer, om cancern har vuxit eller sjukdomen har spridit sig efter tamoxifenbehandling
ARIMIDEX 1mg fungerar inte på kvinnor med bröstcancer som inte har gått igenom klimakteriet (premenopausala kvinnor).
Vem ska inte ta ARIMIDEX?
Ta inte ARIMIDEX 1 mg om du:
- är gravida eller kan bli gravida. ARIMIDEX kan skada ditt ofödda barn. Om du blir gravid medan du tar ARIMIDEX, berätta omedelbart för din läkare.
- inte har gått igenom klimakteriet (är premenopausala)
- har haft en allvarlig allergisk reaktion mot anastrozol eller något av innehållsämnena i ARIMIDEX. Se slutet av denna bipacksedel för en komplett lista över ingredienser i ARIMIDEX. Symtom på en allvarlig allergisk reaktion mot ARIMIDEX inkluderar: svullnad av ansikte, läppar, tunga eller svalg, svårt att andas eller svälja, nässelfeber och klåda.
Vad ska jag berätta för min läkare innan jag tar ARIMIDEX 1mg?
Innan du tar ARIMIDEX, tala om för din läkare om du:
- har inte gått igenom klimakteriet. Tala med din läkare om du är osäker.
- har eller haft hjärtproblem
- har fått veta att du har benförtunning eller svaghet (benskörhet)
- har högt kolesterol
- har andra medicinska tillstånd
- är gravid eller planerar att bli gravid. ARIMIDEX kan skada ditt ofödda barn. Se "Vem bör inte ta ARIMIDEX?"
- ammar eller planerar att amma. Det är inte känt om ARIMIDEX går över i bröstmjölk. Du och din läkare bör bestämma om du ska ta ARIMIDEX 1 mg eller amma. Du ska inte göra båda.
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Tala särskilt om för din läkare om du tar:
- tamoxifen. Du ska inte ta ARIMIDEX om du tar tamoxifen. Att ta ARIMIDEX 1 mg tillsammans med tamoxifen kan sänka mängden ARIMIDEX 1 mg i ditt blod och kan göra att ARIMIDEX 1 mg inte fungerar lika bra.
- Läkemedel som innehåller östrogen. ARIMIDEX 1mg kanske inte fungerar om det tas med något av dessa läkemedel:
- hormon ersättnings terapi
- P-piller
- östrogenkrämer
- vaginalringar
- vaginala stolpiller
Vet vilka mediciner du tar. Håll en lista över dem för att visa din läkare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag ta ARIMIDEX?
- Ta ARIMIDEX precis som din läkare säger åt dig att ta det.
- Fortsätt att ta ARIMIDEX tills din läkare säger åt dig att sluta.
- ARIMIDEX 1 mg kan tas med eller utan mat.
- Om du missar en dos, ta den så snart du kommer ihåg det. Om det nästan är dags för din nästa dos, hoppa över den missade dosen. Ta din nästa regelbundna dos. Ta inte två doser samtidigt.
Om du tar för mycket ARIMIDEX 1 mg, ring din läkare eller gå till närmaste akutmottagning direkt.
Vilka är de möjliga biverkningarna av ARIMIDEX?
ARIMIDEX kan orsaka allvarliga biverkningar inklusive:
- Ser "Vilken är den viktigaste informationen jag borde veta om ARIMIDEX?"
- benförtunning eller svaghet (benskörhet). ARIMIDEX 1mg sänker östrogen i kroppen, vilket kan göra att dina ben blir tunnare och svagare. Detta kan öka risken för frakturer, särskilt på ryggraden, höften och handleden. Din läkare kan beställa ett benmineraldensitetstest
- innan du börjar och under behandlingen med ARIMIDEX för att kontrollera dig med avseende på benförändringar.
- ökat kolesterol i blodet (fett i blodet). Din läkare kan ta blodprover för att kontrollera ditt kolesterol medan du tar ARIMIDEX.
- hudreaktioner. Sluta ta ARIMIDEX 1 mg och kontakta din läkare omedelbart om du får hudskador, sår eller blåsor.
- allvarliga allergiska reaktioner. Få medicinsk hjälp omedelbart om du får:
- svullnad av ansikte, läppar, tunga eller svalg
- problem med att svälja eller andas
- leverproblem. ARIMIDEX 1 mg kan orsaka inflammation i din lever och förändringar i leverfunktionsblodprov. Din läkare kan kontrollera dig för detta. Sluta ta ARIMIDEX 1 mg och kontakta din läkare omedelbart om du har något av dessa tecken eller symtom på leverproblem:
- en allmän känsla av att inte må bra
- gulfärgning av huden eller ögonvitorna
- smärta på höger sida av ditt magområde (buk)
Vanliga biverkningar hos kvinnor som tar ARIMIDEX 1 mg inkluderar:
- värmevallningar
- svaghet
- ledvärk
- ledvärk, stelhet eller svullnad (artrit)
- smärta
- öm hals
- högt blodtryck
- depression
- illamående och kräkningar
- utslag
- ryggont
- sömnproblem
- skelettsmärta
- huvudvärk
- svullnad av dina ben, vrister eller fötter
- ökad hosta
- andnöd
- ansamling av lymfvätska i vävnaderna i din drabbade arm (lymfödem)
ARIMIDEX kan också göra att du får kittling, stickningar eller domningar i huden.
Tala om för din läkare om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av ARIMIDEX. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara ARIMIDEX 1mg?
- Förvara ARIMIDEX 1 mg i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
Förvara ARIMIDEX och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av ARIMIDEX.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en patientinformationsbroschyr. Ta inte ARIMIDEX 1 mg för ett tillstånd som det inte har ordinerats för. Ge inte ARIMIDEX till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Om du vill ha mer information, prata med din läkare. Du kan fråga din apotekspersonal eller läkare om information om ARIMIDEX som är skriven för vårdpersonal. För mer information ring 1-866-992-9276 eller gå till www.ARIMIDEX.com.
Vilka är ingredienserna i ARIMIDEX?
Aktiv beståndsdel: anastrozol
Inaktiva Ingredienser: laktos, magnesiumstearat, hydroxipropylmetylcellulosa, polyetylenglykol, povidon, natriumstärkelseglykolat och titandioxid.
