Behandling för kvinnor: Clomid 100mg, 25mg, 50mg Clomiphene Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Clomid 50mg och hur används det?
Clomid 100mg är ett receptbelagt läkemedel som används för att behandla symtom på infertilitet hos kvinnor som har ägglossningssvikt. Clomid kan användas ensamt eller tillsammans med andra mediciner.
Clomid tillhör en klass av läkemedel som kallas selektiva östrogenreceptormodulatorer.
Det är inte känt om Clomid är säkert och effektivt hos barn.
Vilka är de möjliga biverkningarna av Clomid?
Clomid kan orsaka allvarliga biverkningar inklusive:
- magont,
- uppblåsthet,
- illamående,
- kräkningar,
- diarre,
- snabb viktökning (särskilt i ansiktet och mittpartiet),
- lite eller ingen urinering,
- smärta när du andas,
- snabb puls, och
- andnöd
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Clomid inkluderar:
- rodnad (värme, rodnad eller stickningar),
- illamående,
- kräkningar,
- uppblåsthet,
- bröstsmärtor eller ömhet,
- huvudvärk och
- genombrottsblödning eller stänkblödning
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Clomid. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
CLOMID (klomifencitrattabletter USP) är ett oralt administrerat, icke-steroidalt, ägglossningsstimulerande medel betecknat kemiskt som 2-[p-(2-klor-1,2-difenylvinyl)fenoxi]trietylamincitrat (1:1). Den har molekylformeln C26H28ClNO • C6H8O7 och en molekylvikt på 598,09. Det representeras strukturellt som:
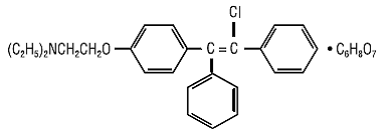
Klomifencitrat är ett vitt till ljusgult, i huvudsak luktfritt, kristallint pulver. Det är fritt lösligt i metanol; löslig i etanol; lätt löslig i aceton, vatten och kloroform; och olöslig i eter.
CLOMID 50mg är en blandning av två geometriska isomerer [cis (zuklomifen) och trans (enklomifen)] som innehåller mellan 30 % och 50 % av cis-isomeren.
Varje tablett med vit skåra innehåller 50 mg klomifencitrat USP. Tabletten innehåller också följande inaktiva ingredienser: majsstärkelse, laktos, magnesiumstearat, förgelatinerad majsstärkelse och sackaros.
INDIKATIONER
CLOMID 100mg är indicerat för behandling av ovulatorisk dysfunktion hos kvinnor som önskar graviditet. Hinder för att uppnå graviditet måste uteslutas eller behandlas adekvat innan behandling med CLOMID 50 mg påbörjas. De patienter som mest sannolikt kommer att nå framgång med klomifenterapi inkluderar patienter med polycystiskt ovariesyndrom (se VARNINGAR : Ovarialt hyperstimuleringssyndrom ), amenorré-galaktorrésyndrom, psykogen amenorré, post-oral-preventiv amenorré och vissa fall av sekundär amenorré av obestämd etiologi.
Rätt tidsinställd samlag i förhållande till ägglossning är viktigt. En basal kroppstemperaturgraf eller andra lämpliga tester kan hjälpa patienten och hennes läkare att avgöra om ägglossning inträffade. När ägglossningen har fastställts bör varje kur med CLOMID 100 mg påbörjas på eller omkring den 5:e dagen av cykeln. Långvarig cyklisk terapi rekommenderas inte utöver totalt cirka sex cykler (inklusive tre ägglossningscykler). (Ser DOSERING OCH ADMINISTRERING och FÖRSIKTIGHETSÅTGÄRDER .)
CLOMID är endast indicerat till patienter med påvisad ovulatorisk dysfunktion som uppfyller de tillstånd som beskrivs nedan:
Dessutom bör patienter som väljs ut för CLOMID-behandling utvärderas med avseende på följande:
Det finns inga adekvata eller välkontrollerade studier som visar effektiviteten av CLOMID 100 mg vid behandling av manlig infertilitet. Dessutom har testikeltumörer och gynekomasti rapporterats hos män som använder klomifen. Orsak och verkan mellan rapporter om testikeltumörer och administrering av CLOMID 25 mg är inte känt.
Även om den medicinska litteraturen föreslår olika metoder, finns det ingen allmänt accepterad standardregim för kombinerad terapi (dvs. CLOMID i kombination med andra ägglossningsframkallande läkemedel). På liknande sätt finns det ingen standard CLOMID-regim för induktion av ägglossning i in vitro-fertiliseringsprogram för att producera ägg för befruktning och återintroduktion. Därför rekommenderas inte CLOMID 50mg för dessa användningar.
DOSERING OCH ADMINISTRERING
allmänna överväganden
Utarbetandet och behandlingen av kandidater för behandling med CLOMID 100 mg bör övervakas av läkare med erfarenhet av behandling av gynekologiska eller endokrina störningar. Patienter bör väljas för behandling med CLOMID 50 mg endast efter noggrann diagnostisk utvärdering (se INDIKATIONER ). Behandlingsplanen bör beskrivas i förväg. Hinder för att uppnå målet med behandlingen måste uteslutas eller behandlas adekvat innan CLOMID påbörjas. Det terapeutiska målet bör balanseras med potentiella risker och diskuteras med patienten och andra inblandade i uppnåendet av en graviditet.
Ägglossning sker oftast från 5 till 10 dagar efter en CLOMID-kur. Samlag bör tidsinställas för att sammanfalla med den förväntade tiden för ägglossning. Lämpliga tester för att fastställa ägglossning kan vara användbara under denna tid.
Rekommenderad dosering
Behandling av den valda patienten bör börja med en låg dos, 50 mg dagligen (1 tablett) i 5 dagar. Dosen bör endast ökas hos de patienter som inte har ägglossning som svar på cyklisk 50 mg CLOMID. En låg dos eller behandlingslängd rekommenderas särskilt om man misstänker ovanlig känslighet för hypofysgonadotropin, såsom hos patienter med polycystiskt ovariesyndrom (se VARNINGAR ; Ovarialt hyperstimuleringssyndrom ).
Patienten bör utvärderas noggrant för att utesluta graviditet, äggstocksförstoring eller cystor på äggstockarna mellan varje behandlingscykel.
Om progestininducerad blödning planeras, eller om spontan uterin blödning inträffar före behandling, bör kuren med 50 mg dagligen i 5 dagar påbörjas på eller omkring den 5:e dagen av cykeln. Behandling kan påbörjas när som helst hos patienten som inte har haft någon livmoderblödning nyligen. När ägglossning inträffar vid denna dos, är det ingen fördel att öka dosen i efterföljande behandlingscykler.
Om ägglossningen inte tycks inträffa efter den första behandlingskuren, bör en andra kur på 100 mg dagligen (två 50 mg tabletter som en enstaka daglig dos) ges under 5 dagar. Denna kurs kan påbörjas så tidigt som 30 dagar efter den föregående efter att försiktighetsåtgärder vidtagits för att utesluta graviditet. Ökning av dosen eller behandlingslängden över 100 mg/dag under 5 dagar rekommenderas inte.
Majoriteten av patienterna som ska ha ägglossning kommer att göra det efter den första behandlingen. Om ägglossning inte inträffar efter tre behandlingskurer, rekommenderas inte ytterligare behandling med CLOMID 50 mg och patienten bör omvärderas. Om tre ägglossningssvar inträffar, men graviditet inte har uppnåtts, rekommenderas inte ytterligare behandling. Om menstruation inte inträffar efter ett ägglossningssvar, bör patienten omvärderas. Långvarig cyklisk terapi rekommenderas inte utöver totalt cirka sex cykler (se FÖRSIKTIGHETSÅTGÄRDER ).
HUR LEVERERAS
NDC 0068-0226-30: 50 mg tabletter i kartonger med 30 tabletter är runda, vita, skårade och präglade CLOMID 50. Förvara tabletter vid kontrollerad rumstemperatur 59-86°F (15-30°C). Skydda mot värme, ljus och överdriven luftfuktighet och förvara i slutna behållare.
Tillverkad av: A SANOFI COMPANY, sanofi-aventis US LLC, Bridgewater, NJ 08807. Reviderad: juli 2017
BIEFFEKTER
Biverkningar från kliniska prövningar.
CLOMID, vid rekommenderade doser, tolereras i allmänhet väl. Biverkningarna har vanligtvis varit milda och övergående och de flesta har försvunnit omedelbart efter att behandlingen har avbrutits. Biverkningar som rapporterats hos patienter som behandlats med klomifencitrat under kliniska studier visas i tabell 2.
Följande biverkningar har rapporterats hos färre än 1 % av patienterna i kliniska prövningar: Akut buk, ökad aptit, förstoppning, dermatit eller hudutslag, depression, diarré, yrsel, trötthet, håravfall/torrt hår, ökad urinfrekvens/volym, sömnlöshet, yrsel, nervös spänning, vaginal torrhet, svindel, viktökning/förlust.
Patienter på långvarig behandling med CLOMID 25 mg kan visa förhöjda serumnivåer av desmosterol. Detta beror med största sannolikhet på en direkt störning av kolesterolsyntesen. Serumsterolerna hos patienter som får den rekommenderade dosen av CLOMID 50 mg är dock inte signifikant förändrade. Ovariecancer har sällan rapporterats hos patienter som har fått fertilitetsläkemedel. Infertilitet är en primär riskfaktor för äggstockscancer; epidemiologiska data tyder dock på att långvarig användning av klomifen kan öka risken för en borderline eller invasiv äggstockstumör.
Biverkningar efter marknadsföring
Följande biverkningar har identifierats under användning av Clomid efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Kroppen som helhet: Feber, tinnitus, svaghet
Kardiovaskulär: Arytmi, bröstsmärtor, ödem, högt blodtryck, hjärtklappning, flebit, lungemboli, andnöd, takykardi, tromboflebit
Centrala nervsystemet: Migränhuvudvärk, parestesi, anfall, stroke, synkope
Dermatologiska: Akne, allergisk reaktion, erytem, erythema multiforme, erythema nodosum, hypertrichosis, pruritus, urticaria
Foster/neonatala anomalier:
- Onormal benutveckling: skelettmissbildningar i skalle, ansikte, näsgångar, käke, hand, lem (ekromelia inklusive amelia, hemimelia och phocomelia), fot (klumpfot), ryggrad och leder
- Hjärtavvikelser: septalhjärtdefekter, muskelkammarseptumdefekt, patent ductus arteriosus, tetralogi av Fallot och koarktation av aortan
- Kromosomala störningar: Downs syndrom
- Öronavvikelser och dövhet
- Avvikelser i mag-tarmkanalen: läpp- och gomspalt, imperforerad anus, trakeesofageal fistel, diafragmabråck, omphalocele
- Genitaliaavvikelser: hypospadi, kloakexstrofi
- Missbildningar i lungvävnaden
- Missbildningar i ögat och linsen (katarakt)
- Neoplasmer: neuroektodermal tumör, sköldkörteltumör, hepatoblastom, lymfatisk leukemi
- Avvikelser i nervsystemet: neuralrörsdefekter (anencefali, meningomyelocele), mikrocefali och hydrocefalus
- Njuravvikelser: njur-agenes och renal dysgenes
- Andra: dvärgväxt, utvecklingsstörning
Gastrointestinala: Pankreatit
Genitourinära: Endometrios, ovariecystor (ovarieförstoring eller cystor kan som sådan kompliceras av adnexal torsion), äggstocksblödning, äggledargraviditet, livmoderblödning, minskad endometrietjocklek
Lever: Transaminaser ökade, hepatit
Metabolismstörningar: Hypertriglyceridemi, i vissa fall med pankreatit
Muskuloskeletala: Artralgi, ryggont, myalgi
Neoplasmer: Lever (hepatiskt hemangiosarkom, levercellsadenom, hepatocellulärt karcinom); bröst (fibrocystisk sjukdom, bröstkarcinom); endometrium (endometriekarcinom); nervsystemet (astrocytom, hypofystumör, prolaktinom, neurofibromatos, glioblastoma multiforme, hjärnabcess); äggstock (luteom av graviditet, dermoid cysta i äggstocken, äggstockscancer); trofoblastisk (hydatiform mullvad, choriocarcinom); diverse (melanom, myelom, perianala cystor, njurcellscancer, Hodgkins lymfom, tungcancer, blåscancer)
Psykiatrisk: Ångest, irritabilitet, humörförändringar, psykoser
Synstörningar: Onormal logi, grå starr, ögonsmärta, makulaödem, optikusneurit, fotopsi, posterior glaskroppsavlossning, retinal blödning, retinal trombos, retinal vaskulär spasm, tillfällig eller långvarig synförlust, möjligen irreversibel.
Övrig: Leukocytos, sköldkörtelstörning
LÄKEMEDELSINTERAKTIONER
Läkemedelsinteraktioner med CLOMID har inte dokumenterats.
Narkotikamissbruk och beroende
Tolerans, missbruk eller beroende av CLOMID har inte rapporterats.
VARNINGAR
Visuella symtom
Patienter bör informeras om att suddighet eller andra synsymtom såsom fläckar eller blixtar (scintillerande scotomater) ibland kan uppstå under behandling med CLOMID. Dessa visuella symtom ökar i incidens med ökande totaldos eller behandlingslängd. Dessa synstörningar är vanligtvis reversibla; dock har fall av långvarig synstörning rapporterats, varav några inträffade efter utsättande av CLOMID 50 mg. Synstörningarna kan vara irreversibla, särskilt med ökad dos eller behandlingslängd. Patienter bör varnas för att dessa visuella symtom kan göra sådana aktiviteter som att köra bil eller använda maskiner mer riskfyllda än vanligt, särskilt under förhållanden med varierande belysning.
Dessa visuella symtom verkar bero på intensifiering och förlängning av efterbilder. Symtomen uppträder ofta först eller accentueras vid exponering för en starkt upplyst miljö. Även om uppmätt synskärpa vanligtvis inte har påverkats, utvecklade en studiepatient som tog 200 mg CLOMID dagligen synsuddighet på den 7:e behandlingsdagen, vilket steg till en kraftig minskning av synskärpan den 10:e dagen. Ingen annan abnormitet hittades och synskärpan återgick till det normala den 3:e dagen efter att behandlingen avslutats.
Oftalmologiskt definierbara scotomater och förändringar i retinala cellfunktioner (elektroretinografiska) har också rapporterats. En patient som behandlades under kliniska studier utvecklade fosfener och scotomater under långvarig administrering av CLOMID 50 mg, som försvann den 32:a dagen efter avslutad behandling.
Övervakning efter marknadsföring av biverkningar har också avslöjat andra visuella tecken och symtom under behandling med CLOMID (se NEGATIVA REAKTIONER ).
Även om etiologin för dessa visuella symtom ännu inte är klarlagd, bör patienter med visuella symtom avbryta behandlingen och få en fullständig oftalmologisk utvärdering omedelbart.
Ovarialt hyperstimuleringssyndrom
Ovarialt hyperstimuleringssyndrom (OHSS) har rapporterats förekomma hos patienter som får klomifencitratbehandling för induktion av ägglossning. OHSS kan utvecklas snabbt (inom 24 timmar till flera dagar) och bli en allvarlig medicinsk störning. I vissa fall inträffade OHSS efter cyklisk användning av klomifencitratbehandling eller när klomifencitrat användes i kombination med gonadotropiner. Övergående avvikelser i leverfunktionstest som tyder på leverdysfunktion, som kan åtföljas av morfologiska förändringar på leverbiopsi, har rapporterats i samband med OHSS.
OHSS är en medicinsk händelse som skiljer sig från okomplicerad äggstocksförstoring. De kliniska tecknen på detta syndrom i svåra fall kan inkludera kraftig äggstocksförstoring, gastrointestinala symtom, ascites, dyspné, oliguri och pleurautgjutning. Dessutom har följande symtom rapporterats i samband med detta syndrom: perikardiell utgjutning, anasarca, hydrothorax, akut buk, hypotoni, njursvikt, lungödem, intraperitoneal och ovarieblödning, djup ventrombos, vridning av äggstockarna och akut andning ångest. De tidiga varningstecknen på OHSS är buksmärtor och utspändhet, illamående, kräkningar, diarré och viktökning. Förhöjda steroidnivåer i urinen, olika grader av elektrolytobalans, hypovolemi, hemokoncentration och hypoproteinemi kan förekomma. Död på grund av hypovolemisk chock, hemokoncentration eller tromboembolism har inträffat. På grund av bräcklighet hos förstorade äggstockar i svåra fall bör buk- och bäckenundersökning utföras mycket försiktigt. Om befruktning resulterar, kan snabb progression till den allvarliga formen av syndromet inträffa.
För att minimera risken förknippad med enstaka onormal äggstocksförstoring i samband med behandling med CLOMID 100 mg, bör den lägsta dosen som överensstämmer med förväntade kliniska resultat användas. Maximal förstoring av äggstocken, vare sig den är fysiologisk eller onormal, kanske inte inträffar förrän flera dagar efter avslutad behandling med den rekommenderade dosen av CLOMID. Vissa patienter med polycystiskt ovariesyndrom som är ovanligt känsliga för gonadotropin kan ha ett överdrivet svar på vanliga doser av CLOMID. Därför bör patienter med polycystiskt ovariesyndrom påbörjas med den lägsta rekommenderade dosen och kortaste behandlingstiden för den första behandlingen (se DOSERING OCH ADMINISTRERING ).
Om förstoring av äggstocken inträffar ska ytterligare CLOMID-behandling inte ges förrän äggstockarna har återgått till storleken före behandlingen, och dosen eller varaktigheten av nästa kur bör reduceras. Äggstocksförstoring och cystbildning i samband med CLOMID 50 mg-behandling går vanligtvis tillbaka spontant inom några dagar eller veckor efter avslutad behandling. Den potentiella nyttan av efterföljande behandling med CLOMID 25 mg i dessa fall bör överstiga risken. Såvida det inte finns kirurgisk indikation för laparotomi, bör sådan cystisk förstoring alltid hanteras konservativt.
Ett orsakssamband mellan ovariehyperstimulering och äggstockscancer har inte fastställts. Men eftersom en korrelation mellan äggstockscancer och nulliparitet, infertilitet och ålder har föreslagits, om ovariecystor inte regresserar spontant, bör en grundlig utvärdering göras för att utesluta förekomsten av ovarieneoplasi.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Noggrann uppmärksamhet bör ägnas valet av kandidater för CLOMID-behandling. Bäckenundersökning är nödvändig före behandling med CLOMID och före varje efterföljande behandling (se KONTRAINDIKATIONER och VARNINGAR ).
Karcinogenes, Mutagenes, Nedsatt fertilitet
Långtidstoxicitetsstudier på djur har inte utförts för att utvärdera den karcinogena eller mutagena potentialen hos klomifencitrat.
Oral administrering av CLOMID 25 mg till hanråttor i doser på 0,3 eller 1 mg/kg/dag orsakade minskad fertilitet, medan högre doser orsakade tillfällig infertilitet. Orala doser på 0,1 mg/kg/dag hos honråttor avbröt temporärt det normala cykliska vaginalutstrykningsmönstret och förhindrade befruktning. Doser på 0,3 mg/kg/dag minskade något ägglossade ägg och corpora lutea, medan 3 mg/kg/dag hämmade ägglossningen.
Graviditet
Sammanfattning av fosterrisk
Användning av CLOMID 100 mg till gravida kvinnor är kontraindicerat, eftersom behandling med CLOMID 25 mg inte ger någon nytta för denna population.
Tillgängliga humandata tyder inte på en ökad risk för medfödda anomalier över bakgrundspopulationsrisken. Reproduktionstoxikologiska studier på djur visade dock ökad embryo-fosterförlust och strukturella missbildningar hos avkomma. Om detta läkemedel används under graviditet, eller om patienten blir gravid medan du tar detta läkemedel, bör patienten informeras om de potentiella riskerna för fostret.
Kliniska överväganden
För att undvika oavsiktlig administrering av CLOMID 25 mg under tidig graviditet, bör lämpliga tester användas under varje behandlingscykel för att fastställa om ägglossning och/eller graviditet inträffar. Patienter bör utvärderas noggrant för att utesluta ovarieförstoring eller cystor på äggstockarna mellan varje behandlingscykel. Nästa kur med CLOMID-behandling bör skjutas upp tills dessa tillstånd har uteslutits.
Mänskliga data
Tillgängliga humandata från epidemiologiska studier visar inte något tydligt orsaks- och effektsamband mellan klomifencitrat perikonceptuell exponering och en ökad risk för övergripande fosterskador eller någon specifik anomali. Men på grund av det lilla antalet fall av medfödda anomalier som förekommer hos klomifencitratbehandlade kvinnor, kunde dessa epidemiologiska studier endast utesluta stora skillnader i risk. Studierna tog inte hänsyn till faktorer associerade med kvinnlig subfertilitet och kunde inte justera för andra viktiga konfounders. Dessutom stödjer inte tillgängliga data en ökad frekvens av spontanaborter bland subfertila kvinnor som behandlats med klomifencitrat för induktion av ägglossning.
Djurdata
Oral administrering av klomifencitrat till dräktiga råttor under organogenes i doser på 1 till 2 mg/kg/dag resulterade i hydramnion och svaga, ödemösa foster med vågiga revben och andra tillfälliga benförändringar. Doser på 8 mg/kg/dag eller mer orsakade också ökade resorptioner och döda foster, dystoki och försenad förlossning, och 40 mg/kg/dag resulterade i ökad mödradödlighet. Engångsdoser på 50 mg/kg orsakade grå starr hos fostret, medan 200 mg/kg orsakade gomspalt. Efter injektion av klomifencitrat 2 mg/kg till möss och råttor under graviditeten uppvisade avkomman metaplastiska förändringar i fortplantningsorganen. Nyfödda möss och råttor som injicerades under de första dagarna av livet utvecklade också metaplastiska förändringar i livmoder- och slidslemhinnan, såväl som för tidig öppning av slidan och ovarier. Dessa fynd liknar det onormala reproduktionsbeteendet och steriliteten som beskrivs med andra östrogener och antiöstrogener.
Hos kaniner sågs vissa tillfälliga benförändringar hos foster från mödrar som fått orala doser på 20 eller 40 mg/kg/dag under graviditeten, men inte efter 8 mg/kg/dag. Inga permanenta missbildningar observerades i dessa studier. Rhesusapor som fick orala doser på 1,5 till 4,5 mg/kg/dag under olika perioder under graviditeten fick inte heller några onormala avkommor.
Ammande mödrar
Det är inte känt om CLOMID utsöndras i modersmjölk. Eftersom många läkemedel utsöndras i bröstmjölk bör försiktighet iakttas om CLOMID ges till en ammande kvinna. Hos vissa patienter kan CLOMID minska amningen.
Äggstockscancer
Långvarig användning av klomifencitrattabletter USP kan öka risken för en borderline eller invasiv äggstockstumör (se NEGATIVA REAKTIONER ).
ÖVERDOS
Tecken och symtom
Toxiska effekter som åtföljer akut överdosering av CLOMID 50 mg har inte rapporterats. Tecken och symtom på överdosering som ett resultat av användning av mer än den rekommenderade dosen under behandling med CLOMID 100 mg inkluderar illamående, kräkningar, vasomotoriska rodningar, synsudd, fläckar eller blixtar, scotomat, äggstocksförstoring med bäcken- eller buksmärtor. (Ser KONTRAINDIKATIONER : Cystor på äggstockarna .)
Oral LD50
Den akuta orala LD50 för CLOMID 25 mg är 1700 mg/kg hos möss och 5750 mg/kg hos råttor. Den toxiska dosen hos människor är inte känd.
Dialys
Det är inte känt om CLOMID är dialyserbart.
Behandling
I händelse av överdosering bör lämpliga stödåtgärder vidtas utöver gastrointestinal dekontaminering.
KONTRAINDIKATIONER
Överkänslighet
CLOMID 100mg är kontraindicerat för patienter med känd överkänslighet eller allergi mot klomifencitrat eller mot något av dess ingredienser.
Graviditet
Användning av CLOMID till gravida kvinnor är kontraindicerat, eftersom CLOMID inte ger någon nytta i denna population.
Tillgängliga humandata tyder inte på en ökad risk för medfödda anomalier över bakgrundspopulationsrisken vid användning enligt indikation. Reproduktionstoxikologiska studier på djur visade dock ökad embryo-fosterförlust och strukturella missbildningar hos avkomma. Om detta läkemedel används under graviditet, eller om patienten blir gravid medan du tar detta läkemedel, bör patienten informeras om de potentiella riskerna för fostret. (Ser FÖRSIKTIGHETSÅTGÄRDER : Graviditet .)
Leversjukdom
Behandling med CLOMID 25 mg är kontraindicerad hos patienter med leversjukdom eller tidigare leverdysfunktion (se även INDIKATIONER och NEGATIVA REAKTIONER ).
Onormal livmoderblödning
CLOMID 25mg är kontraindicerat hos patienter med onormal livmoderblödning av obestämt ursprung (se INDIKATIONER ).
Cystor på äggstockarna
CLOMID är kontraindicerat hos patienter med ovariecystor eller förstoring som inte beror på polycystiskt ovariesyndrom (se INDIKATIONER och VARNINGAR ).
Övrig
CLOMID är kontraindicerat hos patienter med okontrollerad sköldkörtel- eller binjuredysfunktion eller i närvaro av en organisk intrakraniell lesion såsom hypofystumör (se INDIKATIONER ).
KLINISK FARMAKOLOGI
Handling
CLOMID 25mg är ett läkemedel med betydande farmakologisk styrka. Med noggrant urval och korrekt behandling av patienten har CLOMID 100 mg visat sig vara en användbar terapi för den anovulatoriska patienten som önskar graviditet.
Klomifencitrat kan interagera med östrogenreceptorinnehållande vävnader, inklusive hypotalamus, hypofysen, äggstocken, endometrium, slidan och livmoderhalsen. Det kan konkurrera med östrogen om östrogen-receptorbindningsställen och kan fördröja påfyllning av intracellulära östrogenreceptorer. Klomifencitrat initierar en serie endokrina händelser som kulminerar i en preovulatorisk gonadotropinökning och efterföljande follikelruptur. Den första endokrina händelsen som svar på en kur av klomifenterapi är en ökning av frisättningen av hypofysgonadotropiner. Detta initierar steroidogenes och follikulogenes, vilket resulterar i tillväxt av äggstocksfollikeln och en ökning av den cirkulerande nivån av östradiol. Efter ägglossning stiger och faller plasmaprogesteron och östradiol som de skulle göra i en normal ägglossningscykel.
Tillgängliga data tyder på att både de östrogena och antiöstrogena egenskaperna hos klomifen kan delta i initieringen av ägglossningen. De två klomifenisomererna har visat sig ha blandade östrogena och antiöstrogena effekter, som kan variera från en art till en annan. Vissa data tyder på att zuklomifen har större östrogen aktivitet än enklomifen.
Klomifencitrat har inga uppenbara progestationella, androgena eller antiandrogena effekter och verkar inte störa hypofys-binjure- eller hypofys-tyreoideafunktionen. Även om det inte finns några bevis för en "överföringseffekt" av CLOMID, har spontana ägglossningsmenstruationer noterats hos vissa patienter efter behandling med CLOMID 100 mg.
Farmakokinetik
Baserat på tidiga studier med 14C-märkt klomifencitrat visades läkemedlet absorberas lätt oralt hos människor och utsöndras huvudsakligen i avföringen. Kumulativ urin- och fekal utsöndring av 14C var i genomsnitt cirka 50 % av den orala dosen och 37 % av en intravenös dos efter 5 dagar. Den genomsnittliga urinutsöndringen var cirka 8 % med fekal utsöndring på cirka 42 %.
En del 14C-märkning fanns fortfarande i avföringen 6 veckor efter administrering. Efterföljande enkeldosstudier på normala frivilliga visade att zuklomifen (cis) har en längre halveringstid än enklomifen (trans). Detekterbara nivåer av zuklomifen kvarstod i längre än en månad hos dessa patienter. Detta kan tyda på stereospecifik enterohepatisk återvinning eller sekvestrering av zuklomifenen. Det är således möjligt att något aktivt läkemedel kan finnas kvar i kroppen under tidig graviditet hos kvinnor som blir gravida i menstruationscykeln under CLOMID-behandling.
Kliniska studier
Under kliniska undersökningar fick 7578 patienter CLOMID, av vilka några hade andra hinder för ägglossning än ägglossningsstörning (se INDIKATIONER ). I dessa kliniska prövningar inträffade framgångsrik terapi karakteriserad av graviditet hos cirka 30 % av dessa patienter.
Det rapporterades totalt 2635 graviditeter under den kliniska prövningsperioden. Av dessa graviditeter fanns information om utfallet endast tillgänglig för 2369 av fallen. Tabell 1 sammanfattar utgången av dessa fall.
Av de rapporterade graviditeterna var incidensen av flerbördsgraviditeter 7,98 %: 6,9 % tvilling, 0,5 % trilling, 0,3 % fyrling och 0,1 % femling. Av de 165 tvillinggraviditeter för vilka tillräcklig information fanns tillgänglig var förhållandet mellan enäggstvillingar och tvåäggstvillingar cirka 1:5. Tabell 1 rapporterar överlevnadsgraden för de levande flerfödda barnen.
En sextuplettfödsel rapporterades efter slutförandet av ursprungliga kliniska studier; ingen av sextupletterna överlevde (var och en vägde mindre än 400 g), även om var och en verkade grovt normal.
Den totala överlevnaden för spädbarn från flerbördsgraviditeter inklusive spontana aborter, dödfödslar och neonatala dödsfall är 73 %.
Fetal/neonatala anomalier och dödlighet
Följande fetala abnormiteter har rapporterats efter graviditeter efter ägglossningsinduktionsbehandling med CLOMID under kliniska prövningar. Var och en av följande fosteravvikelser rapporterades i en frekvens av
Dessutom har rapporter om medfödda anomalier mottagits under övervakning efter marknadsföring av CLOMID (se NEGATIVA REAKTIONER ).
PATIENTINFORMATION
Syftet med och riskerna med CLOMID-behandling ska presenteras för patienten innan behandlingen påbörjas. Det bör betonas att målet med CLOMID-behandling är ägglossning för efterföljande graviditet. Läkaren bör ge patienten råd med särskild hänsyn till följande potentiella risker:
Visuella symtom
Meddela att suddighet eller andra visuella symtom ibland kan uppstå under eller strax efter CLOMID-behandling. Det bör göras klart för patienten att synstörningar i vissa fall kan vara långvariga och möjligen irreversibla, särskilt med ökad dos eller behandlingslängd. Varna för att visuella symtom kan göra sådana aktiviteter som att köra bil eller använda maskiner mer farliga än vanligt, särskilt under förhållanden med varierande belysning (se VARNINGAR ).
Patienten bör instrueras att informera läkaren närhelst några ovanliga synsymptom uppstår. Om patienten har några synsymptom ska behandlingen avbrytas och fullständig oftalmologisk utvärdering utföras.
Buksmärta/bäckensmärta eller utspändhet
Förstoring av äggstockarna kan inträffa under eller kort efter behandling med CLOMID. För att minimera riskerna förknippade med äggstocksförstoring bör patienten instrueras att informera läkaren om eventuell buk- eller bäckensmärta, viktökning, obehag eller utspändhet efter att ha tagit CLOMID (se VARNINGAR ).
Multipelgraviditet
Informera patienten om att det finns en ökad risk för flerbördsgraviditet, inklusive bilateral äggledargraviditet och samexisterande äggledar- och intrauterin graviditet, när befruktning inträffar i samband med CLOMID-behandling. De potentiella komplikationerna och riskerna med flerbördsgraviditet bör förklaras.
Spontan abort och medfödda anomalier
Informera patienten om att tillgängliga data inte tyder på någon ökning av frekvensen av spontana abort (missfall) eller medfödda anomalier med moderns användning av CLOMID 50 mg jämfört med frekvensen i den allmänna befolkningen.
Under klinisk undersökning visar erfarenheten från patienter med känt graviditetsutfall (tabell 1) en spontanabortfrekvens på 20,4 % och frekvens av dödfödsel på 1,0 %. (Ser Kliniska studier ). Bland de födelseanomalier som spontant rapporterats som individuella fall sedan den kommersiella tillgängligheten av Clomid har andelen neuralrörsdefekter varit hög bland graviditeter i samband med ägglossning inducerad av Clomid, men detta har inte stöds av data från populationsbaserade studier.
