Singulair 10mg, 4mg, 5mg Montelukast Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Singulair och hur används det?
Singulair 5mg är ett receptbelagt läkemedel som används för att behandla symtom på astma, ansträngningsutlöst bronkospasm och allergisk eller året runt (perenn) rinit. Singulair kan användas ensamt eller tillsammans med andra läkemedel.
- Singulair tillhör en klass av läkemedel som kallas Leukotriene Receptor Antagonists.
- Det är inte känt om Singulair är säkert och effektivt för barn yngre än 1 år.
Vilka är de möjliga biverkningarna av Singulair?
Singulair kan orsaka allvarliga biverkningar inklusive:
- ovanliga förändringar i humör eller beteende,
- hudutslag,
- blåmärken,
- kraftig stickning,
- domningar,
- smärta,
- muskelsvaghet,
- öronsmärta,
- svullnad,
- värme,
- feber,
- öm hals,
- svullnad i ansiktet eller tungan,
- brännande i ögonen, och
- hudsmärta, följt av ett rött eller lila utslag som sprider sig till din överkropp och orsakar blåsor och fjällning
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Singulair inkluderar:
- magont,
- diarre,
- feber,
- influensa symptom,
- förkylningssymtom (täppt näsa, smärta i bihålorna, hosta, ont i halsen),
- huvudvärk och
- sängvätning eller förlust av urinblåsan hos barn
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Singulair. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Montelukastnatrium, den aktiva ingrediensen i SINGULAIR 4mg, är en selektiv och oralt aktiv leukotrienreceptorantagonist som hämmar cysteinylleukotrien CysLT1-receptorn.
Montelukastnatrium beskrivs kemiskt som [R-(E)]-1-[[[1-[3-[2-(7-klor-2-kinolinyl)etenyl]fenyl]-3-[2-(1-hydroxi -1-metyletyl)fenyl]propyl]tio]metyl]cyklopropanättiksyra, mononatriumsalt.
Den empiriska formeln är C35H35ClNNaO3S, och dess molekylvikt är 608,18. Strukturformeln är:
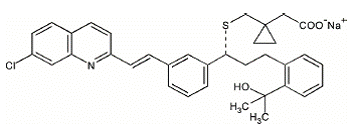
Montelukastnatrium är ett hygroskopiskt, optiskt aktivt, vitt till benvitt pulver. Montelukastnatrium är fritt lösligt i etanol, metanol och vatten och praktiskt taget olösligt i acetonitril.
Varje 10 mg filmdragerad SINGULAIR-tablett innehåller 10,4 mg montelukastnatrium, vilket motsvarar 10 mg montelukast, och följande inaktiva ingredienser: mikrokristallin cellulosa, laktosmonohydrat, kroskarmellosnatrium, hydroxipropylcellulosa och magnesiumstearat. Filmbeläggningen består av hydroxipropylmetylcellulosa, hydroxipropylcellulosa, titandioxid, röd järnoxid, gul järnoxid och karnaubavax.
Varje 4 mg och 5 mg tuggbar SINGULAIR tablett innehåller 4,2 respektive 5,2 mg montelukastnatrium, vilket motsvarar 4 respektive 5 mg montelukast. Båda tuggtabletterna innehåller följande inaktiva ingredienser: mannitol, mikrokristallin cellulosa, hydroxipropylcellulosa, röd järnoxid, kroskarmellosnatrium, körsbärsarom, aspartam och magnesiumstearat.
Varje förpackning med SINGULAIR 4 mg orala granulat innehåller 4,2 mg montelukastnatrium, vilket motsvarar 4 mg montelukast. Den orala granulformuleringen innehåller följande inaktiva ingredienser: mannitol, hydroxipropylcellulosa och magnesiumstearat.
INDIKATIONER
Astma
SINGULAIR® är indicerat för profylax och kronisk behandling av astma hos vuxna och pediatriska patienter 12 månader och äldre.
Ansträngningsinducerad bronkokonstriktion (EIB)
SINGULAIR är indicerat för förebyggande av ansträngningsutlöst bronkokonstriktion (EIB) hos patienter 6 år och äldre.
Allergisk rinit
SINGULAIR 10 mg är indicerat för lindring av symtom på säsongsbunden allergisk rinit hos patienter 2 år och äldre och perenn allergisk rinit hos patienter 6 månader och äldre. Eftersom fördelarna med SINGULAIR 4mg kanske inte uppväger risken för neuropsykiatriska symtom hos patienter med allergisk rinit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ], reservanvändning för patienter som har ett otillräckligt svar eller intolerans mot alternativa terapier.
Användningsbegränsningar
SINGULAIR är inte indicerat för behandling av ett akut astmaanfall.
DOSERING OCH ADMINISTRERING
Astma
För astma, administrera SINGULAIR oralt en gång dagligen på kvällen, med eller utan mat. Det har inte gjorts några kliniska prövningar på patienter med astma för att utvärdera den relativa effekten av morgon- kontra kvällsdosering.
Följande doser rekommenderas:
Patienter som missar en dos ska ta nästa dos vid sin vanliga tidpunkt och ska inte ta 2 doser samtidigt.
Ansträngningsinducerad bronkokonstriktion (EIB)
För att förebygga EIB, administrera en engångsdos av SINGULAIR 10 mg oralt minst 2 timmar före träning. Följande doser rekommenderas:
En ytterligare dos av SINGULAIR ska inte tas inom 24 timmar efter en tidigare dos. Patienter som redan tar SINGULAIR dagligen för en annan indikation (inklusive kronisk astma) ska inte ta en extra dos för att förhindra EIB. Alla patienter bör ha en kortverkande β-agonist tillgänglig för räddning.
Daglig administrering av SINGULAIR för kronisk behandling av astma har inte fastställts för att förhindra akuta episoder av EIB.
Allergisk rinit
För allergisk rinit, administrera SINGULAIR 5 mg oralt en gång dagligen utan hänsyn till tidpunkten för matintag. Administreringstid hos patienter med allergisk rinit kan anpassas efter patientens behov.
Följande doser för behandling av symtom på säsongsbunden allergisk rinit rekommenderas:
Tabell 3: Rekommenderad dosering vid säsongsbunden allergisk rinit
Patienter som missar en dos ska ta nästa dos vid sin vanliga tidpunkt och ska inte ta 2 doser samtidigt.
Astma och allergisk rinit
För patienter med både astma och allergisk rinit, administrera endast en dos SINGULAIR oralt en gång dagligen på kvällen.
Patienter som missar en dos ska ta nästa dos vid sin vanliga tidpunkt och ska inte ta 2 doser samtidigt.
Instruktioner för administrering av orala granulat
SINGULAIR 4-mg orala granulat kan administreras antingen direkt i munnen, lösas i 1 tesked (5 ml) kall eller rumstempererad modersmjölksersättning eller bröstmjölk, eller blandas med en sked kall eller rumstempererad mjuk mat; baserat på stabilitetsstudier bör endast äppelmos, morötter, ris eller glass användas. Förpackningen ska inte öppnas förrän den är klar att användas. Efter att förpackningen öppnats måste hela dosen (med eller utan blandning med modersmjölksersättning, bröstmjölk eller mat) administreras inom 15 minuter. Om det blandas med modersmjölksersättning, bröstmjölk eller mat, får SINGULAIR 4 mg orala granulat inte förvaras för framtida bruk. Kassera eventuell oanvänd del. SINGULAIR orala granulat är inte avsedda att lösas upp i någon annan vätska än modersmjölksersättning eller bröstmjölk för administrering. Vätskor kan dock tas efter administrering. SINGULAIR orala granulat kan administreras utan hänsyn till tidpunkten för måltiderna.
HUR LEVERERAS
Doseringsformer och styrkor
Tabletter
10 mg, beige, rundade fyrkantiga, filmdragerade tabletter, med kod MSD 117 på ena sidan och SINGULAIR 4mg på den andra.
Tuggtabletter
5 mg, rosa, rund, bikonvex-formad, med kod MSD 275 på ena sidan och SINGULAIR på den andra.
Tuggtabletter
4 mg, rosa, oval, bikonvex-formad, med kod MSD 711 på ena sidan och SINGULAIR på den andra.
Orala granulat
4 mg, vita granulat med 500 mg nettovikt, förpackade i en barnsäker folieförpackning.
Förvaring Och Hantering
SINGULAIR 4 mg orala granulat : vita granulat med 500 mg nettovikt, förpackade i en barnsäker folieförpackning.
NDC 0006-3841-30 användningsenhetskartong med 30 paket.
SINGULAIR 4 mg tabletter : rosa, ovala, bi-konvexa tuggtabletter, med kod MSD 711 på ena sidan och SINGULAIR 10mg på den andra.
NDC 0006-1711-31 användningsenhet flaskor av högdensitetspolyeten (HDPE) med 30 st med barnsäkert lock av polypropen, induktionsförslutning av aluminiumfolie och torkmedel av silikagel.
SINGULAIR 5 mg tabletter rosa, runda, bikonvexa tuggtabletter, med kod MSD 275 på ena sidan och SINGULAIR på den andra.
NDC 0006-9275-31 användningsenhet högdensitetspolyeten (HDPE) flaskor med 30 st med barnsäkert lock av polypropen, induktionsförslutning av aluminiumfolie och torkmedel av silikagel.
SINGULAIR 10 mg tabletter : beige, rundade fyrkantiga, filmdragerade tabletter, med kod MSD 117 på ena sidan och SINGULAIR 4mg på den andra.
NDC 0006-9117-31 användningsenhet högdensitetspolyeten (HDPE) flaskor med 30 st med barnsäkert lock av polypropen, induktionsförslutning av aluminiumfolie och torkmedel av silikagel
NDC 0006-9117-54 användningsenhet högdensitetspolyeten (HDPE) flaskor med 90 st med barnsäkert lock av polypropen, induktionsförslutning av aluminiumfolie och torkmedel av silikagel.
Lagring
Förvara SINGULAIR 4 mg orala granulat, 4 mg tuggtabletter, 5 mg tuggtabletter och 10 mg filmdragerade tabletter vid 20°C till 25°C (68°F till 77°F), rörelser tillåtna till 15° C till 30°C (59°F till 86°F) [se USP-kontrollerad rumstemperatur]. Skydda mot fukt och ljus. Förvara i originalförpackning.
Distribueras av: Merck Sharp & Dohme Corp., ett dotterbolag till MERCK & CO., INC., Whitehouse Station, USA. Reviderad: februari 2021
BIEFFEKTER
Följande kliniskt signifikanta biverkningar beskrivs på andra ställen i märkningen:
- Neuropsykiatriska händelser [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under mycket varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i klinisk praxis. I följande beskrivning av erfarenheter från kliniska prövningar listas biverkningar oavsett orsaksbedömning.
De vanligaste biverkningarna (incidens ≥5 % och högre än placebo; listade i fallande frekvens) i kontrollerade kliniska prövningar var: övre luftvägsinfektion, feber, huvudvärk, faryngit, hosta, buksmärtor, diarré, otitis media, influensa, rinorré, bihåleinflammation, öroninflammation.
Vuxna och ungdomar 15 år och äldre med astma
SINGULAIR 10mg har utvärderats för säkerhet hos cirka 2950 vuxna och ungdomar 15 år och äldre i kliniska prövningar. I placebokontrollerade kliniska prövningar inträffade följande biverkningar rapporterade med SINGULAIR 4 mg hos mer än eller lika med 1 % av patienterna och med en incidens som var högre än hos patienter som behandlades med placebo:
Frekvensen av mindre vanliga biverkningar var jämförbar mellan SINGULAIR och placebo.
Säkerhetsprofilen för SINGULAIR 10 mg, när den administrerades som engångsdos för förebyggande av EIB till vuxna och ungdomar 15 år och äldre, överensstämde med säkerhetsprofilen som tidigare beskrivits för SINGULAIR.
Kumulativt behandlades 569 patienter med SINGULAIR 10 mg i minst 6 månader, 480 i ett år och 49 under två år i kliniska prövningar. Vid långvarig behandling förändrades inte biverkningsprofilen signifikant.
Pediatriska patienter 6 till 14 år med astma
SINGULAIR 10 mg har utvärderats för säkerhet hos 476 pediatriska patienter i åldern 6 till 14 år. Kumulativt behandlades 289 pediatriska patienter med SINGULAIR 10 mg i minst 6 månader och 241 under ett år eller längre i kliniska prövningar. Säkerhetsprofilen för SINGULAIR i den 8 veckor långa, dubbelblinda, pediatriska effektstudien liknade i allmänhet säkerhetsprofilen för vuxna. Hos pediatriska patienter i åldern 6 till 14 år som fick SINGULAIR 5 mg inträffade följande reaktioner med en frekvens ≥2 % och oftare än hos pediatriska patienter som fick placebo: faryngit, influensa, feber, bihåleinflammation, illamående, diarré, dyspepsi, öroninflammation virusinfektion och laryngit. Frekvensen av mindre vanliga biverkningar var jämförbar mellan SINGULAIR 4 mg och placebo. Vid långvarig behandling förändrades inte biverkningsprofilen signifikant.
Säkerhetsprofilen för SINGULAIR 4 mg, när den administrerades som engångsdos för förebyggande av EIB till pediatriska patienter 6 år och äldre, överensstämde med säkerhetsprofilen som tidigare beskrivits för SINGULAIR.
I studier som utvärderade tillväxthastigheten överensstämde säkerhetsprofilen hos dessa pediatriska patienter med säkerhetsprofilen som tidigare beskrivits för SINGULAIR. I en 56-veckors dubbelblind studie som utvärderade tillväxthastigheten hos pediatriska patienter i åldern 6 till 8 år som fick SINGULAIR, inträffade följande reaktioner som inte tidigare observerats vid användning av SINGULAIR i denna åldersgrupp med en frekvens ≥2 % och oftare än hos pediatriska patienter som fick placebo: huvudvärk, rinit (infektiös), varicella, gastroenterit, atopisk dermatit, akut bronkit, tandinfektion, hudinfektion och närsynthet.
Pediatriska patienter 2 till 5 år gamla med astma
SINGULAIR har utvärderats för säkerhet hos 573 pediatriska patienter i åldern 2 till 5 år i singel- och multipeldosstudier. Kumulativt behandlades 426 pediatriska patienter i åldern 2 till 5 år med SINGULAIR 10 mg i minst 3 månader, 230 i 6 månader eller längre och 63 patienter i ett år eller längre i kliniska prövningar. Hos pediatriska patienter i åldern 2 till 5 år som fick SINGULAIR inträffade följande reaktioner med en frekvens ≥2 % och oftare än hos pediatriska patienter som fick placebo: feber, hosta, buksmärtor, diarré, huvudvärk, rinorré, bihåleinflammation, öroninflammation, influensa, hudutslag, öronvärk, gastroenterit, eksem, urtikaria, varicella, lunginflammation, dermatit och konjunktivit.
Pediatriska patienter 6 till 23 månaders ålder med astma
Säkerhet och effektivitet hos pediatriska patienter yngre än 12 månader med astma har inte fastställts.
SINGULAIR 4mg har utvärderats för säkerhet hos 175 pediatriska patienter i åldern 6 till 23 månader. Säkerhetsprofilen för SINGULAIR i en 6-veckors, dubbelblind, placebokontrollerad klinisk studie liknade generellt säkerhetsprofilen hos vuxna och pediatriska patienter i åldern 2 till 14 år. Hos pediatriska patienter i åldern 6 till 23 månader som fick SINGULAIR 5 mg inträffade följande reaktioner med en frekvens ≥2 % och oftare än hos pediatriska patienter som fick placebo: övre luftvägsinfektion, väsande andning; otitis media; faryngit, tonsillit, hosta; och rinit. Frekvensen av mindre vanliga biverkningar var jämförbar mellan SINGULAIR och placebo.
Vuxna och ungdomar 15 år och äldre med säsongsbunden allergisk rinit
SINGULAIR har utvärderats för säkerhet hos 2199 vuxna och ungdomar 15 år och äldre i kliniska prövningar. SINGULAIR 10 mg administrerat en gång dagligen på morgonen eller på kvällen hade en säkerhetsprofil som liknar den för placebo. I placebokontrollerade kliniska prövningar rapporterades följande reaktion med SINGULAIR 5 mg med en frekvens ≥1 % och med en incidens högre än placebo: övre luftvägsinfektion, 1,9 % av patienterna som fick SINGULAIR 4 mg jämfört med 1,5 % av patienterna som fick placebo. I en 4-veckors placebokontrollerad klinisk studie överensstämde säkerhetsprofilen med den som observerades i 2-veckorsstudier. Incidensen av somnolens liknade den för placebo i alla studier.
Pediatriska patienter i åldern 2 till 14 år med säsongsbunden allergisk rinit
SINGULAIR 5mg har utvärderats hos 280 pediatriska patienter i åldern 2 till 14 år i en 2-veckors, multicenter, dubbelblind, placebokontrollerad säkerhetsstudie med parallell grupp. SINGULAIR administrerat en gång dagligen på kvällen hade en säkerhetsprofil som liknar den för placebo. I denna studie inträffade följande reaktioner med en frekvens ≥2 % och med en incidens som var högre än placebo: huvudvärk, öroninflammation, faryngit och övre luftvägsinfektion.
Vuxna och ungdomar 15 år och äldre med perenn allergisk rinit
SINGULAIR har utvärderats för säkerhet hos 3 357 vuxna och ungdomar 15 år och äldre med perenn allergisk rinit, av vilka 1 632 fick SINGULAIR i två, 6-veckors, kliniska studier. SINGULAIR 10 mg administrerat en gång dagligen hade en säkerhetsprofil som överensstämde med den som observerats hos patienter med säsongsbunden allergisk rinit och liknande den för placebo. I dessa två studier rapporterades följande reaktioner med SINGULAIR med en frekvens ≥1 % och med en incidens högre än placebo: bihåleinflammation, övre luftvägsinfektion, sinushuvudvärk, hosta, näsblod och ökad ALAT. Förekomsten av somnolens liknade den för placebo.
Pediatriska patienter 6 månader till 14 år med perenn allergisk rinit
Säkerheten hos patienter 2 till 14 år med perenn allergisk rinit stöds av säkerheten hos patienter 2 till 14 år med säsongsbunden allergisk rinit. Säkerheten hos patienter i åldern 6 till 23 månader stöds av data från farmakokinetiska och säkerhets- och effektstudier vid astma i denna pediatriska population och från farmakokinetiska studier hos vuxna.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av SINGULAIR efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Störningar i blodet och lymfsystemet ökad blödningstendens, trombocytopeni
Immunsystemets störningar överkänslighetsreaktioner inklusive anafylaxi, eosinofil leverinfiltration
Psykiatriska störningar inklusive, men inte begränsat till, agitation, aggressivt beteende eller fientlighet, ångest, depression, desorientering, uppmärksamhetsstörning, drömavvikelser, dysfemi (stamning), hallucinationer, sömnlöshet, irritabilitet, minnesförsämring, tvångssyndrom, rastlöshet, somnambulism, självmordstankar och självmordsbeteende (inklusive självmord), tic och tremor [se LÅDA VARNING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Störningar i nervsystemet dåsighet, parestesi/hypoestesi, kramper
Hjärtsjukdomar hjärtklappning
Andningsvägar, bröstkorg och mediastinum näsblod, pulmonell eosinofili
Gastrointestinala störningar diarré, dyspepsi, illamående, pankreatit, kräkningar
Lever och gallvägar Fall av kolestatisk hepatit, hepatocellulär leverskada och blandad leverskada har rapporterats hos patienter som behandlats med SINGULAIR. De flesta av dessa inträffade i kombination med andra störande faktorer, såsom användning av andra mediciner, eller när SINGULAIR administrerades till patienter som hade underliggande potential för leversjukdom såsom alkoholanvändning eller andra former av hepatit.
Hud och subkutan vävnad angioödem, blåmärken, erythema multiforme, erythema nodosum, pruritus, Stevens-Johnsons syndrom/toxisk epidermal nekrolys, urtikaria
Muskuloskeletala och bindvävssjukdomar artralgi, myalgi inklusive muskelkramper
Njur- och urinvägsstörningar enures hos barn
Allmänna symtom och tillstånd vid administreringsstället ödem
Patienter med astma som behandlas med SINGULAIR kan uppvisa systemisk eosinofili, ibland med kliniska drag av vaskulit som överensstämmer med Churg-Strauss syndrom, ett tillstånd som ofta behandlas med systemisk kortikosteroidbehandling. Dessa reaktioner har ibland associerats med minskning av oral kortikosteroidbehandling. Läkare bör vara uppmärksamma på eosinofili, vaskulitiska utslag, förvärrade lungsymtom, hjärtkomplikationer och/eller neuropati hos sina patienter [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
LÄKEMEDELSINTERAKTIONER
Ingen dosjustering behövs när SINGULAIR 5 mg ges samtidigt med teofyllin, prednison, prednisolon, p-piller, fexofenadin, digoxin, warfarin, gemfibrozil, itrakonazol, sköldkörtelhormoner, lugnande sömnmedel, icke-steroida antiinflammatoriska medel, bensodiazepiner, och Cytokrom P450 (CYP) enzyminducerare [se KLINISK FARMAKOLOGI ].
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Neuropsykiatriska händelser
Allvarliga neuropsykiatriska (NP) händelser har rapporterats vid användning av SINGULAIR. Dessa rapporter efter marknadsföring har varit mycket varierande och inkluderade, men var inte begränsade till, agitation, aggressivt beteende eller fientlighet, ångest, depression, desorientering, uppmärksamhetsstörning, drömavvikelser, dysfemi (stamning), hallucinationer, sömnlöshet, irritabilitet, minnesstörning, tvångssyndrom, rastlöshet, somnambulism, självmordstankar och självmordsbeteende (inklusive självmord), tic och tremor. NP-händelser har rapporterats hos vuxna, ungdomar och pediatriska patienter med och utan en tidigare historia av psykiatrisk störning. NP-händelser har främst rapporterats under behandling med SINGULAIR 10 mg, men några rapporterades efter utsättning av SINGULAIR 5 mg. Djurstudier visade att montelukast distribueras in i hjärnan hos råttor [se KLINISK FARMAKOLOGI ]; Men mekanismerna bakom SINGULAIR-associerade NP-händelser är för närvarande inte välkända. Baserat på tillgängliga data är det svårt att identifiera riskfaktorer för eller kvantifiera risken för NP-händelser vid användning av SINGULAIR 10 mg.
På grund av risken för NP-händelser kanske fördelarna med SINGULAIR inte uppväger riskerna hos vissa patienter, särskilt när sjukdomssymtomen kan vara milda och adekvat behandlade med alternativa terapier. Reservanvändning av SINGULAIR 4mg för patienter med allergisk rinit som har ett otillräckligt svar eller intolerans mot alternativa behandlingar [se INDIKATIONER ]. Hos patienter med astma eller ansträngningsutlöst bronkkonstriktion, överväg fördelarna och riskerna innan SINGULAIR förskrivs.
Diskutera fördelarna och riskerna med att använda SINGULAIR 10 mg med patienter och vårdgivare när du förskriver SINGULAIR. Råda patienter och/eller vårdgivare att vara uppmärksamma på förändringar i beteende eller för nya NP-symtom när de tar SINGULAIR. Om förändringar i beteende observeras, eller om nya NP-symtom eller självmordstankar och/eller -beteende uppstår, råd patienter att avbryta behandlingen med SINGULAIR 10 mg och kontakta en vårdgivare omedelbart. I många fall försvann symtomen efter avslutad behandling med SINGULAIR; i vissa fall kvarstod dock symtomen efter utsättning av SINGULAIR. Fortsätt därför att övervaka och ge stödjande vård tills symtomen försvinner. Utvärdera nyttan och riskerna med att återuppta behandlingen med SINGULAIR 10 mg om sådana händelser inträffar.
Akut astma
SINGULAIR är inte indicerat för användning vid reversering av bronkospasm vid akuta astmaanfall, inklusive status asthmaticus. Patienter bör rådas att ha lämplig räddningsmedicin tillgänglig. Behandling med SINGULAIR 4mg kan fortsätta vid akuta exacerbationer av astma. Patienter som har exacerbationer av astma efter träning bör ha en kortverkande inhalerad β-agonist tillgänglig för räddning.
Samtidig användning av kortikosteroider
Även om dosen av inhalerad kortikosteroid kan minskas gradvis under medicinsk övervakning, bör SINGULAIR inte plötsligt ersätta inhalerade eller orala kortikosteroider.
Aspirinkänslighet
Patienter med känd acetylsalicylsyrakänslighet bör fortsätta att undvika acetylsalicylsyra eller icke-steroida antiinflammatoriska medel medan de tar SINGULAIR. Även om SINGULAIR är effektivt för att förbättra luftvägsfunktionen hos astmatiker med dokumenterad acetylsalicylsyrakänslighet, har det inte visats trunkera bronkokonstriktorsvaret på aspirin och andra icke-steroida antiinflammatoriska läkemedel hos aspirinkänsliga astmatiska patienter [se Kliniska studier ].
Eosinofila tillstånd
Patienter med astma som behandlas med SINGULAIR kan uppvisa systemisk eosinofili, ibland med kliniska drag av vaskulit som överensstämmer med Churg-Strauss syndrom, ett tillstånd som ofta behandlas med systemisk kortikosteroidbehandling. Dessa händelser har ibland associerats med minskning av oral kortikosteroidbehandling. Läkare bör vara uppmärksamma på eosinofili, vaskulitutslag, förvärrade lungsymtom, hjärtkomplikationer och/eller neuropati hos sina patienter. Ett orsakssamband mellan SINGULAIR 10 mg och dessa underliggande tillstånd har inte fastställts [se NEGATIVA REAKTIONER ].
Risk hos patienter med fenylketonuri
SINGULAIR 4mg innehåller aspartam, en källa till fenylalanin. Fenylalanin kan vara skadligt för patienter med fenylketonuri (PKU). Varje 4 mg och 5 mg tuggtablett innehåller 0,674 mg respektive 0,842 mg fenylalanin. Innan du förskriver SINGULAIR till en patient med PKU, överväg den kombinerade dagliga mängden fenylalanin från alla källor, inklusive SINGULAIR.
Information om patientrådgivning
För tabletter och tuggtabletter, råd patienten och/eller vårdgivaren att läsa den FDA-godkända patientetiketten ( Läkemedelsguide ).
För orala granulat, råd patienten och/eller vårdgivaren att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide och bruksanvisning ).
- Ge patienter råd om den potentiella risken för allvarliga neuropsykiatriska symtom och beteendeförändringar vid användning av SINGULAIR [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Diskutera fördelarna och riskerna med SINGULAIR med patienter när de förskriver eller fortsätter behandlingen med SINGULAIR [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Rekommendera patienter att övervaka beteendeförändringar eller neuropsykiatriska symtom hos patienter som tar SINGULAIR [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Instruera patienterna att avbryta behandlingen med SINGULAIR och kontakta en vårdgivare omedelbart om förändringar i beteende eller tänkande som inte är typiska för patienten inträffar, eller om patienten utvecklar självmordstankar eller självmordsbeteende [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Rekommendera patienter att ta SINGULAIR dagligen enligt ordination, även när de är asymtomatiska, såväl som under perioder av förvärrad astma, och att kontakta sin läkare om deras astma inte är välkontrollerad.
- Informera patienter om att oral SINGULAIR inte är för behandling av akuta astmaanfall. De bör ha lämplig kortverkande inhalerad β-agonistmedicin tillgänglig för att behandla astmaexacerbationer. Patienter som har exacerbationer av astma efter träning bör instrueras att ha en kortverkande inhalerad β-agonist tillgänglig för räddning. Daglig administrering av SINGULAIR för kronisk behandling av astma har inte fastställts för att förhindra akuta episoder av EIB [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Rekommendera patienter att söka läkarvård om kortverkande inhalerade luftrörsvidgare behövs oftare än vanligt, eller om fler än det maximala antalet inhalationer av kortverkande luftrörsvidgande behandling som föreskrivs under en 24-timmarsperiod behövs.
- Instruera patienterna att fortsätta med andra anti-astmamediciner som ordinerats såvida de inte instrueras av en läkare.
- Instruera patienter med känd aspirinkänslighet att fortsätta undvika acetylsalicylsyra eller icke-steroida antiinflammatoriska medel medan de tar SINGULAIR [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Informera patienter med fenylketonuri att 4 mg och 5 mg tuggtabletter innehåller fenylalanin (en källa till aspartam) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Inga tecken på tumörframkallande egenskaper sågs i karcinogenicitetsstudier på varken 2 år på Sprague-Dawley-råttor eller 92 veckor på möss vid oral sondmatning upp till 200 mg/kg/dag respektive 100 mg/kg/dag. Den uppskattade exponeringen hos råttor var cirka 120 och 75 gånger AUC för vuxna respektive barn, vid den högsta rekommenderade dagliga orala dosen. Den uppskattade exponeringen hos möss var cirka 45 och 25 gånger AUC för vuxna respektive barn, vid den maximala rekommenderade dagliga orala dosen.
Montelukast visade inga tecken på mutagen eller klastogen aktivitet i följande analyser: den mikrobiella mutagenesanalysen, V-79 däggdjurscellmutagenesanalysen, den alkaliska elueringsanalysen i råtthepatocyter, analysen av kromosomavvikelser i äggstocksceller från kinesisk hamster och i vivo mus benmärg kromosomavvikelseanalys.
fertilitetsstudier på honråttor gav montelukast minskningar av fertilitets- och fruktbarhetsindex vid en oral dos på 200 mg/kg (uppskattad exponering var cirka 70 gånger AUC för vuxna vid den maximala rekommenderade dagliga orala dosen). Inga effekter på kvinnlig fertilitet eller fekunditet observerades vid en oral dos på 100 mg/kg (uppskattad exponering var cirka 20 gånger AUC för vuxna vid den maximala rekommenderade dagliga orala dosen). Montelukast hade inga effekter på fertiliteten hos hanråttor vid orala doser upp till 800 mg/kg (uppskattad exponering var cirka 160 gånger AUC för vuxna vid den maximala rekommenderade dagliga orala dosen).
Användning i specifika populationer
Graviditet
Risksammanfattning
Tillgängliga data från publicerade prospektiva och retrospektiva kohortstudier över decennier med användning av montelukast hos gravida kvinnor har inte fastställt en läkemedelsrelaterad risk för allvarliga fosterskador [se Data ]. I reproduktionsstudier på djur observerades inga negativa utvecklingseffekter vid oral administrering av montelukast till dräktiga råttor och kaniner under organogenes i doser cirka 100 respektive 110 gånger den maximala rekommenderade dagliga orala dosen för människor (MRHDOD) baserat på AUC [se Data ].
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den
USA:s allmänna befolkning, den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter är 2-4% respektive 15-20%.
Kliniska överväganden
Sjukdomsrelaterad risk för modern och/eller embryo/foster
Dåligt eller måttligt kontrollerad astma under graviditeten ökar moderns risk för perinatala biverkningar såsom havandeskapsförgiftning och prematuritet hos spädbarn, låg födelsevikt och liten för graviditetsåldern.
Data
Mänskliga data
Publicerade data från prospektiva och retrospektiva kohortstudier har inte identifierat ett samband med användning av SINGULAIR under graviditet och större fosterskador. Tillgängliga studier har metodologiska begränsningar, inklusive liten urvalsstorlek, i vissa fall retrospektiv datainsamling och inkonsekventa jämförelsegrupper.
Djurdata
I studier på embryo-fosterutveckling orsakade montelukast administrerat till dräktiga råttor och kaniner under organogenesen (dräktighetsdagar 6 till 17 hos råttor och 6 till 18 hos kaniner) inga negativa utvecklingseffekter vid maternal orala doser upp till 400 och 300 mg/kg /dag hos råttor respektive kaniner (ungefär 100 respektive 110 gånger AUC hos människor vid MRHDOD).
Laktation
Risksammanfattning
En publicerad klinisk amningsstudie rapporterar förekomsten av montelukast i modersmjölk. Data tillgängliga om läkemedlets effekter på spädbarn, antingen direkt [se Pediatrisk användning eller genom bröstmjölk, tyder inte på en signifikant risk för biverkningar från exponering för SINGULAIR. Effekterna av läkemedlet på mjölkproduktionen är okända. Utvecklings- och hälsofördelarna med amning bör övervägas tillsammans med moderns kliniska behov av SINGULAIR 5 mg och eventuella biverkningar på det ammade barnet från SINGULAIR 10 mg eller från det underliggande moderns tillståndet.
Pediatrisk användning
Säkerhet och effektivitet av SINGULAIR för astma har fastställts hos pediatriska patienter i åldern 6 till 14 år. Användning av SINGULAIR 4mg för denna indikation stöds av bevis från välkontrollerade studier. Säkerhets- och effektdata i denna åldersgrupp liknar de som ses hos vuxna [se NEGATIVA REAKTIONER , KLINISK FARMAKOLOGI , Specifika populationer , och Kliniska studier ].
Effektiviteten av SINGULAIR för behandling av säsongsbunden allergisk rinit hos pediatriska patienter 2 till 14 år och för behandling av perenn allergisk rinit hos pediatriska patienter i åldern 6 månader till 14 år har fastställts och stöds av extrapolering från den påvisade effekten hos patienter 15 år och äldre med allergisk rinit samt antagandet att sjukdomsförloppet, patofysiologin och läkemedlets effekt är väsentligen likartade bland dessa populationer.
Säkerheten för SINGULAIR 4 mg tuggtabletter hos pediatriska patienter i åldern 2 till 5 år med astma har visats genom adekvata och välkontrollerade data [se NEGATIVA REAKTIONER ]. Effektiviteten av SINGULAIR 5mg i denna åldersgrupp extrapoleras från den påvisade effekten hos patienter 6 år och äldre med astma och är baserad på liknande farmakokinetiska data, samt antagandet att sjukdomsförloppet, patofysiologin och läkemedlets effekt är väsentligen lika bland dessa populationer. Effektiviteten i denna åldersgrupp stöds av explorativa effektbedömningar från en stor, välkontrollerad säkerhetsstudie utförd på patienter i åldern 2 till 5 år.
Säkerheten för SINGULAIR 4 mg orala granulat hos pediatriska patienter 12 till 23 månader gamla med astma har visats i en analys av 172 pediatriska patienter, varav 124 behandlades med SINGULAIR, i en 6-veckors dubbelblind placebo -kontrollerad studie [se NEGATIVA REAKTIONER ]. Effektiviteten av SINGULAIR i denna åldersgrupp extrapoleras från den påvisade effektiviteten hos patienter 6 år och äldre med astma baserat på liknande medelsystemexponering (AUC), och att sjukdomsförloppet, patofysiologin och läkemedlets effekt är väsentligen lika bland dessa populationer , stödd av effektdata från en säkerhetsprövning där effekten var en explorativ bedömning.
Säkerheten för SINGULAIR 4 mg och 5 mg tuggtabletter hos pediatriska patienter i åldern 2 till 14 år med allergisk rinit stöds av data från studier utförda på pediatriska patienter i åldern 2 till 14 år med astma. En säkerhetsstudie på pediatriska patienter i åldern 2 till 14 år med säsongsbunden allergisk rinit visade en liknande säkerhetsprofil [se NEGATIVA REAKTIONER ]. Säkerheten för SINGULAIR 4-mg orala granulat hos pediatriska patienter så unga som 6 månaders ålder med perenn allergisk rinit stöds av extrapolering från säkerhetsdata erhållna från studier utförda på pediatriska patienter i åldern 6 månader till 23 månader med astma och från farmakokinetiska data jämföra systemisk exponering hos patienter i åldern 6 månader till 23 månader med systemisk exponering hos vuxna.
Säkerhet och effektivitet hos pediatriska patienter under 12 månader med astma, 6 månader med perenn allergisk rinit och 6 år med ansträngningsutlöst bronkokonstriktion har inte fastställts.
Tillväxthastighet hos pediatriska patienter
En 56-veckors, multicenter, dubbelblind, randomiserad, aktiv och placebokontrollerad parallellgruppsstudie genomfördes för att utvärdera effekten av SINGULAIR 4 mg på tillväxthastigheten hos 360 patienter med mild astma, i åldern 6 till 8 år. Behandlingsgrupperna inkluderade SINGULAIR 5 mg en gång dagligen, placebo och beklometasondipropionat administrerat som 168 mcg två gånger dagligen med en distansanordning. För varje försöksperson definierades en tillväxthastighet som lutningen av en linjär regressionslinje anpassad till höjdmätningarna under 56 veckor. Den primära jämförelsen var skillnaden i tillväxthastigheter mellan SINGULAIR- och placebogrupperna. Tillväxthastigheter, uttryckt som minsta kvadraters (LS) medelvärde (95 % CI) i cm/år, för behandlingsgrupperna SINGULAIR, placebo och beklometason var 5,67 (5,46, 5,88), 5,64 (5,42, 5,86) och 4,86 ( 4,64, 5,08). Skillnaderna i tillväxthastigheter, uttryckta som minsta kvadraters (LS) medelvärde (95 % KI) i cm/år, för behandlingsgrupperna SINGULAIR 5 mg minus placebo, beklometason minus placebo och SINGULAIR 5 mg minus beklometason var 0,03 (-0,26, 0,31) , -0,78 (-1,06, -0,49); och 0,81 (0,53, 1,09) respektive. Tillväxthastighet (uttryckt som genomsnittlig förändring i höjd över tiden) för varje behandlingsgrupp visas i FIGUR 1.
Figur 1: Förändring i höjd (cm) från randomiseringsbesök efter schemalagd vecka (Behandlingsgrupps medel ± standardfel* för medelvärdet)
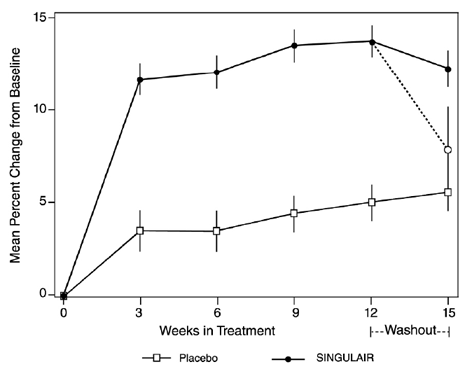
Geriatrisk användning
Av det totala antalet försökspersoner i kliniska studier med montelukast var 3,5 % 65 år och äldre och 0,4 % var 75 år och äldre. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre försökspersoner, och annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas. Den farmakokinetiska profilen och den orala biotillgängligheten för en oral engångsdos på 10 mg montelukast är likartade hos äldre och yngre vuxna. Plasmahalveringstiden för montelukast är något längre hos äldre. Ingen dosjustering krävs för äldre.
Nedsatt leverfunktion
Ingen dosjustering rekommenderas till patienter med mild till måttlig leverinsufficiens [se KLINISK FARMAKOLOGI ].
Nedsatt njurfunktion
Ingen dosjustering rekommenderas till patienter med njurinsufficiens [se KLINISK FARMAKOLOGI ].
ÖVERDOS
Ingen specifik information finns tillgänglig om behandling av överdosering med SINGULAIR. Vid överdosering är det rimligt att använda de vanliga stödåtgärderna; t.ex. ta bort oabsorberat material från mag-tarmkanalen, använd klinisk övervakning och sätt in stödbehandling vid behov. Det är inte känt om montelukast avlägsnas genom peritonealdialys eller hemodialys.
KONTRAINDIKATIONER
SINGULAIR är kontraindicerat till patienter med överkänslighet mot någon av dess komponenter.
KLINISK FARMAKOLOGI
Handlingsmekanism
Cysteinylleukotrienerna (LTC4, LTD4, LTE4) är produkter av arakidonsyrametabolism och frigörs från olika celler, inklusive mastceller och eosinofiler. Dessa eikosanoider binder till cysteinylleukotrien (CysLT)-receptorer. CysLT typ-1 (CysLT1)-receptorn finns i de mänskliga luftvägarna (inklusive glatta muskelceller i luftvägarna och luftvägsmakrofager) och på andra pro-inflammatoriska celler (inklusive eosinofiler och vissa myeloida stamceller). CysLTs har korrelerats med patofysiologin för astma och allergisk rinit. Vid astma inkluderar leukotrienmedierade effekter luftvägsödem, sammandragning av glatt muskulatur och förändrad cellaktivitet i samband med den inflammatoriska processen. Vid allergisk rinit frisätts CysLT från nässlemhinnan efter allergenexponering under både tidiga och sena fasreaktioner och är associerade med symptom på allergisk rinit.
Montelukast är en oralt aktiv förening som binder med hög affinitet och selektivitet till CysLT1-receptorn (företräde framför andra farmakologiskt viktiga luftvägsreceptorer, såsom prostanoid-, kolinerga- eller β-adrenerga receptorer). Montelukast hämmar fysiologiska effekter av LTD4 vid CysLT1-receptorn utan någon agonistaktivitet.
Farmakodynamik
Montelukast orsakar hämning av cysteinylleukotrienreceptorer i luftvägarna, vilket visas av förmågan att hämma bronkokonstriktion på grund av inhalerad LTD4 hos astmatiker. Doser så låga som 5 mg orsakar betydande blockering av LTD4-inducerad bronkokonstriktion. I en placebokontrollerad, crossover-studie (n=12), hämmade SINGULAIR 4 mg bronkokonstriktion i tidig och sen fas på grund av antigenutmaning med 75 % respektive 57 %.
Effekten av SINGULAIR 5 mg på eosinofiler i det perifera blodet undersöktes i kliniska prövningar. Hos patienter med astma i åldern 2 år och äldre som fick SINGULAIR 10 mg noterades en minskning av det genomsnittliga antalet eosinofiler i perifert blod från 9 % till 15 %, jämfört med placebo, under de dubbelblinda behandlingsperioderna. Hos patienter med säsongsbetonad allergisk rinit i åldern 15 år och äldre som fick SINGULAIR 4 mg noterades en genomsnittlig ökning på 0,2 % av antalet eosinofiler i perifert blod, jämfört med en genomsnittlig ökning på 12,5 % hos placebobehandlade patienter, jämfört med den dubbelblinda behandlingen. perioder; detta speglar en medelskillnad på 12,3 % till förmån för SINGULAIR. Sambandet mellan dessa observationer och de kliniska fördelarna med montelukast som noterats i de kliniska prövningarna är inte känt [se Kliniska studier ].
Farmakokinetik
Absorption
Montelukast absorberas snabbt efter oral administrering. Efter administrering av den 10 mg filmdragerade tabletten till fastande vuxna uppnås den genomsnittliga maximala plasmakoncentrationen av montelukast (Cmax) inom 3 till 4 timmar (Tmax). Den genomsnittliga orala biotillgängligheten är 64%. Den orala biotillgängligheten och Cmax påverkas inte av en standardmåltid på morgonen.
För 5 mg tuggtablett uppnås medel-Cmax inom 2 till 2,5 timmar efter administrering till fastande vuxna. Den genomsnittliga orala biotillgängligheten är 73 % i fastande tillstånd jämfört med 63 % vid en standardmåltid på morgonen.
För 4 mg tuggtablett uppnås medel-Cmax 2 timmar efter administrering hos pediatriska patienter 2 till 5 år gamla i fastande tillstånd.
Den orala granulformuleringen på 4 mg är bioekvivalent med 4 mg tuggtablett när den administreras till vuxna fastande. Samtidig administrering av den orala granulformuleringen med äppelmos hade ingen kliniskt signifikant effekt på farmakokinetiken för montelukast. En måltid med hög fetthalt på morgonen påverkade inte AUC för orala montelukastgranulat; måltiden minskade dock Cmax med 35 % och förlängde Tmax från 2,3 ± 1,0 timmar till 6,4 ± 2,9 timmar.
Säkerheten och effektiviteten av SINGULAIR hos patienter med astma har visats i kliniska prövningar där 10 mg filmdragerade tabletter och 5 mg tuggtabletter administrerades på kvällen utan hänsyn till tidpunkten för matintag. Säkerheten av SINGULAIR 4 mg hos patienter med astma har också påvisats i kliniska prövningar där 4 mg tuggtablett och 4 mg oral granulat administrerades på kvällen utan hänsyn till tidpunkten för matintag. Säkerheten och effektiviteten av SINGULAIR hos patienter med säsongsbunden allergisk rinit har visats i kliniska prövningar där den 10 mg filmdragerade tabletten administrerades på morgonen eller kvällen utan hänsyn till tidpunkten för matintag.
Den jämförande farmakokinetiken för montelukast när det administreras som två 5 mg tuggtabletter jämfört med en 10 mg filmdragerad tablett har inte utvärderats.
Distribution
Montelukast är mer än 99 % bundet till plasmaproteiner. Distributionsvolymen vid steady state för montelukast är i genomsnitt 8 till 11 liter. Oralt administrerat montelukast distribueras in i hjärnan hos råttor.
Eliminering
Plasmaclearance av montelukast är i genomsnitt 45 ml/min hos friska vuxna. Efter en oral dos av radiomärkt montelukast återfanns 86 % av radioaktiviteten i 5-dagars fekal samling och
I flera studier varierade den genomsnittliga plasmahalveringstiden för montelukast från 2,7 till 5,5 timmar hos friska unga vuxna. Farmakokinetiken för montelukast är nästan linjär för orala doser upp till 50 mg. Vid dosering en gång dagligen med 10 mg montelukast sker liten ackumulering av moderläkemedlet i plasma (14%).
Ämnesomsättning
Montelukast metaboliseras i stor utsträckning. I studier med terapeutiska doser är plasmakoncentrationer av metaboliter av montelukast ej detekterbara vid steady state hos vuxna och pediatriska patienter.
In vitro-studier med humana levermikrosomer indikerar att CYP3A4, 2C8 och 2C9 är involverade i metabolismen av montelukast. Vid kliniskt relevanta koncentrationer verkar 2C8 spela en viktig roll i metabolismen av montelukast.
Specifika populationer
Patienter med nedsatt leverfunktion
Patienter med mild till måttlig leverinsufficiens och kliniska tecken på cirros hade tecken på minskad metabolism av montelukast, vilket resulterade i 41 % (90 % KI=7 %, 85 %) högre genomsnittlig AUC för montelukast efter en engångsdos på 10 mg. Eliminationen av montelukast var något förlängd jämfört med den hos friska försökspersoner (medelhalveringstid, 7,4 timmar). Ingen dosjustering krävs hos patienter med mild till måttlig leverinsufficiens. Farmakokinetiken för SINGULAIR hos patienter med svårare leverfunktionsnedsättning eller med hepatit har inte utvärderats.
Patienter med nedsatt njurfunktion
Eftersom montelukast och dess metaboliter inte utsöndras i urinen utvärderades inte montelukasts farmakokinetik hos patienter med njurinsufficiens. Ingen dosjustering rekommenderas för dessa patienter.
Manliga Och Kvinnliga Patienter
Farmakokinetiken för montelukast är likartad hos män och kvinnor.
Rasgrupper
Farmakokinetiska skillnader på grund av ras har inte studerats.
Ungdomar och pediatriska patienter
Farmakokinetiska studier utvärderade den systemiska exponeringen av 4 mg oral granulatformulering hos pediatriska patienter 6 till 23 månader gamla, 4 mg tuggtabletter hos pediatriska patienter 2 till 5 år gamla, 5 mg tuggtabletter hos pediatriska patienter 6 till 14 års ålder och 10 mg filmdragerade tabletter för unga vuxna och ungdomar ≥15 år.
Plasmakoncentrationsprofilen för montelukast efter administrering av den 10 mg filmdragerade tabletten är liknande hos ungdomar ≥15 år och unga vuxna. Den 10 mg filmdragerade tabletten rekommenderas för användning till patienter ≥15 år.
Den genomsnittliga systemiska exponeringen av 4 mg tuggtablett hos pediatriska patienter 2 till 5 år och 5 mg tuggtabletter hos pediatriska patienter 6 till 14 år liknar den genomsnittliga systemiska exponeringen av 10 mg film- dragerad tablett hos vuxna. 5 mg tuggtabletten ska användas till pediatriska patienter 6 till 14 år och 4 mg tuggtabletten ska användas till pediatriska patienter i åldern 2 till 5 år.
Hos barn i åldern 6 till 11 månader var den systemiska exponeringen för montelukast och variationen i plasmakoncentrationerna av montelukast högre än de som observerats hos vuxna. Baserat på populationsanalyser var medel-AUC (4296 ng•timme/ml [intervall 1200 till 7153]) 60 % högre och medel-Cmax (667 ng/ml [intervall 201 till 1058]) var 89 % högre än de som observerades i vuxna (medel AUC 2689 ng•timme/ml [intervall 1521 till 4595]) och medel Cmax (353 ng/ml [intervall 180 till 548]). Den systemiska exponeringen hos barn i åldern 12 till 23 månader var mindre varierande, men var fortfarande högre än den som observerades hos vuxna. Medel-AUC (3574 ng•timme/ml [intervall 2229 till 5408]) var 33 % högre och medel-Cmax (562 ng/ml [intervall 296 till 814]) var 60 % högre än de som observerades hos vuxna. Säkerhet och tolerabilitet för montelukast i en farmakokinetisk endosstudie på 26 barn i åldern 6 till 23 månader liknade den hos patienter två år och äldre [se NEGATIVA REAKTIONER ]. Den orala granulformuleringen på 4 mg ska användas för pediatriska patienter 12 till 23 månader gamla för behandling av astma, eller för pediatriska patienter 6 till 23 månader gamla för behandling av perenn allergisk rinit. Eftersom den orala granulatformuleringen på 4 mg är bioekvivalent med tuggtabletten på 4 mg, kan den också användas som en alternativ formulering till tuggtabletten på 4 mg hos pediatriska patienter i åldern 2 till 5 år.
Läkemedelsinteraktionsstudier
Teofyllin, Prednison och Prednisolon
SINGULAIR har administrerats tillsammans med andra behandlingar som rutinmässigt används vid profylax och kronisk behandling av astma utan uppenbar ökning av biverkningar. I läkemedelsinteraktionsstudier hade den rekommenderade kliniska dosen av montelukast inte kliniskt viktiga effekter på farmakokinetiken för följande läkemedel: teofyllin, prednison och prednisolon.
Montelukast i en dos på 10 mg en gång dagligen doserad till farmakokinetisk steady state, orsakade inga kliniskt signifikanta förändringar i kinetiken för en intravenös engångsdos av teofyllin [huvudsakligen ett cytokrom P450 (CYP) 1A2-substrat]. Montelukast i doser på ≥100 mg dagligen doserat till farmakokinetisk steady state, orsakade ingen kliniskt signifikant förändring i plasmaprofiler för prednison eller prednisolon efter administrering av antingen oral prednison eller intravenös prednisolon.
Orala preventivmedel, Fexofenadin, Digoxin och Warfarin
läkemedelsinteraktionsstudier hade den rekommenderade kliniska dosen av montelukast inte kliniskt viktiga effekter på farmakokinetiken för följande läkemedel: orala preventivmedel (noretindron 1 mg/etinylestradiol 35 mikrogram), digoxin och warfarin. Montelukast vid doser på ≥100 mg dagligen doserat till farmakokinetisk steady state förändrade inte signifikant plasmakoncentrationerna av någon av komponenterna i ett oralt preventivmedel innehållande noretindron 1 mg/etinylestradiol 35 mikrogram. Montelukast i en dos på 10 mg en gång dagligen doserad till farmakokinetisk steady state förändrade inte plasmakoncentrationsprofilen för fexofenadin, förändrade inte den farmakokinetiska profilen eller urinutsöndringen av immunreaktivt digoxin; förändrade inte den farmakokinetiska profilen för warfarin (primärt ett substrat av CYP2C9, 3A4 och 1A2) eller påverkade effekten av en enstaka 30 mg oral dos warfarin på protrombintiden eller det internationella normaliserade förhållandet (INR).
Sköldkörtelhormoner, lugnande hypnotika, icke-steroida antiinflammatoriska medel, bensodiazepiner och avsvällande medel
Även om ytterligare specifika interaktionsstudier inte utfördes, användes SINGULAIR samtidigt med ett brett spektrum av vanligt föreskrivna läkemedel i kliniska studier utan tecken på kliniska negativa interaktioner. Dessa mediciner inkluderade sköldkörtelhormoner, lugnande hypnotika, icke-steroida antiinflammatoriska medel, bensodiazepiner och avsvällande medel.
Cytokrom P450 (CYP) enzyminducerare
Fenobarbital, som inducerar levermetabolism, minskade arean under plasmakoncentrationskurvan (AUC) för montelukast med cirka 40 % efter en engångsdos på 10 mg montelukast. Ingen dosjustering för SINGULAIR rekommenderas. Det är rimligt att använda lämplig klinisk övervakning när potenta CYP-enzyminducerare, såsom fenobarbital eller rifampin, administreras samtidigt med SINGULAIR.
Effekt av Montelukast på cytokrom P450 (CYP) enzymer
Montelukast är en potent hämmare av CYP2C8 in vitro. Data från en klinisk läkemedelsinteraktionsstudie med montelukast och rosiglitazon (ett sondsubstrat som är representativt för läkemedel som primärt metaboliseras av CYP2C8) hos 12 friska individer visade dock att farmakokinetiken för rosiglitazon inte förändras när läkemedlen ges samtidigt, vilket tyder på att montelukast gör inte hämmar CYP2C8 in vivo. Därför förväntas inte montelukast förändra metabolismen av läkemedel som metaboliseras av detta enzym (t.ex. paklitaxel, rosiglitazon och repaglinid). Baserat på ytterligare in vitro-resultat i humana levermikrosomer, hämmar inte terapeutiska plasmakoncentrationer av montelukast CYP 3A4, 2C9, 1A2, 2A6, 2C19 eller 2D6.
Cytokrom P450 (CYP) enzymhämmare
In vitro-studier har visat att montelukast är ett substrat för CYP 2C8, 2C9 och 3A4. Samtidig administrering av montelukast och itrakonazol, en stark CYP 3A4-hämmare, resulterade inte i någon signifikant ökning av den systemiska exponeringen av montelukast. Data från en klinisk läkemedelsinteraktionsstudie som involverade montelukast och gemfibrozil (en hämmare av både CYP 2C8 och 2C9) visade att gemfibrozil vid en terapeutisk dos ökade den systemiska exponeringen av montelukast med 4,4 gånger. Samtidig administrering av itrakonazol, gemfibrozil och montelukast ökade inte ytterligare den systemiska exponeringen av montelukast. Baserat på tillgänglig klinisk erfarenhet krävs ingen dosjustering av montelukast vid samtidig administrering med gemfibrozil [se ÖVERDOS ].
Kliniska studier
Astma
Vuxna och ungdomar 15 år och äldre med astma
Kliniska prövningar på vuxna och ungdomar från 15 år och äldre har visat att det inte finns någon ytterligare klinisk nytta av montelukastdoser över 10 mg en gång dagligen.
Effekten av SINGULAIR för kronisk behandling av astma hos vuxna och ungdomar 15 år och äldre visades i två (USA och multinationella) liknande utformade, randomiserade, 12-veckors, dubbelblinda, placebokontrollerade studier på 1576 patienter ( 795 behandlade med SINGULAIR, 530 behandlade med placebo och 251 behandlade med aktiv kontroll). Medianåldern var 33 år (intervall 15 till 85); 56,8% var kvinnor och 43,2% var män. Den etniska/rasfördelningen i dessa studier var 71,6 % kaukasiska, 17,7 % latinamerikanska, 7,2 % andra ursprung och 3,5 % svarta. Patienterna hade mild eller måttlig astma och var icke-rökare som krävde cirka 5 bloss av inhalerad β-agonist per dag på en "vid behov". Patienterna hade en genomsnittlig baslinjeprocent av förutsagd forcerad utandningsvolym på 1 sekund (FEV1) på 66 % (ungefärligt intervall, 40 till 90 %). De co-primära effektmåtten i dessa studier var FEV1 och astmasymtom dagtid. I båda studierna efter 12 veckor byttes en slumpmässig undergrupp av patienter som fick SINGULAIR 5 mg till placebo under ytterligare 3 veckors dubbelblind behandling för att utvärdera eventuella rebound-effekter.
Resultaten av den amerikanska studien på det primära effektmåttet, FEV1 på morgonen, uttryckt som genomsnittlig procentuell förändring från baslinjen i genomsnitt över den 12 veckor långa behandlingsperioden, visas i FIGUR 2. Jämfört med placebo, behandling med en SINGULAIR 10 mg tablett dagligen i kvällen resulterade i en statistiskt signifikant ökning av FEV1 procentuell förändring från baslinjen (13,0 %-förändring i gruppen som behandlades med SINGULAIR 4 mg vs. 4,2 %-ändring i placebogruppen, p
Figur 2: FEV1 genomsnittlig procentuell förändring från baslinjen (USA-försök: SINGULAIR 5mg N=406; Placebo N=270) (ANOVA-modell)
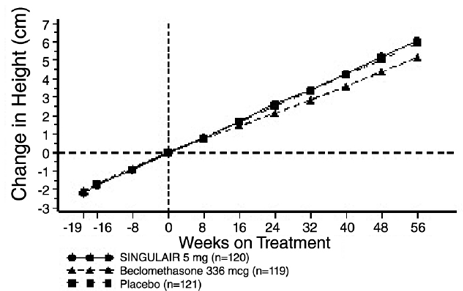
Effekten av SINGULAIR 5 mg på andra primära och sekundära effektmått, representerade av den multinationella studien, visas i TABELL 6. Resultaten för dessa effektmått var liknande i den amerikanska studien.
Båda studierna utvärderade effekten av SINGULAIR 4mg på sekundära utfall, inklusive astmaanfall (användning av sjukvårdsresurser såsom ett oplanerat besök på läkarmottagning, akutmottagning eller sjukhus; eller behandling med oral, intravenös eller intramuskulär kortikosteroid), och användning av orala kortikosteroider för astmaräddning. I den multinationella studien upplevde signifikant färre patienter (15,6 % av patienterna) på SINGULAIR astmaanfall jämfört med patienter på placebo (27,3 %, p
Början av åtgärder och underhåll av effekter
I varje placebokontrollerad prövning på vuxna uppnåddes behandlingseffekten av SINGULAIR 4 mg, mätt med dagliga dagbokkortparametrar, inklusive symtompoäng, "vid behov" β-agonistanvändning och PEFR-mätningar, efter den första dosen och bibehölls under hela doseringsintervallet (24 timmar). Ingen signifikant förändring i behandlingseffekt observerades vid kontinuerlig administrering en gång dagligen på kvällen i icke-placebokontrollerade förlängningsstudier i upp till ett år. Utsättning av SINGULAIR 4 mg hos astmatiska patienter efter 12 veckors kontinuerlig användning orsakade inte rebound-förvärring av astma.
Pediatriska patienter 6 till 14 år med astma
Effekten av SINGULAIR 5 mg hos pediatriska patienter i åldern 6 till 14 år visades i en 8 veckor lång, dubbelblind, placebokontrollerad studie på 336 patienter (201 behandlade med SINGULAIR och 135 behandlade med placebo) med en inhalerad β-agonist på "efter behov". Patienterna hade en genomsnittlig baslinjeprocent förutspådd FEV1 på 72 % (ungefärligt intervall, 45 till 90 %) och ett genomsnittligt dagligt behov av inhalerad β-agonist på 3,4 bloss albuterol. Cirka 36 % av patienterna fick inhalerade kortikosteroider. Medianåldern var 11 år (intervall 6 till 15); 35,4% var kvinnor och 64,6% var män. Den etniska/rasfördelningen i denna studie var 80,1 % kaukasiska, 12,8 % svarta, 4,5 % latinamerikanska och 2,7 % av annat ursprung.
Jämfört med placebo resulterade behandling med en 5 mg SINGULAIR 4 mg tuggtablett dagligen i en signifikant förbättring av den genomsnittliga FEV1-procentiga förändringen på morgonen från baslinjen (8,7 % i gruppen som behandlades med SINGULAIR 4 mg jämfört med 4,2 % förändring från baslinjen i placebogruppen, p
likhet med vuxenstudierna observerades ingen signifikant förändring av behandlingseffekten under kontinuerlig administrering en gång dagligen i en öppen förlängningsstudie utan samtidig placebogrupp i upp till 6 månader.
Pediatriska patienter 2 till 5 år gamla med astma
Effekten av SINGULAIR för kronisk behandling av astma hos pediatriska patienter i åldern 2 till 5 år undersöktes i en 12-veckors placebokontrollerad säkerhets- och tolerabilitetsstudie på 689 patienter, varav 461 behandlades med SINGULAIR. Medianåldern var 4 år (intervall 2 till 6); 41,5% var kvinnor och 58,5% var män. Den etniska/rasfördelningen i denna studie var 56,5 % kaukasiska, 20,9 % latinamerikanska, 14,4 % andra ursprung och 8,3 % svarta.
Medan det primära målet var att fastställa säkerheten och tolerabiliteten för SINGULAIR 10 mg i denna åldersgrupp, inkluderade studien explorativa effektutvärderingar, inklusive astmasymtompoäng dagtid och över natten, användning av β-agonist, oral kortikosteroidräddning och läkarens globala utvärdering. Resultaten av dessa explorativa effektutvärderingar, tillsammans med farmakokinetik och extrapolering av effektdata från äldre patienter, stödjer den övergripande slutsatsen att SINGULAIR är effektivt vid underhållsbehandling av astma hos patienter i åldern 2 till 5 år.
Effekter hos patienter på samtidiga inhalerade kortikosteroider
Separata prövningar på vuxna utvärderade förmågan hos SINGULAIR 10 mg att öka den kliniska effekten av inhalerade kortikosteroider och att tillåta inhalerade kortikosteroidnedskärningar när de används samtidigt.
En randomiserad, placebokontrollerad, parallellgruppsstudie (n=226) inkluderade vuxna med stabil astma med ett genomsnittligt FEV1 på cirka 84 % av de förutspådda som tidigare hållits på olika inhalerade kortikosteroider (tillförda med aerosol- eller torrpulverinhalatorer med uppmätta doser). ). Medianåldern var 41,5 år (intervall 16 till 70); 52,2% var kvinnor och 47,8% var män. Den etniska/rasfördelningen i denna studie var 92,0 % kaukasiska, 3,5 % svarta, 2,2 % latinamerikanska och 2,2 % asiatiska. Typerna av inhalerade kortikosteroider och deras genomsnittliga baslinjebehov inkluderade beklometasondipropionat (medeldos, 1203 mcg/dag), triamcinolonacetonid (medeldos, 2004 mcg/dag), flunisolid (medeldos, 1971 mcg/dag), flutikasonpropionat ( dos, 1083 mcg/dag), eller budesonid (medeldos, 1192 mcg/dag). Vissa av dessa inhalerade kortikosteroider var icke-amerikanskt godkända formuleringar och de uttryckta doserna kanske inte är ex-aktuator. Behovet av inhalerade kortikosteroider från förstudien minskade med cirka 37 % under en placebo-inkörningsperiod på 5 till 7 veckor, utformad för att titrera patienter mot deras lägsta effektiva inhalerade kortikosteroiddos. Behandling med SINGULAIR 4 mg resulterade i ytterligare 47 % minskning av medeldosen för inhalerad kortikosteroid jämfört med en genomsnittlig minskning på 30 % i placebogruppen under den 12-veckors aktiva behandlingsperioden (p≤0,05). Det är inte känt om resultaten av denna studie kan generaliseras till patienter med astma som kräver högre doser av inhalerade kortikosteroider eller systemiska kortikosteroider.
en annan randomiserad, placebokontrollerad, parallellgruppsstudie (n=642) på en liknande population av vuxna patienter som tidigare bibehållits, men inte tillräckligt kontrollerade, på inhalerade kortikosteroider (beklometason 336 mikrogram/dag), resulterade tillägget av SINGULAIR till beklometason i statistiskt signifikanta förbättringar av FEV1 jämfört med de patienter som fortsatte med enbart beklometason eller de patienter som avbröts från beklometason och behandlades med enbart montelukast eller placebo under de sista 10 veckorna av den 16 veckor långa, blinda behandlingsperioden. Patienter som randomiserades till behandlingsarmar innehållande beklometason hade statistiskt signifikant bättre astmakontroll än de patienter som randomiserades till enbart SINGULAIR eller enbart placebo, vilket indikeras av FEV1, astmasymtom dagtid, PEFR, nattliga uppvaknanden på grund av astma och "vid behov" β- agonistkrav.
Hos vuxna patienter med astma med dokumenterad acetylsalicylsyrakänslighet, av vilka nästan alla fick samtidigt inhalerade och/eller orala kortikosteroider, visade en 4-veckors, randomiserad, parallellgruppsstudie (n=80) att SINGULAIR 10 mg, jämfört med placebo, resulterade i i betydande förbättring av parametrar för astmakontroll. Effektstorleken av SINGULAIR 4 mg hos aspirinkänsliga patienter liknade den effekt som observerades i den allmänna populationen av studerade astmapatienter. Effekten av SINGULAIR på bronkokonstriktorsvaret på aspirin eller andra icke-steroida antiinflammatoriska läkemedel hos aspirinkänsliga astmatiska patienter har inte utvärderats [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Ansträngningsinducerad bronkokonstriktion (EIB)
Träningsutlöst bronkokonstriktion (vuxna, ungdomar och pediatriska patienter 6 år och äldre)
Effekten av SINGULAIR 5 mg, 10 mg, när den gavs som engångsdos 2 timmar före träning för att förebygga EIB, undersöktes i tre (USA och multinationella), randomiserade, dubbelblinda, placebokontrollerade crossover-studier som inkluderade totalt 160 vuxna och ungdomar 15 år och äldre med EIB. Utmaningstestning utfördes 2 timmar, 8,5 eller 12 timmar och 24 timmar efter administrering av en enstaka dos av studieläkemedlet (SINGULAIR 10 mg eller placebo). Det primära effektmåttet var det genomsnittliga maximala procentuella fallet i FEV1 efter 2 timmars träningsutmaning efter dosen i alla tre studierna (studie A, studie B och studie C). I studie A visade en engångsdos av SINGULAIR 10 mg en statistiskt signifikant skyddande fördel mot EIB när den togs 2 timmar före träning. Vissa patienter skyddades från EIB 8,5 och 24 timmar efter administrering; vissa patienter var dock inte det. Resultaten för den genomsnittliga maximala procentminskningen vid varje tidpunkt i studie A visas i tabell 7 och är representativa för resultaten från de andra två studierna.
Effekten av SINGULAIR 5-mg tuggtabletter, när de gavs som engångsdos 2 timmar före träning för att förebygga EIB, undersöktes i en multinationell, randomiserad, dubbelblind, placebokontrollerad crossover-studie som omfattade totalt 64 pediatriska patienter 6 till 14 år med EIB. Utmaningstestning utfördes 2 timmar och 24 timmar efter administrering av en enstaka dos av studieläkemedlet (SINGULAIR 5 mg eller placebo). Det primära effektmåttet var det genomsnittliga maximala procentuella fallet i FEV1 efter 2 timmars träningsutmaning efter dosen. En engångsdos av SINGULAIR 5 mg visade en statistiskt signifikant skyddande fördel mot EIB när den togs 2 timmar före träning (TABELL 8). Liknande resultat visades 24 timmar efter dosering (en sekundär effektmått). Vissa patienter skyddades från EIB 24 timmar efter administrering; vissa patienter var dock inte det. Inga tidpunkter bedömdes mellan 2 och 24 timmar efter dosering.
Effekten av SINGULAIR 5 mg för att förebygga EIB hos patienter under 6 år har inte fastställts.
Daglig administrering av SINGULAIR 4 mg för kronisk behandling av astma har inte fastställts för att förhindra akuta episoder av EIB.
en 12-veckors, randomiserad, dubbelblind, parallell gruppstudie av 110 vuxna och ungdomar astmatiker 15 år och äldre, med en genomsnittlig baslinje FEV1 procent av förutspådd på 83 % och med dokumenterad träningsinducerad exacerbation av astma, behandling med SINGULAIR, 10 mg, en gång dagligen på kvällen, resulterade i en statistiskt signifikant minskning av den genomsnittliga maximala procentuella minskningen av FEV1 och medeltiden till återhämtning till inom 5 % av FEV1 före träning. Träningsutmaning utfördes i slutet av doseringsintervallet (dvs. 20 till 24 timmar efter föregående dos). Denna effekt bibehölls under hela den 12 veckor långa behandlingsperioden, vilket tyder på att tolerans inte inträffade. SINGULAIR 4 mg förhindrade dock inte kliniskt signifikant försämring av maximal procentuell minskning av FEV1 efter träning (dvs. ≥20 % minskning från baslinjen före träning) hos 52 % av de studerade patienterna. I en separat crossover-studie på vuxna observerades en liknande effekt efter två doser på 10 mg SINGULAIR en gång dagligen.
Hos pediatriska patienter i åldern 6 till 14 år, som använde 5 mg tuggtablett, visade en 2-dagars crossover-studie effekter liknande de som observerades hos vuxna när träningsutmaning utfördes i slutet av doseringsintervallet (dvs. 20 till 24 timmar efter föregående dos).
Allergisk rinit (säsongsbetonad och flerårig)
Säsongsbunden allergisk rinit
Effekten av SINGULAIR-tabletter för behandling av säsongsbunden allergisk rinit undersöktes i 5 liknande utformade, randomiserade, dubbelblinda, parallellgrupps-, placebo- och aktivkontrollerade (loratadin) studier utförda i Nordamerika. De 5 studierna inkluderade totalt 5029 patienter, av vilka 1799 behandlades med SINGULAIR-tabletter. Patienterna var 15 till 82 år gamla med en historia av säsongsbunden allergisk rinit, ett positivt hudtest på minst ett relevant säsongsbetonat allergen och aktiva symtom på säsongsbunden allergisk rinit vid studiestart.
Perioden för randomiserad behandling var 2 veckor i 4 prövningar och 4 veckor i en prövning. Den primära utfallsvariabeln var genomsnittlig förändring från baslinjen i poäng för nässymtom dagtid (genomsnittet av individuella poäng för nästäppa, rinorré, näsklåda, nysningar) som bedömts av patienter på en 0-3 kategorisk skala.
Fyra av de fem studierna visade en signifikant minskning av poängen för nasala symtom dagtid med SINGULAIR 10 mg tabletter jämfört med placebo. Resultaten av en studie visas nedan. Medianåldern i denna studie var 35,0 år (intervall 15 till 81); 65,4% var kvinnor och 34,6% var män. Den etniska/rasfördelningen i denna studie var 83,1 % kaukasiska, 6,4 % andra ursprung, 5,8 % svarta och 4,8 % latinamerikanska. De genomsnittliga förändringarna från utgångsvärdet för nässymtom på dagtid i behandlingsgrupperna som fick SINGULAIR 4 mg tabletter, loratadin och placebo visas i TABELL 9. De återstående tre studierna som visade effekt visade liknande resultat. Effekt har visats för säsongsbunden allergisk rinit när montelukast administrerades på morgonen eller kvällen.
Perenn allergisk rinit
Effekten av SINGULAIR 5 mg tabletter för behandling av perenn allergisk rinit undersöktes i 2 randomiserade, dubbelblinda, placebokontrollerade studier utförda i Nordamerika och Europa. De två studierna inkluderade totalt 3357 patienter, av vilka 1632 fick SINGULAIR 10 mg tabletter. Patienter i åldern 15 till 82 år med perenn allergisk rinit som bekräftats av historia och ett positivt hudtest på minst ett relevant perenn allergen (dammkvalster, djurmjäll och/eller mögelsporer), som hade aktiva symtom vid tidpunkten för studien inträde, var inskrivna.
studien där effekt visades var medianåldern 35 år (intervall 15 till 81); 64,1% var kvinnor och 35,9% var män. Den etniska/rasfördelningen i denna studie var 83,2 % kaukasiska, 8,1 % svarta, 5,4 % latinamerikanska, 2,3 % asiatiska och 1,0 % andra ursprung. SINGULAIR 10 mg tabletter en gång dagligen visade sig signifikant minska symtomen på perenn allergisk rinit under en 6-veckors behandlingsperiod (TABELL 10); i denna studie var den primära utfallsvariabeln genomsnittlig förändring från baslinjen i poäng för nasala symtom på dagtid (genomsnittet av individuella poäng av nästäppa, rinorré och nysningar).
Den andra 6-veckorsstudien utvärderade SINGULAIR 10 mg (n=626), placebo (n=609) och en aktiv kontroll (cetirizin 10 mg; n=120). Den primära analysen jämförde den genomsnittliga förändringen från baslinjen i poäng för nasala symtom dagtid för SINGULAIR vs. placebo under de första 4 veckorna av behandlingen; studien var inte utformad för statistisk jämförelse mellan SINGULAIR och den aktiva kontrollen. Den primära utfallsvariabeln inkluderade näsklåda förutom nästäppa, rinorré och nysningar. Den uppskattade skillnaden mellan SINGULAIR och placebo var -0,04 med en 95 % KI på (-0,09, 0,01). Den uppskattade skillnaden mellan den aktiva kontrollen och placebo var -0,10 med en 95 % KI på (-0,19, -0,01).
PATIENTINFORMATION
SINGULAIR® (SING-u-lair)(montelukastnatrium) tuggtabletter
Vilken är den viktigaste informationen jag borde veta om SINGULAIR 4mg?Allvarliga psykiska problem har inträffat hos personer som tar SINGULAIR eller till och med efter att behandlingen har upphört.
Detta kan hända hos personer med eller utan en historia av psykiska problem. Sluta ta SINGULAIR och berätta omedelbart för din vårdgivare om du eller ditt barn har några ovanliga förändringar i beteende eller tänkande, inklusive något av dessa symtom:
- agitation, inklusive aggressivt beteende eller fientlighet
- uppmärksamhetsproblem
- dåliga eller livliga drömmar
- depression
- desorientering (förvirring)
- känner sig orolig
- irritabilitet
- hallucinationer (att se eller höra saker som inte riktigt finns där)
- minnesproblem
- tvångssyndrom
- rastlöshet
- sova promenader
- stamning
- självmordstankar och -handlingar (inklusive självmord)
- darrning
- sömnproblem
- okontrollerade muskelrörelser
Vad är SINGULAIR 10mg?
SINGULAIR 4mg är ett receptbelagt läkemedel som blockerar ämnen i kroppen som kallas leukotriener. Detta kan hjälpa till att förbättra symtom på astma och inflammation i nässlemhinnan (allergisk rinit). SINGULAIR innehåller ingen steroid. SINGULAIR används för att:
- utomhusallergier som inträffar en del av året (säsongsbunden allergisk rinit) hos vuxna och barn i åldrarna 2 år och äldre, och
- inomhusallergier som inträffar året runt (perenn allergisk rinit) hos vuxna och barn i åldrarna 6 månader och äldre.
Låt bli ta SINGULAIR om du är allergisk mot något av dess ingredienser. Se slutet av denna medicineringsguide för en komplett lista över ingredienserna i SINGULAIR.
Innan du tar SINGULAIR 4mg, berätta för din vårdgivare om alla dina medicinska tillstånd, inklusive om du:
- är allergiska mot aspirin.
- har fenylketonuri. SINGULAIR tuggtabletter innehåller aspartam, en källa till fenylalanin.
- har eller har haft psykiska problem.
- är gravid eller planerar att bli gravid. Prata med din vårdgivare om du är gravid eller planerar att bli gravid, SINGULAIR 4mg kanske inte är rätt för dig.
- ammar eller planerar att amma. Det är inte känt om SINGULAIR går över i din bröstmjölk. Prata med din vårdgivare om det bästa sättet att mata ditt barn medan du tar SINGULAIR.
Berätta för din vårdgivare om alla läkemedel du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Vissa läkemedel kan påverka hur SINGULAIR verkar, eller SINGULAIR 4 mg kan påverka hur dina andra läkemedel fungerar.
Hur ska jag ta SINGULAIR 10mg?
För någon vem tar SINGULAIR:
- Läs den detaljerade Användningsinstruktioner som kommer med SINGULAIR orala granulat.
- Ta SINGULAIR 4mg exakt som ordinerats av din läkare. Din vårdgivare kommer att tala om för dig hur mycket SINGULAIR du ska ta, och när man ska ta det.
- Sluta ta SINGULAIR 5mg och berätta omedelbart för din vårdgivare om du eller ditt barn har några ovanliga förändringar i beteende eller tänkande.
- Du kan ta SINGULAIR 5 mg med eller utan mat. Se avsnittet "Hur kan jag ge SINGULAIR orala granulat till mitt barn?" i Användningsinstruktioner för information om vilka livsmedel och vätskor som kan tas med SINGULAIR 10 mg orala granulat.
- Om du eller ditt barn missar en dos av SINGULAIR, ta bara nästa dos vid din vanliga tidpunkt. Ta inte 2 doser samtidigt.
- Om du tar för mycket SINGULAIR, ring din vårdgivare omedelbart.
För vuxna och barn 12 månader och äldre med astma:
- Ta SINGULAIR 1 gång varje dag, på kvällen. Fortsätt att ta SINGULAIR 5 mg varje dag så länge som din läkare ordinerar det, även om du inte har några astmasymtom.
- Berätta omedelbart för din vårdgivare om dina astmasymtom blir värre eller om du behöver använda din räddningsinhalator oftare för astmaanfall.
- Ha alltid din räddningsinhalatormedicin med dig för astmaanfall.
- Fortsätt att ta dina andra astmamediciner enligt ordination om inte din läkare säger åt dig att ändra hur du tar dessa läkemedel.
För personer 6 år och äldre för att förebygga ansträngningsutlöst astma:
- Ta SINGULAIR minst 2 timmar före träning.
- Ha alltid din räddningsinhalatormedicin med dig för astmaanfall.
- Om du tar SINGULAIR 10 mg varje dag för kronisk astma eller allergisk rinit, låt bli ta ytterligare en dos för att förhindra ansträngningsutlöst astma. Prata med din vårdgivare om din behandling för ansträngningsutlöst astma.
- Ta inte 2 doser av SINGULAIR 5 mg inom 24 timmar (1 dag).
För alla 2 år och äldre med säsongsbunden allergisk rinit, eller för alla 6 månader och äldre med perenn allergisk rinit:
- Ta SINGULAIR 1 gång varje dag, ungefär vid samma tidpunkt varje dag.
Vad ska jag undvika när jag tar SINGULAIR 10mg?
Om du har astma och acetylsalicylsyra förvärrar dina astmasymtom, fortsätt att undvika att ta aspirin eller andra läkemedel som kallas icke-steroida antiinflammatoriska läkemedel (NSAID) medan du tar SINGULAIR.
Vilka är de möjliga biverkningarna av SINGULAIR?
SINGULAIR kan orsaka allvarliga biverkningar, inklusive:
- Ser "Vilken är den viktigaste informationen jag borde veta om SINGULAIR 4mg?"
- Ökning av vissa vita blodkroppar (eosinofiler) och möjliga inflammerade blodkärl i hela kroppen (systemisk vaskulit). I sällsynta fall kan detta hända hos personer med astma som tar SINGULAIR. Detta händer ibland hos personer som också tar en steroidmedicin genom munnen som stoppas eller dosen sänks.
Berätta genast för din vårdgivare om du får ett eller flera av dessa symtom:
- en känsla av nålar eller domningar i armar eller ben
- en influensaliknande sjukdom
- utslag
- allvarlig inflammation (smärta och svullnad) i bihålorna (bihåleinflammation)
De vanligaste biverkningarna av SINGULAIR inkluderar:
- övre luftvägsinfektion
- feber
- huvudvärk
- öm hals
- hosta
- magont
- diarre
- öronvärk eller öroninfektion
- influensa
- rinnande näsa
- bihåleinflammation
Dessa är inte alla möjliga biverkningar av SINGULAIR. Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara SINGULAIR?
- Förvara SINGULAIR 10 mg i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
- Förvara SINGULAIR 4mg i förpackningen den kommer i.
- Förvara SINGULAIR 4mg på en torr plats och håll den borta från ljus.
- Förvara SINGULAIR och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av SINGULAIR.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte SINGULAIR för ett tillstånd som det inte har ordinerats för. Ge inte SINGULAIR till andra personer även om de har samma symtom som du har. Det kan skada dem.
Du kan fråga din apotekspersonal eller vårdgivare om information om SINGULAIR 10mg som är skriven för vårdpersonal.
Vilka är ingredienserna i SINGULAIR?
Aktiv beståndsdel: montelukastnatrium
Inaktiva Ingredienser:
- 4 mg orala granulat: mannitol, hydroxipropylcellulosa och magnesiumstearat.
- 4 mg och 5 mg tuggtabletter: mannitol, mikrokristallin cellulosa, hydroxipropylcellulosa, röd järnoxid, kroskarmellosnatrium, körsbärsarom, aspartam och magnesiumstearat.
- Personer med fenylketonuri: SINGULAIR 4 mg tuggtabletter innehåller 0,674 mg fenylalanin och SINGULAIR 5 mg tuggtabletter innehåller 0,842 mg fenylalanin.
- 10 mg tablett: mikrokristallin cellulosa, laktosmonohydrat, kroskarmellosnatrium, hydroxipropylcellulosa och magnesiumstearat. Filmbeläggningen innehåller: hydroxipropylmetylcellulosa, hydroxipropylcellulosa, titandioxid, röd järnoxid, gul järnoxid och karnaubavax.
Användningsinstruktioner
SINGULAIR® (SING-u-lair)(montelukastnatrium) orala granulat
Denna bruksanvisning innehåller information om hur man använder SINGULAIR 10 mg orala granulat.
Viktig information:
- Innan du ger en dos av SINGULAIR orala granulat, läs denna bruksanvisning för att vara säker på att du förbereder och ger det orala granulatet korrekt.
- Ge SINGULAIR orala granulat till ditt barn exakt enligt instruktioner från din vårdgivare.
- Sluta ge SINGULAIR 5 mg och berätta omedelbart för din vårdgivare om ditt barn har några ovanliga förändringar i beteende eller tänkande.
- Fortsätt att ge ditt barn sina astmamediciner enligt ordination, såvida inte din vårdgivare säger åt dig att ändra hur du ger dessa läkemedel.
- Du kan ge SINGULAIR 5 mg orala granulat med mat eller utan mat.
Hur kan jag ge SINGULAIR 4 mg orala granulat till mitt barn?
- Låt bli öppna paketet tills det ska användas.
- Det finns olika sätt att ge SINGULAIR 4 mg orala granulat. Du bör välja den bästa metoden för ditt barn:
- rakt in i munnen
- löst i 1 tesked (5 ml) kall eller rumstempererad modersmjölksersättning eller bröstmjölk
- blandas med 1 sked av någon av följande mjuka livsmedel vid kall eller rumstemperatur: äppelmos, mosade morötter, ris eller glass.
- Ge barnet hela blandningen inom 15 minuter.
- Förvara inga överblivna SINGULAIR-blandningar (orala granulat blandat med mat, modersmjölksersättning eller bröstmjölk) för användning vid ett senare tillfälle. Kasta bort all oanvänd del.
- Blanda inte SINGULAIR orala granulat med någon annan flytande dryck än modersmjölksersättning eller bröstmjölk. Ditt barn kan dricka andra vätskor efter att ha svalt blandningen.
Hur ska jag förvara SINGULAIR 5mg?
- Förvara SINGULAIR 4mg i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
- Förvara SINGULAIR i förpackningen den kommer i.
- Förvara SINGULAIR 5mg på en torr plats och håll den borta från ljus.
- Förvara SINGULAIR och alla läkemedel utom räckhåll för barn.
Denna bruksanvisning har godkänts av US Food and Drug Administration
