Buspar 5mg, 10mg Buspirone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Buspar och hur används det?
Buspar 5mg är ett receptbelagt läkemedel som används för att behandla symtom på ångestsyndrom. Buspar 5mg kan användas ensamt eller tillsammans med andra läkemedel.
Buspar tillhör en klass av läkemedel som kallas ångestdämpande medel, anxiolytika, icke-bensodiazepiner.
Vilka är de möjliga biverkningarna av Buspar?
Vilka är de möjliga biverkningarna av Buspar 5mg?
Buspar kan orsaka allvarliga biverkningar inklusive:
- bröstsmärta,
- andnöd, och
- yrsel
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Buspar inkluderar:
- huvudvärk,
- yrsel,
- dåsighet,
- sömnproblem (sömnlöshet),
- illamående,
- orolig mage, och
- känner sig nervös eller upprymd
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Buspar. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Buspironhydrokloridtabletter, USP är ett ångestdämpande medel som inte är kemiskt eller farmakologiskt relaterat till bensodiazepinerna, barbiturater eller andra lugnande/ångestdämpande läkemedel.
Buspironhydroklorid, USP är ett vitt kristallint pulver. Det är mycket lösligt i vatten; fritt löslig i metanol och i metylenklorid; svårlöslig i etanol och i acetonitril; mycket svagt löslig i etylacetat och praktiskt taget olöslig i hexaner. Dess molekylvikt är 422. Kemiskt sett är buspironhydroklorid 8-[4-[4-(2-pyrimidinyl)-1-piperazinyl]butyl]-8-azaspiro[4.5]dekan-7,9-dionmonohydroklorid. Molekylformeln C21H31N5O2•HCl representeras av följande strukturformel:
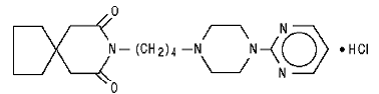
Varje buspironhydrokloridtablett avsedd för oral administrering innehåller 5 mg eller 10 mg eller 15 mg eller 30 mg buspironhydroklorid (motsvarande 4,6 mg, 9,1 mg, 13,7 mg respektive 27,4 mg fri bas av buspiron). Dessutom innehåller varje tablett följande inaktiva ingredienser: kolloidal kiseldioxid, laktosmonohydrat, magnesiumstearat, mikrokristallin cellulosa och natriumstärkelseglykolat. Tabletterna på 5 mg och 10 mg är skårade så att de kan delas i två delar. Således kan 5 mg-tabletten också ge en 2,5 mg-dos, och 10 mg-tabletten kan ge en 5 mg-dos. Tabletterna på 15 mg och 30 mg är skårade så att de kan delas i två eller tre. Således kan en enstaka 15 mg tablett ge följande doser: 15 mg (hela tabletten), 10 mg (två tredjedelar av en tablett), 7,5 mg (halva tabletten) eller 5 mg (en tredjedel av en tablett) . En enstaka 30 mg tablett kan ge följande doser: 30 mg (hela tabletten), 20 mg (två tredjedelar av en tablett), 15 mg (halva tabletten) eller 10 mg (en tredjedel av en tablett).
INDIKATIONER
Buspironhydrokloridtabletter är indicerade för hantering av ångestsyndrom eller kortvarig lindring av ångestsymtom. Ångest eller spänningar i samband med stress i vardagen kräver vanligtvis inte behandling med ett ångestdämpande medel.
Effekten av buspironhydrokloridtabletter har visats i kontrollerade kliniska prövningar av öppenvårdspatienter vars diagnos ungefär motsvarar generaliserat ångestsyndrom (GAD). Många av patienterna som ingick i dessa studier hade också samexisterande depressiva symtom och buspironhydrokloridtabletter lindrade ångest i närvaro av dessa samexisterande depressiva symtom. Patienterna som utvärderades i dessa studier hade upplevt symtom under perioder på 1 månad till över 1 år före studien, med en genomsnittlig symtomvaraktighet på 6 månader. Generalized Anxiety Disorder (300.02) beskrivs i American Psychiatric Association's Diagnostic and Statistical Manual, III1 enligt följande:
Generaliserad, ihållande ångest (under minst 1 månads kontinuerlig varaktighet), manifesterad av symtom från tre av följande fyra kategorier:
Motorspänning
Skakighet, darrning, hoppighet, darrningar, spänningar, muskelvärk, trötthet, oförmåga att slappna av, ryckningar i ögonlocket, rynkade ögonbryn, ansträngt ansikte, rörelser, rastlöshet, lätt skrämsel.
Autonom hyperaktivitet
Svettning, hjärtklappning, förkylning, klibbiga händer, muntorrhet, yrsel, yrsel, parestesier (stickningar i händer eller fötter), orolig mage, varma eller kalla perioder, frekvent urinering, diarré, obehag i maggropen, knöl i halsen, rodnad, blekhet, hög vilopuls och andningsfrekvens.
Orolig förväntan
Ångest, oro, rädsla, grubblande och förväntan om olycka för sig själv eller andra.
Vaksamhet och skanning
Hyperuppmärksamhet som resulterar i distraherbarhet, koncentrationssvårigheter, sömnlöshet, känsla "på kanten", irritabilitet, otålighet.
Ovanstående symtom skulle inte bero på en annan psykisk störning, såsom en depressiv sjukdom eller schizofreni. Men milda depressiva symtom är vanliga vid GAD.
Effektiviteten av buspironhydrokloridtabletter vid långvarig användning, det vill säga i mer än 3 till 4 veckor, har inte visats i kontrollerade studier. Det finns inga tillgängliga bevis som systematiskt behandlar lämplig behandlingslängd för GAD. I en studie av långtidsanvändning behandlades dock 264 patienter med buspironhydrokloridtabletter under 1 år utan negativ effekt. Därför bör den läkare som väljer att använda buspironhydrokloridtabletter under längre perioder med jämna mellanrum omvärdera läkemedlets användbarhet för den enskilda patienten.
DOSERING OCH ADMINISTRERING
Den rekommenderade initialdosen är 15 mg dagligen (7,5 mg två gånger dagligen). För att uppnå ett optimalt terapeutiskt svar kan dosen ökas med 5 mg per dag med 2 till 3 dagars intervall efter behov. Den maximala dagliga dosen bör inte överstiga 60 mg per dag. I kliniska prövningar som tillåter dostitrering användes vanligtvis uppdelade doser på 20 mg till 30 mg per dag.
Biotillgängligheten av buspiron ökar när det ges tillsammans med mat jämfört med fastande (se KLINISK FARMAKOLOGI ). Följaktligen bör patienter ta buspiron på ett konsekvent sätt med avseende på tidpunkten för dosering; antingen alltid med eller alltid utan mat.
När buspiron ska ges tillsammans med en potent hämmare av CYP3A4, ska de dosrekommendationer som beskrivs i LÄKEMEDELSINTERAKTIONER avsnitt ska följas.
HUR LEVERERAS
Buspironhydrokloridtabletter USP, 5 mg är vita till benvita, kapselformade, plana tabletter med fasade kanter präglade med tvåskärning på ena sidan; en sida av bisect är präglad med "ZE" och en annan är präglad med "36" och andra sidan är vanlig
Tillverkarens uppgifter: N/A. Reviderad: maj 2016
BIEFFEKTER
Ingen information lämnas.
LÄKEMEDELSINTERAKTIONER
Psykotropa medel
MAO-hämmare
Det rekommenderas att buspironhydrokloridtabletter inte används samtidigt med MAO-hämmare (se VARNINGAR ).
Amitriptylin
Efter tillägg av buspiron till amitriptylindosregimen observerades inga statistiskt signifikanta skillnader i steady-state farmakokinetiska parametrar (Cmax, AUC och Cmin) för amitriptylin eller dess metabolit nortriptylin.
Diazepam
Efter tillägg av buspiron till diazepamdosregimen observerades inga statistiskt signifikanta skillnader i farmakokinetiska parametrar vid steady-state (Cmax, AUC och Cmin) för diazepam, men ökningar på cirka 15 % sågs för nordiazepam och mindre negativa kliniska effekter. (yrsel, huvudvärk och illamående) observerades.
Haloperidol
I en studie på normala frivilliga, resulterade samtidig administrering av buspiron och haloperidol i ökade serumkoncentrationer av haloperidol. Den kliniska betydelsen av detta fynd är inte klarlagt.
Nefazodon
[ser Hämmare och inducerare av Cytokrom P450 3A4 (CYP3A4) ].
Trazodon
Det finns en rapport som tyder på att samtidig användning av Desyrel®# (trazodonhydroklorid) och buspiron kan ha orsakat 3- till 6-faldiga förhöjningar av SGPT (ALT) hos ett fåtal patienter. I en liknande studie som försökte replikera detta fynd, identifierades ingen interaktiv effekt på levertransaminaser.
Triazolam/Flurazepam
Samtidig administrering av buspiron med antingen triazolam eller flurazepam verkade inte förlänga eller intensifiera de sedativa effekterna av varken bensodiazepin.
Andra psykotropa ämnen
Eftersom effekterna av samtidig administrering av buspiron med de flesta andra psykotropa läkemedel inte har studerats, bör samtidig användning av buspiron med andra CNS-aktiva läkemedel behandlas med försiktighet.
Hämmare och inducerare av Cytokrom P450 3A4 (CYP3A4)
Buspiron har visats in vitro att metaboliseras av CYP3A4. Detta fynd överensstämmer med de in vivo-interaktioner som observerats mellan buspiron och följande:
Diltiazem och Verapamil
en studie med nio friska frivilliga ökade samtidig administrering av buspiron (10 mg som engångsdos) med verapamil (80 mg tid) eller diltiazem (60 mg tid) plasmakoncentrationerna av buspiron (verapamil ökade AUC och Cmax för buspiron 3,4 gånger medan diltiazem ökad AUC och Cmax 5,5- respektive 4-faldigt.) Biverkningar hänförliga till buspiron kan vara mer sannolika vid samtidig administrering med antingen diltiazem eller verapamil. Efterföljande dosjustering kan vara nödvändig och bör baseras på klinisk bedömning.
Erytromycin
en studie på friska frivilliga ökade samtidig administrering av buspiron (10 mg som engångsdos) och erytromycin (1,5 g/dag i 4 dagar) plasmakoncentrationerna av buspiron (5-faldig ökning av Cmax och 6-faldig ökning av AUC). Dessa farmakokinetiska interaktioner åtföljdes av en ökad förekomst av biverkningar hänförliga till buspiron. Om de två läkemedlen ska användas i kombination rekommenderas en låg dos buspiron (t.ex. 2,5 mg två gånger dagligen). Efterföljande dosjustering av båda läkemedlen bör baseras på klinisk bedömning.
Grapefruktjuice
I en studie på friska frivilliga ökade samtidigt administrering av buspiron (10 mg som engångsdos) med grapefruktjuice (200 ml dubbelstyrka tid under 2 dagar) plasmakoncentrationerna av buspiron (4,3-faldig ökning av Cmax; 9,2-faldig ökning av AUC ). Patienter som får buspiron bör rådas att undvika att dricka så stora mängder grapefruktjuice.
Itrakonazol
en studie på friska frivilliga ökade samtidig administrering av buspiron (10 mg som engångsdos) och itrakonazol (200 mg/dag under 4 dagar) plasmakoncentrationerna av buspiron (13-faldig ökning av Cmax och 19-faldig ökning av AUC). Dessa farmakokinetiska interaktioner åtföljdes av en ökad förekomst av biverkningar hänförliga till buspiron. Om de två läkemedlen ska användas i kombination rekommenderas en låg dos buspiron (t.ex. 2,5 mg varje dag). Efterföljande dosjustering av båda läkemedlen bör baseras på klinisk bedömning.
Nefazodon
en studie av steady-state farmakokinetik hos friska frivilliga, resulterade samtidig administrering av buspiron (2,5 eller 5 mg två gånger dagligen) med nefazodon (250 mg två gånger dagligen) i markanta ökningar av plasmakoncentrationen av buspiron (ökningar upp till 20 gånger i Cmax och upp till 50 gånger) -faldig AUC) och statistiskt signifikanta minskningar (cirka 50 %) i plasmakoncentrationer av buspironmetaboliten 1-PP. Med 5 mg två gånger dagliga doser av buspiron observerades lätta ökningar av AUC för nefazodon (23 %) och dess metaboliter hydroxynefazodon (HO-NEF) (17 %) och meta-klorfenylpiperazin (9 %). Lätt ökning av Cmax observerades för nefazodon (8 %) och dess metabolit HO-NEF (11 %).
Försökspersoner som fick buspiron 5 mg två gånger dagligen och nefazodon 250 mg två gånger dagligen upplevde yrsel, asteni, yrsel och somnolens, biverkningar som också observerades med endera läkemedlet ensamt. Om de två läkemedlen ska användas i kombination rekommenderas en låg dos buspiron (t.ex. 2,5 mg varje dag). Efterföljande dosjustering av båda läkemedlen bör baseras på klinisk bedömning.
Rifampin
I en studie på friska frivilliga, minskade samtidig administrering av buspiron (30 mg som engångsdos) med rifampin (600 mg/dag i 5 dagar) plasmakoncentrationerna (83,7 % minskning av Cmax; 89,6 % minskning av AUC) och farmakodynamiska effekter av buspiron. Om de två läkemedlen ska användas i kombination kan dosen av buspiron behöva justeras för att bibehålla den anxiolytiska effekten.
Andra hämmare och inducerare av CYP3A4
Substanser som hämmar CYP3A4, såsom ketokonazol eller ritonavir, kan hämma buspironmetabolismen och öka plasmakoncentrationerna av buspiron, medan substanser som inducerar CYP3A4, såsom dexametason, eller vissa antikonvulsiva medel (fenytoin, fenobarbital, karbamazepin) kan öka metabolismen av buspiron. Om en patient har titrerats till en stabil dos av buspiron, kan en dosjustering av buspiron vara nödvändig för att undvika biverkningar som kan tillskrivas buspiron eller minskad anxiolytisk aktivitet. Följaktligen, när det administreras med en potent hämmare av CYP3A4, rekommenderas en låg dos av buspiron med försiktighet. När det används i kombination med en potent inducerare av CYP3A4 kan dosen av buspiron behöva justeras för att bibehålla den anxiolytiska effekten.
Andra droger
Cimetidin
Samtidig administrering av buspiron och cimetidin visade sig öka Cmax (40 %) och Tmax (2 gånger), men hade minimal effekt på AUC för buspiron.
Proteinbindning
In vitro ersätter buspiron inte hårt bundna läkemedel som fenytoin, propranolol och warfarin från serumproteiner. Det har dock förekommit en rapport om förlängd protrombintid när buspiron lades till kuren för en patient som behandlats med warfarin. Patienten fick också kroniskt fenytoin, fenobarbital, digoxin och Synthroid®*. In vitro kan buspiron ersätta mindre fast bundna läkemedel som digoxin. Den kliniska betydelsen av denna egenskap är okänd.
Terapeutiska nivåer av aspirin, desipramin, diazepam, flurazepam, ibuprofen, propranolol, tioridazin och tolbutamid hade endast en begränsad effekt på omfattningen av bindningen av buspiron till plasmaproteiner (se KLINISK FARMAKOLOGI ).
Interaktioner med läkemedel/laboratorietest
Buspironhydroklorid kan störa urinmetanefrin/katekolaminanalysen. Det har av misstag lästs som metanefrin under rutinanalyser för feokromocytom, vilket resulterade i ett falskt positivt laboratorieresultat. Buspironhydroklorid bör därför avbrytas i minst 48 timmar innan urinprov tas för katekolaminer.
Narkotikamissbruk och beroende
Kontrollerat ämnesklass
Buspironhydroklorid är inte ett kontrollerat ämne.
Fysiskt och psykologiskt beroende
studier på människor och djur har buspiron inte visat någon potential för missbruk eller avledning och det finns inga bevis för att det orsakar tolerans eller vare sig fysiskt eller psykiskt beroende. Mänskliga frivilliga med en historia av rekreationsdrog- eller alkoholanvändning studerades i två dubbelblinda kliniska undersökningar. Ingen av försökspersonerna kunde skilja mellan buspironhydrokloridtabletter och placebo. Däremot visade försökspersonerna en statistiskt signifikant preferens för metakvalon och diazepam. Studier på apor, möss och råttor har visat att buspiron saknar potential för missbruk. Efter kronisk administrering till råtta, resulterade plötsligt uttag av buspiron inte i den viktminskning som vanligtvis observeras med substanser som orsakar fysiskt beroende.
Även om det inte finns några direkta bevis för att buspironhydrokloridtabletter orsakar fysiskt beroende eller drogsökande beteende, är det svårt att utifrån experiment förutsäga i vilken utsträckning ett CNS-aktivt läkemedel kommer att missbrukas, avledas och/eller missbrukas när det väl marknadsförts. Följaktligen bör läkare noggrant utvärdera patienter med avseende på en historia av drogmissbruk och följa sådana patienter noggrant, observera dem för tecken på missbruk eller missbruk av buspironhydrokloridtabletter (t.ex. utveckling av tolerans, ökning av dosen, läkemedelssökande beteende).
Kontrollerat ämnesklass
Buspironhydroklorid är inte ett kontrollerat ämne.
Fysiskt och psykologiskt beroende
studier på människor och djur har buspiron inte visat någon potential för missbruk eller avledning och det finns inga bevis för att det orsakar tolerans eller vare sig fysiskt eller psykiskt beroende. Mänskliga frivilliga med en historia av rekreationsdrog- eller alkoholanvändning studerades i två dubbelblinda kliniska undersökningar. Ingen av försökspersonerna kunde skilja mellan buspironhydrokloridtabletter och placebo. Däremot visade försökspersonerna en statistiskt signifikant preferens för metakvalon och diazepam. Studier på apor, möss och råttor har visat att buspiron saknar potential för missbruk. Efter kronisk administrering till råtta, resulterade plötsligt uttag av buspiron inte i den viktminskning som vanligtvis observeras med substanser som orsakar fysiskt beroende.
Även om det inte finns några direkta bevis för att buspironhydrokloridtabletter orsakar fysiskt beroende eller drogsökande beteende, är det svårt att utifrån experiment förutsäga i vilken utsträckning ett CNS-aktivt läkemedel kommer att missbrukas, avledas och/eller missbrukas när det väl marknadsförts. Följaktligen bör läkare noggrant utvärdera patienter med avseende på en historia av drogmissbruk och följa sådana patienter noggrant, observera dem för tecken på missbruk eller missbruk av buspironhydrokloridtabletter (t.ex. utveckling av tolerans, ökning av dosen, läkemedelssökande beteende).
VARNINGAR
Administrering av buspironhydrokloridtabletter till en patient som tar en monoaminoxidashämmare (MAO-hämmare) kan utgöra en fara. Det har förekommit rapporter om förekomsten av förhöjt blodtryck när buspironhydrokloridtabletter har lagts till en regim som inkluderar en MAO-hämmare. Därför rekommenderas att buspironhydrokloridtabletter inte används samtidigt med en MAO-hämmare.
Eftersom buspironhydrokloridtabletter inte har någon etablerad antipsykotisk aktivitet, bör de inte användas i stället för lämplig antipsykotisk behandling.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Interferens med kognitiva och motoriska prestanda
Studier tyder på att buspironhydrokloridtabletter är mindre lugnande än andra ångestdämpande medel och att det inte ger någon betydande funktionsnedsättning. Dess CNS-effekter hos en enskild patient kanske inte är förutsägbara. Därför bör patienter varnas för att köra en bil eller använda komplexa maskiner tills de är rimligt säkra på att buspironbehandling inte påverkar dem negativt.
Även om formella studier av interaktionen mellan buspironhydroklorid och alkohol indikerar att buspiron inte ökar alkoholinducerad försämring av motorisk och mental prestation, är det klokt att undvika samtidig användning av alkohol och buspiron.
Potentiell för abstinensreaktioner hos patienter som är beroende av lugnande/hypnotiska/ångestdämpande läkemedel
Eftersom buspironhydrokloridtabletter inte uppvisar korstolerans med bensodiazepiner och andra vanliga sedativa/hypnotiska läkemedel, kommer det inte att blockera abstinenssyndromet som ofta ses vid upphörande av behandlingen med dessa läkemedel. Innan behandling med buspironhydrokloridtabletter påbörjas är det därför tillrådligt att gradvis dra ut patienterna, särskilt patienter som har använt ett CNS-depressivt läkemedel kroniskt, från sin tidigare behandling. Rebound- eller abstinenssymtom kan förekomma under varierande tidsperioder, delvis beroende på typen av läkemedel och dess effektiva halveringstid för eliminering.
Syndromet med abstinens från lugnande/hypnotiska/ångestdämpande läkemedel kan uppträda som vilken kombination som helst av irritabilitet, ångest, agitation, sömnlöshet, tremor, magkramper, muskelkramper, kräkningar, svettning, influensaliknande symtom utan feber och ibland även som anfall .
Möjliga farhågor relaterade till buspirons bindning till dopaminreceptorer
Eftersom buspiron kan binda till centrala dopaminreceptorer har en fråga väckts om dess potential att orsaka akuta och kroniska förändringar i dopaminmedierad neurologisk funktion (t.ex. dystoni, pseudoparkinsonism, akatisi och tardiv dyskinesi). Klinisk erfarenhet av kontrollerade studier har misslyckats med att identifiera någon signifikant neuroleptikaliknande aktivitet; dock har ett syndrom av rastlöshet, som uppträder kort efter påbörjad behandling, rapporterats hos en liten del av buspironbehandlade patienter. Syndromet kan förklaras på flera sätt. Till exempel kan buspiron öka central noradrenerg aktivitet; alternativt kan effekten hänföras till dopaminerga effekter (dvs representerar akatisi). Ser NEGATIVA REAKTIONER : Erfarenhet efter marknadsföring .
Information för patienter
För att säkerställa säker och effektiv användning av buspironhydrokloridtabletter bör följande information och instruktioner ges till patienter:
Informera din läkare om eventuella mediciner, receptbelagda eller receptfria, alkohol eller droger som du nu tar eller planerar att ta under din behandling med buspironhydrokloridtabletter.
Informera din läkare om du är gravid, eller om du planerar att bli gravid, eller om du blir gravid medan du tar buspironhydrokloridtabletter.
Informera din läkare om du ammar ett spädbarn.
Tills du upplever hur denna medicin påverkar dig, kör inte bil eller använd potentiellt farliga maskiner.
Du bör ta buspironhydroklorid konsekvent, antingen alltid med eller alltid utan mat.
Undvik att dricka stora mängder grapefruktjuice under din behandling med buspironhydrokloridtabletter.
Laboratorietester
Det finns inga specifika laboratorietester att rekommendera.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Inga tecken på karcinogen potential observerades hos råttor under en 24 månader lång studie med cirka 133 gånger den maximala rekommenderade orala dosen för människor; eller på möss, under en 18 månader lång studie med cirka 167 gånger den maximala rekommenderade orala dosen för människor.
Med eller utan metabolisk aktivering inducerade buspiron inte punktmutationer i fem stammar av Salmonella typhimurium (Ames Test) eller muslymfom L5178YTK+ cellkulturer, inte heller observerades DNA-skada med buspiron i Wi-38 mänskliga celler. Kromosomavvikelser eller avvikelser förekom inte i benmärgsceller hos möss som fick en eller fem dagliga doser buspiron.
Graviditet
Teratogena effekter
Graviditetskategori B
Ingen fertilitetsförsämring eller fosterskada observerades i reproduktionsstudier utförda på råttor och kaniner vid buspirondoser på cirka 30 gånger den maximala rekommenderade dosen för människor. På människor har dock inte adekvata och välkontrollerade studier under graviditeten utförts. Eftersom reproduktionsstudier på djur inte alltid förutsäger mänskligt svar, bör detta läkemedel endast användas under graviditet om det verkligen behövs.
Arbete och leverans
Effekten av buspironhydroklorid på förlossning och förlossning hos kvinnor är okänd. Inga negativa effekter noterades i reproduktionsstudier på råttor.
Ammande mödrar
Omfattningen av utsöndringen i bröstmjölk av buspiron eller dess metaboliter är inte känd. Hos råttor utsöndras dock buspiron och dess metaboliter i mjölk. Administrering av buspironhydrokloridtabletter till ammande kvinnor bör undvikas om det är kliniskt möjligt.
Pediatrisk användning
Säkerheten och effektiviteten av buspiron utvärderades i två placebokontrollerade 6-veckorsstudier med totalt 559 pediatriska patienter (från 6 till 17 år) med GAD. De studerade doserna var 7,5 mg till 30 mg två gånger dagligen (15 till 60 mg/dag). Det fanns inga signifikanta skillnader mellan buspiron och placebo med avseende på symtomen på GAD efter doser som rekommenderas för behandling av GAD hos vuxna. Farmakokinetiska studier har visat att, för identiska doser, är plasmaexponeringen för buspiron och dess aktiva metabolit, 1-PP, lika med eller högre hos pediatriska patienter än hos vuxna. Inga oväntade säkerhetsfynd associerades med buspiron i dessa studier. Det finns inga långsiktiga säkerhets- eller effektdata i denna population.
Geriatrisk användning
en studie av 6632 patienter som fick buspiron för behandling av ångest var 605 patienter ≥ 65 år och 41 var ≥ 75 år gamla; säkerhets- och effektprofilerna för dessa 605 äldre patienter (medelålder =70,8 år) liknade dem i den yngre populationen (medelålder = 43,3 år). Genomgång av spontant rapporterade biverkningar har inte identifierat skillnader mellan äldre och yngre patienter, men större känslighet hos vissa äldre patienter kan inte uteslutas.
Det fanns inga effekter av ålder på farmakokinetiken för buspiron (se KLINISK FARMAKOLOGI , Särskilda populationer ).
Användning hos patienter med nedsatt lever- eller njurfunktion
Buspiron metaboliseras av levern och utsöndras via njurarna. En farmakokinetisk studie på patienter med nedsatt lever- eller njurfunktion visade ökade plasmanivåer och en förlängd halveringstid för buspiron. Därför kan administrering av buspironhydrokloridtabletter till patienter med gravt nedsatt lever- eller njurfunktion inte rekommenderas (se KLINISK FARMAKOLOGI ).
ÖVERDOS
Ingen information lämnas.
KONTRAINDIKATIONER
Buspironhydrokloridtabletter är kontraindicerade hos patienter som är överkänsliga mot buspironhydroklorid.
KLINISK FARMAKOLOGI
Verkningsmekanismen för buspiron är okänd. Buspiron skiljer sig från typiska bensodiazepiner anxiolytika genom att det inte utövar antikonvulsiva eller muskelavslappnande effekter. Det saknar också den framträdande lugnande effekten som är förknippad med mer typiska anxiolytika. In vitro prekliniska studier har visat att buspiron har hög affinitet för serotonin (5-HT1A) receptorer. Buspiron har ingen signifikant affinitet för bensodiazepinreceptorer och påverkar inte GABA-bindningen in vitro eller in vivo när den testas i prekliniska modeller.
Buspiron har måttlig affinitet för hjärnans D2-dopaminreceptorer. Vissa studier tyder på att buspiron kan ha indirekta effekter på andra signalsubstanser.
Buspironhydroklorid absorberas snabbt hos människor och genomgår omfattande first-pass metabolism. I en radiomärkt studie stod oförändrat buspiron i plasman för endast cirka 1 % av radioaktiviteten i plasman. Efter oral administrering är plasmakoncentrationerna av oförändrat buspiron mycket låga och varierar mellan försökspersoner. Maximala plasmanivåer på 1 ng/ml till 6 ng/ml har observerats 40 till 90 minuter efter orala engångsdoser på 20 mg. Biotillgängligheten för engångsdos av oförändrad buspiron när den tas som tablett är i genomsnitt cirka 90 % av en ekvivalent dos lösning, men det finns stor variation.
Effekterna av mat på biotillgängligheten av buspironhydrokloridtabletter har studerats hos åtta försökspersoner. De fick en dos på 20 mg med och utan mat; arean under plasmakoncentration-tidkurvan (AUC) och maximal plasmakoncentration (Cmax) för oförändrad buspiron ökade med 84 % respektive 116 %, men den totala mängden av buspironimmunreaktivt material förändrades inte. Detta tyder på att mat kan minska graden av presystemisk clearance av buspiron (se DOSERING OCH ADMINISTRERING ).
En flerdosstudie utförd på 15 försökspersoner tyder på att buspiron har olinjär farmakokinetik. Dosökningar och upprepad dosering kan således leda till något högre blodnivåer av oförändrat buspiron än vad som skulle förutsägas från resultat av endosstudier.
En proteinbindningsstudie in vitro visade att cirka 86 % av buspironet är bundet till plasmaproteiner. Det observerades också att aspirin ökade plasmanivåerna av fritt buspiron med 23 %, medan flurazepam minskade plasmanivåerna av fritt buspiron med 20 %. Det är dock inte känt om dessa läkemedel orsakar liknande effekter på plasmanivåerna av fritt buspiron in vivo, eller om sådana förändringar, om de inträffar, orsakar kliniskt signifikanta skillnader i behandlingsresultat. En in vitro-studie visade att buspiron inte undanträngde mycket proteinbundna läkemedel som fenytoin, warfarin och propranolol från plasmaprotein, och att buspiron kan ersätta digoxin.
Buspiron metaboliseras primärt genom oxidation, som in vitro har visat sig förmedlas av cytokrom P450 3A4 (CYP3A4) (se LÄKEMEDELSINTERAKTIONER ). Flera hydroxylerade derivat och en farmakologiskt aktiv metabolit, 1-pyrimidinylpiperazin (1-PP), produceras. I djurmodeller som förutsäger anxiolytisk potential, har 1-PP ungefär en fjärdedel av aktiviteten av buspiron, men är närvarande i upp till 20 gånger större mängder. Men detta är förmodligen inte viktigt för människor: blodprover från människor som kroniskt exponerats för buspironhydroklorid uppvisar inte höga nivåer av 1-PP; medelvärden är cirka 3 ng/ml och den högsta humana blodnivån som registrerats bland 108 kroniskt doserade patienter var 17 ng/ml, mindre än 1/200 av 1-PP-nivåer som hittades hos djur som fått stora doser buspiron utan tecken på toxicitet.
I en endosstudie med 14C-märkt buspiron utsöndrades 29 % till 63 % av dosen i urinen inom 24 timmar, främst som metaboliter; fekal utsöndring stod för 18 % till 38 % av dosen. Den genomsnittliga eliminationshalveringstiden för oförändrat buspiron efter engångsdoser på 10 mg till 40 mg är cirka 2 till 3 timmar.
Särskilda populationer
Ålder och kön effekter
Efter enstaka eller flera doser hos vuxna observerades inga signifikanta skillnader i buspirons farmakokinetik (AUC och Cmax) mellan äldre och yngre försökspersoner eller mellan män och kvinnor.
Nedsatt leverfunktion
Efter flera doser av buspiron till patienter med nedsatt leverfunktion ökade steady-state AUC för buspiron 13 gånger jämfört med friska försökspersoner (se FÖRSIKTIGHETSÅTGÄRDER ).
Nedsatt njurfunktion
Efter flera doser av buspiron till patienter med nedsatt njurfunktion (Clcr = 10 till 70 ml/min/1,73 m2) ökade steady-state AUC för buspiron fyra gånger jämfört med friska (Clcr ≥ 80 ml/min/1,73 m2) försökspersoner (ser FÖRSIKTIGHETSÅTGÄRDER ).
Raseffekter
Effekterna av ras på farmakokinetiken för buspiron har inte studerats.
PATIENTINFORMATION
Buspironhydroklorid Tabletter, USP För 15 mg och 30 mg tabletter
HUR MAN ANVÄNDER
Svaret på buspiron varierar mellan individer. Din läkare kan finna det nödvändigt att justera din dos för att få rätt svar.
Varje tablett är skårad och kan brytas exakt.
För att bryta en tablett exakt och enkelt, håll tabletten mellan tummarna och pekfingrarna nära lämplig tablettskåra (spår). Sedan, med tablettskåran vänd mot dig, tryck och knäpp isär tablettsegmenten (segment som går sönder felaktigt ska inte användas).
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
