Protonix 20mg, 40mg Pantoprazole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Protonix 40mg och hur används det?
Protonix 40mg är ett receptbelagt läkemedel som används för att behandla symtom på esofagit orsakad av magsyra på grund av gastroesofageal refluxsjukdom eller GERD och Zollinger-Ellisons syndrom eller andra tillstånd som orsakar överskott av magsyra. Protonix 40mg kan användas ensamt eller tillsammans med andra läkemedel.
Protonix tillhör en klass av läkemedel som kallas protonpumpshämmare (PPI).
Det är inte känt om Protonix är säkert och effektivt för barn yngre än 5 år.
Vilka är de möjliga biverkningarna av Protonix?
Protonix kan orsaka allvarliga biverkningar, inklusive:
- svåra magsmärtor,
- diarré som är vattnig eller har blod i sig,
- plötslig smärta eller svårighet att röra höften, handleden eller ryggen,
- blåmärken eller svullnad på injektionsstället,
- lite eller ingen urinering,
- blod i urinen,
- svullnad,
- snabb viktökning,
- yrsel,
- snabb eller oregelbunden hjärtfrekvens,
- skakningar (skakningar) eller ryckiga rörelser,
- känner sig orolig,
- muskelkramper eller spasmer i händer eller fötter,
- hosta,
- kvävande känsla,
- ledvärk och
- hudutslag på kinderna eller armarna som förvärras på natten
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Protonix inkluderar:
- huvudvärk,
- yrsel,
- magont,
- gas,
- illamående,
- kräkningar,
- diarre,
- ledvärk,
- feber,
- utslag, och
- förkylningssymtom (vanligast hos barn)
Tala om för din läkare om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Prometrium. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Den aktiva ingrediensen i PROTONIX (pantoprazolnatrium) för oral suspension med fördröjd frisättning och PROTONIX (pantoprazolnatrium) tabletter med fördröjd frisättning, en PPI, är en substituerad bensimidazol, natrium 5-(difluormetoxi)-2-[[(3,4-) dimetoxi-2-pyridinyl)metyl]sulfinyl]-1H-bensimidazolseskvihydrat, en förening som hämmar magsyrasekretion. Dess empiriska formel är C16H14F2N3NaO4S x 1,5 H2O, med en molekylvikt på 432,4. Strukturformeln är:
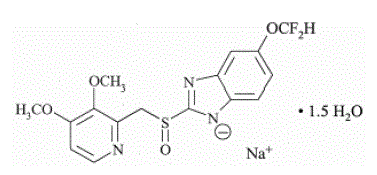
Pantoprazolnatriumseskvihydrat är ett vitt till benvitt kristallint pulver och är racemiskt. Pantoprazol har svagt basiska och sura egenskaper. Pantoprazolnatriumseskvihydrat är fritt lösligt i vatten, mycket svagt lösligt i fosfatbuffert vid pH 7,4 och praktiskt taget olösligt i n-hexan.
Stabiliteten av föreningen i vattenlösning är pH-beroende. Nedbrytningshastigheten ökar med sjunkande pH. Vid rumstemperatur är nedbrytningshalveringstiden cirka 2,8 timmar vid pH 5 och cirka 220 timmar vid pH 7,8.
PROTONIX 40mg levereras som oral suspension för fördröjd frisättning i enhetsdosförpackningar, tillgänglig i en styrka (40 mg) pantoprazol, (motsvarande 45,1 mg pantoprazolnatrium), och som en tablett med fördröjd frisättning, tillgänglig i två styrkor 20 mg pantoprazol (motsvarande 22,56 mg pantoprazolnatrium) och 40 mg pantoprazol (motsvarande 45,1 mg pantoprazolnatrium).
PROTONIX tabletter med fördröjd frisättning innehåller följande inaktiva ingredienser: kalciumstearat, krospovidon, hypromellos, järnoxid, mannitol, metakrylsyrasampolymer, polysorbat 80, povidon, propylenglykol, natriumkarbonat, natriumlaurylsulfat, titandioxidcitrat, och. PROTONIX tabletter med fördröjd frisättning (40 mg och 20 mg) överensstämmer med USP-upplösningstest 2.
PROTONIX 40 mg oral suspension med fördröjd frisättning innehåller följande inaktiva ingredienser: krospovidon, hypromellos, metakrylsyrasampolymer, mikrokristallin cellulosa, polysorbat 80, povidon, natriumkarbonat, natriumlaurylsulfat, talk, titandioxid, trietylferricitratoxid, trietylferricitratoxid.
INDIKATIONER
PROTONIX för oral suspension med fördröjd frisättning och PROTONIX 40 mg tabletter med fördröjd frisättning är indikerade för:
Kortvarig behandling av erosiv esofagit associerad med gastroesofageal refluxsjukdom (GERD)
PROTONIX 20 mg är indicerat för vuxna och pediatriska patienter som är fem år och äldre för korttidsbehandling (upp till 8 veckor) för läkning och symptomatisk lindring av erosiv esofagit (EE). För de vuxna patienter som inte har läkt efter 8 veckors behandling kan ytterligare 8 veckors behandling med PROTONIX övervägas. Säkerhet vid behandling utöver 8 veckor hos pediatriska patienter har inte fastställts.
Underhåll av läkning av erosiv esofagit
PROTONIX är indicerat för underhåll av läkning av EE och minskning av återfallsfrekvensen av symtom på halsbränna dag och natt hos vuxna patienter med GERD. Kontrollerade studier sträckte sig inte längre än 12 månader.
Patologiska hypersekretoriska tillstånd inklusive Zollinger-Ellisons syndrom
PROTONIX 20 mg är indicerat för långtidsbehandling av patologiska hypersekretoriska tillstånd, inklusive Zollinger-Ellison (ZE) syndrom.
DOSERING OCH ADMINISTRERING
Rekommenderat doseringsschema
PROTONIX tillhandahålls som granulat med fördröjd frisättning i förpackningar för beredning av orala suspensioner eller som tabletter med fördröjd frisättning. De rekommenderade doserna anges i tabell 1.
Administrationsinstruktioner
Instruktioner för administreringssätt för varje doseringsform presenteras i tabell 2.
Ta en missad dos så snart som möjligt. Om det nästan är dags för nästa dos, hoppa över den missade dosen och ta nästa dos vid den ordinarie schemalagda tiden. Ta inte 2 doser samtidigt.
PROTONIX tabletter med fördröjd frisättning
Svälj PROTONIX tabletter med fördröjd frisättning hela, med eller utan mat i magen. För patienter som inte kan svälja en 40 mg tablett kan två 20 mg tabletter tas. Samtidig administrering av antacida påverkar inte absorptionen av PROTONIX tabletter med fördröjd frisättning.
PROTONIX för oral suspension med fördröjd frisättning
Administrera PROTONIX för oral suspension med fördröjd frisättning cirka 30 minuter före måltid via oral administrering i äppeljuice eller äppelmos eller enbart nasogastrisk sond i äppeljuice. Eftersom korrekt pH är nödvändigt för stabilitet, administrera inte PROTONIX 20mg för oral suspension med fördröjd frisättning i andra vätskor än äppeljuice, eller annan mat än äppelmos.
Dela inte 40 mg PROTONIX 20 mg oral suspension för fördröjd frisättning för att skapa en 20 mg dos för pediatriska patienter som inte kan ta tablettformuleringen.
PROTONIX för oral suspension med fördröjd frisättning - Oral administrering i äppelmos
- Öppna paketet.
- Strö granulat på en tesked äppelmos. ANVÄND INTE ANNAN LIVSMEDEL ELLER KROSSA ELLER TUGGA GRANULEN.
- Ta inom 10 minuter efter förberedelse.
- Ta klunkar vatten för att se till att granulat sköljs ner i magen. Upprepa vattenklumpar vid behov.
PROTONIX för oral suspension med fördröjd frisättning -Oral administrering i äppeljuice
- Öppna paketet.
- Töm granulat i en liten kopp eller tesked som innehåller en tesked äppeljuice.
- Rör om i 5 sekunder (granulat löses inte upp) och svälj omedelbart.
- För att säkerställa att hela dosen tas, skölj behållaren en eller två gånger med äppeljuice för att ta bort eventuella kvarvarande granulat. Svälj omedelbart.
PROTONIX 40 mg för oral suspension med fördröjd frisättning - Nasogastrisk (NG) slang eller administrering av gastrostomi
För patienter som har en nasogastrisk sond eller gastrostomisond på plats, kan PROTONIX 40 mg för oral suspension med fördröjd frisättning ges enligt följande:
- Ta bort kolven från cylindern på en 2 ounce (60 ml) kateterspetsspruta. Kassera kolven.
- Anslut kateterspetsen på sprutan till ett 16 franskt (eller större) rör.
- Håll sprutan fäst vid slangen så högt som möjligt samtidigt som du ger PROTONIX för fördröjd frisättning oral suspension för att förhindra böjning av slangen.
- Töm innehållet i förpackningen i sprutans cylinder.
- Tillsätt 10 mL (2 teskedar) äppeljuice och knacka försiktigt och/eller skaka sprutans cylinder för att skölja sprutan och tuben. Upprepa minst två gånger till med samma mängd äppeljuice (10 ml eller 2 teskedar) varje gång. Inga granulat ska finnas kvar i sprutan.
HUR LEVERERAS
Doseringsformer och styrkor
Tabletter med fördröjd frisättning:
- 40 mg pantoprazol, gula ovala bikonvexa tabletter präglade med PROTONIX (brunt bläck) på ena sidan
- 20 mg pantoprazol, gula ovala bikonvexa tabletter präglade med P20 (brunt bläck) på ena sidan
För oral suspension med fördröjd frisättning:
- 40 mg pantoprazol, svagt gulaktig till mörkbrunaktig, enterodragerad granulat i en dosförpackning
Förvaring Och Hantering
PROTONIX (pantoprazolnatrium) tabletter med fördröjd frisättning levereras som gula, ovala bikonvexa tabletter med fördröjd frisättning präglade med PROTONIX (brunt bläck) på ena sidan innehållande 40 mg pantoprazol och finns tillgängliga enligt följande:
NDC 0008-0841-81, flaskor med 90 st
PROTONIX (pantoprazolnatrium) tabletter med fördröjd frisättning levereras som gula ovala bikonvexa tabletter med fördröjd frisättning präglade med P20 (brunt bläck) på ena sidan innehållande 20 mg pantoprazol och är tillgängliga enligt följande:
NDC 0008-0843-81, flaskor med 90 st
PROTONIX (pantoprazolnatrium) För oral suspension med fördröjd frisättning levereras som blekt gulaktiga till mörkbruna, enterodragerade granulat innehållande 40 mg pantoprazol i en enhetsdosförpackning och finns tillgängliga enligt följande:
NDC 0008-0844-02, endoskartong med 30 st
Lagring
Förvara PROTONIX 40 mg för oral suspension med fördröjd frisättning och PROTONIX 20 mg tabletter med fördröjd frisättning vid 20° till 25°C (68° till 77°F); utflykter tillåtna till 15° till 30°C (59° till 86°F) [se USP-kontrollerad rumstemperatur ].
Distribuerat av: Wyeth Pharmaceuticals LLC, ett dotterbolag till Pfizer Inc., Philadelphia, PA 19101. Reviderad: nov 2020
BIEFFEKTER
Följande allvarliga biverkningar beskrivs nedan och på andra ställen i märkningen:
- Akut Tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Clostridium difficile-associerad diarré [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kutan och systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Cyanokobalamin (Vitamin B-12) Brist [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypomagnesemi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Fundiska körtelpolyper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Biverkningsprofilerna för PROTONIX (pantoprazolnatrium) för oral suspension med fördröjd frisättning och PROTONIX (pantoprazolnatrium) tabletter med fördröjd frisättning är likartade.
Eftersom kliniska prövningar genomförs under mycket varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i klinisk praxis.
Vuxna
Säkerhet i nio randomiserade jämförande amerikanska kliniska prövningar på patienter med GERD inkluderade 1 473 patienter på oral PROTONIX (20 mg eller 40 mg), 299 patienter på en H2-receptorantagonist, 46 patienter på en annan PPI och 82 patienter på placebo. De vanligast förekommande biverkningarna listas i Tabell 3.
Ytterligare biverkningar som rapporterades för PROTONIX 20 mg i kliniska prövningar med en frekvens på ≤2 % listas nedan per kroppssystem:
Kroppen som helhet: allergisk reaktion, pyrexi, ljuskänslighetsreaktion, ansiktsödem
Gastrointestinala: förstoppning, muntorrhet, hepatit
Hematologiska: leukopeni, trombocytopeni
Metaboliskt/näringsmässigt: förhöjt CK (kreatinkinas), generaliserat ödem, förhöjda triglycerider, förhöjda leverenzymer
Muskuloskeletala: muskelvärk
Nervös: depression, svindel
Hud och bihang: urtikaria, utslag, klåda
Särskilda sinnen: suddig syn
Pediatriska patienter
Säkerheten för PROTONIX vid behandling av EE i samband med GERD utvärderades hos pediatriska patienter i åldrarna 1 år till 16 år i tre kliniska prövningar. Säkerhetsprövningar involverade pediatriska patienter med EE; Men eftersom EE är ovanligt i den pediatriska populationen utvärderades också 249 pediatriska patienter med endoskopiskt bevisad eller symtomatisk GERD. Alla biverkningar hos vuxna på PROTONIX 20 mg anses relevanta för pediatriska patienter. Hos patienter i åldrarna 1 år till 16 år inkluderar de vanligast rapporterade (>4 %) biverkningarna: URI, huvudvärk, feber, diarré, kräkningar, hudutslag och buksmärtor.
För säkerhetsinformation för patienter yngre än 1 år se Användning i specifika populationer .
Ytterligare biverkningar som rapporterades för PROTONIX 20 mg hos pediatriska patienter i kliniska prövningar med en frekvens på ≤4 % listas nedan per kroppssystem:
Kroppen som helhet: allergisk reaktion, ansiktsödem
Gastrointestinala: förstoppning, flatulens, illamående
Metaboliskt/näringsmässigt: förhöjda triglycerider, förhöjda leverenzymer, förhöjt CK (kreatinkinas)
Muskuloskeletala: artralgi, myalgi
Nervös: yrsel, svindel
Hud och bihang: urtikaria
Följande biverkningar som setts hos vuxna i kliniska prövningar rapporterades inte hos pediatriska patienter i kliniska prövningar, men anses relevanta för pediatriska patienter: ljuskänslighetsreaktion, muntorrhet, hepatit, trombocytopeni, generaliserat ödem, depression, klåda, leukopeni och dimsyn .
Zollinger-Ellison (ZE) syndrom
I kliniska studier av ZE-syndrom var biverkningar rapporterade hos 35 patienter som tog PROTONIX 80 mg/dag till 240 mg/dag i upp till 2 år liknande de som rapporterats hos vuxna patienter med GERD.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats under användning av PROTONIX efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Dessa biverkningar listas nedan per kroppssystem:
Gastrointestinala störningar: fundiska körtelpolyper
Allmänna störningar och administrationsförhållanden: asteni, trötthet, sjukdomskänsla
Hematologiska: pancytopeni, agranulocytos
Lever och gallvägar: hepatocellulär skada som leder till gulsot och leversvikt
Immunsystemets störningar: anafylaxi (inklusive anafylaktisk chock), systemisk lupus erythematosus
Infektioner och angrepp: Clostridium difficile associerad diarré
Undersökningar: viktförändringar
Metabolism och näringsstörningar: hyponatremi, hypomagnesemi
Muskuloskeletala sjukdomar: rabdomyolys, benfraktur
Nervös: ageusia, dysgeusia
Psykiatriska störningar: hallucinationer, förvirring, sömnlöshet, somnolens
Njur- och urinvägsstörningar: akut tubulointerstitiell nefrit
Hud och subkutan vävnad: allvarliga dermatologiska reaktioner (vissa dödliga), inklusive erythema multiforme, Stevens-Johnsons syndrom, toxisk epidermal nekrolys (TEN, vissa dödlig), angioödem (Quinckes ödem) och kutan lupus erythematosus
LÄKEMEDELSINTERAKTIONER
Tabell 4 inkluderar läkemedel med kliniskt viktiga läkemedelsinteraktioner och interaktion med diagnostik när de administreras samtidigt med PROTONIX och instruktioner för att förebygga eller hantera dem.
Se märkningen av samtidigt använda läkemedel för att få ytterligare information om interaktioner med PPI.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Förekomst av magmalignitet
Hos vuxna utesluter inte symtomatisk respons på behandling med PROTONIX förekomsten av gastrisk malignitet. Överväg ytterligare uppföljning och diagnostiska tester hos vuxna patienter som har ett suboptimalt svar eller ett tidigt symtomatiskt återfall efter avslutad behandling med PPI. Hos äldre patienter, överväg också en endoskopi.
Akut Tubulointerstitiell nefrit
Akut tubulointerstitiell nefrit (TIN) har observerats hos patienter som tar PPI och kan uppträda när som helst under PPI-behandling. Patienter kan uppvisa olika tecken och symtom från symtomatiska överkänslighetsreaktioner till ospecifika symtom på nedsatt njurfunktion (t.ex. sjukdomskänsla, illamående, anorexi). I rapporterade fallserier diagnostiserades vissa patienter på biopsi och i frånvaro av extrarenala manifestationer (t.ex. feber, hudutslag eller artralgi). Avbryt PROTONIX 20 mg och utvärdera patienter med misstänkt akut TIN [se KONTRAINDIKATIONER ].
Clostridium difficile-associerad diarré
Publicerade observationsstudier tyder på att PPI-behandling som PROTONIX 20 mg kan vara associerad med en ökad risk för Clostridium difficile-associerad diarré, särskilt hos patienter som är inlagda på sjukhus. Denna diagnos bör övervägas för diarré som inte förbättras [se NEGATIVA REAKTIONER ].
Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas.
Benfraktur
Flera publicerade observationsstudier tyder på att PPI-behandling kan vara associerad med en ökad risk för osteoporosrelaterade frakturer i höften, handleden eller ryggraden. Risken för frakturer var ökad hos patienter som fick höga doser, definierade som flera dagliga doser, och långvarig PPI-behandling (ett år eller längre). Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas. Patienter med risk för osteoporosrelaterade frakturer bör hanteras enligt fastställda behandlingsriktlinjer [se DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER ].
Kutan och systemisk lupus erythematosus
Kutan lupus erythematosus (CLE) och systemisk lupus erythematosus (SLE) har rapporterats hos patienter som tar PPI, inklusive pantoprazolnatrium. Dessa händelser har inträffat som både nyuppkomst och förvärring av befintlig autoimmun sjukdom. Majoriteten av PPI-inducerade lupus erytematösa fall var CLE.
Den vanligaste formen av CLE som rapporterats hos patienter som behandlats med PPI var subakut CLE (SCLE) och inträffade inom veckor till år efter kontinuerlig läkemedelsbehandling hos patienter från spädbarn till äldre. I allmänhet observerades histologiska fynd utan organinblandning.
Systemisk lupus erythematosus (SLE) rapporteras mindre vanligt än CLE hos patienter som får PPI. PPI-associerad SLE är vanligtvis mildare än icke-läkemedelsinducerad SLE. Debut av SLE inträffade vanligtvis inom dagar till år efter påbörjad behandling, främst hos patienter från unga vuxna till äldre. Majoriteten av patienterna fick utslag; dock rapporterades också artralgi och cytopeni.
Undvik administrering av PPI under längre tid än vad som är medicinskt indicerat. Om tecken eller symtom som överensstämmer med CLE eller SLE noteras hos patienter som får PROTONIX 40 mg, avbryt läkemedlet och hänvisa patienten till lämplig specialist för utvärdering. De flesta patienter förbättras med avbrytande av enbart PPI inom 4 till 12 veckor. Serologiska tester (t.ex. ANA) kan vara positiva och förhöjda serologiska testresultat kan ta längre tid att lösa än kliniska manifestationer.
Cyanokobalamin (Vitamin B-12) Brist
allmänhet kan daglig behandling med syradämpande mediciner under en lång tidsperiod (t.ex. längre än 3 år) leda till malabsorption av cyanokobalamin (vitamin B-12) orsakad av hypo- eller aklorhydri. Sällsynta rapporter om cyanokobalaminbrist som inträffat vid syrahämmande behandling har rapporterats i litteraturen. Denna diagnos bör övervägas om kliniska symtom som överensstämmer med cyanokobalaminbrist observeras.
Hypomagnesemi
Hypomagnesemi, symtomatisk och asymtomatisk, har rapporterats i sällsynta fall hos patienter som behandlats med PPI under minst tre månader, och i de flesta fall efter ett års behandling. Allvarliga biverkningar inkluderar stelkramp, arytmier och kramper. Hos de flesta patienter krävde behandling av hypomagnesemi magnesiumersättning och avbrytande av PPI.
För patienter som förväntas vara på långvarig behandling eller som tar PPI tillsammans med mediciner som digoxin eller läkemedel som kan orsaka hypomagnesemi (t.ex. diuretika), kan sjukvårdspersonal överväga att övervaka magnesiumnivåerna innan PPI-behandlingen påbörjas och med jämna mellanrum [se NEGATIVA REAKTIONER ].
Tumörframkallande egenskaper
På grund av den kroniska karaktären av GERD kan det finnas en potential för förlängd administrering av PROTONIX. I långtidsstudier på gnagare var pantoprazol karcinogent och orsakade sällsynta typer av gastrointestinala tumörer. Relevansen av dessa fynd för tumörutveckling hos människor är okänd [se Icke-klinisk toxikologi ].
Fundic körtelpolyper
PPI-användning är förknippad med en ökad risk för fundiska körtelpolyper som ökar vid långvarig användning, särskilt efter ett år. De flesta PPI-användare som utvecklade fundic gland polyper var asymtomatiska och fundic gland polyper identifierades tillfälligt vid endoskopi. Använd den kortaste varaktigheten av PPI-behandlingen som är lämplig för det tillstånd som behandlas.
Interferens med undersökningar för neuroendokrina tumörer
Serumkromogranin A (CgA)-nivåer ökar sekundärt till läkemedelsinducerade minskningar i magsyra. Den ökade CgA-nivån kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer. Vårdgivare bör tillfälligt avbryta behandlingen med PROTONIX 20 mg minst 14 dagar innan CgA-nivåerna bedöms och överväga att upprepa testet om de initiala CgA-nivåerna är höga. Om serietest utförs (t.ex. för övervakning), bör samma kommersiella laboratorium användas för testning, eftersom referensintervallen mellan testerna kan variera [se KLINISK FARMAKOLOGI ].
Interferens med urinskärm för THC
Det har förekommit rapporter om falskt positiva urinscreeningstester för tetrahydrocannabinol (THC) hos patienter som fått PPI, inklusive PROTONIX [se LÄKEMEDELSINTERAKTIONER ].
Samtidig användning av PROTONIX med metotrexat
Litteratur tyder på att samtidig användning av PPI med metotrexat (främst i höga doser; se metotrexatförskrivningsinformation) kan höja och förlänga serumnivåerna av metotrexat och/eller dess metabolit, vilket kan leda till metotrexattoxicitet. Vid administrering av högdos metotrexat kan ett tillfälligt utsättande av PPI övervägas hos vissa patienter [se LÄKEMEDELSINTERAKTIONER ].
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide och bruksanvisning ).
Magmalignitet
Råda patienterna att återvända till sin vårdgivare om de har ett suboptimalt svar eller ett tidigt symtomatiskt återfall [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Akut Tubulointerstitiell nefrit
Rekommendera patienter att omedelbart ringa sin vårdgivare om de upplever tecken och/eller symtom associerade med akut tubulointerstitiell nefrit [se KONTRAINDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Clostridium Difficile-associerad diarré
Råda patienter att omedelbart ringa sin vårdgivare om de upplever diarré som inte förbättras [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Benfraktur
Rekommendera patienter att rapportera eventuella frakturer, särskilt på höften, handleden eller ryggraden, till sin vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kutan och systemisk lupus erythematosus
Rekommendera patienter att omedelbart ringa sin vårdgivare för alla nya eller försämrade symtom associerade med kutan eller systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Cyanokobalamin (Vitamin B-12) Brist
Rekommendera patienter att rapportera eventuella kliniska symtom som kan vara associerade med cyankobalaminbrist till sin vårdgivare om de har fått PROTONIX 40 mg i mer än 3 år [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hypomagnesemi
Rekommendera patienter att rapportera eventuella kliniska symtom som kan vara associerade med hypomagnesemi till sin vårdgivare, om de har fått PROTONIX 40 mg i minst 3 månader [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Läkemedelsinteraktioner
Instruera patienterna att informera sin vårdgivare om alla andra mediciner de för närvarande tar, inklusive produkter som innehåller rilpivirin [se KONTRAINDIKATIONER ] digoxin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ] och högdos metotrexat [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Graviditet
Informera en gravid kvinna om den potentiella risken för ett foster. Rekommendera kvinnor med reproduktionspotential att informera sin vårdgivare om en känd eller misstänkt graviditet [se Användning i specifika populationer ].
Administrering
- Dela, krossa eller tugga inte PROTONIX For Oral Suspension med fördröjd frisättning och PROTONIX 20 mg tabletter med fördröjd frisättning.
- PROTONIX oral suspensionsförpackning är en fast dos och kan inte delas för att göra en mindre dos.
- Svälj PROTONIX 20 mg tabletter med fördröjd frisättning hela, med eller utan mat i magen.
- Samtidig administrering av antacida påverkar inte absorptionen av PROTONIX tabletter med fördröjd frisättning.
- Ta PROTONIX 20 mg för oral suspension med fördröjd frisättning cirka 30 minuter före måltid.
- Administrera PROTONIX för oral suspension med fördröjd frisättning i äppeljuice eller äppelmos, enligt beskrivningen i bruksanvisningen. Administrera inte i vatten, andra vätskor eller livsmedel.
- För patienter med nasogastrisk (NG) eller gastrostomisond kan PROTONIX For Delayed-Release Oral Suspension administreras med äppeljuice, enligt beskrivningen i bruksanvisningen.
- Ta en missad dos så snart som möjligt. Om det nästan är dags för nästa dos, hoppa över den missade dosen och ta nästa dos vid den ordinarie schemalagda tiden. Ta inte 2 doser samtidigt.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
en 24-månaders karcinogenicitetsstudie behandlades Sprague-Dawley-råttor oralt med pantoprazoldoser på 0,5 till 200 mg/kg/dag, cirka 0,1 till 40 gånger exponeringen på kroppsytabasis för en 50 kg person doserad med 40 mg /dag. I magfundus gav behandling med 0,5 till 200 mg/kg/dag enterokromaffinliknande (ECL) cellhyperplasi och benigna och maligna neuroendokrina celltumörer på ett dosrelaterat sätt. I förmagen gav behandling med 50 och 200 mg/kg/dag (cirka 10 och 40 gånger den rekommenderade humana dosen på basis av kroppsyta) godartade skivepitelcellspapillom och maligna skivepitelcancer. Sällsynta gastrointestinala tumörer associerade med pantoprazolbehandling inkluderade ett adenokarcinom i tolvfingertarmen med 50 mg/kg/dag och benigna polyper och adenokarcinom i magfundus med 200 mg/kg/dag. I levern gav behandling med 0,5 till 200 mg/kg/dag dosrelaterade ökningar av förekomsten av hepatocellulära adenom och karcinom. I sköldkörteln gav behandling med 200 mg/kg/dag ökade förekomster av follikulära celladenom och karcinom för både han- och honråttor.
en 24-månaders karcinogenicitetsstudie behandlades Fischer 344-råttor oralt med doser på 5 till 50 mg/kg/dag av pantoprazol, ungefär 1 till 10 gånger den rekommenderade dosen för människor baserat på kroppsyta. I magfundus producerade behandling med 5 till 50 mg/kg/dag enterokromaffinliknande (ECL) cellhyperplasi och benigna och maligna neuroendokrina celltumörer. Val av dos för denna studie kanske inte var adekvat för att heltäckande utvärdera den karcinogena potentialen hos pantoprazol.
I en 24-månaders karcinogenicitetsstudie behandlades B6C3F1-möss oralt med doser på 5 till 150 mg/kg/dag av pantoprazol, 0,5 till 15 gånger den rekommenderade dosen för människor baserat på kroppsyta. I levern gav behandling med 150 mg/kg/dag ökade förekomster av hepatocellulära adenom och karcinom hos honmöss. Behandling med 5 till 150 mg/kg/dag gav också gastrisk-fundisk ECL-cellhyperplasi.
En 26-veckors p53 +/-transgen muskarcinogenicitetsstudie var inte positiv.
Pantoprazol var positivt i in vitro-analyser av humana lymfocyter av kromosomavvikelser, i ett av två mikrokärntest på mus för klastogena effekter, och i in vitro analysen av äggstocksceller från kinesisk hamster/HGPRT framåtmutation för mutagena effekter. Tvetydiga resultat observerades i in vivo-testet för kovalent bindning av DNA från råttlever. Pantoprazol var negativ i Ames-mutationsanalysen in vitro, in vitro-analysen av oplanerad DNA-syntes (UDS) med råtthepatocyter, in vitro AS52/GPT-genmutationsanalysen för däggdjursceller framåt, tymidinkinasmutationstestet in vitro med muslymfom L5178Y celler och in vivo råttbenmärgscellskromosomavvikelseanalysen.
Det fanns inga effekter på fertilitet eller reproduktionsförmåga när pantoprazol gavs i orala doser upp till 500 mg/kg/dag till hanråttor (98 gånger den rekommenderade dosen för människa baserat på kroppsyta) och 450 mg/kg/dag till honråttor. (88 gånger den rekommenderade humandosen baserat på kroppsyta).
Användning i specifika populationer
Graviditet
Risksammanfattning
Tillgängliga data från publicerade observationsstudier visade inte ett samband mellan allvarliga missbildningar eller andra negativa graviditetsresultat med pantoprazol.
I reproduktionsstudier på djur observerades inga tecken på negativa utvecklingsresultat med pantoprazol. Reproduktionsstudier har utförts på råttor vid orala doser upp till 450 mg/kg/dag (cirka 88 gånger den rekommenderade humandosen) och kaniner vid orala doser upp till 40 mg/kg/dag (ca 16 gånger den rekommenderade humandosen) med administrering av pantoprazol under organogenes hos dräktiga djur och har inte visat några tecken på skada på fostret på grund av pantoprazol i denna studie (se Data ).
En toxicitetsstudie för pre- och postnatal utveckling på råttor med ytterligare endpoints för att utvärdera effekten på benutvecklingen utfördes med pantoprazolnatrium. Orala pantoprazoldoser på 5, 15 och 30 mg/kg/dag (ungefär 1, 3 och 6 gånger den mänskliga dosen på 40 mg/dag) administrerades till gravida kvinnor från dräktighetsdagen (GD) 6 till och med amningsdagen (LD) ) 21. Förändringar i benmorfologi observerades hos ungar exponerade för pantoprazol in utero och genom mjölk under laktationsperioden samt genom oral dosering från postnatal dag (PND) 4 till PND 21 [se Användning i specifika populationer ]. Det fanns inga läkemedelsrelaterade fynd hos moderns djur. Informera gravida kvinnor om den potentiella risken för fosterskador.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i de kliniskt erkända graviditeterna 2 till 4 % respektive 15 till 20 %.
Data
Mänskliga data
Tillgängliga data från publicerade observationsstudier kunde inte visa ett samband mellan negativa graviditetsrelaterade utfall och användning av pantoprazol. Metodologiska begränsningar av dessa observationsstudier kan inte definitivt fastställa eller utesluta någon läkemedelsrelaterad risk under graviditet. I en prospektiv studie av European Network of Teratology Information Services, jämfördes resultaten från en grupp på 53 gravida kvinnor som administrerades dagliga mediandoser på 40 mg pantoprazol med en kontrollgrupp på 868 gravida kvinnor som inte tog några protonpumpshämmare (PPI) . Det fanns ingen skillnad i frekvensen av större missbildningar mellan kvinnor exponerade för PPI och kontrollgruppen, motsvarande en relativ risk (RR)=0,55, [95 % konfidensintervall (CI) 0,08-3,95]. I en populationsbaserad retrospektiv kohortstudie som täckte alla levande födda i Danmark från 1996 till 2008, fanns det ingen signifikant ökning av större fosterskador under analys av första trimesterns exponering för pantoprazol hos 549 levande barn. En metaanalys som jämförde 1 530 gravida kvinnor exponerade för PPI åtminstone under första trimestern med 133 410 oexponerade gravida kvinnor visade ingen signifikant ökning av risken för medfödda missbildningar eller spontan abort med exponering för PPI (för större missbildningar OR=1,12 ([95 %) KI 0,86-1,45] och för spontanaborter OR=1,29 [95% KI 0,84-1,97]).
Djurdata
Reproduktionsstudier har utförts på råttor med orala pantoprazoldoser upp till 450 mg/kg/dag (ca 88 gånger den rekommenderade dosen för människa baserat på kroppsyta) och på kaniner vid orala doser upp till 40 mg/kg/dag (ca 16 gånger den rekommenderade humana dosen baserat på kroppsyta) med administrering av pantoprazolnatrium under organogenes hos dräktiga djur. Studierna har inte avslöjat några tecken på försämrad fertilitet eller skada på fostret på grund av pantoprazol.
En toxicitetsstudie för pre- och postnatal utveckling på råttor med ytterligare endpoints för att utvärdera effekten på benutvecklingen utfördes med pantoprazolnatrium. Orala pantoprazoldoser på 5, 15 och 30 mg/kg/dag (ungefär 1, 3 och 6 gånger den mänskliga dosen på 40 mg/dag på basis av kroppsyta) administrerades till gravida kvinnor från och med dräktighetsdagen (GD) 6 till och med laktationsdag (LD) 21. På postnatal dag (PND 4) till PND 21, administrerades ungarna orala doser på 5, 15 och 30 mg/kg/dag (ungefär 1, 2,3 och 3,2 gånger exponeringen ( AUC) hos människor i en dos på 40 mg). Det fanns inga läkemedelsrelaterade fynd hos moderns djur. Under doseringsfasen före avvänjningen (PND 4 till 21) av ungarna, var det ökad mortalitet och/eller dödlighet och minskad kroppsvikt och kroppsviktsökning vid 5 mg/kg/dag (ungefär lika exponeringar (AUC) hos människor som fick de 40 mg dos) och högre doser. På PND 21 observerades minskad genomsnittlig lårbenslängd och vikt och förändringar i lårbensbenmassa och geometri hos avkomman vid 5 mg/kg/dag (ungefär lika exponeringar (AUC) hos människor vid dosen 40 mg) och högre doser. Fynden av lårbenet inkluderade lägre total yta, benmineralinnehåll och -densitet, periosteal och endosteal omkrets och tvärsnitts tröghetsmoment. Det fanns inga mikroskopiska förändringar i det distala lårbenet, proximala skenbenet eller kvävlederna. Förändringar i benparametrar var delvis reversibla efter en återhämtningsperiod, med fynd på PND 70 begränsade till lägre lårbensmetafys kortikal/subkortikal bentäthet hos honungar vid 5 mg/kg/dag (ungefär lika exponeringar (AUC) hos människor vid 40 mg dos) och högre doser.
Laktation
Risksammanfattning
Pantoprazol har upptäckts i bröstmjölk hos en ammande mamma efter en oral engångsdos på 40 mg pantoprazol. Det fanns inga effekter på det ammade barnet (se Data ). Det finns inga data om pantoprazols effekter på mjölkproduktionen.

Utvecklings- och hälsofördelarna med amning bör beaktas tillsammans med moderns kliniska behov av PROTONIX 40 mg och eventuella negativa effekter på det ammade barnet från pantoprazol eller från det underliggande moderns tillståndet.
Data
Bröstmjölken hos en 42-årig kvinna som fick 40 mg oral pantoprazol, 10 månader efter förlossningen, studerades under 24 timmar för att påvisa låga nivåer av pantoprazol i bröstmjölken. Pantoprazol kunde detekteras i mjölk endast 2 och 4 timmar efter dosen med mjölknivåer på cirka 36 mcg/L respektive 24 mcg/L. Ett förhållande mellan mjölk och plasma på 0,022 observerades 2 timmar efter läkemedelsadministrering. Pantoprazol kunde inte detekteras (
Pediatrisk användning
Säkerheten och effektiviteten av PROTONIX för korttidsbehandling (upp till åtta veckor) av EE i samband med GERD har fastställts hos pediatriska patienter i åldern 1 till 16 år. Effektivitet för EE har inte visats hos patienter yngre än 1 år. Dessutom, för patienter under 5 år, finns det ingen lämplig doseringsstyrka i en åldersanpassad formulering tillgänglig. Därför är PROTONIX indicerat för korttidsbehandling av EE i samband med GERD för patienter 5 år och äldre. Säkerheten och effektiviteten av PROTONIX för andra pediatriska användningar än EE har inte fastställts.
1 år till 16 års ålder
Användning av PROTONIX hos pediatriska patienter i åldern 1 till 16 år för korttidsbehandling (upp till åtta veckor) av EE i samband med GERD stöds av: a) extrapolering av resultat från adekvata och välkontrollerade studier som stödde godkännandet av PROTONIX för behandling av EE associerat med GERD hos vuxna, och b) säkerhets-, effektivitets- och farmakokinetiska studier utförda på pediatriska patienter [se Kliniska studier , KLINISK FARMAKOLOGI ].
Säkerheten för PROTONIX 40 mg vid behandling av EE associerad med GERD hos pediatriska patienter i åldern 1 till 16 år utvärderades i tre multicenter, randomiserade, dubbelblinda, parallella behandlingsstudier, som involverade 249 pediatriska patienter, inklusive 8 med EE (4 patienter) åldrarna 1 år till 5 år och 4 patienter 5 år till 11 år). Barnen i åldrarna 1 år till 5 år med endoskopiskt diagnostiserad EE (definierad som en endoskopisk Hetzel-Dent-poäng ≥2) behandlades en gång dagligen i 8 veckor med en av två dosnivåer av PROTONIX (ungefär 0,6 mg/kg eller 1,2 mg/kg ). Alla 4 av dessa patienter med EE var helade (Hetzel-Dent-poäng på 0 eller 1) efter 8 veckor. Eftersom EE är ovanligt i den pediatriska populationen inkluderades även övervägande pediatriska patienter med endoskopiskt bevisad eller symtomatisk GERD i dessa studier. Patienterna behandlades med olika doser av PROTONIX 20 mg en gång dagligen i 8 veckor. För säkerhetsresultat se NEGATIVA REAKTIONER Eftersom dessa pediatriska studier inte hade någon placebo, aktiv jämförelse eller tecken på dossvar, var prövningarna osäkra angående den kliniska nyttan av PROTONIX 20 mg för symtomatisk GERD i den pediatriska populationen. Effektiviteten av PROTONIX 40 mg för behandling av symtomatisk GERD hos pediatriska patienter har inte fastställts.
Även om data från de kliniska prövningarna stöder användning av PROTONIX för korttidsbehandling av EE i samband med GERD hos pediatriska patienter 1 år till 5 år, finns det ingen kommersiellt tillgänglig dosformulering lämplig för patienter under 5 år [se DOSERING OCH ADMINISTRERING ].
en populationsfarmakokinetisk analys hade clearance-värdena hos barn 1 till 5 år gamla med endoskopiskt påvisad GERD ett medianvärde på 2,4 l/h. Efter en ekvivalent dos på 1,2 mg/kg (15 mg för ≤12,5 kg och 20 mg för >12,5 till
Nyfödda till mindre än ett års ålder
PROTONIX 20 mg visade sig inte vara effektivt i en multicenter, randomiserad, dubbelblind, placebokontrollerad, behandlingsutsättningsstudie av 129 pediatriska patienter i åldern 1 till 11 månader. Patienter inkluderades om de hade symtomatisk GERD baserat på medicinsk historia och inte hade svarat på icke-farmakologiska interventioner för GERD under två veckor. Patienterna fick PROTONIX dagligen i fyra veckor i en öppen fas, därefter randomiserades patienterna i lika stor andel för att få PROTONIX 40 mg behandling eller placebo under de efterföljande fyra veckorna på ett dubbelblindt sätt. Effekten utvärderades genom att observera tiden från randomisering till studieavbrott på grund av symtomförsämring under den fyra veckor långa behandlings- och utsättningsfasen. Det fanns ingen statistiskt signifikant skillnad mellan PROTONIX 20 mg och placebo i graden av utsättning.
denna studie var de biverkningar som rapporterades vanligare (skillnad på ≥4%) i den behandlade populationen jämfört med placebopopulationen förhöjd CK, otitis media, rinit och laryngit.
I en populationsfarmakokinetisk analys var den systemiska exponeringen högre hos patienter yngre än 1 år med GERD jämfört med vuxna som fick en engångsdos på 40 mg (geometriskt medelvärde för AUC var 103 % högre hos prematura spädbarn och nyfödda som fick en engångsdos på 2,5 mg av PROTONIX och 23 % högre hos spädbarn i åldern 1 till 11 månader som får en engångsdos på cirka 1,2 mg/kg). Hos dessa patienter ökade det skenbara clearance (CL/F) med åldern (medianclearance: 0,6 l/timme, intervall: 0,03 till 3,2 l/timme).
Dessa doser resulterade i farmakodynamiska effekter på magsäckens men inte matstrupens pH. Efter dosering en gång dagligen av 2,5 mg PROTONIX 20 mg till för tidigt födda spädbarn och nyfödda, skedde en ökning av det genomsnittliga pH-värdet i magsäcken (från 4,3 vid baslinjen till 5,2 vid steady-state) och i den genomsnittliga tiden som magsäckens pH var > 4 ( från 60 % vid baslinjen till 80 % vid steady-state). Efter dosering en gång dagligen av cirka 1,2 mg/kg PROTONIX 20 mg till spädbarn i åldern 1 till 11 månader, skedde en ökning av det genomsnittliga pH-värdet i magsäcken (från 3,1 vid baslinjen till 4,2 vid steady-state) och i den genomsnittliga tiden som magsäckens pH var > 4 (från 32 % vid baslinjen till 60 % vid steady-state). Emellertid observerades inga signifikanta förändringar i genomsnittligt intraesofagealt pH eller % tid som matstrupens pH var
Eftersom PROTONIX 20 mg inte visades vara effektivt i den randomiserade, placebokontrollerade studien i denna åldersgrupp, är användning av PROTONIX för behandling av symtomatisk GERD hos spädbarn yngre än 1 år inte indicerat.
Djurtoxicitetsdata
I en pre- och postnatal utvecklingsstudie på råttor, administrerades ungarna orala doser av pantoprazol på 5, 15 och 30 mg/kg/dag (ungefär 1, 2,3 och 3,2 gånger exponeringen (AUC) hos barn i åldern 6 till 11 år vid en dos på 40 mg) på postnatal dag (PND 4) till och med PND 21, förutom amningsexponering genom mjölk. På PND 21 observerades minskad genomsnittlig lårbenslängd och vikt och förändringar i lårbensbenmassa och geometri hos avkomman vid 5 mg/kg/dag (ungefär lika exponeringar (AUC) hos barn i åldrarna 6 till 11 år vid dosen 40 mg) och högre doser. Förändringar i benparametrar var delvis reversibla efter en återhämtningsperiod.
Hos neonatala/juvenila djur (råttor och hundar) var toxiciteten liknande den som observerats hos vuxna djur, inklusive magförändringar, minskning av röda blodkroppar, ökningar av lipider, enzyminduktion och hepatocellulär hypertrofi. En ökad förekomst av eosinofila huvudceller hos vuxna och neonatala/juvenila råttor, och atrofi av huvudceller hos vuxna råttor och hos neonatala/juvenila hundar, observerades i magslemhinnan i magsäcken i studier med upprepade doser. Full till partiell återhämtning av dessa effekter noterades hos djur i båda åldersgrupperna efter en återhämtningsperiod.
Geriatrisk användning
I kortsiktiga kliniska prövningar i USA var EE-läkningsfrekvensen hos de 107 äldre patienter (≥65 år) som behandlades med PROTONIX liknande de som hittades hos patienter under 65 år. Incidensfrekvensen av biverkningar och laboratorieavvikelser hos patienter i åldern 65 år och äldre liknade de som associerades med patienter yngre än 65 år.
ÖVERDOS
Erfarenhet av patienter som tar mycket höga doser av PROTONIX (större än 240 mg) är begränsad. Spontana rapporter om överdosering efter marknadsföring ligger i allmänhet inom den kända säkerhetsprofilen för PROTONIX.
Pantoprazol avlägsnas inte genom hemodialys. Vid överdosering bör behandlingen vara symptomatisk och stödjande.
Enstaka orala doser av pantoprazol på 709 mg/kg, 798 mg/kg och 887 mg/kg var dödliga för möss, råttor respektive hundar. Symtomen på akut toxicitet var hypoaktivitet, ataxi, böjt sittande, lemspinning, sidoläge, segregation, frånvaro av öronreflex och tremor.
Om överexponering för PROTONIX 20 mg inträffar, ring ditt giftkontrollcenter på 1-800-222-1222 för aktuell information om hantering av förgiftning eller överdosering.
KONTRAINDIKATIONER
- PROTONIX är kontraindicerat hos patienter med känd överkänslighet mot någon komponent i formuleringen eller någon substituerad bensimidazol. Överkänslighetsreaktioner kan inkludera anafylaxi, anafylaktisk chock, angioödem, bronkospasm, akut tubulointerstitiell nefrit och urtikaria [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
- Protonpumpshämmare (PPI), inklusive PROTONIX, är kontraindicerade hos patienter som får produkter som innehåller rilpivirin [se LÄKEMEDELSINTERAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Pantoprazol är en PPI som undertrycker det sista steget i magsyraproduktionen genom att kovalent binda till enzymsystemet (H+, K+)-ATPas vid den sekretoriska ytan av magparietalcellen. Denna effekt leder till hämning av både basal och stimulerad magsyrasekretion, oavsett stimulans. Bindningen till (H+, K+)-ATPas resulterar i en varaktighet av antisekretorisk effekt som kvarstår längre än 24 timmar för alla testade doser (20 mg till 120 mg).
Farmakodynamik
PROTONIX 20 mg för oral suspension med fördröjd frisättning, 40 mg har visats vara jämförbar med PROTONIX tabletter med fördröjd frisättning när det gäller att undertrycka pentagastrinstimulerad MAO hos patienter (n = 49) med GERD och en historia av EE. I denna multicenter, farmakodynamiska crossover-studie jämfördes en 40 mg oral dos av PROTONIX för oral suspension med fördröjd frisättning administrerad i en tesked äppelmos med en 40 mg oral dos av PROTONIX tabletter med fördröjd frisättning efter administrering av varje formulering en gång dagligen i 7 dagar. Båda medicinerna administrerades trettio minuter före frukost. Pentagastrinstimulerad (MAO) bedömdes från timme 23 till 24 vid steady state.
Antisekretorisk aktivitet
Under maximala syrastimulerande förhållanden med pentagastrin inträffar en dosberoende minskning av magsyraproduktionen efter en engångsdos av oral (20-80 mg) eller en enstaka dos av intravenös (20-120 mg) pantoprazol hos friska försökspersoner. Pantoprazol givet en gång dagligen resulterar i ökad hämning av magsyrasekretionen. Efter den initiala orala dosen på 40 mg pantoprazol uppnåddes en genomsnittlig hämning på 51 % efter 2,5 timmar. Med dosering en gång om dagen i 7 dagar ökade den genomsnittliga hämningen till 85 %. Pantoprazol undertryckte syrasekretionen med över 95 % hos hälften av försökspersonerna. Syrautsöndringen hade återgått till det normala inom en vecka efter den sista dosen av pantoprazol; det fanns inga tecken på rebound hypersekretion.
en serie dos-respons-studier orsakade pantoprazol, vid orala doser från 20 till 120 mg, dosrelaterade ökningar av median basalt pH i magen och i procent av tiden gastriskt pH var >3 och >4. Behandling med 40 mg pantoprazol gav signifikant större ökningar i magsäckens pH än dosen på 20 mg. Doser högre än 40 mg (60, 80, 120 mg) resulterade inte i ytterligare signifikanta ökningar av median mag-pH. Effekterna av pantoprazol på median-pH från en dubbelblind överkorsningsstudie visas i tabell 5.
Serum Gastrin Effekter
Fastande gastrinnivåer i serum bedömdes i två dubbelblinda studier av akut läkning av EE där 682 patienter med gastroesofageal refluxsjukdom (GERD) fick 10, 20 eller 40 mg PROTONIX 20 mg i upp till 8 veckor. Vid 4 veckors behandling skedde en ökning av genomsnittliga gastrinnivåer med 7 %, 35 % och 72 % jämfört med förbehandlingsvärdena i behandlingsgrupperna på 10, 20 respektive 40 mg. En liknande ökning av gastrinnivåer i serum noterades vid det 8 veckor långa besöket med genomsnittliga ökningar på 3 %, 26 % och 84 % för de tre dosgrupperna för pantoprazol. Medianhalten av gastrin i serum förblev inom normala gränser under underhållsbehandling med PROTONIX tabletter med fördröjd frisättning.
internationella långtidsstudier som involverade över 800 patienter observerades en 2- till 3-faldig genomsnittlig ökning från gastrinnivån i fastande serum för behandling under de första månaderna av behandling med pantoprazol i doser på 40 mg per dag under GERD-underhållsstudier och 40 mg eller högre per dag hos patienter med refraktär GERD. Fastande gastrinnivåer i serum förblev i allmänhet cirka 2 till 3 gånger baslinjen under upp till 4 års periodisk uppföljning i kliniska prövningar.
Efter korttidsbehandling med PROTONIX 20 mg återgår förhöjda gastrinnivåer till det normala efter minst 3 månader.
Enterokromaffinliknande (ECL) celleffekter
Hos 39 patienter som behandlades med oral pantoprazol 40 mg till 240 mg dagligen (majoriteten fick 40 mg till 80 mg) i upp till 5 år, var det en måttlig ökning av ECL-celltätheten, med början efter det första året av användning, vilket verkade platå efter 4 år.
en icke-klinisk studie på Sprague-Dawley-råttor resulterade livstidsexponering (24 månader) för pantoprazol i doser på 0,5 till 200 mg/kg/dag i dosrelaterade ökningar av gastrisk ECL-cellproliferation och gastriska neuroendokrina (NE)-celltumörer . Gastriska NE-cellstumörer hos råttor kan bero på kroniska förhöjda gastrinkoncentrationer i serum. Den höga tätheten av ECL-celler i råttmagen gör denna art mycket mottaglig för de proliferativa effekterna av förhöjda gastrinkoncentrationer som produceras av PPI. Det observerades dock inga förhöjningar av serumgastrin efter administrering av pantoprazol i en dos på 0,5 mg/kg/dag. I en separat studie observerades en gastrisk NE-cellstumör utan samtidiga ECL-cellsproliferativa förändringar hos 1 honråtta efter 12 månaders dosering med pantoprazol med 5 mg/kg/dag och 9 månaders återhämtning utanför dosen [se Icke-klinisk toxikologi ].
Endokrina effekter
en klinisk farmakologisk studie hade PROTONIX 40 mg givet en gång dagligen i 2 veckor ingen effekt på nivåerna av följande hormoner: kortisol, testosteron, trijodtyronin (T3), tyroxin (T4), sköldkörtelstimulerande hormon (TSH), tyronin- bindande protein, bisköldkörtelhormon, insulin, glukagon, renin, aldosteron, follikelstimulerande hormon, luteiniserande hormon, prolaktin och tillväxthormon.
I en 1-årig studie av GERD-patienter som behandlats med PROTONIX 40 mg eller 20 mg, förekom inga förändringar från baslinjen i de totala nivåerna av T3, T4 och TSH.
Farmakokinetik
PROTONIX 40 mg tabletter med fördröjd frisättning framställs som magsaftresistenta tabletter så att absorptionen av pantoprazol börjar först efter att tabletten lämnat magsäcken. Maximal serumkoncentration (Cmax) och arean under serumkoncentrationstidskurvan (AUC) ökar på ett sätt som är proportionellt mot orala och intravenösa doser från 10 mg till 80 mg. Pantoprazol ackumuleras inte och dess farmakokinetik är oförändrad vid flera dagliga doser. Efter oral eller intravenös administrering sjunker serumkoncentrationen av pantoprazol biexponentiellt, med en terminal halveringstid på cirka en timme.
Hos extensiva metaboliserare med normal leverfunktion som får en oral dos av den enterodragerade 40 mg pantoprazoltabletten är toppkoncentrationen (Cmax) 2,5 μg/ml; tiden för att nå toppkoncentrationen (tmax) är 2,5 timmar, och den genomsnittliga totala arean under kurvan för plasmakoncentration kontra tid (AUC) är 4,8 μg•h/mL (intervall 1,4 till 13,3 μg•h/mL). Efter intravenös administrering av pantoprazol till omfattande metaboliserare är dess totala clearance 7,6-14,0 l/h och dess skenbara distributionsvolym är 11,0-23,6 l.
En oral engångsdos av PROTONIX för oral suspension med fördröjd frisättning, 40 mg, visade sig vara bioekvivalent när den administrerades till friska försökspersoner (N = 22) som granulat strödda över en tesked äppelmos, som granulat blandat med äppeljuice, eller blandat med äppeljuice följt av administrering genom en nasogastrisk sond. De farmakokinetiska plasmaparametrarna från en crossover-studie på friska försökspersoner sammanfattas i tabell 6.
Absorption
Efter administrering av en enstaka eller flera orala 40 mg doser av PROTONIX 20 mg tabletter med fördröjd frisättning uppnåddes den maximala plasmakoncentrationen av pantoprazol på cirka 2,5 timmar och Cmax var 2,5 μg/ml. Pantoprazol genomgår liten first-pass-metabolism, vilket resulterar i en absolut biotillgänglighet på cirka 77 %. Pantoprazols absorption påverkas inte av samtidig administrering av antacida.
Administrering av PROTONIX tabletter med fördröjd frisättning med mat kan fördröja dess absorption upp till 2 timmar eller längre; Cmax och graden av pantoprazolabsorption (AUC) förändras dock inte. Således kan PROTONIX 40 mg tabletter med fördröjd frisättning tas utan hänsyn till tidpunkten för måltiderna.
Administrering av pantoprazolgranulat, 40 mg, tillsammans med en måltid med hög fetthalt fördröjde mediantiden till maximal plasmakoncentration med 2 timmar. Med en samtidig måltid med hög fetthalt minskade Cmax och AUC för pantoprazolgranulat, 40 mg, stänkt på äppelmos med 51 % respektive 29 %. Därför bör PROTONIX 20 mg för fördröjd frisättning oral suspension tas cirka 30 minuter före måltid.
Distribution
Den skenbara distributionsvolymen för pantoprazol är cirka 11 till 23,6 L, fördelad huvudsakligen i extracellulär vätska. Serumproteinbindningen av pantoprazol är cirka 98 %, främst till albumin.
Eliminering
Ämnesomsättning
Pantoprazol metaboliseras i stor utsträckning i levern genom cytokrom P450 (CYP)-systemet. Pantoprazols metabolism är oberoende av administreringssättet (intravenöst eller oralt). Den huvudsakliga metaboliska vägen är demetylering, genom CYP2C19, med efterföljande sulfatering; andra metabola vägar inkluderar oxidation av CYP3A4. Det finns inga bevis för att någon av pantoprazolmetaboliterna har signifikant farmakologisk aktivitet.
Exkretion
Efter en oral eller intravenös engångsdos av 14C-märkt pantoprazol till friska, normala ämnesomsättningspersoner, utsöndrades cirka 71 % av dosen i urinen och 18 % utsöndrades i avföringen genom gallutsöndring. Det fanns ingen renal utsöndring av oförändrad pantoprazol.
Specifika populationer
Geriatriska patienter
Endast små till måttliga ökningar av AUC (43 %) och Cmax (26 %) för pantoprazol hittades hos äldre försökspersoner (64 till 76 år) efter upprepad oral administrering, jämfört med yngre försökspersoner [se Användning i specifika populationer ].
Pediatriska patienter
Pantoprazols farmakokinetik studerades hos barn under 16 år i fyra randomiserade, öppna kliniska prövningar på pediatriska patienter med förmodad/beprövad GERD. En pediatrisk granulatformulering studerades på barn upp till 5 års ålder och PROTONIX 40 mg tabletter med fördröjd frisättning studerades på barn äldre än 5 år.
I en populations-PK-analys ökade totalt clearance med ökande kroppsvikt på ett icke-linjärt sätt. Den totala clearancen ökade också med stigande ålder endast hos barn under 3 år.
Nyfödd upp till 5 års ålder
[ser Användning i specifika populationer ]
Barn och ungdomar i åldern 6 till 16 år
Farmakokinetiken för PROTONIX tabletter med fördröjd frisättning utvärderades hos barn i åldrarna 6 till 16 år med en klinisk diagnos av GERD. PK-parametrarna efter en oral engångsdos på 20 mg eller 40 mg PROTONIX 40 mg tabletter hos barn i åldrarna 6 till 16 år var mycket varierande (%CV varierar mellan 40 och 80%). Det geometriska medelvärdet av AUC uppskattat från populationsfarmakaanalys efter en 40 mg PROTONIX 40 mg tablett hos pediatriska patienter var cirka 39 % respektive 10 % högre hos 6 till 11 och 12 till 16 år gamla barn, jämfört med hos vuxna (tabell 7). .
Manliga Och Kvinnliga Patienter
Det finns en måttlig ökning av AUC och Cmax för pantoprazol hos kvinnor jämfört med män. Däremot är viktnormaliserade clearancevärden likartade hos kvinnor och män.
Hos pediatriska patienter i åldrarna 1 till 16 år fanns inga kliniskt relevanta effekter av kön på clearance av pantoprazol, vilket framgår av populationsfarmakokinetisk analys.
Patienter med nedsatt njurfunktion
Hos patienter med gravt nedsatt njurfunktion var de farmakokinetiska parametrarna för pantoprazol liknande de hos friska försökspersoner.
Patienter med nedsatt leverfunktion
Hos patienter med lätt till gravt nedsatt leverfunktion (Child-Pugh A till C cirros) ökade maximala pantoprazolkoncentrationer endast något (1,5 gånger) jämfört med friska försökspersoner. Även om halveringstiden i serum ökade till 7-9 timmar och AUC-värdena ökade med 5 till 7 gånger hos patienter med nedsatt leverfunktion, var dessa ökningar inte större än de som observerades hos CYP2C19-fattiga metaboliserare, där ingen dosjustering är motiverad. Dessa farmakokinetiska förändringar hos patienter med nedsatt leverfunktion resulterar i minimal läkemedelsackumulering efter administrering en gång dagligen med flera doser. Doser högre än 40 mg/dag har inte studerats hos patienter med nedsatt leverfunktion.
Läkemedelsinteraktionsstudier
Effekt av andra droger på Pantoprazol
Pantoprazol metaboliseras huvudsakligen av CYP2C19 och i mindre utsträckning av CYP 3A4, 2D6 och 2C9. I in vivo läkemedelsinteraktionsstudier med CYP2C19-substrat (diazepam [även ett CYP3A4-substrat] och fenytoin [även en CYP3A4-inducerare] och klopidogrel), nifedipin, midazolam och klaritromycin (CYP3A4-substrat), substrat CYP2D6a, substrat CYP2D6a. , naproxen och piroxikam (CYP2C9-substrat) och teofyllin (ett CYP1A2-substrat) hos friska försökspersoner, förändrades inte pantoprazols farmakokinetik signifikant.
Effekt av Pantoprazol på andra droger
Clopidogrel
Klopidogrel metaboliseras till sin aktiva metabolit delvis av CYP2C19. I en klinisk crossover-studie fick 66 friska försökspersoner klopidogrel (300 mg laddningsdos följt av 75 mg per dag) enbart och tillsammans med pantoprazol (80 mg samtidigt som klopidogrel) i 5 dagar. På dag 5 reducerades medel-AUC för den aktiva metaboliten av klopidogrel med cirka 14 % (geometriskt medelförhållande var 86 %, med 90 % KI på 79 till 93 %) när pantoprazol administrerades samtidigt med klopidogrel jämfört med klopidogrel administrerat ensamt. Farmakodynamiska parametrar mättes också och visade att förändringen i hämning av trombocytaggregation (inducerad av 5 μM ADP) var korrelerad med förändringen i exponeringen för klopidogrel aktiv metabolit. Den kliniska betydelsen av detta fynd är inte klarlagt.
Mykofenolatmofetil (MMF)
Administrering av pantoprazol 40 mg två gånger dagligen i 4 dagar och en engångsdos på 1000 mg MMF cirka en timme efter den sista dosen av pantoprazol till 12 friska försökspersoner i en cross-over-studie resulterade i en minskning med 57 % av Cmax och 27 % minskning. i AUC för MPA. Transplantationspatienter som fick cirka 2000 mg MMF per dag (n=12) jämfördes med transplantationspatienter som fick ungefär samma dos av MMF och pantoprazol 40 mg per dag (n=21). Det var en 78 % minskning av Cmax och en 45 % minskning av AUC för MPA hos patienter som fick både pantoprazol och MMF [se LÄKEMEDELSINTERAKTIONER ].
Andra droger
In vivo-studier tyder också på att pantoprazol inte signifikant påverkar kinetiken för följande läkemedel (cisaprid, teofyllin, diazepam [och dess aktiva metabolit, desmetyldiazepam], fenytoin, metoprolol, nifedipin, karbamazepin, midazolam, klaritromycin, diklofenak, naproxen, och orala preventivmedel [levonorgestrel/etinylestradiol]). I andra in vivo-studier hade digoxin, etanol, glyburid, antipyrin, koffein, metronidazol och amoxicillin inga kliniskt relevanta interaktioner med pantoprazol.
Även om inga signifikanta läkemedelsinteraktioner har observerats i kliniska studier, har potentialen för signifikanta läkemedelsinteraktioner vid dosering mer än en gång dagligen med höga doser av pantoprazol inte studerats hos låga metaboliserare eller individer som har nedsatt leverfunktion.
Antacida
Det förekom inte heller någon interaktion med samtidigt administrerade antacida.
Farmakogenomik
CYP2C19 uppvisar en känd genetisk polymorfism på grund av dess brist i vissa subpopulationer (t.ex. är cirka 3 % av kaukasierna och afroamerikaner och 17 % till 23 % av asiaten dåliga metaboliserare). Även om dessa subpopulationer av pantoprazol-fattiga metaboliserare har elimineringshalveringstider på 3,5 till 10 timmar hos vuxna, har de fortfarande minimal ackumulering (23 % eller mindre) vid dosering en gång dagligen. För vuxna patienter som är CYP2C19-fattiga metaboliserare behövs ingen dosjustering.
I likhet med vuxna uppvisade pediatriska patienter som har genotypen CYP2C19 med låg metaboliserare (CYP2C19 *2/*2) mer än en 6-faldig ökning av AUC jämfört med extensiv pediatrisk (CYP2C19 *1/*1) och intermediär (CYP2C19 *1) /*x) metaboliserare. Dåliga metaboliserare uppvisade ungefär 10 gånger lägre skenbart oralt clearance jämfört med omfattande metaboliserare.
För kända pediatriskt dåliga metaboliserare bör en dosreduktion övervägas.
Kliniska studier
PROTONIX 20 mg tabletter med fördröjd frisättning användes i följande kliniska prövningar.
Erosiv esofagit (EE) associerad med gastroesofageal refluxsjukdom (GERD)
Vuxna patienter
En amerikansk multicenter, dubbelblind, placebokontrollerad studie av PROTONIX 10 mg, 20 mg eller 40 mg en gång dagligen genomfördes på 603 patienter med refluxsymtom och endoskopiskt diagnostiserad EE av grad 2 eller högre (Hetzel-Dent-skalan). I den här studien hade cirka 25 % av de inskrivna patienterna svår EE av grad 3 och 10 % hade grad 4. Procentandelen av patienter som helade (enligt protokoll, n = 541) i denna studie visas i tabell 8.
I denna studie hade alla PROTONIX-behandlingsgrupper signifikant högre läkningshastigheter än placebogruppen. Detta gällde oavsett H. pylori-status för behandlingsgrupperna 40 mg och 20 mg PROTONIX 40 mg. Dosen på 40 mg av PROTONIX 20 mg resulterade i läkningshastigheter som var betydligt högre än de som hittades med antingen 20 mg eller 10 mg dosen.
En signifikant större andel av patienterna som tog PROTONIX 40 mg upplevde fullständig lindring av halsbränna dag- och nattetid och frånvaro av uppstötningar, från och med första behandlingsdagen, jämfört med placebo. Patienter som tog PROTONIX konsumerade betydligt färre antacida tabletter per dag än de som fick placebo.
PROTONIX 40 mg och 20 mg en gång dagligen jämfördes också med nizatidin 150 mg två gånger dagligen i en amerikansk multicenter, dubbelblind studie av 243 patienter med refluxsymtom och endoskopiskt diagnostiserad EE av grad 2 eller högre. Procentandelen av patienter som blivit helade (per protokoll, n = 212) visas i tabell 9.
Behandling en gång dagligen med PROTONIX 40 mg eller 20 mg resulterade i signifikant överlägsen läkningshastighet vid både 4 och 8 veckor jämfört med behandling två gånger dagligen med 150 mg nizatidin. För 40 mg-behandlingsgruppen uppnåddes signifikant högre läkningshastigheter jämfört med nizatidin oavsett H. pylori-status.
En signifikant större andel av patienterna i PROTONIX-behandlingsgrupperna upplevde fullständig lindring av halsbränna under natten och uppstötningar, med början den första dagen och halsbrännan under dagen den andra dagen, jämfört med de som tog nizatidin 150 mg två gånger dagligen. Patienter som tog PROTONIX konsumerade betydligt färre antacida tabletter per dag än de som tog nizatidin.
Pediatriska patienter i åldern 5 år till 16 år
Effekten av PROTONIX vid behandling av EE associerad med GERD hos pediatriska patienter i åldrarna 5 år till 16 år extrapoleras från adekvata och väl genomförda studier på vuxna, eftersom patofysiologin tros vara densamma. Fyra pediatriska patienter med endoskopiskt diagnostiserad EE studerades i multicenter, randomiserade, dubbelblinda, parallella behandlingsstudier. Barn med endoskopiskt diagnosticerad EE (definierad som en endoskopisk Hetzel-Dent-poäng ≥2) behandlades en gång dagligen i 8 veckor med en av två dosnivåer av PROTONIX (20 mg eller 40 mg). Alla fyra patienter med EE helades (Hetzel-Dent-poäng på 0 eller 1) efter 8 veckor.
Långsiktigt underhåll av läkning av erosiv esofagit
Två oberoende, multicenter, randomiserade, dubbelblinda, komparatorkontrollerade studier av identisk design utfördes på vuxna GERD-patienter med endoskopiskt bekräftad läkt EE för att visa effektiviteten av PROTONIX vid långtidsupprätthållande av läkning. De två amerikanska studierna inkluderade 386 respektive 404 patienter för att få antingen 10 mg, 20 mg eller 40 mg PROTONIX 40 mg tabletter med fördröjd frisättning en gång dagligen eller 150 mg ranitidin två gånger dagligen. Som visas i tabell 10 var PROTONIX 40 mg och 20 mg signifikant överlägsna ranitidin vid varje tidpunkt med avseende på upprätthållande av läkning. Dessutom var PROTONIX 40 mg överlägsen alla andra studerade behandlingar.
PROTONIX 40 mg var överlägset ranitidin när det gällde att minska antalet episoder av halsbränna dag- och nattetid från den första till och med den tolfte behandlingsmånaden. PROTONIX 20 mg, administrerat en gång dagligen, var också effektivt för att minska episoder av halsbränna dag- och nattetid i en studie, som presenteras i Tabell 11.
Patologiska hypersekretoriska tillstånd inklusive Zollinger-Ellisons syndrom
en multicenter, öppen studie med 35 patienter med patologiska hypersekretoriska tillstånd, såsom Zollinger-Ellisons syndrom, med eller utan multipel endokrin neoplasi typ I, kontrollerade PROTONIX framgångsrikt magsyrasekretionen. Doser från 80 mg dagligen till 240 mg dagligen bibehöll magsyraproduktionen under 10 mEq/h hos patienter utan föregående syrareducerande kirurgi och under 5 mEq/h hos patienter med tidigare syrareducerande kirurgi.
Doserna titrerades initialt till individuella patientbehov och justerades hos vissa patienter baserat på det kliniska svaret med tiden [se DOSERING OCH ADMINISTRERING ]. PROTONIX 40 mg tolererades väl vid dessa dosnivåer under långa perioder (mer än 2 år hos vissa patienter).
PATIENTINFORMATION
PROTONIX (pro-TAH-nix)(pantoprazolnatrium) tabletter med fördröjd frisättning och PROTONIX (pro-TAH-nix) (pantoprazolnatrium) för oral suspension med fördröjd frisättning
Vilken är den viktigaste informationen jag borde veta om PROTONIX?
Du ska ta PROTONIX 20 mg precis som ordinerats, i lägsta möjliga dos och under den kortaste tiden som behövs.
PROTONIX kan hjälpa dina syrarelaterade symtom, men du kan fortfarande ha allvarliga magproblem. Prata med din läkare.
PROTONIX kan orsaka allvarliga biverkningar, inklusive:
- En typ av njurproblem (akut tubulointerstitiell nefrit). Vissa personer som tar protonpumpshämmare (PPI), inklusive PROTONIX 40 mg, kan utveckla ett njurproblem som kallas akut tubulointerstitiell nefrit som kan inträffa när som helst under behandlingen med PROTONIX. Ring din läkare omedelbart om du har en minskning av mängden du kissar eller om du har blod i urinen.
- Diarré orsakad av en infektion (Clostridium difficile) i dina tarmar. Ring din läkare omedelbart om du har vattnig avföring eller magsmärtor som inte försvinner. Du kanske har feber eller inte.
- Benfrakturer (höft, handled eller ryggrad). Benfrakturer i höften, handleden eller ryggraden kan inträffa hos personer som tar flera dagliga doser av PPI-läkemedel och under en lång tidsperiod (ett år eller längre). Tala om för din läkare om du har en benfraktur, särskilt i höften, handleden eller ryggraden.
- Vissa typer av lupus erythematosus. Lupus erythematosus är en autoimmun sjukdom (kroppens immunceller attackerar andra celler eller organ i kroppen). Vissa personer som tar PPI-läkemedel, inklusive PROTONIX 40 mg, kan utveckla vissa typer av lupus erythematosus eller få försämring av den lupus de redan har. Ring din läkare omedelbart om du har ny eller förvärrad ledvärk eller utslag på kinderna eller armarna som blir värre i solen.
Tala med din läkare om din risk för dessa allvarliga biverkningar.
PROTONIX kan ha andra allvarliga biverkningar. Ser "Vilka är de möjliga biverkningarna av PROTONIX?"
Vad är PROTONIX 20mg?
Ett receptbelagt läkemedel som kallas protonpumpshämmare (PPI) som används för att minska mängden syra i magen.
Hos vuxna, PROTONIX används för:
- upp till 8 veckor för läkning och symtomlindring av syrarelaterade skador på slemhinnan i matstrupen (kallad erosiv esofagit eller EE). Din läkare kan ordinera ytterligare 8 veckor av PROTONIX 20 mg till patienter vars EE inte läker.
- bibehålla läkning av EE och för att förhindra återkomst av halsbränna symtom orsakade av GERD. Det är inte känt om PROTONIX 40 mg är säkert och effektivt när det används i mer än 12 månader för detta ändamål.
- långtidsbehandling av tillstånd där din mage gör för mycket syra. Detta inkluderar ett sällsynt tillstånd som kallas Zollinger-Ellisons syndrom.
Hos barn från 5 år och äldre, PROTONIX används för:
- upp till 8 veckor för läkning och symtomlindring av EE. Det är inte känt om PROTONIX 20 mg är säkert om det används längre än 8 veckor till barn.
PROTONIX 20mg är inte avsett för barn under 5 år. Det är inte känt om PROTONIX 40 mg är säkert och effektivt för barn för annan behandling än EE.
Ta inte PROTONIX 20 mg om du är:
- allergisk mot pantoprazolnatrium, något annat PPI-läkemedel eller något av innehållsämnena i PROTONIX. Se slutet av denna medicinguide för en komplett lista över ingredienser.
- tar ett läkemedel som innehåller rilpivirin (EDURANT, COMPLERA, ODEFSEY, JULUCA) som används för att behandla HIV-1 (humant immunbristvirus).
Innan du tar PROTONIX, berätta för din läkare om alla dina medicinska tillstånd, inklusive om du:
- har låga magnesiumnivåer i blodet.
- är gravid eller planerar att bli gravid. PROTONIX 40 mg kan skada ditt ofödda barn. Tala om för din läkare om du blir gravid eller tror att du kan vara gravid under behandling med PROTONIX.
- ammar eller planerar att amma. PROTONIX kan passera över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar PROTONIX.
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Tala särskilt om för din läkare om du tar metotrexat (Otrexup, Rasuvo, Trexall, XATMEP), digoxin (LANOXIN) eller ett vattenpiller (diuretikum).
Hur ska jag ta PROTONIX 20mg?
- Ta PROTONIX 40 mg precis som din läkare har ordinerat.
PROTONIX tabletter med fördröjd frisättning (PROTONIX 20 mg tabletter):
-
- Dela, tugga eller krossa inte PROTONIX 40 mg tabletter.
- Svälj PROTONIX 20 mg tabletter hela, med eller utan mat.
- Tala om för din läkare om du inte kan svälja din PROTONIX 20 mg tablett.
- Du kan använda antacida medan du tar PROTONIX 40 mg tabletter.
PROTONIX 40 mg för oral suspension med fördröjd frisättning (PROTONIX för oral suspension):
-
- Dela, tugga eller krossa inte PROTONIX 20 mg för oral suspension.
- Ta PROTONIX 40 mg för oral suspension cirka 30 minuter före måltid.
- PROTONIX för oral suspension ska endast ges genom munnen blandat i äppeljuice eller äppelmos eller genom en nasogastrisk (NG) sond eller gastrostomisond blandad i äppeljuice. Blanda inte PROTONIX för oral suspension i andra vätskor än äppeljuice eller annan mat än äppelmos.
- Dela inte ett paket PROTONIX 20 mg för oral suspension för att göra en mindre dos.
- Se den "Användningsinstruktioner" i slutet av denna medicinguide för instruktioner om hur man blandar och tar PROTONIX 40mg för oral suspension genom munnen i äppelmos eller äppeljuice eller hur man blandar och ger suspensionen genom ett NG-rör eller en gastrostomisond blandat i äppeljuice.
- Om du missar en dos av PROTONIX, ta den så snart som möjligt. Om det nästan är dags för din nästa dos, ta inte den missade dosen. Ta nästa dos vid din ordinarie tid. Ta inte 2 doser samtidigt.
- Om du tar för mycket PROTONIX, ring din läkare eller din giftcentral på 1-800-222-1222 omedelbart eller gå till närmaste akutmottagning.
Vilka är de möjliga biverkningarna av PROTONIX 40 mg?
PROTONIX 20mg kan orsaka allvarliga biverkningar, inklusive:
- Ser "Vilken är den viktigaste informationen jag borde veta om PROTONIX?"
- Låga vitamin B-12 nivåer i din kropp kan inträffa hos personer som har tagit PROTONIX 40 mg under lång tid (mer än 3 år). Tala om för din läkare om du har symtom på låga vitamin B-12-nivåer, inklusive andnöd, yrsel, oregelbunden hjärtrytm, muskelsvaghet, blek hud, trötthetskänsla, humörförändringar och stickningar eller domningar i armar och ben.
- Låga magnesiumnivåer i din kropp kan inträffa hos personer som har tagit PROTONIX i minst 3 månader. Tala om för din läkare om du har symtom på låga magnesiumnivåer, inklusive kramper, yrsel, oregelbunden hjärtrytm, darrning, muskelvärk eller svaghet och spasmer i händer, fötter eller röst.
- Magutväxter (fundiska körtelpolyper). Personer som tar PPI-läkemedel under lång tid har en ökad risk att utveckla en viss typ av magtillväxt som kallas fundic gland polyper, särskilt efter att ha tagit PPI-läkemedel i mer än 1 år.
De vanligaste biverkningarna av PROTONIX 40 mg hos vuxna inkluderar: huvudvärk, diarré, illamående, smärta i magområdet (buk), kräkningar, gaser, yrsel och ledvärk.
De vanligaste biverkningarna av PROTONIX 40 mg hos barn inkluderar: övre luftvägsinfektion, huvudvärk, feber, diarré, kräkningar, utslag och magsmärtor (buksmärtor). Dessa är inte alla möjliga biverkningar av PROTONIX. Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara PROTONIX 40mg?
Förvara PROTONIX 20 mg i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
Förvara PROTONIX och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av PROTONIX.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte PROTONIX för ett tillstånd som det inte har ordinerats för. Ge inte PROTONIX 20 mg till andra personer, även om de har samma symtom som du har. Det kan skada dem. Du kan fråga din läkare eller apotekspersonal om information om PROTONIX 20mg som är skriven för vårdpersonal.
Vilka är ingredienserna i PROTONIX?
Aktiv beståndsdel: pantoprazolnatriumseskvihydrat
Inaktiva ingredienser i PROTONIX tabletter med fördröjd frisättning: kalciumstearat, krospovidon, hypromellos, järnoxid, mannitol, metakrylsyrasampolymer, polysorbat 80, povidon, propylenglykol, natriumkarbonat, natriumlaurylsulfat, titandioxid och trietylcitrat.
Inaktiva ingredienser i PROTONIX 40 mg för oral suspension med fördröjd frisättning: krospovidon, hypromellos, metakrylsyrasampolymer, mikrokristallin cellulosa, polysorbat 80, povidon, natriumkarbonat, natriumlaurylsulfat, talk, titandioxid, trietylcitrat och gul järnoxid.
Användningsinstruktioner
PROTONIX (pro-TAH-nix) (pantoprazolnatrium) för oral suspension med fördröjd frisättning
PROTONIX 40 mg för fördröjd frisättning oral suspension (PROTONIX 40 mg för oral suspension):
Viktig information:
- Dela, tugga eller krossa inte PROTONIX för oral suspension.
- Ta PROTONIX för oral suspension cirka 30 minuter före måltid.
- PROTONIX för oral suspension:
- skall endast tas med äppelmos eller äppeljuice.
- skall inte blandas i vatten eller andra vätskor eller andra livsmedel.
- förpackningen ska inte delas för att göra en mindre dos.
Att ta PROTONIX 20 mg för oral suspension med äppelmos:
Att ta PROTONIX 40 mg för oral suspension med äppeljuice:
Att ge PROTONIX 40 mg för oral suspension genom en nasogastrisk sond eller gastrostomisond:
- PROTONIX för oral suspension kan ges genom en NG-sond eller gastrostomisond storlek 16 fransk eller större. Ge inte PROTONIX 20 mg för oral suspension genom en NG-slang eller gastrostomisond som är mindre än storlek 16 French.
- Blanda PROTONIX 20 mg för oral suspension endast i äppeljuice när man ger genom en NG-sond eller gastrostomisond.
Hur ska jag förvara PROTONIX 20mg?
Förvara PROTONIX 20 mg i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
Förvara PROTONIX 40 mg och alla läkemedel utom räckhåll för barn.
Denna medicineringsguide och bruksanvisning har godkänts av US Food and Drug Administration.
