Prilosec 40mg, 10mg, 20mg Omeprazole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Prilosec 40mg och hur används det?
Prilosec 40mg är ett receptbelagt och receptfritt läkemedel som används för att behandla symtom på gastroesofageal refluxsjukdom (GERD), magsår och andra tillstånd orsakade av för mycket magsyra. Prilosec 10mg kan användas ensamt eller tillsammans med andra läkemedel.
Prilosec tillhör en klass av läkemedel som kallas protonpumpshämmare.
Det är inte känt om Prilosec 40 mg är säkert och effektivt för barn yngre än 1 månad.
Vilka är de möjliga biverkningarna av Prilosec 10mg?
Prilosec kan orsaka allvarliga biverkningar inklusive:
- svåra magsmärtor,
- diarré som är vattnig eller blodig,
- ny eller ovanlig smärta i handled, lår, höft eller rygg,
- anfall (kramper),
- lite eller ingen urinering,
- blod i urinen,
- svullnad,
- snabb viktökning,
- yrsel,
- oregelbundna hjärtslag,
- känner sig orolig,
- muskelkramp,
- muskelryckningar,
- hosta,
- kvävande känsla,
- ledvärk och
- hudutslag på kinderna eller armarna som förvärras av solljus
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Prilosec inkluderar:
- magont,
- gas,
- illamående,
- kräkningar,
- diarré och
- huvudvärk
BESKRIVNING
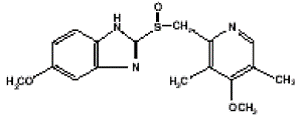
Den aktiva ingrediensen i PRILOSEC (omeprazol) kapslar med fördröjd frisättning är en substituerad bensimidazol, 5-metoxi-2-[[(4-metoxi-3, 5-dimetyl-2-pyridinyl) metyl] sulfinyl]-1H-bensimidazol, en förening som hämmar magsyrasekretionen. Dess empiriska formel är C17H19N3O3S, med en molekylvikt på 345,42. Strukturformeln är:
Omeprazol är ett vitt till benvitt kristallint pulver som smälter vid sönderdelning vid cirka 155°C. Det är en svag bas, fritt löslig i etanol och metanol, och lätt löslig i aceton och isopropanol och mycket svagt löslig i vatten. Omeprazols stabilitet är en funktion av pH; det bryts snabbt ned i sura medier, men har acceptabel stabilitet under alkaliska förhållanden.
Den aktiva ingrediensen i PRILOSEC (omeprazolmagnesium) för oral suspension med fördröjd frisättning är 5-metoxi-2-[[(4-metoxi-3,5-dimetyl-2-pyridinyl)metyl]sulfinyl]-1H-bensimidazol, magnesium salt (2:1)
Omeprazolmagnesium är ett vitt till benvitt pulver med en smältpunkt vid nedbrytning vid 200°C. Saltet är svagt lösligt (0,25 mg/ml) i vatten vid 25°C och det är lösligt i metanol. Halveringstiden är starkt pH-beroende.
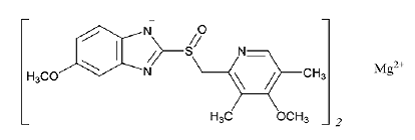
Den empiriska formeln för omeprazolmagnesium är (C17H18N3O3S)2 Mg, molekylvikten är 713,12 och strukturformeln är:
PRILOSEC levereras som kapslar med fördröjd frisättning för oral administrering. Varje kapsel med fördröjd frisättning innehåller antingen 10 mg, 20 mg eller 40 mg omeprazol i form av enterodragerade granuler med följande inaktiva ingredienser: cellulosa, dinatriumvätefosfat, hydroxipropylcellulosa, hypromellos, laktos, mannitol, natriumlaurylsulfat och andra ingredienser. Kapselskalen har följande inaktiva ingredienser: gelatin-NF, FD&C Blue #1, FD&C Red #40, D&C Red #28, titandioxid, syntetisk svart järnoxid, isopropanol, butylalkohol, FD&C Blue #2, D&C Red #7 Calcium Lake, och dessutom innehåller kapselskalen på 10 mg och 40 mg också D&C Yellow #10.
Varje förpackning med PRILOSEC For Delayed-Release Oral Suspension innehåller antingen 2,8 mg eller 11,2 mg omeprazolmagnesium (motsvarande 2,5 mg eller 10 mg omeprazol), i form av enterodragerade granuler med följande inaktiva ingredienser: glycerylmonostearat, hydroxipropyl cellulosa, hypromellos, magnesiumstearat, metakrylsyrasampolymer C, polysorbat, sockersfärer, talk och trietylcitrat, och även inaktiva granulat. De inaktiva granulerna består av följande ingredienser: citronsyra, krospovidon, dextros, hydroxipropylcellulosa, järnoxid och xantamgummi. Omeprazolgranulerna och inaktiva granulerna består av vatten för att bilda en suspension och ges genom oral, nasogastrisk eller direkt magadministrering.
INDIKATIONER
Behandling av aktivt duodenalsår
PRILOSEC 20 mg är indicerat för korttidsbehandling av aktivt duodenalsår hos vuxna. De flesta patienter läker inom fyra veckor. Vissa patienter kan behöva ytterligare fyra veckors terapi.
Utrotning av Helicobacter pylori för att minska risken för återfall av duodenalsår
Utrotning av H. pylori har visat sig minska risken för återfall av duodenalsår.
Trippelterapi
PRILOSEC 40 mg i kombination med klaritromycin och amoxicillin, är indicerat för behandling av patienter med H. pylori-infektion och duodenalsår (aktiv eller upp till 1 års historia) för att utrota H. pylori hos vuxna.
Dubbel terapi
PRILOSEC i kombination med klaritromycin är indicerat för behandling av patienter med H. pylori-infektion och duodenalsår för att utrota H. pylori hos vuxna.
Bland patienter som misslyckas med behandlingen är det mer sannolikt att PRILOSEC med klaritromycin associeras med utvecklingen av klaritromycinresistens jämfört med trippelbehandling. Hos patienter som misslyckas med behandlingen bör känslighetstest göras. Om resistens mot klaritromycin påvisas eller känslighetstestning inte är möjlig, bör alternativ antimikrobiell behandling sättas in [se KLINISK FARMAKOLOGI och klaritromycinförskrivningsinformationen, avsnittet Mikrobiologi].
Behandling av aktivt benignt magsår
PRILOSEC är indicerat för korttidsbehandling (4 till 8 veckor) av aktivt benignt magsår hos vuxna.
Behandling av symtomatisk gastroesofageal refluxsjukdom (GERD)
PRILOSEC är indicerat för behandling av halsbränna och andra symtom associerade med GERD i upp till 4 veckor hos patienter 1 år och äldre.
Behandling av erosiv esofagit (EE) på grund av syramedierad GERD
Pediatriska patienter 1 års ålder till vuxna
PRILOSEC 20 mg är indicerat för korttidsbehandling (4 till 8 veckor) av EE på grund av syramedierad GERD som har diagnostiserats med endoskopi hos patienter 1 år och äldre.
Effekten av PRILOSEC 10 mg som använts i mer än 8 veckor hos patienter med EE har inte fastställts. Om en patient inte svarar på 8 veckors behandling kan ytterligare 4 veckors behandling ges. Om EE- eller GERD-symtom återkommer (t.ex. halsbränna) kan ytterligare 4 till 8 veckors kurer med PRILOSEC övervägas.
Pediatriska patienter från 1 månad till yngre än 1 års ålder
PRILOSEC är indicerat för korttidsbehandling (upp till 6 veckor) av EE på grund av syramedierad GERD hos pediatriska patienter från 1 månad till yngre än 1 år.
Underhåll av läkning av EE på grund av syramedierad GERD
PRILOSEC 40 mg är indicerat för underhållsläkning av EE på grund av syramedierad GERD hos patienter 1 år och äldre.
Kontrollerade studier sträcker sig inte längre än 12 månader.
Patologiska hypersekretoriska tillstånd
PRILOSEC 40 mg är indicerat för långtidsbehandling av patologiska hypersekretoriska tillstånd (t.ex. Zollinger-Ellisons syndrom, multipla endokrina adenom och systemisk mastocytos) hos vuxna.
DOSERING OCH ADMINISTRERING
Rekommenderad dosering för vuxna efter indikation
Tabell 1 visar den rekommenderade dosen av PRILOSEC 40 mg till vuxna patienter efter indikation.
Rekommenderad pediatrisk dosering enligt indikation
Tabell 2 visar den rekommenderade dosen av PRILOSEC till pediatriska patienter efter indikation.
Administrationsinstruktioner
- PRILOSEC 40 mg är avsett att beredas i vatten och administreras oralt eller via en nasogastrisk (NG) eller magsond.
- Ta PRILOSEC 40 mg före måltid.
- Antacida kan användas samtidigt med PRILOSEC.
- Missade doser: Om en dos missas, administrera så snart som möjligt. Men om nästa schemalagda dos är beräknad, ta inte den missade dosen och ta nästa dos i tid. Ta inte två doser på en gång för att kompensera för en missad dos.
Oral administrering i vatten
Administrering med vatten via en NG eller magsond (storlek 6 eller större)
HUR LEVERERAS
Doseringsformer och styrkor
PRILOSEC för oral suspension med fördröjd frisättning: 2,5 mg och 10 mg omeprazol i endosförpackningar innehållande ett fint gult pulver, bestående av vita till brunaktiga omeprazolmagnesiumgranuler och blekgula inaktiva granuler.
Förvaring Och Hantering
PRILOSEC (omeprazolmagnesium) för oral suspension med fördröjd frisättning, 2,5 mg eller 10 mg omeprazol, levereras som en enhetsdosförpackning innehållande ett fint gult pulver, bestående av vita till brunaktiga omeprazolmagnesiumgranuler och ljusgula inaktiva granuler. PRILOSEC enhetsdosförpackningar levereras enligt följande:
NDC 70515-625–01 enhetsdosförpackningar om 30: 2,5 mg förpackningar NDC 70515-610–01 enhetsdosförpackningar om 30: 10 mg förpackningar
Lagring
Förvara PRILOSEC för oral suspension med fördröjd frisättning vid 25°C (77°F); utflykter tillåtna till 15–30°C (59–86°F). [Ser USP-kontrollerad rumstemperatur .]
Tillverkad för: Covis Pharma, Zug, 6300 Schweiz. Reviderad: mars 2022
BIEFFEKTER
Följande allvarliga biverkningar beskrivs nedan och på andra ställen i märkningen:
- Akut Tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Clostridium difficile-associerad diarré [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Allvarliga kutana biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kutan och systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Cyanokobalamin (Vitamin B-12) Brist [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypomagnesemi och mineralmetabolism [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Fundiska körtelpolyper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar med PRILOSEC
Monoterapi
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Säkerhetsdata som beskrivs nedan återspeglar exponering för omeprazolmagnesium kapslar med fördröjd frisättning hos 3096 patienter från globala kliniska prövningar (465 patienter från amerikanska studier och 2631 patienter från internationella studier). Indikationer som studerats kliniskt i amerikanska prövningar inkluderar duodenalsår, resistent sår och Zollinger-Ellisons syndrom. De internationella kliniska prövningarna var dubbelblinda och öppna i design. De vanligaste rapporterade biverkningarna (dvs. med en incidens ≥2 %) från PRILOSEC-behandlade patienter som inkluderades i dessa studier var huvudvärk (7 %), buksmärtor (5 %), illamående (4 %), diarré (4 %). ), kräkningar (3 %) och flatulens (3 %).
Ytterligare biverkningar som rapporterades med en incidens ≥1 % inkluderade sura uppstötningar (2 %), övre luftvägsinfektion (2 %), förstoppning (2 %), yrsel (2 %), utslag (2 %), asteni (1 % ), ryggsmärtor (1 %) och hosta (1 %).
Den kliniska prövningens säkerhetsprofil hos patienter äldre än 65 år liknade den hos patienter 65 år eller yngre.
Den kliniska prövningens säkerhetsprofil hos pediatriska patienter som fick omeprazolmagnesium kapslar med fördröjd frisättning liknade den hos vuxna patienter. Unikt för den pediatriska populationen, men biverkningar av andningsorganen rapporterades ofta i åldersgruppen 1 månad till Användning i specifika populationer ].
Erfarenhet av kliniska prövningar med PRILOSEC 20 mg i kombinationsterapi för utrotning av H. pylori
kliniska prövningar med användning av antingen dubbelterapi med omeprazolmagnesium fördröjd frisättningskapslar och klaritromycin, eller trippelterapi med omeprazolmagnesiumfördröjd frisättningskapslar, klaritromycin och amoxicillin, observerades inga biverkningar unika för dessa läkemedelskombinationer. De observerade biverkningarna var begränsade till de som tidigare rapporterats med enbart omeprazol, klaritromycin eller amoxicillin.
Dubbelterapi (omeprazol magnesium kapslar med fördröjd frisättning/klaritromycin)
Biverkningar som observerats i kontrollerade kliniska prövningar med kombinationsbehandling med omeprazolmagnesium kapslar med fördröjd frisättning och klaritromycin (n = 346) som skilde sig från de som tidigare beskrivits för enbart omeprazolmagnesium kapslar med fördröjd frisättning var smakperversion (15 %), missfärgning av tungan (2 %), rinit (2 %), faryngit (1 %) och influensasyndrom (1 %). (För mer information om klaritromycin, se förskrivningsinformationen för klaritromycin, avsnittet Biverkningar.)
Trippelterapi (omeprazol magnesium kapslar med fördröjd frisättning/klaritromycin/amoxicillin)
De vanligaste biverkningarna som observerats i kliniska prövningar med kombinationsbehandling med omeprazolmagnesium kapslar med fördröjd frisättning, klaritromycin och amoxicillin (n = 274) var diarré (14 %), smakperversion (10 %) och huvudvärk (7 %). Ingen av dessa inträffade med en högre frekvens än den som rapporterats av patienter som endast tog antimikrobiella medel. (För mer information om klaritromycin eller amoxicillin, se respektive förskrivningsinformation, avsnitten Biverkningar.)
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av omeprazol efter godkännande. Eftersom dessa reaktioner frivilligt rapporteras från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras faktiska frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Kroppen som helhet: Överkänslighetsreaktioner inklusive anafylaxi, anafylaktisk chock, angioödem, bronkospasm, interstitiell nefrit, urtikaria (se även Hud nedan); feber; smärta; Trötthet; obehag; systemisk lupus erythematosus
Kardiovaskulär: Bröstsmärta eller angina, takykardi, bradykardi, hjärtklappning, förhöjt blodtryck, perifert ödem
Endokrin: Gynekomasti
Gastrointestinala: Pankreatit (vissa dödlig), anorexi, colon irriterad, fekal missfärgning, esofagus candidiasis, slemhinneatrofi i tungan, stomatit, buksvullnad, muntorrhet, mikroskopisk kolit, fundiska körtelpolyper.
Gastroduodenala karcinoider har rapporterats hos patienter med ZE-syndrom under långtidsbehandling med omeprazol. Detta fynd tros vara en manifestation av det underliggande tillståndet, som är känt för att vara associerat med sådana tumörer.
Lever: Leversjukdom inklusive leversvikt (viss dödlig), levernekros (vissa dödlig), hepatisk encefalopati hepatocellulär sjukdom, kolestatisk sjukdom, blandad hepatit, gulsot och förhöjda leverfunktionstester [ALT, AST, GGT, alkaliskt fosfatas och bilirubin]
Infektioner och angrepp: Clostridium difficile-associerad diarré
Metabolism och näringsstörningar: Hypomagnesemi, hypokalcemi, hypokalemi [Varningar och försiktighetsåtgärder 5.9], hyponatremi, hypoglykemi, viktökning
Muskuloskeletala: Muskelsvaghet, myalgi, muskelkramper, ledvärk, bensmärta, benfraktur
Nervsystemet/psykiatrisk: Psykiatriska och sömnstörningar inklusive depression, agitation, aggression, hallucinationer, förvirring, sömnlöshet, nervositet, apati, somnolens, ångest och drömavvikelser; skakningar, parestesi; vertigo
Andningsvägar: Näsblod, svalgsmärta
Hud: Allvarliga generaliserade hudreaktioner inklusive toxisk SJS/TEN (vissa dödlig), DRESS, AGEP, kutan lupus erythematosus och erythema multiforme; ljuskänslighet; urtikaria; utslag; hudinflammation; klåda; petekier; purpura; alopeci; torr hud; hyperhidros
Särskilda sinnen: Tinnitus, smakperversion
Okulär: Optisk atrofi, främre ischemisk optisk neuropati, optisk neurit, torra ögonsyndrom, ögonirritation, dimsyn, dubbelseende
Urogenital: Interstitiell nefrit, hematuri, proteinuri, förhöjt serumkreatinin, mikroskopisk pyuri, urinvägsinfektion, glykosuri, urinfrekvens, testikelsmärta
Hematologiska: Agranulocytos (vissa dödlig), hemolytisk anemi, pancytopeni, neutropeni, anemi, trombocytopeni, leukopeni, leukocytos
LÄKEMEDELSINTERAKTIONER
Tabell 3 och 4 inkluderar läkemedel med kliniskt viktiga läkemedelsinteraktioner och interaktion med diagnostik när de administreras samtidigt med omeprazol och instruktioner för att förebygga eller hantera dem.
Se märkningen av samtidigt använda läkemedel för att få ytterligare information om interaktioner med PPI.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Förekomst av magmalignitet
Hos vuxna utesluter inte symtomatisk respons på behandling med PRILOSEC förekomst av gastrisk malignitet. Överväg ytterligare uppföljning och diagnostiska tester hos vuxna patienter som har ett suboptimalt svar eller ett tidigt symtomatiskt återfall efter avslutad behandling med PPI. Hos äldre patienter, överväg också en endoskopi.
Akut Tubulointerstitiell nefrit
Akut tubulointerstitiell nefrit (TIN) har observerats hos patienter som tar PPI och kan uppträda när som helst under PPI-behandling. Patienter kan uppvisa olika tecken och symtom från symtomatiska överkänslighetsreaktioner till ospecifika symtom på nedsatt njurfunktion (t.ex. sjukdomskänsla, illamående, anorexi). I rapporterade fallserier diagnostiserades vissa patienter på biopsi och i frånvaro av extrarenala manifestationer (t.ex. feber, hudutslag eller artralgi). Avbryt behandlingen med PRILOSEC 40 mg och utvärdera patienter med misstänkt akut TIN [se KONTRAINDIKATIONER ].
Clostridium Difficile-associerad diarré
Publicerade observationsstudier tyder på att PPI-behandling som PRILOSEC kan vara associerad med en ökad risk för Clostridium difficile-associerad diarré, särskilt hos inlagda patienter. Denna diagnos bör övervägas för diarré som inte förbättras [se NEGATIVA REAKTIONER ].
Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas.
Clostridium difficile-associerad diarré (CDAD) har rapporterats vid användning av nästan alla antibakteriella medel. För mer information specifik för antibakteriella medel (klaritromycin och amoxicillin) indicerade för användning i kombination med PRILOSEC, se avsnitten Varningar och försiktighet i motsvarande förskrivningsinformation.
Benfraktur
Flera publicerade observationsstudier tyder på att behandling med protonpumpshämmare (PPI) kan vara associerad med en ökad risk för osteoporosrelaterade frakturer i höften, handleden eller ryggraden. Risken för frakturer var ökad hos patienter som fick höga doser, definierade som flera dagliga doser, och långvarig PPI-behandling (ett år eller längre). Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas. Patienter med risk för osteoporosrelaterade frakturer bör hanteras enligt fastställda behandlingsriktlinjer [se DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER ].
Allvarliga kutana biverkningar
Allvarliga kutana biverkningar, inklusive Stevens-Johnsons syndrom (SJS) och toxisk epidermal nekrolys (TEN), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) och akut generaliserad exantematös pustulos (AGEP) har rapporterats i samband med användning av PPI. [ser NEGATIVA REAKTIONER ]. Avbryt PRILOSEC vid de första tecknen eller symtomen på allvarliga kutana biverkningar eller andra tecken på överkänslighet och överväg ytterligare utvärdering.
Kutan och systemisk lupus erythematosus
Kutan lupus erythematosus (CLE) och systemisk lupus erythematosus (SLE) har rapporterats hos patienter som tar PPI, inklusive omeprazol. Dessa händelser har inträffat som både nyuppkomst och förvärring av befintlig autoimmun sjukdom. Majoriteten av PPI-inducerade lupus erythematosus fall var CLE.
Den vanligaste formen av CLE som rapporterats hos patienter som behandlats med PPI var subakut CLE (SCLE) och inträffade inom veckor till år efter kontinuerlig läkemedelsbehandling hos patienter från spädbarn till äldre. I allmänhet observerades histologiska fynd utan organinblandning.
Systemisk lupus erythematosus (SLE) rapporteras mindre vanligt än CLE hos patienter som får PPI. PPI-associerad SLE är vanligtvis mildare än icke-läkemedelsinducerad SLE. Debut av SLE inträffade vanligtvis inom dagar till år efter påbörjad behandling, främst hos patienter från unga vuxna till äldre. Majoriteten av patienterna fick utslag; dock rapporterades också artralgi och cytopeni.
Undvik administrering av PPI under längre tid än vad som är medicinskt indicerat. Om tecken eller symtom som överensstämmer med CLE eller SLE noteras hos patienter som får PRILOSEC 10 mg, avbryt läkemedlet och hänvisa patienten till lämplig specialist för utvärdering. De flesta patienter förbättras med avbrytande av enbart PPI inom 4 till 12 veckor. Serologiska tester (t.ex. ANA) kan vara positiva och förhöjda serologiska testresultat kan ta längre tid att lösa än kliniska manifestationer.
Interaktion med Clopidogrel
Undvik samtidig användning av PRILOSEC 10 mg och klopidogrel. Clopidogrel är en prodrug. Hämning av trombocytaggregation av klopidogrel beror helt på en aktiv metabolit. Metabolismen av klopidogrel till dess aktiva metabolit kan försämras vid användning med samtidig medicinering, såsom omeprazol, som hämmar CYP2C19-aktivitet. Samtidig användning av klopidogrel och 80 mg omeprazol minskar den farmakologiska aktiviteten av klopidogrel, även när det administreras med 12 timmars mellanrum.
När du använder PRILOSEC, överväg alternativ anti-trombocytbehandling [se LÄKEMEDELSINTERAKTIONER och KLINISK FARMAKOLOGI ].
Cyanokobalamin (Vitamin B-12) Brist
Daglig behandling med syradämpande mediciner under en lång tidsperiod (t.ex. längre än 3 år) kan leda till malabsorption av cyanokobalamin (vitamin B-12) orsakad av hypo- eller aklorhydri. Sällsynta rapporter om cyanokobalaminbrist som inträffat vid syrahämmande behandling har rapporterats i litteraturen. Denna diagnos bör övervägas om kliniska symtom som överensstämmer med cyanokobalaminbrist observeras hos patienter som behandlas med PRILOSEC.
Hypomagnesemi och mineralmetabolism
Hypomagnesemi, symtomatisk och asymtomatisk, har i sällsynta fall rapporterats hos patienter som behandlats med PPI under minst tre månader, i de flesta fall efter ett års behandling. Allvarliga biverkningar inkluderar stelkramp, arytmier och kramper. Hypomagnesemi kan leda till hypokalcemi och/eller hypokalemi och kan förvärra underliggande hypokalcemi hos riskpatienter. Hos de flesta patienter krävde behandling av hypomagnesemi magnesiumersättning och avbrytande av PPI.
För patienter som förväntas vara på långvarig behandling eller som tar PPI tillsammans med mediciner som digoxin eller läkemedel som kan orsaka hypomagnesemi (t.ex. diuretika), kan sjukvårdspersonal överväga att övervaka magnesiumnivåerna innan PPI-behandlingen påbörjas och med jämna mellanrum [se NEGATIVA REAKTIONER ].
Överväg att övervaka magnesium- och kalciumnivåerna innan behandling med PRILOSEC påbörjas och regelbundet under behandling hos patienter med en redan existerande risk för hypokalcemi (t.ex. hypoparatyreos). Komplettera med magnesium och/eller kalcium vid behov. Om hypokalcemi är behandlingsrefraktär, överväg att avbryta PPI.
Interaktion med johannesört eller rifampin
Läkemedel som inducerar CYP2C19 eller CYP3A4 (som johannesört eller rifampin) kan avsevärt minska omeprazolkoncentrationerna [se LÄKEMEDELSINTERAKTIONER ]. Undvik samtidig användning av PRILOSEC och johannesört eller rifampin.
Interaktioner med diagnostiska undersökningar för neuroendokrina tumörer
Serumkromogranin A (CgA)-nivåer ökar sekundärt till läkemedelsinducerade minskningar i magsyra. Den ökade CgA-nivån kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer. Vårdgivare bör tillfälligt avbryta behandlingen med PRILOSEC 20 mg minst 14 dagar innan CgA-nivåerna bedöms och överväga att upprepa testet om de initiala CgA-nivåerna är höga. Om serietest utförs (t.ex. för övervakning), bör samma kommersiella laboratorium användas för testning, eftersom referensintervallen mellan testerna kan variera [se LÄKEMEDELSINTERAKTIONER ].
Interaktion med metotrexat
Litteraturen tyder på att samtidig användning av PPI med metotrexat (främst i höga doser) kan höja och förlänga serumnivåerna av metotrexat och/eller dess metabolit, vilket kan leda till metotrexattoxicitet. Vid administrering av högdos metotrexat kan ett tillfälligt utsättande av PPI övervägas hos vissa patienter [se LÄKEMEDELSINTERAKTIONER ].
Fundic körtelpolyper
PPI-användning är förknippad med en ökad risk för fundiska körtelpolyper som ökar vid långvarig användning, särskilt efter ett år. De flesta PPI-användare som utvecklade fundic gland polyper var asymtomatiska och fundic gland polyper identifierades tillfälligt vid endoskopi. Använd den kortaste varaktigheten av PPI-behandlingen som är lämplig för det tillstånd som behandlas.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide och bruksanvisning ).
Akut Tubulointerstitiell nefrit
Råda patienten eller vårdgivaren att omedelbart ringa patientens vårdgivare om de upplever tecken och/eller symtom associerade med akut tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Clostridium Difficile-associerad diarré
Råda patienten eller vårdgivaren att omedelbart ringa patientens vårdgivare om de upplever diarré som inte förbättras [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Benfraktur
Råda patienten eller vårdgivaren att rapportera eventuella frakturer, särskilt på höften, handleden eller ryggraden, till patientens vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Allvarliga kutana biverkningar
Råda patienten eller vårdgivaren att avbryta behandlingen med PRILOSEC 40 mg och rapportera till sin vårdgivare vid första uppkomsten av en allvarlig kutan biverkning eller andra tecken på överkänslighet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kutan och systemisk lupus erythematosus
Rekommendera patienten eller vårdgivaren att omedelbart ringa patientens vårdgivare för alla nya eller försämrade symtom associerade med kutan eller systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Cyanokobalamin (Vitamin B-12) Brist
Rekommendera patienten eller vårdgivaren att rapportera alla kliniska symtom som kan vara associerade med cyanokobalaminbrist till patientens vårdgivare om de har fått PRILOSEC i mer än 3 år [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hypomagnesemi och mineralmetabolism
Rekommendera patienten eller vårdgivaren att rapportera alla kliniska symtom som kan vara associerade med hypomagnesemi, hypokalcemi och/eller hypokalemi, till patientens vårdgivare, om de har fått PRILOSEC i minst 3 månader [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Läkemedelsinteraktioner
Råda patienter att rapportera till sin vårdgivare om de påbörjar behandling med produkter som innehåller rilpivirin, klopidogrel, johannesört eller rifampin; eller, om de tar högdos metotrexat [se KONTRAINDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Administrering
- PRILOSEC är avsett att beredas i vatten och administreras oralt eller via en nasogastrisk (NG) eller magsond, enligt beskrivningen i medicineringsguiden.
- Ta PRILOSEC före måltid.
- Antacida kan användas samtidigt med PRILOSEC.
- Missade doser: Om en dos missas, administrera så snart som möjligt. Men om nästa schemalagda dos är beräknad, ta inte den missade dosen och ta nästa dos i tid. Ta inte två doser samtidigt för att kompensera för en missad dos.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
två 24-månaders karcinogenicitetsstudier på råttor, omeprazol i dagliga doser på 1,7, 3,4, 13,8, 44,0 och 140,8 mg/kg/dag (cirka 0,4 till 34 gånger en human dos på 40 mg/dag, uttryckt på en kroppsyta areabas) producerade gastriska ECL-cellkarcinoider på ett dosrelaterat sätt i både han- och honråttor; förekomsten av denna effekt var markant högre hos honråttor, som hade högre blodnivåer av omeprazol. Magkarcinoider förekommer sällan hos obehandlad råtta. Dessutom var ECL-cellshyperplasi närvarande i alla behandlade grupper av båda könen. I en av dessa studier behandlades honråttor med 13,8 mg omeprazol/kg/dag (cirka 3,4 gånger en human dos på 40 mg/dag, baserat på kroppsyta) under ett år, och följdes sedan under ytterligare ett år utan läkemedel. Inga karcinoider sågs hos dessa råttor. En ökad incidens av behandlingsrelaterad ECL-cellshyperplasi observerades vid slutet av ett år (94 % behandlade vs. 10 % kontroller). Vid det andra året var skillnaden mellan behandlade och kontrollråttor mycket mindre (46 % mot 26 %) men visade fortfarande mer hyperplasi i den behandlade gruppen. Gastriskt adenokarcinom sågs hos en råtta (2%). Ingen liknande tumör sågs hos han- eller honråttor som behandlats under två år. För denna råttstam har ingen liknande tumör noterats historiskt, men ett fynd som involverar endast en tumör är svårt att tolka. I en 52-veckors toxicitetsstudie på Sprague-Dawley-råttor hittades hjärnastrocytom hos ett litet antal hanar som fick omeprazol i dosnivåer på 0,4, 2 och 16 mg/kg/dag (cirka 0,1 till 3,9 gånger den mänskliga dosen 40 mg/dag, baserat på kroppsyta). Inga astrocytom observerades hos honråttor i denna studie. I en 2-årig karcinogenicitetsstudie på Sprague-Dawley-råttor hittades inga astrocytom hos hanar eller honor med den höga dosen 140,8 mg/kg/dag (cirka 34 gånger den mänskliga dosen på 40 mg/dag på basis av kroppsyta). . En 78-veckors karcinogenicitetsstudie på mus av omeprazol visade inte ökad förekomst av tumörer, men studien var inte avgörande. En 26-veckors p53 (+/-) transgen mus carcinogenicitetsstudie var inte positiv.
Omeprazol var positivt för klastogena effekter i en kromosomavvikelsetest av humana lymfocyter in vitro, i ett av två mikrokärntest på mus in vivo och i en kromosomavvikelsetest av benmärgsceller in vivo. Omeprazol var negativ i Ames-testet in vitro, en in vitro-analys av muslymfomceller framåtmutation och en in vivo-analys av lever-DNA-skada från råtta.
Omeprazol vid orala doser upp till 138 mg/kg/dag hos råttor (cirka 34 gånger en oral human dos på 40 mg på basis av kroppsyta) visade sig inte ha någon effekt på fertilitet och reproduktionsförmåga.
I 24-månaders karcinogenicitetsstudier på råttor observerades en dosrelaterad signifikant ökning av gastriska karcinoida tumörer och ECL-cellshyperplasi hos både han- och hondjur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Karcinoida tumörer har också observerats hos råttor som utsatts för fundektomi eller långtidsbehandling med andra protonpumpshämmare eller höga doser av H2-receptorantagonister.
Användning i specifika populationer
Graviditet
Risksammanfattning
Det finns inga adekvata och välkontrollerade studier med omeprazol på gravida kvinnor. Tillgängliga epidemiologiska data visar inte på en ökad risk för allvarliga medfödda missbildningar eller andra negativa graviditetsresultat vid användning av omeprazol i första trimestern. Reproduktionsstudier på råttor och kaniner resulterade i dosberoende embryodödlighet vid omeprazoldoser som var cirka 3,4 till 34 gånger en oral human dos på 40 mg (baserat på en kroppsyta för en person på 60 kg).
Teratogenicitet observerades inte i reproduktionsstudier på djur med administrering av oral esomeprazol (en enantiomer av omeprazol) magnesium hos råttor och kaniner under organogenes med doser cirka 68 gånger respektive 42 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol baserat på kroppsyta för en person på 60 kg).
Förändringar i benmorfologi observerades hos avkommor till råttor som doserades under större delen av dräktigheten och laktationen i doser lika med eller större än cirka 34 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol. När maternell administrering var begränsad till enbart dräktighet, fanns det inga effekter på benfysisk morfologi hos avkomman vid någon ålder [se Data ].
De uppskattade bakgrundsriskerna för stora fosterskador och missfall för den indikerade populationen är okända. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Data
Mänskliga data
Fyra publicerade epidemiologiska studier jämförde frekvensen av medfödda abnormiteter bland spädbarn födda av kvinnor som använde omeprazol under graviditeten med frekvensen av abnormiteter bland spädbarn till kvinnor som exponerats för H2-receptorantagonister eller andra kontroller.
En populationsbaserad retrospektiv kohort epidemiologisk studie från Svenska medicinska födelseregistret, som täckte cirka 99 % av graviditeterna, från 1995 till 99, rapporterade om 955 spädbarn (824 exponerade under första trimestern med 39 av dessa exponerade efter första trimestern, och 131 exponerade efter första trimestern) vars mödrar använde omeprazol under graviditeten. Antalet spädbarn som exponerades in utero för omeprazol som hade någon missbildning, låg födelsevikt, låg Apgar-poäng eller sjukhusvistelse var liknande det antal som observerades i denna population. Antalet spädbarn födda med ventrikulära septumdefekter och antalet dödfödda spädbarn var något högre hos de omeprazolexponerade spädbarnen än det förväntade antalet i denna population.
En populationsbaserad retrospektiv kohortstudie som täckte alla levande födda i Danmark från 1996 till 2009, rapporterade 1 800 levande födda barn vars mödrar använde omeprazol under graviditetens första trimester och 837 317 levande födda barn vars mödrar inte använde någon protonpumpshämmare. Den totala andelen fosterskador hos spädbarn födda av mödrar med exponering för omeprazol i första trimestern var 2,9 % och 2,6 % hos spädbarn födda till mödrar som inte exponerats för någon protonpumpshämmare under den första trimestern.
En retrospektiv kohortstudie rapporterade på 689 gravida kvinnor som exponerades för antingen H2-blockerare eller omeprazol under första trimestern (134 exponerade för omeprazol) och 1 572 gravida kvinnor som inte exponerades för någondera under första trimestern. Den totala missbildningsfrekvensen hos avkommor födda till mödrar med exponering för omeprazol i första trimestern, en H2-blockerare, eller var oexponerade var 3,6 %, 5,5 % respektive 4,1 %.
En liten prospektiv observationskohortstudie följde 113 kvinnor som exponerats för omeprazol under graviditeten (89 % med exponeringar i första trimestern). Den rapporterade frekvensen av allvarliga medfödda missbildningar var 4 % i omeprazolgruppen, 2 % i kontroller exponerade för icke-teratogener och 2,8 % i sjukdomsparade kontroller. Antalet spontana och elektiva aborter, prematura förlossningar, graviditetsålder vid förlossningen och genomsnittlig födelsevikt var likartade bland grupperna.
Flera studier har inte rapporterat några uppenbara negativa korttidseffekter på spädbarnet när engångsdos oral eller intravenös omeprazol administrerades till över 200 gravida kvinnor som premedicinering för kejsarsnitt under allmän anestesi.
Djurdata
Omeprazol
Reproduktionsstudier utförda med omeprazol på råttor vid orala doser upp till 138 mg/kg/dag (ca 34 gånger en oral human dos på 40 mg på basis av kroppsyta) och på kaniner vid doser upp till 69,1 mg/kg/dag ( cirka 34 gånger en oral human dos på 40 mg på basis av kroppsyta) under organogenesen avslöjade inga bevis för en teratogen potential hos omeprazol. Hos kaniner gav omeprazol i ett dosintervall på 6,9 till 69,1 mg/kg/dag (cirka 3,4 till 34 gånger en oral human dos på 40 mg på kroppsytabasis) administrerat under organogenes dosrelaterade ökningar av embryodödlighet, fosterresorptioner och graviditetsstörningar. Hos råttor observerades dosrelaterad embryo-/fostertoxicitet och postnatal utvecklingstoxicitet hos avkommor från föräldrar som behandlats med omeprazol i 13,8 till 138,0 mg/kg/dag (ca 3,4 till 34 gånger en oral humandos på 40 mg på en kroppsyta areabas), administreras före parning under laktationsperioden.
Esomeprazol
Data som beskrivs nedan genererades från studier med användning av esomeprazol, en enantiomer av omeprazol. Dosmultipel från djur till människa är baserad på antagandet om lika systemisk exponering för esomeprazol hos människor efter oral administrering av antingen 40 mg esomeprazol eller 40 mg omeprazol.
Inga effekter på embryo-fosterutveckling observerades i reproduktionsstudier med esomeprazolmagnesium på råttor vid orala doser upp till 280 mg/kg/dag (cirka 68 gånger en oral human dos på 40 mg på basis av kroppsyta) eller på kaniner vid orala doser upp till 86 mg/kg/dag (cirka 42 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta) administrerade under organogenesen.
En pre- och postnatal utvecklingstoxicitetsstudie på råttor med ytterligare effektmått för att utvärdera benutveckling utfördes med esomeprazolmagnesium i orala doser på 14 till 280 mg/kg/dag (ca 3,4 till 68 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta). Neonatal/tidig postnatal (födsel till avvänjning) överlevnad minskade vid doser lika med eller större än 138 mg/kg/dag (cirka 34 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta). Kroppsvikt och viktökning minskade och neurobeteende eller allmänna utvecklingsförseningar under den omedelbara tidsramen efter avvänjning var uppenbara vid doser lika med eller större än 69 mg/kg/dag (cirka 17 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta). Dessutom noterades minskad lårbenslängd, bredd och tjocklek av kortikalt ben, minskad tjocklek på tibial tillväxtplatta och minimal till mild benmärgshypocellularitet vid doser lika med eller större än 14 mg/kg/dag (ca 3,4 gånger en oral människa dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta). Fysisk dysplasi i lårbenet observerades hos avkommor till råttor som behandlats med orala doser av esomeprazolmagnesium i doser lika med eller större än 138 mg/kg/dag (cirka 34 gånger en oral humandos på 40 mg esomeprazol eller 40 mg omeprazol på en kropp ytarea).
Effekter på moderns ben observerades hos dräktiga och ammande råttor i den pre- och postnatala toxicitetsstudien när esomeprazolmagnesium administrerades i orala doser på 14 till 280 mg/kg/dag (cirka 3,4 till 68 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta). När råttor doserades från graviditetsdag 7 till avvänjning på postnatal dag 21, observerades en statistiskt signifikant minskning av moderns lårbensvikt på upp till 14 % (jämfört med placebobehandling) vid doser lika med eller större än 138 mg/kg/dag (cirka 34 gånger en oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta).
En pre- och postnatal utvecklingsstudie på råttor med esomeprazol strontium (med ekvimolära doser jämfört med esomeprazolmagnesiumstudie) gav liknande resultat på mödrar och ungar som beskrivits ovan.
En uppföljningsstudie av utvecklingstoxicitet på råttor med ytterligare tidpunkter för att utvärdera utvecklingen av ungben från postnatal dag 2 till vuxen ålder utfördes med esomeprazolmagnesium i orala doser på 280 mg/kg/dag (cirka 68 gånger en oral human dos på 40 mg på baserat på kroppsyta) där administrering av esomeprazol var från antingen graviditetsdag 7 eller graviditetsdag 16 fram till förlossningen. När maternell administrering var begränsad till enbart graviditet, fanns det inga effekter på benfysisk morfologi hos avkomman vid någon ålder.
Laktation
Risksammanfattning
Begränsade data tyder på att omeprazol kan finnas i bröstmjölk. Det finns inga kliniska data om effekterna av omeprazol på det ammade barnet eller på mjölkproduktionen. Utvecklings- och hälsofördelarna med amning bör övervägas tillsammans med moderns kliniska behov av PRILOSEC 40 mg och eventuella negativa effekter på det ammade barnet från PRILOSEC 20 mg eller från det underliggande moderns tillståndet.
Pediatrisk användning
Säkerheten och effektiviteten av PRILOSEC 40 mg har fastställts hos pediatriska patienter 1 till 16 år för behandling av symtomatisk GERD, behandling av EE på grund av syramedierad GERD och upprätthållande av läkning av EE på grund av syramedierad GERD. Användning av PRILOSEC 10 mg i denna åldersgrupp stöds av adekvata och välkontrollerade studier på vuxna och okontrollerade säkerhets-, effekt- och farmakokinetiska studier utförda på pediatriska och ungdomar [se KLINISK FARMAKOLOGI , Kliniska studier ].
Säkerheten och effektiviteten av PRILOSEC 10 mg har fastställts hos pediatriska patienter från 1 månad till yngre än 1 år för behandling av EE på grund av syramedierad GERD och stöds av adekvata och välkontrollerade studier på vuxna och säkerhet, farmakokinetik, och farmakodynamiska studier utförda på pediatriska patienter [se KLINISK FARMAKOLOGI ].
I den pediatriska populationen rapporterades ofta biverkningar av andningsorganen i hela åldersgruppen (1 månad till 16 år). Öroninflammation rapporterades ofta i åldersgruppen 1 månad till NEGATIVA REAKTIONER ].
Säkerheten och effektiviteten för PRILOSEC har inte fastställts i:
- patienter yngre än 1 år för:
- Behandling av symtomatisk GERD
- Upprätthållande av läkning av EE på grund av syramedierad GERD
- pediatriska patienter för:
- Behandling av aktivt duodenalsår
- H. pylori-utrotning för att minska risken för återfall av duodenalsår
- Behandling av aktivt benignt magsår
- Patologiska hypersekretoriska tillstånd
- patienter yngre än 1 månad för någon indikation.
Data från unga djur
Esomeprazol, en enantiomer av omeprazol, visade sig minska kroppsvikt, kroppsviktsökning, lårbensvikt, lårbenslängd och total tillväxt vid orala doser cirka 34 till 68 gånger en daglig dos för människa på 40 mg esomeprazol eller 40 mg omeprazol baserat på kropp ytarea i en toxicitetsstudie av juvenil råtta. Dosmultipel från djur till människa är baserad på antagandet om lika systemisk exponering för esomeprazol hos människor efter oral administrering av antingen 40 mg esomeprazol eller 40 mg omeprazol.
En 28-dagars toxicitetsstudie med en 14-dagars återhämtningsfas utfördes på unga råttor med esomeprazolmagnesium i doser på 70 till 280 mg/kg/dag (cirka 17 till 68 gånger en daglig oral human dos på 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta). En ökning av antalet dödsfall vid den höga dosen på 280 mg/kg/dag observerades när juvenila råttor administrerades esomeprazolmagnesium från postnatal dag 7 till postnatal dag 35. Dessutom doser lika med eller större än 140 mg/kg/ dag (cirka 34 gånger en daglig oral human dos av 40 mg esomeprazol eller 40 mg omeprazol på basis av kroppsyta), gav behandlingsrelaterade minskningar i kroppsvikt (cirka 14 %) och kroppsviktsökning, minskningar i lårbensvikt och lårben. längd och påverkade den totala tillväxten. Jämförbara fynd som beskrivs ovan har också observerats i denna studie med ett annat esomeprazolsalt, esomeprazol strontium, vid ekvimolära doser av esomeprazol.
Geriatrisk användning
Omeprazol administrerades till över 2 000 äldre personer (≥ 65 år) i kliniska prövningar i USA och Europa. Det fanns inga skillnader i säkerhet och effektivitet mellan äldre och yngre försökspersoner. Andra rapporterade kliniska erfarenheter har inte identifierat skillnader i svar mellan äldre och yngre försökspersoner, men större känslighet hos vissa äldre individer kan inte uteslutas.
Farmakokinetiska studier har visat att eliminationshastigheten minskade något hos äldre och biotillgängligheten ökade. Plasmaclearance av omeprazol var 250 ml/min (ungefär hälften av det för unga frivilliga) och dess plasmahalveringstid var i genomsnitt en timme, ungefär dubbelt så högt som för unga friska frivilliga. Ingen dosjustering är dock nödvändig hos äldre [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Hos patienter med nedsatt leverfunktion (Child-Pugh klass A, B eller C) ökade exponeringen för omeprazol avsevärt jämfört med friska försökspersoner. Dosreduktion av PRILOSEC 10 mg till 10 mg en gång dagligen rekommenderas för patienter med nedsatt leverfunktion för att upprätthålla läkning av EE [se DOSERING OCH ADMINISTRERING , KLINISK FARMAKOLOGI ].
Asiatisk befolkning
I studier av friska försökspersoner hade asiater ungefär fyra gånger högre exponering än kaukasier. Dosminskning av PRILOSEC 20 mg till 10 mg en gång dagligen rekommenderas för asiatiska patienter för upprätthållande av läkning av EE [se DOSERING OCH ADMINISTRERING , KLINISK FARMAKOLOGI ].
ÖVERDOS
Rapporter har mottagits om överdosering av omeprazol hos människor. Doserna varierade upp till 2400 mg (120 gånger den vanliga rekommenderade kliniska dosen). Manifestationerna var varierande, men inkluderade förvirring, dåsighet, dimsyn, takykardi, illamående, kräkningar, diafores, rodnad, huvudvärk, muntorrhet och andra biverkningar som liknar de som ses i normal klinisk erfarenhet [se NEGATIVA REAKTIONER ]. Symtomen var övergående och inga allvarliga kliniska resultat har rapporterats när PRILOSEC 20 mg togs enbart. Ingen specifik motgift för överdosering av omeprazol är känd.
Omeprazol är i hög grad proteinbundet och är därför inte lätt dialyserbart. I händelse av överdosering ska behandlingen vara symptomatisk och stödjande.
Om överexponering inträffar, ring ditt giftkontrollcenter på 1-800-222-1222 för aktuell information om hantering av förgiftning eller överdosering.
KONTRAINDIKATIONER
- PRILOSEC är kontraindicerat hos patienter med känd överkänslighet mot substituerade bensimidazoler eller mot någon komponent i formuleringen. Överkänslighetsreaktioner kan inkludera anafylaxi, anafylaktisk chock, angioödem, bronkospasm, akut tubulointerstitiell nefrit och urtikaria [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
- Protonpumpshämmare (PPI), inklusive PRILOSEC 10 mg, är kontraindicerade hos patienter som får produkter som innehåller rilpivirin [se LÄKEMEDELSINTERAKTIONER ].
- För information om kontraindikationer för antibakteriella medel (klaritromycin och amoxicillin) indikerade i kombination med PRILOSEC 40 mg, se avsnittet KONTRAINDIKATIONER i deras bipacksedel.
KLINISK FARMAKOLOGI
Handlingsmekanism
Omeprazol tillhör en klass av antisekretoriska föreningar, de substituerade bensimidazolerna, som undertrycker magsyrasekretion genom specifik hämning av H+/K+ ATPas-enzymsystemet vid den sekretoriska ytan av magparietalcellen. Eftersom detta enzymsystem betraktas som syrapumpen (proton) i magslemhinnan, har omeprazol karakteriserats som en magsyrapumpshämmare genom att det blockerar det sista steget i syraproduktionen. Denna effekt är dosrelaterad och leder till hämning av både basal och stimulerad syrasekretion oavsett stimulans.
Farmakodynamik
Antisekretorisk aktivitet
Efter oral administrering inträder den antisekretoriska effekten av omeprazol inom en timme, med den maximala effekten inom två timmar. Hämning av utsöndring är cirka 50 % av maximum vid 24 timmar och varaktigheten av hämningen varar upp till 72 timmar. Den antisekretoriska effekten varar således mycket längre än vad som skulle förväntas från den mycket korta (mindre än en timme) plasmahalveringstiden, uppenbarligen på grund av förlängd bindning till parietal H+/K+ ATPas-enzymet. När läkemedlet avbryts återgår sekretorisk aktivitet gradvis, under 3 till 5 dagar. Den hämmande effekten av omeprazolonsyrasekretion ökar med upprepad dosering en gång dagligen och når en platå efter fyra dagar.
Resultat från ett flertal studier av den antisekretoriska effekten av flera doser på 20 mg och 40 mg omeprazol hos friska försökspersoner och patienter visas nedan. "max"-värdet representerar bestämningar vid en tidpunkt för maximal effekt (2 till 6 timmar efter dosering), medan "min"-värden är de 24 timmar efter den sista dosen av omeprazol.
Enstaka dagliga orala doser av omeprazol som sträcker sig från en dos på 10 mg till 40 mg har producerat 100 % hämning av 24-timmars intragastrisk surhet hos vissa patienter.
Serum Gastrin Effekter
studier som involverade mer än 200 patienter ökade serumgastrinnivåerna under de första 1 till 2 veckorna av administrering en gång dagligen av terapeutiska doser av omeprazol parallellt med hämning av syrasekretionen. Ingen ytterligare ökning av serumgastrin inträffade vid fortsatt behandling. Jämfört med histamin H2-receptorantagonister var medianökningarna producerade av 20 mg doser av omeprazol högre (1,3 till 3,6 gånger jämfört med 1,1 till 1,8 gånger ökning). Gastrinvärdena återgick till nivåerna före behandling, vanligtvis inom 1 till 2 veckor efter avslutad behandling.
Ökat gastrin orsakar enterokromaffinliknande cellhyperplasi och ökade serumnivåer av kromogranin A (CgA). De ökade CgA-nivåerna kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Enterokromaffinliknande (ECL) celleffekter
Humana gastriska biopsiprover har erhållits från mer än 3000 patienter (både barn och vuxna) som behandlats med omeprazol i kliniska långtidsstudier. Incidensen av ECL-cellshyperplasi i dessa studier ökade med tiden; dock har inget fall av ECL-cellkarcinoider, dysplasi eller neoplasi hittats hos dessa patienter. Dessa studier är emellertid av otillräcklig varaktighet och storlek för att utesluta den möjliga inverkan av långtidsadministrering av omeprazol på utvecklingen av premaligna eller maligna tillstånd.
Andra effekter
Systemiska effekter av omeprazol i CNS, kardiovaskulära system och andningsorgan har hittills inte hittats. Omeprazol, givet i orala doser på 30 eller 40 mg under 2 till 4 veckor, hade ingen effekt på sköldkörtelfunktionen, kolhydratmetabolismen eller cirkulerande nivåer av bisköldkörtelhormon, kortisol, östradiol, testosteron, prolaktin, kolecystokinin eller sekretin.
Ingen effekt på magtömningen av de fasta och flytande komponenterna i en testmåltid visades efter en engångsdos av omeprazol 90 mg. Hos friska försökspersoner hade en intravenös engångsdos av omeprazol (0,35 mg/kg) ingen effekt på utsöndring av inre faktor. Ingen systematisk dosberoende effekt har observerats på basal eller stimulerad pepsinproduktion hos människor.
Men när det intragastriska pH hålls vid 4,0 eller högre är basal pepsinproduktion låg och pepsinaktiviteten minskar.
Liksom andra medel som höjer det intragastriska pH, gav omeprazol administrerat i 14 dagar till friska försökspersoner en signifikant ökning av de intragastriska koncentrationerna av livskraftiga bakterier. Mönstret för bakteriearterna var oförändrat från det som vanligtvis finns i saliv. Alla förändringar försvann inom tre dagar efter avslutad behandling.
Förloppet av Barretts matstrupe hos 106 patienter utvärderades i en amerikansk dubbelblind kontrollerad studie av PRILOSEC 40 mg två gånger dagligen i 12 månader följt av 20 mg två gånger dagligen i 12 månader eller ranitidin 300 mg två gånger dagligen i 24 månader. Ingen kliniskt signifikant påverkan på Barretts slemhinna av antisekretorisk terapi observerades. Även om neosquamöst epitel utvecklades under antisekretorisk terapi, uppnåddes inte fullständig eliminering av Barretts slemhinna. Ingen signifikant skillnad observerades mellan behandlingsgrupper i utveckling av dysplasi i Barretts slemhinna och ingen patient utvecklade matstrupscancer under behandlingen. Inga signifikanta skillnader mellan behandlingsgrupperna observerades i utveckling av ECL-cellshyperplasi, corpus atrofisk gastrit, corpus intestinal metaplasi eller kolonpolyper som översteg 3 mm i diameter.
Farmakokinetik
Absorption
PRILOSEC 20 mg för oral suspension med fördröjd frisättning innehåller omeprazolmagnesiumgranulat och inaktiva granulat som ska administreras i vatten. Absorptionen av omeprazol börjar först efter att de gastroresistenta granulerna lämnar magen. Farmakokinetiken för omeprazol är tidsberoende, med högre plasmakoncentrationer vid steady state jämfört med efter en engångsdos. Den systemiska exponeringen (AUC och Cmax) för omeprazol efter dosering en gång dagligen av 20 mg oral suspension med fördröjd frisättning under 5 dagar är 51 % respektive 58 % högre än efter den första dosen. Maximala plasmakoncentrationer av omeprazol efter upprepade doser av oral suspension med fördröjd frisättning inträffar inom 1,5 till 2 timmar. Hos friska försökspersoner är plasmahalveringstiden 0,5 till 1 timme.
Distribution
Proteinbindningen är cirka 95%.
Eliminering
Ämnesomsättning
Omeprazol metaboliseras i stor utsträckning av enzymsystemet cytokrom P450 (CYP). Huvuddelen av dess metabolism är beroende av det polymorft uttryckta CYP2C19, som ansvarar för bildningen av hydroxiomeprazol, huvudmetaboliten i plasma. Den återstående delen är beroende av en annan specifik isoform, CYP3A4, ansvarig för bildandet av omeprazolsulfon.
Exkretion
Efter oral administrering av en buffrad lösning av omeprazol, utsöndrades lite om något oförändrat läkemedel i urinen. Majoriteten av dosen (cirka 77 %) eliminerades i urinen som minst sex metaboliter. Två identifierades som hydroxiomeprazol och motsvarande karboxylsyra. Resten av dosen kunde återvinnas i avföring. Detta innebär en betydande gallutsöndring av metaboliterna av omeprazol. Tre metaboliter har identifierats i plasma, sulfid- och sulfonderivaten av omeprazol och hydroxiomeprazol. Dessa metaboliter har mycket liten eller ingen antisekretorisk aktivitet.
Kombinationsterapi med antimikrobiella medel
Omeprazol 40 mg dagligen gavs i kombination med klaritromycin 500 mg var 8:e timme till friska vuxna manliga försökspersoner. Plasmakoncentrationerna av omeprazol vid steady state ökade (Cmax, AUC0-24 och T½ ökningar med 30 %, 89 % respektive 34 %) vid samtidig administrering av klaritromycin. De observerade ökningarna av omeprazols plasmakoncentration var associerade med följande farmakologiska effekter. Det genomsnittliga 24-timmars pH-värdet i magsäcken var när omeprazol administrerades ensamt och 5,7 när det administrerades samtidigt med klaritromycin.
Plasmakoncentrationerna av klaritromycin och 14-hydroxi-klaritromycin ökade vid samtidig administrering av omeprazol. För klaritromycin var medel-Cmax 10% högre, medel-Cmin var 27% högre och medel-AUC0-8 var 15% högre när klaritromycin administrerades med omeprazol än när klaritromycin administrerades ensamt. Liknande resultat sågs för 14-hydroxi-klaritromycin, medel-Cmax var 45% högre, medel-Cmin var 57% högre och medel-AUC0-8 var 45% högre. Klaritromycinkoncentrationerna i magvävnaden och slemmet ökade också vid samtidig administrering av omeprazol.
Specifika populationer
Geriatriska patienter
Elimineringshastigheten för omeprazol minskade något hos äldre och biotillgängligheten ökade. Omeprazol var 76 % biotillgängligt när en enstaka 40 mg oral dos av omeprazol (buffrad lösning) gavs till friska äldre frivilliga försökspersoner, jämfört med 58 % hos unga frivilliga som fick samma dos. Nästan 70 % av dosen återfanns i urinen som metaboliter av omeprazol och inget oförändrat läkemedel upptäcktes. Plasmaclearance av omeprazol var 250 ml/min (ungefär hälften av det för unga frivilliga) och dess plasmahalveringstid var i genomsnitt en timme, ungefär dubbelt så högt som för unga friska frivilliga.
Pediatriska patienter
2 till 16 års ålder
Farmakokinetiken för omeprazol har undersökts hos pediatriska patienter i åldern 2 till 16 år:
Efter jämförbara mg/kg doser av omeprazol har yngre barn (2 till 5 år) lägre AUC än barn 6 till 16 år eller vuxna; AUC för de två sistnämnda grupperna skilde sig inte [se DOSERING OCH ADMINISTRERING ].
1 till 11 månaders ålder
En populationsfarmakokinetikmodell användes för att bestämma lämpliga doser av PRILOSEC 40 mg hos pediatriska patienter
1 månad till yngre än 1 år för behandling (upp till 6 veckor) av erosiv esofagit på grund av syramedierad GERD. Modellen baserades på data från 64 barn i åldern 0,5 månad till 16 år. Endast begränsade data fanns tillgängliga för barn yngre än 1 år. Omeprazol administrerades till pediatriska patienter i dessa studier som en oral suspension framställd av kapslarna med fördröjd frisättning. Pediatriska doser simulerades i åldersgruppen 1 till 11 månader för att uppnå jämförbar exponering för omeprazol med vuxna efter behandling med 20 mg en gång dagligen [se DOSERING OCH ADMINISTRERING ].
Ras eller etniska grupper
[Ser KLINISK FARMAKOLOGI ].
Patienter med nedsatt njurfunktion
Hos patienter med kroniskt nedsatt njurfunktion (kreatininclearance mellan 10 och 62 ml/min/1,73 m²) var fördelningen av omeprazol mycket lik den hos friska försökspersoner, även om det fanns en liten ökning av biotillgängligheten. Eftersom urinutsöndring är en primär utsöndringsväg för omeprazolmetaboliter, bromsades deras utsöndring i proportion till det minskade kreatininclearancen. Denna ökning av biotillgänglighet anses inte vara kliniskt betydelsefull.
Patienter med nedsatt leverfunktion
Hos patienter med kronisk leversjukdom klassificerad som Child-Pugh klass A (n=3), B (n=4) och C (n=1), ökade biotillgängligheten till cirka 100 % jämfört med friska försökspersoner, vilket återspeglar minskad första passage effekt, och plasmahalveringstiden för läkemedlet ökade till nästan 3 timmar jämfört med halveringstiden hos friska försökspersoner på 0,5 till 1 timme. Plasmaclearance var i genomsnitt 70 ml/min, jämfört med ett värde på 500 till 600 ml/min hos friska försökspersoner [se DOSERING OCH ADMINISTRERING , Användning i specifika populationer ].
Läkemedelsinteraktionsstudier
Effekt av omeprazol på andra droger
Omeprazol är en tidsberoende hämmare av CYP2C19 och kan öka den systemiska exponeringen av samtidigt administrerade läkemedel som är CYP2C19-substrat. Dessutom ökar administrering av omeprazol intragastriskt pH och kan förändra den systemiska exponeringen av vissa läkemedel som uppvisar pH-beroende löslighet.
Antiretrovirala medel
För vissa antiretrovirala läkemedel, såsom rilpivirin, atazanavir och nelfinavir, har minskade serumkoncentrationer rapporterats när de ges tillsammans med omeprazol [se LÄKEMEDELSINTERAKTIONER ].
Rilpivirin: Efter flera doser av rilpivirin (150 mg, dagligen) och omeprazol (20 mg, dagligen), minskade AUC med 40 %, Cmax med 40 % och Cmin med 33 % för rilpivirin.
Nelfinavir: Efter flera doser av nelfinavir (1250 mg, två gånger dagligen) och omeprazol (40 mg dagligen), minskade AUC med 36 % och 92 %, Cmax med 37 % och 89 % och Cmin med 39 % respektive 75 % för nelfinavir och M8 .
Atazanavir: Efter flera doser av atazanavir (400 mg, dagligen) och omeprazol (40 mg, dagligen, 2 timmar före atazanavir), minskade AUC med 94 %, Cmax med 96 % och Cmin med 95 %.
Saquinavir: Efter upprepad dosering av saquinavir/ritonavir (1000/100 mg) två gånger dagligen i 15 dagar med omeprazol 40 mg dagligen samtidigt administrerat dagarna 11 till 15.
AUC ökade med 82 %, Cmax med 75 % och Cmin med 106 %. Mekanismen bakom denna interaktion är inte helt klarlagd.
Clopidogrel
I en överkorsad klinisk studie fick 72 friska försökspersoner klopidogrel (300 mg laddningsdos följt av 75 mg per dag) enbart och med omeprazol (80 mg samtidigt som klopidogrel) i 5 dagar. Exponeringen för den aktiva metaboliten av klopidogrel minskade med 46 % (dag 1) och 42 % (dag 5) när klopidogrel och omeprazol administrerades tillsammans.
Resultat från en annan korsningsstudie på friska försökspersoner visade en liknande farmakokinetisk interaktion mellan klopidogrel (300 mg laddningsdos/75 mg daglig underhållsdos) och omeprazol 80 mg dagligen vid samtidig administrering i 30 dagar. Exponeringen för den aktiva metaboliten av klopidogrel minskade med 41 % till 46 % under denna tidsperiod.
I en annan studie gavs 72 friska försökspersoner samma doser av klopidogrel och 80 mg omeprazol men läkemedlen administrerades med 12 timmars mellanrum; resultaten var liknande, vilket tyder på att administrering av klopidogrel och omeprazol vid olika tidpunkter inte förhindrar deras interaktion [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ].
Mykofenolatmofetil
Administrering av omeprazol 20 mg två gånger dagligen under 4 dagar och en engångsdos på 1000 mg MMF cirka en timme efter den sista dosen av omeprazol till 12 friska försökspersoner i en cross-over-studie resulterade i en 52 % minskning av Cmax och 23 % minskning i AUC för MPA [se LÄKEMEDELSINTERAKTIONER ].
Cilostazol
Omeprazol verkar som en hämmare av CYP2C19. Omeprazol, givet i doser om 40 mg dagligen under en vecka till 20 friska försökspersoner i en cross-over-studie, ökade Cmax och AUC för cilostazol med 18 % respektive 26 %. Cmax och AUC för en av de aktiva metaboliterna, 3,4-dihydro-cilostazol, som har 4-7 gånger aktiviteten av cilostazol, ökade med 29% respektive 69%. Samtidig administrering av cilostazol och omeprazol förväntas öka koncentrationerna av cilostazol och den ovan nämnda aktiva metaboliten [se LÄKEMEDELSINTERAKTIONER ].
Diazepam
Samtidig administrering av omeprazol 20 mg en gång dagligen och diazepam 0,1 mg/kg givet intravenöst resulterade i 27 % minskning av clearance och 36 % ökning av diazepams halveringstid [se LÄKEMEDELSINTERAKTIONER ].
Digoxin
Samtidig administrering av omeprazol 20 mg en gång dagligen och digoxin hos friska försökspersoner ökade biotillgängligheten av digoxin med 10 % (30 % hos två försökspersoner) [se LÄKEMEDELSINTERAKTIONER ].
Effekt av andra droger på omeprazol
Vorikonazol
Samtidig administrering av omeprazol och voriconazol (en kombinerad hämmare av CYP2C19 och CYP3A4) resulterade i mer än en fördubbling av exponeringen för omeprazol. När vorikonazol (400 mg var 12:e timme under en dag, följt av 200 mg en gång dagligen i 6 dagar) gavs tillsammans med omeprazol (40 mg en gång dagligen i 7 dagar) till friska försökspersoner, var steady-state Cmax och AUC0-24 för omeprazol signifikant ökad: i genomsnitt 2 gånger (90 % KI: 1,8, 2,6) respektive 4 gånger (90 % KI: 3,3, 4,4), jämfört med när omeprazol gavs utan vorikonazol [se LÄKEMEDELSINTERAKTIONER ].
Mikrobiologi
Dubbelbehandling med omeprazol och klaritromycin och trippelbehandling med omeprazol, klaritromycin och amoxicillin har visat sig vara aktiva mot de flesta stammar av Helicobacter pylori in vitro och vid kliniska infektioner [se INDIKATIONER OCH ANVÄNDNING , Kliniska studier ].
Helicobacter pylori
Känslighetstestning av H. pylori-isolat utfördes för amoxicillin och klaritromycin med användning av metodik för utspädning av agar1, och lägsta hämmande koncentrationer (MIC) bestämdes.
Standardiserade förfaranden för känslighetstest kräver användning av laboratoriekontrollmikroorganismer för att kontrollera de tekniska aspekterna av laboratorieförfarandena.
Förbehandlingsmotstånd
Förbehandlingsresistensfrekvensen för klaritromycin var 3,5 % (4/113) i studierna med dubbelterapi omeprazol/klaritromycin (4 och 5) och 9,3% (41/439) i trippelterapistudier med omeprazol/klaritromycin/amoxicillin (1, 2 och 3).
Förbehandlingskänsliga isolat för amoxicillin (≤ 0,25 μg/ml) hittades hos 99,3 % (436/439) av patienterna i trippelterapistudierna omeprazol/klaritromycin/amoxicillin (1, 2 och 3). Amoxicillin förbehandling lägsta hämmande koncentrationer (MIC) > 0,25 μg/ml förekom hos 0,7 % (3/439) av patienterna, som alla var i studiegruppen klaritromycin och amoxicillin. En patient hade en obekräftad minsta hämmande amoxicillinkoncentration (MIC) för amoxicillin på > 256 μg/ml av Etest®.
Patienter som inte utrotats av H. pylori efter trippelbehandling med omeprazol/klaritromycin/amoxicillin eller dubbelbehandling med omeprazol/klaritromycin kommer sannolikt att ha klaritromycinresistenta H. pylori-isolat. Därför bör klaritromycinkänslighetstest göras om möjligt. Patienter med klaritromycinresistent H. pylori ska inte behandlas med något av följande: omeprazol/klaritromycin dubbelbehandling, omeprazol/klaritromycin/amoxicillin trippelbehandling eller andra kurer som inkluderar klaritromycin som det enda antimikrobiella medlet.
Amoxicillinkänslighetstestresultat och kliniska/bakteriologiska resultat
de kliniska prövningarna med trippelterapi utrotades 84,9 % (157/185) av patienterna i omeprazol/klaritromycin/amoxicillinbehandlingsgruppen som hade amoxicillinkänsliga MICs (≤ 0,25 μg/ml) för behandling av H. pylori och 285 % (185 μg/ml). /185) misslyckad terapi. Av de 28 patienter som misslyckades med trippelterapi hade 11 inga resultat från känslighetstest efter behandling och 17 hade H. pylori-isolat efter behandling med amoxicillinkänsliga MIC. Elva av patienterna som misslyckades med trippelterapi hade också H. pylori-isolat efter behandling med klaritromycinresistenta MIC.
Känslighetstest för Helicobacter pylori
För information om känslighetstestning om Helicobacter pylori, se avsnittet Mikrobiologi i förskrivningsinformation för klaritromycin och amoxicillin.
Effekter på gastrointestinal mikrobiell ekologi
Minskad surhet i magsäcken på grund av alla medel, inklusive protonpumpshämmare, ökar magräkningen av bakterier som normalt finns i mag-tarmkanalen. Behandling med protonpumpshämmare kan leda till något ökad risk för gastrointestinala infektioner som Salmonella och Campylobacter och, hos inlagda patienter, eventuellt även Clostridium difficile.
Farmakogenomik
CYP2C19, ett polymorft enzym, är involverat i metabolismen av omeprazol. CYP2C19*1-allelen är fullt funktionell medan CYP2C19*2- och *3-allelen är icke-funktionella. Det finns andra alleler associerade med ingen eller reducerad enzymfunktion. Patienter som bär på två fullt fungerande alleler är omfattande metaboliserare och de som bär två alleler med förlust av funktion är dåliga metaboliserare. Hos omfattande metaboliserare metaboliseras omeprazol primärt av CYP2C19.
Den systemiska exponeringen för omeprazol varierar med patientens ämnesomsättningsstatus: dåliga metaboliserare > mellanliggande metaboliserare > omfattande metaboliserare. Ungefär 3 % av kaukasierna och 15 till 20 % av asiterna är CYP2C19-fattiga metaboliserare.
I en farmakokinetisk studie av en engångsdos omeprazol på 20 mg var AUC för omeprazol hos asiatiska försökspersoner ungefär fyra gånger så högt som hos kaukasier [se DOSERING OCH ADMINISTRERING , Användning i specifika populationer ].
Kliniska studier
Aktivt duodenalsår
en multicenter, dubbelblind, placebokontrollerad studie av 147 patienter med endoskopiskt dokumenterat sår på tolvfingertarmen, var andelen patienter läkta (enligt protokoll) vid 2 och 4 veckor signifikant högre med omeprazolmagnesium kapslar med fördröjd frisättning 20 mg en gång dagligen än med placebo (p ≤ 0,01).
Behandling av aktivt duodenalsår % av patienterna läkta
Fullständig smärtlindring dag och natt inträffade signifikant snabbare (p ≤ 0,01) hos patienter som behandlades med omeprazolmagnesium kapslar med fördröjd frisättning 20 mg än hos patienter som behandlades med placebo. I slutet av studien hade signifikant fler patienter som hade fått omeprazolmagnesium kapslar med fördröjd frisättning fullständig lindring av smärta under dagen (p ≤ 0,05) och nattlig smärta (p ≤ 0,01).
en dubbelblind multicenterstudie av 293 patienter med endoskopiskt dokumenterat sår på tolvfingertarmen, var andelen patienter läkta (enligt protokoll) vid 4 veckor signifikant högre med omeprazolmagnesium kapslar med fördröjd frisättning 20 mg en gång dagligen än med ranitidin 150 mg två gånger dagligen ( p
Behandling av aktivt duodenalsår % av patienterna läkta
Läkning skedde signifikant snabbare hos patienter som behandlats med omeprazolmagnesium kapslar med fördröjd frisättning än hos de som behandlades med ranitidin 150 mg två gånger dagligen (p
I en utländsk multinationell randomiserad, dubbelblind studie av 105 patienter med endoskopiskt dokumenterat sår på tolvfingertarmen jämfördes 20 mg och 40 mg omeprazolmagnesium kapslar med fördröjd frisättning med 150 mg ranitidin två gånger dagligen vid 2, 4 och 8 veckor. Vid 2 och 4 veckor var båda doserna av PRILOSEC 10 mg statistiskt överlägsna (enligt protokoll) ranitidin, men 40 mg var inte överlägsen 20 mg omeprazolmagnesium kapslar med fördröjd frisättning, och vid 8 veckor fanns det ingen signifikant skillnad mellan någon av de aktiva droger.
Behandling av aktivt duodenalsår % av patienterna läkta
H. pylori-utrotning hos patienter med duodenalsår
Trippelterapi (omeprazol magnesium kapslar med fördröjd frisättning/klaritromycin/amoxicillin)
Tre amerikanska, randomiserade, dubbelblinda kliniska studier på patienter med H. pylori-infektion och duodenalsår (n = 558) jämförde omeprazolmagnesium kapslar med fördröjd frisättning plus klaritromycin plus amoxicillin med klaritromycin plus amoxicillin. Två studier (1 och 2) utfördes på patienter med ett aktivt sår på tolvfingertarmen, och den andra studien (3) utfördes på patienter med en historia av sår på tolvfingertarmen under de senaste 5 åren men utan sår vid tidpunkten för inskrivningen . Dosregimen i studierna var omeprazolmagnesium kapslar med fördröjd frisättning 20 mg två gånger dagligen plus klaritromycin 500 mg två gånger dagligen plus amoxicillin 1 g två gånger dagligen i 10 dagar; eller klaritromycin 500 mg två gånger dagligen plus amoxicillin 1 g två gånger dagligen i 10 dagar. I studier 1 och 2 fick patienter som tog omeprazolkuren också ytterligare 18 dagar med omeprazolmagnesium kapslar med fördröjd frisättning 20 mg en gång dagligen. Slutpunkter som studerades var utrotning av H. pylori och läkning av duodenalsår (endast studier 1 och 2). H. pylori-status bestämdes av CLOtest®, histologi och kultur i alla tre studierna. För en given patient ansågs H. pylori vara utrotad om minst två av dessa tester var negativa och ingen var positiv.
Kombinationen av omeprazol plus klaritromycin plus amoxicillin var effektiv för att utrota H. pylori.
Dubbelterapi (omeprazol magnesium kapslar med fördröjd frisättning/klaritromycin)
Fyra randomiserade, dubbelblinda, multicenterstudier (4, 5, 6 och 7) utvärderade omeprazolmagnesium kapslar med fördröjd frisättning 40 mg en gång dagligen plus klaritromycin 500 mg tre gånger dagligen i 14 dagar, följt av omeprazolmagnesium fördröjd frisättning kapslar 20 mg en gång dagligen (studier 4, 5 och 7) eller med omeprazol magnesium kapslar med fördröjd frisättning 40 mg en gång dagligen (studie 6) i ytterligare 14 dagar hos patienter med aktivt duodenalsår i samband med H. pylori. Studie 4 och 5 genomfördes i USA och Kanada och inkluderade 242 respektive 256 patienter. H. pylori-infektion och duodenalsår bekräftades hos 219 patienter i studie 4 och 228 patienter i studie 5. Dessa studier jämförde kombinationsregimen med omeprazolmagnesium kapslar med fördröjd frisättning och klaritromycinmonoterapier. Studie 6 och 7 genomfördes i Europa och inkluderade 154 respektive 215 patienter. H. pylori-infektion och duodenalsår bekräftades hos 148 patienter i studie 6 och 208 patienter i studie 7. Dessa studier jämförde kombinationsregimen med monoterapi med omeprazol. Resultaten för effektanalyserna för dessa studier beskrivs nedan. H. pylori-utrotning definierades som inget positivt test (odling eller histologi) vid 4 veckor efter avslutad behandling, och två negativa test krävdes för att anses vara utrotade av H. pylori. I analysen per protokoll exkluderades följande patienter: avhopp, patienter med saknade H. pylori-test efter behandlingen och patienter som inte bedömdes för utrotning av H. pylori eftersom de visade sig ha ett sår i slutet av behandlingen .
Kombinationen av omeprazol och klaritromycin var effektiv för att utrota H. pylori.
Sårläkning var inte signifikant annorlunda när klaritromycin lades till omeprazolbehandling jämfört med omeprazolbehandling enbart.
Kombinationen av omeprazol och klaritromycin var effektiv för att utrota H. pylori och minskade återfall av duodenalsår.
Aktivt benignt magsår
I en amerikansk multicenter, dubbelblind studie av omeprazol 40 mg en gång dagligen, 20 mg en gång dagligen och placebo på 520 patienter med endoskopiskt diagnostiserat magsår, erhölls följande resultat.
Behandling av magsår % av patienter läkta (alla behandlade patienter)
För de stratifierade grupperna av patienter med en sårstorlek mindre än eller lika med 1 cm, upptäcktes ingen skillnad i läkningshastigheter mellan 40 mg och 20 mg vare sig efter 4 eller 8 veckor. För patienter med sårstorlek större än 1 cm var 40 mg signifikant effektivare än 20 mg efter 8 veckor.
en utländsk, multinationell, dubbelblind studie av 602 patienter med endoskopiskt diagnostiserat magsår, utvärderades omeprazol 40 mg en gång dagligen, 20 mg en gång dagligen och ranitidin 150 mg två gånger om dagen.
Behandling av magsår % av patienter läkta (alla behandlade patienter)
Symtomatisk GERD
En placebokontrollerad studie genomfördes i Skandinavien för att jämföra effekten av omeprazol 20 mg eller 10 mg en gång dagligen i upp till 4 veckor vid behandling av halsbränna och andra symtom hos GERD-patienter utan EE. Resultaten visas nedan.
% framgångsrikt symtomatiskt resultat1
EE på grund av syramedierad GERD
I en amerikansk multicenter dubbelblind placebokontrollerad studie av 20 mg eller 40 mg omeprazolmagnesium kapslar med fördröjd frisättning hos patienter med symtom på GERD och endoskopiskt diagnostiserad EE av grad 2 eller högre, var den procentuella läkningshastigheten (enligt protokoll) som följer :
denna studie var 40 mg dosen inte överlägsen 20 mg dosen av omeprazolmagnesium kapslar med fördröjd frisättning i procentuell läkningshastighet. Andra kontrollerade kliniska prövningar har också visat att omeprazolmagnesium kapslar med fördröjd frisättning är effektiva vid svår GERD. I jämförelse med histamin H2-receptorantagonister hos patienter med EE, grad 2 eller högre, var omeprazolmagnesium kapslar med fördröjd frisättning i en dos på 20 mg signifikant effektivare än de aktiva kontrollerna. Fullständig lindring av halsbränna dag och natt inträffade signifikant snabbare (p
I denna och fem andra kontrollerade GERD-studier rapporterade signifikant fler patienter som tog 20 mg omeprazol (84 %) fullständig lindring av GERD-symtom än patienter som fick placebo (12 %).
Underhåll av läkning av EE på grund av syramedierad GERD
en amerikansk dubbelblind, randomiserad, multicenter, placebokontrollerad studie studerades två dosregimer av omeprazolmagnesium kapslar med fördröjd frisättning hos patienter med endoskopiskt bekräftad läkt esofagit. Resultat för att fastställa bibehållande av läkning av EE visas nedan.
Livstabellsanalys
I en internationell multicenter dubbelblind studie jämfördes omeprazolmagnesium kapslar med fördröjd frisättning 20 mg dagligen och 10 mg dagligen med ranitidin 150 mg två gånger dagligen hos patienter med endoskopiskt bekräftad läkt esofagit. Tabellen nedan visar resultaten av denna studie för upprätthållande av läkning av EE.
Livstabellsanalys
Hos patienter som initialt hade grad 3 eller 4 erosiv esofagit, för underhåll efter läkning var 20 mg omeprazolmagnesium kapslar med fördröjd frisättning effektiv, medan 10 mg inte visade effekt.
Patologiska hypersekretoriska tillstånd
öppna studier av 136 patienter med patologiska hypersekretoriska tillstånd, såsom Zollinger-Ellison (ZE) syndrom med eller utan multipla endokrina adenom, hämmade omeprazolmagnesium kapslar med fördröjd frisättning signifikant magsyrasekretionen och kontrollerade associerade symtom på diarré, anorexi och smärta. Doser som sträckte sig från 20 mg varannan dag till 360 mg per dag bibehöll basalsyrasekretionen under 10 mEq/timme hos patienter utan föregående gastrisk operation och under 5 mEq/timme hos patienter med tidigare gastrisk operation.
Initiala doser titrerades till individuella patientbehov och justeringar var nödvändiga med tiden hos vissa patienter [se DOSERING OCH ADMINISTRERING ]. Omeprazolmagnesium kapslar med fördröjd frisättning tolererades väl vid dessa höga dosnivåer under långa perioder (> 5 år hos vissa patienter). Hos de flesta ZE-patienter modifierades inte serumgastrinnivåerna av omeprazolmagnesiumkapslar med fördröjd frisättning. Hos vissa patienter ökade dock serumgastrin till nivåer som var högre än de som fanns innan behandling med omeprazol påbörjades. Minst 11 patienter med ZE-syndrom på långtidsbehandling med omeprazolmagnesium kapslar med fördröjd frisättning utvecklade magkarcinoider. Dessa fynd tros vara en manifestation av det underliggande tillståndet, som är känt för att vara associerat med sådana tumörer, snarare än resultatet av administrering av omeprazolmagnesium kapslar med fördröjd frisättning [se NEGATIVA REAKTIONER ].
Pediatriska studier för behandling av symtomatisk GERD, behandling av EE på grund av syramedierad GERD och underhåll av läkning av EE på grund av syramedierad GERD
Behandling av symtomatisk GERD
Effektiviteten av kapslar med fördröjd frisättning av omeprazolmagnesium för behandling av symtomatisk GERD hos pediatriska patienter i åldern 1 till 16 år baseras delvis på data från 125 pediatriska patienter i två okontrollerade kliniska studier.
Den första studien inkluderade 12 pediatriska patienter i åldern 1 till 2 år med en historia av kliniskt diagnostiserad GERD. Patienterna fick en engångsdos av omeprazol (0,5 mg/kg, 1 mg/kg eller 1,5 mg/kg) under 8 veckor som en öppen kapsel i 8,4 % natriumbikarbonatlösning. Sjuttiofem procent (9/12) av patienterna hade kräkningar/uppstötningar minskade från baslinjen med minst 50 %.
Den andra studien inkluderade 113 pediatriska patienter i åldern 2 till 16 år med en historia av symtom som tyder på symtomatisk GERD. Patienterna administrerades en engångsdos av omeprazol (10 mg eller 20 mg, baserat på kroppsvikt) under 4 veckor, antingen som en intakt kapsel eller som en öppen kapsel i äppelmos. Framgångsrik respons definierades som inga måttliga eller svåra episoder av vare sig smärtrelaterade symtom eller kräkningar/uppstötningar under de sista 4 dagarna av behandlingen. Resultaten visade framgångsfrekvenser på 60 % (9/15; 10 mg omeprazol) respektive 59 % (58/98; 20 mg omeprazol).
Behandling av EE på grund av syramedierad GERD
en okontrollerad, öppen dostitreringsstudie, för behandling av EE hos pediatriska patienter i åldern 1 till 16 år, krävdes doser som varierade från 0,7 till 3,5 mg/kg/dag (80 mg/dag). Doserna initierades med 0,7 mg/kg/dag. Doserna ökades i steg om 0,7 mg/kg/dag (om intraesofagealt pH visade ett pH på
Underhåll av läkning av EE på grund av syramedierad GERD
en okontrollerad, öppen studie av upprätthållande av läkning av EE hos 46 pediatriska patienter i åldern 1 till 16 år, krävde 54 % av patienterna halva läkningsdosen. De återstående patienterna ökade läkningsdosen (0,7 till maximalt 2,8 mg/kg/dag) antingen under hela underhållsperioden eller återgick till halva dosen innan den avslutades. Av de 46 patienter som gick in i underhållsfasen hade 19 (41%) inget återfall under uppföljningen (intervall 4 till 25 månader). Dessutom ledde underhållsbehandling till EE-patienter till att 63 % av patienterna inte hade några övergripande symtom.
REFERENSER
1. Clinical and Laboratory Standards Institute (CLSI). Metoder för utspädning Antimikrobiella känslighetstester för bakterier som växer aerobt; Godkänd standard - tionde upplagan. CLSI Document M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania, 19087, USA 2015.
PATIENTINFORMATION
PRILOSEC® (pry-lo-sec) (omeprazolmagnesium) för oral suspension med fördröjd frisättning
Vilken är den viktigaste informationen jag borde veta om PRILOSEC?
PRILOSEC 10 mg kan hjälpa dina syrarelaterade symtom, men du kan fortfarande ha allvarliga magproblem. Prata med din läkare.
PRILOSEC kan orsaka allvarliga biverkningar, inklusive:
- En typ av njurproblem (akut tubulointerstitiell nefrit). Vissa personer som tar protonpumpshämmare (PPI), inklusive PRILOSEC, kan utveckla ett njurproblem som kallas akut tubulointerstitiell nefrit som kan inträffa när som helst under behandlingen med PRILOSEC. Ring din läkare omedelbart om du har en minskning av mängden du kissar eller om du har blod i urinen.
- Diarré orsakad av en infektion (Clostridium difficile) i dina tarmar. Ring din läkare omedelbart om du har vattnig avföring eller magsmärtor som inte försvinner. Du kanske har feber eller inte.
- Benfrakturer (höft, handled eller ryggrad). Benfrakturer i höften, handleden eller ryggraden kan inträffa hos personer som tar flera dagliga doser av PPI-läkemedel och under en lång tidsperiod (ett år eller längre). Tala om för din läkare om du har benfraktur, särskilt i höften, handleden eller ryggraden.
- Vissa typer av lupus erythematosus. Lupus erythematosus är en autoimmun sjukdom (kroppens immunceller attackerar andra celler eller organ i kroppen). Vissa personer som tar PPI-läkemedel, inklusive PRILOSEC 10mg, kan utveckla vissa typer av lupus erythematosus eller få försämring av den lupus de redan har. Ring din läkare omedelbart om du har ny eller förvärrad ledvärk eller utslag på kinderna eller armarna som blir värre i solen.
Tala med din läkare om din risk för dessa allvarliga biverkningar. PRILOSEC 10mg kan ha andra allvarliga biverkningar. Se "Vilka är de möjliga biverkningarna av PRILOSEC 20mg?"
Vad är PRILOSEC 20mg?
Ett receptbelagt läkemedel som kallas protonpumpshämmare (PPI) som används för att minska mängden syra i magen.
Hos vuxna, PRILOSEC 20mg används för:
- upp till 8 veckor för läkning av duodenalsår.
- 10 till 14 dagar med vissa antibiotika för att behandla en infektion orsakad av bakterier som kallas H. pylori. Om det behövs kan din läkare ordinera ytterligare 14 till 18 dagar med PRILOSEC efter behandling med antibiotika.
- upp till 8 veckor för att läka magsår.
- upp till 4 veckor för att behandla halsbränna och andra symtom som uppstår vid gastroesofageal refluxsjukdom (GERD).
- upp till 8 veckor för läkning och symtomlindring av syrarelaterade skador på slemhinnan i matstrupen (kallad erosiv esofagit eller EE). Din läkare kan ordinera ytterligare 4 veckor med PRILOSEC 20 mg till patienter vars EE inte läker.
- bibehålla läkning av EE och för att förhindra återkomst av halsbränna symtom orsakade av GERD. Det är inte känt om PRILOSEC är säkert och effektivt när det används i mer än 12 månader för detta ändamål.
- långtidsbehandling av tillstånd där din mage gör för mycket syra. Detta inkluderar ett sällsynt tillstånd som kallas Zollinger-Ellisons syndrom.
Hos barn 1 till 16 år, PRILOSEC 20mg används för:
- upp till 4 veckor för att behandla halsbränna och andra symtom som händer med GERD.
- upp till 8 veckor för att behandla GERD med EE.
- bibehålla läkning av EE och för att förhindra återkomst av halsbränna symtom orsakade av GERD. Det är inte känt om PRILOSEC är säkert och effektivt när det används längre än 12 månader för detta ändamål.
Hos barn från 1 månad till yngre än 12 månader, PRILOSEC 10mg används för:
- upp till 6 veckor för att behandla GERD med EE. Det är inte känt om PRILOSEC är säkert och effektivt för andra användningar hos barn som är 1 månad till under 12 månader eller till barn under 1 månads ålder.
Ta inte PRILOSEC om du är:
- allergisk mot omeprazol, något annat PPI-läkemedel eller något av innehållsämnena i PRILOSEC. Se slutet av denna medicinguide för en komplett lista över ingredienser.
- tar ett läkemedel som innehåller rilpivirin (EDURANT, COMPLERA, ODEFSEY) som används för att behandla HIV-1 (humant immunbristvirus).
Innan du tar PRILOSEC 20 mg, berätta för din läkare om alla dina medicinska tillstånd, inklusive om du:
- har låga magnesiumnivåer, låga kalciumnivåer och låga kaliumnivåer i ditt blod.
- är gravid eller planerar att bli gravid. Det är inte känt om PRILOSEC 10 mg kommer att skada ditt ofödda barn.
- ammar eller planerar att amma. PRILOSEC 40 mg kan passera över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar PRILOSEC.
- Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Tala särskilt om för din läkare om du tar ett läkemedel som innehåller klaritromycin eller amoxicillin, klopidogrel (Plavix), metotrexat (Otrxup, Rasuvo, Trexall, XATMEP), digoxin (LANOXIN), ett vattenpiller (diuretikum), johannesört (Hypericum perforatum) eller rifampin (Rimactane, Rifater, Rifamate).
Hur ska jag ta PRILOSEC 20mg?
- Ta PRILOSEC 20 mg precis som din läkare har ordinerat.
- Ändra inte din dos eller sluta inte med PRILOSEC 40 mg utan att tala med din läkare.
- PRILOSEC tas vanligtvis 1 gång varje dag.
- Ta PRILOSEC 20 mg före måltid.
- Antacida kan tas tillsammans med PRILOSEC.
- PRILOSEC blandas med vatten och kan tas genom munnen eller ges genom en nasogastrisk sond (NG) eller magsond.
- Se den "Användningsinstruktioner" i slutet av denna medicineringsguide för instruktioner om hur man blandar och tar PRILOSEC 10 mg genom munnen i vatten eller hur man blandar och ger PRILOSEC genom ett NG-rör eller magsond blandat i vatten.
- Om du missar en dos av PRILOSEC, ta den så snart du kommer ihåg det. Om det nästan är dags för din nästa dos, ta inte den missade dosen. Ta nästa dos vid din ordinarie tid. Ta inte 2 doser samtidigt.
- Om du tar för mycket PRILOSEC, ring din läkare eller din giftkontrollcentral på 1-800-222-1222 omedelbart eller gå till närmaste akutmottagning.
Vilka är de möjliga biverkningarna av PRILOSEC 40mg?
PRILOSEC kan orsaka allvarliga biverkningar, inklusive:
- Ser "Vilken är den viktigaste informationen jag borde veta om PRILOSEC 40mg?"
- Låga vitamin B-12 nivåer din kropp kan inträffa hos personer som har tagit PRILOSEC 40 mg under en längre tid (mer än 3 år). Tala om för din läkare om du har symtom på låga vitamin B-12-nivåer, inklusive andnöd, yrsel, oregelbunden hjärtrytm, muskelsvaghet, blek hud, trötthetskänsla, humörförändringar och stickningar eller domningar i armar och ben.
- Låga magnesiumnivåer och mineralmetabolism i din kropp kan inträffa hos personer som har tagit PRILOSEC i minst 3 månader. Tala om för din läkare om du har symtom på låga magnesiumnivåer, inklusive kramper, yrsel, oregelbunden hjärtrytm, darrning, muskelvärk eller svaghet och spasmer i händer, fötter eller röst.
- Magutväxter (fundiska körtelpolyper). Personer som tar PPI-läkemedel under lång tid har en ökad risk att utveckla en viss typ av magtillväxt som kallas fundic gland polyper, särskilt efter att ha tagit PPI-läkemedel i mer än 1 år.
- Allvarliga hudreaktioner. PRILOSEC kan orsaka sällsynta men allvarliga hudreaktioner som kan påverka vilken del av din kropp som helst. Dessa allvarliga hudreaktioner kan behöva behandlas på sjukhus och kan vara livshotande:
- Hudutslag som kan ha blåsor, fjällning eller blödning på någon del av huden (inklusive dina läppar, ögon, mun, näsa, könsorgan, händer eller fötter).
- Du kan också ha feber, frossa, värk i kroppen, andnöd eller förstorade lymfkörtlar.
Sluta ta PRILOSEC 20 mg och kontakta din läkare omedelbart. Dessa symtom kan vara det första tecknet på en allvarlig hudreaktion.
De vanligaste biverkningarna av PRILOSEC 40 mg hos vuxna inkluderar: huvudvärk, smärta i magområdet (buk), illamående, diarré, kräkningar och gaser.
De vanligaste biverkningarna av PRILOSEC hos barn 1 till 16 år inkluderar: övre luftvägsinfektion, feber, huvudvärk, magsmärtor (buksmärtor), illamående, diarré, kräkningar och gaser. Dessa är inte alla möjliga biverkningar av PRILOSEC. Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara PRILOSEC 40mg?
Förvara PRILOSEC i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
Förvara PRILOSEC 20mg och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av PRILOSEC.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte PRILOSEC för ett tillstånd som det inte ordinerats för. Ge inte PRILOSEC 40 mg till andra personer, även om de har samma symtom som du har. Det kan skada dem. Du kan fråga din läkare eller apotekspersonal om information om PRILOSEC 20mg som är skriven för vårdpersonal.
Vilka är ingredienserna i PRILOSEC?
Aktiv beståndsdel: omeprazol magnesium
Inaktiva Ingredienser: glycerylmonostearat, hydroxipropylcellulosa, hypromellos, magnesiumstearat, metakrylsyrasampolymer C, polysorbat, sockersfärer, talk och trietylcitrat, och även inaktiva granuler. De inaktiva granulerna är sammansatta av citronsyra, krospovidon, dextros, hydroxipropylcellulosa, järnoxid och xantangummi.
ANVÄNDNINGSINSTRUKTIONER
PRILOSEC® (pry-lo-sec) (omeprazolmagnesium) för oral suspension med fördröjd frisättning
Att ta PRILOSEC 40 mg i vatten:
Att ge PRILOSEC med vatten genom en nasogastrisk sond (NG) eller magsond:
För personer som har en NG-sond eller magsond som är storlek 6 eller större, kan PRILOSEC ges enligt följande:
Denna medicineringsguide har godkänts av US Food and Drug Administration
