Pentasa 400mg Mesalamine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Pentasa och hur används det?
Pentasa är ett receptbelagt läkemedel som används för att behandla symtom på ulcerös kolit. Pentasa 400mg kan användas ensamt eller tillsammans med andra läkemedel.
Pentasa tillhör en klass av läkemedel som kallas 5-aminosalicylsyraderivat.
Det är inte känt om Pentasa är säkert och effektivt för barn äldre än 5 år.
Vilka är de möjliga biverkningarna av Pentasa?
Pentasa kan orsaka allvarliga biverkningar inklusive:
- svåra magsmärtor,
- kramp i magen,
- blodig diarré,
- feber,
- huvudvärk,
- hudutslag,
- blodig eller tjäraktig avföring,
- hosta blod,
- kräks som ser ut som kaffesump,
- lite eller ingen urinering,
- smärtsam eller svår urinering,
- svullnad i dina fötter eller vrister,
- känner sig trött eller andfådd,
- aptitlöshet,
- ont i övre magen,
- trötthet,
- lätta blåmärken eller blödningar,
- mörk urin,
- lerfärgade pallar, och
- gulfärgning av huden eller ögonen
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Pentasa 400mg inkluderar:
- illamående,
- kräkningar,
- magont,
- diarre,
- dålig matsmältning,
- gas,
- huvudvärk,
- utslag, och
- onormala leverfunktionstester
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Pentasa. För mer information, fråga din läkare eller apotekspersonal.
BESKRIVNING
PENTASA (mesalamin) för oral administrering är en formulering med kontrollerad frisättning av mesalamin, ett aminosalicylat antiinflammatoriskt medel för gastrointestinal användning.
Kemiskt är mesalamin 5-amino-2-hydroxibensoesyra. Den har en molekylvikt på 153,14.
Strukturformeln är:
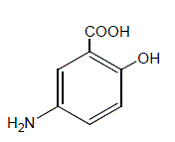
Varje 250 mg kapsel innehåller 250 mg mesalamin. Den innehåller också följande inaktiva ingredienser: acetylerad monoglycerid, ricinolja, kolloidal kiseldioxid, etylcellulosa, hydroxipropylmetylcellulosa, stärkelse, stearinsyra, socker, talk och vitt vax. Kapselskalet innehåller D&C Yellow #10, FD&C Blue #1, FD&C Green #3, gelatin, titandioxid och andra ingredienser.
Varje 500 mg kapsel innehåller 500 mg mesalamin. Den innehåller också följande inaktiva ingredienser: acetylerad monoglycerid, ricinolja, kolloidal kiseldioxid, etylcellulosa, hydroxipropylmetylcellulosa, stärkelse, stearinsyra, socker, talk och vitt vax. Kapselskalet innehåller FD&C Blue #1, gelatin, titandioxid och andra ingredienser.
INDIKATIONER
PENTASA 400 mg är indicerat för induktion av remission och för behandling av vuxna patienter med lätt till måttligt aktiv ulcerös kolit.
DOSERING OCH ADMINISTRERING
Den rekommenderade dosen för induktion av remission och symtomatisk behandling av mild till måttligt aktiv ulcerös kolit hos vuxna är 1 g (4 PENTASA 250 mg kapslar eller 2 PENTASA 500 mg kapslar) 4 gånger dagligen för en total daglig dos på 4 g. Behandlingslängden i kontrollerade studier var upp till 8 veckor.
PENTASA-kapslar kan sväljas hela, eller alternativt kan kapseln öppnas och hela innehållet strö på äppelmos eller yoghurt. Hela innehållet bör konsumeras omedelbart. Kapslarna och kapselinnehållet får inte krossas eller tuggas.
Drick en tillräcklig mängd vätska.
Säkerhet och effekt av PENTASA 400 mg hos pediatriska patienter har inte fastställts.
HUR LEVERERAS
PENTASA förlängd 250 mg kapslar levereras i flaskor med 240 kapslar ( NDC 54092-189-81). Varje grön och blå kapsel innehåller 250 mg mesalamin i pärlor med förlängd frisättning. PENTASA kapslar med förlängd frisättning identifieras med en femkantig starburst-logotyp och numret 2010 på den gröna delen och S429 250 mg på den blå delen av kapslarna.
PENTASA förlängd frisättning 500 mg kapslar levereras i flaskor med 120 kapslar ( NDC 54092-191-12). Varje blå kapsel innehåller 500 mg mesalamin i pärlor med förlängd frisättning. PENTASA 400 mg kapslar med förlängd frisättning identifieras med en femkantig starburst-logotyp och S429 500 mg på kapslarna.
Förvara vid 25°C (77°F); utflykter tillåtna till 15°C till 30°C (59°F till 86°F) [se USP Controlled Room Temperature].
För att rapportera MISSTÄNKTA BIVERKNINGAR, kontakta Takeda Pharmaceuticals på 1800-828-2088 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
Distribueras av: Takeda Pharmaceuticals America, Inc. Lexington, MA 02421, USA. Reviderad: nov 2021
BIEFFEKTER
I kombinerade inhemska och utländska kliniska prövningar fick mer än 2100 patienter med ulcerös kolit eller Crohns sjukdom PENTASA-behandling. I allmänhet tolererades PENTASA-terapi väl. De vanligaste händelserna (dvs större än eller lika med 1 %) var diarré (3,4 %), huvudvärk (2,0 %), illamående (1,8 %), buksmärtor (1,7 %), dyspepsi (1,6 %), kräkningar (1,5 %). %) och utslag (1,0 %).
två inhemska placebokontrollerade studier som involverade över 600 patienter med ulcerös kolit, var biverkningarna färre hos PENTASA (mesalamin)-behandlade patienter än i placebogruppen (PENTASA 14 % jämfört med placebo 18 %) och var inte dosrelaterade. Händelser som inträffar hos mer än 1 % visas i tabellen nedan. Av dessa var endast illamående och kräkningar vanligare i PENTASA-gruppen. Avbrytande från behandling på grund av biverkningar var vanligare med placebo än PENTASA (7 % mot 4 %).
Kliniska laboratoriemätningar visade inga signifikanta onormala trender för något test, inklusive mätning av hematologisk funktion, lever- och njurfunktion.
Följande biverkningar, presenterade av kroppens system, rapporterades sällan (dvs mindre än 1%) under inhemsk ulcerös kolit och prövningar av Crohns sjukdom. I många fall har förhållandet till PENTASA inte fastställts.
Gastrointestinala: abdominal distention, anorexi, förstoppning, duodenalsår, dysfagi, eruktion, matstrupesår, fekal inkontinens, GGTP-ökning, GI-blödning, ökat alkaliskt fosfatas, LDH-ökning, munsår, oral moniliasis, pankreatit, PTSG-ökning, PTSGOT-ökning, avföringsavvikelser (färg- eller strukturförändring), törst
Dermatologiska: akne, alopeci, torr hud, eksem, erythema nodosum, nagelstörning, ljuskänslighet, klåda, svettning, urtikaria
Nervsystem: depression, yrsel, sömnlöshet, somnolens, parestesi
Kardiovaskulär: hjärtklappning, perikardit, vasodilatation
Övrig: albuminuri, amenorré, amylasökning, artralgi, asteni, bröstsmärtor, konjunktivit, ekkymos, ödem, feber, hematuri, hypomenorré, Kawasaki-liknande syndrom, benkramper, lichen planus, lipasökning, sjukdomskänsla, menorgiragi, mymonorragi, , trombocytemi, trombocytopeni, urinfrekvens
En vecka efter slutförandet av en 8-veckors ulcerös kolitstudie utvecklade en 72-årig man, utan tidigare lungproblem, dyspné. Patienten diagnostiserades därefter med interstitiell lungfibros utan eosinofili av en läkare och bronkiolit obliterans med organiserande pneumonit av en andra läkare. Ett orsakssamband mellan denna händelse och mesalaminbehandling har inte fastställts.
Publicerade fallrapporter och/eller spontan övervakning efter marknadsföring har beskrivit sällsynta fall av perikardit, dödlig myokardit, bröstsmärtor och T-vågsavvikelser, överkänslighetspneumonit, pankreatit, nefrotiskt syndrom, interstitiell nefrit, hepatit, aplastisk anemi, leukocytisk anemi, pneumonit, pneumoni, pneumoni, anemi medan du får mesalaminbehandling. Anemi kan vara en del av den kliniska presentationen av inflammatorisk tarmsjukdom. Allergiska reaktioner, som kan involvera eosinofili, kan ses i samband med behandling med PENTASA 400 mg.
Rapporter efter marknadsföring
Följande händelser har identifierats vid användning av mesalamin av märket PENTASA efter godkännande i klinisk praxis. Eftersom de rapporteras frivilligt från en population av okänd storlek, kan uppskattningar av frekvensen inte göras. Dessa händelser har valts för inkludering på grund av en kombination av allvarlighetsgrad, frekvens av rapportering eller potentiellt orsakssamband till mesalamin:
Gastrointestinala: Rapporter om hepatotoxicitet, inklusive förhöjda leverenzymer (SGOT/AST, SGPT/ALT, GGT, LDH, alkaliskt fosfatas, bilirubin), hepatit, gulsot, kolestatisk gulsot, skrumplever och möjliga levercellsskador inklusive levernekros och leversvikt. Några av dessa fall var dödliga. Ett fall av Kawasaki-liknande syndrom som inkluderade leverfunktionsförändringar rapporterades också.
Övrig: anafylaktisk reaktion, SJS/TEN, DRESS, AGEP, pleurit/pleurit, pneumonit, granulocytopeni, systemisk lupus erythematosus, lupusliknande syndrom, akut njursvikt, interstitiell lungsjukdom, överkänslighetspneumonit (inklusive interstitiell lunginflammation, pneuminofilneit), pneumonitiell allergisk inflammation. kronisk njursvikt, nefrogen diabetes insipidus, nefrolitiasis, intrakraniell hypertoni, angioödem och oligospermi (reversibel).
LÄKEMEDELSINTERAKTIONER
Inga undersökningar av interaktioner mellan PENTASA 400mg och andra läkemedel har utförts; dock har följande läkemedelsinteraktioner rapporterats för produkter som innehåller mesalamin:
Nefrotoxiska medel, inklusive icke-steroida antiinflammatoriska läkemedel
Samtidig användning av mesalamin och kända nefrotoxiska medel, inklusive icke-steroida antiinflammatoriska läkemedel (NSAID), kan öka risken för nefrotoxicitet. Övervaka patienter som tar nefrotoxiska läkemedel för förändringar i njurfunktionen och mesalaminrelaterade biverkningar.

Azatioprin eller 6-merkaptopurin
Samtidig användning av mesalamin med azatioprin eller 6-merkaptopurin och/eller andra läkemedel som är kända för att orsaka myelotoxicitet kan öka risken för blodsjukdomar, benmärgssvikt och associerade komplikationer. Om samtidig användning av PENTASA och azatioprin eller 6-merkaptopurin inte kan undvikas, övervaka blodprov, inklusive fullständigt antal blodkroppar och trombocytantal.
VARNINGAR
Ingen information tillhandahålls
FÖRSIKTIGHETSÅTGÄRDER
Nedsatt njurfunktion
Nedsatt njurfunktion, inklusive minimal förändringssjukdom, akut och kronisk interstitiell nefrit och njursvikt har rapporterats hos patienter som fått PENTASA eller andra produkter som innehåller mesalamin eller omvandlas till mesalamin.
Mesalamin är känt för att utsöndras till stor del via njurarna, och risken för biverkningar kan vara större hos patienter med nedsatt njurfunktion. Utvärdera njurfunktionen hos alla patienter före start och regelbundet under behandling med PENTASA. Utvärdera riskerna och fördelarna med att använda PENTASA till patienter med känd njurfunktionsnedsättning eller tidigare njursjukdom eller som samtidigt tar nefrotoxiska läkemedel.
Mesalamin-inducerat akut intoleranssyndrom
Mesalamin har associerats med ett akut intoleranssyndrom som kan vara svårt att skilja från en uppblossning av inflammatorisk tarmsjukdom. Symtomen inkluderar kramper, akut buksmärta, blodig diarré och ibland feber, huvudvärk och utslag. Övervaka patienter för försämring av dessa symtom under behandling. Om akut intoleranssyndrom misstänks, avbryt omedelbart behandlingen med PENTASA.
Överkänslighetsreaktioner
Överkänslighetsreaktioner har rapporterats hos patienter som tar sulfasalazin. Vissa patienter kan ha en liknande reaktion som PENTASA eller andra föreningar som innehåller eller omvandlas till mesalamin.
Liksom med sulfasalazin kan mesalamininducerade överkänslighetsreaktioner uppträda som inre organpåverkan, inklusive myokardit, perikardit, nefrit, hepatit, pneumonit och hematologiska abnormiteter. Utvärdera patienter omedelbart om tecken eller symtom på en överkänslighetsreaktion förekommer. Avbryt PENTASA om en alternativ etiologi för tecknen och symtomen inte kan fastställas.
Leversvikt
Det har förekommit rapporter om leversvikt hos patienter med redan existerande leversjukdom som har fått andra produkter som innehåller mesalamin. Utvärdera riskerna och fördelarna med att använda PENTASA 400mg hos patienter med känd leverinsufficiens.
Allvarliga kutana biverkningar
Allvarliga kutana biverkningar, såsom Stevens-Johnsons syndrom (SJS) och toxisk epidermal nekrolys (TEN), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) och akut generaliserad exantematös pustulos (AGEP) har rapporterats vid användning av mesalamin (ser NEGATIVA REAKTIONER ). Avbryt PENTASA vid de första tecknen eller symtomen på allvarliga kutana biverkningar eller andra tecken på överkänslighet och överväg ytterligare utvärdering.
Ljuskänslighet
Patienter med redan existerande hudåkommor såsom atopisk dermatit och atopiskt eksem har rapporterat allvarligare ljuskänslighetsreaktioner. Rekommendera patienter att undvika solexponering, bära skyddskläder och använda ett brett spektrum solskyddsmedel när de är utomhus.
Nefrolitiasis
Fall av nefrolitiasis har rapporterats vid användning av mesalamin, inklusive stenar med 100 % mesalamininnehåll. Mesalamininnehållande stenar är radiotransparenta och omöjliga att upptäcka med standardröntgen eller datortomografi (CT). Säkerställ tillräcklig hydrering under behandlingen.
Interferens med laboratorietester
Användning av mesalamin kan leda till falskt förhöjda testresultat vid mätning av urinnormetanefrin genom vätskekromatografi med elektrokemisk detektion på grund av likheten i kromatogrammen för normetanefrin och mesalamins huvudmetabolit, N-acetyl-5-aminosalicylsyra (N-Ac-5-ASA) ). Överväg en alternativ, selektiv analys för normetanefrin.
Karcinogenes, Mutagenes, Nedsatt fertilitet
I en 104-veckors dietary carcinogenicitetsstudie av mesalamin behandlades CD-1-möss med doser upp till 2500 mg/kg/dag och de var inte tumörframkallande. För en person på 50 kg med medellängd (1,46 m2 kroppsyta) motsvarar detta 2,5 gånger den rekommenderade dosen för människa på basis av kroppsyta (2960 mg/m2/dag). I en 104-veckors kostkarcinogenicitetsstudie på Wistar-råttor var mesalamin upp till en dos på 800 mg/kg/dag inte tumörframkallande. Denna dos representerar 1,5 gånger den rekommenderade humandosen på basis av kroppsyta.
Inga tecken på mutagenicitet observerades i ett in vitro Ames-test och i ett in vivo mus-mikronkärntest.
Inga effekter på fertilitet eller reproduktionsförmåga observerades hos han- eller honråttor vid orala doser av mesalamin upp till 400 mg/kg/dag (0,8 gånger den rekommenderade dosen för människa baserat på kroppsyta).
Spermaavvikelser och infertilitet hos män, som har rapporterats i samband med sulfasalazin, har inte setts med PENTASA 400 mg kapslar under kontrollerade kliniska prövningar.
Graviditet
Teratogena effekter
Publicerade data från metaanalyser, kohortstudier och fallserier om användning av mesalamin under graviditet har inte på ett tillförlitligt sätt informerat om ett samband med mesalamin och större fosterskador, missfall eller ogynnsamma resultat hos modern eller foster. Det finns inga tydliga bevis för att exponering för mesalamin i tidig graviditet är associerad med en ökad risk för allvarliga medfödda missbildningar, inklusive hjärtmissbildningar. Publicerade epidemiologiska studier har viktiga metodologiska begränsningar som hindrar tolkningen av data, inklusive oförmåga att kontrollera för konfounders, såsom underliggande modern sjukdom, modern användning av samtidig medicinering och saknad information om dos och varaktighet för användning av mesalaminprodukter. PENTASA ska endast användas under graviditet om fördelarna överväger riskerna.
reproduktionsstudier på djur visade oral administrering av mesalamin under organogenesen till dräktiga råttor i doser upp till 1000 mg/kg/dag (5900 mg/m²) och kaniner i doser på 800 mg/kg/dag (6856 mg/m²) inga bevis. av teratogena effekter eller skador på fostret på grund av mesalamin.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för de angivna populationerna är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Icke-ratogena effekter
Publicerade data tyder på att ökad sjukdomsaktivitet är associerad med risken för att utveckla negativa graviditetsresultat hos kvinnor med ulcerös kolit. Negativa graviditetsresultat inkluderar för tidig förlossning (före 37 veckors graviditet), spädbarn med låg födelsevikt (mindre än 2500 g) och små för graviditetsåldern vid födseln.
Ammande mödrar
Data från publicerad litteratur rapporterar förekomsten av mesalamin och dess metabolit, N-acetyl-5-aminosalicylsyra, i bröstmjölk i små mängder med relativa spädbarnsdoser (RID) på 0,1 % eller mindre för mesalamin. Den kliniska betydelsen av detta har inte fastställts och det finns begränsad erfarenhet av att ammande kvinnor använder mesalamin.
Det finns rapporter om diarré hos ammade spädbarn som exponerats för mesalamin. Effekten av PENTASA 400 mg på mjölkproduktionen är okänd. Iaktta försiktighet om PENTASA 400mg administreras till en ammande kvinna och övervaka ammade spädbarn för diarré.
publicerade amningsstudier varierade moderns mesalamindoser från olika orala och rektala formuleringar och produkter från 500 mg till 4,8 g dagligen. Den genomsnittliga koncentrationen av mesalamin i mjölk varierade från icke-detekterbar till 0,5 mg/L. Medelkoncentrationen av N-acetyl-5-aminosalicylsyra i mjölk varierade från 0,2 till 9,3 mg/L. Baserat på dessa koncentrationer är uppskattade dagliga doser för ett spädbarn som endast ammas 0 till 0,075 mg/kg/dag av mesalamin (RID 0% till 0,1%) och 0,03 till 1,4 mg/kg/dag av N-acetyl-5-aminosalicylsyra. syra.
Pediatrisk användning
Säkerhet och effekt av PENTASA hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Kliniska prövningar av PENTASA 400 mg inkluderade inte tillräckligt många patienter i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre patienter. Rapporter från okontrollerade kliniska studier och rapporteringssystem efter marknadsföring antydde en högre förekomst av bloddyskrasier (dvs agranulocytos, neutropeni och pancytopeni) hos patienter som fick mesalamininnehållande produkter såsom PENTASA 400 mg som var 65 år eller äldre jämfört med yngre patienter. Övervaka fullständigt antal blodkroppar och trombocytantal hos äldre patienter under behandling med PENTASA.
Överväg generellt den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion och samtidig sjukdom eller annan läkemedelsbehandling hos äldre patienter när PENTASA förskrivs.
ÖVERDOS
PENTASA 400mg är ett aminosalicylat, och symtom på salicylattoxicitet kan vara möjliga, såsom: illamående, kräkningar, buksmärtor, takypné, hyperpné, tinnitus och neurologiska symtom (huvudvärk, yrsel, förvirring, kramper). Allvarlig förgiftning med salicylater kan leda till elektrolyt- och pH-obalans i blodet och potentiellt till andra organskador (t.ex. njur- och lever).
Behandling av överdosering
Det finns ingen specifik motgift mot överdosering av mesalamin; Konventionell terapi för salicylattoxicitet kan dock vara fördelaktig vid akut överdosering och kan innefatta dekontaminering av mag-tarmkanalen för att förhindra ytterligare absorption. Korrigera vätske- och elektrolytobalans genom administrering av lämplig intravenös terapi och bibehåll adekvat njurfunktion.
KONTRAINDIKATIONER
PENTASA är kontraindicerat hos patienter med känd eller misstänkt överkänslighet mot salicylater, aminosalicylater eller någon del av detta läkemedel.
KLINISK FARMAKOLOGI
Sulfasalazin delas genom bakteriell verkan i tjocktarmen till sulfapyridin (SP) och mesalamin (5-ASA). Den vanliga orala dosen av sulfasalazin för aktiv ulcerös kolit hos vuxna är 2 till 4 g per dag i uppdelade doser. Fyra gram sulfasalazin ger 1,6 g fri mesalamin till tjocktarmen.
Verkningsmekanismen för mesalamin (och sulfasalazin) är inte helt klarlagd, men det verkar vara en lokal antiinflammatorisk effekt på epitelceller i tjocktarmen. Slemhinneproduktion av arakidonsyra (AA) metaboliter, både genom cyklooxygenasvägarna (dvs prostanoider) och genom lipoxygenasvägarna (dvs leukotriener (LTs) och hydroxyeicosatetraenoic syror (HETEs), ökar hos patienter med ulcerös kolit, och det är möjligt att mesalamin minskar inflammation genom att blockera cyklooxygenas och hämma produktionen av prostaglandin (PG) i tjocktarmen.
Människans farmakokinetik och metabolism
Absorption
PENTASA är en etylcellulosabelagd formulering av mesalamin med förlängd frisättning utformad för att frigöra terapeutiska mängder mesalamin i hela mag-tarmkanalen. Baserat på data om urinutsöndring, absorberas 20 % till 30 % av mesalaminet i PENTASA. Däremot, när mesalamin administreras oralt som en oformulerad 1-g vattensuspension, absorberas mesalamin till cirka 80 %.
Plasmamesalaminkoncentrationen nådde en topp på cirka 1 mcg/ml 3 timmar efter en 1-g PENTASA-dos och minskade på ett bifasiskt sätt. Litteraturen beskriver en genomsnittlig terminal halveringstid på 42 minuter för mesalamin efter intravenös administrering. På grund av den kontinuerliga frisättningen och absorptionen av mesalamin från PENTASA i hela mag-tarmkanalen, kan den verkliga eliminationshalveringstiden inte fastställas efter oral administrering. N-acetyl-5-aminosalicylsyra, huvudmetaboliten av mesalamin (5-aminosalicylsyra), nådde sin topp efter cirka 3 timmar vid 1,8 mcg/ml, och dess koncentration följde en bifasisk minskning. Farmakologiska aktiviteter av N-acetyl-5-aminosalicylsyra är okända och andra metaboliter har inte identifierats.
Oral mesalamins farmakokinetik var olinjär när PENTASA-kapslar doserades från 250 mg till 1 g fyra gånger dagligen, med steady-state mesalaminplasmakoncentrationer som ökade cirka nio gånger, från 0,14 mcg/ml till 1,21 mcg/ml, vilket tyder på mättbar förstapassagemetabolism. Farmakokinetiken för N-acetyl-5-aminosalicylsyra var linjär.
Eliminering
Cirka 130 mg fri mesalamin återvanns i avföringen efter en engångsdos på 1 g PENTASA 400 mg, vilket var jämförbart med de 140 mg mesalamin som utvanns från den molära ekvivalenta sulfasalazintablettdosen på 2,5 g. Eliminationen av fritt mesalamin och salicylater i feces ökade proportionellt med PENTASA-dosen. N-acetyl-5-aminosalicylsyra var den primära föreningen som utsöndrades i urinen (19 % till 30 %) efter PENTASA 400 mg dosering.
Kliniska tester
två randomiserade, dubbelblinda, placebokontrollerade, dos-respons-studier (UC-1 och UC-2) på 625 patienter med aktiv mild till måttlig ulcerös kolit, PENTASA 400 mg, vid en oral dos på 4 g/dag givet 1 g fyra gånger dagligen, gav konsekvent förbättring av prospektivt identifierade primära effektparametrar, PGA, Tx F och SI som visas i tabellen nedan.
4-g-dosen av PENTASA gav också konsekvent förbättring av sekundära effektparametrar, nämligen frekvensen av toalettbesök, avföringskonsistens, rektal blödning, buk/rektal smärta och brådska. 4-g-dosen av PENTASA inducerade remission enligt endoskopiska och symtomatiska effektmått.
Hos vissa patienter observerades 2-g-dosen av PENTASA 400 mg för att förbättra de uppmätta effektparametrarna. Dosen på 2 g gav dock inkonsekventa resultat i primära effektparametrar i de två adekvata och välkontrollerade studierna.
PATIENTINFORMATION
Ingen information tillhandahålls. Vänligen se FÖRSIKTIGHETSÅTGÄRDER sektion.
