Prevacid 15mg, 30mg Lansoprazole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Prevacid och hur används det?
Prevacid 15mg är ett receptbelagt läkemedel som används för att behandla symtom på magsår och tarmsår och för att minska mängden syra som produceras i magen. Prevacid 15mg kan användas ensamt eller tillsammans med andra läkemedel.
- Prevacid 15mg är en protonpumpshämmare.
Vilka är de möjliga biverkningarna av Prevacid 30mg?
Prevacid 30mg kan orsaka allvarliga biverkningar inklusive:
- svåra magsmärtor,
- diarré som innehåller blod,
- anfall (kramper,
- svårt att urinera,
- blod i urinen,
- svullnad,
- snabb viktökning,
- yrsel,
- snabb eller oregelbunden hjärtfrekvens,
- skakning,
- ryckiga muskelrörelser,
- känner sig orolig,
- muskelkramper eller spasmer i händer eller fötter,
- hosta,
- känner att du kvävs,
- ledvärk och
- hudutslag på kinderna eller armarna som förvärras i solljus
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Prevacid 15mg inkluderar:
- illamående,
- magont,
- diarre,
- förstoppning och
- huvudvärk
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Prevacid. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
FÖREGÅENDE (lansoprazol) oralt sönderfallande tabletter med fördröjd frisättning
BESKRIVNING
Den aktiva ingrediensen i PREVACID 30mg kapslar med fördröjd frisättning och PREVACID 15mg SoluTab oralt sönderfallande tabletter med fördröjd frisättning är lansoprazol, en substituerad bensimidazol, 2-[[[3-metyl-4-(2,2,2trifluoretoxi]-2-pyridyl]-2- metyl] sulfinyl] bensimidazol, en förening som hämmar magsyrasekretion. Dess empiriska formel är C16H14F3N3O2S med en molekylvikt på 369,37. Lansoprazol har följande struktur:
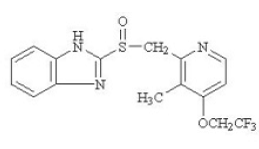
Lansoprazol är ett vitt till brunvitt luktfritt kristallint pulver som smälter under sönderdelning vid cirka 166°C. Lansoprazol är fritt lösligt i dimetylformamid; löslig i metanol; svårlöslig i etanol; lätt löslig i etylacetat, diklormetan och acetonitril; mycket svagt löslig i eter och praktiskt taget olöslig i hexan och vatten.
Lansoprazol är stabilt när det utsätts för ljus i upp till två månader. Nedbrytningshastigheten av föreningen i en vattenlösning ökar med sjunkande pH. Nedbrytningshalveringstiden för läkemedelssubstansen i en vattenlösning vid 25°C är cirka 0,5 timmar vid pH 5,0 och cirka 18 timmar vid pH 7,0.
PREVACID levereras i kapslar med fördröjd frisättning och PREVACID 15 mg SoluTab tillhandahålls i oralt sönderfallande tabletter med fördröjd frisättning (SoluTab) för oral administrering.
PREVACID finns i två doseringsstyrkor: 15 och 30 mg lansoprazol per kapsel. Varje kapsel med fördröjd frisättning innehåller enterodragerade granuler bestående av 15 eller 30 mg lansoprazol (aktiv ingrediens) och följande inaktiva ingredienser: sockersfär, sackaros, metakrylsyrasampolymer, lågsubstituerad hydroxipropylcellulosa, stärkelse, magnesiumkarbonat, talk, polyeten glykol, titandioxid, polysorbat 80, hydroxipropylcellulosa, kolloidal kiseldioxid, D&C Red No. 28, FD&C Blue No. 1, FD&C Green No. 31, och FD&C Red No. 40.
PREVACID 30 mg SoluTab finns i två doseringsstyrkor: 15 och 30 mg lansoprazol per tablett. Varje oralt sönderfallande tablett med fördröjd frisättning innehåller enterodragerade mikrogranuler som består av 15 eller 30 mg lansoprazol (aktiv ingrediens) och följande inaktiva ingredienser: mannitol, metakrylsyra, hydroxipropylcellulosa, laktosmonohydrat-mikrokristallin cellulosasfär, trikroetylcellulosacitrat, polyakrylat, magnesiumkarbonat, aspartam2, glycerylmonostearat, hypromellos, magnesiumstearat, citronsyra, titandioxid, talk, konstgjord jordgubbsarom, polyetylenglykol, polysorbat 80 och järnoxid.
1PREVACID endast 15 mg kapslar. 2Phenylketonurics: PREVACID SoluTab Innehåller fenylalanin 2,5 mg per 15 mg tablett och 5,1 mg per 30 mg tablett.
INDIKATIONER
Behandling av aktivt duodenalsår
PREVACID och PREVACID SoluTab är indicerade till vuxna för korttidsbehandling (under fyra veckor) för läkning och symtomlindring av aktivt duodenalsår [se Kliniska studier ].
Utrotning av H. pylori för att minska risken för återfall av duodenalsår
Trippelterapi: PREVACID eller PREVACID SoluTab/amoxicillin/klaritromycin
PREVACID eller PREVACID 30 mg SoluTab i kombination med amoxicillin plus klaritromycin som trippelterapi är indicerat för vuxna för behandling av patienter med H. pylori-infektion och duodenalsår (aktiv eller ett års anamnes på duodenalsår) för att utrota H. pylori. Utrotning av H. pylori har visat sig minska risken för återfall av duodenalsår [se Kliniska studier ].
Se den fullständiga förskrivningsinformationen för amoxicillin och klaritromycin.
Dubbelterapi: PREVACID eller PREVACID SoluTab/amoxicillin
PREVACID eller PREVACID 15mg SoluTab i kombination med amoxicillin som dubbelterapi är indicerat till vuxna för behandling av patienter med H. pylori-infektion och duodenalsårsjukdom (aktiv eller ett års anamnes på duodenalsår) som är antingen allergiska eller intoleranta mot klaritromycin eller hos vilka resistens mot klaritromycin är känd eller misstänkt (se förskrivningsinformation för klaritromycin, avsnittet Mikrobiologi). Utrotning av H. pylori har visat sig minska risken för återfall av duodenalsår [se Kliniska studier ].
Se hela förskrivningsinformationen för amoxicillin.
Underhåll av läkta duodenalsår
PREVACID och PREVACID SoluTab är indicerade för vuxna för att bibehålla läkning av duodenalsår. Kontrollerade studier sträcker sig inte längre än 12 månader [se Kliniska studier ].
Behandling av aktivt benignt magsår
PREVACID och PREVACID 30 mg SoluTab är indicerade till vuxna för korttidsbehandling (upp till åtta veckor) för läkning och symtomlindring av aktivt benignt magsår [se Kliniska studier ].
Läkning av NSAID-associerat magsår
PREVACID 30mg och PREVACID SoluTab är indicerade för vuxna för behandling av NSAID-associerade magsår hos patienter som fortsätter att använda NSAID. Kontrollerade studier sträckte sig inte längre än åtta veckor [se Kliniska studier ].
Riskminskning av NSAID-associerat magsår
PREVACID 15mg och PREVACID SoluTab är indicerade för vuxna för att minska risken för NSAID-associerade magsår hos patienter med en historia av ett dokumenterat magsår som kräver användning av ett NSAID. Kontrollerade studier sträckte sig inte längre än 12 veckor [se Kliniska studier ].
Behandling av symtomatisk gastroesofageal refluxsjukdom (GERD)
PREVACID 15mg och PREVACID 30mg SoluTab är indicerade för korttidsbehandling hos vuxna och pediatriska patienter 12 till 17 år (upp till åtta veckor) och pediatriska patienter från 1 till 11 år (upp till 12 veckor) för behandling av halsbränna och andra symtom associerade med GERD [se Kliniska studier ].
Behandling av erosiv esofagit (EE)
PREVACID 15mg och PREVACID 30mg SoluTab är indicerade för korttidsbehandling hos vuxna och pediatriska patienter 12 till 17 år (upp till åtta veckor) och pediatriska patienter från 1 till 11 år (upp till 12 veckor) för läkning och symtomlindring av alla grader av EE.
För vuxna som inte läker med PREVACID 30mg eller PREVACID 15mg SoluTab under åtta veckor (5 till 10%), kan det vara bra att ge ytterligare åtta veckors behandling. Om det finns ett återfall av erosiv esofagit kan ytterligare åtta veckors behandling med PREVACID 30 mg eller PREVACID SoluTab övervägas [se Kliniska studier ].
Underhåll av läkning av EE
PREVACID och PREVACID SoluTab är indicerade för vuxna för att bibehålla läkning av EE. Kontrollerade studier sträckte sig inte längre än 12 månader [se Kliniska studier ].
Patologiska hypersekretoriska tillstånd inklusive Zollinger-Ellisons syndrom (ZES)
PREVACID 15mg och PREVACID SoluTab är indicerade för vuxna för långtidsbehandling av patologiska hypersekretoriska tillstånd, inklusive Zollinger-Ellisons syndrom [se Kliniska studier ].
DOSERING OCH ADMINISTRERING
Rekommenderad vuxendosering enligt indikation
Rekommenderad pediatrisk dosering enligt indikation
Pediatriska patienter i åldern 1 till 11 år
I kliniska studier administrerades PREVACID inte längre än 12 veckor till 1 till 11 åringar. Det är inte känt om PREVACID är säkert och effektivt om det används längre än den rekommenderade varaktigheten. Överskrid inte den rekommenderade dosen och användningstiden för pediatriska patienter som beskrivs nedan [se Användning i specifika populationer ].
Nedsatt leverfunktion
Den rekommenderade dosen är 15 mg oralt dagligen hos patienter med gravt nedsatt leverfunktion (Child-Pugh C) [se Användning i specifika populationer ].
Viktig administrationsinformation
- Ta PREVACID eller PREVACID 30mg SoluTab före måltid.
- Krossa eller tugga inte PREVACID 15mg kapsel eller PREVACID 30mg SoluTab.
- Ta PREVACID eller PREVACID 30 mg SoluTab minst 30 minuter före sukralfat [se LÄKEMEDELSINTERAKTIONER ].
- Antacida kan användas samtidigt med PREVACID eller PREVACID SoluTab.
- Missade doser: Om en dos missas, administrera så snart som möjligt. Men om nästa schemalagda dos är beräknad, ta inte den missade dosen och ta nästa dos i tid. Ta inte två doser samtidigt för att kompensera för en missad dos.
PREVACID kapslar
- Svälj hela; tugga inte.
- För patienter som har svårt att svälja kapslar kan PREVACID kapslar öppnas och administreras oralt eller via en nasogastrisk sond i de mjuka livsmedel eller vätskor som anges nedan.
- Administrering av PREVACID i andra livsmedel eller vätskor än de som diskuteras nedan har inte studerats kliniskt och rekommenderas därför inte.
Administration i mjuka livsmedel (äppelmos, ENSURE-pudding, keso, yoghurt eller silade päron):
Administrering i vätskor (äppeljuice, apelsinjuice eller tomatjuice):
Administrering med äppeljuice genom en nasogastrisk slang (≥16 franska)
PREVACID 15mg SoluTab
- Bryt eller skär inte.
- Placera tabletten på tungan, låt den sönderfalla, med eller utan vatten, tills mikrogranulerna kan sväljas. Tugga inte mikrogranulerna.
- Tabletten sönderfaller vanligtvis på mindre än en minut.
- Alternativt, för barn eller andra patienter som har svårt att svälja tabletter, kan PREVACID SoluTab administreras med vatten via oral spruta eller NG-slang enligt följande:
Administration Med Vatten I En Oral Sprutan
Administrering med vatten via ett NG-rör (≥8 franska)
HUR LEVERERAS
Doseringsformer och styrkor
PREVACID 15mg Kapslar med fördröjd frisättning
- Styrkan 15 mg är en ogenomskinlig, rosa och grön kapsel präglad med "TAP" och "PREVACID 15".
- Styrkan 30 mg är en ogenomskinlig, rosa och svart kapsel präglad med "TAP" och "PREVACID 30".
PREVACID 30mg SoluTab oralt sönderfallande tabletter med fördröjd frisättning
- Styrkan 15 mg är en vit till gulaktig vit, odragerad rund tablett innehållande orange till mörkbruna prickar med "15" präglad på ena sidan.
- Styrkan 30 mg är en vit till gulaktig vit, odragerad rund tablett innehållande orange till mörkbruna prickar med "30" präglad på ena sidan.
Förvaring Och Hantering
PREVACID kapslar med fördröjd frisättning , 15 mg, är ogenomskinliga, rosa och gröna med "TAP" och "PREVACID 15" präglade på kapslarna. 30 mg kapslarna med fördröjd frisättning är ogenomskinliga, rosa och svarta med "TAP" och "PREVACID 30" präglade på kapslarna. De finns tillgängliga enligt följande:
PREVACID 30mg SoluTab oralt sönderfallande tabletter med fördröjd frisättning , 15 mg, är vita till gulvita, runda odragerade tabletter som innehåller orange till mörkbruna prickar, med "15" präglad på ena sidan av tabletten. De 30 mg är vita till gulvita, runda odragerade tabletter som innehåller orange till mörkbruna prickar, med "30" präglad på ena sidan av tabletten. Tabletterna finns tillgängliga enligt följande:
Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F)[se USP-kontrollerad rumstemperatur ].
Distribuerat av: Takeda Pharmaceuticals America, Inc., Deerfield, IL 60015. Reviderad: juni 2018
BIEFFEKTER
Följande allvarliga biverkningar beskrivs nedan och på andra ställen i märkningen:
- Akut Tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Clostridium difficile-associerad diarré [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Allvarliga kutana biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kutan och systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Cyanokobalamin (vitamin B12) brist [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypomagnesemi och mineralmetabolism [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Fundiska körtelpolyper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under mycket varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i klinisk praxis.
Över hela världen har över 10 000 patienter behandlats med PREVACID 30 mg i fas 2 eller fas 3 kliniska prövningar som involverar olika doser och behandlingslängder. Generellt sett har behandling med PREVACID 30 mg tolererats väl i både korttids- och långtidsstudier.
Följande biverkningar rapporterades av den behandlande läkaren ha ett möjligt eller troligt samband med läkemedel hos 1 % eller fler av de PREVACID-behandlade patienterna och inträffade i högre grad hos PREVACID-behandlade patienter än placebobehandlade patienter i Tabell 1.
Huvudvärk sågs också med mer än 1 % incidens men var vanligare med placebo. Incidensen av diarré var likartad mellan patienter som fick placebo och patienter som fick 15 och 30 mg PREVACID, men högre hos patienterna som fick 60 mg PREVACID (2,9, 1,4, 4,2 respektive 7,4%).
Den vanligaste rapporterade möjligen eller troligen behandlingsrelaterade biverkningen under underhållsbehandling var diarré.
riskreduktionsstudien av PREVACID för NSAID-associerade magsår var incidensen av diarré för patienter som behandlades med PREVACID 30 mg, misoprostol och placebo 5, 22 respektive 3 %.
En annan studie för samma indikation, där patienterna tog antingen en COX-2-hämmare eller lansoprazol och naproxen, visade att säkerhetsprofilen liknade den tidigare studien. Ytterligare reaktioner från denna studie som inte tidigare observerats i andra kliniska prövningar med PREVACID 30 mg inkluderade kontusion, duodenit, epigastriskt obehag, esofagusstörning, trötthet, hunger, hiatal bråck, heshet, försämrad magtömning, metaplasi och nedsatt njurfunktion.
Ytterligare biverkningar som inträffade hos mindre än 1 % av patienterna eller försökspersonerna som fick PREVACID 15 mg i inhemska prövningar visas nedan:
Kroppen som helhet - buken förstorad, allergisk reaktion, asteni, ryggsmärta, candidiasis, karcinom, bröstsmärtor (ej specificerat på annat sätt), frossa, ödem, feber, influensasyndrom, halitos, infektion (ej specificerat på annat sätt), sjukdomskänsla, nacksmärta, stelhet i nacken, smärta , bäckensmärta
Kardiovaskulära systemet - angina, arytmi, bradykardi, cerebrovaskulär olycka/hjärninfarkt, hypertoni/hypotension, migrän, hjärtinfarkt, hjärtklappning, chock (cirkulationssvikt), synkope, takykardi, vasodilatation
Matsmältningssystemet - onormal avföring, anorexi, bezoar, kardiospasm, kolelithiasis, kolit, muntorrhet, dyspepsi, dysfagi, enterit, erctation, esofagusstenos, esofagusår, esofagit, fekal missfärgning, flatulens, gastrisk anor gastropsengit gastropsengit, gastrisk anor gastropsengitis , gastrointestinala störningar, gastrointestinala blödningar, glossit, tandköttsblödningar, hematemes, ökad aptit, ökad salivutsöndring, melena, munsår, illamående och kräkningar, illamående och kräkningar och diarré, gastrointestinal moniliasis, ändtarmsinflammation, ändtarmsinflammation, ändtarmsinflammation, ändtarmsinflammation, tungstörning, ulcerös kolit, ulcerös stomatit
Endokrina systemet - diabetes mellitus, struma, hypotyreos Hemiska och lymfatiska systemet - anemi, hemolys, lymfadenopati
Metabolism och näringsstörningar - avitaminos, gikt, uttorkning, hyperglykemi/hypoglykemi, perifert ödem, viktökning/förlust
Muskuloskeletala systemet - artralgi, artrit, bensjukdom, ledstörning, benkramper, muskel- och skelettsmärta, myalgi, myasteni, ptos, synovit
Nervsystem - onormala drömmar, agitation, minnesförlust, ångest, apati, förvirring, kramper, demens, depersonalisering, depression, dubbelsidighet, yrsel, känslomässig labilitet, hallucinationer, hemiplegi, förvärrad fientlighet, hyperkinesi, hypertoni, hypestesi, sömnlöshet, minskad libido, minskad nervös/inkreatur neuros, parestesi, sömnstörning, somnolens, tankeavvikelse, tremor, yrsel
Andningssystem - astma, bronkit, ökad hosta, andnöd, näsblod, hemoptys, hicka, larynxneoplasi, lungfibros, faryngit, pleural störning, lunginflammation, andningsstörning, övre luftvägsinflammation/infektion, rinit, bihåleinflammation, stridor
Hud och bihang - akne, alopeci, kontaktdermatit, torr hud, fast utslag, hårstörning, makulopapulära utslag, nagelstörning, klåda, hudutslag, hudcancer, hudsjukdom, svettning, urtikaria
Särskilda sinnen - onormal syn, amblyopi, blefarit, dimsyn, grå starr, konjunktivit, dövhet, torra ögon, öron-/ögonsjukdom, ögonsmärta, glaukom, otitis media, parosmi, fotofobi, retinal degeneration/störning, smakförlust, smakförvrängning, tinnitus, syn fältdefekt
Urogenitala systemet - onormal menstruation, bröstförstoring, bröstsmärta, ömhet i brösten, dysmenorré, dysuri, gynekomasti, impotens, njursten, njursmärta, leukorré, menorragi, menstruationsstörning, penisstörning, polyuri, testikelstörning, urinrörssmärta, urinfrekvens, urinvägsinfektion, brådskande urinering, nedsatt urinering, vaginit
Erfarenhet efter marknadsföring
Ytterligare biverkningar har rapporterats sedan PREVACID och PREVACID 30 mg SoluTab har marknadsförts. Majoriteten av dessa fall är utländska och ett samband med PREVACID 15mg eller PREVACID SoluTab har inte fastställts. Eftersom dessa reaktioner rapporterades frivilligt från en population av okänd storlek, kan uppskattningar av frekvensen inte göras. Dessa händelser listas nedan av COSTART kroppssystem.
Kroppen som helhet - anafylaktiska/anafylaktoida reaktioner, systemisk lupus erythematosus;
Matsmältningssystemet - hepatotoxicitet, pankreatit, kräkningar;
Hemiska och lymfatiska systemet - agranulocytos, aplastisk anemi, hemolytisk anemi, leukopeni, neutropeni, pancytopeni, trombocytopeni och trombotisk trombocytopen purpura;
Infektioner och angrepp - Clostridium difficile-associerad diarré;
Metabolism och näringsstörningar - hypomagnesemi, hypokalcemi, hypokalemi, hyponatremi;
Muskuloskeletala systemet - benfraktur, myosit;
Hud och bihang - allvarliga dermatologiska reaktioner inklusive erythema multiforme, SJS/TEN (vissa dödliga), DRESS, AGEP, kutan lupus erythematosus;
Särskilda sinnen - talstörning;
Urogenitala systemet - interstitiell nefrit, urinretention.
Kombinationsterapi med amoxicillin och klaritromycin
I kliniska prövningar med kombinationsbehandling med PREVACID plus amoxicillin och klaritromycin, och PREVACID 30 mg plus amoxicillin, observerades inga biverkningar som var speciella för dessa läkemedelskombinationer. Biverkningar som har inträffat har begränsats till de som tidigare rapporterats med PREVACID 15 mg, amoxicillin eller klaritromycin.
Trippelterapi: PREVACID/amoxicillin/klaritromycin
De vanligast rapporterade biverkningarna för patienter som fick trippelbehandling under 14 dagar var diarré (7 %), huvudvärk (6 %) och smakförvrängning (5 %). Det fanns inga statistiskt signifikanta skillnader i frekvensen av rapporterade biverkningar mellan 10 och 14 dagars trippelbehandlingsregimer. Inga behandlingsuppkomna biverkningar observerades i signifikant högre frekvens med trippelterapi än med någon dubbelterapiregim.
Dubbelterapi: PREVACID/amoxicillin
De vanligaste rapporterade biverkningarna för patienter som fick PREVACID 30 mg tre gånger dagligen plus amoxicillin tre gånger dagligen dubbelbehandling var diarré (8 %) och huvudvärk (7 %). Inga behandlingsuppkomna biverkningar observerades i signifikant högre frekvens med PREVACID 30 mg tre gånger dagligen plus amoxicillin tre gånger dagligen dubbelbehandling än med PREVACID 15 mg enbart.
För information om biverkningar med antibakteriella medel (amoxicillin och klaritromycin) indikerade i kombination med PREVACID eller PREVACID SoluTab, se avsnittet Biverkningar i deras förskrivningsinformation.
Laboratorievärden
Följande förändringar i laboratorieparametrar hos patienter som fick PREVACID 30 mg rapporterades som biverkningar:
Onormala leverfunktionstester, ökad SGOT (AST), ökad SGPT (ALT), ökat kreatinin, ökat alkaliskt fosfatas, ökat globuliner, ökat GGTP, ökat/minskat/onormalt WBC, onormalt AG-förhållande, onormalt RBC, bilirubinemi, ökat kalium i blodet, ökad blodurea, kristallin urin närvarande, eosinofili, sänkt hemoglobin, hyperlipemi, ökade/sänkta elektrolyter, ökat/sänkt kolesterol, ökade glukokortikoider, ökat LDH, ökat/minskat/onormalt blodplättar, ökade gastrinnivåer och positivt fekalt ockult blod. Urinavvikelser som albuminuri, glykosuri och hematuri rapporterades också. Ytterligare isolerade laboratorieavvikelser rapporterades.
de placebokontrollerade studierna, när SGOT (AST) och SGPT (ALT) utvärderades, hade 0,4 % (4/978) och 0,4 % (11/2677) patienter, som fick placebo respektive PREVACID, enzymförhöjningar större än tre gånger den övre gränsen för normalområdet vid det sista behandlingsbesöket. Ingen av dessa patienter som fick PREVACID 30 mg rapporterade gulsot vid något tillfälle under studien.
I kliniska prövningar med kombinationsbehandling med PREVACID 15 mg plus amoxicillin och klaritromycin, och PREVACID plus amoxicillin, observerades inga ökade laboratorieavvikelser speciellt för dessa läkemedelskombinationer.
För information om förändringar i laboratorievärden med antibakteriella medel (amoxicillin och klaritromycin) indikerade i kombination med PREVACID eller PREVACID 30 mg SoluTab, se avsnittet Biverkningar i deras förskrivningsinformation.
LÄKEMEDELSINTERAKTIONER
Tabell 2 och 3 inkluderar läkemedel med kliniskt viktiga läkemedelsinteraktioner och interaktion med diagnostik när de administreras samtidigt med PREVACID 15mg eller PREVACID SoluTab och instruktioner för att förebygga eller hantera dem.
Se märkningen av samtidigt använda läkemedel för att få ytterligare information om interaktioner med PPI.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Förekomst av magmalignitet
Hos vuxna utesluter inte symtomatisk respons på behandling med PREVACID 15mg eller PREVACID SoluTab förekomst av magmalignitet. Överväg ytterligare uppföljning och diagnostiska tester hos vuxna patienter som har ett suboptimalt svar eller ett tidigt symtomatiskt återfall efter avslutad behandling med PPI. Hos äldre patienter, överväg också en endoskopi.
Akut Tubulointerstitiell nefrit
Akut tubulointerstial nefrit (TIN) har observerats hos patienter som tar PPI och kan uppträda när som helst under PPI-behandling. Patienter kan uppvisa olika tecken och symtom från symtomatiska överkänslighetsreaktioner till ospecifika symtom på nedsatt njurfunktion (t.ex. sjukdomskänsla, illamående, anorexi). I rapporterade fallserier diagnostiserades vissa patienter på biopsi och i frånvaro av extrarenala manifestationer (t.ex. feber, hudutslag eller artralgi). Avbryt behandling med PREVACID eller PREVACID 15 mg SoluTab och utvärdera patienter med misstänkt akut TIN [se KONTRAINDIKATIONER ].
Clostridium Difficile-associerad diarré
Publicerade observationsstudier tyder på att PPI-behandling som PREVACID 30mg och PREVACID 30mg SoluTab kan vara associerad med en ökad risk för Clostridium difficile-associerad diarré (CDAD), särskilt hos inlagda patienter. Denna diagnos bör övervägas för diarré som inte förbättras [se NEGATIVA REAKTIONER ].
Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas.
CDAD har rapporterats med användning av nästan alla antibakteriella medel. För mer information specifik för antibakteriella medel (klaritromycin och amoxicillin) indicerade för användning i kombination med PREVACID 15mg eller PREVACID 15mg SoluTab, se avsnittet Varningar och försiktighet i deras förskrivningsinformation.
Benfraktur
Flera publicerade observationsstudier tyder på att PPI-behandling kan vara associerad med en ökad risk för osteoporosrelaterade frakturer i höften, handleden eller ryggraden. Risken för frakturer ökade hos patienter som fick höga doser, definierade som flera dagliga doser, och långvarig PPI-behandling (ett år eller längre). Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas. Patienter med risk för osteoporosrelaterade frakturer bör hanteras enligt fastställda behandlingsriktlinjer [se DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER ].
Allvarliga kutana biverkningar
Allvarliga kutana biverkningar, inklusive Stevens-Johnsons syndrom (SJS) och toxisk epidermal nekrolys (TEN), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) och akut generaliserad exantematös pustulos (AGEP) har rapporterats i samband med användning av PPI. [ser NEGATIVA REAKTIONER ]. Avbryt behandlingen med PREVACID 30 mg eller PREVACID SoluTab vid de första tecknen eller symtomen på allvarliga kutana biverkningar eller andra tecken på överkänslighet och överväg ytterligare utvärdering.
Kutan och systemisk lupus erythematosus
Kutan lupus erythematosus (CLE) och systemisk lupus erythematosus (SLE) har rapporterats hos patienter som tar PPI, inklusive lansoprazol. Dessa händelser har inträffat som både nyuppkomst och förvärring av befintlig autoimmun sjukdom. Majoriteten av PPI-inducerade lupus erythematosus fall var CLE.
Den vanligaste formen av CLE som rapporterats hos patienter som behandlats med PPI var subakut CLE (SCLE) och inträffade inom veckor till år efter kontinuerlig läkemedelsbehandling hos patienter från spädbarn till äldre. I allmänhet observerades histologiska fynd utan organinblandning.
Systemisk lupus erythematosus (SLE) rapporteras mindre vanligt än CLE hos patienter som får PPI. PPI-associerad SLE är vanligtvis mildare än icke-läkemedelsinducerad SLE. Debut av SLE inträffade vanligtvis inom dagar till år efter påbörjad behandling, främst hos patienter från unga vuxna till äldre. Majoriteten av patienterna fick utslag; dock rapporterades också artralgi och cytopeni.
Undvik administrering av PPI under längre tid än vad som är medicinskt indicerat. Om tecken eller symtom som överensstämmer med CLE eller SLE noteras hos patienter som får PREVACID 15 mg eller PREVACID SoluTab, avbryt läkemedlet och hänvisa patienten till lämplig specialist för utvärdering. De flesta patienter förbättras med avbrytande av enbart PPI inom fyra till 12 veckor. Serologiska tester (t.ex. ANA) kan vara positiva och förhöjda serologiska testresultat kan ta längre tid att lösa än kliniska manifestationer.
Cyanokobalamin (vitamin B12) brist
Daglig behandling med syradämpande mediciner under lång tid (t.ex. längre än tre år) kan leda till malabsorption av cyanokobalamin (vitamin B12) orsakad av hypo- eller aklorhydri. Sällsynta rapporter om cyanokobalaminbrist som inträffat vid syrahämmande behandling har rapporterats i litteraturen. Denna diagnos bör övervägas om kliniska symtom som överensstämmer med cyanokobalaminbrist observeras hos patienter som behandlas med PREVACID eller PREVACID SoluTab.
Hypomagnesemi och mineralmetabolism
Hypomagnesemi, symtomatisk och asymtomatisk, har i sällsynta fall rapporterats hos patienter som behandlats med PPI under minst tre månader, i de flesta fall efter ett års behandling. Allvarliga biverkningar inkluderar stelkramp, arytmier och kramper. Hypomagnesemi kan leda till hypokalcemi och/eller hypokalemi och kan förvärra underliggande hypokalcemi hos riskpatienter. Hos de flesta patienter krävde behandling av hypomagnesemi magnesiumersättning och avbrytande av PPI.
För patienter som förväntas vara på långvarig behandling eller som tar PPI tillsammans med mediciner som digoxin eller läkemedel som kan orsaka hypomagnesemi (t.ex. diuretika), kan sjukvårdspersonal överväga att övervaka magnesiumnivåerna innan PPI-behandlingen påbörjas och med jämna mellanrum [se NEGATIVA REAKTIONER ].
Överväg att övervaka magnesium- och kalciumnivåerna innan behandling med PREVACID 30 mg eller PREVACID SoluTab påbörjas och regelbundet under behandling hos patienter med redan existerande risk för hypokalcemi (t.ex. hypoparatyreos). Komplettera med magnesium och/eller kalcium vid behov. Om hypokalcemi är behandlingsrefraktär, överväg att avbryta PPI.
Interaktioner med undersökningar för neuroendokrina tumörer
Serumkromogranin A (CgA)-nivåer ökar sekundärt till läkemedelsinducerade minskningar i magsyra. Den ökade CgA-nivån kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer. Sjukvårdsgivare bör tillfälligt avbryta lansoprazolbehandlingen minst 14 dagar innan CgA-nivåerna bedöms och överväga att upprepa testet om initiala CgA-nivåer är höga. Om serietest utförs (t.ex. för övervakning), bör samma kommersiella laboratorium användas för testning, eftersom referensintervallen mellan testerna kan variera [se LÄKEMEDELSINTERAKTIONER , KLINISK FARMAKOLOGI ].
Interaktion med metotrexat
Litteraturen tyder på att samtidig användning av PPI med metotrexat (främst i höga doser) kan höja och förlänga serumnivåerna av metotrexat och/eller dess metabolit, vilket kan leda till metotrexattoxicitet. Vid administrering av högdos metotrexat kan ett tillfälligt utsättande av PPI övervägas hos vissa patienter [se LÄKEMEDELSINTERAKTIONER , KLINISK FARMAKOLOGI ].
Patienter med fenylketonuri
Fenylalanin kan vara skadligt för patienter med fenylketonuri (PKU). PREVACID 30mg SoluTab innehåller fenylalanin, en komponent i aspartam. Varje 15 mg tablett innehåller 2,5 mg och varje 30 mg tablett innehåller 5,1 mg fenylalanin. Innan du förskriver PREVACID SoluTab till en patient med PKU, överväg den kombinerade dagliga mängden fenylalanin från alla källor, inklusive PREVACID 30 mg SoluTab.
Fundic körtelpolyper
PPI-användning är förknippad med en ökad risk för fundiska körtelpolyper som ökar vid långvarig användning, särskilt efter ett år. De flesta PPI-användare som utvecklade fundic gland polyper var asymtomatiska och fundic gland polyper identifierades tillfälligt vid endoskopi. Använd den kortaste varaktigheten av PPI-behandlingen som är lämplig för det tillstånd som behandlas.
Risk för förtjockning av hjärtklaffar hos pediatriska patienter yngre än ett år
PREVACID 30mg och PREVACID SoluTab är inte godkända för pediatriska patienter yngre än ett år. Icke-kliniska studier på unga råttor med lansoprazol har visat en negativ effekt av hjärtklaffförtjockning. Risken för hjärtklaffskada verkar inte vara relevant för patienter från ett år och äldre [se Användning i specifika populationer ].
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide och Användningsinstruktioner ).
Råda patienterna att:
Akut Tubulointerstitiell nefrit
Att ringa sin vårdgivare om de upplever tecken och/eller symtom associerade med akut tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Clostridium Difficile-associerad diarré
Att omedelbart ringa sin vårdgivare om de upplever diarré som inte förbättras [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Benfraktur
Att rapportera eventuella frakturer, särskilt i höften, handleden eller ryggraden, till sin vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Allvarliga kutana biverkningar
Att avbryta behandlingen med PREVACID eller PREVACID 30mg SoluTab och omedelbart ringa sin vårdgivare för ytterligare utvärdering [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kutan och systemisk lupus erythematosus
Att omedelbart ringa sin vårdgivare för eventuella nya eller förvärrade symtom associerade med kutan eller systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Cyanokobalamin (vitamin B12) brist
 Att rapportera eventuella kliniska symtom som kan vara associerade med cyanokobalaminbrist till sin vårdgivare, om de har fått PREVACID eller PREVACID SoluTab i mer än tre år [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hypomagnesemi och mineral
Metabolism Att rapportera eventuella kliniska symtom som kan vara associerade med hypomagnesemi, hypokalcemi och/eller hypokalemi till sin vårdgivare, om de har fått PREVACID eller PREVACID 15 mg SoluTab i minst tre månader [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Läkemedelsinteraktioner
Råda patienter att rapportera till sin vårdgivare om de tar produkter som innehåller rilpivirin [se KONTRAINDIKATIONER ] eller högdos metotrexat [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Graviditet
Informera en gravid kvinna om den potentiella risken för ett foster. Rekommendera kvinnor med reproduktionspotential att informera sin vårdgivare om en känd eller misstänkt graviditet [se Användning i specifika populationer ].
Administrering
- Missade doser: Om en dos missas, administrera så snart som möjligt. Men om nästa schemalagda dos är beräknad, ta inte den missade dosen och ta nästa dos i tid. Ta inte två doser samtidigt för att kompensera för en missad dos.
- PREVACID eller PREVACID 30 mg SoluTab ska tas innan du äter.
- Krossa eller tugga inte PREVACID 15 mg kapsel eller PREVACID SoluTab.
- Ta PREVACID eller PREVACID 30 mg SoluTab minst 30 minuter före sukralfat.
- Fenylketonurika: Innehåller fenylalanin 2,5 mg per 15 mg PREVACID 30 mg SoluTab tablett och 5,1 mg per 30 mg PREVACID SoluTab tablett.
PREVACID kapslar
- Svälj hela; tugga inte.
- För patienter som har svårt att svälja kapslar:
- PREVACID 15mg kapslar kan öppnas och strö på äppelmos, ENSURE pudding, keso, yoghurt eller silade päron
- PREVACID 15 mg kapslar kan också tömmas i en liten volym av antingen äppeljuice, apelsinjuice eller tomatjuice
- Alternativt kan PREVACID-kapslar administreras med äppeljuice via nasogastrisk sond
- Se bruksanvisningen för en beskrivning av alla berednings- och administreringsanvisningar
FÖREGÅENDE SoluTab
- Bryt eller skär inte.
- Placera tabletten på tungan; låt det sönderfalla, med eller utan vatten, tills partiklarna kan sväljas. Tugga inte partiklarna.
- Tabletten sönderfaller vanligtvis på mindre än en minut.
- Alternativt, för barn eller andra patienter som har svårt att svälja tabletter, kan PREVACID 30mg SoluTab administreras med vatten via oral spruta eller NG-rör, enligt beskrivningen i bruksanvisningen.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
två 24 månader långa karcinogenicitetsstudier behandlades Sprague-Dawley-råttor med orala lansoprazoldoser på 5 till 150 mg/kg/dag, ungefär en till 40 gånger exponeringen på en kroppsyta (mg/m²) för en person på 50 kg. av medelhöjd [1,46 m² kroppsyta (BSA)] givet den rekommenderade humandosen på 30 mg/dag. Lansoprazol producerade dosrelaterad gastrisk enterokromaffin-liknande (ECL) cellhyperplasi och ECL-cellkarcinoider hos både han- och honråttor. Det ökade också förekomsten av intestinal metaplasi av magepitel hos båda könen. Hos hanråttor gav lansoprazol en dosrelaterad ökning av testikulära interstitiell celladenom. Incidensen av dessa adenom hos råttor som fick doser på 15 till 150 mg/kg/dag (fyra till 40 gånger den rekommenderade humana dosen baserat på BSA) översteg den låga bakgrundsincidensen (intervall = 1,4 till 10 %) för denna råttstam.
en 24 månader lång karcinogenicitetsstudie behandlades CD-1-möss med orala lansoprazoldoser på 15 till 600 mg/kg/dag, två till 80 gånger den rekommenderade humana dosen baserat på BSA. Lansoprazol gav en dosrelaterad ökad incidens av gastrisk ECL-cellshyperplasi. Det gav också en ökad förekomst av levertumörer (hepatocellulärt adenom plus karcinom). Tumörincidensen hos möss av hankön som behandlats med 300 och 600 mg/kg/dag (40 till 80 gånger den rekommenderade humana dosen baserat på BSA) och möss av honkön behandlade med 150 till 600 mg/kg/dag (20 till 80 gånger den rekommenderade humana dosen) dos baserad på BSA) överskred intervallen för bakgrundsincidenser i historiska kontroller för denna mössstam. Lansoprazolbehandling producerade adenom i rete testis hos möss av hankön som fick 75 till 600 mg/kg/dag (10 till 80 gånger den rekommenderade humana dosen baserat på BSA).
En 26 veckor lång p53 (+/-) transgen muskarcinogenicitetsstudie var inte positiv.
Lansoprazol var positivt i Ames-testet och in vitro-analysen av humana lymfocyters kromosomavvikelse. Lansoprazol var inte genotoxiskt i ex vivo-testet för oplanerad DNA-syntes av hepatocyter från råtta (UDS), mikrokärntestet in vivo eller kromosomavvikelsetestet för benmärgsceller från råtta.
Lansoprazol vid orala doser upp till 150 mg/kg/dag (40 gånger den rekommenderade humana dosen baserat på BSA) visade sig inte ha någon effekt på fertilitet och reproduktionsförmåga hos han- och honråttor.
Användning i specifika populationer
Graviditet
Risksammanfattning
Tillgängliga data från publicerade observationsstudier indikerar totalt sett inte ett samband mellan negativa graviditetsresultat med lansoprazolbehandling (se Data ).
I reproduktionsstudier på djur gav oral administrering av lansoprazol till råttor under organogenes genom laktation vid 6,4 gånger den maximala rekommenderade humana dosen minskningar hos avkomman i lårbensvikt, lårbenslängd, krans-rumplängd och tillväxtplattans tjocklek (endast hanar) på postnatal dag 21 (se Data ). Dessa effekter var förknippade med minskad kroppsviktsökning. Informera gravida kvinnor om den potentiella risken för fostret.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för de angivna populationerna är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 till 4 % respektive 15 till 20 %.
Om PREVACID 15mg eller PREVACID 15mg SoluTab administreras med klaritromycin, gäller graviditetsinformationen för klaritromycin även för kombinationsregimen. Se förskrivningsinformationen för klaritromycin för mer information om användning under graviditet.
Data
Mänskliga data
Tillgängliga data från publicerade observationsstudier kunde inte visa ett samband mellan negativa graviditetsrelaterade utfall och lansoprazolanvändning. Metodologiska begränsningar av dessa observationsstudier kan inte definitivt fastställa eller utesluta någon läkemedelsrelaterad risk under graviditet. I en prospektiv studie av European Network of Teratology Information Services jämfördes resultaten från en grupp på 62 gravida kvinnor som administrerade median dagliga doser av 30 mg lansoprazol med en kontrollgrupp på 868 gravida kvinnor som inte tog några PPI. Det fanns ingen skillnad i frekvensen av större missbildningar mellan kvinnor exponerade för PPI och kontrollgruppen, motsvarande en relativ risk (RR)=1,04, [95 % konfidensintervall (CI) 0,25-4,21]. I en populationsbaserad retrospektiv kohortstudie som täckte alla levande födda i Danmark från 1996 till 2008, fanns det ingen signifikant ökning av större fosterskador under analys av första trimesterns exponering för lansoprazol hos 794 levande födda. En metaanalys som jämförde 1 530 gravida kvinnor exponerade för PPI åtminstone under första trimestern med 133 410 oexponerade gravida kvinnor visade ingen signifikant ökning av risken för medfödda missbildningar eller spontan abort med exponering för PPI (för större missbildningar Odds Ratio (OR)=1,12 , [95 % KI 0,86-1,45] och för spontanaborter OR=1,29, [95 % KI 0,841,97]).
Djurdata
Inga negativa effekter på embryo-fosterutveckling inträffade i studier utförda på dräktiga råttor vid orala lansoprazoldoser upp till 150 mg/kg/dag (40 gånger den rekommenderade dosen för människa [30 mg/dag] baserat på kroppsyta) administrerade under organogenes och gravida kaniner vid orala lansoprazoldoser upp till 30 mg/kg/dag (16 gånger den rekommenderade dosen för människa baserat på kroppsyta) administrerad under organogenesen.
En pre- och postnatal utvecklingstoxicitetsstudie på råttor med ytterligare effektmått för att utvärdera benutveckling utfördes med lansoprazol i orala doser på 10 till 100 mg/kg/dag (0,7 till 6,4 gånger den maximala rekommenderade humana lansoprazoldosen på 30 mg baserat på AUC [area under plasmakoncentration-tid-kurvan]) administrerat under organogenes genom laktation. Maternala effekter observerade vid 100 mg/kg/dag (6,4 gånger den maximala rekommenderade humana lansoprazoldosen på 30 mg baserat på AUC) inkluderade ökad graviditetsperiod, minskad kroppsviktsökning under graviditeten och minskad födokonsumtion. Antalet dödfödda födda ökade vid denna dos, vilket kan ha varit sekundärt till maternell toxicitet. Kroppsvikten för valparna minskade med 100 mg/kg/dag med början på dag 11 efter födseln. Lårbensvikt, lårbenslängd och längd på hjässan minskade med 100 mg/kg/dag på dag 21 efter födseln. Lårbensvikten minskade fortfarande i gruppen 100 mg/kg/dag vid åldern 17 till 18 veckor. Tillväxtplattans tjocklek minskade hos män med 100 mg/kg/dag på postnatal dag 21 och ökade hos män med 30 och 100 mg/kg/dag vid åldern 17 till 18 veckor. Effekterna på benparametrar var förknippade med minskning av kroppsviktsökning.
Laktation
Risksammanfattning
Det finns ingen information om förekomsten av lansoprazol i bröstmjölk, effekterna på det ammade barnet eller effekterna på mjölkproduktionen. Lansoprazol och dess metaboliter finns dock i råttmjölk. Utvecklings- och hälsofördelarna med amning bör övervägas tillsammans med moderns kliniska behov av PREVACID 30 mg eller PREVACID 30 mg SoluTab och eventuella negativa effekter på det ammade barnet från PREVACID 30 mg eller PREVACID SoluTab eller från det underliggande moderns tillståndet.
Pediatrisk användning
Säkerheten och effektiviteten av PREVACID 15 mg och PREVACID 30 mg SoluTab har fastställts hos pediatriska patienter i åldern ett år till 17 år för korttidsbehandling av symtomatisk GERD och erosiv esofagit.
kliniska studier av symtomatisk GERD och erosiv esofagit administrerades inte PREVACID 30 mg längre än 12 veckor till patienter i åldern ett år till 11 år. Det är inte känt om PREVACID 30mg och PREVACID SoluTab är säkra och effektiva om de används längre än den rekommenderade varaktigheten. Överskrid inte den rekommenderade dosen och varaktigheten för användning hos pediatriska patienter (se Toxicitetsdata för unga djur ).
PREVACID var inte effektivt hos pediatriska patienter med symtomatisk GERD en månad till yngre än ett år i en multicenter, dubbelblind, placebokontrollerad studie. Därför har säkerhet och effekt inte fastställts hos patienter yngre än ett år. Icke-kliniska studier på juvenila råttor har visat en negativ effekt av hjärtklaffförtjockning och benförändringar vid lansoprazoldoser högre än den maximalt rekommenderade ekvivalenta humandosen.
Nyfödda till mindre än ett års ålder
Lansoprazols farmakokinetik studerades hos pediatriska patienter med GERD i åldern mindre än 28 dagar och en till 11 månader. Jämfört med friska vuxna som fick 30 mg hade nyfödda högre exponering (medelviktbaserade normaliserade AUC-värden 2,04 och 1,88 gånger högre vid doser på 0,5 respektive 1 mg/kg/dag). Spädbarn i åldern ≤10 veckor hade clearance- och exponeringsvärden som liknade nyfödda. Spädbarn äldre än 10 veckor som fick 1 mg/kg/dag hade genomsnittliga AUC-värden som liknade vuxna som fick en dos på 30 mg.
Lansoprazol visade sig inte vara effektivt i en amerikansk och polsk fyra veckors, multicenter, dubbelblind, placebokontrollerad, parallellgruppsstudie av 162 patienter mellan en månad och yngre än 12 månader med symtomatisk GERD baserat på en medicinsk historia av gråt/tjat/irritabilitet i samband med matningar som inte hade svarat på konservativ GERD-hantering (dvs icke-farmakologisk intervention) under sju till 14 dagar. Patienter fick
lansoprazol som en suspension dagligen (0,2 till 0,3 mg/kg/dag hos spädbarn ≤10 veckor gamla eller 1,0 till 1,5 mg/kg/dag hos spädbarn äldre än 10 veckor eller placebo) i upp till fyra veckors dubbelblind behandling.
Det primära effektmåttet utvärderades genom mer än 50 % minskning från baslinjen i antingen procentandelen matningar med en episode av gråt/krångel/irritabilitet eller varaktigheten (minuter) av en episod av gråt/krångel/irritation inom en timme efter utfodring.
Det fanns ingen skillnad i andelen som svarade mellan gruppen lansoprazol pediatrisk suspension och placebogruppen (54 % i båda grupperna).
Det har inte rapporterats några biverkningar i pediatriska kliniska studier (en månad till yngre än 12 månader) som inte tidigare observerats hos vuxna.
Baserat på resultaten från fas 3-effektstudien visades lansoprazol inte vara effektivt. Därför stöder dessa resultat inte användningen av lansoprazol vid behandling av symtomatisk GERD hos spädbarn.
Ett år till 11 års ålder
I en okontrollerad, öppen amerikansk multicenterstudie fick 66 pediatriska patienter (ett år till 11 år) med GERD, baserat på kroppsvikt, en initial dos på antingen PREVACID 15 mg dagligen om ≤30 kg eller PREVACID 30 mg dagligen om mer än 30 kg administreras under åtta till 12 veckor. PREVACID-dosen ökades (upp till 30 mg två gånger dagligen) hos 24 av 66 pediatriska patienter efter två eller fler veckors behandling om de förblev symtomatiska. Vid baslinjen hade 85 % av patienterna lindriga till måttliga övergripande GERD-symtom (bedömda av forskarintervju), 58 % hade icke-erosiv GERD och 42 % hade erosiv esofagit (bedömd med endoskopi).
Efter åtta till 12 veckors behandling med PREVACID 15 mg visade intent-to-treat-analysen en ungefärlig 50 % minskning av frekvens och svårighetsgrad av GERD-symtom.
Tjugoen av 27 patienter med erosiv esofagit läktes vid åtta veckor och 100 % av patienterna helades vid 12 veckor genom endoskopi (tabell 4).
en studie av 66 pediatriska patienter i åldersgruppen ett år till 11 år efter behandling med PREVACID 15 mg oralt i doser på 15 mg dagligen till 30 mg två gånger dagligen, var ökningar av gastrinnivåer i serum liknande de som observerats i vuxna studier. Medianvärden för gastrin i serum i fasta ökade med 89 % från 51 pg/ml vid baslinjen till 97 pg/ml [interkvartilintervall (25:e till 75:e percentilen) på 71 till 130 pg/ml] vid det sista besöket.
Den pediatriska säkerheten för PREVACID 30 mg kapslar har utvärderats hos 66 pediatriska patienter i åldern ett till 11 år. Av de 66 patienterna med GERD tog 85 % (56/66) PREVACID 30 mg i åtta veckor och 15 % (10/66) tog det i 12 veckor.
De mest frekvent rapporterade (två eller fler patienter) behandlingsrelaterade biverkningarna hos patienter mellan 1 och 11 år (N=66) var förstoppning (5 %) och huvudvärk (3 %).
Tolv år till 17 års ålder
en okontrollerad, öppen amerikansk multicenterstudie behandlades 87 ungdomar (12 år till 17 år) med symtomatisk GERD med PREVACID i åtta till 12 veckor. Baslinje av övre endoskopier klassificerade dessa patienter i två grupper: 64 (74 %) icke-erosiv GERD och 23 (26 %) erosiv esofagit (EE). De icke-erosiva GERD-patienterna fick PREVACID 15 mg dagligen i åtta veckor och EE-patienterna fick PREVACID 30 mg dagligen i åtta till 12 veckor. Vid baslinjen hade 89 % av dessa patienter milda till måttliga övergripande GERD-symtom (bedömda av utredarintervjuer). Under åtta veckors behandling med PREVACID 15 mg upplevde tonårspatienter en 63 % minskning av frekvensen och en 69 % minskning av svårighetsgraden av GERD-symtom baserat på dagboksresultat.
Tjugoen av 22 (95,5 %) patienter med erosiv esofagit hos ungdomar helades efter åtta veckors behandling med PREVACID 15 mg. En patient förblev oläkt efter 12 veckors behandling (tabell 5).
Hos dessa 87 tonårspatienter var ökningar i serumgastrinnivåer liknande de som observerades i vuxenstudier, medianvärde av fastande serumgastrinnivåer ökade med 42 % från 45 pg/ml vid baslinjen till 64 pg/ml [interkvartilintervall (25:e till 75:e percentilen) av 44 till 88 pg/ml] vid det sista besöket. (Normala gastrinnivåer i serum är 25 till 111 pg/ml.)
Säkerheten för PREVACID kapslar har utvärderats hos dessa 87 tonårspatienter. Av de 87 tonårspatienterna med GERD tog 6 % (5/87) PREVACID 15 mg i mindre än sex veckor, 93 % (81/87) i sex till 10 veckor och 1 % (1/87) i mer än 10 veckor .
De vanligast rapporterade (minst 3 %) behandlingsrelaterade biverkningarna hos dessa patienter var huvudvärk (7 %), buksmärtor (5 %), illamående (3 %) och yrsel (3 %). Behandlingsrelaterad yrsel, som rapporterats i denna förskrivningsinformation som förekommer hos mindre än 1 % av vuxna patienter, rapporterades i denna studie av tre tonårspatienter med icke-erosiv GERD, som hade yrsel samtidigt med andra reaktioner (såsom migrän, dyspné, och kräkningar).
Toxicitetsdata för unga djur
Hjärtklaffsförtjockning
två orala toxicitetsstudier inträffade förtjockning av mitralisklaffen hos unga råttor som behandlats med lansoprazol. Hjärtklaffförtjockning observerades primärt med oral dosering som påbörjades på postnatal dag 7 (ålder motsvarande neonatala människor) och postnatal dag 14 (human åldersekvivalent på cirka ett år) vid doser på 250 mg/kg/dag och högre (vid postnatal dag 7) och postnatal dag 14, 6,2 gånger respektive 4,2 gånger den dagliga pediatriska dosen på 15 mg hos pediatriska patienter i åldern ett till 11 år som väger 30 kg eller mindre, baserat på AUC). Behandlingstiden förknippad med hjärtklaffförtjockning varierade från 5 dagar till 8 veckor. Fynden vände eller trendade mot reversibilitet efter en 4-veckors läkemedelsfri återhämtningsperiod. Incidensen av hjärtklaffförtjockning efter påbörjad dosering på postnatal dag 21 (human åldersekvivalent på cirka två år) var begränsad till en enstaka råtta (1/24) i grupper som fick 500 mg/kg/dag i 4 eller 8 veckor (ungefär 8 veckor) 5,2 gånger den dagliga pediatriska dosen på 15 mg hos pediatriska patienter i åldern ett till 11 år som väger 30 kg eller mindre, baserat på AUC). Baserat på exponeringsmarginaler verkar risken för hjärtklaffskada inte vara relevant för patienter från ett år och äldre.
Benförändringar
I en åtta veckor lång oral toxicitetsstudie på juvenila råttor med dosering inledd på postnatal dag 7, doser lika med eller större än 100 mg/kg/dag (2,5 gånger den dagliga pediatriska dosen på 15 mg hos barn i åldern ett till 11 år som väger 30 år) kg eller mindre, baserat på AUC) gav fördröjd tillväxt, med försämring av viktökningen observerades så tidigt som postnatal dag 10 (ålder motsvarande neonatala människor). I slutet av behandlingen inkluderade tecknen på nedsatt tillväxt vid 100 mg/kg/dag och högre minskningar i kroppsvikt (14 till 44 % jämfört med kontroller), absolut vikt av flera organ, lårbensvikt, lårbenslängd och krona. rumpans längd. Femoral tillväxtplattans tjocklek reducerades endast hos män och endast vid dosen 500 mg/kg/dag. Effekterna relaterade till fördröjd tillväxt kvarstod under slutet av den fyra veckor långa återhämtningsperioden. Långtidsdata samlades inte in.
Geriatrisk användning
Av det totala antalet patienter (n=21 486) i kliniska studier av PREVACID var 16 % av patienterna 65 år och äldre, medan 4 % var 75 år och äldre. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa patienter och yngre patienter och annan rapporterad klinisk erfarenhet har inte identifierat signifikanta skillnader i svar mellan geriatriska och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas [se KLINISK FARMAKOLOGI ].

Nedsatt leverfunktion
Hos patienter med olika grader av kroniskt nedsatt leverfunktion ökade exponeringen för lansoprazol jämfört med friska försökspersoner med normal leverfunktion [se KLINISK FARMAKOLOGI ]. Ingen dosjustering för PREVACID eller PREVACID SoluTab är nödvändig för patienter med mild (Child-Pugh klass A) eller måttlig (Child-Pugh klass B) nedsatt leverfunktion. Den rekommenderade dosen är 15 mg oralt dagligen hos patienter med gravt nedsatt leverfunktion (Child-Pugh klass C) [se DOSERING OCH ADMINISTRERING ].
ÖVERDOS
Lansoprazol avlägsnas inte från cirkulationen genom hemodialys. I en rapporterad överdos konsumerade en patient 600 mg PREVACID 15 mg utan biverkningar. Orala lansoprazoldoser upp till 5000 mg/kg hos råttor [cirka 1300 gånger den mänskliga dosen på 30 mg baserat på kroppsyta (BSA)] och hos möss (cirka 675,7 gånger den mänskliga dosen på 30 mg baserat på BSA) gav inga dödsfall eller några kliniska tecken.
I händelse av överexponering bör behandlingen vara symtomatisk och stödjande.
Om överexponering inträffar, ring ditt giftkontrollcenter på 1-800-222-1222 för aktuell information om hantering av förgiftning eller överexponering.
KONTRAINDIKATIONER
- PREVACID 15mg och PREVACID 15mg SoluTab är kontraindicerade hos patienter med känd överkänslighet mot någon komponent i formuleringen. Överkänslighetsreaktioner kan inkludera anafylaxi, anafylaktisk chock, angioödem, bronkospasm, akut tubulointerstitiell nefrit och urtikaria [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
- Protonpumpshämmare (PPI), inklusive PREVACID och PREVACID SoluTab, är kontraindicerade med produkter som innehåller rilpivirin [se LÄKEMEDELSINTERAKTIONER ].
- För information om kontraindikationer för antibakteriella medel (klaritromycin och amoxicillin) indikerade i kombination med PREVACID eller PREVACID 30mg SoluTab, se avsnittet Kontraindikationer i deras förskrivningsinformation.
KLINISK FARMAKOLOGI
Handlingsmekanism
Lansoprazol tillhör en klass av antisekretoriska föreningar, de substituerade bensimidazolerna, som undertrycker magsyrasekretionen genom specifik hämning av enzymsystemet (H+, K+)-ATPas vid den sekretoriska ytan av magparietalcellen. Eftersom detta enzymsystem betraktas som syrapumpen (proton) i parietalcellen, har lansoprazol karakteriserats som en magsyrapumpshämmare, genom att den blockerar det sista steget i syraproduktionen. Denna effekt är dosrelaterad och leder till hämning av både basal och stimulerad magsyrasekretion oavsett stimulans. Lansoprazol uppvisar inte antikolinerg eller histamin typ 2-antagonistaktivitet.
Farmakodynamik
Antisekretorisk aktivitet
Efter oral administrering visades lansoprazol signifikant minska basalsyraproduktionen och signifikant öka det genomsnittliga pH-värdet i magen och i procent av tiden som magsäckens pH var högre än tre och högre än fyra. Lansoprazol reducerade också signifikant måltidsstimulerad magsyraproduktion och sekretionsvolym, såväl som pentagastrinstimulerad syraproduktion. Hos patienter med hypersekretion av syra reducerade lansoprazol signifikant basal och pentagastrinstimulerad magsyrasekretion. Lansoprazol hämmade den normala ökningen av sekretionsvolym, surhet och syraproduktion som inducerades av insulin.
De intragastriska pH-resultaten från en fem dagars, farmakodynamisk, crossover-studie med 15 och 30 mg lansoprazol en gång dagligen presenteras i Tabell 6:
Efter den initiala dosen i denna studie sågs ett ökat pH i magen inom en till två timmar med 30 mg lansoprazol och två till tre timmar med 15 mg lansoprazol. Efter flera dagliga doser sågs ett ökat mag-pH inom den första timmen efter dosering med 30 mg lansoprazol och inom en till två timmar efter dosering med 15 mg lansoprazol.
Syrasuppression kan förstärka effekten av antimikrobiella medel för att utrota Helicobacter pylori (H. pylori). Procentandelen av den tid som gastriskt pH höjdes över fem och sex utvärderades i en crossover-studie av PREVACID givet dagligen, två gånger dagligen och tre gånger dagligen (tabell 7).
Hämningen av magsyrasekretionen mätt med intragastriskt pH återgick gradvis till det normala under två till fyra dagar efter flera doser. Det fanns ingen indikation på rebound magsyra.
Enterokromaffinliknande (ECL) celleffekter
Under livstidsexponering av råttor med upp till 150 mg/kg/dag lansoprazol doserat sju dagar i veckan, observerades markant hypergastrinemi följt av ECL-cellproliferation och bildning av karcinoida tumörer, särskilt hos honråttor. Magbiopsiprover från magkroppen från cirka 150 patienter som behandlats kontinuerligt med lansoprazol i minst ett år visade inga tecken på ECL-celleffekter liknande de som setts i råttstudier. Långtidsdata behövs för att utesluta möjligheten för en ökad risk för utveckling av magtumörer hos patienter som får långtidsbehandling med lansoprazol [se Icke-klinisk toxikologi ].
Andra mageffekter hos människor
Lansoprazol påverkade inte slemhinneblodflödet i fundus i magsäcken signifikant. På grund av den normala fysiologiska effekten orsakad av hämningen av magsyrasekretionen sågs en minskning med cirka 17 % i blodflödet i antrum, pylorus och duodenalbulben. Lansoprazol bromsade signifikant magtömningen av smältbara fasta ämnen. Lansoprazol ökade serumpepsinogennivåerna och minskade pepsinaktiviteten under basala förhållanden och som svar på måltidsstimulering eller insulininjektion. Liksom med andra medel som höjer intragastriskt pH var ökningar i magsäckens pH associerade med ökningar av nitratreducerande bakterier och förhöjd nitritkoncentration i magsaft hos patienter med magsår. Ingen signifikant ökning av nitrosaminkoncentrationer observerades.
Serum Gastrin Effekter
Hos över 2 100 patienter ökade medianvärdena för gastrin i serum i fasta med 50 till 100 % från baslinjen men förblev inom normalområdet efter behandling med 15 till 60 mg oralt lansoprazol. Dessa höjningar nådde en platå inom två månader efter behandlingen och återgick till nivåerna före behandlingen inom fyra veckor efter avslutad behandling.
Ökat gastrin orsakar enterokromaffinliknande cellhyperplasi och ökade CgA-nivåer i serum. De ökade CgA-nivåerna kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Endokrina effekter
Mänskliga studier i upp till ett år har inte upptäckt några kliniskt signifikanta effekter på det endokrina systemet. Hormoner som studerats inkluderar testosteron, luteiniserande hormon (LH), follikelstimulerande hormon (FSH), könshormonbindande globulin (SHBG), dehydroepiandrosteronsulfat (DHEA-S), prolaktin, kortisol, östradiol, insulin, aldosteron, parathormon, glukagon, sköldkörtelstimulerande hormon (TSH), trijodtyronin (T3), tyroxin (T4) och somatotropt hormon (STH). Lansoprazol i orala doser på 15 till 60 mg i upp till ett år hade ingen kliniskt signifikant effekt på sexuell funktion. Dessutom hade lansoprazol i orala doser på 15 till 60 mg under två till åtta veckor ingen kliniskt signifikant effekt på sköldkörtelfunktionen. I 24 månaders karcinogenicitetsstudier på Sprague-Dawley-råttor med dagliga lansoprazoldoser upp till 150 mg/kg ökade proliferativa förändringar i Leydig-cellerna i testiklarna, inklusive benign neoplasm, jämfört med kontrollråttor.
Andra effekter
Inga systemiska effekter av lansoprazol på det centrala nervsystemet, lymfoida, hematopoetiska, njur-, lever-, kardiovaskulära eller andningsorganen har hittats hos människor. Bland 56 patienter som hade omfattande ögonutvärderingar vid utgångsläget observerades ingen visuell toxicitet efter lansoprazolbehandling (upp till 180 mg/dag) i upp till 58 månader. Efter livstidsexponering för lansoprazol hos råttor sågs fokal pankreatrofi, diffus lymfoid hyperplasi i tymus och spontan retinal atrofi.
Farmakokinetik
Absorption
PREVACID 15mg och PREVACID SoluTab innehåller en enterodragerad granulformulering av lansoprazol (eftersom lansoprazol är syralabilt), så att absorptionen av lansoprazol börjar först efter att granulerna lämnat magen. De genomsnittliga maximala plasmanivåerna av lansoprazol inträffar efter cirka 1,7 timmar. Efter en engångsdos av 15 till 60 mg oral lansoprazol var de maximala plasmakoncentrationerna (Cmax) av lansoprazol och arean under plasmakoncentrationskurvorna (AUC) för lansoprazol ungefär proportionella mot den administrerade dosen. Lansoprazol ackumuleras inte och dess farmakokinetik är oförändrad vid upprepad dosering. Den absoluta biotillgängligheten är över 80 %. Hos friska försökspersoner var den genomsnittliga (±SD) plasmahalveringstiden 1,5 (±1,0) timmar. Både Cmax och AUC minskar med cirka 50 till 70 % om lansoprazol ges 30 minuter efter mat, jämfört med fastetillståndet. Det finns ingen signifikant födoeffekt om lansoprazol ges före måltid.
Distribution
Lansoprazol är till 97 % bundet till plasmaproteiner. Plasmaproteinbindningen är konstant över koncentrationsintervallet 0,05 till 5 mcg/ml.
Eliminering
Ämnesomsättning
Lansoprazol metaboliseras i stor utsträckning i levern. Två metaboliter har identifierats i mätbara mängder i plasma (de hydroxylerade sulfinyl- och sulfonderivaten av lansoprazol). Dessa metaboliter har mycket liten eller ingen antisekretorisk aktivitet. Lansoprazol tros omvandlas till två aktiva arter som hämmar syrasekretionen genom att blockera protonpumpen [(H+, K+)-ATPas-enzymsystemet] vid den sekretoriska ytan av den gastriska parietalcellen. De två aktiva arterna finns inte i den systemiska cirkulationen. Halveringstiden för plasmaeliminering av lansoprazol är mindre än två timmar medan den syrahämmande effekten varar i mer än 24 timmar. Därför återspeglar plasmaelimineringshalveringstiden för lansoprazol inte dess varaktighet av suppression av magsyrasekretion.
Exkretion
Efter oral engångsdos av PREVACID utsöndrades praktiskt taget inget oförändrat lansoprazol i urinen. I en studie, efter en oral engångsdos av 14Clansoprazol, utsöndrades ungefär en tredjedel av den administrerade strålningen i urinen och två tredjedelar återfanns i avföringen. Detta innebär en betydande gallutsöndring av lansoprazolmetaboliterna.
Specifika populationer
Pediatriska patienter
Ett till 17 års ålder
Lansoprazols farmakokinetik studerades hos pediatriska patienter med GERD i åldern ett till 11 år och 12 till 17 år i två separata kliniska studier. Hos barn i åldrarna ett till 11 år gavs lansoprazol 15 mg dagligen för försökspersoner som vägde ≤30 kg och 30 mg dagligen för försökspersoner som vägde mer än 30 kg. Medelvärden för Cmax och AUC som observerades på dag 5 av doseringen var likartade mellan de två dosgrupperna och påverkades inte av vikt eller ålder inom varje viktjusterad dosgrupp som användes i studien. Hos ungdomar i åldern 12 till 17 år randomiserades försökspersonerna till att få lansoprazol med 15 eller 30 mg dagligen. Medelvärden för Cmax och AUC för lansoprazol påverkades inte av kroppsvikt eller ålder; och nästan dosproportionella ökningar av genomsnittliga Cmax- och AUC-värden observerades mellan de två dosgrupperna i studien. Sammantaget var lansoprazols farmakokinetik hos pediatriska patienter i åldern 1 till 17 år liknande den som observerats hos friska vuxna försökspersoner.
Geriatriska patienter
Clearance av lansoprazol är minskat hos äldre, med halveringstid för eliminering ökad med cirka 50 till 100 %. Eftersom den genomsnittliga halveringstiden hos äldre förblir mellan 1,9 till 2,9 timmar, leder upprepad dosering en gång dagligen inte till ackumulering av lansoprazol. Toppplasmanivåer ökade inte hos äldre [se Användning i specifika populationer ].
Manliga Och Kvinnliga Patienter
I en studie som jämförde 12 manliga och sex kvinnliga försökspersoner som fick lansoprazol fann man inga könsrelaterade skillnader i farmakokinetik och intragastriska pH-resultat.
Ras eller etniska grupper
De sammanslagna farmakokinetiska medelparametrarna för PREVACID från tolv amerikanska studier (N=513) jämfördes med de genomsnittliga farmakokinetiska parametrarna från två asiatiska studier (N=20). De genomsnittliga AUC:erna för PREVACID 30 mg hos asiatiska försökspersoner var ungefär två gånger de som sågs i poolade amerikanska data; variabiliteten mellan individer var dock hög. Cmax-värdena var jämförbara.
Patienter med nedsatt njurfunktion
Hos patienter med gravt nedsatt njurfunktion minskade plasmaproteinbindningen med 1 till 1,5 % efter administrering av 60 mg lansoprazol. Patienter med nedsatt njurfunktion hade en förkortad eliminationshalveringstid och minskad total AUC (fritt och bundet). AUC för fritt lansoprazol i plasma var dock inte relaterat till graden av nedsatt njurfunktion; och Cmax och Tmax (tiden för att nå maximal koncentration) skilde sig inte från Cmax och Tmax från patienter med normal njurfunktion. Lansoprazols farmakokinetik var därför inte kliniskt annorlunda hos patienter med mild, måttlig eller gravt nedsatt njurfunktion jämfört med friska försökspersoner med normal njurfunktion.
Patienter med nedsatt leverfunktion
Hos patienter med mild (Child-Pugh klass A) eller måttlig (Child-Pugh klass B) nedsatt leverfunktion sågs en ungefärlig 3-faldig ökning av genomsnittlig AUC jämfört med friska försökspersoner med normal leverfunktion efter flera orala doser på 30 mg PREVACID 30 mg i sju dagar. Motsvarande genomsnittliga plasmahalveringstid för lansoprazol förlängdes från 1,5 till fyra timmar (Child-Pugh A) eller fem timmar (Child-Pugh B).
Hos patienter med kompenserad och dekompenserad cirros var det en ungefärlig 6- respektive 5-faldig ökning av AUC jämfört med friska försökspersoner med normal leverfunktion efter en oral engångsdos på 30 mg PREVACID [se DOSERING OCH ADMINISTRERING , Användning i specifika populationer ].
Läkemedelsinteraktionsstudier
Effekt av Lansoprazol på andra droger
Cytokrom P450-interaktioner
Lansoprazol metaboliseras genom cytokrom P450-systemet, specifikt genom isozymerna CYP3A och CYP2C19. Studier har visat att PREVACID 15mg inte har kliniskt signifikanta interaktioner med andra läkemedel som metaboliseras av cytokrom P450-systemet, såsom warfarin, antipyrin, indometacin, ibuprofen, fenytoin, propranolol, prednison, diazepam eller klaritromycin hos friska försökspersoner. Dessa föreningar metaboliseras genom olika cytokrom P450-isozymer inklusive CYP1A2, CYP2C9, CYP2C19, CYP2D6 och CYP3A.
Teofyllin
När PREVACID 30 mg administrerades samtidigt med teofyllin (CYP1A2, CYP3A) sågs en mindre ökning (10 %) i clearance av teofyllin. På grund av den lilla omfattningen och riktningen av effekten på teofyllinclearance är det osannolikt att denna interaktion är av klinisk betydelse [se LÄKEMEDELSINTERAKTIONER ].
Metotrexat och 7-hydroximetotrexat
en öppen, enkelarmad, åtta dagars, farmakokinetisk studie av 28 vuxna patienter med reumatoid artrit (som krävde kronisk användning av 7,5 till 15 mg metotrexat varje vecka), administrering av sju dagars naproxen 500 mg två gånger dagligen och PREVACID 30 mg dagligen hade ingen effekt på farmakokinetiken för metotrexat och 7-hydroximetotrexat. Även om denna studie inte var utformad för att bedöma säkerheten för denna kombination av läkemedel, noterades inga större biverkningar. Denna studie genomfördes dock med låga doser metotrexat. En läkemedelsinteraktionsstudie med höga doser metotrexat har inte utförts [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Amoxicillin
PREVACID 30 mg har inte heller visat sig ha någon kliniskt signifikant interaktion med amoxicillin.
Sukralfat
I en endosövergångsstudie som undersökte PREVACID 30 mg administrerat ensamt och samtidigt med sukralfat 1 gram, fördröjdes absorptionen av lansoprazol och biotillgängligheten minskade med 17 % när det administrerades samtidigt med sukralfat [se DOSERING OCH ADMINISTRERING , LÄKEMEDELSINTERAKTIONER ].
Antacida
kliniska prövningar administrerades antacida samtidigt med PREVACID 15 mg och det fanns inga tecken på en förändring i effekten av PREVACID.
Clopidogrel
Klopidogrel metaboliseras till sin aktiva metabolit delvis av CYP2C19. En studie på friska försökspersoner som var CYP2C19-extensiva metaboliserare, som fick en gång dagligen administrering av klopidogrel 75 mg ensamt eller samtidigt med PREVACID 30 mg (n=40), under nio dagar genomfördes. Medel-AUC för den aktiva metaboliten av klopidogrel minskade med cirka 14 % (genomsnittligt AUC-förhållande var 86 %, med 90 % KI på 80 till 92 %) när PREVACID gavs samtidigt jämfört med administrering av enbart klopidogrel.
Farmakodynamiska parametrar mättes också och visade att förändringen i hämning av trombocytaggregation (inducerad av 5 mcM ADP) var relaterad till förändringen i exponeringen för klopidogrel aktiv metabolit. Effekten på exponering för den aktiva metaboliten av klopidogrel och på klopidogrel-inducerad trombocythämning anses inte vara kliniskt viktig.
Effekt av andra droger på Lansoprazol
Eftersom lansoprazol metaboliseras av CYP2C19 och CYP3A4, kan inducerare och hämmare av dessa enzymer potentiellt förändra exponeringen av lansoprazol.
Mikrobiologi
Mikrobiologi
Lansoprazol, klaritromycin och/eller amoxicillin har visat sig vara aktiva mot de flesta stammar av Helicobacter pylori in vitro och vid kliniska infektioner [se INDIKATIONER OCH ANVÄNDNING ].
Helicobacter Pylori förbehandlingsresistens
Klaritromycinförbehandlingsresistens (≥2,0 mcg/ml) var 9,5 % (91/960) enligt E-test och 11,3 % (12/106) med agarutspädning i de kliniska prövningarna med dubbel- och trippelterapi (M93-125, M93-130, M93131, M95-392 och M95-399).
Förbehandlingskänsliga isolat för amoxicillin (≤0,25 mcg/ml) förekom hos 97,8 % (936/957) och 98,0 % (98/100) av patienterna i de kliniska prövningarna med dubbel- och trippelterapi med E-test respektive agarutspädning. Tjugoen av 957 patienter (2,2 %) genom E-test, och två av 100 patienter (2,0 %) med agarutspädning, hade amoxicillin förbehandlings-MIC som var större än 0,25 mikrogram/ml. En patient på 14-dagars trippelbehandlingsregimen hade en obekräftad lägsta hämmande koncentration av amoxicillin (MIC) före behandling som var större än 256 mcg/ml genom E-test och patienten utrotades av H. pylori (tabell 8).
Patienter som inte utrotats av H. pylori efter trippelbehandling med lansoprazol/amoxicillin/klaritromycin kommer sannolikt att ha klaritromycinresistent H. pylori. Därför, för de patienter som misslyckas med behandlingen, bör klaritromycinkänslighetstest göras när det är möjligt. Patienter med klaritromycinresistent H. pylori bör inte behandlas med trippelterapi med lansoprazol/amoxicillin/klaritromycin eller med regimer som inkluderar klaritromycin som det enda antimikrobiella medlet.
Resultat från amoxicillinkänslighetstest och kliniska/bakteriologiska resultat
de kliniska prövningarna med dubbel- och trippelterapi utrotades H. pylori hos 82,6 % (195/236) av patienterna som hade amoxicillinkänsliga MIC (≤0,25 mcg/ml) före behandling. Av dem med förbehandling amoxicillin MIC på mer än 0,25 mcg/ml, hade tre av sex H. pylori utrotats. Totalt 30 % (21/70) av patienterna misslyckades med lansoprazol 30 mg tre gånger dagligen/amoxicillin 1 g tre gånger dagligen dubbelbehandling och totalt 12,8 % (22/172) av patienterna misslyckades med 10 och 14 dagars trippel. terapiregimer. Resultat efter behandling erhölls inte på 11 av patienterna som misslyckades med behandlingen. Nio av de 11 patienterna med amoxicillin efter behandling med MIC som misslyckades med trippelbehandlingsregimen hade också klaritromycinresistenta H. pylori-isolat.
Känslighetstest för Helicobacter pylori
För känslighetstestningsinformation om Helicobacter pylori, se Mikrobiologi avsnitt i förskrivningsinformation för klaritromycin och amoxicillin .
Kliniska studier
Duodenalsår
en amerikansk multicenter, dubbelblind, placebokontrollerad dos-respons (15, 30 och 60 mg PREVACID en gång dagligen) studie av 284 patienter med endoskopiskt dokumenterat sår på tolvfingertarmen, var andelen patienter läkta efter två och fyra veckor. signifikant högre med alla doser av PREVACID än med placebo. Det fanns inga tecken på ett större eller tidigare svar med de två högre doserna jämfört med PREVACID 15 mg. Baserat på denna studie och den andra studien som beskrivs nedan är den rekommenderade dosen av PREVACID 15 mg vid duodenalsår 15 mg per dag (tabell 9).
PREVACID 15 mg var signifikant effektivare än placebo för att lindra buksmärtor dag och natt och för att minska mängden antacida som togs per dag.
en andra amerikansk multicenterstudie, även dubbelblind, placebokontrollerad, dosjämförelse (15 och 30 mg PREVACID 15 mg en gång dagligen), och inklusive en jämförelse med ranitidin, på 280 patienter med endoskopiskt dokumenterat duodenalsår, patienter som läkte efter fyra veckor var signifikant högre med båda doserna av PREVACID 15 mg än med placebo. Det fanns inga tecken på ett större eller tidigare svar med den högre dosen av PREVACID. Även om 15 mg-dosen av PREVACID var överlägsen ranitidin efter fyra veckor, lämnar avsaknaden av signifikant skillnad efter två veckor och frånvaron av en skillnad mellan 30 mg PREVACID och ranitidin den jämförande effektiviteten av de två medlen obestämd (tabell 10) [ ser INDIKATIONER OCH ANVÄNDNING ].
Utrotning av H. pylori för att minska risken för återfall av duodenalsår
Randomiserade, dubbelblinda kliniska studier utförda i USA på patienter med H. pylori och duodenalsårsjukdom (definierad som ett aktivt sår eller historia av ett sår inom ett år) utvärderade effekten av PREVACID i kombination med amoxicillin och klaritromycin som trippel 14 dagsterapi eller i kombination med amoxicillin som dubbel 14 dagars terapi för utrotning av H. pylori. Baserat på resultaten av dessa studier fastställdes säkerheten och effekten av två olika utrotningsregimer:
Trippelterapi : PREVACID 30 mg två gånger dagligen/amoxicillin 1 g två gånger dagligen/klaritromycin 500 mg två gånger dagligen
Dubbel terapi : PREVACID 30 mg tre gånger dagligen/amoxicillin 1 g tre gånger dagligen
Alla behandlingar var under 14 dagar. H. pylori-utrotning definierades som två negativa tester (odling och histologi) fyra till sex veckor efter avslutad behandling.
Trippelterapi visade sig vara effektivare än alla möjliga kombinationer av dubbelterapi. Dubbelterapi visade sig vara effektivare än båda monoterapierna. Utrotning av H. pylori har visat sig minska risken för återfall av duodenalsår.
En randomiserad, dubbelblind klinisk studie utförd i USA på patienter med H. pylori och duodenalsårsjukdom (definierad som ett aktivt sår eller historia av ett sår inom ett år) jämförde effekten av PREVACID trippelbehandling under 10 och 14 dagar. Denna studie fastställde att 10 dagars trippelterapi var ekvivalent med 14 dagars trippelterapi för att utrota H. pylori (tabellerna 11 och 12) [se INDIKATIONER OCH ANVÄNDNING ].
Underhåll av läkta duodenalsår
PREVACID har visat sig förhindra återfall av duodenalsår. Två oberoende, dubbelblinda, multicenter, kontrollerade studier utfördes på patienter med endoskopiskt bekräftade läkta duodenalsår. Patienterna förblev läkta betydligt längre och antalet återfall av duodenalsår var signifikant färre hos patienter som behandlades med PREVACID 15 mg än hos patienter som behandlades med placebo under en 12-månadersperiod (tabell 13) [se INDIKATIONER OCH ANVÄNDNING ].
I försök #2 noterades ingen signifikant skillnad mellan PREVACID 15 och 30 mg för att bibehålla remission.
Magsår
I en amerikansk multicenter, dubbelblind, placebokontrollerad studie av 253 patienter med endoskopiskt dokumenterat magsår, var andelen patienter läkta vid fyra och åtta veckor signifikant högre med PREVACID 15 och 30 mg en gång dagligen än med placebo (tabell 14) ) [ser INDIKATIONER OCH ANVÄNDNING ].
Patienter som behandlats med vilken PREVACID-dos som helst rapporterade signifikant mindre buksmärtor dag och natt tillsammans med färre dagar av antacida användning och färre antacida tabletter per dag än placebogruppen.
Oberoende belägg för effektiviteten av PREVACID 30 mg gavs genom en metaanalys av publicerade och opublicerade data.
Läkning av NSAID-associerat magsår
två amerikanska och kanadensiska multicenter, dubbelblinda, aktivkontrollerade studier på patienter med endoskopiskt bekräftat NSAID-associerat magsår som fortsatte sin NSAID-användning, var andelen patienter som läkte efter åtta veckor statistiskt signifikant högre med 30 mg PREVACID än med den aktiva kontrollen. Totalt 711 patienter inkluderades i studien och 701 patienter behandlades. Patienterna varierade i ålder från 18 till 88 år (medianåldern 59 år), med 67 % kvinnliga patienter och 33 % manliga patienter. Rasen fördelade sig enligt följande: 87 % kaukasiskt, 8 % svart, 5 % övrigt. Det fanns ingen statistiskt signifikant skillnad mellan PREVACID 30 mg dagligen och den aktiva kontrollen avseende symtomlindring (dvs buksmärtor) (tabell 15) [se INDIKATIONER OCH ANVÄNDNING ].
Riskminskning av NSAID-associerat magsår
en stor amerikansk, multicenter, dubbelblind, placebo- och misoprostolkontrollerad (misoprostol blindad endast för endoskopisten) studie på patienter som krävde kronisk användning av ett NSAID och som hade en historia av ett endoskopiskt dokumenterat magsår, var andelen av patienter som förblev fria från magsår vid fyra, åtta och 12 veckor var signifikant högre med 15 eller 30 mg PREVACID 15 mg än placebo. Totalt 537 patienter inkluderades i studien och 535 patienter behandlades. Patienterna varierade i ålder från 23 till 89 år (medianåldern 60 år), med 65 % kvinnliga patienter och 35 % manliga patienter. Rasen fördelade sig enligt följande: 90 % kaukasiskt, 6 % svart, 4 % annat. 30 mg-dosen av PREVACID visade ingen ytterligare fördel i riskminskning av det NSAID-associerade magsåret än 15 mg-dosen (tabell 16) [se INDIKATIONER OCH ANVÄNDNING ].
Symtomatisk gastroesofageal refluxsjukdom (GERD)
Symtomatisk GERD
en amerikansk multicenter, dubbelblind, placebokontrollerad studie av 214 patienter med frekventa GERD-symtom, men inga esofaguserosion genom endoskopi, observerades signifikant större lindring av halsbränna i samband med GERD vid administrering av lansoprazol 15 mg en gång dagligen upp till åtta veckor än med placebo. Ingen signifikant ytterligare nytta av lansoprazol 30 mg en gång dagligen observerades.
Intent-to-treat-analyserna visade signifikant minskning av frekvens och svårighetsgrad av halsbränna dag och natt. Data för frekvens och svårighetsgrad för behandlingsperioden på åtta veckor presenteras i tabell 17 och i figur 1 och 2:
Figur 1: Dagens genomsnittliga svårighetsgrad Halsbränna efter studiedag för utvärderbara patienter (3=svår, 2=måttlig, 1=lindrig, 0=ingen)
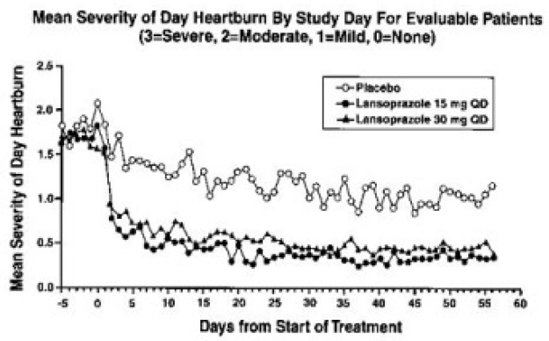
Figur 2: Genomsnittlig svårighetsgrad av halsbränna på natten efter studiedag för utvärderbara patienter (3=svår, 2=måttlig, 1=lindrig, 0=ingen)
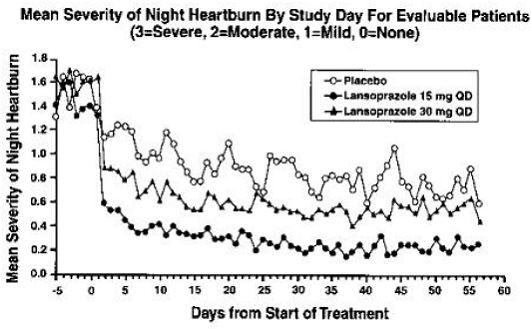
två amerikanska, multicenter dubbelblinda, ranitidinkontrollerade studier av totalt 925 patienter med frekventa GERD-symtom, men inga esofageala erosioner genom endoskopi, var lansoprazol 15 mg överlägset ranitidin 150 mg (två gånger dagligen) när det gäller att minska frekvensen och svårighetsgraden av dagen. och nattlig halsbränna i samband med GERD under behandlingsperioden på åtta veckor. Ingen signifikant ytterligare fördel med lansoprazol 30 mg en gång dagligen observerades [se INDIKATIONER OCH ANVÄNDNING ].
Erosiv esofagit
I en amerikansk, multicenter, dubbelblind, placebokontrollerad studie av 269 patienter som kommer in med en endoskopisk diagnos av esofagit med slemhinnegradering av två eller fler och grad tre och fyra som betecknar erosiv sjukdom, presenteras procentandelen patienter med läkning i tabell 18:
denna studie rapporterade alla PREVACID-grupper signifikant större lindring av halsbränna och mindre buksmärtor dag och natt tillsammans med färre dagar av antacida användning och färre antacida tabletter per dag än placebogruppen. Även om alla doser var effektiva, föreslår den tidigare läkningen i de två högre doserna 30 mg dagligen som rekommenderad dos.
PREVACID jämfördes också i en amerikansk, multicenter, dubbelblind studie med en låg dos ranitidin hos 242 patienter med erosiv refluxesofagit. PREVACID vid en dos på 30 mg var signifikant effektivare än ranitidin 150 mg två gånger dagligen som visas nedan (tabell 19).
Dessutom rapporterade patienter som behandlats med PREVACID 30 mg mindre halsbränna dag och natt och tog mindre antacida tabletter under färre dagar än patienter som tog ranitidin 150 mg två gånger dagligen.
Även om denna studie visar effektiviteten av PREVACID 15 mg för att läka erosiv esofagit, representerar den inte en adekvat jämförelse med ranitidin eftersom den rekommenderade ranitidindosen för esofagit är 150 mg fyra gånger dagligen, två gånger den dos som användes i denna studie.
I de två beskrivna prövningarna och i flera mindre studier som involverade patienter med måttlig till svår erosiv esofagit, gav PREVACID läkningshastigheter liknande de som visas ovan.
en amerikansk, multicenter, dubbelblind, aktivt kontrollerad studie jämfördes 30 mg PREVACID 30 mg med ranitidin 150 mg två gånger dagligen hos 151 patienter med erosiv refluxesofagit som svarade dåligt på minst 12 veckors behandling med minst 12 veckors behandling. en H2-receptorantagonist ges i den dos som anges för symtomlindring eller mer, nämligen cimetidin 800 mg/dag, ranitidin 300 mg/dag, famotidin 40 mg/dag eller nizatidin 300 mg/dag. PREVACID 30 mg var effektivare än ranitidin 150 mg två gånger dagligen för att läka refluxesofagit, och andelen patienter med läkning var följande. Denna studie utgör inte en jämförelse av effektiviteten av histamin H2-receptorantagonister med PREVACID 30 mg, eftersom alla patienter hade visat att de inte svarade på histamin H2-receptorantagonisternas behandlingssätt. Det tyder dock på att PREVACID 30 mg kan vara användbart för patienter som misslyckas med en histamin H2-receptorantagonist (tabell 20) [se INDIKATIONER OCH ANVÄNDNING ].
Underhåll av läkning av erosiv esofagit
Två oberoende, dubbelblinda, multicenter, kontrollerade studier utfördes på patienter med endoskopiskt bekräftad läkt esofagit. Patienterna förblev i remission signifikant längre och antalet återfall av erosiv esofagit var signifikant färre hos patienter som behandlades med PREVACID 30 mg än hos patienter som behandlades med placebo under en 12-månadersperiod (tabell 21).
Oavsett initial grad av erosiv esofagit var PREVACID 15 och 30 mg likartade när det gäller att upprätthålla remission.
en amerikansk, randomiserad, dubbelblind studie jämfördes PREVACID 15 mg dagligen (n=100) med ranitidin 150 mg två gånger dagligen (n=106), i den rekommenderade dosen, hos patienter med endoskopiskt bevisad läkt erosiv esofagit under en 12 månaders period. Behandling med PREVACID 15 mg resulterade i att patienter förblev läkta (grad 0 lesioner) av erosiv esofagit under signifikant längre tidsperioder än de som behandlades med ranitidin (p INDIKATIONER OCH ANVÄNDNING ].
Patologiska hypersekretoriska tillstånd inklusive Zollinger-Ellisons syndrom
öppna studier av 57 patienter med patologiska hypersekretoriska tillstånd, såsom Zollinger-Ellisons syndrom (ZES) med eller utan multipla endokrina adenom, hämmade PREVACID 15 mg signifikant magsyrasekretionen och kontrollerade associerade symtom på diarré, anorexi och smärta. Doser från 15 mg varannan dag till 180 mg per dag bibehöll basalsyrasekretionen under 10 mEq/timme hos patienter utan föregående gastrisk operation och under 5 mEq/timme hos patienter med tidigare gastrisk operation.
Initiala doser titrerades till individuella patientbehov och justeringar var nödvändiga med tiden hos vissa patienter [se DOSERING OCH ADMINISTRERING ]. PREVACID tolererades väl vid dessa höga dosnivåer under långa perioder (mer än fyra år hos vissa patienter). Hos de flesta ZES-patienter modifierades inte serumgastrinnivåerna av PREVACID. Hos vissa patienter ökade dock serumgastrin till nivåer högre än de som fanns före start av lansoprazolbehandling [se INDIKATIONER OCH ANVÄNDNING ].
PATIENTINFORMATION
FÖREGÅENDE (prev-a-sid) (lansoprazol) kapslar med fördröjd frisättning, för oral användning och
FÖREGÅENDE SoluTab (prev-a-sid sol-u-tab) (lansoprazol) oralt sönderfallande tabletter med fördröjd frisättning
Vilken är den viktigaste informationen jag borde veta om PREVACID och PREVACID 15mg SoluTab?
Du ska ta PREVACID och PREVACID 15 mg SoluTab precis som ordinerats, i lägsta möjliga dos och under den kortaste tid som behövs.
PREVACID och PREVACID SoluTab kan hjälpa dina syrarelaterade symtom, men du kan fortfarande ha allvarliga magproblem.
Prata med din läkare. PREVACID 30mg och PREVACID 30mg SoluTab kan orsaka allvarliga biverkningar, inklusive:
- En typ av njurproblem (akut tubulointerstitiell nefrit). Vissa personer som tar protonpumpshämmare (PPI), inklusive PREVACID 30mg och PREVACID 15mg SoluTab, kan utveckla ett njurproblem som kallas akut tubulointerstitiell nefrit som kan inträffa när som helst under behandling med PPI-läkemedel inklusive PREVACID och PREVACID SoluTab. Ring din läkare omedelbart om du har en minskning av mängden du kissar eller om du har blod i urinen.
- Diarré orsakad av en infektion (Clostridium difficile) i dina tarmar. Ring din läkare omedelbart om du har vattnig avföring eller magsmärtor som inte försvinner. Du kanske har feber eller inte.
- Benfrakturer (höft, handled eller ryggrad). Benfrakturer i höften, handleden eller ryggraden kan inträffa hos personer som tar flera dagliga doser av PPI-läkemedel och under en lång tidsperiod (ett år eller längre). Tala om för din läkare om du har en benfraktur, särskilt i höften, handleden eller ryggraden.
- Vissa typer av lupus erythematosus. Lupus erythematosus är en autoimmun sjukdom (kroppens immunceller attackerar andra celler eller organ i kroppen). Vissa personer som tar PPI-läkemedel, inklusive PREVACID 15mg och PREVACID 30mg SoluTab, kan utveckla vissa typer av lupus erythematosus eller få en försämring av den lupus de redan har. Ring din läkare omedelbart om du har ny eller förvärrad ledvärk eller utslag på kinderna eller armarna som blir värre i solen.
Tala med din läkare om din risk för dessa allvarliga biverkningar.
PREVACID 15mg och PREVACID SoluTab kan ha andra allvarliga biverkningar. Ser "Vilka är de möjliga biverkningarna av PREVACID och PREVACID SoluTab?".
Vad är PREVACID och PREVACID 30mg SoluTab?
Ett receptbelagt läkemedel som kallas protonpumpshämmare (PPI) som används för att minska mängden syra i magen.
Hos vuxna, PREVACID 15mg och PREVACID SoluTab används för:
- 4 veckor för läkning och symtomlindring av duodenalsår.
- 10 till 14 dagar med vissa antibiotika för att behandla en infektion orsakad av bakterier som kallas H. pylori.
- bibehålla läkning av duodenalsår. PREVACID 30mg har inte studerats längre än 12 månader för detta ändamål.
- upp till 8 veckor för läkning och symtomlindring av magsår.
- upp till 8 veckor för läkning av magsår hos personer som tar smärtstillande läkemedel som kallas icke-steroida antiinflammatoriska läkemedel (NSAID). PREVACID 30 mg har inte studerats längre än 8 veckor för detta ändamål.
- minska risken för magsår hos personer som löper risk att utveckla magsår med NSAID. PREVACID har inte studerats längre än 12 veckor för detta ändamål.
- upp till 8 veckor för att behandla halsbränna och andra symtom som uppstår vid gastroesofageal refluxsjukdom (GERD). GERD inträffar när syra i magen backar upp i röret (esofagus) som förbinder munnen med magen. Detta kan orsaka en brännande känsla i bröstet eller halsen, sur smak eller rapningar.
- upp till 8 veckor för läkning och symtomlindring av syrarelaterade skador på slemhinnan i matstrupen (kallad erosiv esofagit eller EE). Din läkare kan ordinera ytterligare 8 till 16 veckor med PREVACID eller PREVACID 15 mg SoluTab för patienter vars EE inte förbättras eller vars symtom återkommer.
- upprätthålla läkning av EE. PREVACID har inte studerats längre än 12 månader för detta ändamål.
- långtidsbehandling av tillstånd där din mage gör för mycket syra. Detta inkluderar ett sällsynt tillstånd som kallas Zollinger-Ellisons syndrom.
Barn: Ge PREVACID 30mg och PREVACID 30mg SoluTab precis som ordinerats av ditt barns läkare. Öka inte dosen av PREVACID och PREVACID SoluTab eller ge ditt barn PREVACID 15 mg och PREVACID 15 mg SoluTab längre än den tid som din läkare har ordinerat.
Hos barn 1 till 11 år, PREVACID 15mg och PREVACID 15mg SoluTab används för:
- upp till 12 veckor för att behandla halsbränna och andra symtom som kan hända med GERD.
- upp till 12 veckor för läkning och symtomlindring av EE.
Hos barn 12 till 17 år, PREVACID och PREVACID SoluTab används för:
- upp till 8 veckor för att behandla halsbränna och andra symtom som kan hända med GERD.
- upp till 8 veckor för läkning och symtomlindring av EE.
PREVACID 30mg och PREVACID SoluTab rekommenderas inte för behandling av symtom på GERD hos barn under 1 år och kan skada dem.
Ta inte PREVACID eller PREVACID 15mg SoluTab om du är:
- allergisk mot lansoprazol, något annat PPI-läkemedel eller något av innehållsämnena i PREVACID 15mg eller PREVACID 30mg SoluTab. Se slutet av denna medicinguide för en komplett lista över ingredienser i PREVACID och PREVACID 30mg SoluTab.
- tar ett läkemedel som innehåller rilpivirin (EDURANT, COMPLERA, ODEFSEY, JULUCA) som används för att behandla HIV-1 (humant immunbristvirus).
Innan du tar PREVACID 15mg eller PREVACID SoluTab, berätta för din läkare om alla dina medicinska tillstånd, inklusive om du:
- har låga nivåer av magnesium, kalcium, kalium eller natrium i blodet eller du tar ett diuretikum.
- har leverproblem.
- har fenylketonuri. PREVACID SoluTab innehåller aspartam.
- är gravid, tror att du kan vara gravid eller planerar att bli gravid. PREVACID eller PREVACID SoluTab kan skada ditt ofödda barn. Tala med din läkare om de möjliga riskerna för ett ofött barn om PREVACID 30 mg eller PREVACID 15 mg SoluTab tas under graviditet.
- ammar eller planerar att amma. Det är inte känt om PREVACID eller PREVACID 30 mg SoluTab går över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar PREVACID eller PREVACID SoluTab.
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Tala särskilt om för din läkare om du tar metotrexat (OTREXUP, RASUVO, TREXALL, REDITREX, XATMEP).
Hur ska jag ta PREVACID 15mg och PREVACID 30mg SoluTab?
- Ta PREVACID 30mg eller PREVACID SoluTab precis som din läkare har ordinerat.
- Ändra inte din dos eller sluta ta PREVACID 30mg eller PREVACID SoluTab utan att tala med din läkare.
- Ta PREVACID 30mg eller PREVACID 15mg SoluTab före måltid.
PREVACID 15 mg kapslar:
-
- Svälj PREVACID 30 mg kapslar hela.
- Krossa eller tugga inte PREVACID kapslar.
- Om du har problem med att svälja en hel kapsel kan du öppna kapseln och ta innehållet med vissa livsmedel eller juicer. Se "Användningsinstruktioner" i slutet av denna medicineringsguide för instruktioner om hur du tar PREVACID 30 mg kapslar med vissa livsmedel eller juicer.
- Se "Användningsinstruktioner" i slutet av denna medicineringsguide för instruktioner om hur man blandar och ger PREVACID 30 mg kapslar genom en nasogastrisk sond (NG-slang).
PREVACID SoluTab:
-
- PREVACID 30mg SoluTab är en tablett som smälter i munnen med eller utan vatten.
- Ta inte sönder, skär, krossa eller tugga tabletterna.
- Se "Användningsinstruktioner" i slutet av denna medicineringsguide för instruktioner om hur man blandar och ger PREVACID SoluTab genom en spruta och NG-slang.
- Om du missar en dos av PREVACID eller PREVACID 30 mg SoluTab, ta den så snart du kommer ihåg. Om det nästan är dags för din nästa dos, ta inte den missade dosen. Ta din nästa dos vid din vanliga tidpunkt. Ta inte 2 doser samtidigt.
- Om du tar för mycket PREVACID eller PREVACID 30mg SoluTab, ring din läkare eller din giftkontrollcentral på 1-800-222-1222 omedelbart eller gå till närmaste akutmottagning.
Vilka är de möjliga biverkningarna av PREVACID och PREVACID SoluTab?
PREVACID och PREVACID SoluTab kan orsaka allvarliga biverkningar, inklusive:
- Ser "Vilken är den viktigaste informationen jag borde veta om PREVACID 30mg och PREVACID SoluTab?".
- Låga vitamin B12 nivåer kroppen kan inträffa hos personer som har tagit PREVACID 30mg eller PREVACID SoluTab under lång tid (mer än 3 år). Berätta för din läkare om du har symtom på låga vitamin B12-nivåer, inklusive andnöd, yrsel, oregelbunden hjärtrytm, muskelsvaghet, blek hud, trötthetskänsla, humörförändringar och stickningar eller domningar i armar och ben.
- Magutväxter (fundiska körtelpolyper). Personer som tar PPI-läkemedel under lång tid har en ökad risk att utveckla en viss typ av magtillväxt som kallas fundic gland polyper, särskilt efter att ha tagit PPI-läkemedel i mer än 1 år.
- Låga magnesiumnivåer i kroppen kan inträffa hos personer som har tagit PREVACID i minst 3 månader. Berätta omedelbart för din läkare om du har symtom på låga magnesiumnivåer, inklusive kramper, yrsel, oregelbunden hjärtrytm, darrning, muskelvärk eller svaghet och spasmer i händer, fötter eller röst.
- Allvarliga hudreaktioner. PREVACID 15mg kan orsaka sällsynta men allvarliga hudreaktioner som kan påverka vilken del av din kropp som helst. Dessa allvarliga hudreaktioner kan behöva behandlas på sjukhus och kan vara livshotande:
- Hudutslag som kan ha blåsor, fjällning eller blödning på någon del av huden (inklusive dina läppar, ögon, mun, näsa, könsorgan, händer eller fötter).
- Du kan också ha feber, frossa, värk i kroppen, andnöd eller förstorade lymfkörtlar.
Sluta ta PREVACID och kontakta din läkare omedelbart. Dessa symtom kan vara det första tecknet på en allvarlig hudreaktion.
De vanligaste biverkningarna av PREVACID och PREVACID SoluTab inkluderar: diarré, smärta i magområdet (buk), illamående och förstoppning.
Dessa är inte alla möjliga biverkningar av PREVACID 30mg och PREVACID 30mg SoluTab.
Ring din läkare för medicinsk rådgivning om biverkningar.
Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara PREVACID och PREVACID 30mg SoluTab?
Förvara PREVACID i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
Förvara PREVACID 15mg och PREVACID SoluTab och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av PREVACID 15mg och PREVACID SoluTab.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte PREVACID eller PREVACID 30mg SoluTab för tillstånd som det inte har ordinerats för. Ge inte PREVACID 30mg eller PREVACID SoluTab till andra personer, även om de har samma symtom som du har. Det kan skada dem. Du kan fråga din läkare eller apotekspersonal om information om PREVACID 30mg och PREVACID 15mg SoluTab som är skriven för vårdpersonal.
Vilka är ingredienserna i PREVACID och PREVACID SoluTab?
Aktiv beståndsdel: lansoprazol.
Inaktiva ingredienser i PREVACID 30mg kapslar: sockersfär, sackaros, metakrylsyrasampolymer, lågsubstituerad hydroxipropylcellulosa, stärkelse, magnesiumkarbonat, talk, polyetylenglykol, titandioxid, polysorbat 80, hydroxipropylcellulosa, kolloidal kiseldioxid, D&C Red No. 28, FD&C Blue No. 1, och FD&C Röd nr 40.
Endast PREVACID 15 mg kapsel: FD&C Grön nr 3.
Inaktiva ingredienser i PREVACID 15mg SoluTab: mannitol, metakrylsyra, hydroxipropylcellulosa, laktosmonohydrat-mikrokristallin cellulosasfär, trietylcitrat, krospovidon, polyakrylat, magnesiumkarbonat, aspartam, glycerylmonostearat, hypromellos, magnesiumstearat, citronsyra, titandioxid, konstgjord smakämne, polyglycen, talk. polysorbat 80 och järnoxid.
PREVACID SoluTab innehåller 2,5 mg fenylalanin i varje 15 mg tablett och 5,1 mg fenylalanin i varje 30 mg tablett.
ANVÄNDNINGSINSTRUKTIONER
FÖREGÅENDE (prev-a-sid) (lansoprazol) kapslar med fördröjd frisättning, för oral användning och
FÖREGÅENDE SoluTab (prev-a-sid sol-u-tab) (lansoprazol) oralt sönderfallande tabletter med fördröjd frisättning
Viktig:
- Ta PREVACID 15mg eller PREVACID 15mg SoluTab före måltid.
- Krossa eller tugga inte PREVACID 15mg kapslar eller PREVACID 30mg SoluTab.
- PREVACID eller PREVACID 15mg SoluTab ska endast användas med de livsmedel och juicer som anges nedan.
PREVACID kapslar med fördröjd frisättning (PREVACID 30mg kapslar)
Att ta PREVACID 15 mg kapslar med vissa livsmedel:
Du kan bara använda äppelmos, ENSURE pudding, keso, yoghurt eller silade päron.
Att ta PREVACID kapslar med vissa juicer:
Du kan bara använda äppeljuice, apelsinjuice eller tomatjuice.
Att ge PREVACID kapslar genom en nasogastrisk sond (NG-slang) storlek 16 French eller större:
Du kan bara använda äppeljuice.
PREVACID 15mg SoluTab oralt sönderfallande tabletter med fördröjd frisättning (PREVACID SoluTab)
För patienter som har problem med att svälja tabletter kan PREVACID SoluTab ges enligt följande:
Att ge PREVACID SoluTab med vatten med en oral spruta:
Att ge PREVACID 15 mg SoluTab med vatten genom en nasogastrisk sond (NG-slang) storlek 8 French eller större:
Hur ska jag förvara PREVACID och PREVACID 30mg SoluTab?
- Förvara PREVACID kapslar och PREVACID 15mg SoluTab i rumstemperatur mellan 20°C till 25°C (68°F till 77°F).
Förvara PREVACID och PREVACID 30mg SoluTab och alla läkemedel utom räckhåll för barn.
Denna bruksanvisning har godkänts av US Food and Drug Administration.
