Aciphex 10mg, 20mg Rabeprazole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Aciphex 10mg och hur används det?
Aciphex 10mg är ett receptbelagt läkemedel som används för att behandla symtomen på gastroesofageal refluxsjukdom (GERD), Helicobacter Pylori och tarmsår. Aciphex 10mg kan användas ensamt eller tillsammans med andra läkemedel.
Aciphex är en protonpumpshämmare.
Det är inte känt om Aciphex 20mg tablett med fördröjd frisättning är säker och effektiv för barn yngre än 12 år. Det är inte känt om Aciphex 10 mg tablett med fördröjd frisättning (strössel) är säker och effektiv hos barn yngre än 1 år.
Vilka är de möjliga biverkningarna av Aciphex 10mg?
Aciphex kan orsaka allvarliga biverkningar inklusive:
- svåra magsmärtor,
- blodig diarré,
- plötslig smärta eller svårighet att röra höft, handled eller rygg,
- anfall (kramper),
- urinerar mindre än vanligt,
- blod i urinen,
- svullnad,
- snabb viktökning,
- ledvärk,
- hudutslag på kinderna eller armarna som förvärras av solljus,
- yrsel,
- snabb eller oregelbunden hjärtfrekvens,
- skakande eller ryckande muskelrörelser (skakningar),
- känner sig orolig,
- muskelkramper eller spasmer i händer eller fötter,
- hosta,
- svårigheter att svälja eller kvävning,
- huvudvärk,
- svaghet,
- blåmärken,
- ovanlig blödning (näsblod, tandkött),
- röd eller rosa urin,
- kraftigt menstruationsflöde,
- blodig eller tjäraktig avföring,
- hosta upp blod eller kräks som ser ut som kaffesump,
- blödning som är svår att kontrollera,
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Aciphex inkluderar:
- huvudvärk,
- illamående,
- kräkningar,
- diarre,
- förstoppning,
- magont,
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Aciphex. För mer information, fråga din läkare eller apotekspersonal.
BESKRIVNING
Den aktiva ingrediensen i ACIPHEX 20 mg tabletter med fördröjd frisättning är rabeprazolnatrium, som är en protonpumpshämmare. Det är en substituerad bensimidazol kemiskt känd som 2-[[[4-(3metoxipropoxi)-3-metyl-2-pyridinyl]-metyl]sulfinyl]-1H-bensimidazolnatriumsalt. Den har en empirisk formel av C18H20N3NaO3S och en molekylvikt på 381,42. Rabeprazolnatrium är ett vitt till svagt gulvitt fast ämne. Det är mycket lösligt i vatten och metanol, fritt lösligt i etanol, kloroform och etylacetat och olösligt i eter och n-hexan. Stabiliteten av rabeprazolnatrium är en funktion av pH; det bryts snabbt ned i sura medier och är mer stabilt under alkaliska förhållanden. Den strukturella figuren är:
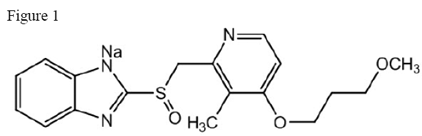
ACIPHEX finns tillgängligt för oral administrering som enterodragerade tabletter med fördröjd frisättning innehållande 20 mg rabeprazolnatrium.
Inaktiva ingredienser i 20 mg tabletten är karnaubavax, krospovidon, diacetylerade monoglycerider, etylcellulosa, hydroxipropylcellulosa, hypromellosftalat, magnesiumstearat, mannitol, propylenglykol, natriumhydroxid, natriumstearylfumarat, talk och titandioxid. Järnoxidgul är färgämnet för tablettöverdraget. Rött järnoxid är bläckpigmentet.
INDIKATIONER
Läkning av erosiv eller ulcerös GERD hos vuxna
ACIPHEX 20 mg tabletter med fördröjd frisättning är indicerade för korttidsbehandling (4 till 8 veckor) för läkning och symtomatisk lindring av erosiv eller ulcerös gastroesofageal refluxsjukdom (GERD). För de patienter som inte har läkt efter 8 veckors behandling kan ytterligare 8 veckors behandling med ACIPHEX övervägas.
Underhåll av läkning av erosiv eller ulcerös GERD hos vuxna
ACIPHEX tabletter med fördröjd frisättning är indicerade för att bibehålla läkning och minskning av återfallsfrekvensen av halsbränna hos patienter med erosiv eller ulcerös gastroesofageal refluxsjukdom (GERD Maintenance). Kontrollerade studier sträcker sig inte längre än 12 månader.
Behandling av symtomatisk GERD hos vuxna
ACIPHEX 20 mg tabletter med fördröjd frisättning är indicerade för behandling av halsbränna dag och natt och andra symtom associerade med GERD hos vuxna i upp till 4 veckor.
Läkning Av Duodenalsår Hos Vuxna
ACIPHEX 20 mg tabletter med fördröjd frisättning är indicerade för korttidsbehandling (upp till fyra veckor) för läkning och symtomatisk lindring av duodenalsår. De flesta patienter läker inom fyra veckor.
Helicobacter Pylori utrotning för att minska risken för återfall av duodenalsår hos vuxna
ACIPHEX 10 mg tabletter med fördröjd frisättning, i kombination med amoxicillin och klaritromycin som en treläkemedelsbehandling, är indicerade för behandling av patienter med H. pylori-infektion och duodenalsårsjukdom (aktiv eller tidigare under de senaste 5 åren) för att utrota H. pylori . Utrotning av H. pylori har visat sig minska risken för återfall av duodenalsår.
Hos patienter som misslyckas med behandlingen bör känslighetstest göras. Om resistens mot klaritromycin påvisas eller känslighetstestning inte är möjlig, bör alternativ antimikrobiell behandling sättas in [se KLINISK FARMAKOLOGI och den fullständiga förskrivningsinformationen för klaritromycin].
Behandling av patologiska hypersekretoriska tillstånd, inklusive Zollinger-Ellisons syndrom hos vuxna
ACIPHEX tabletter med fördröjd frisättning är indicerade för långtidsbehandling av patologiska hypersekretoriska tillstånd, inklusive Zollinger-Ellisons syndrom.
Behandling av symtomatisk GERD hos ungdomar 12 år och äldre
ACIPHEX 20 mg tabletter med fördröjd frisättning är indicerade för behandling av symtomatisk GERD hos ungdomar från 12 år och uppåt i upp till 8 veckor.
DOSERING OCH ADMINISTRERING
Tabell 1 visar den rekommenderade dosen av ACIPHEX tabletter med fördröjd frisättning till vuxna och ungdomar 12 år och äldre. Användning av ACIPHEX tabletter med fördröjd frisättning rekommenderas inte för användning till pediatriska patienter från 1 år till yngre än 12 år eftersom den lägsta tillgängliga tablettstyrkan (20 mg) överstiger den rekommenderade dosen för dessa patienter. Använd en annan rabeprazolformulering för pediatriska patienter 1 år till yngre än 12 år.
Administrationsinstruktioner
- Svälj ACIPHEX 20 mg tabletter med fördröjd frisättning hela. Tugga, krossa eller dela inte tabletter.
- För behandling av duodenalsår, ta ACIPHEX tabletter med fördröjd frisättning efter en måltid.
- För utrotning av Helicobacter pylori, ta ACIPHEX 20 mg tabletter med fördröjd frisättning tillsammans med mat.
- För alla andra indikationer kan ACIPHEX tabletter med fördröjd frisättning tas med eller utan mat.
- Ta en missad dos så snart som möjligt. Om det nästan är dags för nästa dos, hoppa över den missade dosen och gå tillbaka till det normala schemat. Ta inte två doser samtidigt.
HUR LEVERERAS
Doseringsformer och styrkor
ACIPHEX 10 mg tabletter med fördröjd frisättning tillhandahålls i en styrka, 20 mg. Tabletterna är runda, ljusgula, enterodragerade, bikonvexa tabletter. ”ACIPHEX 20” är märkt i rött på ena sidan av tabletten.
Förvaring Och Hantering
ACIPHEX 20 mg levereras som ljusgula enterotabletter med fördröjd frisättning. Namnet och styrkan, i mg, (ACIPHEX 20) är märkta på ena sidan.
Flaskor med 30 st ( NDC 69784-243-30)
Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur ]. Skydda mot fukt.
Distribueras av Eisai Inc., Woodcliff Lake, NJ 07677. Reviderad: Mar 2022
BIEFFEKTER
Följande allvarliga biverkningar beskrivs nedan och på andra ställen i märkningen:
- Akut Tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Clostridium difficile-associerad diarré [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Allvarliga kutana biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kutan och systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Cyanokobalamin (Vitamin B-12) Brist [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypomagnesemi och mineralmetabolism [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Fundiska körtelpolyper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska studier
Eftersom kliniska prövningar utförs under varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Vuxna
Data som beskrivs nedan återspeglar exponering för ACIPHEX tabletter med fördröjd frisättning hos 1064 vuxna patienter exponerade i upp till 8 veckor. Studierna var främst placebo- och aktivkontrollerade studier på vuxna patienter med erosiv eller ulcerös gastroesofageal refluxsjukdom (GERD), duodenalsår och magsår. Befolkningen hade en medelålder på 53 år (intervall 18-89 år) och hade en andel på cirka 60 % män: 40 % kvinnor. Rasfördelningen var 86 % kaukasiska, 8 % afroamerikaner, 2 % asiatiska och 5 % övriga. De flesta patienter fick antingen 10 mg, 20 mg eller 40 mg per dag av ACIPHEX 20 mg tabletter med fördröjd frisättning.
En analys av biverkningar som förekom hos ≥2 % av patienterna som behandlades med ACIPHEX 10 mg tabletter med fördröjd frisättning (n=1064) och med en högre frekvens än placebo (n=89) i kontrollerade nordamerikanska och europeiska akuta behandlingsstudier, visade följande biverkningar: smärta (3 % vs. 1 %), faryngit (3 % vs. 2 %), flatulens (3 % vs. 1 %), infektion (2 % vs. 1 %) och förstoppning (2 % vs. 1 %).
Tre långsiktiga underhållsstudier bestod av totalt 740 vuxna patienter; minst 54 % av de vuxna patienterna exponerades för ACIPHEX 20 mg tabletter med fördröjd frisättning i 6 månader och minst 33 % exponerades i 12 månader. Av de 740 vuxna patienterna fick 247 (33 %) och 241 (33 %) patienter 10 mg respektive 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning, medan 169 (23 %) patienter fick placebo och 83 (11 %) omeprazol.
Säkerhetsprofilen för rabeprazol i underhållsstudierna på vuxna överensstämde med vad som observerades i de akuta studierna.
Mindre vanliga biverkningar som setts i kontrollerade kliniska prövningar (
Kombinationsbehandling med amoxicillin och klaritromycin
I kliniska prövningar med kombinationsbehandling med rabeprazol plus amoxicillin och klaritromycin (RAC) observerades inga biverkningar unika för denna läkemedelskombination. I den amerikanska multicenterstudien var de vanligast rapporterade läkemedelsrelaterade biverkningarna för patienter som fick RAC-behandling i 7 eller 10 dagar diarré (8 % och 7 %) och smakförvrängning (6 % respektive 10 %).
Inga kliniskt signifikanta laboratorieavvikelser som är specifika för läkemedelskombinationerna observerades.
För mer information om biverkningar eller laboratorieförändringar med amoxicillin eller klaritromycin, se deras respektive förskrivningsinformation, avsnittet Biverkningar.
Pediatrik
en multicenter, öppen studie av ungdomar i åldern 12 till 16 år med en klinisk diagnos av symptomatisk GERD eller endoskopiskt bevisad GERD, var biverkningsprofilen liknande den hos vuxna. De biverkningar som rapporterades utan hänsyn till samband med ACIPHEX 20 mg tabletter med fördröjd frisättning som inträffade hos ≥2 % av 111 patienter var huvudvärk (9,9 %), diarré (4,5 %), illamående (4,5 %), kräkningar (3,6 %) och buksmärtor (3,6%). De relaterade rapporterade biverkningarna som inträffade hos ≥2 % av patienterna var huvudvärk (5,4 %) och illamående (1,8 %). Det har inte rapporterats några biverkningar i denna studie som inte tidigare observerats hos vuxna.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats under användning av rabeprazol efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering:
Blod- och lymfsystemet: agranulocytos, hemolytisk anemi, leukopeni, pancytopeni, trombocytopeni
Öron- och labyrintsjukdomar: vertigo
Ögonstörningar: suddig syn
Gastrointestinala störningar: fundiska körtelpolyper
Allmänna störningar och villkor för administrationsplatsen: plötslig död
Lever och gallvägar: gulsot
Immunsystemets störningar: anafylaxi, angioödem, systemisk lupus erythematosus, Stevens-Johnsons syndrom, toxisk epidermal nekrolys (vissa dödlig), DRESS, AGEP
Infektioner och angrepp: Clostridium difficile-associerad diarré
Undersökningar: Ökning av protrombintid/INR (hos patienter som behandlas med samtidig warfarin), TSH-höjningar
Metabolism och näringsstörningar: hyperammonemi, hypomagnesemi, hypokalcemi, hypokalemi [Varningar och försiktighetsåtgärder 5.8], hyponatremi
Muskuloskeletala systemet: benfraktur, rabdomyolys
Störningar i nervsystemet: koma
Psykiatriska störningar: delirium, desorientering
Njur- och urinvägsstörningar: interstitiell nefrit
Andningsvägar, bröstkorg och mediastinum: interstitiell lunginflammation
Hud och subkutan vävnad: allvarliga dermatologiska reaktioner inklusive bullösa och andra läkemedelsutbrott i huden, kutan lupus erythematosus, erythema multiforme
LÄKEMEDELSINTERAKTIONER
Tabell 2 inkluderar läkemedel med kliniskt viktiga läkemedelsinteraktioner och interaktion med diagnostik när de administreras samtidigt med ACIPHEX 10 mg tabletter med fördröjd frisättning och instruktioner för att förebygga eller hantera dem.
Se märkningen av samtidigt använda läkemedel för att få ytterligare information om interaktioner med PPI.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Förekomst av magmalignitet
Hos vuxna utesluter inte symtomatisk respons på behandling med ACIPHEX 10 mg förekomst av gastrisk malignitet. Överväg ytterligare uppföljning och diagnostiska tester hos vuxna patienter som har ett suboptimalt svar eller ett tidigt symtomatiskt återfall efter avslutad behandling med PPI.
Interaktion med Warfarin
Steady state-interaktioner mellan rabeprazol och warfarin har inte utvärderats tillräckligt hos patienter. Det har rapporterats om ökad INR och protrombintid hos patienter som fått en protonpumpshämmare och warfarin samtidigt. Ökning av INR och protrombintid kan leda till onormal blödning och till och med död. Patienter som behandlas med ACIPHEX 10 mg tabletter med fördröjd frisättning och warfarin samtidigt kan behöva övervakas för ökad INR och protrombintid [se LÄKEMEDELSINTERAKTIONER ].
Akut Tubulointerstitiell nefrit
Akut tubulointerstitiell nefrit (TIN) har observerats hos patienter som tar PPI och kan uppträda när som helst under PPI-behandling. Patienter kan uppvisa olika tecken och symtom från symtomatiska överkänslighetsreaktioner till ospecifika symtom på nedsatt njurfunktion (t.ex. sjukdomskänsla, illamående, anorexi). I rapporterade fallserier diagnostiserades vissa patienter på biopsi och i frånvaro av extrarenala manifestationer (t.ex. feber, hudutslag eller artralgi).
Avbryt ACIPHEX och utvärdera patienter med misstänkt akut TIN [se KONTRAINDIKATION ].
Clostridium Difficile-associerad diarré
Publicerade observationsstudier tyder på att PPI-behandling som ACIPHEX kan vara associerad med en ökad risk för Clostridium difficile-associerad diarré, särskilt hos inlagda patienter. Denna diagnos bör övervägas för diarré som inte förbättras [se NEGATIVA REAKTIONER ].
Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas.
Clostridium difficile-associerad diarré (CDAD) har rapporterats vid användning av nästan alla antibakteriella medel. För mer information specifik för antibakteriella medel (klaritromycin och amoxicillin) indicerade för användning i kombination med ACIPHEX, se avsnitten Varningar och försiktighet i motsvarande förskrivningsinformation.
Benfraktur
Flera publicerade observationsstudier på vuxna tyder på att PPI-behandling kan vara associerad med en ökad risk för osteoporosrelaterade frakturer i höften, handleden eller ryggraden. Risken för frakturer var ökad hos patienter som fick höga doser, definierade som flera dagliga doser, och långvarig PPI-behandling (ett år eller längre). Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas. Patienter med risk för osteoporosrelaterade frakturer bör hanteras enligt fastställda behandlingsriktlinjer [se DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER ].
Allvarliga kutana biverkningar
Allvarliga kutana biverkningar, inklusive Stevens-Johnsons syndrom (SJS) och toxisk epidermal nekrolys (TEN), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) och akut generaliserad exantematös pustulos (AGEP) har rapporterats i samband med användning av PPI. [ser NEGATIVA REAKTIONER ]. Avbryt ACIPHEX vid första tecken eller symtom på allvarliga kutana biverkningar eller andra tecken på överkänslighet och överväg ytterligare utvärdering.
Kutan och systemisk lupus erythematosus
Kutan lupus erythematosus (CLE) och systemisk lupus erythematosus (SLE) har rapporterats hos patienter som tar PPI, inklusive rabeprazol. Dessa händelser har inträffat som både nyuppkomst och förvärring av befintlig autoimmun sjukdom. Majoriteten av PPI-inducerade lupus erythematosus fall var CLE.
Den vanligaste formen av CLE som rapporterats hos patienter som behandlats med PPI var subakut CLE (SCLE) och inträffade inom veckor till år efter kontinuerlig läkemedelsbehandling hos patienter från spädbarn till äldre. I allmänhet observerades histologiska fynd utan organinblandning.
Systemisk lupus erythematosus (SLE) rapporteras mindre vanligt än CLE hos patienter som får PPI. PPI-associerad SLE är vanligtvis mildare än icke-läkemedelsinducerad SLE. Debut av SLE inträffade vanligtvis inom dagar till år efter påbörjad behandling, främst hos patienter från unga vuxna till äldre. Majoriteten av patienterna fick utslag; dock rapporterades också artralgi och cytopeni.
Undvik administrering av PPI under längre tid än vad som är medicinskt indicerat. Om tecken eller symtom som överensstämmer med CLE eller SLE noteras hos patienter som får ACIPHEX, avbryt läkemedlet och hänvisa patienten till lämplig specialist för utvärdering. De flesta patienter förbättras med avbrytande av enbart PPI inom 4 till 12 veckor. Serologiska tester (t.ex. ANA) kan vara positiva och förhöjda serologiska testresultat kan ta längre tid att lösa än kliniska manifestationer.
Cyanokobalamin (Vitamin B-12) Brist
Daglig behandling med syradämpande mediciner under en lång tidsperiod (t.ex. längre än 3 år) kan leda till malabsorption av cyanokobalamin (vitamin B-12) orsakad av hypo- eller aklorhydri. Sällsynta rapporter om cyanokobalaminbrist som inträffat vid syrahämmande behandling har rapporterats i litteraturen. Denna diagnos bör övervägas om kliniska symtom som överensstämmer med cyanokobalaminbrist observeras hos patienter som behandlas med ACIPHEX.
Hypomagnesemi och mineralmetabolism
Hypomagnesemi, symtomatisk och asymtomatisk, har i sällsynta fall rapporterats hos patienter som behandlats med PPI under minst tre månader, i de flesta fall efter ett års behandling. Allvarliga biverkningar inkluderar stelkramp, arytmier och kramper. Hypomagnesemi kan leda till hypokalcemi och/eller hypokalemi och kan förvärra underliggande hypokalcemi hos riskpatienter. Hos de flesta patienter krävde behandling av hypomagnesemi magnesiumersättning och avbrytande av PPI.
För patienter som förväntas vara på långvarig behandling eller som tar PPI tillsammans med mediciner som digoxin eller läkemedel som kan orsaka hypomagnesemi (t.ex. diuretika), kan sjukvårdspersonal överväga att övervaka magnesiumnivåerna innan PPI-behandlingen påbörjas och med jämna mellanrum [se NEGATIVA REAKTIONER ].
Överväg att övervaka magnesium- och kalciumnivåerna innan behandling med ACIPHEX påbörjas och regelbundet under behandling hos patienter med redan existerande risk för hypokalcemi (t.ex. hypoparatyreos). Komplettera med magnesium och/eller kalcium vid behov. Om hypokalcemi är behandlingsrefraktär, överväg att avbryta PPI.
Interaktion med metotrexat
Litteratur tyder på att samtidig användning av PPI med metotrexat (främst i höga doser; se metotrexatförskrivningsinformation) kan höja och förlänga serumkoncentrationerna av metotrexat och/eller dess metabolit, vilket kan leda till metotrexattoxicitet. Vid administrering av högdos metotrexat kan ett tillfälligt utsättande av PPI övervägas hos vissa patienter [se LÄKEMEDELSINTERAKTIONER ].
Fundic körtelpolyper
PPI-användning är förknippad med en ökad risk för fundiska körtelpolyper som ökar vid långvarig användning, särskilt efter ett år. De flesta PPI-användare som utvecklade fundic gland polyper var asymtomatiska och fundic gland polyper identifierades tillfälligt vid endoskopi. Använd den kortaste varaktigheten av PPI-behandlingen som är lämplig för det tillstånd som behandlas.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide ).
Akut Tubulointerstitiell nefrit
Råda patienten eller vårdgivaren att omedelbart ringa patientens vårdgivare om de upplever tecken och/eller symtom associerade med akut tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Clostridium Difficile-associerad diarré
Råda patienten eller vårdgivaren att omedelbart ringa patientens vårdgivare om de upplever diarré som inte förbättras [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Benfraktur
Råda patienten eller vårdgivaren att rapportera eventuella frakturer, särskilt på höften, handleden eller ryggraden, till patientens vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Allvarliga kutana biverkningar
Råda patienten eller vårdgivaren att avbryta behandlingen med ACIPHEX 20 mg och rapportera eventuella tecken och symtom på en allvarlig kutan biverkning eller andra tecken på överkänslighet till vårdgivaren [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kutan och systemisk lupus erythematosus
Rekommendera patienten eller vårdgivaren att omedelbart ringa patientens vårdgivare för alla nya eller försämrade symtom associerade med kutan eller systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Cyanokobalamin (Vitamin B-12) Brist
Rekommendera patienten eller vårdgivaren att rapportera eventuella kliniska symtom som kan vara associerade med cyanokobalaminbrist till patientens vårdgivare om de har fått ACIPHEX 20 mg i mer än 3 år [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hypomagnesemi och mineralmetabolism
Rekommendera patienten eller vårdgivaren att rapportera alla kliniska symtom som kan vara associerade med hypomagnesemi, hypokalcemi, hypokalemi och hyponatremi till patientens vårdgivare, om de har fått ACIPHEX i minst 3 månader [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Läkemedelsinteraktioner
Råda patienter att rapportera till sin vårdgivare om de tar produkter som innehåller rilpivirin [se KONTRAINDIKATIONER ], warfarin, digoxin eller högdos metotrexat [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Administrering
- Svälj ACIPHEX 10 mg tabletter med fördröjd frisättning hela. Tugga, krossa eller dela inte tabletterna.
- För behandling av duodenalsår, ta ACIPHEX tabletter med fördröjd frisättning efter en måltid.
- För utrotning av Helicobacter pylori, ta ACIPHEX 20 mg tabletter med fördröjd frisättning tillsammans med mat.
- För alla andra indikationer kan ACIPHEX 10 mg tabletter med fördröjd frisättning tas med eller utan mat.
- Ta en missad dos så snart som möjligt. Om det nästan är dags för nästa dos, hoppa över den missade dosen och gå tillbaka till det normala schemat. Ta inte två doser samtidigt.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
en 88/104-veckors karcinogenicitetsstudie på CD-1-möss gav rabeprazol i orala doser upp till 100 mg/kg/dag ingen ökad förekomst av tumörer. Den högsta testade dosen gav en systemisk exponering för rabeprazol (AUC) på 1,40 μg•tim/ml, vilket är 1,6 gånger den mänskliga exponeringen (plasma AUC0-∞ = 0,88 μg•h/mL) vid den rekommenderade dosen för GERD (20 mg/ dag). I en 28-veckors karcinogenicitetsstudie på p53+/-transgena möss orsakade rabeprazol vid orala doser på 20, 60 och 200 mg/kg/dag inte en ökning av förekomsten av tumörer, men gav magslemhinnan hyperplasi vid alla doser. Den systemiska exponeringen för rabeprazol vid 200 mg/kg/dag är cirka 17 till 24 gånger den mänskliga exponeringen vid den rekommenderade dosen för GERD. I en 104-veckors karcinogenicitetsstudie på Sprague-Dawley-råttor behandlades hanar med orala doser på 5, 15, 30 och 60 mg/kg/dag och honor med 5, 15, 30, 60 och 120 mg/kg/dag . Rabeprazol producerade gastrisk enterokromaffin-liknande (ECL) cellhyperplasi hos han- och honråttor och ECL-cellkarcinoida tumörer hos honråttor vid alla doser inklusive den lägsta testade dosen. Den lägsta dosen (5 mg/kg/dag) gav en systemisk exponering för rabeprazol (AUC) på cirka 0,1 μg•timme/ml vilket är cirka 0,1 gånger den mänskliga exponeringen vid den rekommenderade dosen för GERD. Hos hanråttor observerades inga behandlingsrelaterade tumörer vid doser upp till 60 mg/kg/dag, vilket gav en plasmaexponering för rabeprazol (AUC) på cirka 0,2 μg•timme/ml (0,2 gånger den mänskliga exponeringen vid den rekommenderade dosen för GERD).
Rabeprazol var positivt i Ames-testet, den kinesiska hamsterns äggstockscell (CHO/HGPRT) framåtgående genmutationstest och muslymfomcellen (L5178Y/TK+/–) framåtgenmutationstestet. Dess demetylerade metabolit var också positiv i Ames-testet. Rabeprazol var negativt i in vitro-testet för kromosomavvikelse i kinesisk hamster i lungceller, mikrokärntestet in vivo och in vivo- och ex vivo-testerna för oschemalagd DNA-syntes av hepatocyter från råtta (UDS).
Rabeprazol vid intravenösa doser upp till 30 mg/kg/dag (plasma-AUC på 8,8 μg•timme/ml, cirka 10 gånger den mänskliga exponeringen vid den rekommenderade dosen för GERD) visade sig inte ha någon effekt på fertilitet och reproduktionsförmåga hos män och honråttor.
Användning i specifika populationer
Graviditet
Risksammanfattning
Det finns inga tillgängliga humandata om användning av ACIPHEX 10 mg hos gravida kvinnor för att informera om läkemedelsrelaterade risker. Bakgrundsrisken för stora fosterskador och missfall för de angivna populationerna är okänd. Däremot är bakgrundsrisken i den allmänna befolkningen i USA för allvarliga fosterskador 2 till 4 % och för missfall är 15 till 20 % av kliniskt erkända graviditeter. Inga tecken på negativa utvecklingseffekter sågs i reproduktionsstudier på djur med rabeprazol administrerat under organogenesen vid 13 och 8 gånger den mänskliga arean under plasmakoncentration-tidkurvan (AUC) vid den rekommenderade dosen för GERD, på råttor respektive kaniner [se Data ].
Förändringar i benmorfologi observerades hos avkommor till råttor som behandlats med orala doser av en annan PPI under större delen av graviditeten och amningen. När maternell administrering var begränsad till enbart dräktighet, fanns det inga effekter på benfysisk morfologi hos avkomman vid någon ålder [se Data ].
Data
Djurdata
Embryo-fosterutvecklingsstudier har utförts på råttor under organogenes vid intravenösa doser av rabeprazol upp till 50 mg/kg/dag (plasma-AUC på 11,8 μg•timme/ml, cirka 13 gånger den mänskliga exponeringen vid den rekommenderade orala dosen för GERD) och kaniner vid intravenösa doser upp till 30 mg/kg/dag (plasma-AUC på 7,3 μg•tim/ml, cirka 8 gånger den mänskliga exponeringen vid den rekommenderade orala dosen för GERD) och har inte visat några tecken på fostrets skada p.g.a. rabeprazol.
Administrering av rabeprazol till råttor i sen dräktighet och under laktation i en oral dos på 400 mg/kg/dag (cirka 195 gånger den orala dosen för människor baserat på mg/m²) resulterade i en minskning av kroppsviktsökningen hos valparna.
En pre- och postnatal utvecklingstoxicitetsstudie på råttor med ytterligare endpoints för att utvärdera benutveckling utfördes med en annan PPI vid cirka 3,4 till 57 gånger en oral human dos på basis av kroppsyta. Minskad lårbenslängd, bredd och tjocklek på kortikalt ben, minskad tjocklek på tibial tillväxtplatta och minimal till mild benmärgshypocellularitet noterades vid doser av denna PPI lika med eller större än 3,4 gånger en oral human dos på basis av kroppsyta. . Fysisk dysplasi i lårbenet observerades också hos avkommor efter exponering för PPI in utero och laktation vid doser lika med eller större än 33,6 gånger en oral human dos på basis av kroppsyta. Effekter på moderns ben observerades hos dräktiga och digivande råttor i en pre- och postnatal toxicitetsstudie när PPI administrerades i orala doser på 3,4 till 57 gånger en oral human dos på basis av kroppsyta. När råttor doserades från graviditetsdag 7 till avvänjning på postnatal dag 21, observerades en statistiskt signifikant minskning av moderns lårbensvikt på upp till 14 % (jämfört med placebobehandling) vid doser lika med eller större än 33,6 gånger en oral human dos på basis av kroppsyta.
En uppföljande studie av utvecklingstoxicitet på råttor med ytterligare tidpunkter för att utvärdera utvecklingen av ungben från postnatal dag 2 till vuxen ålder utfördes med en annan PPI vid orala doser på 280 mg/kg/dag (cirka 68 gånger en oral human dos på en kroppsyta) där läkemedelsadministrationen var från antingen graviditetsdag 7 eller graviditetsdag 16 fram till förlossningen. När maternell administrering var begränsad till enbart graviditet, fanns det inga effekter på benfysisk morfologi hos avkomman vid någon ålder.
Laktation
Risksammanfattning
Amningsstudier har inte utförts för att bedöma förekomsten av rabeprazol i modersmjölk, effekterna av rabeprazol på det ammade barnet eller effekterna av rabeprazol på mjölkproduktionen. Rabeprazol finns i råttmjölk. Utvecklingen och hälsofördelarna med amning bör beaktas tillsammans med moderns kliniska behov av ACIPHEX och eventuella negativa effekter på det ammade barnet från ACIPHEX eller från det underliggande moderns tillståndet.
Pediatrisk användning
Säkerheten och effekten av ACIPHEX 20 mg tabletter med fördröjd frisättning har fastställts hos pediatriska patienter för tonårspatienter 12 år och äldre för behandling av symtomatisk GERD. Användning av ACIPHEX 20 mg tabletter med fördröjd frisättning i denna åldersgrupp stöds av adekvata och välkontrollerade studier på vuxna och en multicenter, randomiserad, öppen, parallellgruppsstudie på 111 ungdomar i åldern 12 till 16 år. Patienterna hade en klinisk diagnos av symtomatisk GERD, eller misstänkt eller endoskopiskt bevisad GERD och randomiserades till antingen 10 mg eller 20 mg en gång dagligen i upp till 8 veckor för utvärdering av säkerhet och effekt. Biverkningsprofilen hos ungdomar liknade den hos vuxna. De relaterade rapporterade biverkningarna som inträffade hos ≥2 % av patienterna var huvudvärk (5 %) och illamående (2 %). Det har inte rapporterats några biverkningar i dessa studier som inte tidigare observerats hos vuxna.
Säkerheten och effekten av ACIPHEX 10 mg tabletter med fördröjd frisättning har inte fastställts hos pediatriska patienter för:
- Läkning av erosiv eller ulcerös GERD
- Underhåll av läkning av erosiv eller ulcerös GERD
- Behandling av symtomatisk GERD
- Läkning av duodenalsår
- Utrotning av Helicobacter pylori för att minska risken för återfall av duodenalsår
- Behandling av patologiska hypersekretoriska tillstånd, inklusive Zollinger-Ellisons syndrom
ACIPHEX 20 mg tabletter med fördröjd frisättning rekommenderas inte för användning till pediatriska patienter under 12 år eftersom tablettstyrkan överstiger den rekommenderade dosen för dessa patienter [se DOSERING OCH ADMINISTRERING ]. För pediatriska patienter från 1 år till yngre än 12 år överväg en annan rabeprazolformulering. Säkerheten och effektiviteten för en annan doseringsform och doseringsstyrka av rabeprazol har fastställts hos pediatriska patienter 1 till 11 år för behandling av GERD.
Data från unga djur
Studier på unga och unga vuxna råttor och hundar utfördes. I studier på juvenila djur administrerades rabeprazolnatrium oralt till råttor i upp till 5 veckor och till hundar i upp till 13 veckor, var och en med början på dag 7 efter förlossningen och följt av en 13-veckors återhämtningsperiod. Råttor doserades med 5, 25 eller 150 mg/kg/dag och hundar doserades med 3, 10 eller 30 mg/kg/dag. Data från dessa studier var jämförbara med de som rapporterats för unga vuxna djur. Farmakologiskt medierade förändringar, inklusive ökade serumgastrinnivåer och magförändringar, observerades vid alla dosnivåer hos både råtta och hund. Dessa observationer var reversibla under de 13 veckor långa återhämtningsperioderna. Även om kroppsvikter och/eller längder på krona och bakdel minskade minimalt under dosering, noterades inga effekter på utvecklingsparametrarna hos vare sig unga råttor eller hundar.
När unga djur behandlades i 28 dagar med en annan PPI i doser lika med eller större än 34 gånger den dagliga orala humandosen på basis av kroppsyta, påverkades den totala tillväxten och behandlingsrelaterade minskningar i kroppsvikt (ungefär 14 %) och kroppsviktsökning och minskningar i lårbensvikt och lårbenslängd observerades.
Geriatrisk användning
Av det totala antalet försökspersoner (n=2009) i kliniska studier av ACIPHEX 20 mg tabletter med fördröjd frisättning var 19 % 65 år och äldre, medan 4 % var 75 år och äldre. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre försökspersoner, och annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas.
Nedsatt leverfunktion
Administrering av ACIPHEX tabletter med fördröjd frisättning till patienter med lätt till måttligt nedsatt leverfunktion (Child-Pugh klass A respektive B) resulterade i ökad exponering och minskad eliminering [se KLINISK FARMAKOLOGI ]. Ingen dosjustering är nödvändig hos patienter med lätt till måttligt nedsatt leverfunktion. Det finns ingen information om patienter med gravt nedsatt leverfunktion (Child-Pugh klass C). Undvik användning av ACIPHEX tabletter med fördröjd frisättning till patienter med gravt nedsatt leverfunktion; men om behandling är nödvändig, övervaka patienterna för biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
ÖVERDOS
Sju rapporter om oavsiktlig överdosering med rabeprazol har inkommit. Den maximala rapporterade överdosen var 80 mg. Det fanns inga kliniska tecken eller symtom associerade med någon rapporterad överdos. Patienter med Zollinger-Ellisons syndrom har behandlats med upp till 120 mg rabeprazol en gång dagligen. Ingen specifik antidot för rabeprazol är känd. Rabeprazol är i hög grad proteinbundet och är inte lätt dialyserbart.
händelse av överdosering ska behandlingen vara symptomatisk och stödjande.
Om överexponering inträffar, ring ditt giftkontrollcenter på 1-800-222-1222 för aktuell information om hantering av förgiftning eller överdosering.
KONTRAINDIKATIONER
- ACIPHEX 10 mg är kontraindicerat hos patienter med känd överkänslighet mot rabeprazol, substituerade bensimidazoler eller mot någon komponent i formuleringen. Överkänslighetsreaktioner kan inkludera anafylaxi, anafylaktisk chock, angioödem, bronkospasm, akut tubulointerstitiell nefrit och urtikaria [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
- PPI, inklusive ACIPHEX, är kontraindicerade med produkter som innehåller rilpivirin [se LÄKEMEDELSINTERAKTIONER ].
- För information om kontraindikationer för antibakteriella medel (klaritromycin och amoxicillin) indikerade i kombination med ACIPHEX 20 mg tabletter med fördröjd frisättning, se avsnittet Kontraindikationer i deras bipacksedel.
KLINISK FARMAKOLOGI
Handlingsmekanism
Rabeprazol tillhör en klass av antisekretoriska föreningar (substituerade bensimidazol-protonpumpshämmare) som inte uppvisar antikolinerga eller histamin H2-receptorantagonistegenskaper, men som undertrycker magsyrasekretion genom att hämma magsäckens H+, K+ATPas vid magsäckens sekretoriska yta. parietalcell. Eftersom detta enzym betraktas som syrapumpen (proton) i parietalcellen, har rabeprazol karakteriserats som en gastrisk protonpumpshämmare. Rabeprazol blockerar det sista steget i magsyrautsöndringen.
I gastriska parietalceller protoneras rabeprazol, ackumuleras och omvandlas till en aktiv sulfenamid. Vid studier in vitro aktiveras rabeprazol kemiskt vid pH 1,2 med en halveringstid på 78 sekunder. Det hämmar syratransport i magblåsor hos svin med en halveringstid på 90 sekunder.
Farmakodynamik
Antisekretorisk aktivitet
Den antisekretoriska effekten börjar inom en timme efter oral administrering av 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning. Den medianhämmande effekten av rabeprazol på 24-timmars surhet i magen är 88 % av maximal efter den första dosen. En 20 mg dos av ACIPHEX tabletter med fördröjd frisättning hämmar basal- och peptonmålsstimulerad syrasekretion jämfört med placebo med 86 % respektive 95 %, och ökar procentandelen av en 24-timmarsperiod som magsäckens pH>3 från 10 % till 65 % (se tabell nedan). Denna relativt förlängda farmakodynamiska verkan jämfört med den korta farmakokinetiska halveringstiden (1 till 2 timmar) återspeglar den ihållande inaktiveringen av H+, K+ATPas.
Jämfört med placebo minskade 10 mg, 20 mg och 40 mg ACIPHEX tabletter med fördröjd frisättning, administrerade en gång dagligen i 7 dagar, signifikant intragastrisk surhet med alla doser för vart och ett av fyra måltidsrelaterade intervall och den totala 24-timmarsperioden. I denna studie fanns det inga statistiskt signifikanta skillnader mellan doserna; det fanns dock en signifikant dosrelaterad minskning av surheten i magen. Förmågan hos rabeprazol att orsaka en dosrelaterad minskning av genomsnittlig intragastrisk surhet illustreras nedan.

Efter administrering av 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning en gång dagligen i åtta dagar, var den genomsnittliga procentandelen av tiden som magsäckens pH överstiger 3 eller magsäckens pH högre än 4 efter en engångsdos (dag 1) och flera doser (dag 8) signifikant högre än placebo (se tabell nedan). Minskningen av surheten i magsäcken och ökningen av pH i magen som observerades med 20 mg ACIPHEX 10 mg tabletter med fördröjd frisättning administrerade en gång dagligen i åtta dagar jämfördes med samma parametrar för placebo, som illustreras nedan:
Effekter på exponering av esofagussyra
Hos patienter med GERD och måttlig till svår exponering för esofagussyra minskade en dos på 20 mg och 40 mg per dag av ACIPHEX 20 mg tabletter med fördröjd frisättning 24-timmarsexponeringen av esofagussyra. Efter sju dagars behandling minskade andelen tid som matstrupens pH var mindre än 4 från baslinjerna på 24,7 % för 20 mg och 23,7 % för 40 mg till 5,1 % respektive 2,0 %. Normalisering av 24-timmars intraesofageal syraexponering korrelerades till magsäckens pH högre än 4 under minst 35 % av 24-timmarsperioden; denna nivå uppnåddes hos 90 % av försökspersonerna som fick ACIPHEX 20 mg och hos 100 % av försökspersonerna som fick ACIPHEX 40 mg. Med ACIPHEX 20 mg och 40 mg per dag noterades signifikanta effekter på mag- och matstrupens pH efter en dags behandling och mer uttalad efter sju dagars behandling.
Effekter på Serum Gastrin
Medianhalten av fastande gastrin ökade på ett dosrelaterat sätt hos patienter som behandlats en gång dagligen med ACIPHEX 10 mg tabletter med fördröjd frisättning i upp till åtta veckor för ulcerös eller erosiv esofagit och hos patienter som behandlats i upp till 52 veckor för att förhindra att sjukdomen återkommer. Gruppens medianvärden höll sig inom det normala intervallet.
Hos en grupp patienter som behandlats med 20 mg ACIPHEX tabletter med fördröjd frisättning under 4 veckor observerades en fördubbling av genomsnittliga serumgastrinkoncentrationer. Cirka 35 % av dessa behandlade patienter utvecklade serumgastrinkoncentrationer över den övre normalgränsen.
Effekter på enterokromaffinliknande (ECL) celler
Ökat serumgastrin sekundärt till antisekretoriska medel stimulerar proliferation av gastriska ECL-celler, vilket med tiden kan resultera i ECL-cellshyperplasi hos råttor och möss och magkarcinoider hos råttor, särskilt hos honor [se Icke-klinisk toxikologi ].
Hos över 400 patienter som behandlats med ACIPHEX tabletter med fördröjd frisättning (10 eller 20 mg) en gång dagligen i upp till ett år, ökade incidensen av ECL-cellshyperplasi med tiden och dosen, vilket överensstämmer med den farmakologiska effekten av protonpumpshämmaren. Ingen patient utvecklade adenomatoida, dysplastiska eller neoplastiska förändringar av ECL-celler i magslemhinnan. Ingen patient utvecklade de karcinoida tumörer som observerats hos råttor.
Endokrina effekter
Studier på människor i upp till ett år har inte avslöjat kliniskt signifikanta effekter på det endokrina systemet. Hos friska manliga försökspersoner som behandlats med ACIPHEX tabletter med fördröjd frisättning i 13 dagar har inga kliniskt relevanta förändringar upptäckts i följande undersökta endokrina parametrar: 17 β-estradiol, sköldkörtelstimulerande hormon, tri-jodtyronin, tyroxin, tyroxinbindande protein, paratyreoidea hormon, insulin, glukagon, renin, aldosteron, follikelstimulerande hormon, luteotrofiskt hormon, prolaktin, somatotrofiskt hormon, dehydroepiandrosteron, kortisolbindande globulin och urin-6β-hydroxikortisol, serumtestosteron och dygnsrytmkortisolprofil.
Andra effekter
Hos människor som behandlats med ACIPHEX 10 mg tabletter med fördröjd frisättning i upp till ett år har inga systemiska effekter observerats på det centrala nervsystemet, lymfoida, hematopoetiska, njur-, lever-, kardiovaskulära eller andningsorganen. Inga data finns tillgängliga om långtidsbehandling med ACIPHEX 10 mg tabletter med fördröjd frisättning och okulära effekter.
Farmakokinetik
Efter oral administrering av 20 mg ACIPHEX 10 mg tabletter med fördröjd frisättning uppträder maximala plasmakoncentrationer (Cmax) av rabeprazol inom ett intervall av 2 till 5 timmar (Tmax). Rabeprazols Cmax och AUC är linjära över ett oralt dosintervall på 10 mg till 40 mg. Det finns ingen märkbar ackumulering när doser på 10 mg till 40 mg administreras var 24:e timme; farmakokinetiken för rabeprazol förändras inte vid upprepad dosering.
Absorption
Absolut biotillgänglighet för en 20 mg oral tablett av rabeprazol (jämfört med intravenös administrering) är cirka 52 %. När ACIPHEX 10 mg tabletter med fördröjd frisättning administreras tillsammans med en måltid med hög fetthalt, varierar Tmax; vilket samtidigt födointag kan fördröja absorptionen upp till 4 timmar eller längre. Cmax och graden av rabeprazolabsorption (AUC) förändras dock inte signifikant. Således kan ACIPHEX tabletter med fördröjd frisättning tas utan hänsyn till tidpunkten för måltider.
Distribution
Rabeprazol är till 96,3 % bundet till humana plasmaproteiner.
Eliminering
Ämnesomsättning
Rabeprazol metaboliseras i stor utsträckning. En betydande del av rabeprazol metaboliseras via systemisk icke-enzymatisk reduktion till en tioeterförening. Rabeprazol metaboliseras också till sulfon- och desmetylföreningar via cytokrom P450 i levern. Tioetern och sulfonen är de primära metaboliterna som mäts i human plasma. Dessa metaboliter observerades inte ha signifikant antisekretorisk aktivitet. In vitro-studier har visat att rabeprazol metaboliseras i levern huvudsakligen av cytokrom P450 3A (CYP3A) till en sulfonmetabolit och cytokrom P450 2C19 (CYP2C19) till desmetylrabeprazol. CYP2C19 uppvisar en känd genetisk polymorfism på grund av dess brist i vissa subpopulationer (t.ex. 3 till 5 % av kaukasier och 17 till 20 % av asiater). Rabeprazolmetabolismen är långsam i dessa subpopulationer, därför kallas de för dåliga metaboliserare av läkemedlet.
Exkretion
Efter en oral engångsdos på 20 mg av 14C-märkt rabeprazol eliminerades cirka 90 % av läkemedlet i urinen, främst som tioeterkarboxylsyra; dess glukuronid och metaboliter av merkaptursyra. Resten av dosen återfanns i avföringen. Total återvinning av radioaktivitet var 99,8 %. Inget oförändrat rabeprazol återfanns i urinen eller avföringen.
Specifika populationer
Geriatriska patienter
Hos 20 friska äldre försökspersoner som administrerades 20 mg ACIPHEX tabletter med fördröjd frisättning en gång dagligen i sju dagar, fördubblades AUC-värdena ungefär och Cmax ökade med 60 % jämfört med värdena i en parallell yngre kontrollgrupp. Det fanns inga tecken på läkemedelsackumulering efter administrering en gång dagligen [se Använd i specifik population ].
Pediatriska patienter
Farmakokinetiken för rabeprazol studerades hos 12 ungdomar med GERD i åldern 12 till 16 år i en multicenterstudie. Patienterna fick 20 mg ACIPHEX tabletter med fördröjd frisättning en gång dagligen i fem eller sju dagar. En ungefärlig ökning på 40 % av rabeprazolexponeringen noterades efter 5 till 7 dagars dosering jämfört med exponeringen efter 1 dags dosering. Farmakokinetiska parametrar hos ungdomar med GERD i åldern 12 till 16 år låg inom det intervall som observerades hos friska vuxna försökspersoner.
Manliga Och Kvinnliga Patienter Och Ras eller Etniska Grupper
I analyser justerade för kroppsmassa och längd visade rabeprazols farmakokinetik inga kliniskt signifikanta skillnader mellan manliga och kvinnliga försökspersoner. I studier som använde olika formuleringar av rabeprazol var AUC0-∞-värdena för friska japanska män cirka 50 till 60 % högre än värden som härrörde från sammanslagna data från friska män i USA.
Patienter med nedsatt njurfunktion
Hos 10 patienter med stabil njursjukdom i slutstadiet som kräver underhållshemodialys (kreatininclearance ≤5 ml/min/1,73 m²) observerades inga kliniskt signifikanta skillnader i farmakokinetiken för rabeprazol efter en engångsdos på 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning jämfört med 10 friska försökspersoner.
Patienter med nedsatt leverfunktion
I en singeldosstudie på 10 patienter med lätt till måttligt nedsatt leverfunktion (Child-Pugh klass A respektive B) som fick en engångsdos på 20 mg ACIPHEX 10 mg tabletter med fördröjd frisättning, fördubblades AUC0-24 ungefär, elimineringen halveringstiden var 2 till 3 gånger högre och total kroppsclearance minskade till mindre än hälften jämfört med värden hos friska män.
en multipeldosstudie med 12 patienter med lätt till måttligt nedsatt leverfunktion som administrerades 20 mg ACIPHEX 10 mg tabletter med fördröjd frisättning en gång dagligen i åtta dagar, ökade AUC0-∞- och Cmax-värdena med cirka 20 % jämfört med värden hos friska ålders- och könsmatchade ämnen. Dessa ökningar var inte statistiskt signifikanta.
Det finns ingen information om rabeprazoldisposition hos patienter med gravt nedsatt leverfunktion (Child-Pugh klass C) [se Användning i specifika populationer ].
Läkemedelsinteraktionsstudier
Kombinerad administrering med antimikrobiella medel
Sexton friska försökspersoner genotypade som omfattande metaboliserare med avseende på CYP2C19 fick 20 mg ACIPHEX tabletter med fördröjd frisättning, 1000 mg amoxicillin, 500 mg klaritromycin eller alla 3 läkemedlen i en fyravägsöverkorsningsstudie. Var och en av de fyra regimerna administrerades två gånger dagligen under 6 dagar. AUC och Cmax för klaritromycin och amoxicillin var inte olika efter kombinerad administrering jämfört med värden efter engångsadministrering. Emellertid ökade rabeprazols AUC och Cmax med 11 % respektive 34 % efter kombinerad administrering. AUC och Cmax för 14-hydroxiklaritromycin (aktiv metabolit av klaritromycin) ökade också med 42 % respektive 46 %. Denna ökning av exponeringen för rabeprazol och 14-hydroxiklaritromycin förväntas inte orsaka säkerhetsproblem.
Effekter av andra droger på Rabeprazol
Antacida
Samtidig administrering av ACIPHEX 20 mg tabletter med fördröjd frisättning och antacida gav inga kliniskt relevanta förändringar i plasmakoncentrationer av rabeprazol.
Effekter av Rabeprazol på andra droger
Studier på friska försökspersoner har visat att rabeprazol inte har kliniskt signifikanta interaktioner med andra läkemedel som metaboliseras av CYP450-systemet, såsom teofyllin (CYP1A2) som ges som enstaka orala doser, diazepam (CYP2C9 och CYP3A4) som en intravenös engångsdos och fenytoin ( CYP2C9 och CYP2C19) ges som en intravenös engångsdos (med extra oral dosering). Steady state-interaktioner mellan rabeprazol och andra läkemedel som metaboliseras av detta enzymsystem har inte studerats hos patienter.
Clopidogrel
Klopidogrel metaboliseras till sin aktiva metabolit delvis av CYP2C19. En studie av friska försökspersoner inklusive CYP2C19 omfattande och medelhöga metaboliserare som fick administrering en gång dagligen av klopidogrel 75 mg samtidigt med placebo eller med 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning (n=36), under 7 dagar genomfördes. Medel-AUC för den aktiva metaboliten av klopidogrel reducerades med cirka 12 % (genomsnittligt AUC-förhållande var 88 %, med 90 % KI på 81,7 till 95,5 %) när ACIPHEX tabletter med fördröjd frisättning administrerades samtidigt jämfört med administrering av klopidogrel och placebo [se LÄKEMEDELSINTERAKTIONER ].
Digoxin
Hos friska vuxna försökspersoner (n=16) resulterade samtidig administrering av 20 mg rabeprazolnatrium-tabletter med fördröjd frisättning och 2,5 mg en gång dagligen doser av digoxin vid steady state i cirka 29 % och 19 % ökning av genomsnittlig Cmax och AUC(0- 24) av digoxin [se LÄKEMEDELSINTERAKTIONER ].
Ketokonazol
Hos friska vuxna försökspersoner (n=19) resulterade samtidig administrering av 20 mg rabeprazolnatrium-tabletter med fördröjd frisättning vid steady state med en oral engångsdos på 400 mg ketokonazol i ungefär en genomsnittlig minskning av både Cmax och AUC(0-) på 31 %. inf) av ketokonazol [se LÄKEMEDELSINTERAKTIONER ].
Cyklosporin
In vitro-inkubationer med humana levermikrosomer indikerade att rabeprazol hämmade cyklosporinmetabolismen med en IC50 på 62 mikromolar, en koncentration som är över 50 gånger högre än Cmax hos friska frivilliga efter 14 dagars dosering med 20 mg ACIPHEX 10 mg fördröjda tabletter. Denna grad av hämning liknar den av omeprazol vid ekvivalenta koncentrationer.
Mikrobiologi
Följande in vitro-data finns tillgängliga men den kliniska betydelsen är okänd.
Rabeprazolnatrium, amoxicillin och klaritromycin som en treläkemedelsregim har visat sig vara aktiva mot de flesta stammar av Helicobacter pylori in vitro och vid kliniska infektioner [se INDIKATIONER OCH ANVÄNDNING , Kliniska studier ].
Helicobacter pylori
Känslighetstestning av H. pylori-isolat utfördes för amoxicillin och klaritromycin med användning av metodik för utspädning av agar1, och lägsta hämmande koncentrationer (MIC) bestämdes.
Standardiserade förfaranden för känslighetstest kräver användning av laboratoriekontrollmikroorganismer för att kontrollera de tekniska aspekterna av laboratorieförfarandena.
Förekomst av antibiotikaresistenta organismer bland kliniska isolat
Förbehandlingsmotstånd
Förbehandlingsresistensfrekvensen för klaritromycin (MIC ≥1 mcg/ml) mot H. pylori var 9 % (51/560) vid baslinjen i alla behandlingsgrupper tillsammans. Mer än 99 % (558/560) av patienterna hade H. pylori-isolat som ansågs vara känsliga (MIC ≤0,25 mcg/ml) för amoxicillin vid baslinjen. Två patienter hade baseline H. pylori isolat med en amoxicillin MIC på 0,5 mcg/ml.
För information om känslighetstestning om Helicobacter pylori, se avsnittet Mikrobiologi i förskrivningsinformation för klaritromycin och amoxicillin.
Patienter med ihållande H. pylori-infektion efter behandling med rabeprazol, amoxicillin och klaritromycin kommer sannolikt att ha klaritromycinresistenta kliniska isolat. Därför bör klaritromycinkänslighetstest göras när det är möjligt. Om resistens mot klaritromycin påvisas eller känslighetstestning inte är möjlig, bör alternativ antimikrobiell behandling sättas in.
Amoxicillinkänslighetstestresultat och kliniska/bakteriologiska resultat
den amerikanska multicenterstudien hade mer än 99 % (558/560) av patienterna H. pylori-isolat som ansågs vara känsliga (MIC ≤0,25 mcg/ml) för amoxicillin vid baslinjen. De andra 2 patienterna hade baseline H. pylori-isolat med en amoxicillin MIC på 0,5 mcg/ml, och båda isolaten var klaritromycinresistenta vid baslinjen; i ett fall utrotades H. pylori. I 7- och 10-dagarsbehandlingsgrupperna utrotades 75 % (107/145) respektive 79 % (112/142) av patienterna som hade förbehandling amoxicillinkänsliga MIC (≤0,25 mcg/ml) av H. pylori . Inga patienter utvecklade amoxicillinresistent H. pylori under behandlingen.
Farmakogenomik
en klinisk studie för att utvärdera ACIPHEX tabletter med fördröjd frisättning hos vuxna japanska patienter kategoriserade efter CYP2C19-genotyp (n=6 per genotypkategori), var magsyrasuppression högre hos dåliga metaboliserare jämfört med omfattande metaboliserare. Detta kan bero på högre plasmanivåer av rabeprazol hos dåliga metaboliserare. Den kliniska relevansen av detta är inte känd. Huruvida interaktioner mellan rabeprazolnatrium och andra läkemedel som metaboliseras av CYP2C19 skulle vara olika mellan omfattande metaboliserare och låga metaboliserare har inte studerats.
Kliniska studier
Läkning av erosiv eller ulcerös GERD hos vuxna
en amerikansk, multicenter, randomiserad, dubbelblind, placebokontrollerad studie behandlades 103 patienter i upp till åtta veckor med placebo, 10 mg, 20 mg eller 40 mg ACIPHEX tabletter med fördröjd frisättning en gång dagligen. För denna och alla studier av GERD-läkning var endast patienter med GERD-symtom och minst grad 2 esofagit (modifierad Hetzel-Dent-graderingsskala) kvalificerade för inträde. Endoskopisk läkning definierades som grad 0 eller 1. Varje rabeprazoldos var signifikant överlägsen placebo när det gällde endoskopisk läkning efter fyra och åtta veckors behandling. Andelen patienter som visade endoskopisk läkning var följande:
Dessutom fanns det en statistiskt signifikant skillnad till förmån för ACIPHEX 10 mg, 20 mg och 40 mg doserna jämfört med placebo vid vecka 4 och 8 avseende fullständig upplösning av GERD halsbränna frekvens (p≤0,026). Alla ACIPHEX-grupper rapporterade signifikant högre grad av fullständig upplösning av GERD-halsbränna dagtid jämfört med placebo vid vecka 4 och 8 (p≤0,036). Genomsnittlig minskning från baslinjen i daglig antaciddos var statistiskt signifikant för alla ACIPHEX-grupper jämfört med placebo vid både vecka 4 och 8 (p≤0,007).
I en nordamerikansk, randomiserad, dubbelblind, aktivt kontrollerad multicenterstudie av 336 patienter var andelen patienter som läkte vid endoskopi efter fyra och åtta veckors behandling statistiskt överlägsen hos patienterna som behandlades med ACIPHEX tabletter med fördröjd frisättning jämfört med ranitidin. :
En dos på 20 mg en gång dagligen av ACIPHEX tabletter med fördröjd frisättning var signifikant effektivare än ranitidin 150 mg fyra gånger dagligen i procenten av patienter med fullständigt upphörande av halsbränna vid vecka 4 och 8 (p
Den rekommenderade dosen av ACIPHEX 10 mg tabletter med fördröjd frisättning är 20 mg en gång dagligen i 4 till 8 veckor.
Långsiktigt underhåll av läkning av erosiv eller ulcerös GERD hos vuxna
Långtidsupprätthållandet av läkning hos patienter med erosiv eller ulcerös GERD som tidigare läkt med gastrisk antisekretorisk terapi utvärderades i två amerikanska, multicenter, randomiserade, dubbelblinda, placebokontrollerade studier med identisk design av 52 veckors varaktighet. De två studierna randomiserade 209 respektive 285 patienter till att få antingen 10 mg eller 20 mg ACIPHEX tabletter med fördröjd frisättning en gång dagligen eller placebo. Som visas i tabellerna 10 och 11 nedan var patienter som behandlades med ACIPHEX tabletter med fördröjd frisättning signifikant överlägsna placebo i båda studierna med avseende på upprätthållande av läkning av GERD och andelen patienter som förblev fria från halsbränna vid 52 veckor. Den rekommenderade dosen av ACIPHEX 20 mg tabletter med fördröjd frisättning är 20 mg en gång dagligen.
Behandling av symtomatisk GERD hos vuxna
Två amerikanska, multicenter, dubbelblinda, placebokontrollerade studier utfördes på 316 vuxna patienter med halsbränna dag- och nattetid. Patienterna rapporterade 5 eller fler perioder av måttlig till mycket svår halsbränna under placebobehandlingsfasen veckan före randomiseringen. Patienterna bekräftades genom endoskopi att de inte hade några esofaguserosion.
Procentandelen halsbränna fria dag- och/eller nattperioder var högre med 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning jämfört med placebo under de fyra veckorna av studien i studien RABUSA-2 (47 % vs. 23 %) och studien RAB-USA- 3 (52 % mot 28 %). De genomsnittliga minskningarna från baslinjen i genomsnittliga poäng för halsbränna dag- och nattetid var signifikant högre för ACIPHEX 20 mg jämfört med placebo vid vecka 4. Grafiska visningar som visar de dagliga medelvärdena dagtid och natt visas i figurerna 2 till 5.
Figur 2: Medelvärde för halsbränna dagtid RAB-USA-2
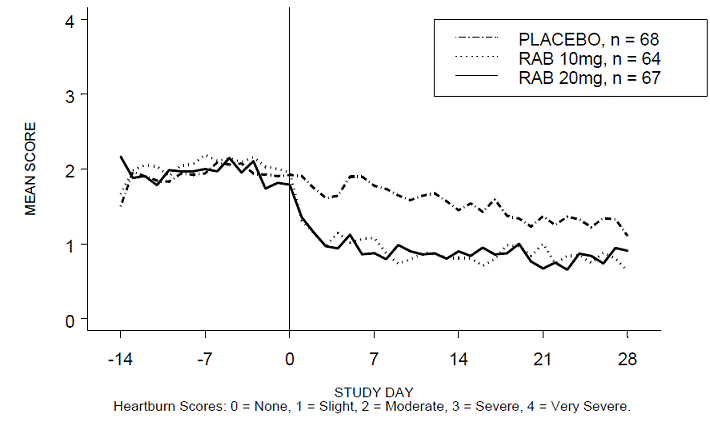
Figur 3: Medelvärde för halsbränna på natten RAB-USA-2
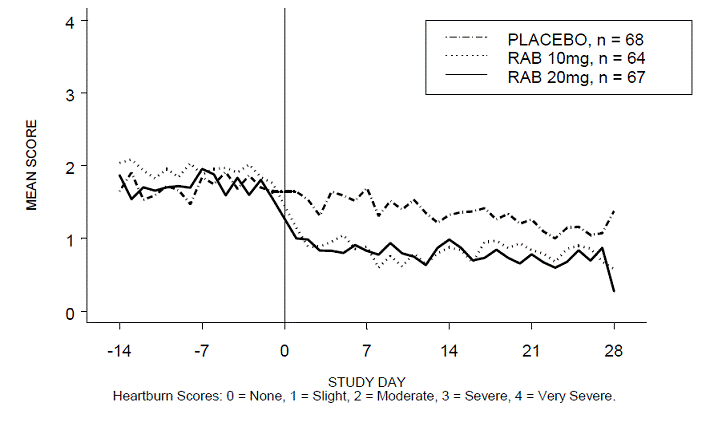
Figur 4: Medelvärde för halsbränna dagtid RAB-USA-3 Figur 3: Medelvärde för halsbränna dagtid RAB - USA –3
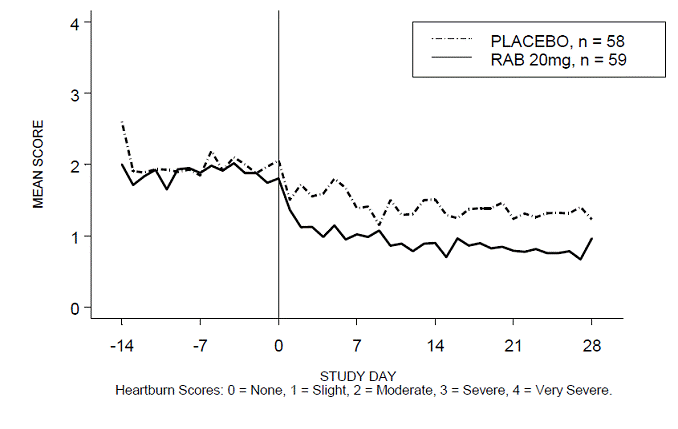
Figur 5: Medelvärde för halsbränna på natten RAB-USA-3
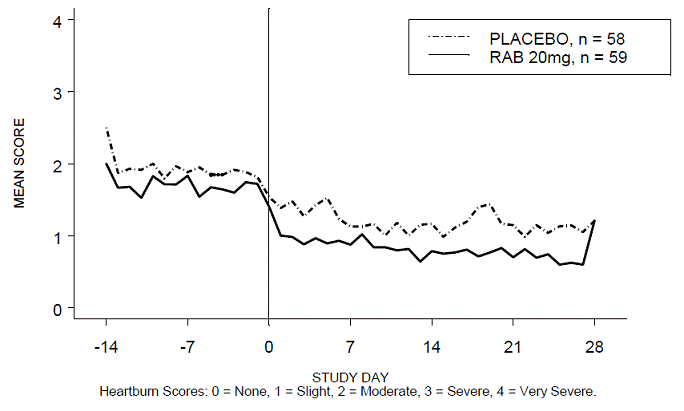
Dessutom visade den kombinerade analysen av dessa två studier att 20 mg ACIPHEX 10 mg tabletter med fördröjd frisättning signifikant förbättrade andra GERD-associerade symtom (uppstötningar, rapningar och tidig mättnad) vid vecka 4 jämfört med placebo (alla p-värden
En dos på 20 mg ACIPHEX 20 mg tabletter med fördröjd frisättning minskade också signifikant daglig konsumtion av antacida jämfört med placebo under 4 veckor (p
Den rekommenderade dosen av ACIPHEX tabletter med fördröjd frisättning är 20 mg en gång dagligen i 4 veckor.
Läkning Av Duodenalsår Hos Vuxna
en amerikansk, randomiserad, dubbelblind, multicenterstudie som utvärderade effektiviteten av 20 mg och 40 mg ACIPHEX 10 mg tabletter med fördröjd frisättning en gång dagligen jämfört med placebo för att läka endoskopiskt definierade duodenalsår, behandlades 100 patienter i upp till fyra veckor. ACIPHEX var signifikant överlägsen placebo när det gällde läkning av duodenalsår. Procentandelen patienter med endoskopisk läkning presenteras nedan:
Vid vecka 2 och 4 rapporterade signifikant fler patienter i ACIPHEX 20- och 40 mg-grupperna fullständig upplösning av sårsmärtans frekvens (p≤0,018), svårighetsgrad av smärta under dagtid (p≤0,023) och svårighetsgrad av smärta på natten (p≤0,035) jämfört med placebopatienter. Det enda undantaget var 40 mg-gruppen kontra placebo vid vecka 2 för smärtfrekvens i duodenalsår (p=0,094). Signifikanta skillnader i upplösning av smärta under dagtid och natt noterades i båda ACIPHEX-grupperna jämfört med placebo i slutet av studiens första vecka. Signifikanta minskningar av daglig användning av antacida noterades också i båda ACIPHEX-grupperna jämfört med placebo vid vecka 2 och 4 (p
En internationell randomiserad, dubbelblind, aktivt kontrollerad studie genomfördes på 205 patienter som jämförde 20 mg ACIPHEX tabletter med fördröjd frisättning en gång dagligen med 20 mg omeprazol en gång dagligen. Studien utformades för att ge minst 80 % kraft för att utesluta en skillnad på minst 10 % mellan ACIPHEX 10 mg och omeprazol, med antagande om fyra veckors läkningssvar på 93 % för båda grupperna. Hos patienter med endoskopiskt definierade duodenalsår som behandlades i upp till fyra veckor var ACIPHEX jämförbar med omeprazol när det gällde läkning av duodenalsår. Procentandelen patienter med endoskopisk läkning efter två och fyra veckor presenteras nedan:
ACIPHEX 20 mg och omeprazol var jämförbara när det gäller att ge fullständig upplösning av symtomen.
Den rekommenderade dosen av ACIPHEX 20 mg tabletter med fördröjd frisättning är 20 mg en gång dagligen i 4 veckor.
Utrotning av Helicobacter pylori hos patienter med magsårssjukdom eller symtomatisk icke-ulcussjukdom hos vuxna
Den amerikanska multicenterstudien var en dubbelblind parallellgruppsjämförelse av ACIPHEX tabletter med fördröjd frisättning, amoxicillin och klaritromycin under 3, 7 eller 10 dagar jämfört med omeprazol, amoxicillin och klaritromycin under 10 dagar. Behandlingen bestod av rabeprazol 20 mg två gånger dagligen, amoxicillin 1000 mg två gånger dagligen och klaritromycin 500 mg två gånger dagligen (RAC) eller omeprazol 20 mg två gånger dagligen, amoxicillin 1000 mg två gånger dagligen och klaritromycin 500 mg två gånger dagligen (OAC). Patienter med H. pylori-infektion stratifierades i förhållandet 1:1 för de med magsår (aktiva eller har haft magsår under de senaste fem åren) [PUD] och de som var symtomatiska men utan magsår [NPUD], som bestäms genom övre gastrointestinala endoskopi. De totala H. pylori-utrotningsfrekvenserna, definierade som negativa 13C-UBT för H. pylori ≥6 veckor från slutet av behandlingen, visas i följande tabell. Utrotningsfrekvensen i 7-dagars- och 10-dagars RAC-regimerna visade sig vara liknande 10-dagars OAC-regimer med användning av antingen Intent-to-Treat (ITT) eller Per-Protocol (PP) populationer. Utrotningsfrekvensen i RAC 3-dagarsregimen var sämre än de andra regimerna.
Den rekommenderade dosen av ACIPHEX 20 mg tabletter med fördröjd frisättning är 20 mg två gånger dagligen med amoxicillin och klaritromycin i 7 dagar.
Patologiska hypersekretoriska tillstånd, inklusive Zollinger-Ellisons syndrom hos vuxna
Tolv patienter med idiopatisk gastrisk hypersekretion eller Zollinger-Ellisons syndrom har framgångsrikt behandlats med ACIPHEX 10 mg tabletter med fördröjd frisättning i doser från 20 till 120 mg i upp till 12 månader. ACIPHEX 10 mg gav tillfredsställande hämning av magsyrasekretionen hos alla patienter och fullständig upplösning av tecken och symtom på syra-peptisk sjukdom där sådana förekom. ACIPHEX 20 mg förhindrade också återfall av gastrisk hypersekretion och manifestationer av syra-peptisk sjukdom hos alla patienter. De höga doser av ACIPHEX som användes för att behandla denna lilla kohort av patienter med gastrisk hypersekretion tolererades väl.
Den rekommenderade startdosen av ACIPHEX tabletter med fördröjd frisättning är 60 mg en gång dagligen.
REFERENSER
1. Clinical and Laboratory Standards Institute (CLSI). Metoder för utspädning Antimikrobiella känslighetstester för bakterier som växer aerobt; Godkänd standard - tionde upplagan. CLSI Document M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania, 19087, USA 2015.
PATIENTINFORMATION
ACIPHEX® (a-se-feks) (rabeprazolnatrium) tabletter med fördröjd frisättning
Vilken är den viktigaste informationen jag borde veta om ACIPHEX 10mg?
Du ska ta ACIPHEX 20 mg precis som ordinerats, i lägsta möjliga dos och under den kortaste tid som behövs.
ACIPHEX 20 mg kan hjälpa dina syrarelaterade symtom, men du kan fortfarande ha allvarliga magproblem. Prata med din läkare.
ACIPHEX 20mg kan orsaka allvarliga biverkningar, inklusive:
- En typ av njurproblem (akut tubulointerstitiell nefrit). Vissa personer som tar protonpumpshämmare (PPI), inklusive ACIPHEX, kan utveckla ett njurproblem som kallas akut tubulointerstitiell nefrit som kan inträffa när som helst under behandling med ACIPHEX. Ring din läkare omedelbart om du har en minskning av mängden du kissar eller om du har blod i urinen.
- Diarré orsakad av en infektion (Clostridium difficile) i dina tarmar. Ring din läkare omedelbart om du har vattnig avföring eller magsmärtor som inte försvinner. Du kanske har feber eller inte.
- Benfrakturer (höft, handled eller ryggrad). Benfrakturer i höften, handleden eller ryggraden kan inträffa hos personer som tar flera dagliga doser av PPI-läkemedel och under en lång tidsperiod (ett år eller längre). Tala om för din läkare om du har en benfraktur, särskilt i höften, handleden eller ryggraden.
- Vissa typer av lupus erythematosus. Lupus erythematosus är en autoimmun sjukdom (kroppens immunceller attackerar andra celler eller organ i kroppen). Vissa personer som tar PPI-läkemedel, inklusive ACIPHEX, kan utveckla vissa typer av lupus erythematosus eller få försämring av den lupus de redan har. Ring din läkare omedelbart om du har ny eller förvärrad ledvärk eller utslag på kinderna eller armarna som blir värre i solen.
Tala med din läkare om din risk för dessa allvarliga biverkningar.
ACIPHEX 10mg kan ha andra allvarliga biverkningar. Se "Vilka är de möjliga biverkningarna av ACIPHEX 10mg?"
Vad är ACIPHEX 20mg?
ACIPHEX 10mg är ett receptbelagt läkemedel som kallas protonpumpshämmare (PPI).
ACIPHEX 20mg minskar mängden syra i magen.
Hos vuxna, ACIPHEX används för:
- 8 veckor upp till 16 veckor för att läka syrarelaterade skador på slemhinnan i matstrupen (kallad erosiv esofagit eller EE) och för att lindra symtom, såsom halsbränna.
- bibehålla läkning av matstrupen och lindring av symtom relaterade till EE. Det är inte känt om ACIPHEX 20mg är säkert och effektivt om det används längre än 12 månader (1 år).
- upp till 4 veckor för att behandla halsbränna dag- och nattetid och andra symtom som inträffar med gastroesofageal refluxsjukdom (GERD).
- upp till 4 veckor för läkning och lindring av symtom på duodenalsår.
- 7 dagar med vissa antibiotiska läkemedel för att behandla en infektion och magsår (duodenalsår) orsakade av bakterier som kallas H. pylori.
- långtidsbehandling av tillstånd där din mage gör för mycket syra. Detta inkluderar ett sällsynt tillstånd som kallas Zollinger-Ellisons syndrom.
Hos ungdomar 12 år och äldre, ACIPHEX 10 mg används i upp till 8 veckor för att behandla symtom på GERD.
Det är inte känt om ACIPHEX är säkert och effektivt för barn under 12 år för annan användning.
ACIPHEX tabletter med fördröjd frisättning ska inte användas till barn under 12 år.
Ta inte ACIPHEX 10 mg om du är:
- allergisk mot rabeprazol, något annat PPI-läkemedel eller något av innehållsämnena i ACIPHEX. Se slutet av denna medicinguide för en komplett lista över ingredienser.
- tar ett läkemedel som innehåller rilpivirin (EDURANT, COMPLERA, ODEFSEY) som används för att behandla HIV-1 (humant immunbristvirus).
Innan du tar ACIPHEX, berätta för din läkare om alla dina medicinska tillstånd, inklusive om du:
- har låga magnesiumnivåer, låga kalciumnivåer och låga kaliumnivåer i ditt blod.
- har leverproblem.
- är gravid eller planerar att bli gravid. Det är inte känt om ACIPHEX 20 mg kan skada ditt ofödda barn.
- ammar eller planerar att amma. Det är inte känt om ACIPHEX 10 mg passerar över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar ACIPHEX.
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Berätta särskilt för din läkare om du tar ett antibiotikum som innehåller klaritromycin eller amoxicillin eller om du tar warfarin (COUMADIN, JANTOVEN), metotrexat (OTREXUP, RASUVO, TREXALL, XATMEP), digoxin (LANOXIN) eller ett vattendrivande medel (diuretikum).
Hur ska jag ta ACIPHEX?
- Ta ACIPHEX exakt som ordinerats.
- ACIPHEX tas vanligtvis 1 gång varje dag. Din läkare kommer att tala om för dig när på dygnet du ska ta ACIPHEX, baserat på ditt medicinska tillstånd.
- ACIPHEX 10 mg kan tas med eller utan mat. Din läkare kommer att tala om för dig om du ska ta detta läkemedel med eller utan mat baserat på ditt medicinska tillstånd.
- Svälj varje ACIPHEX 20 mg tablett hel. Tugga, krossa eller dela inte ACIPHEX 10 mg tabletter. Tala om för din läkare om du inte kan svälja tabletter hela.
- Om du missar en dos av ACIPHEX 10 mg, ta den så snart som möjligt. Om det nästan är dags för nästa dos ska du inte ta den missade dosen. Du bör ta din nästa dos vid din vanliga tidpunkt. Ta inte 2 doser samtidigt.
- Om du tar för mycket ACIPHEX 20mg, ring din läkare eller din giftkontrollcentral på 1-800-222-1222 omedelbart, eller gå till närmaste akutmottagning.
- Om din läkare ordinerar antibiotika med ACIPHEX, läs patientinformationen som följer med antibiotikaläkemedlen innan du tar dem.
Vilka är de möjliga biverkningarna av ACIPHEX 20mg?
ACIPHEX 10mg kan orsaka allvarliga biverkningar, inklusive:
- Se "Vad är den viktigaste informationen jag borde veta om ACIPHEX 20mg?"
- Interaktion med warfarin. Att ta warfarin med ett PPI-läkemedel kan leda till en ökad risk för blödning och död. Om du tar warfarin kan din läkare kontrollera ditt blod för att se om du har en ökad risk för blödning. Om du tar warfarin under behandling med ACIPHEX 20 mg, berätta omedelbart för din läkare om du har några tecken eller symtom på blödning, inklusive:
- smärta, svullnad eller obehag
- huvudvärk, yrsel eller svaghet
- ovanliga blåmärken (blåmärken som uppstår utan känd orsak eller som växer i storlek)
- näsblod
- blödande tandkött
- blödning från skärsår tar lång tid att sluta
- menstruationsblödning som är tyngre än normalt
- rosa eller brun urin
- röd eller svart avföring
- hosta blod
- kräks blod eller kräks som ser ut som kaffesump
- Låga vitamin B-12 nivåer kroppen kan hända hos personer som har tagit ACIPHEX 10mg under lång tid (mer än 3 år). Tala om för din läkare om du har symtom på låga vitamin B-12-nivåer, inklusive andnöd, yrsel, oregelbunden hjärtrytm, muskelsvaghet, blek hud, trötthetskänsla, humörförändringar och stickningar eller domningar i armar och ben.
- Låga magnesiumnivåer i kroppen kan inträffa hos personer som har tagit ACIPHEX 20 mg i minst 3 månader. Tala om för din läkare om du har symtom på låga magnesiumnivåer, inklusive kramper, yrsel, oregelbunden hjärtrytm, darrning, muskelvärk eller svaghet och spasmer i händer, fötter eller röst.
- Magutväxter (fundiska körtelpolyper). Personer som tar PPI-läkemedel under lång tid har en ökad risk att utveckla en viss typ av magtillväxt som kallas fundic gland polyper, särskilt efter att ha tagit PPI-läkemedel i mer än 1 år.
- Allvarliga hudreaktioner. ACIPHEX kan orsaka sällsynta men allvarliga hudreaktioner som kan påverka någon del av din kropp. Dessa allvarliga hudreaktioner kan behöva behandlas på sjukhus och kan vara livshotande:
- Hudutslag som kan ha blåsor, fjällning eller blödning på någon del av huden (inklusive dina läppar, ögon, mun, näsa, könsorgan, händer eller fötter).
- Du kan också ha feber, frossa, värk i kroppen, andnöd eller förstorade lymfkörtlar.
Sluta ta ACIPHEX 20 mg och kontakta din läkare omedelbart. Dessa symtom kan vara det första tecknet på en allvarlig hudreaktion.
De vanligaste biverkningarna av ACIPHEX 20 mg hos vuxna inkluderar: smärta, ont i halsen, gaser, infektion och förstoppning.
De vanligaste biverkningarna av ACIPHEX hos ungdomar 12 år och äldre inkluderar: huvudvärk, diarré, illamående, kräkningar och smärta i magområdet (buken).
Dessa är inte alla möjliga biverkningar av ACIPHEX. Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara ACIPHEX?
Förvara ACIPHEX tabletter på en torr plats i rumstemperatur mellan 68°F till 77°F (20°C till 25°C).
Förvara ACIPHEX 20mg och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av ACIPHEX.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte ACIPHEX för ett tillstånd som det inte har ordinerats för. Ge inte ACIPHEX till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Du kan fråga din läkare eller apotekspersonal om information om ACIPHEX som är skriven för vårdpersonal.
Vilka är ingredienserna i ACIPHEX 10mg?
Aktiv beståndsdel: rabeprazolnatrium
Inaktiva Ingredienser: karnaubavax, krospovidon, diacetylerade monoglycerider, etylcellulosa, hydroxipropylcellulosa, hypromellosftalat, magnesiumstearat, mannitol, natriumhydroxid, natriumstearylfumarat, talk och titandioxid. Järnoxidgul är färgämnet för tablettöverdraget. Rött järnoxid är bläckpigmentet.
Denna medicineringsguide har godkänts av US Food and Drug Administration. Reviderad: 03/2022
