Pepcid 20mg, 40mg Famotidine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Pepcid och hur används det?
Pepcid (famotidin) används för att behandla halsbränna, GERD och Zollinger-Ellisons syndrom. Det finns receptfritt. Pepcid 20mg finns tillgängligt som ett generiskt läkemedel.
Vilka är möjliga biverkningar av att använda Pepcid?
Biverkningar är ovanliga, men kan inkludera:
- Trötthet,
- kräkningar,
- illamående,
- Abdominalt obehag,
- anorexi,
- torr mun,
- utslag, och
- muskelkramp
BESKRIVNING
Den aktiva ingrediensen i PEPCID® (famotidin) är en histamin H2-receptorantagonist. Famotidin är N'(aminosulfonyl)-3-[[[2-[(diaminometylen)amino]-4-tiazolyl]metyl]tio]propanimidamid. Den empiriska formeln för famotidin är C8H15N7O2S3 och dess molekylvikt är 337,43. Dess strukturformel är:
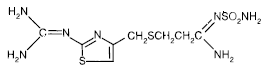
Famotidin är en vit till blekgul kristallin förening som är fritt löslig i isättika, lätt löslig i metanol, mycket svagt löslig i vatten och praktiskt taget olöslig i etanol.
Varje tablett för oral administrering innehåller antingen 20 mg eller 40 mg famotidin och följande inaktiva ingredienser: hydroxipropylcellulosa, hypromellos, järnoxider, magnesiumstearat, mikrokristallin cellulosa, majsstärkelse, talk, titandioxid och karnaubavax.
INDIKATIONER
PEPCID 40mg indikeras i:
DOSERING OCH ADMINISTRERING
Duodenalsår
Akut terapi: Den rekommenderade orala dosen för vuxna för aktivt duodenalsår är 40 mg en gång om dagen vid sänggåendet. De flesta patienter läker inom 4 veckor; det finns sällan anledning att använda PEPCID i full dos längre än 6 till 8 veckor. En regim på 20 mg två gånger dagligen är också effektiv.
Underhållsterapi: Den rekommenderade orala dosen för vuxna är 20 mg en gång om dagen vid sänggåendet.
Benignt magsår
Akut terapi: Den rekommenderade orala dosen för vuxna för aktivt benignt magsår är 40 mg en gång om dagen vid sänggåendet.
Gastroesofageal refluxsjukdom (GERD)
Den rekommenderade orala dosen för behandling av vuxna patienter med symtom på GERD är 20 mg två gånger dagligen i upp till 6 veckor. Den rekommenderade orala dosen för behandling av vuxna patienter med esofagit inklusive erosioner och sår och åtföljande symtom på grund av GERD är 20 eller 40 mg två gånger dagligen i upp till 12 veckor (se KLINISK FARMAKOLOGI hos vuxna , Kliniska studier ).
Dosering för pediatriska patienter
Ser FÖRSIKTIGHETSÅTGÄRDER , Pediatriska patienter
Studierna som beskrivs i FÖRSIKTIGHETSÅTGÄRDER, pediatriska patienter
Dosering för pediatriska patienter i åldern 1-16 år
Ser FÖRSIKTIGHETSÅTGÄRDER , Pediatriska patienter 1-16 år.
Studierna som beskrivs i FÖRSIKTIGHETSÅTGÄRDER, pediatriska patienter 1-16 år föreslår följande startdoser för pediatriska patienter 1-16 år:
Magsår - 0,5 mg/kg/dag po vid sänggåendet eller delat bud upp till 40 mg/dag.
Gastroesofageal refluxsjukdom med eller utan esofagit inklusive erosioner och sår - 1,0 mg/kg/dag po uppdelat bud upp till 40 mg två gånger dagligen
Medan publicerade okontrollerade studier tyder på effektiviteten av famotidin vid behandling av gastroesofageal refluxsjukdom och magsår, är data från pediatriska patienter otillräckliga för att fastställa procentuell respons med dos och behandlingslängd. Därför bör behandlingslängd (inledningsvis baserat på rekommendationer om varaktighet för vuxna) och dos individualiseras baserat på kliniskt svar och/eller pH-bestämning (mag eller matstrupe) och endoskopi. Publicerade okontrollerade kliniska studier på pediatriska patienter 1-16 år har använt doser upp till 1 mg/kg/dag för magsår och 2 mg/kg/dag för GERD med eller utan esofagit inklusive erosioner och sårbildning.
Patologiska hypersekretoriska tillstånd (t.ex. Zollinger-Ellisons syndrom, multipla endokrina adenom)
Doseringen av PEPCID till patienter med patologiska hypersekretoriska tillstånd varierar med den enskilda patienten. Den rekommenderade orala startdosen för vuxna för patologiska hypersekretoriska tillstånd är 20 mg q 6 timmar. Hos vissa patienter kan en högre startdos behövas. Doserna bör anpassas till individuella patientbehov och bör fortsätta så länge som kliniskt indicerat. Doser upp till 160 mg q 6 timmar har administrerats till vissa vuxna patienter med svårt Zollinger-Ellisons syndrom.
Samtidig användning av antacida
Antacida kan ges samtidigt vid behov.
Dosjustering för patienter med måttlig eller svår njurinsufficiens
Hos vuxna patienter med måttlig (kreatininclearance
Baserat på jämförelsen av farmakokinetiska parametrar för PEPCID hos vuxna och pediatriska patienter, bör dosjustering hos pediatriska patienter med måttlig eller svår njurinsufficiens övervägas.
HUR LEVERERAS
PEPCID 40mg tabletter 20 mg, är beigefärgade, rundade fyrkantiga, filmdragerade tabletter märkta MSD på ena sidan och släta på den andra. De levereras enligt följande:
NDC 42998-639-09 användningsenhet flaskor med 30 st NDC 42998-639-98 flaskor med 100 användningsenheter.
PEPCID 40 mg tabletter, 40 mg, är bruna, rundade kvadratiska, filmdragerade tabletter kodade MSD på ena sidan och släta på den andra. De levereras enligt följande:
NDC 42998-649-09 flaskor med 30 användningsenheter NDC 42998-649-98 användningsenhet flaskor om 100. Förvaring
Förvara vid kontrollerad rumstemperatur.
PEPCID® (famotidin) tabletter 20 mg och tabletter 40 mg tillverkas för: Marathon Pharmaceuticals, LLC, Northbrook, IL 60062, USA. Utgiven februari 2014.
BIEFFEKTER
De biverkningar som anges nedan har rapporterats under inhemska och internationella kliniska prövningar på cirka 2500 patienter. I de kontrollerade kliniska prövningarna där PEPCID 40 mg tabletter jämfördes med placebo, var förekomsten av biverkningar i gruppen som fick PEPCID tabletter, 40 mg vid sänggåendet, liknande den i placebogruppen.
Följande biverkningar har rapporterats förekomma hos mer än 1 % av patienterna i behandling med PEPCID i kontrollerade kliniska prövningar och kan vara orsaksrelaterade till läkemedlet: huvudvärk (4,7 %), yrsel (1,3 %), förstoppning (1,2 % diarré (1,7%).
Följande andra biverkningar har rapporterats sällan i kliniska prövningar eller sedan läkemedlet marknadsfördes. Relationen till behandling med PEPCID 20 mg har varit oklar i många fall. Inom varje kategori listas biverkningarna i ordning efter minskande svårighetsgrad:
Kroppen som helhet: feber, asteni, trötthet
Kardiovaskulär: arytmi, AV-block, hjärtklappning. Förlängt QT-intervall, hos patienter med nedsatt njurfunktion, har rapporterats i mycket sällsynta fall.
Gastrointestinala: kolestatisk gulsot, hepatit, leverenzymavvikelser, kräkningar, illamående, bukbesvär, anorexi, muntorrhet
Hematologiska: sällsynta fall av agranulocytos, pancytopeni, leukopeni, trombocytopeni
Överkänslighet: anafylaxi, angioödem, orbital- eller ansiktsödem, urtikaria, utslag, konjunktival injektion
Muskuloskeletala: rabdomyolys, muskuloskeletal smärta inklusive muskelkramper, artralgi
Nervsystemet/psykiatrisk: grand mal-anfall; psykiska störningar, som var reversibla i fall för vilka uppföljning erhölls, inklusive hallucinationer, förvirring, agitation, depression, ångest, minskad libido; parestesi; sömnlöshet; sömnighet. Kramper, hos patienter med nedsatt njurfunktion, har rapporterats i mycket sällsynta fall.
Andningsvägar: bronkospasm, interstitiell pneumoni
Hud: giftig epidermal nekrolys/Stevens-Johnsons syndrom (mycket sällsynt), alopeci, akne, klåda, torr hud, rodnad
Särskilda sinnen: tinnitus, smakstörning
Övrig: sällsynta fall av impotens och sällsynta fall av gynekomasti har rapporterats; I kontrollerade kliniska prövningar var dock incidensen inte högre än de som sågs med placebo.
De biverkningar som rapporterats för PEPCID-tabletter kan också förekomma med PEPCID 20 mg för oral suspension.
Pediatriska patienter
I en klinisk studie på 35 pediatriska patienter
LÄKEMEDELSINTERAKTIONER
Inga läkemedelsinteraktioner har identifierats. Studier med famotidin på människa, i djurmodeller och in vitro har inte visat någon signifikant störning av dispositionen av föreningar som metaboliseras av de hepatiska mikrosomala enzymerna, t.ex. cytokrom P450-systemet. Föreningar som testats på människa inkluderar warfarin, teofyllin, fenytoin, diazepam, aminopyrin och antipyrin. Indocyaningrönt som ett index för leverläkemedelsextraktion har testats och inga signifikanta effekter har hittats.
VARNINGAR
Ingen information lämnas
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Symtomatiskt svar på behandling med PEPCID utesluter inte förekomsten av gastrisk malignitet.
Patienter med måttlig eller svår njurinsufficiens
Eftersom CNS-biverkningar har rapporterats hos patienter med måttlig och svår njurinsufficiens, kan längre intervall mellan doserna eller lägre doser behöva användas hos patienter med måttlig (kreatininclearance KLINISK FARMAKOLOGI hos vuxna och DOSERING OCH ADMINISTRERING ). Förlängt QT-intervall har rapporterats i mycket sällsynta fall hos patienter med nedsatt njurfunktion vars dos/dosintervall av famotidin kanske inte har justerats på lämpligt sätt.
Karcinogenes, Mutagenes, Nedsatt fertilitet
I en 106-veckors studie på råttor och en 92-veckors studie på möss som fick orala doser på upp till 2000 mg/kg/dag (ungefär 2500 gånger den rekommenderade dosen för människor för aktivt duodenalsår), fanns det inga tecken på cancerframkallande potential för PEPCID.
Famotidin var negativt i det mikrobiella mutagentestet (Ames-testet) med Salmonella typhimurium och Escherichia coli med eller utan råttleverenzymaktivering vid koncentrationer upp till 10 000 mcg/platta. I in vivo-studier på möss, med ett mikronukleustest och ett kromosomavvikelsetest, observerades inga tecken på en mutagen effekt.
I studier med råttor som fick orala doser på upp till 2000 mg/kg/dag eller intravenösa doser på upp till 200 mg/kg/dag, påverkades inte fertiliteten och reproduktionsförmågan.

Graviditet
Graviditetskategori B
Reproduktionsstudier har utförts på råttor och kaniner vid orala doser på upp till 2000 respektive 500 mg/kg/dag och på båda arterna vid IV-doser på upp till 200 mg/kg/dag, och har inte visat några signifikanta bevis för nedsatt fertilitet eller skada på fostret på grund av PEPCID. Även om inga direkta fostertoxiska effekter har observerats, observerades sporadiska aborter som endast förekom hos mödrar som uppvisade markant minskat födointag hos vissa kaniner vid orala doser på 200 mg/kg/dag (250 gånger den vanliga humana dosen) eller högre. Det finns dock inga adekvata eller välkontrollerade studier på gravida kvinnor. Eftersom reproduktionsstudier på djur inte alltid förutsäger mänskligt svar, bör detta läkemedel endast användas under graviditet om det verkligen behövs.
Ammande mödrar
Studier utförda på digivande råttor har visat att famotidin utsöndras i bröstmjölk. Övergående tillväxtdepression observerades hos unga råttor som di från mödrar som behandlats med maternotoxiska doser på minst 600 gånger den vanliga humana dosen. Famotidin kan detekteras i bröstmjölk. På grund av risken för allvarliga biverkningar hos ammande spädbarn från PEPCID, bör ett beslut fattas om att avbryta amningen eller avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern.
Pediatriska patienter
Användning av PEPCID 20 mg hos pediatriska patienter
Två farmakokinetiska studier på pediatriska patienter 3 månader till 1 års ålder liknar det som ses hos äldre pediatriska patienter (1-15 år) och vuxna . Däremot hade pediatriska patienter 0-3 månaders ålder värden för famotidinclearance som var 2 till 4 gånger lägre än hos äldre pediatriska patienter och vuxna. Dessa studier visar också att den genomsnittliga biotillgängligheten hos pediatriska patienter KLINISK FARMAKOLOGI hos pediatriska patienter , Farmakokinetik och farmakodynamik .)
en dubbelblind, randomiserad studie-utsättningsstudie behandlades 35 pediatriska patienter NEGATIVA REAKTIONER , Pediatriska patienter ).
Dessa studier tyder på att en startdos på 0,5 mg/kg/dos av famotidin oral suspension kan vara till nytta för behandling av GERD i upp till 4 veckor en gång dagligen hos patienter
Pediatriska patienter 1-16 år
Användning av PEPCID 40 mg hos pediatriska patienter i åldern 1-16 år stöds av bevis från adekvata och välkontrollerade studier av PEPCID på vuxna och av följande studier på pediatriska patienter: I publicerade studier på ett litet antal pediatriska patienter 1-15 år, var clearance av famotidin liknande det som ses hos vuxna. Hos pediatriska patienter i åldern 11-15 år var orala doser på 0,5 mg/kg associerade med en medelarea under kurvan (AUC) liknande den som ses hos vuxna behandlade oralt med 40 mg. På liknande sätt var intravenösa doser på 0,5 mg/kg hos pediatriska patienter 1-15 år förknippade med en genomsnittlig AUC liknande den som ses hos vuxna behandlade intravenöst med 40 mg. Begränsade publicerade studier tyder också på att sambandet mellan serumkoncentration och syradämpning är liknande hos pediatriska patienter 1-15 år jämfört med vuxna. Dessa studier föreslår en startdos för pediatriska patienter i åldern 1-16 år enligt följande:
Magsår - 0,5 mg/kg/dag po Vid sänggåendet eller delat bud Upp till 40 mg/dag.
Gastroesofageal refluxsjukdom med eller utan esofagit inklusive erosioner och sår - 1,0 mg/kg/dag po uppdelat bud upp till 40 mg två gånger dagligen
Medan publicerade okontrollerade studier tyder på effektiviteten av famotidin vid behandling av gastroesofageal refluxsjukdom och magsår, är data från pediatriska patienter otillräckliga för att fastställa procentuell respons med dos och behandlingslängd. Därför bör behandlingslängd (inledningsvis baserat på rekommendationer om varaktighet för vuxna) och dos individualiseras baserat på kliniskt svar och/eller pH-bestämning (mag eller matstrupe) och endoskopi. Publicerade okontrollerade kliniska studier på pediatriska patienter har använt doser upp till 1 mg/kg/dag för magsår och 2 mg/kg/dag för GERD med eller utan esofagit inklusive erosioner och sårbildning.
Geriatrisk användning
Av de 4 966 försökspersoner i kliniska studier som behandlades med famotidin, var 488 försökspersoner (9,8 %) 65 år och äldre och 88 försökspersoner (1,7 %) var äldre än 75 år. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre försökspersoner. Större känslighet hos vissa äldre individer kan dock inte uteslutas.
Ingen dosjustering krävs baserat på ålder (se KLINISK FARMAKOLOGI hos vuxna , Farmakokinetik ). Detta läkemedel är känt för att väsentligen utsöndras via njurarna, och risken för toxiska reaktioner på detta läkemedel kan vara större hos patienter med nedsatt njurfunktion. Eftersom äldre patienter är mer benägna att ha nedsatt njurfunktion, bör man vara försiktig vid val av dos, och det kan vara användbart att övervaka njurfunktionen. Dosjustering vid måttligt eller gravt nedsatt njurfunktion är nödvändig (se FÖRSIKTIGHETSÅTGÄRDER , Patienter med måttlig eller svår njurinsufficiens och DOSERING OCH ADMINISTRERING , Dosjustering för patienter med måttlig eller svår njurinsufficiens ).
ÖVERDOS
Biverkningarna i fall av överdosering liknar de biverkningar som förekommer i normal klinisk erfarenhet (se NEGATIVA REAKTIONER ). Orala doser på upp till 640 mg/dag har givits till vuxna patienter med patologiska hypersekretoriska tillstånd utan allvarliga biverkningar. I händelse av överdosering ska behandlingen vara symptomatisk och stödjande. Oabsorberat material ska avlägsnas från mag-tarmkanalen, patienten ska övervakas och stödjande terapi ska användas.
Den orala LD50 för famotidin hos råttor och möss av han- och honkön var större än 3000 mg/kg och den minsta dödliga akuta orala dosen hos hundar översteg 2000 mg/kg. Famotidin gav inte uppenbara effekter vid höga orala doser hos möss, råttor, katter och hundar, men inducerade signifikant anorexi och tillväxtdepression hos kaniner som började med 200 mg/kg/dag oralt. Den intravenösa LD50 av famotidin för möss och råttor varierade från 254-563 mg/kg och den minsta dödliga enstaka IV-dosen hos hundar var cirka 300 mg/kg. Tecken på akut förgiftning hos IV-behandlade hundar var emes, rastlöshet, blekhet i slemhinnor eller rodnad i mun och öron, hypotoni, takykardi och kollaps.
KONTRAINDIKATIONER
Överkänslighet mot någon komponent i dessa produkter. Korskänslighet i denna klass av föreningar har observerats. Därför bör PEPCID 40 mg inte administreras till patienter med en historia av överkänslighet mot andra H2-receptorantagonister.
KLINISK FARMAKOLOGI
Klinisk farmakologi hos vuxna
GI-effekter
PEPCID är en kompetitiv hämmare av histamin H2-receptorer. Den primära kliniskt viktiga farmakologiska aktiviteten av PEPCID 40 mg är hämning av magsekretionen. Både syrakoncentrationen och volymen av magsekretionen undertrycks av PEPCID, medan förändringar i pepsinsekretionen är proportionella mot volymutsöndringen.
Hos normala frivilliga och hyperutsöndrare hämmade PEPCID 20 mg basal och nattlig magsekretion, såväl som utsöndring stimulerad av mat och pentagastrin. Efter oral administrering inträdde den antisekretoriska effekten inom en timme; den maximala effekten var dosberoende och inträffade inom en till tre timmar. Varaktigheten av hämning av sekretion med doser på 20 och 40 mg var 10 till 12 timmar.
Enstaka kvällsdoser på 20 och 40 mg hämmade basal och nattlig syrasekretion hos alla försökspersoner; genomsnittlig nattlig magsyrasekretion hämmades med 86 % respektive 94 % under en period av minst 10 timmar. Samma doser som gavs på morgonen dämpade matstimulerad syrasekretion hos alla försökspersoner. Den genomsnittliga suppressionen var 76 % respektive 84 % 3 till 5 timmar efter administrering och 25 % respektive 30 % 8 till 10 timmar efter administrering. Hos vissa försökspersoner som fick 20 mg dosen försvann dock den antisekretoriska effekten inom 6-8 timmar. Det fanns ingen kumulativ effekt vid upprepade doser. Det nattliga intragastriska pH-värdet höjdes med kvällsdoser på 20 och 40 mg PEPCID till medelvärden på 5,0 respektive 6,4. När PEPCID 40 mg gavs efter frukost, höjdes det basala pH-värdet för matsmältningssystemet dagtid vid 3 och 8 timmar efter 20 eller 40 mg PEPCID 40 mg till cirka 5.
PEPCID 40 mg hade liten eller ingen effekt på fastande eller postprandiala serumgastrinnivåer. Magtömning och exokrina pankreasfunktioner påverkades inte av PEPCID.
Andra effekter
Systemiska effekter av PEPCID i CNS, kardiovaskulära, respiratoriska eller endokrina system noterades inte i kliniska farmakologiska studier. Dessutom noterades inga antiandrogena effekter. (Ser NEGATIVA REAKTIONER .) Serumhormonnivåer, inklusive prolaktin, kortisol, tyroxin (T4) och testosteron, förändrades inte efter behandling med PEPCID.
Farmakokinetik
PEPCID 20 mg absorberas ofullständigt. Biotillgängligheten för orala doser är 40-45%. Biotillgängligheten kan öka något av mat eller något minskad av antacida; dessa effekter har dock ingen klinisk konsekvens. PEPCID genomgår minimal first-pass metabolism. Efter orala doser uppträder maximala plasmanivåer inom 1-3 timmar. Plasmanivåer efter flera doser liknar dem efter enstaka doser. Femton till 20 % av PEPCID 20 mg i plasma är proteinbundet. PEPCID har en eliminationshalveringstid på 2,5-3,5 timmar. PEPCID elimineras via njurar (65-70%) och metabola (30-35%) vägar. Njurclearance är 250-450 ml/min, vilket indikerar viss tubulär utsöndring. Tjugofem till 30 % av en oral dos och 65-70 % av en intravenös dos återfinns i urinen som oförändrad förening. Den enda metaboliten som identifieras hos människan är S-oxiden.
Det finns ett nära samband mellan kreatininclearance-värden och eliminationshalveringstiden för PEPCID. Hos patienter med allvarlig njurinsufficiens, dvs kreatininclearance mindre än 10 ml/min, kan eliminationshalveringstiden för PEPCID överstiga 20 timmar och justering av dos eller doseringsintervall vid måttlig och svår njurinsufficiens kan vara nödvändig (se FÖRSIKTIGHETSÅTGÄRDER , DOSERING OCH ADMINISTRERING ).
Hos äldre patienter finns inga kliniskt signifikanta åldersrelaterade förändringar i farmakokinetiken för PEPCID. Hos äldre patienter med nedsatt njurfunktion kan dock clearance av läkemedlet vara minskat (se FÖRSIKTIGHETSÅTGÄRDER , Geriatrisk användning ).
Kliniska studier
Duodenalsår
I en amerikansk multicenter, dubbelblind studie på öppenvårdspatienter med endoskopiskt bekräftat duodenalsår, jämfördes oralt administrerat PEPCID med placebo. Som visas i tabell 1 var 70 % av patienterna som behandlades med PEPCID 40 mg hs helade senast vecka 4.
Patienter som inte läkts i vecka 4 fortsatte i studien. Vid vecka 8 hade 83 % av patienterna behandlade med PEPCID läkt jämfört med 45 % av patienterna som behandlades med placebo. Incidensen av sårläkning med PEPCID var signifikant högre än med placebo vid varje tidpunkt baserat på andelen endoskopiskt bekräftade läkta sår.
I denna studie var tiden till lindring av dag- och nattlig smärta signifikant kortare för patienter som fick PEPCID än för patienter som fick placebo; patienter som fick PEPCID tog också mindre antacida än patienterna som fick placebo.
Långvarig underhållsbehandling av duodenalsår
PEPCID 40 mg, 20 mg pohs, jämfördes med placebo-hs som underhållsbehandling i två dubbelblinda multicenterstudier av patienter med endoskopiskt bekräftade läkta duodenalsår. I den amerikanska studien var den observerade ulcusincidensen inom 12 månader hos patienter behandlade med placebo 2,4 gånger högre än hos patienter som behandlades med PEPCID. De 89 patienter som behandlades med PEPCID hade en kumulativ observerad sårincidens på 23,4 % jämfört med en observerad sårincidens på 56,6 % hos de 89 patienter som fick placebo (p
Magsår
både en amerikansk och en internationell multicenter jämfördes dubbelblind studie på patienter med endoskopiskt bekräftat aktivt benignt magsår, oralt administrerat PEPCID 20 mg, 40 mg hs, med placebo hs Antacida tillåts under studierna, men konsumtionen var inte signifikant annorlunda mellan PEPCID- och placebogrupperna. Som framgår av tabell 2 var förekomsten av sårläkning (bortfall räknas som oläkta) med PEPCID 20 mg statistiskt signifikant bättre än placebo vid veckorna 6 och 8 i den amerikanska studien och vid veckorna 4, 6 och 8 i den internationella studien, baserat på på antalet sår som läkt, bekräftat med endoskopi.
Tiden till fullständig lindring av dag- och nattsmärta var statistiskt signifikant kortare för patienter som fick PEPCID 20 mg än för patienter som fick placebo; I ingen av studierna fanns det dock någon statistiskt signifikant skillnad i andelen patienter vars smärta var lindrad i slutet av studien (vecka 8).
Gastroesofageal refluxsjukdom (GERD)
Oralt administrerat PEPCID jämfördes med placebo i en amerikansk studie som inkluderade patienter med symtom på GERD och utan endoskopiska tecken på erosion eller sårbildning i matstrupen. PEPCID 20 mg två gånger dagligen var statistiskt signifikant överlägsen 40 mg hs och placebo när det gäller att ge ett framgångsrikt symtomatiskt resultat, definierat som måttlig eller utmärkt förbättring av symtomen (tabell 3).
Efter två veckors behandling observerades symtomatisk framgång hos en större andel av patienterna som tog PEPCID 20 mg två gånger dagligen jämfört med placebo (p ≤ 0,01).
Symtomatisk förbättring och läkning av endoskopiskt verifierad erosion och sårbildning studerades i ytterligare två försök. Läkning definierades som fullständig upplösning av alla erosioner eller sår som är synliga med endoskopi. Den amerikanska studien som jämförde PEPCID 40 mg pobid med placebo och PEPCID 20 mg pobid visade en signifikant högre procentuell läkning för PEPCID 40 mg två gånger i veckan vid vecka 6 och 12 (tabell 4).
Jämfört med placebo hade patienter som fick PEPCID snabbare lindring av halsbränna dag och natt och en större andel av patienterna upplevde fullständig lindring av halsbränna på natten. Dessa skillnader var statistiskt signifikanta.
I den internationella studien, när PEPCID 40 mg pobid jämfördes med ranitidin 150 mg pobid, observerades en statistiskt signifikant högre procentandel av läkning med PEPCID 40 mg två gånger dagligen vid vecka 12 (tabell 5). Det fanns dock ingen signifikant skillnad mellan behandlingarna i symtomlindring.
Patologiska hypersekretoriska tillstånd (t.ex. Zollinger-Ellisons syndrom, multipla endokrina adenom)
I studier av patienter med patologiska hypersekretoriska tillstånd såsom Zollinger-Ellisons syndrom med eller utan multipla endokrina adenom, hämmade PEPCID signifikant magsyrasekretionen och kontrollerade associerade symtom. Oralt administrerade doser från 20 till 160 mg q 6 timmar bibehöll basalsyrasekretionen under 10 mEq/timme; initialdoserna titrerades till individuella patientbehov och efterföljande justeringar var nödvändiga med tiden hos vissa patienter. PEPCID 40 mg tolererades väl vid dessa höga dosnivåer under längre perioder (mer än 12 månader) hos åtta patienter, och inga fall rapporterades av gynekomasti, ökade prolaktinnivåer eller impotens som ansågs bero på läkemedlet.
Klinisk farmakologi hos pediatriska patienter
Farmakokinetik
Tabell 6 presenterar farmakokinetiska data från kliniska prövningar och en publicerad studie på pediatriska patienter (
Plasmaclearance reduceras och eliminationshalveringstiden förlängs hos pediatriska patienter 0-3 månaders ålder jämfört med äldre pediatriska patienter. De farmakokinetiska parametrarna för pediatriska patienter, åldrar > 3 månader-15 år, är jämförbara med de som erhålls för vuxna.
Biotillgänglighetsstudier av 8 pediatriska patienter (11-15 år) visade en genomsnittlig oral biotillgänglighet på 0,5 jämfört med vuxenvärden på 0,42 till 0,49. Orala doser på 0,5 mg/kg uppnådde AUC på 645 ± 249 ng-tim/ml och 580 ± 60 ng-tim/ml hos pediatriska patienter
Farmakodynamik
Farmakodynamiken för famotidin utvärderades hos 5 pediatriska patienter i åldern 2-13 år med användning av sigmoid Emax-modellen. Dessa data tyder på att sambandet mellan serumkoncentrationen av famotidin och magsyrasuppression liknar det som observerades i en studie av vuxna (tabell 7).
Fem publicerade studier (tabell 8) undersökte effekten av famotidin på magsäckens pH och varaktigheten av syrasuppression hos pediatriska patienter. Även om varje studie hade en annan design, sammanfattas syraundertryckningsdata över tid enligt följande:
Effektdurationen av famotidin IV 0,5 mg/kg på magsäckens pH och syrasuppression visades i en studie vara längre hos pediatriska patienter
PATIENTINFORMATION
Ingen information lämnas. Vänligen se FÖRSIKTIGHETSÅTGÄRDER sektion.
