Nimotop 30mg Nimodipine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Nimotop 30mg och hur används det?
Nimotop är ett receptbelagt läkemedel som används för att behandla symtom på aneurysm (subaraknoidal blödning). Nimotop kan användas ensamt eller tillsammans med andra läkemedel.
Nimotop tillhör en klass av läkemedel som kallas kalciumkanalblockerare; Neurologi, Övrigt; Kalciumkanalblockerare, dihydrofyridin.
Det är inte känt om Nimotop 30 mg är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Nimotop?
Nimotop kan orsaka allvarliga biverkningar inklusive:
- nässelfeber,
- svårt att andas,
- svullnad av ansikte, läppar, tunga eller svalg,
- yrsel,
- snabb eller långsam puls, och
- svullnad eller dina anklar eller fötter
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Nimotop inkluderar:
- lågt blodtryck (känner sig lätt i huvudet),
- illamående,
- orolig mage,
- långsamma hjärtslag och
- träningsvärk
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Nimotop. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Administrera INTE NIMOTOP (nimodipin) INTRAVENÖST ELLER PÅ ANDRA PARENTERAL VÄG. DÖDSFALL OCH ALLVARLIGA, LIVSHOTANDE BIVERKNINGAR HAR INKOMST NÄR INNEHÅLLET AV NIMOTOP (nimodipin) KAPSLAR HAR INJICERATS PARENTERALT (se VARNINGAR och DOSERING OCH ADMINISTRERING).
BESKRIVNING
Nimotop® (nimodipin) tillhör den klass av farmakologiska medel som kallas kalciumkanalblockerare. Nimodipin är isopropyl-2-metoxietyl-1,4-dihydro-2,6-dimetyl-4-(m-nitrofenyl)-3,5-pyridindikarboxylat. Den har en molekylvikt på 418,5 och en molekylformel av C21H26N2O7. Strukturformeln är:
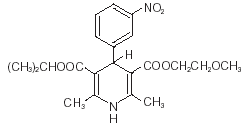
Nimodipin är ett gult kristallint ämne, praktiskt taget olösligt i vatten.
NIMOTOP® (nimodipin) kapslar är formulerade som mjuka gelatinkapslar för oral administrering. Varje vätskefylld kapsel innehåller 30 mg nimodipin i en vehikel av glycerin, pepparmyntsolja, renat vatten och polyetylenglykol 400. Det mjuka gelatinkapselskalet innehåller gelatin, glycerin, renat vatten och titandioxid.
INDIKATIONER
Nimotop® (nimodipin) är indicerat för förbättring av neurologiskt resultat genom att minska förekomsten och svårighetsgraden av ischemiska brister hos patienter med subaraknoidal blödning från brustna intrakraniella bäraneurysm oavsett deras post-ictus neurologiska tillstånd (dvs. Hunt och Hess grad IV).
DOSERING OCH ADMINISTRERING
Administrera INTE NIMOTOP (nimodipin) KAPSLAR INTRAVENÖST ELLER PÅ ANDRA PARENTERAL VÄG (se VARNINGAR). Om Nimotop (nimodipin) oavsiktligt administreras intravenöst, kan kliniskt signifikant hypotoni kräva kardiovaskulärt stöd med pressormedel. Specifika behandlingar för överdosering av kalciumkanalblockerare bör också ges omedelbart.
Nimotop (nimodipin) ges oralt i form av elfenbensfärgat, mjukt gelatin 30 mg kapslar för subaraknoidal blödning.
Den orala dosen är 60 mg (två 30 mg kapslar) var 4:e timme under 21 dagar i följd, helst inte mindre än en timme före eller två timmar efter måltid. Oral Nimotop® (nimodipin)-behandling bör påbörjas inom 96 timmar efter subaraknoidalblödningen.
Om kapseln inte kan sväljas, t.ex. vid operationstillfället, eller om patienten är medvetslös, ska ett hål göras i båda ändarna av kapseln med en 18 gauge nål och kapselns innehåll extraheras i en spruta. En parenteral spruta kan användas för att extrahera vätskan inuti kapseln, men vätskan ska alltid överföras till en spruta som inte kan ta emot en nål och som är avsedd för administrering oralt eller via en naso-gastrisk sond eller PEG. För att hjälpa till att minimera administreringsfel, rekommenderas att sprutan som används för administrering är märkt "Not for IV Use". Innehållet ska sedan tömmas i patientens in situnaso-gastriska sond och sköljas ner i röret med 30 ml normal koksaltlösning (0,9%). Effekten och säkerheten för denna administreringsmetod har inte visats i kliniska prövningar.
Patienter med levercirros har avsevärt minskat clearance och ungefär fördubblat Cmax. Doseringen bör minskas till 30 mg var 4:e timme, med noggrann övervakning av blodtryck och hjärtfrekvens.
HUR LEVERERAS
Varje elfenbensfärgad, mjuk gelatin NIMOTOP® (nimodipin) kapsel är präglad med ordet Nimotop 30 mg och innehåller 30 mg nimodipin. 30 mg kapslarna är förpackade i endosfoliepåsar och levereras i kartonger innehållande 100 kapslar. Produkten finns också i barnsäkra enhetsdos säkerhetsfoliepåsar innehållande 30 kapslar per kartong. Kapslarna ska förvaras i tillverkarens originalfolieförpackning vid 25°C (77°F), utflykter tillåtna till 15-30°C (59-86°F) [Se USP-kontrollerad rumstemperatur.]
Kapslar bör skyddas från ljus och frysning.
Distribueras av: Bayer Pharmaceuticals Corporation, 400 Morgan Lane, West Haven, CT 06516. Tillverkad av: Catalent Pharma Solutions St. Petersburg, FL 33716. FDA revisionsdatum: 2006-01-20
BIEFFEKTER
Biverkningar rapporterades av 92 av 823 patienter med subaraknoidal blödning (11,2%) som fick nimodipin. Den vanligaste rapporterade biverkningen var sänkt blodtryck hos 4,4 % av dessa patienter. Tjugonio av 479 (6,1 %) placebobehandlade patienter rapporterade också biverkningar. De händelser som rapporterats med en frekvens som är större än 1 % visas nedan per dos.
DOS q4h Antal patienter (%) Nimodipin
Det fanns inga andra biverkningar rapporterade av patienterna som fick 0,35 mg/kg q4h, 30 mg q4h eller 120 mg q4h. Biverkningar med en incidens på mindre än 1 % i dosgruppen 60 mg q4h var: hepatit; klåda; gastrointestinala blödningar; trombocytopeni; anemi; hjärtklappning; kräkningar; spolning; diafores; väsande andning; fenytointoxicitet; yrsel; yrsel; rebound vasospasm; gulsot; hypertoni; hematom.
Biverkningar med en incidens på mindre än 1 % i dosgruppen 90 mg q4h var: klåda, gastrointestinala blödningar; trombocytopeni; neurologisk försämring; kräkningar; diafores; hjärtsvikt; hyponatremi; minskat antal blodplättar; disseminerad intravaskulär koagulation; djup ventrombos.
Som framgår av tabellen inkluderade biverkningar som uppträder relaterade till nimodipinanvändning baserat på ökad incidens med högre dos eller högre frekvens jämfört med placebokontroll sänkt blodtryck, ödem och huvudvärk som är kända farmakologiska effekter av kalciumkanalblockerare. Det måste dock noteras att SAH ofta åtföljs av förändringar i medvetandet som leder till underrapportering av negativa upplevelser. Patienter som fick nimodipin i kliniska prövningar för andra indikationer rapporterade rodnad (2,1 %), huvudvärk (4,1 %) och vätskeretention (0,3 %), typiska svar på kalciumkanalblockerare. Som en kalciumkanalblockerare kan nimodipin ha potential att förvärra hjärtsvikt hos känsliga patienter eller störa AV-överledning, men dessa händelser observerades inte.
Inga kliniskt signifikanta effekter på hematologiska faktorer, njur- eller leverfunktion eller kolhydratmetabolism har orsakats av oralt nimodipin. Enstaka fall av icke-fastande förhöjda serumglukosnivåer (0,8%), förhöjda LDH-nivåer (0,4%), minskat antal trombocyter (0,3%), förhöjda alkaliska fosfatasnivåer (0,2%) och förhöjda SGPT-nivåer (0,2%) har rapporterats sällan.

Narkotikamissbruk och beroende
Det har inte rapporterats några fall av drogmissbruk eller beroende av Nimotop® (nimodipin).
LÄKEMEDELSINTERAKTIONER
Det är möjligt att den kardiovaskulära effekten av andra kalciumkanalblockerare kan förstärkas genom tillsats av Nimotop® (nimodipin).
I Europa observerades att Nimotop® (nimodipin) emellanåt förstärker effekten av antihypertensiva föreningar som tas samtidigt av patienter som lider av hypertoni; detta fenomen observerades inte i nordamerikanska kliniska prövningar.
En studie med åtta friska frivilliga har visat en 50 % ökning av genomsnittliga maximala nimodipinplasmakoncentrationer och en 90 % ökning av medelarea under kurvan, efter en veckas kur med cimetidin med 1 000 mg/dag och nimodipin vid 90 mg/dag . Denna effekt kan förmedlas av den kända hämningen av hepatisk cytokrom P-450 av cimetidin, vilket kan minska första-passage-metabolismen av nimodipin.
VARNINGAR
DÖDSFALL PÅ GRUND AV OAVSIKTLIG INTRAVENÖS ADMINISTRERING: Administrera INTE NIMOTOP (nimodipin) INTRAVENÖST ELLER PÅ ANDRA PARENTERAL VÄG. DÖDSFALL OCH ALLVARLIGA, LIVSHOTANDE BIVERKNINGAR, INKLUSIVE HJÄRTSTILL, Hjärt- och kärlkollaps, HYPOTENSION OCH BRADYKARDI, HAR INKOMST NÄR INNEHÅLLET I NIMOTOP (NIMODIPIN) KAPSELAR HAR HALT ADMINOS.
FÖRSIKTIGHETSÅTGÄRDER
Allmän: Blodtryck: Nimodipin har de hemodynamiska effekter som förväntas av en kalciumkanalblockerare, även om de i allmänhet inte är markanta. Emellertid har intravenös administrering av innehållet i Nimotop (nimodipin) kapslar resulterat i allvarliga negativa konsekvenser inklusive död, hjärtstillestånd, kardiovaskulär kollaps, hypotoni och bradykardi. Hos patienter med subaraknoidal blödning som fick Nimotop® (nimodipin) i kliniska studier rapporterades cirka 5 % ha haft blodtryckssänkning och cirka 1 % lämnade studien på grund av detta (alla kunde inte hänföras till nimodipin). Trots det bör blodtrycket övervakas noggrant under behandling med Nimotop® (nimodipin) baserat på dess kända farmakologi och de kända effekterna av kalciumkanalblockerare. (ser VARNINGAR och DOSERING OCH ADMINISTRERING )
Leversjukdom: Metabolismen av Nimotop® (nimodipin) är nedsatt hos patienter med nedsatt leverfunktion. Sådana patienter bör få sitt blodtryck och puls övervakas noggrant och bör ges en lägre dos (se DOSERING OCH ADMINISTRERING ).
Intestinal pseudo-obstruktion och ileus har rapporterats i sällsynta fall hos patienter som behandlats med nimodipin. Något orsakssamband har inte fastställts. Tillståndet har svarat på konservativ ledning.
Interaktioner med laboratorietest: Ingen känd.
Karcinogenes, mutagenes, försämrad fertilitet: en tvåårig studie observerades högre incidens av adenokarcinom i livmodern och Leydig-celladenom i testiklarna hos råttor som fick en diet innehållande 1800 ppm nimodipin (motsvarande 91 till 121 mg/kg/dag nimodipin) än hos placebokontroller. . Skillnaderna var dock inte statistiskt signifikanta och de högre frekvenserna låg väl inom det historiska kontrollintervallet för dessa tumörer i Wistar-stammen.
Nimodipin visade sig inte vara cancerframkallande i en 91-veckors musstudie men den höga dosen på 1800 ppm nimodipin i foder (546 till 774 mg/kg/dag) förkortade djurens förväntade livslängd. Mutagenicitetsstudier, inklusive Ames, mikrokärnan och dominant letala tester var negativa. Nimodipin försämrade inte fertiliteten och den allmänna reproduktionsförmågan hos Wistar-han- och honråttor efter orala doser på upp till 30 mg/kg/dag när det administrerades dagligen i mer än 10 veckor till hanarna och 3 veckor till honorna före parning och fortsatte. till dag 7 av graviditeten. Denna dos i en råtta är cirka 4 gånger den ekvivalenta kliniska dosen på 60 mg q4h hos en 50 kg patient.
Graviditet: Dräktighetskategori C. Nimodipin har visat sig ha en teratogen effekt hos Himalayakaniner. Incidensen av missbildningar och hämmade foster ökade vid orala doser på 1 och 10 mg/kg/dag administrerade (genom sondmatning) från dag 6 till och med dag 18 av graviditeten men inte vid 3,0 mg/kg/dag i en av två identiska kaninstudier. I den andra studien sågs en ökad förekomst av hämmade foster vid 1,0 mg/kg/dag men inte vid högre doser. Nimodipin var embryotoxiskt och orsakade resorption och hämmad tillväxt av foster hos Long Evans-råttor vid 100 mg/kg/dag administrerat genom sondmatning från dag 6 till dag 15 av graviditeten. I två andra råttstudier var doser på 30 mg/kg/dag nimodipin administrerade genom sondmatning från dag 16 av dräktigheten och fortsatte tills avlivning (dag 20 av graviditeten eller dag 21 post partum) associerade med högre incidens av skelettvariationer, hämmade foster och dödfödslar men inga missbildningar. Det finns inga adekvata och välkontrollerade studier på gravida kvinnor för att direkt bedöma effekten på mänskliga foster. Nimodipin ska endast användas under graviditet om den potentiella nyttan överväger den potentiella risken för fostret.
Ammande mödrar: Nimodipin och/eller dess metaboliter har visats förekomma i råttmjölk i koncentrationer som är mycket högre än i moderns plasma. Det är inte känt om läkemedlet utsöndras i modersmjölk. Eftersom många läkemedel utsöndras i bröstmjölk, rekommenderas ammande mödrar att inte amma sina barn när de tar läkemedlet.
Pediatrisk användning: Säkerhet och effektivitet hos barn har inte fastställts.
Geriatrisk användning: Kliniska studier av nimodipin inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. I allmänhet bör dosering till äldre patienter vara försiktig, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och samtidig sjukdom eller annan läkemedelsbehandling.
ÖVERDOS
Det har inte rapporterats om överdosering efter oral administrering av Nimotop® (nimodipin). Symtom på överdosering förväntas vara relaterade till kardiovaskulära effekter såsom överdriven perifer vasodilatation med markant systemisk hypotoni. Kliniskt signifikant hypotoni på grund av Nimotop® (nimodipin) överdosering kan kräva aktivt kardiovaskulärt stöd med pressormedel. Specifika behandlingar för överdosering av kalciumkanalblockerare bör också ges omedelbart. Eftersom Nimotop® (nimodipin) är starkt proteinbundet är det inte troligt att dialys är till nytta.
KONTRAINDIKATIONER
Ingen känd.
KLINISK FARMAKOLOGI
Handlingsmekanism: Nimodipin är en kalciumkanalblockerare. De kontraktila processerna hos glatta muskelceller är beroende av kalciumjoner, som kommer in i dessa celler under depolarisering som långsamma joniska transmembranströmmar. Nimodipin hämmar kalciumjonöverföringen till dessa celler och hämmar därmed sammandragningar av glatt muskulatur i kärlen. I djurförsök hade nimodipin en större effekt på cerebrala artärer än på artärer på andra ställen i kroppen, kanske för att det är mycket lipofilt, vilket gör att det kan passera blod-hjärnbarriären; koncentrationer av nimodipin så höga som 12,5 ng/ml har upptäckts i cerebrospinalvätskan hos nimodipinbehandlade subaraknoidala blödningspatienter (SAH). Den exakta verkningsmekanismen för nimodipin hos människor är okänd. Även om de kliniska studierna som beskrivs nedan visar en gynnsam effekt av nimodipin på svårighetsgraden av neurologiska störningar orsakade av cerebral vasospasm efter SAH, finns det inga arteriografiska bevis för att läkemedlet antingen förebygger eller lindrar spasmen i dessa artärer. Huruvida den använda arteriografiska metodiken var tillräcklig för att upptäcka en kliniskt betydelsefull effekt, om någon, på vasospasm är dock okänt.
Farmakokinetik och metabolism: Hos människa absorberas nimodipin snabbt efter oral administrering och maximala koncentrationer uppnås vanligtvis inom en timme. Den terminala halveringstiden för eliminering är cirka 8 till 9 timmar men tidigare elimineringshastigheter är mycket snabbare, vilket motsvarar en halveringstid på 1-2 timmar; en konsekvens är behovet av frekvent (var 4:e timme) dosering. Det fanns inga tecken på ackumulering när nimodipin gavs tre gånger om dagen i sju dagar. Nimodipin är till över 95 % bundet till plasmaproteiner. Bindningen var koncentrationsoberoende över intervallet 10 ng/ml till 10 µg/ml. Nimodipin elimineras nästan uteslutande i form av metaboliter och mindre än 1 % återfinns i urinen som oförändrat läkemedel. Många metaboliter, som alla är antingen inaktiva eller betydligt mindre aktiva än moderföreningen, har identifierats. På grund av en hög first-pass-metabolism är biotillgängligheten av nimodipin i genomsnitt 13 % efter oral administrering. Biotillgängligheten är signifikant ökad hos patienter med levercirros, med Cmax ungefär dubbelt så högt som för normala, vilket gör det nödvändigt att sänka dosen hos denna patientgrupp (se DOSERING OCH ADMINISTRERING ). I en studie med 24 friska frivilliga män, resulterade administrering av nimodipinkapslar efter en standardfrukost i en 68 % lägre maximal plasmakoncentration och 38 % lägre biotillgänglighet jämfört med dosering under fasta.
I en enskild parallellgruppsstudie med 24 äldre försökspersoner (59-79 år) och 24 yngre försökspersoner (22-40 år), var den observerade AUC och Cmax för nimodipin ungefär 2 gånger högre i den äldre populationen jämfört med den yngre studien försökspersoner efter oral administrering (given som en engångsdos på 30 mg och doserad till steady-state med 30 mg tid i 6 dagar). Det kliniska svaret på dessa åldersrelaterade farmakokinetiska skillnader ansågs dock inte vara signifikant. (Ser FÖRSIKTIGHETSÅTGÄRDER : Geriatrisk användning.)
Kliniska tester: Nimodipin har i 4 randomiserade, dubbelblinda, placebokontrollerade studier visat sig minska svårighetsgraden av neurologiska störningar till följd av vasospasm hos patienter som nyligen har haft en subaraknoidal blödning (SAH). I försöken användes doser från 20-30 mg till 90 mg var 4:e timme, med läkemedel som gavs i 21 dagar i 3 studier och i minst 18 dagar i den andra. Tre av de fyra försöken följde patienter i 3-6 månader. Tre av studierna studerade relativt väl patienter, med alla eller de flesta patienter i Hunt och Hess grad I - III (i huvudsak fria från fokala brister efter den initiala blödningen) den fjärde studerade mycket sjukare patienter, Hunt och Hess grad III - V. Två studier , en amerikansk, en fransk, var likartade i design, med relativt oförhindrade SAH-patienter randomiserade till nimodipin eller placebo. I var och en gjordes en bedömning av om eventuellt sent utvecklat underskott berodde på spasmer eller andra orsaker, och underskotten graderades. Båda studierna visade signifikant färre allvarliga brister på grund av spasm i nimodipingruppen; den andra (franska) studien visade färre spasmrelaterade brister av alla svårighetsgrader. Ingen effekt sågs på underskott som inte var relaterat till spasm.
En tredje, stor, studie utfördes i Storbritannien på SAH-patienter med alla svårighetsgrader (men 89 % var i grad I-III). Nimodipin doserades 60 mg var fjärde timme. Resultaten definierades inte som spasmrelaterade eller inte, men det fanns en signifikant minskning av den totala frekvensen av infarkt och allvarligt invalidiserande neurologiskt utfall efter 3 månader:
En kanadensisk studie gick in på mycket sjukare patienter (Hunt och Hess Grade III-V), som hade en hög frekvens av dödsfall och funktionshinder, och använde en dos på 90 mg var fjärde timme, men liknade i övrigt de två första studierna. Analys av fördröjda ischemiska brister, av vilka många beror på spasmer, visade en signifikant minskning av spasmrelaterade brister. Bland analyserade patienter (72 nimodipin, 82 placebo) fanns följande resultat.
När data kombinerades för de kanadensiska och brittiska studierna var behandlingsskillnaden på framgångsfrekvens (dvs. god återhämtning) på Glasgow Outcome Scale 25,3 % (nimodipin) jämfört med 10,9 % (placebo) för Hunt och Hess grad IV eller V . Tabellen nedan visar att nimodipin tenderar att förbättra god återhämtning av SAH-patienter med dålig neurologisk status post-ictus, samtidigt som det minskar antalet med allvarliga funktionshinder och vegetativ överlevnad.
En dosvarierande studie som jämförde 30, 60 och 90 mg doser fann en generellt låg frekvens av spasmrelaterade neurologiska underskott men inget dosresponssamband.
PATIENTINFORMATION
Ingen information lämnas. Vänligen se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER sektioner.
