Micardis 20mg, 40mg, 80mg Telmisartan Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Micardis 40mg och hur används det?
Micardis är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni) och för att minska risken för hjärt-kärlsjukdomar som stroke och hjärtinfarkt. Micardis 20mg kan användas ensamt eller tillsammans med andra läkemedel.
Micardis 80mg tillhör en klass av läkemedel som kallas ARB.
Det är inte känt om Micardis är säkert och effektivt för barn yngre än 18 år.
Vilka är de möjliga biverkningarna av Micardis?
Micardis 80mg kan orsaka allvarliga biverkningar inklusive:
- yrsel,
- svullnad,
- snabb viktökning,
- illamående,
- svaghet,
- pirrande känsla,
- bröstsmärta,
- oregelbundna hjärtslag och
- förlust av rörelse
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Micardis inkluderar:
- Täppt i näsan,
- sinus smärta,
- ryggont, och
- diarre
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Micardis. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
FETAL TOXICITET
- När graviditet upptäcks, avbryt MICARDIS 40mg så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
- Läkemedel som verkar direkt på renin-angiotensinsystemet kan orsaka skador och dödsfall för fostret under utveckling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
BESKRIVNING
MICARDIS 40mg är anon-peptid angiotensin II-receptor (typ AT1) antagonist.
Telmisartan beskrivs kemiskt som 4'-[(1,4'-dimetyl-2'-propyl[2,6'-bi-1H-bensimidazol]-1'-yl)metyl ]-[1,1'-bifenyl]-2-karboxylsyra. Dess empiriska formel är C33H30N4O2, dess molekylvikt är 514,63 och dess strukturformler:
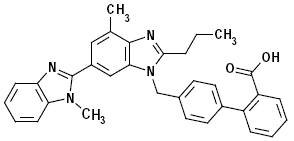
Telmisartan är ett vitt till svagt gulaktigt fast ämne. Det är praktiskt taget olösligt i vatten och i pH-intervallet 3 till 9, svårlösligt i stark syra (förutom olösligt i saltsyra) och lösligt i stark bas.
MICARDIS 20 mg finns som tabletter för oral administrering, innehållande 20 mg, 40 mg eller 80 mg telmisartan. Tabletterna innehåller följande inaktiva ingredienser: natriumhydroxid, meglumin, povidon, sorbitol och magnesiumstearat. MICARDIS tabletter är hygroskopiska och kräver skydd mot fukt.
INDIKATIONER
MICARDIS HCT (telmisartan och hydroklortiazid) är indicerat för behandling av hypertoni för att sänka blodtrycket. Sänkning av blodtrycket minskar risken för dödliga och icke-dödliga kardiovaskulära händelser, främst stroke och hjärtinfarkt. Dessa fördelar har setts i kontrollerade prövningar av antihypertensiva läkemedel från en mängd olika farmakologiska klasser inklusive de klasser som detta läkemedel huvudsakligen tillhör. Det finns inga kontrollerade studier som visar riskreduktion med MICARDIS HCT.
Kontroll av högt blodtryck bör vara en del av omfattande kardiovaskulär riskhantering, inklusive, när så är lämpligt, lipidkontroll, diabetesbehandling, antitrombotisk behandling, rökavvänjning, träning och begränsat natriumintag. Många patienter kommer att behöva mer än ett läkemedel för att uppnå blodtrycksmål. För specifika råd om mål och hantering, se publicerade riktlinjer, såsom de från National High Blood Pressure Education Programs Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Många blodtryckssänkande läkemedel, från en mängd olika farmakologiska klasser och med olika verkningsmekanismer, har i randomiserade kontrollerade studier visats minska kardiovaskulär sjuklighet och mortalitet, och man kan dra slutsatsen att det är blodtryckssänkning och inte någon annan farmakologisk egenskap hos drogerna, som till stor del är ansvarig för dessa fördelar. Den största och mest konsekventa fördelen med kardiovaskulära resultat har varit en minskning av risken för stroke, men minskningar av hjärtinfarkt och kardiovaskulär mortalitet har också setts regelbundet.
Förhöjt systoliskt eller diastoliskt tryck orsakar ökad kardiovaskulär risk, och den absoluta riskökningen per mmHg är större vid högre blodtryck, så att även måttliga minskningar av svår hypertoni kan ge betydande fördelar. Relativ riskreduktion från blodtryckssänkning är likartad i populationer med varierande absolut risk, så den absoluta fördelen är större hos patienter som löper högre risk oberoende av deras hypertoni (till exempel patienter med diabetes eller hyperlipidemi), och sådana patienter kan förväntas att dra nytta av mer aggressiv behandling till ett lägre blodtrycksmål.
Vissa blodtryckssänkande läkemedel har mindre blodtryckseffekter (som monoterapi) hos svarta patienter, och många blodtryckssänkande läkemedel har ytterligare godkända indikationer och effekter (t.ex. på angina, hjärtsvikt eller diabetisk njursjukdom). Dessa överväganden kan styra valet av terapi [se Kliniska studier ].
MICARDIS 40mg HCT är inte indicerat för initial behandling för behandling av hypertoni [se DOSERING OCH ADMINISTRERING ].
MICARDIS HCT kan användas ensamt eller i kombination med andra antihypertensiva medel.
DOSERING OCH ADMINISTRERING
Doseringsinformation
Inled en patient vars blodtryck inte är tillräckligt kontrollerat med telmisartan monoterapi 80 mg på MICARDIS 40 mg HCT, 80 mg/12,5 mg en gång dagligen. Dosen kan vid behov titreras upp till 160 mg/25 mg efter 2 till 4 veckor.
Initiera en patient vars blodtryck inte kontrolleras tillräckligt med 25 mg hydroklortiazid en gång dagligen, eller är kontrollerat men som upplever hypokalemi med denna behandling med MICARDIS HCT 80 mg/12,5 mg en gång dagligen. Dosen kan vid behov titreras upp till 160 mg/25 mg efter 2 till 4 veckor.
Patienter titrerade till de individuella komponenterna (telmisartan och hydroklortiazid) kan istället få motsvarande dos av MICARDIS 20 mg HCT.
MICARDIS 20 mg HCT kan administreras tillsammans med andra antihypertensiva läkemedel.
Dosjustering för nedsatt leverfunktion
Initiera patienter med gallvägsobstruktiva störningar eller leverinsufficiens under noggrann medicinsk övervakning med kombinationen 40 mg/12,5 mg. MICARDIS 40 mg HCT tabletter rekommenderas inte för patienter med gravt nedsatt leverfunktion [se Användning i specifika populationer och KLINISK FARMAKOLOGI ].
Viktiga administrationsinstruktioner
MICARDIS HCT tabletter ska inte tas bort från blister förrän omedelbart före administrering.
HUR LEVERERAS
Doseringsformer och styrkor
- 40 mg/12,5 mg, röda och vita tabletter märkta med Boehringer Ingelheim-logotypen och H4
- 80 mg/12,5 mg, röda och vita tabletter märkta med Boehringer Ingelheim-logotypen och H8
- 80 mg/25 mg, gula och vita tabletter märkta med Boehringer Ingelheim-logotypen och H9
Förvaring Och Hantering
MICARDIS 20mg HCT finns i tre styrkor som bikonvexa tvålagers, avlånga, obelagda tabletter innehållande telmisartan och hydroklortiazid:
- 40 mg/12,5 mg tablett: rött och vitt (kan innehålla röda fläckar) märkta med Boehringer Ingelheim-företagssymbolen och H4; individuellt blisterförseglade i kartonger med 30 tabletter som 3 x 10 kort ( NDC 0597-0043-37)
- 80 mg/12,5 mg tablett: rött och vitt (kan innehålla röda fläckar) märkta med Boehringer Ingelheim-företagssymbolen och H8; individuellt blisterförseglade i kartonger med 30 tabletter som 3 x 10 kort ( NDC 0597-0044-37)
- 80 mg/25 mg tablett: gult och vitt (kan innehålla gula fläckar) märkta med Boehringer Ingelheim-företagssymbolen och H9; individuellt blisterförseglade i kartonger med 30 tabletter som 3 x 10 kort ( NDC 0597-0042-37)
Lagring
Förvara vid 25°C (77°F); utflykter tillåtna till 15°C-30°C (59°F-86°F) [se USP-kontrollerad rumstemperatur]. Tabletter ska inte tas bort från blister förrän omedelbart före administrering.
Distribueras av: Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 USA. Reviderad: oktober 2018
BIEFFEKTER
Följande biverkningar diskuteras på andra ställen i märkningen:
- Hypotoni [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Nedsatt njurfunktion [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Elektrolyter och metabola störningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska studier utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska studierna av ett läkemedel inte direkt jämföras med frekvensen i de kliniska studierna av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
MICARDIS HCT har utvärderats för säkerhet hos fler än 1700 patienter, inklusive 716 behandlade för hypertoni i mer än 6 månader och 420 under mer än 1 år. Biverkningar har begränsats till de som tidigare har rapporterats med telmisartan och/eller hydroklortiazid.
Biverkningar som uppträder med en incidens på ≥2 % hos patienter som behandlas med telmisartan/hydroklortiazid och i en högre frekvens än hos patienter som behandlas med placebo, presenteras i tabell 1 [se Kliniska studier ].
Andra biverkningar som observerats för telmisartan/hydroklortiazid var: smärta (inklusive rygg och buk), dyspepsi, erytem, kräkningar, bronkit och faryngit.
Biverkningar inträffade i ungefär samma frekvens hos män och kvinnor, äldre och yngre patienter och svarta och icke-svarta patienter.
Telmisartan
Andra biverkningar som har rapporterats med telmisartan listas nedan:
Autonoma nervsystemet: impotens, ökad svettning, rodnad
Kroppen som helhet: allergi, feber, bensmärtor, bröstsmärtor
Kardiovaskulär: hjärtklappning, angina pectoris, onormalt EKG, hypertoni, perifert ödem
Centrala nervsystemet: sömnlöshet, somnolens, migrän, parestesi, ofrivilliga muskelsammandragningar, hypoestesi
Gastrointestinala: flatulens, förstoppning, gastrit, muntorrhet, hemorrojder, gastroesofageal reflux, tandvärk
Lever-gallväg: förhöjda leverenzymer eller serumbilirubin
Metaboliskt: gikt, hyperkolesterolemi, diabetes mellitus
Muskuloskeletala: artrit, artralgi, benkramper, myalgi
Psykiatrisk: ångest, depression, nervositet
Motståndsmekanism: infektion, abscess, otitis media
Andningsvägar: astma, rinit, dyspné, näsblod
Hud: dermatit, eksem, klåda
Urin: miktionsfrekvens, cystit
Kärl: cerebrovaskulär störning
Särskilda sinnen: onormal syn, konjunktivit, tinnitus, öronvärk
Hydroklortiazid
Andra biverkningar som har rapporterats med hydroklortiazid listas nedan:
Kroppen som helhet: svaghet
Matsmältningskanalen: pankreatit, gulsot (intrahepatisk kolestatisk gulsot), sialadenit, kramper, magirritation
Hematologiska: aplastisk anemi, agranulocytos, leukopeni, hemolytisk anemi, trombocytopeni
Överkänslighet: purpura, ljuskänslighet, urtikaria, nekrotiserande angiit (vaskulit och kutan vaskulit), feber, andnöd inklusive pneumonit och lungödem, anafylaktiska reaktioner
Metaboliskt: hyperglykemi, glykosuri
Muskuloskeletala: muskelspasm
Nervsystemet/psykiatrisk: rastlöshet
Njur: interstitiell nefrit
Hud: erythema multiforme inklusive Stevens-Johnsons syndrom, exfoliativ dermatit inklusive toxisk epidermal nekrolys
Särskilda sinnen: övergående dimsyn, xantopsi
Kliniska laboratorieresultat
Kreatinin, Blod Urea Kväve (BUN)
Ökning av BUN (≥11,2 mg/dL) och serumkreatinin (≥0,5 mg/dL) observerades hos 2,8 % respektive 1,4 % av patienterna med essentiell hypertoni som behandlats med MICARDIS 80 mg HCT-tabletter i kontrollerade studier. Ingen patient avbröt behandlingen med MICARDIS 80 mg HCT tabletter på grund av en ökning av BUN eller kreatinin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av MICARDIS HCT efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Blod- och lymfsystemet: eosinofili
Hjärtsjukdomar: förmaksflimmer, kongestiv hjärtsvikt, hjärtinfarkt, takykardi, bradykardi
Öron- och labyrintsjukdomar: vertigo
Allmänna störningar och villkor för administrationsplatsen: asteni, ödem
Lever-gallväg: Onormal leverfunktion/leverstörning
Immunsystemets störningar: anafylaktisk reaktion
Infektioner och angrepp: urinvägsinfektion
Undersökningar: ökad CPK
Metabolism och näringsstörningar: hypoglykemi (hos diabetespatienter)
Muskuloskeletala och bindvävssjukdomar: sensmärta (inklusive tendinit, tenosynovit), rabdomyolys
Störningar i nervsystemet: synkope, huvudvärk
Njur- och urinvägsstörningar: njursvikt, nedsatt njurfunktion inklusive akut njursvikt
Reproduktionssystemet och bröststörningar: erektil dysfunktion
Andningsvägar, bröstkorg och mediastinum: hosta
Hud och subkutan vävnad: läkemedelsutbrott (toxiskt hudutslag rapporteras oftast som toxicodermi, hudutslag och urtikaria), angioödem (med dödlig utgång)
Vaskulär sjukdom: ortostatisk hypotension
LÄKEMEDELSINTERAKTIONER
Medel som ökar serumkalium
Samtidig administrering av telmisartan med andra läkemedel som höjer serumkaliumnivåerna kan resultera i hyperkalemi. Övervaka serumkalium hos sådana patienter.
Litium
Ökade serumlitiumkoncentrationer och litiumtoxicitet har rapporterats vid samtidig användning av tiaziddiuretika eller angiotensin II-receptorantagonister, inklusive telmisartan. Övervaka litiumnivåer hos patienter som får MICARDIS 80 mg HCT och litium.
Icke-steroida antiinflammatoriska medel inklusive selektiva Cyclooxygenas E-2-hämmare
Telmisartan
Icke-steroida antiinflammatoriska medel inklusive selektiva cyklooxygenas-2-hämmare (COX-2-hämmare): Hos patienter som är äldre, volymutarmade (inklusive de som får diuretikabehandling), eller med nedsatt njurfunktion, samtidig administrering av NSAID, inklusive selektiva COX-2-hämmare, med ARB, inklusive telmisartan, kan resultera i försämring av njurfunktionen, inklusive eventuell akut njursvikt. Dessa effekter är vanligtvis reversibla. Den antihypertensiva effekten av ARB kan dämpas av NSAID. Övervaka därför njurfunktion och blodtryck regelbundet hos patienter som får MICARDIS 40 mg HCT och NSAID.
Hydroklortiazid
Administrering av ett icke-steroidalt antiinflammatoriskt medel, inklusive en selektiv COX2-hämmare, kan minska de diuretiska, natriuretiska och antihypertensiva effekterna av diuretika. Därför, när MICARDIS HCT och icke-steroida antiinflammatoriska medel inklusive selektiva COX2-hämmare används samtidigt, observera noga för att avgöra om den önskade effekten av diuretikumet uppnås.
Dubbel blockad av Renin-Angiotens In-Aldosteron-systemet och förändringar i njurfunktionen
Dubbel blockad av renin-angiotensin-aldosteronsystemet (RAS) med angiotensinblockerare, ACE-hämmare eller aliskiren är associerad med ökade risker för hypotoni, hyperkalemi och nedsatt njurfunktion. ONTARGET-studien inkluderade 25 620 patienter ≥55 år gamla med aterosklerotisk sjukdom eller diabetes med endorganskada, randomiserade till endast telmisartan (ARB), ramipril (ACE-hämmare) eller kombinationen och följde dem i median 56 månader . Patienter som fick kombinationen av ARB och ACE-hämmare fick ingen ytterligare fördel (ingen ytterligare minskning av risken för kardiovaskulär död, hjärtinfarkt, stroke eller sjukhusvistelse på grund av hjärtsvikt) jämfört med ARB monoterapi eller ACE-hämmare monoterapi, men upplevde en ökad förekomst av njursvikt (t.ex. akut njursvikt) jämfört med monoterapigrupper.
Undvik i allmänhet kombinerad användning av RAS-hämmare. Övervaka noggrant blodtryck, njurfunktion och elektrolyter hos patienter på MICARDIS 40 mg HCT och andra medel som påverkar RAS.
Administrera inte aliskiren samtidigt med MICARDIS HCT till patienter med diabetes. Undvik samtidig användning av aliskiren och MICARDIS HCT hos patienter med nedsatt njurfunktion (GFR
Digoxin
När telmisartan administrerades samtidigt med digoxin, observerades medianökningar i digoxin maximal plasmakoncentration (49 %) och dalkoncentration (20 %). Övervaka digoxinnivåer hos patienter som samtidigt tar MICARDIS 40 mg HCT och digoxin.
Antidiabetiska läkemedel (orala medel och insulin)
Dosjustering av antidiabetika kan behövas vid samtidig administrering med hydroklortiazid.
Kolestyramin och kolestipolhartser
Absorptionen av hydroklortiazid försämras i närvaro av anjonbytarhartser. Fördela doseringen av hydroklortiazid och hartset så att hydroklortiazid administreras minst 4 timmar före eller 4 till 6 timmar efter administrering av hartset.
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Fostertoxicitet
Telmisartan
Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död. Resulterande oligohydramnios kan associeras med fetal lunghypoplasi och skelettdeformationer. Potentiella neonatala biverkningar inkluderar skallhypoplasi, anuri, hypotoni, njursvikt och död. När graviditet upptäcks, avbryt MICARDIS HCT så snart som möjligt.
Hydroklortiazid
Tiazider passerar placentabarriären och uppträder i navelsträngsblod. Biverkningar inkluderar fetal eller neonatal gulsot och trombocytopeni [se Användning i specifika populationer ].
Hypotension hos patienter med volym- eller saltbrist
Hos patienter med ett aktiverat renin-angiotensinsystem, såsom volym- eller saltfattiga patienter (t.ex. de som behandlas med höga doser av diuretika), kan symtomatisk hypotoni förekomma efter initialisering av behandling med MICARDIS HCT. Korrigera volym eller saltutarmning före administrering av MICARDIS 80 mg HCT.
Nedsatt njurfunktion
Förändringar i njurfunktionen inklusive akut njursvikt kan orsakas av läkemedel som hämmar reninangiotensinsystemet och av diuretika. Patienter vars njurfunktion kan bero delvis på aktiviteten hos renin-angiotensinsystemet (t.ex. patienter med njurartärstenos, kronisk njursjukdom, allvarlig hjärtsvikt eller volymförsämring) kan ha en särskild risk att utveckla oliguri, progressiv azotemi , eller akut njursvikt på MICARDIS HCT. Övervaka njurfunktionen regelbundet hos dessa patienter. Överväg att avbryta eller avbryta behandlingen hos patienter som utvecklar en kliniskt signifikant minskning av njurfunktionen på MICARDIS HCT.
Elektrolyter och metabola störningar
Läkemedel, inklusive telmisartan, som hämmar renin-angiotensinsystemet kan orsaka hyperkalemi, särskilt hos patienter med njurinsufficiens, diabetes eller kombinationsanvändning med andra angiotensinreceptorblockerare eller ACE-hämmare och samtidig användning av andra läkemedel som höjer serumkaliumnivåerna [se LÄKEMEDELSINTERAKTIONER ].
Hydroklortiazid kan orsaka hypokalemi och hyponatremi. Tiazider har visats öka urinutsöndringen av magnesium; detta kan resultera i hypomagnesemi. Hypomagnesemi kan resultera i hypokalemi som kan vara svår att behandla trots kaliumtillskott. Övervaka serumelektrolyter regelbundet.
I kontrollerade studier med kombinationsbehandlingen telmisartan/hydroklortiazid upplevde ingen patient som fick 40 mg/12,5 mg, 80 mg/12,5 mg eller 80 mg/25 mg en minskning av kalium ≥1,4 mekv/l och ingen patient upplevde hyperkalemi.
Hydroklortiazid minskar utsöndringen av kalcium i urinen och kan orsaka förhöjda serumkalcium.
Hydroklortiazid kan förändra glukostoleransen och höja serumnivåerna av kolesterol och triglycerider.
Hyperurikemi kan uppstå eller frank gikt kan utlösas hos vissa patienter som får tiazidbehandling. Eftersom telmisartan minskar urinsyran, dämpar telmisartan i kombination med hydroklortiazid den diuretikainducerade hyperurikemin.
Överkänslighetsreaktion
Hydroklortiazid
Överkänslighetsreaktioner mot hydroklortiazid kan förekomma hos patienter med eller utan anamnes på allergi eller bronkialastma, men är mer sannolikt hos patienter med sådan historia [se KONTRAINDIKATIONER ].
Akut närsynthet och sekundär vinkelstängningsglaukom
Hydroklortiazid, en sulfonamid, kan orsaka en idiosynkratisk reaktion, vilket resulterar i akut övergående närsynthet och akut vinkelglaukom. Symtomen inkluderar akut uppkomst av minskad synskärpa eller ögonsmärta och uppträder vanligtvis inom timmar till veckor efter läkemedelsstart. Obehandlad akut vinkelglaukom kan leda till permanent synförlust. Den primära behandlingen är att avbryta behandlingen med hydroklortiazid så snabbt som möjligt. Snabba medicinska eller kirurgiska behandlingar kan behöva övervägas om det intraokulära trycket förblir okontrollerat. Riskfaktorer för att utveckla akut vinkelglaukom kan inkludera en historia av sulfonamid- eller penicillinallergi.
Systemisk lupus erythematosus
Tiaziddiuretika har rapporterats orsaka exacerbation eller aktivering av systemisk lupus erythematosus.
Postsympatiktomipatienter
De antihypertensiva effekterna av hydroklortiazid kan förstärkas hos postsympatiktomipatienter.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION ).
Graviditet
Informera kvinnliga patienter i fertil ålder om konsekvenserna av exponering för MICARDIS 40 mg HCT under graviditet. Diskutera behandlingsalternativ med kvinnor som planerar att bli gravida. Säg till patienterna att rapportera graviditeter till sin läkare så snart som möjligt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Laktation
Avråda ammande kvinnor att inte amma under behandling med MICARDIS HCT [se Användning i specifika populationer ].
Symtomatisk hypotoni och synkope
Informera patienter om att yrsel kan uppstå, särskilt under de första dagarna av behandlingen, och att rapportera det till sin vårdgivare. Informera patienter om att otillräckligt vätskeintag, överdriven svettning, diarré eller kräkningar kan leda till ett överdrivet blodtrycksfall, med samma konsekvenser av yrsel och eventuell synkope. Rekommendera patienter att kontakta sin vårdgivare om synkope inträffar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kaliumtillskott
Rekommendera patienter att inte använda kaliumtillskott eller saltersättningsmedel som innehåller kalium utan att rådfråga den förskrivande läkaren [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och LÄKEMEDELSINTERAKTIONER ].
Akut närsynthet och sekundär vinkelstängningsglaukom
Rekommendera patienter att avbryta behandlingen med MICARDIS 80 mg HCT och omedelbart söka läkarvård om de upplever symtom på akut närsynthet eller sekundärt vinkelstängningsglaukom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Telmisartan och hydroklortiazid
Inga karcinogenicitets-, mutagenicitets- eller fertilitetsstudier har utförts med kombinationen telmisartan och hydroklortiazid.
Telmisartan
Det fanns inga tecken på karcinogenicitet när telmisartan administrerades i kosten till möss och råttor i upp till 2 år. De högsta doserna som administreras till möss (1000 mg/kg/dag) och råttor (100 mg/kg/dag) är, på mg/m2-basis, cirka 59 respektive 13 gånger den maximala rekommenderade humandosen (MRHD) av telmisartan. Samma doser har visat sig ge en genomsnittlig systemisk exponering för telmisartan >100 gånger respektive >25 gånger den systemiska exponeringen hos människor som får MRHD av telmisartan (80 mg/dag).
Genotoxicitetsanalyser avslöjade inga telmisartanrelaterade effekter vare sig på gen- eller kromosomnivå. Dessa analyser inkluderade bakteriell mutagenitetstester med Salmonella och E. coli (Ames), ett genmutationstest med V79-celler från kinesisk hamster, ett cytogenetiskt test med humana lymfocyter och ett mikrokärntest på mus.
Inga läkemedelsrelaterade effekter på reproduktionsförmågan hos han- och honråttor noterades vid 100 mg/kg/dag (den högsta administrerade dosen), cirka 13 gånger, på mg/m2-basis, MRHD för telmisartan. Denna dos hos råtta resulterade i en genomsnittlig systemisk exponering (telmisartan AUC bestämd på dag 6 av dräktigheten) minst 50 gånger den genomsnittliga systemiska exponeringen hos människor vid MRHD (80 mg/dag).
Hydroklortiazid
Tvååriga utfodringsstudier på möss och råttor utförda under överinseende av National Toxicology Program (NTP) avslöjade inga tecken på cancerframkallande potential hos hydroklortiazid hos möss av honkön (vid doser upp till cirka 600 mg/kg/dag) eller hos hanar. och honråttor (vid doser på upp till cirka 100 mg/kg/dag). NTP fann dock tvetydiga bevis för hepatokarcinogenicitet hos möss av hankön.
Hydroklortiazid var inte genotoxiskt in vitro i Ames mutagenicitetsanalysen av Salmonella typhimurium-stammarna TA 98, TA 100, TA 1535, TA 1537 och TA 1538 och i äggstockstestet för kinesisk hamster (CHO) för kromosomavvikelser med användning av vibrationer, eller könscellskromosomer från mus, benmärgskromosomer från kinesisk hamster och genen Drosophila könsbundna recessiva dödliga egenskaper. Positiva testresultat erhölls i in vitro CHO-systerkromatidutbytesanalysen (klastogenicitet), i analysen av muslymfomceller (mutagenicitet) och i Aspergillus nidulans icke-disjunktionsanalysen.
Hydroklortiazid hade inga negativa effekter på fertiliteten hos möss och råttor av båda könen i studier där dessa arter exponerades, via sin diet, för doser på upp till 100 respektive 4 mg/kg, före parning och under hela graviditeten.
Användning i specifika populationer
Graviditet
Risksammanfattning
MICARDIS HCT kan orsaka fosterskador när det ges till en gravid kvinna. Användning av läkemedel som verkar på renin-angiotensinsystemet under andra och tredje trimestern av graviditeten minskar fostrets njurfunktion och ökar foster- och neonatal sjuklighet och död (se Kliniska överväganden ). De flesta epidemiologiska studier som undersöker fosteravvikelser efter exponering för antihypertensiv användning under första trimestern har inte särskiljt läkemedel som påverkar renin-angiotensinsystemet från andra antihypertensiva medel. Studier på råttor och kaniner med telmisartan visade endast fostertoxicitet vid maternellt toxiska doser (se Data ). När graviditet upptäcks, avbryt MICARDIS HCT så snart som möjligt.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Kliniska överväganden
Sjukdomsrelaterad risk för modern och/eller embryo/foster
Hypertoni under graviditeten ökar moderns risk för havandeskapsförgiftning, graviditetsdiabetes, för tidig förlossning och förlossningskomplikationer (t.ex. behov av kejsarsnitt och blödning efter förlossningen). Hypertoni ökar fostrets risk för intrauterin tillväxtbegränsning och intrauterin död. Gravida kvinnor med högt blodtryck bör övervakas noggrant och hanteras därefter.
Fetala/neonatala biverkningar
Telmisartan
Användning av läkemedel som verkar på RAS under andra och tredje trimestern av graviditeten kan resultera i följande: oligohydramnios, nedsatt fosterns njurfunktion som leder till anuri och njursvikt, fosterlunghypoplasi, skelettdeformationer, inklusive skallhypoplasi, hypotoni och dödsfall . I det ovanliga fallet att det inte finns något lämpligt alternativ till behandling med läkemedel som påverkar renin-angiotensinsystemet för en viss patient, informera mamman om den potentiella risken för fostret.
Hos patienter som tar MICARDIS HCT under graviditet, utför seriella ultraljudsundersökningar för att bedöma den intra-amniotiska miljön. Fostertestning kan vara lämpligt, baserat på graviditetsveckan. Om oligohydramnios observeras, avbryt MICARDIS HCT, såvida det inte anses vara livräddande för modern. Patienter och läkare bör dock vara medvetna om att oligohydramnios kanske inte uppträder förrän efter att fostret har fått irreversibel skada.
Observera noga spädbarn med tidigare exponering in utero för MICARDIS 20 mg HCT för hypotoni, oliguri och hyperkalemi. Om oliguri eller hypotoni uppstår, stöd blodtryck och njurperfusion. Utbytestransfusioner eller dialys kan krävas som ett sätt att vända hypotoni och ersätta njurfunktionen [se Användning i specifika populationer ].
Hydroklortiazid
Tiazider passerar placentan och användning av tiazider under graviditet är förknippad med risk för fetal eller neonatal gulsot, trombocytopeni och eventuella andra biverkningar som har inträffat hos vuxna.
Data
Djurdata
MICARDIS 40mg HCT
En utvecklingstoxicitetsstudie utfördes på råttor med telmisartan/hydroklortiaziddoser på 3,2/1,0, 15/4,7, 50/15,6 och 0/15,6 mg/kg/dag. Även om de två högre doskombinationerna verkade vara mer toxiska (betydande minskning av kroppsviktsökning) för moderdjuren än något av läkemedlen ensamt, verkade det inte finnas någon ökning av toxiciteten för de utvecklade embryona.
Telmisartan
Inga teratogena effekter observerades när telmisartan administrerades till dräktiga råttor i orala doser på upp till 50 mg/kg/dag och till dräktiga kaniner vid orala doser på upp till 45 mg/kg/dag. Hos kaniner observerades embryodödlighet förknippad med maternell toxicitet (minskad kroppsviktsökning och födokonsumtion) vid 45 mg/kg/dag (ungefär 12 gånger den maximala rekommenderade humana dosen [MRHD] på 80 mg på mg/m2 basis). Hos råttor observerades maternellt toxiska (minskad kroppsviktsökning och födokonsumtion) telmisartandoser på 15 mg/kg/dag (cirka 1,9 gånger MRHD på mg/m2-basis), administrerade under sen dräktighet och laktation, ge biverkningar hos nyfödda, inklusive minskad livsduglighet, låg födelsevikt, försenad mognad och minskad viktökning. Doserna av icke observerad effekt för utvecklingstoxicitet hos råttor och kaniner, 5 respektive 15 mg/kg/dag, är cirka 0,64 respektive 3,7 gånger, på mg/m2-basis, MRHD för telmisartan (80 mg/dag) ).
Hydroklortiazid
Studier där hydroklortiazid administrerades till gravida möss och råttor under deras respektive perioder av större organogenes i doser upp till 3000 respektive 1000 mg/kg/dag (cirka 600 och 400 gånger MRHD), gav inga tecken på skada på fostret .
Tiazider kan passera placentan och koncentrationer som uppnås i navelvenen närmar sig dem i moderns plasma. Hydroklortiazid kan, liksom andra diuretika, orsaka hypoperfusion av placenta. Det ackumuleras i fostervattnet, med rapporterade koncentrationer upp till 19 gånger högre än i navelvenens plasma. Användning av tiazider under graviditet är associerad med risk för foster- eller neonatal gulsot eller trombocytopeni. Eftersom de inte förhindrar eller förändrar förloppet av EPH (Ödem, Proteinuri, Hypertoni) gestos (föregiftning), bör dessa läkemedel inte användas för att behandla hypertoni hos gravida kvinnor. Användning av hydroklortiazid för andra indikationer (t.ex. hjärtsjukdom) under graviditet bör undvikas.
Laktation
Risksammanfattning
Det finns ingen information om förekomsten av MICARDIS 20 mg HCT eller telmisartan i modersmjölk, effekterna på det ammade barnet eller effekterna på mjölkproduktionen. Begränsade publicerade studier rapporterar att hydroklortiazid finns i bröstmjölk. Det finns dock otillräcklig information för att fastställa effekterna av hydroklortiazid på det ammade barnet eller effekterna av hydroklortiazid på mjölkproduktionen. Telmisartan finns i mjölken från digivande råttor. (ser Data ). På grund av risken för allvarliga biverkningar hos det ammade barnet inklusive hypotoni, hyperkalemi och nedsatt njurfunktion, råd en ammande kvinna att inte amma under behandling med MICARDIS HCT.
Data
Telmisartan fanns i mjölken hos digivande råttor i koncentrationer 1,5 till 2 gånger de som finns i plasma från 4 till 8 timmar efter administrering.
Pediatrisk användning
Säkerhet och effektivitet för MICARDIS HCT hos pediatriska patienter har inte fastställts.
Nyfödda med en historia av exponering i livmodern för MICARDIS HCT
Om oliguri eller hypotoni uppstår, stöd blodtryck och njurperfusion. Utbytestransfusioner eller dialys kan krävas för att vända hypotoni och/eller ersätta störd njurfunktion.
Geriatrisk användning
de kontrollerade kliniska prövningarna (n=1017) var cirka 20 % av patienterna som behandlades med telmisartan/hydroklortiazid 65 år eller äldre och 5 % var 75 år eller äldre. Inga övergripande skillnader i effektivitet och säkerhet för telmisartan/hydroklortiazid observerades hos dessa patienter jämfört med yngre patienter. Andra rapporterade kliniska erfarenheter har inte identifierat skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion och av samtidiga sjukdomar eller annan läkemedelsbehandling.
Användning hos patienter med nedsatt leverfunktion
Patienter med gallvägsobstruktiva störningar eller leverinsufficiens bör påbörja behandling under noggrann medicinsk övervakning med kombinationen 40 mg/12,5 mg.
Telmisartan
Eftersom majoriteten av telmisartan elimineras genom gallutsöndring, kan patienter med gallvägsobstruktiva störningar eller leverinsufficiens förväntas ha minskat clearance och högre blodnivåer.
Hydroklortiazid
Mindre förändringar av vätske- och elektrolytbalansen kan utlösa leverkoma hos patienter med nedsatt leverfunktion eller progressiv leversjukdom.
Användning hos patienter med nedsatt njurfunktion
Säkerhet och effektivitet för MICARDIS 40 mg HCT hos patienter med gravt nedsatt njurfunktion (CrCl ≤30 ml/min) har inte fastställts. Till patienter med gravt nedsatt njurfunktion rekommenderas inte MICARDIS 80 mg HCT-tabletter. Ingen dosjustering krävs hos patienter med lätt (CrCl 60 till 90 ml/min) eller måttligt (CrCl 30 till 60 ml/min) nedsatt njurfunktion.
ÖVERDOS
Telmisartan
Begränsade data finns tillgängliga med avseende på överdosering av telmisartan hos människor. De mest sannolika manifestationerna av överdosering med telmisartan är hypotoni, yrsel och takykardi; bradykardi kan uppstå från parasympatisk (vagal) stimulering. Om symtomatisk hypotoni skulle uppstå, bör stödbehandling sättas in. Telmisartan avlägsnas inte genom hemodialys.
Hydroklortiazid
De vanligaste tecknen och symtomen som observerats hos patienter med en överdos av hydroklortiazid är de som orsakas av utarmning av elektrolyter (hypokalemi, hypokloremi, hyponatremi) och uttorkning till följd av överdriven diures. Om digitalis också har administrerats kan hypokalemi accentuera hjärtarytmier. Graden i vilken hydroklortiazid avlägsnas genom hemodialys har inte fastställts. Den orala LD av hydroklortiazid är högre än 10 g/kg hos både möss och råttor.
KONTRAINDIKATIONER
MICARDIS HCT är kontraindicerat:
- Hos patienter som är överkänsliga mot någon komponent i denna produkt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Hos patienter med anuri.
- För samtidig administrering med aliskiren till patienter med diabetes [se LÄKEMEDELSINTERAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
MICARDIS 40mg HCT
MICARDIS 20mg HCT är en kombination av två läkemedel med antihypertensiva egenskaper: ett tiaziddiuretikum, hydroklortiazid och en angiotensin II-receptorblockerare (ARB), telmisartan.
Telmisartan
Angiotensin II bildas från angiotensin I i en reaktion som katalyseras av angiotensinomvandlande enzym (ACE, kininas II). Angiotensin II är det huvudsakliga pressormedlet i renin-angiotensinsystemet, med effekter som inkluderar vasokonstriktion, stimulering av syntes och frisättning av aldosteron, hjärtstimulering och renal reabsorption av natrium. Telmisartan blockerar de vasokonstriktor- och aldosteronutsöndrande effekterna av angiotensin II genom att selektivt blockera bindningen av angiotensin II till AT1-receptorn i många vävnader, såsom vaskulär glatt muskulatur och binjuren. Dess verkan är därför oberoende av vägarna för angiotensin II-syntes.
Det finns också en AT2-receptor i många vävnader, men AT2 är inte känt för att vara associerat med kardiovaskulär homeostas. Telmisartan har mycket större affinitet (>3 000 gånger) för AT1-receptorn än för AT2-receptorn.
Telmisartan hämmar inte ACE (kininas II) och binder inte heller till eller blockerar andra hormonreceptorer eller jonkanaler som är kända för att vara viktiga för kardiovaskulär reglering.
Blockad av angiotensin II-receptorn hämmar den negativa regulatoriska återkopplingen av angiotensin II på reninsekretion, men den resulterande ökade plasmareninaktiviteten och angiotensin II-cirkulerande nivåer övervinner inte effekten av telmisartan på blodtrycket.
Hydroklortiazid
Hydroklortiazid är ett tiaziddiuretikum. Tiazider påverkar de renala tubulära mekanismerna för elektrolytreabsorption, vilket direkt ökar utsöndringen av natriumsalt och klorid i ungefär motsvarande mängder. Indirekt minskar den diuretiska effekten av hydroklortiazid plasmavolymen, med åtföljande ökning av plasmareninaktivitet, ökning av aldosteronsekretion, ökning av urinförlust av kalium och minskning av serumkalium. Renin-aldosteronkopplingen medieras av angiotensin II, så samtidig administrering av en ARB tenderar att vända den kaliumförlust som är förknippad med dessa diuretika. Mekanismen för den antihypertensiva effekten av tiazider är inte helt klarlagd.
Farmakodynamik
Telmisartan
Hos normala frivilliga hämmade en dos av telmisartan 80 mg pressorsvaret på en intravenös infusion av angiotensin II med cirka 90 % vid maximala plasmakoncentrationer med cirka 40 % hämning som kvarstod i 24 timmar.
Plasmakoncentrationen av angiotensin II och plasmareninaktiviteten ökade på ett dosberoende sätt efter engångsadministrering av telmisartan till friska försökspersoner och upprepad administrering till hypertonipatienter. Administrering en gång dagligen av upp till 80 mg telmisartan till friska försökspersoner påverkade inte plasmaaldosteronkoncentrationerna. I multipeldosstudier med hypertonipatienter fanns inga kliniskt signifikanta förändringar i elektrolyter (serumkalium eller natrium) eller i metabolisk funktion (inklusive serumnivåer av kolesterol, triglycerider, HDL, LDL, glukos eller urinsyra).
De antihypertensiva effekterna av telmisartan har studerats i sex placebokontrollerade kliniska prövningar, inklusive totalt 1773 patienter med mild till måttlig hypertoni (diastoliskt blodtryck på 95 till 114 mmHg), av vilka 1031 behandlades med telmisartan. Efter administrering en gång dagligen av telmisartan var storleken på blodtryckssänkningen från baslinjen efter placebosubtraktion ungefär (SBP/DBP) 6-8/6 mmHg för 20 mg, 9-13/6-8 mmHg för 40 mg och 12 -13/7-8 mmHg för 80 mg. Större doser (upp till 160 mg) verkade inte orsaka en ytterligare sänkning av blodtrycket.
Den antihypertensiva aktiviteten börjar inom 3 timmar, med en maximal minskning med cirka 4 veckor. Vid doser på 20, 40 och 80 mg bibehölls den antihypertensiva effekten av en gång dagligen administrering av telmisartan under hela 24-timmars dosintervallet.
Hos 30 hypertonipatienter med normal njurfunktion som behandlades i 8 veckor med telmisartan 80 mg eller telmisartan 80 mg i kombination med hydroklortiazid 12,5 mg, fanns det inga kliniskt signifikanta förändringar från baslinjen i njurblodflöde, glomerulär filtrationshastighet, filtrationsfraktion, renovaskulärt motstånd, eller kreatininclearance.
Hydroklortiazid
Efter oral administrering av hydroklortiazid börjar diuresen inom 2 timmar, toppar efter cirka 4 timmar och varar cirka 6 till 12 timmar.
Läkemedelsinteraktioner
Hydroklortiazid
Alkohol, barbiturater eller narkotika
Potentiering av ortostatisk hypotoni kan förekomma.
Skelettmuskelavslappnande medel
Möjlig ökad lyhördhet för muskelavslappnande medel som curare-derivat.
Kortikosteroider, ACTH
Intensifierad elektrolytutarmning, särskilt hypokalemi.
Pressoraminer (t.ex. noradrenalin)
Möjligt minskat svar på pressoraminer men inte tillräckligt för att utesluta deras användning.
Farmakokinetik
Telmisartan
Absorption:
Efter oral administrering uppnås maximala koncentrationer (Cmax ) av telmisartan 0,5 till 1 timme efter dosering. Mat minskar biotillgängligheten av telmisartan något, med en minskning av arean under plasmakoncentration-tidkurvan (AUC) med cirka 6 % med 40 mg och cirka 20 % efter en dos på 160 mg. MICARDIS 20 mg HCT kan administreras med eller utan mat. Den absoluta biotillgängligheten för telmisartan är dosberoende. Vid 40 och 160 mg var biotillgängligheten 42 % respektive 58 %. Farmakokinetiken för telmisartan med oralt administrerad MICARDIS 20 mg är olinjär inom dosintervallet 20 till 160 mg, med större än proportionella ökningar av plasmakoncentrationer (Cmax och AUC) med ökande doser. Telmisartan visar bi-exponentiell sönderfallskinetik med en terminal halveringstid på cirka 24 timmar. Lägsta plasmakoncentrationer av telmisartan vid dosering en gång dagligen är cirka 10 % till 25 % av maximala plasmakoncentrationer. Telmisartan har ett ackumuleringsindex i plasma på 1,5 till 2,0 vid upprepad dosering en gång dagligen.
Distribution:
Telmisartan är starkt bundet till plasmaproteiner (>99,5%), främst albumin och α1-syraglykoprotein. Plasmaproteinbindningen är konstant över det koncentrationsintervall som uppnås med rekommenderade doser. Distributionsvolymen för telmisartan är cirka 500 liter, vilket indikerar ytterligare vävnadsbindning.
Ämnesomsättning:
Telmisartan metaboliseras genom konjugering för att bilda en farmakologiskt inaktiv acylglukuronid; glukuroniden i modersubstansen är den enda metaboliten som har identifierats i human plasma och urin. Efter en engångsdos representerar glukuroniden cirka 11 % av den uppmätta radioaktiviteten i plasma. Cytokrom P450 isoenzymer är inte involverade i metabolismen av telmisartan.
Eliminering:
Efter antingen intravenös eller oral administrering av 14C-märkt telmisartan, eliminerades det mesta av den administrerade dosen (>97%) oförändrad i feces via gallutsöndring; endast små mängder hittades i urinen (0,91 % respektive 0,49 % av den totala radioaktiviteten).
Total plasmaclearance för telmisartan är >800 ml/min. Terminal halveringstid och totalt clearance verkar vara oberoende av dos.
Hydroklortiazid
Hydroklortiazid metaboliseras inte utan elimineras snabbt via njurarna. När plasmanivåerna har följts under minst 24 timmar har plasmahalveringstiden observerats variera mellan 5,6 och 14,8 timmar. Minst 61 % av den orala dosen elimineras oförändrad inom 24 timmar.
Hydroklortiazid passerar placenta men inte blod-hjärnbarriären och utsöndras i bröstmjölk.
Specifika populationer
Telmisartan
Njurinsufficiens
Telmisartan avlägsnas inte från blodet genom hemofiltrering [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , och Användning i specifika populationer ].
Leverinsufficiens
Hos patienter med leverinsufficiens ökar plasmakoncentrationerna av telmisartan och den absoluta biotillgängligheten närmar sig 100 % [se Användning i specifika populationer ].
Kön
Plasmakoncentrationerna av telmisartan är i allmänhet 2 till 3 gånger högre hos kvinnor än hos män. I kliniska prövningar har dock inga signifikanta ökningar av blodtryckssvaret eller incidensen av ortostatisk hypotoni påträffats hos kvinnor. Ingen dosjustering är nödvändig.
Geriatriska patienter
Telmisartans farmakokinetik skiljer sig inte mellan äldre och personer yngre än 65 år.
Läkemedelsinteraktionsstudier
Telmisartan
Ramipril
Samtidig administrering av telmisartan 80 mg en gång dagligen och ramipril 10 mg en gång dagligen till friska försökspersoner ökar steady-state Cmax och AUC för ramipril 2,3- respektive 2,1-faldigt, och Cmax och AUC för ramiprilat 2,4- respektive 1,5-faldigt. . Däremot minskar Cmax och AUC för telmisartan med 31 % respektive 16 %. Vid samtidig administrering av telmisartan och ramipril kan svaret vara högre på grund av de eventuellt additiva farmakodynamiska effekterna av de kombinerade läkemedlen, och även på grund av den ökade exponeringen för ramipril och ramiprilat i närvaro av telmisartan.
Andra droger
Samtidig administrering av telmisartan resulterade inte i en kliniskt signifikant interaktion med acetaminofen, amlodipin, glyburid, simvastatin, hydroklortiazid, warfarin eller ibuprofen. Telmisartan metaboliseras inte av cytokrom P450-systemet och hade inga effekter in vitro på cytokrom P450-enzymer, förutom viss hämning av CYP2C19. Telmisartan förväntas inte interagera med läkemedel som hämmar cytokrom P450-enzymer; det förväntas inte heller interagera med läkemedel som metaboliseras av cytokrom P450-enzymer, förutom möjlig hämning av metabolismen av läkemedel som metaboliseras av CYP2C19.
Kliniska studier
Telmisartan och hydroklortiazid
kontrollerade kliniska prövningar med fler än 2500 hypertonipatienter exponerades 1017 patienter för telmisartan (20 mg till 160 mg) och samtidig hydroklortiazid (6,25 mg till 25 mg). Dessa studier inkluderade en faktorstudie (studie 1) med kombinationer av telmisartan (20 mg, 40 mg, 80 mg, 160 mg eller placebo) och hydroklortiazid (6,25 mg, 12,5 mg, 25 mg och placebo). Den faktoriella studien randomiserade 818 patienter, inklusive 493 (60%) män; 596 (73 %) icke-svarta och 222 (27 %) svarta; och 143 (18%) ≥65 år (medianåldern var 53 år). Det genomsnittliga liggande blodtrycket vid baslinjen för den totala populationen var 154/101 mmHg.
Kombinationen av telmisartan och hydroklortiazid resulterade i additiv placebojusterad sänkning av systoliskt och diastoliskt blodtryck vid dalvärdet 16-21/9-11 mmHg för doser mellan 40 mg/12,5 mg och 80 mg/25 mg, jämfört med 9-13 /7-8 mmHg för telmisartan 40 mg till 80 mg monoterapi och 4/4 mmHg för hydroklortiazid 12,5 mg monoterapi. Den antihypertensiva effekten var oberoende av ålder eller kön. Det var i princip ingen förändring i hjärtfrekvensen hos patienter som behandlades med kombinationen telmisartan och hydroklortiazid i den placebokontrollerade studien.
Fyra andra studier av hypertonipatienter med minst sex månaders varaktighet möjliggjorde tillägg av hydroklortiazid för patienter som antingen inte var tillräckligt kontrollerade med den randomiserade telmisartan-monoterapidosen eller inte hade uppnått adekvat blodtryckssvar efter avslutad upptitrering av telmisartan. I aktivt kontrollerade studier minskade tillägget av 12,5 mg hydroklortiazid till titrerade doser av telmisartan hos patienter som inte uppnådde eller bibehöll adekvat svar med telmisartan monoterapi ytterligare det systoliska och diastoliska blodtrycket.
PATIENTINFORMATION
MICARDIS® HCT (my-CAR-dis HCT) (telmis artan och hydroklortiazid) Tabletter
Läs denna patientinformation innan du börjar ta MICARDIS HCT tabletter och varje gång du får påfyllning. Det kan komma ny information. Denna information ersätter inte att prata med din läkare om ditt medicinska tillstånd eller din behandling.
Vilken är den viktigaste informationen jag bör veta om MICARDIS 20mg HCT-tabletter?
MICARDIS HCT kan orsaka skada eller dödsfall för ett ofött barn. Tala med din läkare om andra sätt att sänka ditt blodtryck om du planerar att bli gravid. Om du blir gravid medan du tar MICARDIS 20mg HCT, berätta omedelbart för din läkare.
Vad är MICARDIS HCT?
MICARDIS 40mg HCT är ett receptbelagt läkemedel som används för att behandla högt blodtryck (hypertoni).
MICARDIS 40mg HCT innehåller:
- telmisartan, en angiotensinreceptorblockerare (ARB)
- hydroklortiazid, ett vattenpiller eller diuretikum
Din läkare kan ordinera andra läkemedel som du kan ta tillsammans med MICARDIS 80 mg HCT för att behandla ditt höga blodtryck.
Det är inte känt om MICARDIS 40mg HCT är säkert och effektivt för barn.
Ta inte MICARDIS 20mg HCT tabletter om du:
- har låg eller ingen urinproduktion
- är allergisk (överkänslig) mot de aktiva ingredienserna (telmisartan eller hydroklortiazid) eller något av de andra innehållsämnena som anges i slutet av denna bipacksedel
Vad ska jag berätta för min läkare innan jag använder MICARDIS 40mg HCT-tabletter?
Innan du tar MICARDIS 20 mg HCT tabletter, berätta för din läkare om du:
- är gravid eller planerar att bli gravid. Ser "Vilken är den viktigaste informationen jag borde veta om MICARDIS 20mg HCT-tabletter?"
- ammar eller planerar att amma. MICARDIS 80mg HCT kan passera över i din bröstmjölk och kan skada ditt barn. Du och din läkare bör bestämma om du ska ta MICARDIS HCT eller amma. Du ska inte göra båda. Tala med din läkare om det bästa sättet att mata ditt barn om du tar MICARDIS HCT tabletter.
- har fått veta att du har onormala nivåer av kroppssalt (elektrolyter) i ditt blod
- har leverproblem
- har astma eller tidigare astma
- har lupus
- har diabetes
- har njurproblem
- har andra medicinska tillstånd
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. Tala också om för din läkare om du dricker alkohol.
MICARDIS 20mg HCT kan påverka hur andra läkemedel fungerar, och andra läkemedel kan påverka hur MICARDIS 20mg HCT fungerar. Tala särskilt om för din läkare om du tar:
- aliskiren
- digoxin (Lanoxin®)
- litium (Lithobid®, litiumkarbonat, litiumcitrat)
- andra läkemedel som används för att behandla ditt högt blodtryck eller hjärtproblem
- vattenpiller (vätskedrivande)
- aspirin eller andra icke-steroida antiinflammatoriska läkemedel (NSAID)
- kaliumtillskott eller en saltersättning som innehåller kalium
- läkemedel som används för att behandla diabetes, inklusive insulin
- narkotiska smärtstillande läkemedel
- sömntabletter
- steroidmedicin eller adrenokortikotrofiskt hormon (ACTH)
- barbiturater
- vissa kolesterolsänkande läkemedel (hartser som används för kolesterolsänkning, t.ex. kolestyramin och kolestipolhartser)
Fråga din läkare om du är osäker på om du tar något av läkemedlen som anges ovan.
Vet vilka mediciner du tar. Håll en lista över dem och visa den för din läkare eller apotekspersonal när du får ett nytt läkemedel.
Hur ska jag ta MICARDIS HCT tabletter?
- Ta MICARDIS 40 mg HCT tabletter precis som din läkare säger åt dig att ta det.
- Din läkare kommer att tala om för dig hur mycket MICARDIS HCT du ska ta och när du ska ta det.
- Ändra inte din dos om inte din läkare säger åt dig att göra det.
- Ta MICARDIS HCT en gång varje dag.
- Ta MICARDIS 20 mg HCT tabletter med eller utan mat.
- Om du tar för mycket MICARDIS HCT, ring din läkare eller gå till närmaste akutmottagning direkt.
- Läs "Hur man öppnar blistern" i slutet av denna bipacksedel innan du använder MICARDIS 20 mg HCT. Tala med din läkare om du inte förstår instruktionerna.
Vilka är de möjliga biverkningarna av MICARDIS 80mg HCT tabletter?
MICARDIS 20mg HCT tabletter kan orsaka allvarliga biverkningar, inklusive:
- Skada eller dödsfall på ditt ofödda barn. Ser "Vilken är den viktigaste informationen jag borde veta om MICARDIS HCT-tabletter?"
- Lågt blodtryck (hypotenjon) är mest sannolikt att hända om du också:
- ta vattenpiller (diuretika)
- är på en diet med låg salthalt
- få dialysbehandlingar
- har hjärtproblem
- bli sjuk av kräkningar eller diarré
- drick inte tillräckligt med vätska
- svettas mycket
- Njurproblem, som kan bli värre om du redan har en njursjukdom. Du kan ha förändringar i dina njurtestresultat och du kan behöva en lägre dos av MICARDIS 40 mg HCT-tabletter. Ring din läkare om du får:
- svullnad i dina fötter, vrister eller händer
- oförklarlig viktökning
- leverproblem, som kan bli värre hos personer som redan har leverproblem och tar MICARDIS 40 mg HCT.
- Ögonproblem. Ett av läkemedlen i MICARDIS HCT kan orsaka ögonproblem som kan leda till synförlust. Symtom på ögonproblem kan inträffa inom några timmar till veckor efter start av MICARDIS
HCT. Tala genast om för din läkare om du har:
- minskad syn
- ögonsmärta
- Allergiska reaktioner . Tala genast om för din läkare om du får något av dessa symtom:
- svullnad i ansikte, tunga, svalg
- svårt att andas
- Sämre ändelse av lupus. Tala om för din läkare om din lupus förvärras eller blir aktiv medan du tar MICARDIS 20 mg HCT.
- Förändring av kroppssalter (elektrolyter) i ditt blod och vätskeproblem . Din läkare kan göra tester för att kontrollera ditt blod. Ring din läkare omedelbart om du har:
- torr mun
- törst
- trötthet
- sömnighet
- rastlöshet
- förvirring
- anfall
- snabba hjärtslag
- svaghet
- muskelvärk eller kramper
- mycket låg urinproduktion
- illamående eller kräkningar
Om du känner dig svimfärdig eller yr, lägg dig ner och ring din läkare omedelbart.
Ring din läkare omedelbart om du får något av symtomen som anges ovan.
De vanligaste biverkningarna av MICARDIS 80mg HCT-tabletter inkluderar:
- övre luftvägsinfektioner, inklusive sinussmärta/täppa och ont i halsen
- yrsel
- känner mig trött
- influensaliknande symtom
- ryggont
- diarre
- illamående
Dessa är inte alla möjliga biverkningar med MICARDIS 20 mg HCT-tabletter. Tala om för din läkare om du har någon biverkning som stör dig eller som inte försvinner. Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara MICARDIS 80mg HCT-tabletter?
- Förvara MICARDIS HCT-tabletter i rumstemperatur 68°F till 77°F (20°C till 25°C).
- Ta inte bort MICARDIS 40 mg HCT-tabletter från blister förrän precis innan du tar dem.
Förvara MICARDIS 80mg HCT-tabletter och alla läkemedel utom räckhåll för barn.
Allmän information om MICARDIS 40mg HCT tabletter:
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en patientinformationsbroschyr. Använd inte MICARDIS HCT tabletter för ett tillstånd som det inte har ordinerats för. Ge inte MICARDIS 20 mg HCT tabletter till andra personer, även om de har samma tillstånd som du har. Det kan skada dem.
Denna patientinformationsbroschyr sammanfattar den viktigaste informationen om MICARDIS HCT-tabletter. Om du vill ha mer information, prata med din läkare. Du kan fråga din apotekspersonal eller läkare om information om MICARDIS 20mg HCT-tabletter som är skriven för vårdpersonal.
För aktuell förskrivningsinformation, skanna koden nedan eller ring Boehringer Ingelheim Pharmaceuticals, Inc. på 1-800-542-6257 eller (TTY) 1-800-459-9906.
Vilka är ingredienserna i MICARDIS 20mg HCT tabletter?
Aktiva ingredienser: telmisartan och hydroklortiazid
Inaktiva ingredienser: natriumhydroxid, meglumin, povidon, sorbitol, magnesiumstearat, laktosmonohydrat, mikrokristallin cellulosa, majsstärkelse och natriumstärkelseglykolat
Tabletterna 40 mg/12,5 mg och 80 mg/12,5 mg innehåller också: järnoxidrött.
80 mg/25 mg tabletterna innehåller även: järnoxidgul.
Vad är högt blodtryck (hypertoni)?
Blodtrycket är kraften i dina blodkärl när ditt hjärta slår och när ditt hjärta vilar. Du har högt blodtryck när kraften är för stor. Läkemedel som sänker ditt blodtryck minskar risken att få en stroke eller hjärtinfarkt.
Högt blodtryck gör att hjärtat arbetar hårdare för att pumpa blod genom kroppen och orsakar skador på blodkärlen. MICARDIS 80mg HCT-tabletter kan hjälpa dina blodkärl att slappna av så att ditt blodtryck blir lägre.
Så här öppnar du blistern:
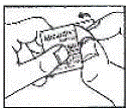
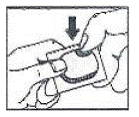
Denna patientinformation har godkänts av US Food and Drug Administration.
