Cordarone 100mg, 50mg Amiodarone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Cordarone 100mg och hur används det?
Cordarone 100mg IV är ett receptbelagt läkemedel som används för att behandla symtom på oregelbunden hjärtrytm (ventrikulära arytmier).
- Cordarone IV kan användas ensamt eller tillsammans med andra läkemedel.
- Cordarone 50mg IV tillhör en klass av läkemedel som kallas Antidysrhythmisc, III.
Vilka är de möjliga biverkningarna av Cordarone 100mg?
Cordarone 100mg kan orsaka allvarliga biverkningar inklusive:
- andnöd,
- svimning,
- snabba eller oregelbundna hjärtslag,
- bröstsmärta,
- väsande andning och
- svårt att andas
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Cordarone 100mg IV inkluderar:
- lågt blodtryck (hypotension),
- långsam puls,
- hjärtstopp,
- illamående,
- feber,
- hjärtsvikt,
- onormal hjärtrytm,
- kardiogen chock och
- avvikelser i leverfunktionstest
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Cordarone. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
VARNING
LUNNG-, LEVER- och HJARTTOXICITET
CORDARONE 100mg är endast avsett att användas till patienter med de indikerade livshotande arytmierna eftersom användningen åtföljs av betydande toxicitet [se INDIKATIONER OCH ANVÄNDNING].
CORDARONE kan orsaka pulmonell toxicitet (överkänslighetspneumonit eller interstitiell/alveolär pneumonit) som har resulterat i kliniskt manifest sjukdom med så höga hastigheter som 17 % hos vissa patientserier. Lungtoxicitet har varit dödlig cirka 10 % av tiden. Skaffa en baslinjeröntgen av thorax och lungfunktionstester, inklusive diffusionskapacitet, när behandlingen med CORDARONE 100 mg påbörjas. Upprepa historia, fysisk undersökning och lungröntgen var 3:e till 6:e månad [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
CORDARONE kan orsaka levertoxicitet, vilket kan vara dödligt. Skaffa baslinje och periodiska levertransaminaser och avbryt eller minska dosen om ökningen överstiger tre gånger det normala, eller fördubblas hos en patient med förhöjd baslinje. Avbryt CORDARONE om patienten upplever tecken eller symtom på klinisk leverskada [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
CORDARONE kan förvärra arytmier. Initiera CORDARONE 50 mg i en klinisk miljö där kontinuerliga elektrokardiogram och hjärträddning är tillgängliga [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER].
BESKRIVNING
CORDARONE (amiodaron HCl) är ett antiarytmiskt läkemedel, tillgängligt för oral administrering som rosa, skårade tabletter innehållande 200 mg amiodaronhydroklorid. De inaktiva ingredienserna som finns är kolloidal kiseldioxid, laktos, magnesiumstearat, povidon, stärkelse och FD&C Red 40. CORDARONE är ett bensofuranderivat: 2-butyl-3-bensofuranyl 4-[2-(dietylamino)-etoxi]-3, 5-dijodfenylketonhydroklorid.
Strukturformeln är som följer:
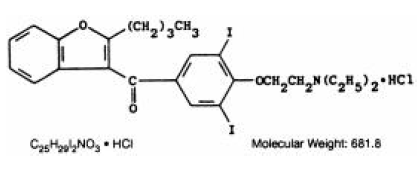
Amiodarone HCl är ett vitt till krämfärgat kristallint pulver. Det är svagt lösligt i vatten, lösligt i alkohol och fritt lösligt i kloroform. Den innehåller 37,3 viktprocent jod.
INDIKATIONER
CORDARONE är indicerat för behandling av dokumenterat, livshotande återkommande ventrikelflimmer och livshotande återkommande hemodynamiskt instabil takykardi hos vuxna som inte har svarat på adekvata doser av andra tillgängliga antiarytmika eller när alternativa medel inte kan tolereras.
DOSERING OCH ADMINISTRERING
Doseringen måste individualiseras baserat på svårighetsgraden av arytmi och respons. Använd den lägsta effektiva dosen. Skaffa baslinjeröntgen thorax, lungfunktionstester, sköldkörtelfunktionstester och leveraminotransferaser. Korrigera hypokalemi, hypomagnesemi och hypokalcemi innan behandlingen påbörjas
Rekommenderad dosering
Inled behandlingen med laddningsdoser på 800 till 1600 mg/dag tills initialt terapeutiskt svar inträffar (vanligtvis 1 till 3 veckor). När arytmikontroll har uppnåtts, eller om biverkningar blir framträdande, reducera dosen CORDARONE 50 mg till 600 till 800 mg/dag under en månad och sedan till underhållsdosen, vanligtvis 400 mg/dag.
Administrering
Administrera CORDARONE konsekvent med avseende på måltider [se KLINISK FARMAKOLOGI ]. Administrering av CORDARONE i uppdelade doser tillsammans med måltider rekommenderas för totala dagliga doser på 1000 mg eller högre, eller när gastrointestinal intolerans uppstår.
HUR LEVERERAS
Doseringsformer och styrkor
200 mg tabletter: runda, konvexa, rosa tabletter med förhöjt "C" och märkta "200" på ena sidan, med baksidan skåra och märkta "WYETH" och "4188".
Förvaring Och Hantering
CORDARONE® (amiodaron HCl) tabletter finns tillgängliga i flaskor med 60 tabletter enligt följande:
200 mg , NDC 0008-4188-04, runda, konvexa, rosa tabletter med ett upphöjt "C" och märkta "200" på ena sidan, med baksidan skåra och märkta "WYETH" och "4188".
Förvara tätt stängd.
Förvara vid kontrollerad rumstemperatur, 20° till 25°C (68° till 77°F).
Skydda från ljus.
Dispensera i en ljusbeständig, tät behållare.
Tillverkad av Sanofi Winthrop Industrie, 1, rue de la Vierge, 33440 Ambares, Frankrike. Distribueras av: Wyeth Pharmaceuticals Inc., ett dotterbolag till Pfizer Inc., Philadelphia, PA 19101. Reviderad: okt 2018
BIEFFEKTER
Följande allvarliga biverkningar beskrivs mer i detalj i andra avsnitt av förskrivningsinformationen:
- Lungtoxicitet [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Leverskada [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Försämrad arytmi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Synnedsättning och synförlust [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Sköldkörtelavvikelser [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Bradykardi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Perifer neuropati [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Ljuskänslighet och missfärgning av huden [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Vid den vanliga underhållsdosen (400 mg/dag) och högre orsakar CORDARONE 100 mg biverkningar hos cirka tre fjärdedelar av alla patienter, vilket resulterar i utsättning hos 7 till 18 %.
I undersökningar av nästan 5 000 patienter som behandlats i öppna amerikanska studier och i publicerade rapporter om behandling med CORDARONE inkluderade de biverkningar som oftast krävde utsättande av CORDARONE lunginfiltrat eller fibros, paroxysmal ventrikulär takykardi, kongestiv hjärtsvikt och förhöjda leverenzymer. Andra symtom som orsakade utsättningar mer sällan inkluderade synstörningar, ljuskänslighet, blå hudmissfärgning, hypertyreos och hypotyreos.
Följande biverkningsfrekvenser är baserade på en retrospektiv studie av 241 patienter som behandlats under 2 till 1 515 dagar (medelvärde 441,3 dagar):
Sköldkörteln
Vanliga: Hypotyreos, hypertyreos.
Kardiovaskulär
Vanliga: Kongestiv hjärtsvikt, hjärtarytmier, SA noddysfunktion.
Gastrointestinala
Mycket vanliga: Illamående, kräkningar.
Vanliga: Förstoppning, anorexi, buksmärtor.
Dermatologiskt
Vanliga: Soleksem/ljuskänslighet.
Neurologisk
Vanliga: sjukdomskänsla och trötthet, tremor/onormala ofrivilliga rörelser, bristande koordination, onormal gång/ataxi, yrsel, parestesier, minskad libido, sömnlöshet, huvudvärk, sömnstörningar.
Oftalmisk
Vanliga: Synstörningar.
Lever
Vanliga: Onormala leverfunktionstester, ospecifika leversjukdomar.
Andningsorgan
Vanliga: Lunginflammation eller fibros.
Övrig
Vanliga: Rodnad, onormal smak och lukt, ödem, onormal salivutsöndring, koagulationsavvikelser.
Mindre vanliga: Blå missfärgning av huden, utslag, spontan ekkymos, alopeci, hypotoni och hjärtöverledningsstörningar.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av CORDARONE efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Hematologiska hemolytisk anemi, aplastisk anemi, pancytopeni, neutropeni, trombocytopeni, agranulocytos, granulom.
Immun : anafylaktisk/anafylaktoid reaktion (inklusive chock), angioödem.
Neurologisk : pseudotumor cerebri, parkinsoniska symtom som akinesi och bradykinesi (ibland reversibel med avbrytande av behandlingen), demyeliniserande polyneuropati.
Psykiatrisk : hallucination, förvirringstillstånd, desorientering, delirium.
Hjärt : hypotoni (ibland dödlig), sinusstopp.
Andningsorgan : eosinofil lunginflammation, akut andnödssyndrom i postoperativ miljö, bronkospasm, bronkiolit obliterans organiserande lunginflammation, lungalveolär blödning, pleural effusion, pleurit.
Gastrointestinala : pankreatit, akut pankreatit.
Lever : hepatit, kolestatisk hepatit, cirros.
Hud och subkutan vävnad urtikaria, toxisk epidermal nekrolys (ibland dödlig), erythema multiforme, Stevens-Johnsons syndrom, exfoliativ dermatit, bullös dermatit, läkemedelsutslag med eosinofili och systemiska symtom (DRESS), eksem, klåda, hudcancer, lupusliknande syndrom.
Muskuloskeletala : myopati, muskelsvaghet, rabdomyolys.
Njur : nedsatt njurfunktion, njurinsufficiens, akut njursvikt.
Reproduktiv : epididymit, impotens.
Kroppen som helhet : feber, muntorrhet.
Endokrina och metabola : sköldkörtelknölar/ sköldkörtelcancer, syndrom av olämplig antidiuretisk hormonsekretion (SIADH).
Kärl : vaskulit.
LÄKEMEDELSINTERAKTIONER
På grund av amiodarons långa halveringstid kan du förvänta dig att läkemedelsinteraktioner kvarstår i veckor till månader efter avslutad behandling med amiodaron.
Läkemedelsinteraktioner med amiodaron beskrivs i Tabell 1 nedan.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Persistens av negativa effekter
På grund av den långa halveringstiden för amiodaron (15 till 142 dagar) och dess aktiva metabolit desetylamiodaron (14 till 75 dagar), kan biverkningar och läkemedelsinteraktioner kvarstå i flera veckor efter avslutad amiodaronbehandling [se KLINISK FARMAKOLOGI ].
Lungtoxicitet
CORDARONE kan orsaka ett kliniskt syndrom av hosta och progressiv dyspné åtföljd av funktionella, röntgenbilder, galliumskanning och patologiska data som överensstämmer med pulmonell toxicitet. Pulmonell toxicitet sekundär till CORDARONE kan vara resultatet av antingen indirekt eller direkt toxicitet som representeras av överkänslighetspneumonit (inklusive eosinofil pneumoni) respektive interstitiell/alveolär pneumonit. Graden av lungtoxicitet har rapporterats vara så hög som 17 % och är dödlig i cirka 10 % av fallen. Skaffa en baslinjeröntgen av thorax och lungfunktionstester, inklusive diffusionskapacitet, när behandlingen med CORDARONE 50 mg påbörjas. Upprepa historia, fysisk undersökning och lungröntgen var 3:e till 6:e månad eller om symtom uppstår. Överväg alternativ antiarytmisk behandling om patienten upplever tecken eller symtom på pulmonell toxicitet. Prednison 40 till 60 mg/dag avsmalnande under flera veckor kan vara till hjälp vid behandling av lungtoxicitet.
Adult Respiratory Distress Syndrome (ARDS)
Postoperativt har förekomster av ARDS rapporterats hos patienter som får CORDARONE-behandling och som har genomgått antingen hjärt- eller icke-hjärtkirurgi. Även om patienter vanligtvis svarar bra på kraftig andningsbehandling, har resultatet i sällsynta fall varit dödligt.
Leverskada
Asymtomatiska förhöjningar av leverenzymnivåer ses ofta, men CORDARONE 100 mg kan orsaka livshotande leverskada. Histologi har liknat alkoholisk hepatit eller cirros. Skaffa baslinje och periodiska levertransaminaser. Om transaminaser överstiger tre gånger det normala, eller fördubblas hos en patient med förhöjd baslinje, avbryt eller minska dosen av CORDARONE 100 mg, skaffa uppföljningstest och behandla på lämpligt sätt.
Förvärrad arytmi
CORDARONE 100 mg kan förvärra den aktuella arytmin hos cirka 2 till 5 % av patienterna eller orsaka nytt kammarflimmer, oupphörlig kammartakykardi, ökat motstånd mot elkonvertering och polymorf kammartakykardi associerad med QTc-förlängning (Torsade dees).
Korrigera hypokalemi, hypomagnesemi och hypokalcemi innan behandling med CORDARONE påbörjas, eftersom dessa störningar kan överdriva graden av QTc-förlängning och öka risken för TdP. Ge särskild uppmärksamhet åt elektrolyt- och syra-basbalansen hos patienter som upplever svår eller långvarig diarré eller som får läkemedel som påverkar elektrolytnivåerna, såsom diuretika, laxermedel, systemiska kortikosteroider eller amfotericin B.
Synnedsättning och synförlust
Optisk neuropati och optisk neurit
Fall av optisk neuropati och optisk neurit, vanligtvis resulterande i synnedsättning och ibland permanent blindhet, har rapporterats hos patienter som behandlats med amiodaron och kan inträffa när som helst under behandlingen. Om symtom på synnedsättning uppträder, såsom förändringar i synskärpa och minskad perifer syn, överväg att avbryta behandlingen med CORDARONE 100 mg och remittera omedelbart för ögonundersökning. Regelbunden oftalmisk undersökning, inklusive funduskopi och spaltlampsundersökning, rekommenderas under administrering av CORDARONE [se NEGATIVA REAKTIONER ].
Korneal mikroavlagringar
Korneala mikroavlagringar förekommer hos majoriteten av vuxna som behandlas med CORDARONE. De är vanligtvis urskiljbara endast genom spaltlampsundersökning, men ger upphov till symtom som synglorier eller dimsyn hos så många som 10 % av patienterna. Korneala mikroavlagringar är reversibla vid minskning av dosen eller avslutande av behandlingen. Enbart asymtomatiska mikroavlagringar är inte en anledning att minska dosen eller avbryta behandlingen [se NEGATIVA REAKTIONER ].
Sköldkörtelavvikelser
CORDARONE 50mg hämmar perifer omvandling av tyroxin (T4) till trijodtyronin (T3) och kan orsaka ökade tyroxinnivåer, minskade T3-nivåer och ökade nivåer av inaktivt omvänt T3 (rT3) hos kliniskt euthyroidpatienter. CORDARONE 50 mg kan orsaka antingen hypotyreos (rapporteras hos upp till 10 % av patienterna) eller hypertyreos (förekommer hos cirka 2 % av patienterna). Övervaka sköldkörtelfunktionen före behandling och regelbundet därefter, särskilt hos äldre patienter, och hos alla patienter med en historia av sköldkörtelknölar, struma eller annan sköldkörteldysfunktion.
Hypertyreos kan inducera genombrott av arytmi. Om några nya tecken på arytmi uppträder bör risken för hypertyreos övervägas. Antityreoidealäkemedel, β-adrenerga blockerare, tillfällig kortikosteroidbehandling kan vara nödvändig för att behandla symtomen på hypertyreos. Verkan av antityreoidealäkemedel kan försenas vid amiodaron-inducerad tyreotoxikos på grund av betydande mängder av förbildade sköldkörtelhormoner som lagras i körteln. Behandling med radioaktiv jod är kontraindicerad på grund av det låga upptaget av radiojod i samband med amiodaron-inducerad hypertyreos. CORDARONE-inducerad hypertyreos kan följas av en övergående period av hypotyreos.
Hypotyreos kan vara primär eller efter upplösning av föregående amiodaroninducerad hypertyreos. Allvarlig hypotyreos och myxödem koma, ibland dödlig, har rapporterats i samband med amiodaronbehandling. Hos vissa patienter behandlade med kliniskt hypotyreoidea amiodaron kan värdena för fritt tyroxinindex vara normala. Hantera hypotyreos genom att minska dosen av eller avbryta behandlingen med CORDARONE och sköldkörtelhormontillskott.
Bradykardi
CORDARONE orsakar symtomatisk bradykardi eller sinusstopp med dämpning av flykthärdar hos 2 till 4 % av patienterna. Risken ökar av elektrolytiska störningar eller användning av samtidig antiarytmika eller negativa kronotroper [se LÄKEMEDELSINTERAKTIONER ]. Bradykardi kan kräva en pacemaker för frekvenskontroll.
Fall av symtomatisk bradykardi efter marknadsföringen, några som kräver insättning av pacemaker och minst en dödlig, har rapporterats när ledipasvir/sofosbuvir eller sofosbuvir med simeprevir påbörjades hos patienter på amiodaron. Bradykardi inträffade vanligen inom timmar till dagar, men i vissa fall upp till 2 veckor efter påbörjad antiviral behandling. Bradykardi försvann i allmänhet efter avslutad antiviral behandling. Mekanismen för denna effekt är okänd. Övervaka hjärtfrekvensen hos patienter som tar eller nyligen avbrutit amiodaron när antiviral behandling påbörjas [se LÄKEMEDELSINTERAKTIONER ].
Implanterbara hjärtenheter
Hos patienter med implanterade defibrillatorer eller pacemakers kan kronisk administrering av antiarytmika påverka stimulerings- eller defibrilleringströskelvärdena. Därför bör trösklar för stimulering och defibrillering bedömas i början av och under behandling med amiodaron.
Fostertoxicitet
CORDARONE kan orsaka fosterskador när det ges till en gravid kvinna. Fosterexponering kan öka risken för hjärt-, sköldkörtel-, neuroutvecklings-, neurologiska och tillväxteffekter hos nyfödda [se Användning i specifika populationer ].
Perifer neuropati
Kronisk administrering av CORDARONE kan leda till perifer neuropati, som kanske inte försvinner när behandlingen med CORDARONE sätts ut.
Ljuskänslighet och missfärgning av huden
CORDARONE inducerar fotosensibilisering hos cirka 10 % av patienterna; visst skydd kan ges solskyddskrämer eller skyddskläder. Vid långtidsbehandling kan en blågrå missfärgning av den exponerade huden uppstå. Risken kan vara ökad hos patienter med ljus hy eller de med överdriven solexponering. Viss vändning av missfärgning kan inträffa vid utsättande av läkemedel.
Kirurgi
Flyktiga anestesimedel
Patienter som behandlas med CORDARONE 100 mg kan vara mer känsliga för de myokarddepressiva och ledningseffekterna av halogenerade inhalationsanestetika.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( Läkemedelsguide ).
Informera gravida kvinnor om den potentiella risken för ett foster. Rekommendera kvinnor med reproduktionspotential att informera sin förskrivare om en känd eller misstänkt graviditet [se Användning i specifika populationer ].
Informera kvinnor om att amning inte rekommenderas under behandling med CORDARONE [se Användning i specifika populationer ].
Rekommendera patienter att undvika grapefruktjuice och johannesört.
Rekommendera patienter att söka läkarvård om de upplever tecken och symtom på lungtoxicitet, försämrad arytmi, bradykardi, synnedsättning eller hypo- och hypertyreos.
Denna produkts etikett kan ha uppdaterats. För fullständig förskrivningsinformation, besök www.pfizer.com.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Amiodaron HCl var associerad med en statistiskt signifikant dosrelaterad ökning av förekomsten av sköldkörteltumörer (follikulärt adenom och/eller karcinom) hos råttor. Incidensen av sköldkörteltumörer var högre än kontrollen vid den lägsta testade dosnivån, dvs. 5 mg/kg/dag (cirka 0,08 gånger den maximala rekommenderade humana underhållsdosen*).
Mutagenicitetsstudier (Ames, mikronukleus och lysogena tester) med CORDARONE var negativa.
I en studie där amiodaron HCl administrerades till han- och honråttor, med början 9 veckor före parning, observerades minskad fertilitet vid en dosnivå på 90 mg/kg/dag (ungefär 1,4 gånger den maximala rekommenderade humana underhållsdosen*).
*600 mg hos en patient på 60 kg (dos jämfört med kroppsyta)
Användning i specifika populationer
Graviditet
Risksammanfattning
Tillgängliga data från rapporter efter marknadsföring och publicerade fallserier indikerar att användning av amiodaron hos gravida kvinnor kan öka risken för fosterbiverkningar inklusive neonatal hypo- och hypertyreos, neonatal bradykardi, neuroutvecklingsavvikelser, för tidig födsel och fostertillväxtbegränsning. Amiodaron och dess metabolit, desetylamiodaron (DEA), passerar placentan. Obehandlade underliggande arytmier, inklusive ventrikulära arytmier, under graviditeten utgör en risk för modern och fostret (se Kliniska överväganden ). I djurstudier resulterade administrering av amiodaron till kaniner, råttor och möss under organogenes i embryofetal toxicitet vid doser lägre än den maximala rekommenderade underhållsdosen för människor (se Data ). Informera gravida kvinnor om den potentiella risken för ett foster.
Den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall för den indikerade populationen är okänd. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2%-4% respektive 15%-20%.
Kliniska överväganden
Sjukdomsrelaterad risk för mödrar och embryo/foster
Förekomsten av ventrikulär takykardi är ökad och kan vara mer symtomatisk under graviditet. Ventrikulära arytmier förekommer oftast hos gravida kvinnor med underliggande kardiomyopati, medfödd hjärtsjukdom, hjärtklaffsjukdom eller mitralisklaffframfall. De flesta takykardiepisoder initieras av ektopiska slag och förekomsten av arytmiepisoder kan därför öka under graviditeten på grund av den ökade benägenheten till ektopisk aktivitet. Genombrottsarytmier kan också förekomma under graviditet, eftersom terapeutiska behandlingsnivåer kan vara svåra att upprätthålla på grund av den ökade distributionsvolymen och ökad läkemedelsmetabolism som är inneboende i det gravida tillståndet.
Fetala/neonatala biverkningar
Amiodaron och dess metabolit har visats passera placentan. Skadliga fostereffekter associerade med maternell amiodaronanvändning under graviditet kan inkludera neonatal bradykardi, QT-förlängning och periodiska ventrikulära extrasystoler, neonatal hypotyreos (med eller utan struma) som upptäcks antenatalt eller hos det nyfödda och rapporteras även efter några dagars exponering, neonatal hypertyroxinemi, neuroutvecklingsavvikelser oberoende av sköldkörtelfunktionen, inklusive talförseningar och svårigheter med skriftspråk och aritmetik, försenad motorisk utveckling och ataxi, rycknystagmus med synkron huvudtitubation, fostertillväxtbegränsning och för tidig födsel. Övervaka det nyfödda barnet för tecken och symtom på sköldkörtelstörningar och hjärtarytmier.
Arbete och leverans
Risken för arytmier kan öka under förlossningen och förlossningen. Patienter som behandlas med CORDARONE bör övervakas kontinuerligt under förlossningen och förlossningen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Data
Djurdata
Hos dräktiga råttor och kaniner under organogenesperioden hade amiodaron HCl i doser på 25 mg/kg/dag (cirka 0,4 respektive 0,9 gånger den maximala rekommenderade humana underhållsdosen*) inga negativa effekter på fostret. Hos kanin orsakade 75 mg/kg/dag (cirka 2,7 gånger den maximala rekommenderade humana underhållsdosen*) aborter hos mer än 90 % av djuren. Hos råtta var doser på 50 mg/kg/dag eller mer associerade med lätt förskjutning av testiklarna och en ökad förekomst av ofullständig förbening av vissa skalle och digitala ben; vid 100 mg/kg/dag eller mer reducerades fostrets kroppsvikt; vid 200 mg/kg/dag fanns en ökad förekomst av fosterresorption. (Dessa doser hos råtta är cirka 0,8, 1,6 och 3,2 gånger den maximala rekommenderade humana underhållsdosen*) Biverkningar på fostrets tillväxt och överlevnad noterades också i en av två mössstammar vid en dos av 5 mg/kg/dag ( cirka 0,04 gånger den maximala rekommenderade underhållsdosen för människor*).
*600 mg hos en patient på 60 kg (doser jämfört med kroppsyta)
Laktation
Risksammanfattning
Amiodaron och en av dess huvudmetaboliter, DEA, finns i bröstmjölk i mellan 3,5 % och 45 % av moderns viktjusterade dos av amiodaron. Det finns fall av hypotyreos och bradykardi hos ammade spädbarn, även om det är oklart om dessa effekter beror på amiodaronexponering i bröstmjölk. Amning rekommenderas inte under behandling med CORDARONE [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Kvinnor Och Hanar Av Reproduktionspotential
Infertilitet
Baserat på fertilitetsstudier hos djur kan CORDARONE minska kvinnlig och manlig fertilitet. Det är inte känt om denna effekt är reversibel. [ser Icke-klinisk toxikologi ].
Pediatrisk användning
Säkerheten och effektiviteten av CORDARONE hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Normala försökspersoner över 65 år uppvisar lägre clearance och ökad läkemedelshalveringstid än yngre försökspersoner [se KLINISK FARMAKOLOGI ]. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling.
ÖVERDOS
Det har förekommit fall, några med dödlig utgång, av överdosering av CORDARONE 50 mg.
Övervaka patientens hjärtrytm och blodtryck, och om bradykardi uppstår kan en β-adrenerg agonist eller en pacemaker användas. Behandla hypotoni med otillräcklig vävnadsperfusion med positiva inotropa och vasopressormedel. Varken CORDARONE 50mg eller dess metabolit är dialyserbara.
KONTRAINDIKATIONER
- Kardiogen chock.
- Sick sinus syndrome, andra eller tredje gradens atrioventrikulära blockering, bradykardi som leder till synkope utan fungerande pacemaker.
- Känd överkänslighet mot läkemedlet eller mot någon av dess komponenter, inklusive jod.
KLINISK FARMAKOLOGI
Handlingsmekanism
Amiodaron anses vara ett klass III antiarytmiskt läkemedel, men det har elektrofysiologiska egenskaper från alla fyra Vaughan Williams klasser. Liksom klass I-läkemedel blockerar amiodaron natriumkanaler vid snabba pacing-frekvenser, och precis som klass II-läkemedel utövar amiodaron en icke-kompetitiv antisympatisk verkan. En av dess huvudsakliga effekter, vid långvarig administrering, är att förlänga hjärtverkan, en klass III-effekt. Den negativa kronotropiska effekten av amiodaron i nodalvävnad liknar effekten av klass IV-läkemedel. Förutom att blockera natriumkanaler, blockerar amiodaron myokardial kaliumkanaler, vilket bidrar till att bromsa ledning och förlänga refraktäritet. Den antisympatiska verkan och blockeringen av kalcium- och kaliumkanaler är ansvariga för de negativa dromotropa effekterna på sinusknutan och för att bromsa ledningen och förlänga refraktäriteten i den atrioventrikulära (AV) noden. Dess vasodilaterande verkan kan minska hjärtarbetsbelastningen och följaktligen myokardial syreförbrukning.
CORDARONE förlänger varaktigheten av aktionspotentialen för alla hjärtfibrer samtidigt som den orsakar minimal minskning av dV/dt (maximal uppslagshastighet för aktionspotentialen). Den refraktära perioden förlängs i alla hjärtvävnader. CORDARONE ökar hjärtrefraktärperioden utan att påverka vilomembranpotentialen, förutom i automatiska celler där prepotentialens lutning är reducerad, vilket i allmänhet minskar automaticiteten. Dessa elektrofysiologiska effekter återspeglas i en minskad sinusfrekvens på 15 till 20 %, ökade PR- och QT-intervall på cirka 10 %, utveckling av U-vågor och förändringar i T-vågskontur. Dessa förändringar bör inte kräva utsättande av CORDARONE 50 mg eftersom de är bevis på dess farmakologiska verkan, även om CORDARONE kan orsaka markant sinusbradykardi eller sinusstopp och hjärtblockering [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Hemodynamik
djurstudier och efter intravenös administrering på människa slappnar CORDARONE 100mg av vaskulär glatt muskulatur, minskar perifert vaskulärt motstånd (efterbelastning) och ökar hjärtindex något. Efter oral dosering ger CORDARONE 100 mg dock ingen signifikant förändring i vänsterkammars ejektionsfraktion (LVEF), även hos patienter med deprimerad LVEF. Efter akut intravenös dosering till människa kan CORDARONE 100 mg ha en mild negativ inotrop effekt.
Farmakodynamik
Det finns inget väletablerat samband mellan plasmakoncentration och effektivitet, men det verkar som om koncentrationer mycket under 1 mg/L ofta är ineffektiva och att nivåer över 2,5 mg/L i allmänhet inte behövs. Plasmakoncentrationsmätningar kan användas för att identifiera patienter vars nivåer är ovanligt låga, och som kan dra nytta av en dosökning, eller ovanligt hög, och som kan ha dosreduktion i hopp om att minimera biverkningar.
Effekter på onormala rytmer ses inte förrän efter 2 till 3 dagar och kräver vanligtvis 1 till 3 veckor, även när en laddningsdos används. Det kan finnas en fortsatt ökning av effekten under längre perioder fortfarande. Det finns bevis för att tiden till effekt är kortare när en laddningsdosregim används.
I enlighet med den långsamma elimineringshastigheten kvarstår antiarytmiska effekter i veckor eller månader efter att CORDARONE 50 mg har avbrutits, men tiden för återfall är varierande och oförutsägbar. I allmänhet, när läkemedlet återupptas efter återfall av arytmin, etableras kontroll relativt snabbt jämfört med det initiala svaret, förmodligen på grund av att vävnadslagren inte var helt uttömda.
Farmakokinetik
Absorption
Efter oral administrering till människor absorberas CORDARONE långsamt och varierande. Biotillgängligheten för CORDARONE är cirka 50 %. Maximala plasmakoncentrationer uppnås 3 till 7 timmar efter en engångsdos. Plasmakoncentrationer med kronisk dosering vid 100 till 600 mg/dag är ungefär dosproportionella, med en genomsnittlig ökning på 0,5 mg/L för varje 100 mg/dag. Dessa medel innefattar emellertid avsevärd individuell variation.
Mat ökar hastigheten och graden av absorption av CORDARONE. Effekterna av mat på biotillgängligheten av CORDARONE har studerats hos 30 friska försökspersoner som fick en engångsdos på 600 mg omedelbart efter att ha ätit en fettrik måltid och efter en fasta över natten. Ytan under plasmakoncentration-tidkurvan (AUC) och maximal plasmakoncentration (Cmax) för amiodaron ökade med 2,3 (intervall 1,7 till 3,6) respektive 3,8 (intervall 2,7 till 4,4) gånger i närvaro av föda. Mat ökade också absorptionshastigheten av amiodaron, vilket minskade tiden till maximal plasmakoncentration (Tmax) med 37 %. Medel-AUC och medel-Cmax för huvudmetaboliten av amiodaron, DEA ökade med 55 % (intervall 58 till 101 %) respektive 32 % (intervall 4 till 84 %), men det var ingen förändring i Tmax i närvaro av mat.
Distribution
CORDARONE är mycket proteinbundet (cirka 96%). CORDARONE har en mycket stor men varierande distributionsvolym, i genomsnitt cirka 60 L/kg, på grund av omfattande ackumulering på olika platser, särskilt fettvävnad och starkt perfunderade organ, såsom lever, lunga och mjälte.
En huvudmetabolit av CORDARONE 50mg, DEA, har identifierats hos människa; den ackumuleras i ännu större utsträckning i nästan alla vävnader. Det finns inga tillgängliga data om aktiviteten av DEA hos människor, men hos djur har den signifikanta elektrofysiologiska och antiarytmiska effekter som i allmänhet liknar amiodaron i sig. DEA:s exakta roll och bidrag till den antiarytmiska aktiviteten av oralt amiodaron är inte säkra. Utvecklingen av maximal ventrikulär klass III-effekt efter oral administrering av CORDARONE 100 mg hos människor korrelerar närmare med DEA-ackumulering över tiden än med amiodaronackumulering.
Eliminering
Efter administrering av engångsdos till 12 friska försökspersoner uppvisade CORDARONE multikompartmentell farmakokinetik med en genomsnittlig skenbar terminal eliminationshalveringstid i plasma på 58 dagar (intervall 15 till 142 dagar) för amiodaron och 36 dagar (intervall 14 till 75 dagar) för den aktiva metabolit (DEA). Hos patienter har CORDARONE 100 mg, efter utsättning av kronisk oral behandling, visat sig ha en bifasisk eliminering med en initial 50 % minskning av plasmanivåerna efter 2,5 till 10 dagar. En mycket långsammare terminal plasmaelimineringsfas visar en halveringstid för modersubstansen som sträcker sig från 26 till 107 dagar, med ett medelvärde på cirka 53 dagar och de flesta patienter i intervallet 40 till 55 dagar. I avsaknad av en laddningsdosperiod skulle steady-state plasmakoncentrationer, vid konstant oral dosering, därför nås mellan 130 och 535 dagar, med ett genomsnitt på 265 dagar. För metaboliten var den genomsnittliga plasmaelimineringshalveringstiden cirka 61 dagar. Dessa data återspeglar troligen en initial eliminering av läkemedel från välperfunderad vävnad (halveringstiden på 2,5 till 10 dagar), följt av en terminal fas som representerar extremt långsam eliminering från dåligt perfunderade vävnadsavdelningar såsom fett.
Den avsevärda variationen mellan individer i båda faserna av eliminering, såväl som osäkerheten om vilken del som är avgörande för läkemedelseffekten, kräver uppmärksamhet på individuella svar när arytmikontroll har uppnåtts med laddningsdoser eftersom den korrekta underhållsdosen bestäms, delvis, av elimineringsgraden. Anpassa underhållsdoser av CORDARONE [se DOSERING OCH ADMINISTRERING ].
Ämnesomsättning
Amiodaron metaboliseras till DEA av cytokrom P450 (CYP) enzymgruppen, specifikt CYP3A och CYP2C8. CYP3A-isoenzymet finns i både levern och tarmarna. In vitro uppvisar amiodaron och DEA en potential att hämma CYP2C9, CYP2C19, CYP2D6, CYP3A, CYP2A6, CYP2B6 och CYP2C8. Amiodaron och DEA har också en potential att hämma vissa transportörer såsom P-glykoprotein och organiska katjontransportörer (OCT2).
Exkretion
Amiodaron elimineras primärt genom levermetabolism och gallutsöndring och det finns försumbar utsöndring av amiodaron eller DEA i urinen. Varken amiodaron eller DEA är dialyserbara.
Specifika populationer
Effekt Av Ålder
Normala försökspersoner över 65 år visar lägre clearance (ca 100 ml/timme/kg) än yngre försökspersoner (ca 150 ml/timme/kg) och en ökning av t½ från ca 20 till 47 dagar.
Nedsatt njurfunktion
Nedsatt njurfunktion påverkar inte farmakokinetiken för amiodaron eller DEA.
Nedsatt leverfunktion
Efter en engångsdos av intravenös amiodaron till cirrospatienter ses signifikant lägre Cmax- och genomsnittliga koncentrationsvärden för DEA, men genomsnittliga amiodaronnivåer är oförändrade.
Hjärtsjukdom
Hos patienter med allvarlig vänsterkammardysfunktion förändras amiodarons farmakokinetik inte signifikant men den terminala elimineringen t½ av DEA förlängs.
Även om ingen dosjustering för patienter med njur-, lever- eller hjärtavvikelser har definierats under kronisk behandling med oralt amiodaron, är noggrann klinisk övervakning lämplig för äldre patienter och de med svår vänsterkammardysfunktion.
Läkemedelsinteraktioner
Effekter av andra medel på Amiodaron
Grapefruktjuice: Grapefruktjuice som gavs till friska frivilliga ökade AUC för amiodaron med 50 % och Cmax med 84 % och minskade DEA till okvantifierbara koncentrationer.
Cimetidin hämmar CYP3A och kan öka amiodaronnivåerna i serum.
Kolestyramin minskar den enterohepatiska cirkulationen av amiodaron och ökar därmed elimineringen. Detta resulterar i minskade amiodaron-serumnivåer och halveringstid.
Effekter av amiodaron på medel
CYP3A-substrat
Amiodaron som tas samtidigt med kinidin ökar kinidinserumkoncentrationen med 33 % efter två dagar. Amiodaron som tas samtidigt med prokainamid under mindre än sju dagar ökar plasmakoncentrationerna av prokainamid och n-acetylprokainamid med 55 % respektive 33 %.
Loratadin, ett icke-sederande antihistamin, metaboliseras huvudsakligen av CYP3A och dess metabolism kan hämmas av amiodaron.
Metabolism av lidokain kan hämmas av amiodaron.
Cyklofosfamid är en prodrug som metaboliseras av CYP450 inklusive CYP3A till en aktiv metabolit. Metabolismen av cyklofosfamid kan hämmas av amiodaron.
Klopidogrel, en inaktiv tienopyridin-prodrug, metaboliseras i levern av CYP3A till en aktiv metabolit. En potentiell interaktion mellan klopidogrel och amiodaron som resulterar i ineffektiv hämning av trombocytaggregationen har rapporterats.
Makrolid/Ketolid antibiotika
Amiodaron kan hämma metabolismen av makrolid/ketolid-antibiotika (förutom azitromycin) och systemiska azol-antimykotika.
P-glykoproteinsubstrat
Amiodaron som tas samtidigt med digoxin ökar digoxinkoncentrationen i serum med 70 % efter en dag.
Dabigatran etexilat när det tas samtidigt med oralt amiodaron kan resultera i förhöjd serumkoncentration av dabigatran.
Dextrometorfan är ett substrat för både CYP2D6 och CYP3A. Amiodaron hämmar CYP2D6. Kronisk (> 2 veckor) oral administrering av amiodaron försämrar metabolismen av dextrometorfan kan leda till ökade serumkoncentrationer.
PATIENTINFORMATION
CORDARONE® (KOR-DU-RON) (amiodaron) tabletter
Vilken är den viktigaste informationen jag borde veta om CORDARONE 50mg?
CORDARONE kan orsaka allvarliga biverkningar som kan leda till döden, inklusive:
- lungproblem
- leverproblem
- förvärrade hjärtslagsproblem
Ring din vårdgivare eller få medicinsk hjälp omedelbart om du har något av följande symtom under behandling med CORDARONE:
- andningssvårigheter, väsande andning, andnöd, hostande bröstsmärtor, blodspott eller feber
- illamående eller kräkningar, brun eller mörkfärgad urin, känner dig tröttare än vanligt, gulfärgning av huden eller ögonvitorna (gulsot), eller smärta i övre högra delen av magen
- hjärtat slår, hoppar över ett slag, slår snabbt eller långsamt, känner dig yr i huvudet eller om du svimmar
- synproblem, inklusive dimsyn, se glorier eller dina ögon blir ljuskänsliga. Du bör göra regelbundna ögonundersökningar före och under behandlingen med CORDARONE.
CORDARONE bör startas på sjukhus så att ditt medicinska tillstånd kan övervakas noggrant.
CORDARONE ska endast användas för att behandla personer som har diagnostiserats med livshotande hjärtslagsproblem som kallas ventrikulära arytmier, när andra behandlingar inte fungerade eller du inte kan tolerera dem.
CORDARONE 50mg kan orsaka andra allvarliga biverkningar. Se "Vilka är de möjliga biverkningarna av CORDARONE 100mg?" Om du får allvarliga biverkningar under behandlingen kan du behöva sluta med CORDARONE, få din dos ändrad eller få medicinsk behandling. Prata med din läkare innan du slutar ta CORDARONE.
Du kan fortfarande få biverkningar efter att du slutat med CORDARONE eftersom läkemedlet stannar kvar i kroppen i månader efter att behandlingen avslutats.
Du bör göra regelbundna kontroller, blodprover, lungröntgen före och under behandling med CORDARONE 100mg för att kontrollera om det finns allvarliga biverkningar. Du bör också genomgå lungfunktionstester innan behandlingen med CORDARONE påbörjas.
Vad är CORDARONE?
CORDARONE är ett receptbelagt läkemedel som används för att behandla personer som har diagnostiserats med livshotande hjärtslagsproblem som kallas ventrikulära arytmier, när andra behandlingar inte fungerade eller du inte kan tolerera dem. Det är inte känt om CORDARONE är säkert och effektivt hos barn.
Vem bör inte ta CORDARONE 100mg?
Ta inte CORDARONE 100 mg om du:
- har ett allvarligt hjärtproblem som kallas kardiogen chock
- har vissa typer av hjärtsjukdomar som kallas hjärtblock, med eller utan långsam puls
- har en långsam puls med yrsel eller yrsel och du inte har en inopererad pacemaker
- är allergisk mot amiodaron, jod eller något av övriga innehållsämnen i CORDARONE. Se slutet av denna medicinguide för en komplett lista över ingredienser i CORDARONE.
Innan du tar CORDARONE 100mg, berätta för din vårdgivare om alla dina medicinska tillstånd, inklusive om du:
- har lung- eller andningsproblem
- har leverproblem
- har eller haft problem med sköldkörteln
- har långsam puls eller blodtrycksproblem
- har diarré eller har haft diarré under en längre tid
- har fått veta att du har låga nivåer av kalium, magnesium eller kalcium i blodet
- har en implanterad pacemaker eller defribrillator
- om du planerar att opereras med narkos
- är gravid eller planerar att bli gravid. CORDARONE kan skada ditt ofödda barn. Berätta omedelbart för din vårdgivare om du blir gravid under behandling med CORDARONE. CORDARONE 100mg kan stanna i din kropp i månader efter att behandlingen avslutats.
- ammar eller planerar att amma. CORDARONE 100 mg kan passera över i din bröstmjölk och kan skada ditt barn. Du bör inte amma medan du tar CORDARONE. CORDARONE kan stanna i din kropp i månader efter att behandlingen har avslutats. Prata med din vårdgivare om det bästa sättet att mata ditt barn under denna tid.
Berätta för din vårdgivare om alla läkemedel du tar inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. CORDARONE 50mg och vissa andra läkemedel kan påverka varandra och orsaka allvarliga biverkningar. Du kan be din apotekspersonal om en lista över läkemedel som interagerar med CORDARONE.
Hur ska jag ta CORDARONE?
- När du skrivs ut från sjukhuset, ta CORDARONE exakt som din läkare säger åt dig att ta det.
- Din vårdgivare kommer att tala om för dig hur mycket CORDARONE du ska ta och när du ska ta det.
- Din vårdgivare kan ändra din dos av CORDARONE 50 mg vid behov om din hjärtrytm är kontrollerad eller om du har vissa biverkningar. Din vårdgivare bör övervaka dig noggrant när din dos av CORDARONE 50 mg ändras.
- Ta din dos CORDARONE på samma sätt varje gång, antingen med eller utan mat.
- Om du tar för mycket CORDARONE 100 mg, ring din vårdgivare eller gå till närmaste akutmottagning direkt. Om du missar en dos, vänta och ta din nästa dos vid normal tid. Ta inte två doser samtidigt. Fortsätt med din nästa regelbundna dos.
Vad ska jag undvika när jag tar CORDARONE?
- Undvik att dricka grapefruktjuice under behandling med CORDARONE. Att dricka grapefruktjuice med CORDARONE 50 mg kan öka mängden CORDARONE i ditt blod, och detta kan leda till biverkningar.
- CORDARONE 100mg kan göra din hud känslig för solljus. Du kan få kraftig solbränna. Använd solkräm och bär en hatt och kläder som täcker din hud för att skydda dig om du måste vara i solljus. Prata med din sjukvård om du blir solbränd. Se "Hudproblem" i avsnittet Läkemedelsguide "Vilka är de möjliga biverkningarna av CORDARONE?" Nedan.
Vilka är de möjliga biverkningarna av CORDARONE?
CORADARONE kan orsaka allvarliga biverkningar, inklusive:
- Ser "Vilken är den viktigaste informationen jag borde veta om CORDARONE?"
- Nervproblem. CORDARONE 100mg kan orsaka nervproblem. Ring din vårdgivare om du utvecklar symtom på nervproblem, inklusive: en känsla av "nålar" eller domningar i dina händer, ben eller fötter, muskelsvaghet, okontrollerade rörelser, dålig koordination eller problem med att gå.
- Hudproblem. CORDARONE kan göra att din hud blir känsligare för solen eller får en blågrå färg. Människor som har ljus hy eller personer som utsätts för mycket sol kan vara mer utsatta för dessa hudproblem. En del av den blågrå hudfärgen kan återgå till det normala efter att ha slutat med CORDARONE.
- Sköldkörtelproblem. CORDARONE kan orsaka att du antingen har nedsatt sköldkörtelfunktion (hypotyreos), som ibland kan vara allvarlig, eller en överaktiv sköldkörtel (hypertyreos), som kan vara allvarlig.
- Om du utvecklar nedsatt sköldkörtelfunktion under behandling med CORDARONE, kan din vårdgivare behöva minska din dos eller avbryta behandlingen med CORDARONE, och eventuellt ordinera medicin för att ersätta ditt sköldkörtelhormon.
- En överaktiv sköldkörtel kan få dig att producera för mycket sköldkörtelhormon. Du kan få onormala hjärtslag även när du får CORDARONE. Din vårdgivare kan ordinera vissa läkemedel för att behandla din överaktiva sköldkörtel. Ring din vårdgivare om du får onormala hjärtslag under behandlingen med CORDARONE. Det kan innebära att du har en överaktiv sköldkörtel.
- Din vårdgivare bör göra tester för att kontrollera din sköldkörtelfunktion innan du börjar och under behandlingen med CORDARONE.
- Ring din vårdgivare om du utvecklar något av följande symtom på sköldkörtelproblem under behandling med CORDARONE:
- svaghet
- viktminskning eller viktökning
- värme- eller kylaintolerans
- hårtunnande
- svettas
- förändringar i din menstruation
- svullnad i nacken (struma)
- nervositet
- irritabilitet
- rastlöshet
- minskad koncentration
- känna sig deprimerad (hos äldre)
- darrning
De vanligaste biverkningarna av CORDARONE inkluderar:
- lungproblem
- hjärtslagsproblem
- hjärtproblem
- leverproblem
CORDARONE 50 mg kan påverka fertiliteten hos män och kvinnor. Det är inte känt om effekterna är reversibla. Prata med din vårdgivare om du är orolig för fertilitet.
Dessa är inte alla möjliga biverkningar av CORDARONE. För mer information, fråga din vårdgivare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara CORDARONE?
- Förvara CORDARONE 100mg i rumstemperatur mellan 20° till 25°C (68° till 77°F).
- Förvara CORDARONE i en väl tillsluten behållare och förvara CORDARONE 50 mg borta från ljuset.
Förvara CORDARONE 50mg och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av CORDARONE
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en läkemedelsguide. Använd inte CORDARONE för ett tillstånd som det inte har ordinerats för. Ge inte CORDARONE till andra personer, även om de har samma symtom som du har. Det kan skada dem. Du kan fråga din apotekspersonal eller vårdgivare om information om CORDARONE som är skriven för vårdpersonal.
Vilka är ingredienserna i CORDARONE 100mg?
Aktiv beståndsdel: amiodaron HCl
Inaktiva Ingredienser: kolloidal kiseldioxid, laktos, magnesiumstearat, povidon, stärkelse och FD&C Red 40.
Denna medicineringsguide har godkänts av US Food and Drug Administration.
