Cartia XT 180mg Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Cartia och hur används det?
Cartia är ett receptbelagt läkemedel som används för att behandla symtomen bröstsmärta (kärlkramp), högt blodtryck (hypertoni), paroxysmal supraventrikulär takykardi och förmaksflimmer (fladder). Cartia kan användas ensamt eller tillsammans med andra läkemedel.
Cartia tillhör en klass av läkemedel som kallas Antidysrhythmics, IV; Kalciumkanalblockerare; Kalciumkanalblockerare, icke-dihydropyridin.
Vilka är de möjliga biverkningarna av Cartia?
Cartia kan orsaka allvarliga biverkningar inklusive:
- bröstsmärta,
- långsamma hjärtslag,
- bultande hjärtslag,
- fladdrande i ditt bröst,
- yrsel,
- svullnad,
- snabb viktökning,
- andnöd,
- feber,
- öm hals,
- brännande ögon,
- hudsmärta och
- röda eller lila hudutslag med blåsor och fjällning
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Cartia inkluderar:
- lätt huvudvärk,
- lätt yrsel och
- förkylningssymtom (täppt näsa, nysningar, ont i halsen)
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Cartia. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Diltiazemhydroklorid är en cellulär inflödeshämmare av kalciumjoner (långsam kanalblockerare eller kalciumantagonist). Kemiskt är diltiazemhydroklorid 1,5-bensotiazepin-4(5H)on,3-(acetyloxi)-5-[2-(dimetylamino)etyl]-2,3-dihydro-2-(4-metoxifenyl)-, monohydroklorid ,(+)-cis-. Den kemiska strukturen är:
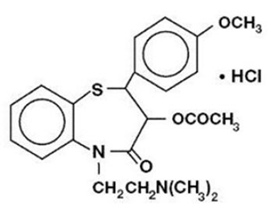
Diltiazemhydroklorid är ett vitt till benvitt kristallint pulver med en bitter smak. Det är lösligt i vatten, metanol och kloroform. Den har en molekylvikt på 450,98. Diltiazemhydroklorid kapsel med förlängd frisättning (dosering en gång dagligen) är formulerad som en kapsel med förlängd frisättning en gång om dagen innehållande 120 mg, 180 mg, 240 mg eller 300 mg diltiazemhydroklorid.
Dessutom innehåller varje kapsel följande inaktiva ingredienser: acetyltributylcitrat, ammoniometakrylatsampolymer-NF, D & C Red #28, D & C Yellow #10, D & C Yellow #10 Aluminium Lake, etylcellulosa, FD & C Blue #1 Aluminium Lake, FD & C Blue #2 Aluminium Lake, FD & C Red #40, FD & C Red #40 Aluminium Lake, gelatin-NF, magnesiumstearat, metakrylsyrasampolymer-NF, propylenglykol, polysorbat 80-NF, stärkelse sackaros, talk USP och titandioxid. Kapslarna på 180 mg och 240 mg innehåller gul järnoxid. Dessutom innehåller 240 mg kapseln även svart järnoxid och röd järnoxid.
För oral administrering.
Detta läkemedel uppfyller USP Drug Release 9.
INDIKATIONER
Diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) är indicerade för behandling av hypertoni. Det kan användas ensamt eller i kombination med andra antihypertensiva läkemedel.
Diltiazemhydroklorid kapslar med förlängd frisättning USP (en gång om dagen) är indicerat för behandling av kronisk stabil angina och angina på grund av kranskärlspasm.
DOSERING OCH ADMINISTRERING
Patienter som kontrolleras på enbart diltiazem eller i kombination med andra läkemedel kan bytas till diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) vid närmaste ekvivalenta totala dagliga dos. Högre doser av diltiazemhydroklorid USP-kapslar med förlängd frisättning (en gång om dagen) kan behövas hos vissa patienter. Patienter bör övervakas noggrant. Efterföljande titrering till högre eller lägre doser kan vara nödvändig och bör initieras om det är kliniskt motiverat. Det finns begränsad generell klinisk erfarenhet av doser över 360 mg, men doser till 540 mg har studerats i kliniska prövningar. Förekomsten av biverkningar ökar när dosen ökar med första gradens AV-block, yrsel och sinusbradykardi som har det starkaste sambandet med dosen.
Hypertoni
Doseringen måste justeras genom titrering till individuella patientbehov. När det används som monoterapi är rimliga startdoser 180 till 240 mg en gång dagligen, även om vissa patienter kan svara på lägre doser. Maximal antihypertensiv effekt observeras vanligtvis efter 14 dagars kronisk terapi; därför bör dosjusteringar planeras i enlighet med detta. Det vanliga dosintervallet som studerades i kliniska prövningar var 240 till 360 mg en gång dagligen. Enskilda patienter kan svara på högre doser på upp till 480 mg en gång dagligen.
Angina
Doser för behandling av angina bör anpassas till varje patients behov, med början med en dos på 120 eller 180 mg en gång dagligen. Enskilda patienter kan svara på högre doser på upp till 480 mg en gång dagligen. Vid behov kan titrering utföras under en period på 7 till 14 dagar.
Diltiazem Hydrochloride USP kapslar med förlängd frisättning (dosering en gång om dagen)
Samtidig användning med andra kardiovaskulära medel
HUR LEVERERAS
OBS: PRODUKTEN KAN HA EN LUKT.
Lagringsförhållanden
Förvara vid 20° till 25°C (68° till 77°F) [Se USP-kontrollerad rumstemperatur ].
Undvik överdriven luftfuktighet.
Fördela i tät, ljusbeständig behållare enligt definitionen i USP.
Tillverkad av: Actavis Laboratories FL, Inc., Fort Lauderdale, FL 33314 USA. Distribueras av: Actavis Pharma, Inc., Parsippany, NJ 07054 USA. Reviderad: dec 2014
BIEFFEKTER
Allvarliga biverkningar har varit sällsynta i studier som hittills genomförts, men det bör noteras att patienter med nedsatt ventrikulär funktion och hjärtledningsstörningar vanligtvis har uteslutits från dessa studier.
Följande tabell visar de vanligaste biverkningarna som rapporterats i placebokontrollerade angina- och hypertonistudier hos patienter som får diltiazemhydroklorid förlängd frisättning av kapsel (dosering en gång om dagen) upp till 360 mg med frekvenser hos placebopatienter som visas för jämförelse.
Diltiazem Hydrochloride Kapsel med förlängd frisättning (en gång om dagen) Placebokontrollerade kärlkramp- och hypertoniförsök kombinerade
kliniska prövningar av diltiazemhydroklorid depotkapslar (en gång om dagen), diltiazemhydrokloridtabletter och diltiazemhydroklorid depotkapslar som involverade över 3200 patienter, var de vanligaste händelserna (dvs mer än 1%) ödem (4,6 %) , huvudvärk (4,6 %), yrsel (3,5 %), asteni (2,6 %), första gradens AV-block (2,4 %), bradykardi (1,7 %), rodnad (1,4 %), illamående (1,4 %) och utslag ( 1,2 %).
Dessutom rapporterades följande händelser sällan (mindre än 1%) i angina- eller hypertonistudier:
Kardiovaskulär: Angina, arytmi, AV-block (andra eller tredje graden), grenblock, kongestiv hjärtsvikt, EKG-avvikelser, hypotoni, hjärtklappning, synkope, takykardi, ventrikulära extrasystoler.
Nervsystem: Onormala drömmar, minnesförlust, depression, onormal gång, hallucinationer, sömnlöshet, nervositet, parestesi, personlighetsförändring, somnolens, tinnitus, tremor.
Gastrointestinala: Anorexi, förstoppning, diarré, muntorrhet, dysgeusi, dyspepsi, milda förhöjningar av SGOT, SGPT, LDH och alkaliskt fosfatas (se VARNINGAR , Akut leverskada ), törst, kräkningar, viktökning.
Dermatologiska: Petekier, ljuskänslighet, klåda, nässelutslag.
Övrig: Amblyopi, CPK-ökning, dyspné, näsblod, ögonirritation, hyperglykemi, hyperurikemi, impotens, muskelkramper, nästäppa, nocturi, osteoartikulär smärta, polyuri, sexuella svårigheter.
Följande händelser efter marknadsföring har rapporterats i sällsynta fall hos patienter som får diltiazem: akut generaliserad exantematös pustulos, allergiska reaktioner, alopeci, angioödem (inklusive ansikts- eller periorbitalt ödem), asystoli, erythema multiforme (inklusive Stevens-Johns-Johnsons dermalitis syndrom), exfolnecrotoxic dermaitis syndrom, , extrapyramidala symtom, gingival hyperplasi, hemolytisk anemi, ökad blödningstid, leukopeni, ljuskänslighet (inklusive lichenoid keratos och hyperpigmentering vid solexponerade hudområden), purpura, retinopati, myopati och trombocytopeni. Dessutom har händelser såsom hjärtinfarkt observerats som inte lätt kan särskiljas från sjukdomens naturliga historia hos dessa patienter. Ett antal väldokumenterade fall av generaliserade utslag, några karakteriserade som leukocytoklastisk vaskulit, har rapporterats. Ett definitivt orsaks- och verkanssamband mellan dessa händelser och diltiazemterapi har dock ännu inte fastställts.
För att rapportera MISSTÄNKTA BIVERKNINGAR, kontakta Actavis på 1-800-272-5525 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
LÄKEMEDELSINTERAKTIONER
På grund av risken för additiva effekter krävs försiktighet och noggrann titrering hos patienter som får diltiazem samtidigt med andra medel som är kända för att påverka hjärtats kontraktilitet och/eller överledning (se VARNINGAR ). Farmakologiska studier tyder på att det kan finnas additiva effekter för att förlänga AV-överledning vid användning av betablockerare eller digitalis samtidigt med diltiazem (se VARNINGAR ).
Som med alla läkemedel bör försiktighet iakttas vid behandling av patienter med flera läkemedel. Diltiazem är både ett substrat och en hämmare av cytokrom P-450 3A4 enzymsystemet. Andra läkemedel som är specifika substrat, inhibitorer eller inducerare av detta enzymsystem kan ha en betydande inverkan på effektiviteten och biverkningsprofilen för diltiazem. Patienter som tar andra läkemedel som är substrat för CYP450 3A4, särskilt patienter med nedsatt njur- och/eller leverfunktion, kan behöva dosjustering vid start eller avbrytande av samtidig administrering av diltiazem för att bibehålla optimala terapeutiska blodnivåer.
Bedövningsmedel
Nedtryckningen av hjärtkontraktilitet, konduktivitet och automatik såväl som den vaskulära utvidgningen i samband med anestetika kan förstärkas av kalciumkanalblockerare. Vid samtidig användning bör anestetika och kalciumblockerare titreras noggrant.
Bensodiazepiner
Studier visade att diltiazem ökade AUC för midazolam och triazolam med 3 till 4 gånger och Cmax med 2 gånger jämfört med placebo. Halveringstiden för eliminering av midazolam och triazolam ökade också (1,5 till 2,5 gånger) vid samtidig administrering med diltiazem. Dessa farmakokinetiska effekter som ses vid samtidig administrering av diltiazem kan resultera i ökade kliniska effekter (t.ex. förlängd sedering) av både midazolam och triazolam.
Betablockerare
Kontrollerade och okontrollerade inhemska studier tyder på att samtidig användning av diltiazem och betablockerare vanligtvis tolereras väl, men tillgängliga data är inte tillräckliga för att förutsäga effekterna av samtidig behandling hos patienter med vänsterkammardysfunktion eller hjärtöverledningsstörningar.
Administrering av diltiazemhydroklorid samtidigt med propranolol hos fem normala frivilliga resulterade i ökade propranololnivåer hos alla försökspersoner och biotillgängligheten av propranolol ökade med cirka 50 %. In vitro verkar propranolol förskjutas från dess bindningsställen av diltiazem. Om kombinationsbehandling initieras eller sätts ut i samband med propranolol, kan en justering av propranololdosen vara motiverad (se VARNINGAR ).
Buspiron
Hos nio friska försökspersoner ökade diltiazem signifikant AUC för buspiron med 5,5 gånger och Cmax 4,1 gånger jämfört med placebo. T½ och Tmax för buspiron påverkades inte signifikant av diltiazem. Förstärkta effekter och ökad toxicitet av buspiron kan vara möjliga vid samtidig administrering med diltiazem. Efterföljande dosjusteringar kan vara nödvändiga vid samtidig administrering och bör baseras på klinisk bedömning.
Karbamazepin
Samtidig administrering av diltiazem och karbamazepin har rapporterats resultera i förhöjda serumnivåer av karbamazepin (40 % till 72 % ökning), vilket i vissa fall resulterar i toxicitet. Patienter som får dessa läkemedel samtidigt bör övervakas med avseende på en potentiell läkemedelsinteraktion.
Cimetidin
En studie med sex friska frivilliga har visat en signifikant ökning av maximala plasmanivåer av diltiazem (58 %) och area-under-the-curve (53 %) efter en 1 veckas kur med cimetidin med 1 200 mg per dag och en engångsdos av diltiazem 60 mg. Ranitidin gav mindre, icke-signifikanta ökningar. Effekten kan förmedlas av cimetidins kända hämning av hepatisk cytokrom P-450, enzymsystemet som ansvarar för first-pass-metabolismen av diltiazem. Patienter som för närvarande behandlas med diltiazem bör övervakas noggrant med avseende på förändringar i farmakologisk effekt när behandlingen med cimetidin påbörjas och avbryts. En justering av diltiazemdosen kan vara motiverad.
Klonidin
Sinusbradykardi som resulterar i sjukhusvistelse och pacemakerinsättning har rapporterats i samband med användning av klonidin samtidigt med diltiazem. Övervaka hjärtfrekvensen hos patienter som samtidigt får diltiazem och klonidin.
Cyklosporin
En farmakokinetisk interaktion mellan diltiazem och ciklosporin har observerats under studier med njur- och hjärttransplanterade patienter. Hos mottagare av njur- och hjärttransplantationer var en minskning av ciklosporindosen varierande från 15 % till 48 % nödvändig för att bibehålla dalkoncentrationer av ciklosporin liknande de som sågs före tillsatsen av diltiazem. Om dessa medel ska administreras samtidigt, bör ciklosporinkoncentrationerna övervakas, särskilt när diltiazembehandling påbörjas, justeras eller avbryts.
Effekten av ciklosporin på plasmakoncentrationer av diltiazem har inte utvärderats.
Digitalis
Administrering av diltiazem med digoxin hos 24 friska manliga försökspersoner ökade plasmakoncentrationen av digoxin med cirka 20 %. En annan utredare fann ingen ökning av digoxinnivåer hos 12 patienter med kranskärlssjukdom. Eftersom det har förekommit motstridiga resultat angående effekten av digoxinnivåer, rekommenderas att digoxinnivåer övervakas vid inledande, justering och avbrytande av diltiazembehandling för att undvika eventuell över- eller underdigitalisering (se VARNINGAR ).
Kinidin
Diltiazem ökar signifikant AUC(0-→) för kinidin med 51 %, T½ med 36 % och minskar dess CL oralt med 33 %. Övervakning av kinidinbiverkningar kan vara motiverad och dosen justeras därefter.
Rifampin
Samtidig administrering av rifampin och diltiazem sänkte plasmakoncentrationerna av diltiazem till odetekterbara nivåer. Samtidig administrering av diltiazem med rifampin eller någon känd CYP3A4-inducerare bör undvikas när det är möjligt och alternativ behandling övervägas.
Statiner
Diltiazem är en hämmare av CYP3A4 och har visats signifikant öka AUC för vissa statiner. Risken för myopati och rabdomyolys med statiner som metaboliseras av CYP3A4 kan öka vid samtidig användning av diltiazem. Om möjligt, använd en icke-CYP3A4-metaboliserad statin tillsammans med diltiazem; Annars bör dosjusteringar för både diltiazem och statin övervägas tillsammans med noggrann övervakning av tecken och symtom på statinrelaterade biverkningar.
en övergångsstudie av friska frivilliga (N=10) resulterade samtidig administrering av en engångsdos på 20 mg simvastatin i slutet av en 14-dagarsregim med 120 mg två gånger dagligen diltiazem SR i en 5-faldig ökning av medel-AUC för simvastatin jämfört med simvastatin ensam. Försökspersoner med ökad genomsnittlig steady-state exponering av diltiazem uppvisade en större ökning av simvastatinexponeringen. Datorbaserade simuleringar visade att vid en daglig dos på 480 mg diltiazem kan en 8- till 9-faldig genomsnittlig ökning av simvastatins AUC förväntas. Om samtidig administrering av simvastatin och diltiazem krävs, begränsa de dagliga doserna av simvastatin till 10 mg och diltiazem till 240 mg.
en randomiserad, öppen, 4-vägs cross-over-studie med tio försökspersoner resulterade samtidig administrering av diltiazem (120 mg två gånger dagligen diltiazem SR under 2 veckor) med en engångsdos på 20 mg lovastatin i en 3- till 4-faldig ökning av medelvärdet. lovastatin AUC och mot enbart lovastatin. I samma studie fanns det ingen signifikant förändring i 20 mg enkeldos pravastatin AUC och vid samtidig administrering av diltiazem. Diltiazemplasmanivåer påverkades inte signifikant av lovastatin eller pravastatin.
VARNINGAR
Hjärtledning
Diltiazem förlänger AV-nodernas refraktära perioder utan att signifikant förlänga sinusknutans återhämtningstid, förutom hos patienter med sick sinus syndrome. Denna effekt kan sällan resultera i onormalt långsamma hjärtfrekvenser (särskilt hos patienter med sick sinus syndrome) eller andra eller tredje gradens AV-block (13 av 3290 patienter eller 0,40%). Samtidig användning av diltiazem och betablockerare eller digitalis kan resultera i additiva effekter på hjärtöverledning. En patient med Prinzmetals angina utvecklade perioder av asystoli (2 till 5 sekunder) efter en singeldos på 60 mg diltiazem (se NEGATIVA REAKTIONER ).
Hjärtsvikt
Även om diltiazem har en negativ inotrop effekt i isolerade djurvävnadspreparat, har hemodynamiska studier på människor med normal ventrikulär funktion inte visat en minskning av hjärtindex eller konsekventa negativa effekter på kontraktilitet (dp/dt). En akut studie av oralt diltiazem hos patienter med nedsatt ventrikulär funktion (ejektionsfraktion 24 % ± 6 %) visade förbättring av index för ventrikulär funktion utan signifikant minskning av kontraktilfunktionen (dp/dt). Försämring av kongestiv hjärtsvikt har rapporterats hos patienter med redan existerande försämring av ventrikulär funktion. Erfarenheten av användning av diltiazemhydroklorid i kombination med betablockerare hos patienter med nedsatt ventrikulär funktion är begränsad. Försiktighet bör iakttas när du använder denna kombination.
Hypotoni
Blodtryckssänkningar i samband med diltiazembehandling kan ibland resultera i symptomatisk hypotoni.
Akut leverskada
Milda förhöjningar av transaminaser med och utan samtidig förhöjning av alkaliskt fosfatas och bilirubin har observerats i kliniska studier. Sådana förhöjningar var vanligtvis övergående och försvann ofta även med fortsatt diltiazembehandling. I sällsynta fall har signifikanta ökningar av enzymer såsom alkaliskt fosfatas, LDH, SGOT, SGPT och andra fenomen som överensstämmer med akut leverskada noterats. Dessa reaktioner tenderade att inträffa tidigt efter behandlingsstart (1 till 8 veckor) och har varit reversibla vid utsättning av läkemedelsbehandling. Förhållandet till diltiazem är osäkert i vissa fall, men troligt i vissa (se FÖRSIKTIGHETSÅTGÄRDER ).
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Diltiazemhydroklorid metaboliseras i stor utsträckning av levern och utsöndras via njurarna och i gallan. Som med alla läkemedel som ges under långa perioder, bör laboratorieparametrar för njur- och leverfunktion övervakas med regelbundna intervall. Läkemedlet bör användas med försiktighet till patienter med nedsatt njur- eller leverfunktion. I subakuta och kroniska hund- och råttastudier utformade för att ge toxicitet, var höga doser diltiazem associerade med leverskada. I speciella subakuta leverstudier var orala doser på 125 mg/kg och högre hos råttor associerade med histologiska förändringar i levern, som var reversibla när läkemedlet avbröts. Hos hundar var doser på 20 mg/kg också associerade med leverförändringar; dessa förändringar var dock reversibla med fortsatt dosering.
Dermatologiska händelser (se NEGATIVA REAKTIONER kan vara övergående och kan försvinna trots fortsatt användning av diltiazem. Men hudutslag som utvecklas till erythema multiforme och/eller exfoliativ dermatit har också rapporterats sällan. Om en dermatologisk reaktion kvarstår, bör läkemedlet avbrytas.
Karcinogenes, Mutagenes, Nedsatt fertilitet
En 24-månaders studie på råttor vid orala dosnivåer på upp till 100 mg/kg/dag och en 21 månader lång studie på möss vid orala dosnivåer på upp till 30 mg/kg/dag visade inga tecken på karcinogenicitet. Det fanns inte heller något mutagent svar in vitro eller in vivo i däggdjurscellanalyser eller in vitro i bakterier. Inga tecken på nedsatt fertilitet observerades i en studie utförd på han- och honråttor vid orala doser på upp till 100 mg/kg/dag.
Graviditet
Kategori C. Reproduktionsstudier har utförts på möss, råttor och kaniner. Administrering av doser som sträcker sig från fem till tio gånger större (på en mg/kg-basis) än den dagliga rekommenderade terapeutiska dosen har resulterat i embryo- och fosterdödlighet. Dessa doser har i vissa studier rapporterats orsaka skelettavvikelser. I de perinatala/postnatala studierna fanns en ökad förekomst av dödfödslar vid doser på 20 gånger den mänskliga dosen eller mer.
Det finns inga välkontrollerade studier på gravida kvinnor; Använd därför diltiazem till gravida kvinnor endast om den potentiella nyttan motiverar den potentiella risken för fostret.
Ammande mödrar
Diltiazem utsöndras i modersmjölk. En rapport tyder på att koncentrationer i bröstmjölk kan vara ungefärliga serumnivåer. Om användningen av diltiazem anses nödvändig, bör en alternativ metod för spädbarnsmatning sättas in.
Pediatrisk användning
Säkerhet och effektivitet hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Kliniska studier av diltiazem inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling.
ÖVERDOS
De orala LD50-värdena hos möss och råttor varierar från 415 till 740 mg/kg respektive från 560 till 810 mg/kg. De intravenösa LD50-värdena hos dessa arter var 60 respektive 38 mg/kg. Den orala LD50 hos hund anses vara över 50 mg/kg, medan dödlighet sågs hos apor vid 360 mg/kg.
Den toxiska dosen hos människa är inte känd. På grund av omfattande metabolism kan blodnivåerna efter en standarddos av diltiazem variera mer än tio gånger, vilket begränsar användbarheten av blodnivåer i överdosfall.
Det har rapporterats om överdosering av diltiazem i mängder från
Händelser som observerats efter överdosering av diltiazem inkluderade bradykardi, hypotoni, hjärtblock och hjärtsvikt. De flesta rapporter om överdosering beskrev någon stödjande medicinsk åtgärd och/eller läkemedelsbehandling. Bradykardi svarade ofta positivt på atropin, liksom hjärtblockad, även om hjärtstimulering också ofta användes för att behandla hjärtblockad. Vätskor och vasopressorer användes för att upprätthålla blodtrycket, och i fall av hjärtsvikt administrerades inotropa medel. Dessutom fick vissa patienter behandling med andningsstöd, magsköljning, aktivt kol och/eller intravenöst kalcium.
Effektiviteten av intravenös administrering av kalcium för att vända de farmakologiska effekterna av överdosering av diltiazem har varit inkonsekvent. I ett fåtal rapporterade fall blev överdosering av kalciumkanalblockerare associerad med hypotoni och bradykardi som initialt var refraktär mot atropin mer känslig för atropin efter att patienterna fått intravenöst kalcium. I vissa fall har intravenöst kalcium administrerats (1 g kalciumklorid eller 3 g kalciumglukonat) under 5 minuter och upprepat var 10:e till 20:e minut vid behov. Kalciumglukonat har också administrerats som en kontinuerlig infusion med en hastighet av 2 g per timme i 10 timmar. Infusioner av kalcium i 24 timmar eller mer kan behövas. Patienter bör övervakas med avseende på tecken på hyperkalcemi.
händelse av överdosering eller överdrivet svar bör lämpliga stödåtgärder vidtas utöver gastrointestinal dekontaminering. Diltiazem verkar inte avlägsnas genom peritoneal eller hemodialys. Begränsade data tyder på att plasmaferes eller kolhemoperfusion kan påskynda eliminering av diltiazem efter överdosering. Baserat på de kända farmakologiska effekterna av diltiazem och/eller rapporterade kliniska erfarenheter, kan följande åtgärder övervägas:
Bradykardi: Administrera atropin (0,6 till 1 mg). Om det inte finns något svar på vagal blockad, administrera isoproterenol försiktigt.
Höggradigt AV-block: Behandla som för bradykardi ovan. Fast höggradigt AV-block bör behandlas med hjärtstimulering.
Hjärtfel: Administrera inotropa medel (isoproterenol, dopamin eller dobutamin) och diuretika.
Hypotoni: Vasopressorer (t.ex. dopamin eller noradrenalin).
Faktisk behandling och dosering bör bero på svårighetsgraden av den kliniska situationen och den behandlande läkarens bedömning och erfarenhet.
KONTRAINDIKATIONER
Diltiazem är kontraindicerat hos (1) patienter med sick sinus syndrome förutom i närvaro av en fungerande ventrikulär pacemaker, (2) patienter med andra eller tredje gradens AV-block förutom i närvaro av en fungerande ventrikulär pacemaker, (3) patienter med hypotoni (mindre än 90 mm Hg systolisk), (4) patienter som har visat överkänslighet mot läkemedlet och (5) patienter med akut hjärtinfarkt och lungstockning dokumenterad med röntgen vid inläggningen.
KLINISK FARMAKOLOGI
De terapeutiska effekterna av USP-kapslar med förlängd frisättning av diltiazemhydroklorid (dosering en gång om dagen) tros vara relaterade till dess förmåga att hämma det cellulära inflödet av kalciumjoner under membrandepolarisering av hjärt- och vaskulär glatt muskulatur.
Verkningsmekanismer
Hypertoni
Diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) ger sin antihypertensiva effekt främst genom avslappning av vaskulär glatt muskulatur och den resulterande minskningen av perifert vaskulärt motstånd. Omfattningen av blodtryckssänkningen är relaterad till graden av hypertoni; sålunda upplever hypertensiva individer en blodtryckssänkande effekt, medan det endast finns ett måttligt blodtrycksfall hos normotensiva.
Angina
Diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) har visat sig ge ökad träningstolerans, troligen på grund av dess förmåga att minska myokardens syrebehov. Detta uppnås genom sänkningar av hjärtfrekvens och systemiskt blodtryck vid submaximala och maximala arbetsbelastningar. Diltiazem har visat sig vara en potent dilator av kranskärl, både epikardiell och subendokardiell. Spontan och ergonovin-inducerad kranskärlspasm hämmas av diltiazem.
djurmodeller stör diltiazem den långsamma inåtriktade (depolariserande) strömmen i exciterbar vävnad. Det orsakar excitation-kontraktion-urkoppling i olika myokardvävnader utan förändringar i konfigurationen av aktionspotentialen. Diltiazem ger avslappning av den glatta muskulaturen i kranskärlen och vidgning av både stora och små kranskärl vid läkemedelsnivåer som orsakar liten eller ingen negativ inotrop effekt. Den resulterande ökningen av kranskärlsblodflödet (epikardiellt och subendokardiellt) inträffar i ischemiska och icke-ischemiska modeller och åtföljs av dosberoende minskningar av systemiskt blodtryck och minskningar av perifert motstånd.
Hemodynamiska och elektrofysiologiska effekter
Liksom andra kalciumkanalantagonister minskar diltiazem sinoatrial och atrioventrikulär ledning i isolerade vävnader och har en negativ inotrop effekt i isolerade preparat. Hos det intakta djuret kan förlängning av AH-intervallet ses vid högre doser.
Hos människan förhindrar diltiazem spontana och ergonovin-provocerade kranskärlsspasmer. Det orsakar en minskning av det perifera kärlmotståndet och ett måttligt blodtrycksfall hos normotensiva individer och, i träningstoleransstudier hos patienter med ischemisk hjärtsjukdom, minskar puls-blodtrycksprodukten för varje given arbetsbelastning. Studier hittills, främst på patienter med god kammarfunktion, har inte visat tecken på en negativ inotrop effekt; hjärtminutvolym, ejektionsfraktion och vänsterkammarändens diastoliska tryck har inte påverkats. Sådana data har inget prediktivt värde med avseende på effekter hos patienter med dålig ventrikulär funktion, och ökad hjärtsvikt har rapporterats hos patienter med redan existerande försämring av ventrikulär funktion. Det finns ännu få data om interaktionen mellan diltiazem och betablockerare hos patienter med dålig ventrikulär funktion. Vilopuls minskas vanligtvis något av diltiazem.
Hos hypertonipatienter ger diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) antihypertensiva effekter både i liggande och stående position. I en dubbelblind, parallell dos-respons-studie som använde doser från 90 till 540 mg en gång dagligen, sänkte diltiazemhydroklorid kapsel med förlängd frisättning (en gång om dagen) det diastoliska blodtrycket i liggande liggande på ett uppenbart linjärt sätt över hela dosintervall studerat. Förändringarna i diastoliskt blodtryck, uppmätt vid dal, för placebo, 90 mg, 180 mg, 360 mg och 540 mg var -2,9, -4,5, -6,1, -9,5 respektive -10,5 mm Hg. Postural hypotoni noteras sällan när man plötsligt intar en upprätt position. Ingen reflextakykardi är associerad med de kroniska antihypertensiva effekterna. Diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) minskar vaskulärt motstånd, ökar hjärtminutvolymen (genom att öka slagvolymen); och ger en lätt minskning eller ingen förändring i hjärtfrekvensen. Under dynamisk träning hämmas ökningar av diastoliskt tryck, medan maximalt uppnåeligt systoliskt tryck vanligtvis reduceras. Kronisk behandling med diltiazemhydroklorid USP-kapslar med förlängd frisättning (en gång om dagen) ger ingen förändring eller en ökning av plasmakatekolaminer. Ingen ökad aktivitet av renin-angiotensin-aldosteron-axeln har observerats. Diltiazemhydroklorid kapslar med förlängd frisättning USP (dosering en gång om dagen) minskar de renala och perifera effekterna av angiotensin II. Hypertensiva djurmodeller svarar på diltiazem med sänkningar av blodtrycket och ökad urinproduktion och natriures utan förändring av natrium/kalium-förhållandet i urinen.
en dubbelblind, parallell dos-respons-studie av doser från 60 mg till 480 mg en gång dagligen, ökade diltiazemhydroklorid kapsel med förlängd frisättning (dosering en gång om dagen) tiden till avbrytande av träningen på ett linjärt sätt över hela dosen räckvidd studeras. Förbättringen av tiden till avbrytande av träningen med användning av ett Bruce träningsprotokoll, mätt vid dalgång, för placebo, 60 mg, 120 mg, 240 mg, 360 mg och 480 mg var 29, 40, 56, 51, 69 och 68 sekunder , respektive. När doserna av diltiazemhydroklorid kapsel med förlängd frisättning (dosering en gång om dagen) ökades, minskade den totala anginafrekvensen. Diltiazemhydroklorid kapsel med förlängd frisättning (dosering en gång om dagen), 180 mg en gång dagligen, eller placebo administrerades i en dubbelblind studie till patienter som samtidigt fick långverkande nitrater och/eller betablockerare. En signifikant ökning av tiden till avslutad träning och en signifikant minskning av den totala anginafrekvensen observerades. I denna studie var den totala frekvensen av biverkningar i behandlingsgruppen med diltiazemhydroklorid depotkapsel (dosering en gång om dagen) densamma som i placebogruppen.
Intravenöst diltiazem i doser om 20 mg förlänger AH-ledningstiden och AV-nods funktionella och effektiva refraktärperioder med cirka 20 %. I en studie som involverade orala enstaka doser av 300 mg diltiazemhydroklorid hos sex normala frivilliga, var den genomsnittliga maximala PR-förlängningen 14 % utan fall av större än första gradens AV-block. Diltiazem-associerad förlängning av AH-intervallet är inte mer uttalad hos patienter med första gradens hjärtblock. Hos patienter med sick sinus syndrome förlänger diltiazem sinuscykellängden avsevärt (upp till 50 % i vissa fall).
Kronisk oral administrering av diltiazemhydroklorid till patienter i doser på upp till 540 mg/dag har resulterat i små ökningar av PR-intervallet och ger ibland onormal förlängning (se VARNINGAR ).
Farmakokinetik och metabolism
Diltiazem absorberas väl från mag-tarmkanalen och är föremål för en omfattande first-pass-effekt, vilket ger en absolut biotillgänglighet (jämfört med intravenös administrering) på cirka 40 %. Diltiazem genomgår omfattande metabolism där endast 2% till 4% av det oförändrade läkemedlet uppträder i urinen. Läkemedel som inducerar eller hämmar levermikrosomala enzymer kan förändra dispositionen av diltiazem.
Total radioaktivitetsmätning efter kort IV-administrering hos friska frivilliga tyder på närvaron av andra oidentifierade metaboliter, som uppnår högre koncentrationer än diltiazem och som elimineras långsammare; halveringstiden för total radioaktivitet är cirka 20 timmar jämfört med 2 till 5 timmar för diltiazem.
In vitro-bindningsstudier visar att diltiazem är 70 % till 80 % bundet till plasmaproteiner. Konkurrerande in vitro ligandbindningsstudier har också visat att diltiazembindning inte förändras av terapeutiska koncentrationer av digoxin, hydroklortiazid, fenylbutazon, propranolol, salicylsyra eller warfarin. Halveringstiden för plasmaeliminering efter administrering av en eller flera läkemedel är cirka 3,0 till 4,5 timmar. Desacetyldiltiazem finns också i plasman i nivåer på 10 % till 20 % av moderläkemedlet och är 25 % till 50 % lika potent som en kranskärlsvidgande medel som diltiazem. Lägsta terapeutiska plasmakoncentrationer av diltiazem verkar vara i intervallet 50 till 200 ng/ml. Det finns ett avsteg från linjäritet när dosstyrkorna ökas; halveringstiden ökar något med dosen. En studie som jämförde patienter med normal leverfunktion med patienter med cirros fann en ökning av halveringstiden och en 69% ökning av biotillgängligheten hos patienter med nedsatt leverfunktion. En enda studie på nio patienter med gravt nedsatt njurfunktion visade ingen skillnad i den farmakokinetiska profilen för diltiazem jämfört med patienter med normal njurfunktion.
Diltiazem hydroklorid kapslar med förlängd frisättning (en gång om dagen)
Jämfört med en regim med diltiazemtabletter vid steady-state, absorberas mer än 95 % av läkemedlet från formuleringen av diltiazemhydroklorid-kapslar med förlängd frisättning (en gång om dagen). En engångsdos på 360 mg av kapseln resulterar i detekterbara plasmanivåer inom 2 timmar och maximala plasmanivåer mellan 10 och 14 timmar; absorption sker under hela doseringsintervallet. När diltiazemhydroklorid kapsel med förlängd frisättning (en gång om dagen) administrerades samtidigt med en frukost med hög fetthalt, påverkades inte graden av diltiazemabsorption. Dosdumpning förekommer inte. Den uppenbara eliminationshalveringstiden efter engångsdosering eller upprepad dosering är 5 till 8 timmar. En avvikelse från linjäritet liknande den som ses med diltiazemtabletter och diltiazemhydrokloridkapslar (två gånger dagligen) observeras. Eftersom dosen av diltiazemhydroklorid kapslar med förlängd frisättning (en gång om dagen) ökas från en daglig dos på 120 mg till 240 mg, ökar arean under kurvan med 2,7 gånger. När dosen ökas från 240 mg till 360 mg sker en ökning av arean-under-kurvan med 1,6 gånger.
PATIENTINFORMATION
Ingen information lämnas. Vänligen se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER avsnitt.
