Behandling mag-tarmkanalen: Nexium 20mg, 40mg Esomeprazole Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Nexium och hur används det?
Nexium är ett receptbelagt läkemedel som används för att behandla symtom på gastroesofageal refluxsjukdom (GERD) och andra tillstånd där det finns överdriven magsyra såsom Zollinger-Ellisons syndrom. Nexium kan användas ensamt eller tillsammans med andra läkemedel.
Nexium 20mg är en protonpumpshämmare.
Det är inte känt om Nexium 20mg är säkert och effektivt för barn yngre än 1 månad för intravenös medicinering och 1 år för oral medicinering.
Vilka är biverkningarna av Nexium 40mg?
Nexium kan orsaka allvarliga biverkningar inklusive:
- svåra magsmärtor,
- diarré som är vattnig eller blodig,
- anfall (kramper),
- lite eller ingen urinering,
- blod i urinen,
- svullnad,
- snabb viktökning,
- yrsel,
- snabb eller oregelbunden hjärtfrekvens,
- skakningar eller ryckande muskelrörelser,
- känner sig orolig,
- muskelkramp,
- muskelspasmer i händer och fötter,
- hosta eller kvävningskänsla,
- ledvärk och
- hudutslag på kinderna eller armarna som förvärras i solen
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Nexium 40mg inkluderar:
- huvudvärk,
- dåsighet,
- mild diarré,
- illamående,
- magont,
- gas,
- förstoppning och
- torr mun
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Nexium. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
Den aktiva ingrediensen i NEXIUM® IV (esomeprazolnatrium) för injektion är (S)-5-metoxi-2[[(4-metoxi-3,5-dimetyl-2-pyridinyl)-metyl]sulfinyl]-1 H-bensimidazol natrium, en protonpumpshämmare som hämmar magsyrautsöndringen. Esomeprazol är S-isomeren av omeprazol, som är en blandning av S- och R-isomererna. Dess empiriska formel är C17H18N3O3SNa med en molekylvikt på 367,4 g/mol (natriumsalt) och 345,4 g/mol (moderförening).
Esomeprazolnatrium är mycket lösligt i vatten och fritt lösligt i etanol (95%). Strukturformeln är:
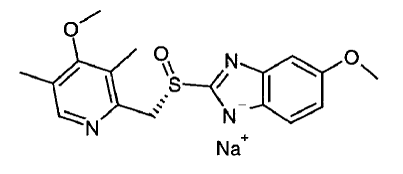
NEXIUM 20mg IV för injektion levereras som en steril, frystorkad, vit till benvit, porös kaka eller pulver i en 5 ml injektionsflaska, avsedd för intravenös administrering efter beredning med 0,9 % natriumkloridinjektion, USP; Laktat Ringer's Injection, USP eller 5% Dextrose Injection, USP. NEXIUM IV för injektion innehåller esomeprazolnatrium 21,3 mg eller 42,5 mg motsvarande esomeprazol 20 mg eller 40 mg, dinatriumedetat 1,5 mg och natriumhydroxid qs för pH-justering. pH-värdet för rekonstituerad lösning av NEXIUM IV för injektion beror på beredningsvolymen och ligger i pH-intervallet 9 till 11. Stabiliteten för esomeprazolnatrium i vattenlösning är starkt pH-beroende. Nedbrytningshastigheten ökar med sjunkande pH.
INDIKATIONER
Behandling av gastroesofageal refluxsjukdom (GERD) med erosiv esofagit (EE)
NEXIUM IV är indicerat för korttidsbehandling av GERD med EE hos vuxna och pediatriska patienter 1 månad till 17 år, inklusive som ett alternativ till oral behandling när oral NEXIUM 40 mg inte är möjlig eller lämplig.
Riskminskning av återblödning från mag- eller duodenalsår efter terapeutisk endoskopi hos vuxna
NEXIUM 40mg IV är indicerat för att minska risken för återblödning av mag- eller duodenalsår efter terapeutisk endoskopi för akut blödande magsår eller duodenalsår hos vuxna.
DOSERING OCH ADMINISTRERING
Dosering för GERD med EE
Vuxna patienter
Den rekommenderade dosen för vuxna är antingen 20 mg eller 40 mg NEXIUM 40 mg IV givet en gång dagligen genom intravenös injektion (under minst 3 minuter) eller intravenös infusion (10 minuter till 30 minuter) i upp till 10 dagar [se DOSERING OCH ADMINISTRERING ].
Pediatriska patienter
Den rekommenderade dosen för pediatriska patienter baseras på ålder och kroppsvikt som visas i tabell 1 nedan. Administreras som en intravenös infusion under 10 till 30 minuter en gång dagligen i upp till 10 dagar [se DOSERING OCH ADMINISTRERING ].
Slutförande av Behandling
- Säkerheten och effektiviteten för NEXIUM 20 mg IV i mer än 10 dagar har inte visats.
- Så snart oral behandling är möjlig eller lämplig, avbryt intravenös behandling med NEXIUM 40 mg IV och fortsätt med oral behandling med NEXIUM 20 mg.
Dosering för riskminskning av återblödning från mag- eller duodenalsår efter terapeutisk endoskopi hos vuxna
Den rekommenderade dosen för vuxna är 80 mg NEXIUM IV administrerat som en intravenös infusion under 30 minuter följt av en kontinuerlig infusion på 8 mg/timme under en total behandlingslängd på 72 timmar (dvs. inkluderar initial 30 minuters laddningsdos plus 71,5 timmar kontinuerlig infusion) [se DOSERING OCH ADMINISTRERING ].
Intravenös terapi är enbart inriktad på den akuta initiala behandlingen av blödande mag- eller duodenalsår och utgör inte full behandling. Administrera oral syrasuppressiv behandling efter intravenös behandling under en hel behandlingskur.
Dosjustering för nedsatt leverfunktion
GERD Med EE
För patienter med gravt nedsatt leverfunktion (Child-Pugh klass C) är den maximala dosen 20 mg en gång dagligen [se Användning i specifika populationer ].
Riskminskning av återblödning från mag- eller duodenalsår efter terapeutisk endoskopi hos vuxna
För patienter med lätt till måttligt nedsatt leverfunktion (Child-Pugh klass A respektive B), administreras 80 mg som en intravenös infusion under 30 minuter, följt av en kontinuerlig infusion av 6 mg/timme i 71,5 timmar.
För patienter med gravt nedsatt leverfunktion (Child-Pugh klass C), administrerad 80 mg som en intravenös infusion under 30 minuter, följt av en kontinuerlig infusion av 4 mg/timme i 71,5 timmar [se Användning i specifika populationer ].
Instruktioner för förberedelse och administration för GERD med EE
Administrera inte NEXIUM 40mg IV samtidigt med andra läkemedel genom samma intravenösa ställe och/eller slangar.
Orala antacida kan användas under behandling med NEXIUM 20mg IV
Intravenös injektion under minst 3 minuter hos vuxna patienter
Intravenös infusion över 10 minuter till 30 minuter hos vuxna och pediatriska patienter
Lagring
Förvara den slutliga (utspädda) NEXIUM IV-lösningen vid rumstemperatur upp till 30°C (86°F) och administrera inom den angivna tidsperioden som anges i tabell 2 nedan.
Förberedelse och administreringsinstruktioner för riskminskning av återblödning från mag- eller tolvfingertarmssår hos vuxna
Administrera inte NEXIUM 40mg IV samtidigt med andra läkemedel genom samma intravenösa ställe och/eller slangar.
Orala antacida kan användas under behandling med NEXIUM IV
Laddningsdos (80 mg)
Kontinuerlig infusion
Lagring
- Förvara den slutliga (utspädda) NEXIUM IV-lösningen i rumstemperatur upp till 30°C (86°F) och administrera inom 12 timmar.
HUR LEVERERAS
Doseringsformer och styrkor
För injektion: 40 mg esomeprazol som ett vitt till benvitt lyofiliserat pulver i en endosflaska för beredning.
Förvaring Och Hantering
NEXIUM 20mg IV levereras i en endosflaska som ett vitt till benvitt frystorkat pulver för beredning innehållande 40 mg esomeprazol.
NEXIUM 40mg IV . finns tillgänglig enligt följande:
Lagring
Förvara vid 25°C (77°F); utflykter tillåtna till 15° till 30°C (59° till 86°F). [Ser USP-kontrollerad rumstemperatur .] Skydda från ljus. Förvara i kartong tills den ska användas.
Efter beredning och administrering, kassera all oanvänd del av esomeprazollösning [se DOSERING OCH ADMINISTRERING ].
Tillverkad för: AstraZeneca Pharmaceuticals LP Wilmington, DE 19850. Reviderad: Mar 2022
BIEFFEKTER
Följande allvarliga biverkningar beskrivs nedan och på andra ställen i märkningen:
- Akut Tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Clostridium difficile-associerad diarré [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Allvarliga kutana biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Kutan och systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypomagnesemi och mineralmetabolism [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Fundiska körtelpolyper [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Symtomatisk GERD och EE
Vuxna
Säkerheten för NEXIUM IV baseras på resultat från kliniska prövningar utförda i fyra olika populationer inklusive friska försökspersoner (n=204) och patienter med blödande mag- eller duodenalsår (n=375). Data som beskrivs nedan återspeglar exponering för NEXIUM 20 mg IV hos 359 patienter i aktivt kontrollerade studier: symtomatisk GERD med eller utan en historia av EE (n=199) och patienter med EE (n=160). Befolkningen var 18 till 77 år gammal; 45 % män, 52 % kaukasiska, 17 % svarta, 3 % asiatiska och 28 % annan ras. De flesta patienter fick doser på antingen 20 eller 40 mg antingen som en infusion eller en injektion. Biverkningar som förekommer hos minst 1 % av patienterna listas nedan i Tabell 3:
Intravenös behandling med NEXIUM 20 mg IV 20 och 40 mg administrerad som en injektion eller som en infusion visade sig ha en säkerhetsprofil som liknar den för oral esomeprazol.
Pediatrik
En randomiserad, öppen, multinationell studie för att utvärdera farmakokinetiken för upprepade intravenösa doser av NEXIUM IV en gång dagligen hos pediatriska patienter från 1 månad till 17 år gamla utfördes [se KLINISK FARMAKOLOGI ]. Säkerhetsresultaten överensstämmer med den kända säkerhetsprofilen för esomeprazol och inga oväntade säkerhetssignaler identifierades.
Riskminskning av återblödning av mag- eller duodenalsår hos vuxna
Data som beskrivs i Tabell 4 nedan återspeglar exponering för NEXIUM 20 mg IV hos 375 patienter som fick endoskopiskt bekräftad mag- eller duodenalsårblödning i en placebokontrollerad studie. Befolkningen var 18 till 98 år gammal; 68 % män, 87 % kaukasiska, 1 % svarta, 7 % asiatiska och 4 % annan ras. Efter endoskopisk hemostas fick patienterna antingen placebo eller 80 mg NEXIUM IV som en intravenös infusion under 30 minuter följt av en kontinuerlig infusion på 8 mg/timme under en total behandlingslängd på 72 timmar. Efter den första 72-timmarsperioden fick alla patienter en oral PPI i 27 dagar.
Med undantag för reaktioner på injektionsstället som beskrivs ovan, visade sig intravenös behandling med NEXIUM 20 mg IV administrerat som en injektion eller som en infusion ha en säkerhetsprofil som liknar den för oral esomeprazol.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av esomeprazol efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Blod- och lymfsystemet: agranulocytos, pancytopeni;
Ögonstörningar: suddig syn;
Gastrointestinala störningar: pankreatit; stomatit; mikroskopisk kolit; fundic körtel polyper;
Lever och gallvägar: leversvikt, hepatit med eller utan gulsot;
Immunsystemets störningar: anafylaktisk reaktion/chock; systemisk lupus erythematosus;
Infektioner och angrepp: GI candidiasis;
Metabolism och näringsstörningar: hypomagnesemi (kan leda till hypokalcemi och/eller hypokalemi) [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ], hyponatremi;
Muskuloskeletala och bindvävssjukdomar: muskelsvaghet, myalgi, benfraktur;
Störningar i nervsystemet: leverencefalopati, smakstörning;
Psykiatriska störningar: aggression, agitation, depression, hallucinationer;
Njur- och urinvägsstörningar: interstitiell nefrit;
Reproduktionssystemet och bröststörningar: gynekomasti;
Andningsvägar, bröstkorg och mediastinum: bronkospasm;
Hud och subkutan vävnad: alopeci, erythema multiforme, hyperhidros, ljuskänslighet, Stevens-Johnsons syndrom, toxisk epidermal nekrolys (TEN, en del dödlig), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS), och akut generaliserad exantematös pustulos (AGEP), kutan lupus erythematosus.
Biverkningar associerade med omeprazol kan också förväntas inträffa med NEXIUM IV. Se hela förskrivningsinformationen för oral omeprazol för fullständig säkerhetsinformation.
LÄKEMEDELSINTERAKTIONER
Tabell 5 och 6 inkluderar läkemedel med kliniskt viktiga läkemedelsinteraktioner och interaktion med diagnostik när de administreras samtidigt med esomeprazol och instruktioner för att förebygga eller hantera dem.
Se märkningen av samtidigt använda läkemedel för att få ytterligare information om interaktioner med PPI.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Förekomst av magmalignitet
Hos vuxna utesluter inte symtomatisk respons på behandling med NEXIUM IV förekomsten av gastrisk malignitet. Överväg ytterligare uppföljning och diagnostiska tester hos vuxna patienter som har suboptimalt svar eller ett tidigt symtomatiskt återfall efter avslutad behandling med PPI. Hos äldre patienter överväga också en endoskopi.
Akut Tubulointerstitiell nefrit
Akut tubulointerstitiell nefrit (TIN) har observerats hos patienter som tar PPI och kan uppträda när som helst under PPI-behandling. Patienter kan uppvisa olika tecken och symtom från symtomatiska överkänslighetsreaktioner till ospecifika symtom på nedsatt njurfunktion (t.ex. sjukdomskänsla, illamående, anorexi). I rapporterade fallserier diagnostiserades vissa patienter på biopsi och i frånvaro av extrarenala manifestationer (t.ex. feber, hudutslag eller artralgi). Avbryt NEXIUM 20mg IV och utvärdera patienter med misstänkt akut TIN [se KONTRAINDIKATIONER ].
Clostridium Difficile-associerad diarré
Publicerade observationsstudier tyder på att PPI-behandling som NEXIUM 20mg IV kan vara associerad med en ökad risk för Clostridium difficile-associerad diarré, särskilt hos inlagda patienter. Denna diagnos bör övervägas för diarré som inte förbättras [se NEGATIVA REAKTIONER ].
Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas.
Benfraktur
Flera publicerade observationsstudier tyder på att behandling med protonpumpshämmare (PPI) kan vara associerad med en ökad risk för osteoporosrelaterade frakturer i höften, handleden eller ryggraden. Risken för frakturer var ökad hos patienter som fick höga doser, definierade som flera dagliga doser, och långvarig PPI-behandling (ett år eller längre). Patienter bör använda den lägsta dosen och kortaste varaktigheten av PPI-behandling som är lämplig för det tillstånd som behandlas. Patienter med risk för osteoporosrelaterade frakturer bör hanteras enligt fastställda behandlingsriktlinjer [se DOSERING OCH ADMINISTRERING , NEGATIVA REAKTIONER ].
Allvarliga kutana biverkningar
Allvarliga kutana biverkningar, inklusive Stevens-Johnsons syndrom (SJS) och toxisk epidermal nekrolys (TEN), läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) och akut generaliserad exantematös pustulos (AGEP) har rapporterats i samband med användning av PPI. [ser NEGATIVA REAKTIONER ]. Avbryt NEXIUM IV vid de första tecknen eller symtomen på allvarliga kutana biverkningar eller andra tecken på överkänslighet och överväg ytterligare utvärdering.
Kutan och systemisk lupus erythematosus
Kutan lupus erythematosus (CLE) och systemisk lupus erythematosus (SLE) har rapporterats hos patienter som tar PPI, inklusive esomeprazol. Dessa händelser har inträffat som både nyuppkomst och förvärring av befintlig autoimmun sjukdom. Majoriteten av PPI-inducerade lupus erythematosus fall var CLE.
Den vanligaste formen av CLE som rapporterats hos patienter som behandlats med PPI var subakut CLE (SCLE) och inträffade inom veckor till år efter kontinuerlig läkemedelsbehandling hos patienter från spädbarn till äldre. I allmänhet observerades histologiska fynd utan organinblandning.
Systemisk lupus erythematosus (SLE) rapporteras mindre vanligt än CLE hos patienter som får PPI. PPI-associerad SLE är vanligtvis mildare än icke-läkemedelsinducerad SLE. Debut av SLE inträffade vanligtvis inom dagar till år efter påbörjad behandling, främst hos patienter från unga vuxna till äldre. Majoriteten av patienterna fick utslag; dock rapporterades också artralgi och cytopeni.
Undvik administrering av PPI under längre tid än vad som är medicinskt indicerat. Om tecken eller symtom som överensstämmer med CLE eller SLE noteras hos patienter som får NEXIUM 20 mg IV, avbryt läkemedlet och hänvisa patienten till lämplig specialist för utvärdering. De flesta patienter förbättras med avbrytande av enbart PPI inom 4 till 12 veckor. Serologiska tester (t.ex. ANA) kan vara positiva och förhöjda serologiska testresultat kan ta längre tid att lösa än kliniska manifestationer.
Interaktion med Clopidogrel
Undvik samtidig användning av NEXIUM IV och klopidogrel. Clopidogrel är en prodrug. Hämning av trombocytaggregation av klopidogrel beror helt på en aktiv metabolit. Metabolismen av klopidogrel till dess aktiva metabolit kan försämras vid användning med samtidig medicinering, såsom esomeprazol, som hämmar CYP2C19-aktivitet. Samtidig användning av klopidogrel och 40 mg esomeprazol minskar den farmakologiska aktiviteten av klopidogrel. När du använder NEXIUM IV överväg alternativ anti-trombocytbehandling [se LÄKEMEDELSINTERAKTIONER ].
Hypomagnesemi och mineralmetabolism
Hypomagnesemi, symtomatisk och asymtomatisk, har i sällsynta fall rapporterats hos patienter som behandlats med PPI under minst tre månader, i de flesta fall efter ett års behandling. Allvarliga biverkningar inkluderar stelkramp, arytmier och kramper. Hypomagnesemi kan leda till hypokalcemi och/eller hypokalemi och kan förvärra underliggande hypokalcemi hos riskpatienter. Hos de flesta patienter krävde behandling av hypomagnesemi magnesiumersättning och avbrytande av PPI.
För patienter som förväntas vara på långvarig behandling eller som tar PPI tillsammans med mediciner som digoxin eller läkemedel som kan orsaka hypomagnesemi (t.ex. diuretika), kan sjukvårdspersonal överväga att övervaka magnesiumnivåerna innan PPI-behandlingen påbörjas och med jämna mellanrum [se NEGATIVA REAKTIONER ].
Överväg att övervaka magnesium- och kalciumnivåerna innan NEXIUM IV påbörjas och regelbundet under behandling hos patienter med en redan existerande risk för hypokalcemi (t.ex. hypoparatyreos). Komplettera med magnesium och/eller kalcium vid behov. Om hypokalcemi är behandlingsrefraktär, överväg att avbryta PPI.
Interaktion med johannesört eller rifampin
Läkemedel som inducerar CYP2C19 eller CYP3A4 (som johannesört eller rifampin) kan avsevärt minska esomeprazolkoncentrationerna [se LÄKEMEDELSINTERAKTIONER ]. Undvik samtidig användning av NEXIUM 40mg IV med johannesört eller rifampin.
Interaktioner med diagnostiska undersökningar för neuroendokrina tumörer
Serumkromogranin A (CgA)-nivåer ökar sekundärt till läkemedelsinducerade minskningar i magsyra. Den ökade CgA-nivån kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer. Vårdgivare bör tillfälligt avbryta behandlingen med esomeprazol minst 14 dagar innan CgA-nivåerna bedöms och överväga att upprepa testet om de initiala CgA-nivåerna är höga. Om serietest utförs (t.ex. för övervakning), bör samma kommersiella laboratorium användas för testning, eftersom referensintervallen mellan testerna kan variera [se LÄKEMEDELSINTERAKTIONER ].
Interaktion med metotrexat
Litteratur tyder på att samtidig användning av PPI med metotrexat (främst i höga doser; se metotrexatförskrivningsinformation) kan höja och förlänga serumnivåerna av metotrexat och/eller dess metabolit, vilket kan leda till metotrexattoxicitet. Vid administrering av högdos metotrexat kan ett tillfälligt utsättande av PPI övervägas hos vissa patienter [se LÄKEMEDELSINTERAKTIONER ].
Fundic körtelpolyper
PPI-användning är förknippad med en ökad risk för fundiska körtelpolyper som ökar vid långvarig användning, särskilt efter ett år. De flesta PPI-användare som utvecklade fundic gland polyper var asymtomatiska och fundic gland polyper identifierades tillfälligt vid endoskopi. Använd den kortaste varaktigheten av PPI-behandlingen som är lämplig för det tillstånd som behandlas.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Esomeprazols karcinogena potential utvärderades med omeprazolstudier. I två 24-månaders orala karcinogenicitetsstudier på råttor, omeprazol i dagliga doser på 1,7, 3,4, 13,8, 44,0 och 140,8 mg/kg/dag (cirka 0,4 till 34 gånger den mänskliga dosen på 40 mg/dag uttryckt på en kroppsyta areabas) producerade gastriska ECL-cellkarcinoider på ett dosrelaterat sätt i både han- och honråttor; förekomsten av denna effekt var markant högre hos honråttor, som hade högre blodnivåer av omeprazol. Magkarcinoider förekommer sällan hos obehandlad råtta. Dessutom var ECL-cellshyperplasi närvarande i alla behandlade grupper av båda könen. I en av dessa studier behandlades honråttor med 13,8 mg omeprazol/kg/dag (cirka 3,4 gånger den mänskliga dosen på 40 mg/dag på basis av kroppsyta) under 1 år, och följdes sedan i ytterligare ett år utan läkemedlet . Inga karcinoider sågs hos dessa råttor. En ökad incidens av behandlingsrelaterad ECL-cellshyperplasi observerades i slutet av 1 år (94 % behandlade vs 10 % kontroller). Vid det andra året var skillnaden mellan behandlade och kontrollråttor mycket mindre (46 % mot 26 %) men visade fortfarande mer hyperplasi i den behandlade gruppen. Gastriskt adenokarcinom sågs hos en råtta (2%). Ingen liknande tumör sågs hos han- eller honråttor som behandlats under 2 år. För denna råttstam har ingen liknande tumör noterats historiskt, men ett fynd som involverar endast en tumör är svårt att tolka. En 78-veckors karcinogenicitetsstudie på mus av omeprazol visade inte ökad förekomst av tumörer, men studien var inte avgörande.
Esomeprazol var negativt i Ames-mutationstestet, i in vivo-testet för benmärgscellskromosomavvikelse hos råtta och in vivo-musmikronkärntestet. Esomeprazol var emellertid positivt i in vitro-testet för kromosomavvikelse av humana lymfocyter. Omeprazol var positivt i in vitro humana lymfocytkromosomavvikelsetest, in vivo musbenmärgscellskromosomavvikelsetest och in vivo musmikronukleustest.
De potentiella effekterna av esomeprazol på fertilitet och reproduktionsförmåga utvärderades med omeprazolstudier. Omeprazol vid orala doser upp till 138 mg/kg/dag hos råttor (cirka 34 gånger den mänskliga dosen på 40 mg/dag på basis av kroppsyta) visade sig inte ha någon effekt på reproduktionsförmågan hos föräldradjur.
Användning i specifika populationer
Graviditet
Risksammanfattning
Det finns inga adekvata och välkontrollerade studier med esomeprazol på gravida kvinnor. Esomeprazol är s-isomeren av omeprazol. Tillgängliga epidemiologiska data visar inte på en ökad risk för allvarliga medfödda missbildningar eller andra negativa graviditetsresultat vid användning av omeprazol i första trimestern. Reproduktionsstudier på råttor och kaniner resulterade i dosberoende embryodödlighet vid omeprazoldoser som var cirka 3,4 till 34 gånger en oral human dos på 40 mg (baserat på en kroppsyta för en person på 60 kg).
Teratogenicitet observerades inte i reproduktionsstudier på djur med administrering av oralt esomeprazolmagnesium till råttor och kaniner med doser cirka 68 gånger respektive 42 gånger en oral human dos på 40 mg (baserat på en kroppsyta för en person på 60 kg). . Förändringar i benmorfologi observerades hos avkommor till råttor som doserades under större delen av dräktigheten och laktationen vid doser lika med eller större än cirka 34 gånger en oral human dos på 40 mg. När maternell administrering begränsades till endast dräktighet, fanns det inga effekter på benfysisk morfologi hos avkomman vid någon ålder (se Data ).
De uppskattade bakgrundsriskerna för stora fosterskador och missfall för den indikerade populationen är okända. Alla graviditeter har en bakgrundsrisk för fosterskador, förlust eller andra negativa utfall. I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
Data
Mänskliga data
Esomeprazol är S-isomeren av omeprazol. Fyra epidemiologiska studier jämförde frekvensen av medfödda avvikelser bland spädbarn födda av kvinnor som använde omeprazol under graviditeten med frekvensen av avvikelser bland spädbarn till kvinnor som exponerats för H2-receptorantagonister eller andra kontroller.
En populationsbaserad retrospektiv kohort epidemiologisk studie från Svenska medicinska födelseregistret, som täckte cirka 99 % av graviditeterna, från 1995 till 99, rapporterade om 955 spädbarn (824 exponerade under första trimestern, 39 av dessa exponerade efter första trimestern och 131 exponerade efter första trimestern) vars mödrar använde omeprazol under graviditeten. Antalet spädbarn som exponerades in utero för omeprazol som hade någon missbildning, låg födelsevikt, låg Apgar-poäng eller sjukhusvistelse var liknande det antal som observerades i denna population. Antalet spädbarn födda med ventrikulära septumdefekter och antalet dödfödda spädbarn var något högre hos de omeprazolexponerade spädbarnen än det förväntade antalet i denna population.

En populationsbaserad retrospektiv kohortstudie som täckte alla levande födda i Danmark från 1996 till 2009, rapporterade 1 800 levande födda barn vars mödrar använde omeprazol under graviditetens första trimester och 837 317 levande födda barn vars mödrar inte använde någon protonpumpshämmare. Den totala andelen fosterskador hos spädbarn födda av mödrar med exponering för omeprazol i första trimestern var 2,9 % och 2,6 % hos spädbarn födda till mödrar som inte exponerats för någon protonpumpshämmare under den första trimestern.
En retrospektiv kohortstudie rapporterade på 689 gravida kvinnor som exponerades för antingen H2-blockerare eller omeprazol under första trimestern (134 exponerade för omeprazol) och 1 572 gravida kvinnor som inte exponerades för någondera under första trimestern. Den totala missbildningsfrekvensen hos avkommor födda till mödrar med exponering för omeprazol i första trimestern, en H2-blockerare, eller var oexponerade var 3,6 %, 5,5 % respektive 4,1 %.
En liten prospektiv observationskohortstudie följde 113 kvinnor som exponerats för omeprazol under graviditeten (89 % med exponeringar i första trimestern). Den rapporterade frekvensen av allvarliga medfödda missbildningar var 4 % i omeprazolgruppen, 2 % i kontroller exponerade för icke-teratogener och 2,8 % i sjukdomsparade kontroller. Antalet spontana och elektiva aborter, prematura förlossningar, graviditetsålder vid förlossningen och genomsnittlig födelsevikt var likartade bland grupperna.
Flera studier har inte rapporterat några uppenbara negativa korttidseffekter på spädbarnet när engångsdos oral eller intravenös omeprazol administrerades till över 200 gravida kvinnor som premedicinering för kejsarsnitt under allmän anestesi.
Djurdata
Omeprazol
Reproduktionsstudier utförda med omeprazol på råttor vid orala doser upp till 138 mg/kg/dag (ca 34 gånger en oral human dos på 40 mg på basis av kroppsyta) och på kaniner vid doser upp till 69,1 mg/kg/dag ( cirka 34 gånger en oral human dos på 40 mg på basis av kroppsyta) under organogenesen avslöjade inga bevis för en teratogen potential hos omeprazol. Hos kaniner gav omeprazol i ett dosintervall på 6,9 till 69,1 mg/kg/dag (cirka 3,4 till 34 gånger en oral human dos på 40 mg på kroppsytabasis) administrerat under organogenes dosrelaterade ökningar av embryodödlighet, fosterresorptioner och graviditetsstörningar. Hos råttor observerades dosrelaterad embryo-/fostertoxicitet och postnatal utvecklingstoxicitet hos avkommor från föräldrar som behandlats med omeprazol i 13,8 till 138,0 mg/kg/dag (cirka 3,4 till 34 gånger en oral human dos på 40 mg på en kroppsyta areabas), administreras före parning under laktationsperioden.
Esomeprazol
Inga effekter på embryo-fosterutveckling observerades i reproduktionsstudier med esomeprazolmagnesium på råttor vid orala doser upp till 280 mg/kg/dag (cirka 68 gånger en oral human dos på 40 mg på basis av kroppsyta) eller på kaniner vid orala doser upp till 86 mg/kg/dag (cirka 41 gånger den mänskliga dosen på basis av kroppsyta) administrerade under organogenesen.
En pre- och postnatal utvecklingstoxicitetsstudie på råttor med ytterligare effektmått för att utvärdera benutveckling utfördes med esomeprazolmagnesium i orala doser på 14 till 280 mg/kg/dag (cirka 3,4 till 68 gånger en oral human dos på 40 mg på en kropp ytarea). Neonatal/tidig postnatal (födelse till avvänjning) överlevnad minskade vid doser lika med eller större än 138 mg/kg/dag (cirka 34 gånger en oral human dos på 40 mg på basis av kroppsyta). Kroppsvikt och kroppsviktsökning minskade och neurobeteende eller allmänna utvecklingsförseningar under den omedelbara tidsramen efter avvänjning var uppenbara vid doser lika med eller större än 69 mg/kg/dag (cirka 17 gånger en oral human dos på 40 mg på en kropp ytarea). Dessutom noterades minskad lårbenslängd, bredd och tjocklek av kortikalt ben, minskad tjocklek på tibial tillväxtplatta och minimal till mild benmärgshypocellularitet vid doser lika med eller större än 14 mg/kg/dag (ca 3,4 gånger en oral människa dos på 40 mg på basis av kroppsyta). Fysisk dysplasi i lårbenet observerades hos avkommor till råttor som behandlats med orala doser av esomeprazolmagnesium i doser lika med eller större än 138 mg/kg/dag (cirka 34 gånger en oral human dos på 40 mg på basis av kroppsyta).
Effekter på moderns ben observerades hos dräktiga och ammande råttor i en pre- och postnatal toxicitetsstudie när esomeprazolmagnesium administrerades i orala doser på 14 till 280 mg/kg/dag (cirka 3,4 till 68 gånger en oral human dos på 40 mg på på basis av kroppsyta). När råttor doserades från graviditetsdag 7 till avvänjning på postnatal dag 21, observerades en statistiskt signifikant minskning av moderns lårbensvikt på upp till 14 % (jämfört med placebobehandling) vid doser lika med eller större än 138 mg/kg/dag (ca 34 gånger en oral human dos på 40 mg på basis av kroppsyta).
En pre- och postnatal utvecklingsstudie på råttor med esomeprazol strontium (med ekvimolära doser jämfört med esomeprazolmagnesiumstudie) gav liknande resultat på mödrar och ungar som beskrivits ovan.
En uppföljningsstudie av utvecklingstoxicitet på råttor med ytterligare tidpunkter för att utvärdera utvecklingen av ungben från postnatal dag 2 till vuxen ålder utfördes med esomeprazolmagnesium i orala doser på 280 mg/kg/dag (cirka 68 gånger en oral human dos på 40 mg på baserat på kroppsyta) där administrering av esomeprazol var från antingen graviditetsdag 7 eller graviditetsdag 16 fram till förlossningen. När maternell administrering var begränsad till enbart graviditet, fanns det inga effekter på benfysisk morfologi hos avkomman vid någon ålder.
Laktation
Risksammanfattning
Esomeprazol är S-isomeren av omeprazol och begränsade data tyder på att omeprazol kan finnas i bröstmjölk. Det finns inga kliniska data om effekterna av esomeprazol på det ammade barnet eller på mjölkproduktionen. De utvecklingsmässiga och hälsomässiga fördelarna med amning bör övervägas tillsammans med moderns kliniska behov av NEXIUM 20 mg och eventuella negativa effekter på det ammade barnet från NEXIUM eller från det underliggande moderns tillståndet.
Pediatrisk användning
Säkerheten och effektiviteten av NEXIUM 20 mg IV har fastställts hos pediatriska patienter i åldern 1 månad till 17 år för korttidsbehandling av GERD med EE, som ett alternativ till oral behandling när oral NEXIUM 40 mg inte är möjlig eller lämplig.
Användning av NEXIUM 40mg IV i denna åldersgrupp baseras på extrapolering av vuxeneffekt till barn och val av dos baserat på exponeringsmatchning av pediatrik till vuxna stöds av följande bevis: a) resultat observerade från en farmakokinetisk (PK) studie på NEXIUM 20 mg IV för injektion hos pediatriska patienter, b) förutsägelser från en PK-populationsmodell som jämför IV PK-data mellan vuxna och pediatriska patienter, och c) samband mellan exponering och farmakodynamiska resultat från vuxen IV och pediatriska orala data och d) PK-resultat från adekvata och välkontrollerade studier som stödde godkännandet av NEXIUM 40mg IV hos vuxna [se NEGATIVA REAKTIONER , KLINISK FARMAKOLOGI , Kliniska studier ].
Säkerheten och effektiviteten av NEXIUM IV har inte fastställts hos patienter yngre än 1 månad för behandling av GERD med EE eller för riskreduktion av återblödning av mag- eller duodenalsår efter terapeutisk endoskopi.
Data från unga djur
I en toxicitetsstudie hos juvenila råttor administrerades esomeprazol med både magnesium- och strontiumsalter i orala doser cirka 34 till 68 gånger en daglig dos på 40 mg för människa baserat på kroppsyta. Ökning av dödsfall sågs vid den höga dosen, och vid alla doser av esomeprazol, var det minskningar i kroppsvikt, kroppsviktsökning, lårbensvikt och lårbenslängd, och minskningar i total tillväxt [se Icke-klinisk toxikologi ].
Geriatrisk användning
en klinisk prövning av patienter med blödande mag- eller duodenalsår var 52 % av 375 patienter randomiserade till NEXIUM IV 65 år och äldre. Inga övergripande skillnader i säkerhet och effekt observerades mellan äldre och yngre individer, och annan rapporterad klinisk erfarenhet av NEXIUM 40 mg IV och oral esomeprazol har inte identifierat skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte identifieras. utesluten.
Nedsatt leverfunktion
GERD Med EE
Exponeringen för esomeprazol ökade avsevärt hos patienter med gravt nedsatt leverfunktion (Child-Pugh klass C) men inte hos patienter med lätt till måttligt nedsatt leverfunktion (Child-Pugh klass A och B) jämfört med patienter med normal leverfunktion [se KLINISK FARMAKOLOGI ].
För vuxna patienter är ingen dosjustering nödvändig för lätt till måttligt nedsatt leverfunktion. För patienter med gravt nedsatt leverfunktion är den maximala rekommenderade dosen 20 mg en gång dagligen [se DOSERING OCH ADMINISTRERING ].
Riskminskning av återblödning från mag- eller duodenalsår efter terapeutisk endoskopi
Det finns inga tillgängliga farmakokinetiska data för NEXIUM 20 mg IV administrerat som kontinuerlig intravenös administrering till patienter med nedsatt leverfunktion. Exponering för intravenös omeprazol, varav esomeprazol är en enantiomer, ökade hos patienter med alla grader av nedsatt leverfunktion jämfört med patienter med normal leverfunktion [se KLINISK FARMAKOLOGI ].
För vuxna patienter är ingen dosjustering av den initiala laddningsdosen NEXIUM IV 80 mg nödvändig för patienter med någon grad av nedsatt leverfunktion. Minska hastigheten för den kontinuerliga infusionen till 6 mg/timme för patienter med lätt till måttligt nedsatt leverfunktion (Child-Pugh klass A och B) och till 4 mg/timme för patienter med gravt nedsatt leverfunktion (Child-Pugh klass C) [se DOSERING OCH ADMINISTRERING ].
ÖVERDOS
Symtomen som beskrivs i samband med avsiktlig överdosering av NEXIUM 40 mg (begränsad erfarenhet av doser över 240 mg/dag) är övergående. Rapporter om överdosering med omeprazol hos människor kan också vara relevanta. Doserna varierade upp till 2 400 mg (120 gånger den vanliga rekommenderade kliniska dosen). Manifestationerna var varierande, men inkluderade förvirring, dåsighet, dimsyn, takykardi, illamående, diafores, rodnad, huvudvärk, muntorrhet och andra biverkningar liknande de som ses vid rekommenderade doser. Se den fullständiga förskrivningsinformationen för oral omeprazol för fullständig säkerhetsinformation. Ingen specifik motgift för esomeprazol är känd. Eftersom esomeprazol är mycket proteinbundet förväntas det inte avlägsnas genom dialys. I händelse av överdosering ska behandlingen vara symptomatisk och stödjande.
Om överexponering inträffar, ring ditt giftkontrollcenter på 1-800-222-1222 för aktuell information om hantering av förgiftning eller överdosering.
KONTRAINDIKATIONER
- NEXIUM 20mg IV är kontraindicerat hos patienter med känd överkänslighet mot substituerade bensimidazoler eller mot någon komponent i formuleringen. Överkänslighetsreaktioner kan inkludera anafylaxi, anafylaktisk chock, angioödem, bronkospasm, akut tubulointerstitiell nefrit och urtikaria [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
- Protonpumpshämmare (PPI), inklusive NEXIUM 20mg IV, är kontraindicerade hos patienter som får produkter som innehåller rilpivirin [se LÄKEMEDELSINTERAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Esomeprazol tillhör en klass av antisekretoriska föreningar, de substituerade bensimidazolerna, som undertrycker magsyrasekretion genom specifik hämning av H+/K+ ATPas-enzymsystemet vid den sekretoriska ytan av magparietalcellen. Esomeprazol protoneras och omvandlas i den sura delen av parietalcellen och bildar den aktiva hämmaren, den akirala sulfenamiden. Eftersom detta enzymsystem betraktas som syrapumpen (proton) i magslemhinnan, har esomeprazol karakteriserats som en magsyrapumpshämmare genom att det blockerar det sista steget i syraproduktionen. Denna effekt är dosrelaterad och leder till hämning av både basal och stimulerad syrasekretion oavsett stimulans.
Farmakodynamik
Antisekretorisk aktivitet
Effekten av esomeprazol på 24-timmars intragastrisk pH hos friska försökspersoner utvärderades i två studier med 20 mg och 40 mg NEXIUM 20 mg IV infunderat intravenöst en gång dagligen under 30 minuter i 5 dagar, som visas i Tabell 7.
Effekterna av esomeprazol på 24-timmars intragastrisk pH efter administrering av en intravenös infusion av 80 mg NEXIUM.IV under 30 minuter följt av en kontinuerlig infusion av 8 mg/timme i 23,5 timmar utvärderades i två studier.
Hos H. pylori-negativa friska kaukasiska försökspersoner (n=24) var den procentuella tiden under 24 timmar (95 % KI) när det intragastriska pH-värdet var > 6 och > 7 52,3 % (40,3, 64,4) och 4,8 % (1,8, 7.8), respektive.
Hos H. pylori-positiva (n=8) och H. pylori-negativa (n=11) friska kinesiska försökspersoner var den procentuella tiden under 24 timmar (95 % KI) när det intragastriska pH-värdet var > 6 och > 7 53 % ( 45,6, 60,3) och 15,1 % (9,5, 20,7). Andelen tid med intragastriskt pH > 6 [59 % vs. 47 %] och med pH > 7 [17 % vs. 11 %] tenderade att vara större hos de H. pylori-positiva försökspersonerna jämfört med H. pylori-negativa försökspersoner.
Serum Gastrin Effekter
Effekten av esomeprazol på serumgastrinkoncentrationer utvärderades hos cirka 2 700 patienter i kliniska prövningar av oralt esomeprazol i upp till 8 veckor och hos över 1 300 patienter som behandlades i upp till 12 månader. Den genomsnittliga fastande gastrinnivån ökade på ett dosrelaterat sätt. Ökningen av gastrinkoncentrationer i serum nådde en platå inom två till tre månader efter behandlingen och återgick till utgångsnivåerna inom fyra veckor efter avslutad behandling.
Ökat gastrin orsakar enterokromaffinliknande cellhyperplasi och ökade serumnivåer av kromogranin A (CgA). De ökade CgA-nivåerna kan orsaka falskt positiva resultat i diagnostiska undersökningar av neuroendokrina tumörer [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Enterokromaffinliknande (ECL) celleffekter
Det finns inga tillgängliga data om effekterna av intravenös esomeprazol på ECL-celler.
Humana gastriska biopsiprover har erhållits från mer än 3 000 patienter (både barn och vuxna) som behandlats oralt med omeprazol i kliniska långtidsstudier. Incidensen av ECL-cellshyperplasi i dessa studier ökade med tiden; dock har inget fall av ECL-cellkarcinoider, dysplasi eller neoplasi hittats hos dessa patienter [se Icke-klinisk toxikologi ].
Hos över 1 000 patienter som behandlats med oral esomeprazol (10 mg, 20 mg eller 40 mg/dag) i upp till 12 månader, ökade prevalensen av ECL-cellshyperplasi med tiden och dosen. Ingen patient utvecklade ECL-cellkarcinoider, dysplasi eller neoplasi i magslemhinnan.
Endokrina effekter
Esomeprazol hade ingen effekt på sköldkörtelfunktionen när det gavs i orala doser på 20 mg eller 40 mg under 4 veckor. Andra effekter av esomeprazol på det endokrina systemet utvärderades i studier av omeprazol. Orala doser av omeprazol 30 mg eller 40 mg per dag under 2 till 4 veckor hade ingen effekt på kolhydratmetabolism, cirkulerande nivåer av bisköldkörtelhormon, kortisol, östradiol, testosteron, prolaktin, kolecystokinin eller sekretin.
Farmakokinetik
Absorption
Farmakokinetiken för esomeprazol hos friska försökspersoner efter administrering av NEXIUM IV 20 mg och 40 mg en gång dagligen som intravenös infusion under 30 minuter i 5 dagar visas i Tabell 8.
Efter intravenös administrering av NEXIUM 40 mg IV till 24 friska försökspersoner som en laddningsdos på 80 mg under 30 minuter följt av en kontinuerlig infusion av 8 mg/timme i 23,5 timmar (i totalt 24 timmar), esomeprazols farmakokinetiska parametrar [geometriskt medelvärde] (95 % KI)] var enligt följande: AUCt 111,1 mikromol*h/L (100,5, 122,7 mikromol*h/L), Cmax 15,0 mikromol/L (13,5, 16,6 mikromol/L) och steady state plasmakoncentration (Css) 3,9 mikromol/L (3,5, 4,5 mikromol/L). I en annan studie av friska kaukasiska försökspersoner administrerades samma behandlingsregim.
Esomeprazol är en tidsberoende hämmare av CYP2C19, vilket resulterar i autoinhibering och olinjär farmakokinetik. Den systemiska exponeringen ökar på ett mer än dosproportionellt sätt efter flera orala doser av esomeprazol. Jämfört med den första dosen ökade den systemiska exponeringen (Cmax och AUC0-24h) vid steady state efter dosering en gång dagligen med 43 % respektive 90 % jämfört med efter den första dosen för 20 mg-dosen och ökade med 95 % respektive 159 % för 40 mg dosen.
Distribution
Esomeprazol är till 97 % bundet till plasmaproteiner. Plasmaproteinbindningen är konstant över koncentrationsintervallet 2 till 20 mikromol/L. Den skenbara distributionsvolymen vid steady state hos friska försökspersoner är cirka 16 L.
Eliminering
Ämnesomsättning
Esomeprazol metaboliseras i stor utsträckning i levern av cytokrom P450 (CYP) enzymsystemet. Metaboliterna av esomeprazol saknar antisekretorisk aktivitet. Huvuddelen av esomeprazols metabolism är beroende av isoenzymet CYP2C19, som bildar hydroxi- och desmetylmetaboliterna. Den återstående mängden är beroende av CYP3A4 som bildar sulfonmetaboliten.
Exkretion
Esomeprazol utsöndras som metaboliter främst i urin men även i avföring. Mindre än 1 % av moderläkemedlet utsöndras i urinen. Esomeprazol elimineras fullständigt från plasma och det sker ingen ackumulering vid administrering en gång dagligen. Halveringstiden i plasma för esomeprazol efter intravenös administrering av NEXIUM IV är cirka 1,1 till 1,4 timmar och förlängs med ökande doser.
Plasmaclearance (CL) är cirka 5,9 till 7,2 l/timme under administrering av NEXIUM 40 mg IV som en intravenös infusion av 80 mg under 30 minuter följt av en kontinuerlig infusion av 8 mg/timme i 23,5 timmar.
Specifika populationer
Geriatriska patienter
AUC- och Cmax-värdena för esomeprazol var något högre (25 % respektive 18 %) hos äldre jämfört med yngre försökspersoner vid steady state. Denna ökning av exponeringen anses inte vara kliniskt relevant.
Pediatriska patienter
Farmakokinetiken för esomeprazol utvärderades hos 50 pediatriska patienter från födseln till 17 års ålder, inklusive (varav 44 pediatriska patienter var 1 månad till 17 år) i en randomiserad, öppen, multinationell, multipeldosstudie med 20 mg NEXIUM 40 mg IV administrerat som en intravenös injektion en gång dagligen på 3 minuter. Esomeprazols AUC-värden i plasma var 183 % och 60 % högre hos pediatriska patienter i åldern 6 till 11 år respektive 12 till 17 år jämfört med vuxna.
Efterföljande farmakokinetiska analyser förutspådde att följande doseringsregimer skulle uppnå jämförbara steady-state plasmaexponeringar (AUC0-24) med de som observerades hos vuxna patienter som administrerades 20 mg NEXIUM IV en gång dagligen: 0,5 mg/kg en gång dagligen för pediatriska patienter 1 månad till 11 månader ålder, 10 mg en gång dagligen för pediatriska patienter 1 år till 17 år med kroppsvikt mindre än 55 kg och 20 mg en gång dagligen för pediatriska patienter 1 år till 17 år med kroppsvikt på 55 kg och mer. En ökning av infusionslängden från 3 minuter till 10 minuter eller 30 minuter förutspåddes ge steady-state Cmax-värden som var jämförbara med de som observerades hos vuxna patienter vid doserna 40 mg respektive 20 mg NEXIUM IV [se Användning i specifika populationer ].
Manliga Och Kvinnliga Patienter
AUC- och Cmax-värdena för esomeprazol var något högre (13 %) hos kvinnor än hos män vid steady state vid oral dosering. Liknande skillnader har setts för intravenös administrering av esomeprazol. Denna ökning av exponeringen anses inte vara kliniskt relevant.
Patienter med nedsatt njurfunktion
Farmakokinetiken för esomeprazol hos patienter med nedsatt njurfunktion förväntas inte förändras i förhållande till friska försökspersoner eftersom mindre än 1 % av esomeprazol utsöndras oförändrat i urinen.
Patienter med nedsatt leverfunktion
Den steady state farmakokinetiken för esomeprazol erhållen efter administrering av 40 mg oralt en gång dagligen till 4 patienter vardera med mild (Child-Pugh klass A), måttlig (Child-Pugh klass B) och svår (Child-Pugh klass C) nedsatt leverfunktion var jämfört med de som erhölls hos 36 manliga och kvinnliga GERD-patienter med normal leverfunktion. Hos patienter med lätt till måttligt nedsatt leverfunktion låg AUC inom det intervall som kunde förväntas hos patienter med normal leverfunktion. Hos patienter med gravt nedsatt leverfunktion var AUC 2 till 3 gånger högre än hos patienter med normal leverfunktion. [ser Användning i specifika populationer ].
Det finns inga tillgängliga farmakokinetiska data för esomeprazol administrerat som kontinuerlig intravenös administrering till patienter med nedsatt leverfunktion. Farmakokinetiken för intravenös omeprazol 80 mg infunderad under 30 minuter, följt av 8 mg/timme under 47,5 timmar hos patienter med mild (Child-Pugh klass A; n=5), måttlig (Child-Pugh klass B; n=4) och allvarlig (Child-Pugh klass C; n=3) nedsatt leverfunktion jämfördes med de som erhölls hos 24 friska manliga och kvinnliga försökspersoner. Hos patienter med lätt och måttligt nedsatt leverfunktion var omeprazolclearance och steady state plasmakoncentrationen cirka 35 % lägre respektive 50 % högre än hos friska försökspersoner. Hos patienter med gravt nedsatt leverfunktion var omeprazolclearance 50 % av det hos friska försökspersoner och plasmakoncentrationen vid steady state var dubbelt så hög som hos friska försökspersoner [se Användning i specifika populationer ].
Läkemedelsinteraktionsstudier
Effekt av Esomeprazol/Omeprazol på andra droger
In vitro- och in vivo-studier har visat att esomeprazol sannolikt inte kommer att hämma CYP 1A2, 2A6, 2C9, 2D6, 2E1 och 3A4.
Antiretrovirala medel
För vissa antiretrovirala läkemedel, såsom rilpivirin, atazanavir och nelfinavir, har minskade serumkoncentrationer rapporterats när de ges tillsammans med omeprazol [se LÄKEMEDELSINTERAKTIONER ].
Rilpivirin
Efter flera doser av rilpivirin (150 mg, dagligen) och omeprazol (20 mg, dagligen), minskade AUC med 40 %, Cmax med 40 % och Cmin med 33 % för rilpivirin [se KONTRAINDIKATIONER ].
Nelfinavir
Efter flera doser av nelfinavir (1250 mg, två gånger dagligen) och omeprazol (40 mg dagligen), minskade AUC med 36 % och 92 %, Cmax med 37 % och 89 % och Cmin med 39 % respektive 75 % för nelfinavir och M8 .
Atazanavir
Efter flera doser av atazanavir (400 mg, dagligen) och omeprazol (40 mg, dagligen, 2 timmar före atazanavir), minskade AUC med 94 %, Cmax med 96 % och Cmin med 95 %.
Saquinavir
Efter upprepad dosering av saquinavir/ritonavir (1000/100 mg) två gånger dagligen i 15 dagar med omeprazol 40 mg dagligen samtidigt administrerat dagarna 11 till 15. AUC ökade med 82 %, Cmax med 75 % och Cmin med 106 %. Mekanismen bakom denna interaktion är inte helt klarlagd.
Clopidogrel
I en crossover-studie fick friska försökspersoner klopidogrel (300 mg laddningsdos följt av 75 mg per dag som underhållsdos i 28 dagar) enbart och med esomeprazol (40 mg oralt en gång dagligen samtidigt som klopidogrel) i 29 dagar. Exponeringen för den aktiva metaboliten av klopidogrel minskade med 35 % till 40 % under denna tidsperiod när klopidogrel och esomeprazol administrerades tillsammans. Farmakodynamiska parametrar mättes också och visade att förändringen i hämning av trombocytaggregation var relaterad till förändringen i exponeringen för klopidogrel aktiv metabolit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , LÄKEMEDELSINTERAKTIONER ].
Mykofenolatmofetil
Administrering av omeprazol 20 mg två gånger dagligen under 4 dagar och en engångsdos på 1000 mg MMF cirka en timme efter den sista dosen av omeprazol till 12 friska försökspersoner i en cross-over-studie resulterade i en 52 % minskning av Cmax och 23 % minskning i AUC för MPA [se LÄKEMEDELSINTERAKTIONER ].
Cilostazol
Omeprazol verkar som en hämmare av CYP2C19. Omeprazol, givet i doser om 40 mg dagligen under en vecka till 20 friska försökspersoner i en cross-over-studie, ökade Cmax och AUC för cilostazol med 18 % respektive 26 %. Cmax och AUC för en av de aktiva metaboliterna, 3,4-dihydro-cilostazol, som har 4-7 gånger aktiviteten av cilostazol, ökade med 29% respektive 69%. Samtidig administrering av cilostazol och omeprazol förväntas öka koncentrationerna av cilostazol och den ovan nämnda aktiva metaboliten [se LÄKEMEDELSINTERAKTIONER ].
Diazepam
Samtidig administrering av esomeprazol 30 mg och diazepam, ett CYP2C19-substrat, resulterade i en 45 % minskning av clearance av diazepam. Ökade plasmanivåer av diazepam observerades 12 timmar efter dosering och framåt. Men vid den tidpunkten var plasmanivåerna av diazepam under det terapeutiska intervallet, och därför är det osannolikt att denna interaktion är av klinisk relevans.
Digoxin
Samtidig administrering av omeprazol 20 mg en gång dagligen och digoxin hos friska försökspersoner ökade biotillgängligheten av digoxin med 10 % (30 % hos två försökspersoner) [se LÄKEMEDELSINTERAKTIONER ].
Andra droger
Samtidig administrering av esomeprazol och antingen naproxen (icke-selektivt NSAID) identifierade inga kliniskt relevanta förändringar i de farmakokinetiska profilerna för dessa NSAID.
Effekt av andra droger på Esomeprazol/Omeprazol
Johannesört
en cross-over-studie på 12 friska manliga försökspersoner minskade johannesört (300 mg tre gånger dagligen i 14 dagar) signifikant den systemiska exponeringen av omeprazol hos CYP2C19-fattiga metaboliserare (Cmax och AUC minskade med 37,5 % och 37,9 %, respektive) och omfattande metaboliserare (Cmax och AUC minskade med 49,6 % respektive 43,9 %) [se LÄKEMEDELSINTERAKTIONER ].
Vorikonazol
Samtidig administrering av omeprazol och voriconazol (en kombinerad hämmare av CYP2C19 och CYP3A4) resulterade i mer än en fördubbling av exponeringen för omeprazol. När vorikonazol (400 mg var 12:e timme under en dag, följt av 200 mg en gång dagligen i 6 dagar) gavs tillsammans med omeprazol (40 mg en gång dagligen i 7 dagar) till friska försökspersoner, var steady-state Cmax och AUC0-24 för omeprazol signifikant ökad: i genomsnitt 2 gånger (90 % KI: 1,8, 2,6) respektive 4 gånger (90 % KI: 3,3, 4,4), jämfört med när omeprazol gavs utan vorikonazol [se LÄKEMEDELSINTERAKTIONER ].
Andra droger
Samtidig administrering av esomeprazol och orala preventivmedel, diazepam, fenytoin, kinidin, naproxen (icke-selektivt NSAID) verkade inte förändra den farmakokinetiska profilen för esomeprazol.
Mikrobiologi
Effekter på gastrointestinal mikrobiell ekologi
Minskad surhet i magsäcken på grund av alla medel, inklusive protonpumpshämmare, ökar magräkningen av bakterier som normalt finns i mag-tarmkanalen. Behandling med protonpumpshämmare kan leda till något ökad risk för gastrointestinala infektioner som Salmonella och Campylobacter och, hos inlagda patienter, eventuellt även Clostridium difficile.
Farmakogenomik
CYP2C19, ett polymorft enzym, är involverat i metabolismen av esomeprazol. CYP2C19*1-allelen är fullt funktionell medan CYP2C19*2- och *3-allelen är icke-funktionella. Det finns andra alleler associerade med ingen eller reducerad enzymfunktion. Patienter som bär på två fullt fungerande alleler är omfattande metaboliserare och de som bär två alleler med förlust av funktion är dåliga metaboliserare. Den systemiska exponeringen för esomeprazol varierar med patientens ämnesomsättningsstatus: dåliga metaboliserare > mellanliggande metaboliserare > omfattande metaboliserare. Ungefär 3 % av kaukasierna och 15 till 20 % av asiterna är CYP2C19-fattiga metaboliserare.
Systemiska esomeprazolexponeringar var måttligt högre (cirka 17 %) hos CYP2C19 intermediära metaboliserare (IM; n=6) jämfört med omfattande metaboliserare (EM; n=17) av CYP2C19. Liknande farmakokinetiska skillnader noterades över dessa genotyper i en studie av kinesiska friska försökspersoner som inkluderade 7 EM och 11 IM. Det finns mycket begränsad farmakokinetisk information för dåliga metaboliserare (PM) från dessa studier.
Vid steady state efter administrering en gång dagligen av NEXIUM 40 mg IV 40 mg, är förhållandet mellan AUC hos Poor Metabolizers och AUC i resten av befolkningen (EM) cirka 1,5. Denna förändring i exponering anses inte vara kliniskt betydelsefull.
Djurtoxikologi och/eller farmakologi
Reproduktionsstudier
Reproduktionsstudier har utförts på råttor vid orala doser upp till 280 mg/kg/dag (cirka 68 gånger en oral human dos på 40 mg på basis av kroppsyta) och på kaniner vid orala doser upp till 86 mg/kg/dag (cirka 42 gånger en oral human dos på 40 mg på basis av kroppsyta) och har inte visat några tecken på nedsatt fertilitet eller fostret skada på grund av esomeprazol [se Användning i specifika populationer ].
Studie av unga djur
En 28-dagars toxicitetsstudie med en 14-dagars återhämtningsfas utfördes på unga råttor med esomeprazolmagnesium i doser på 70 till 280 mg/kg/dag (ca 17 till 68 gånger en daglig oral human dos på 40 mg på en kroppsyta arealbas). En ökning av antalet dödsfall vid den höga dosen på 280 mg/kg/dag observerades när juvenila råttor administrerades esomeprazolmagnesium från postnatal dag 7 till postnatal dag 35. Dessutom doser lika med eller större än 140 mg/kg/ dag (cirka 34 gånger en daglig oral human dos på 40 mg på basis av kroppsyta), gav behandlingsrelaterade minskningar i kroppsvikt (cirka 14 %) och kroppsviktsökning, minskningar i lårbensvikt och lårbenslängd, och påverkade totalt sett tillväxt. Jämförbara fynd som beskrivs ovan har också observerats i denna studie med ett annat esomeprazolsalt, esomeprazol strontium, vid ekvimolära doser av esomeprazol.
Kliniska studier
Syra undertryckande i GERD
Fyra multicenter, öppna, tvåperioders crossover-studier genomfördes för att jämföra de farmakodynamiska effekterna av esomeprazol efter intravenös eller oral administrering på syrasuppression hos 206 patienter med symtom på GERD med eller utan erosiv esofagit. Patienterna randomiserades till att få antingen 20 eller 40 mg NEXIUM 40 mg IV eller oralt esomeprazol en gång dagligen i 10 dagar (period 1), och byttes sedan i period 2 till den andra formuleringen under 10 dagar, vilket matchade deras respektive dos från period 1. NEXIUM 40 mg IV 20 mg och 40 mg administrerades som en 3-minuters injektion i två av studierna och som en 15-minuters infusion i de andra två studierna.
Patientpopulationen varierade från 18 till 72 år gamla; 54 % var kvinnor; 53 % kaukasiska, 24 % svarta, 5 % asiatiska och 17 % annan ras. Basalsyraproduktion (BAO) och maximal syraproduktion (MAO) bestämdes 22 till 24 timmar efter dosering på period 1, dag 11; på period 2, dag 3; och på period 2, dag 11. BAO och MAO uppskattades från 1-timmes kontinuerliga samlingar av maginnehåll före och efter (respektive) subkutan injektion av 6,0 mcg/kg pentagastrin.
I dessa studier, efter 10 dagars administrering en gång dagligen, liknade NEXIUM IV 20 mg och 40 mg motsvarande orala doser av esomeprazol i deras förmåga att undertrycka BAO och MAO hos dessa GERD-patienter (se tabell 9 nedan).
Det fanns inga större förändringar i syradämpningen vid byte mellan intravenösa och orala beredningsformer.
Blödande mag- eller duodenalsår
En randomiserad, dubbelblind, placebokontrollerad klinisk studie utfördes på 764 patienter som fick endoskopiskt bekräftad mag- eller duodenalsårblödning. Befolkningen var 18 till 98 år gammal; 68 % var män, 87 % kaukasiska, 1 % svarta, 7 % asiatiska och 4 % annan ras. Efter endoskopisk hemostas randomiserades patienterna till antingen placebo eller NEXIUM IV 80 mg som en intravenös infusion under 30 minuter följt av en kontinuerlig infusion av 8 mg/timme under totalt 72 timmar. Efter den första 72-timmarsperioden fick alla patienter en oral PPI i 27 dagar. Förekomsten av återblödning inom 3 dagar efter randomisering var 5,9 % i den NEXIUM 20 mg IV-behandlade gruppen jämfört med 10,3 % för placebogruppen (behandlingsskillnad -4,4 %; 95 % konfidensintervall: -8,3 %, -0,6 %; p=0,03 ). Denna behandlingsskillnad liknade den som observerades vid dag 7 och dag 30, under vilka alla patienter fick en oral PPI.
En randomiserad, dubbelblind, placebokontrollerad singelcenterstudie utförd i Hongkong visade också en minskning jämfört med placebo i risken för återblödning inom 72 timmar hos patienter med blödande mag- eller duodenalsår som fick racemisk omeprazol, varav 50 % är S-enantiomeren esomeprazol.
PATIENTINFORMATION
Negativa reaktioner
Rekommendera patienter att rapportera till sin vårdgivare om de upplever några tecken eller symtom som överensstämmer med:
- Överkänslighetsreaktioner [se KONTRAINDIKATIONER ]
- Akut Tubulointerstitiell nefrit [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Clostridium difficile-associerad diarré [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Benfraktur [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Allvarliga kutana biverkningar [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Kutan och systemisk lupus erythematosus [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hypomagnesemi och mineralmetabolism [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Läkemedelsinteraktioner
Rekommendera patienter att rapportera till sin vårdgivare innan de påbörjar behandling med något av följande:
- Rilpivirin-innehållande produkter [se KONTRAINDIKATIONER ]
- Clopidogrel [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Johannesört eller rifampin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Högdos metotrexat [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Administrering
- Informera patienterna om att antacida kan användas när de tar NEXIUM 40mg IV
