Rhinocort 100mcg Budesonide Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Rhinocort Aqua och hur används det?
Rhinocort Aqua (budesonid) nässpray är en steroid som används för att behandla nasala symtom som trängsel, nysningar och rinnande näsa orsakade av säsongsbetonade allergier eller allergier året runt. Rhinocort Aqua nässpray används också för att förhindra att näspolyper återkommer efter kirurgiskt avlägsnande.
Vilka är biverkningarna av Rhinocort 100mcg Aqua?
Vanliga biverkningar av Rhinocort Aqua nässpray inkluderar:
- torr näsa/hals eller irritation,
- öm hals,
- hosta,
- nysning,
- näsblod,
- obehaglig smak/lukt,
- sår eller vita fläckar inuti eller runt näsan, eller
- smärta, svullnad, sveda, klåda eller irritation runt näsan.
Tala om för din läkare om du har sällsynta men allvarliga biverkningar av Rhinocort Aqua nässpray inklusive:
- förlust av smak eller lukt, eller
- smärta eller sår i näsan.
BESKRIVNING
Budesonid, den aktiva ingrediensen i RHINOCORT AQUA (budesonid) nässpray, är en antiinflammatorisk syntetisk kortikosteroid.
Det betecknas kemiskt som (RS)-11-beta, 16-alfa, 17, 21-tetrahydroxipregna-l,4-dien-3,20-dion cyklisk 16, 17-acetal med butyraldehyd.
Budesonid tillhandahålls som en blandning av två epimerer (22R och 22S).
Den empiriska formeln för budesonid är C25H34O6 och dess molekylvikt är 430,5.
Dess strukturformel är:
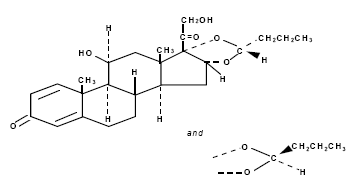
Budesonid är ett vitt till benvitt, luktfritt pulver som är praktiskt taget olösligt i vatten och i heptan, svårlösligt i etanol och fritt lösligt i kloroform.
Dess fördelningskoefficient mellan oktanol och vatten vid pH 5 är 1,6 x 103.
RHINOCORT AQUA (budesonid) nässpray är en oparfymerad, uppmätta doser, manuell pumpade sprayformulering som innehåller en mikroniserad suspension av budesonid i ett vattenhaltigt medium. Mikrokristallin cellulosa och karboximetylcellulosanatrium, vattenfri dextros, polysorbat 80, dinatriumedetat, kaliumsorbat och renat vatten finns i detta medium; saltsyra tillsätts för att justera pH till ett mål på 4,5.
RHINOCORT 100 mcg AQUA nässpray ger 32 mcg budesonid per spray.
Varje flaska RHINOCORT 100 mcg AQUA (budesonid) nässpray 32 mcg innehåller 120 doserade sprayer efter initial priming.
Före första användningen måste behållaren skakas försiktigt och pumpen måste förberedas genom att man aktiverar den åtta gånger. Om pumpen används dagligen behöver den inte fyllas på igen. Om den inte har använts under två på varandra följande dagar, fyll på med en spray eller tills en fin spray dyker upp. Om den inte har använts på mer än 14 dagar, skölj applikatorn och fyll på med två sprayer eller tills en fin spray dyker upp.
INDIKATIONER
Behandling av säsongsbunden eller perenn allergisk rinit
RHINOCORT AQUA (budesonid) Nässpray är indicerat för behandling av nässymtom på säsongsbunden eller perenn allergisk rinit hos vuxna och barn från sex år och äldre.
DOSERING OCH ADMINISTRERING
Den rekommenderade startdosen för vuxna och barn 6 år och äldre är 64 mcg per dag administrerat som en spray per näsborre av RHINOCORT AQUA (budesonid) nässpray 32 mcg en gång dagligen. Vissa patienter som inte uppnår symtomkontroll vid den rekommenderade startdosen kan ha nytta av en ökad dos. Den maximala rekommenderade dosen för vuxna (12 år och äldre) är 256 mcg per dag administrerat som fyra sprayer per näsborre en gång dagligen av RHINOCORT AQUA (budesonid) nässpray 32 mcg och den maximala rekommenderade dosen för pediatriska patienter (6 till
Det är alltid önskvärt att titrera en enskild patient till den lägsta effektiva dosen för att minska risken för biverkningar. En förbättring av nasala symtom kan noteras hos patienter inom 10 timmar efter att de först använt RHINOCORT 100 mcg AQUA (budesonid) nässpray, men klinisk förbättring tar vanligtvis 1-2 dagar med maximal nytta på cirka 2 veckor. När maximal nytta har uppnåtts och symtomen har kontrollerats, kan en minskning av dosen vara effektiv för att upprätthålla kontrollen över symtomen på allergisk rinit hos patienter som initialt kontrollerades med högre doser.
Före första användningen måste behållaren skakas försiktigt och pumpen måste förberedas genom att man aktiverar den åtta gånger. Om pumpen används dagligen behöver den inte fyllas på igen. Om den inte har använts under två på varandra följande dagar, fyll på med en spray eller tills en fin spray dyker upp. Om den inte har använts på mer än 14 dagar, skölj applikatorn och fyll på med två sprayer eller tills en fin spray dyker upp. Skaka behållaren försiktigt före varje användning.
Illustrerad Patientens bruksanvisning åtfölja varje förpackning med RHINOCORT AQUA (budesonid) nässpray 32 mcg.
HUR LEVERERAS
Doseringsformer och styrkor
RHINOCORT AQUA (budesonid) Nässpray är en nässpraysuspension. Varje spray ger 32 mcg budesonid. Varje flaska RHINOCORT 100 mcg AQUA (budesonid) nässpray 32 mcg innehåller 120 doserade sprayer efter initial priming.
RHINOCORT 100 mcg AQUA (budesonid) nässpray 32 mcg finns i en bärnstensfärgad glasflaska med en pumpspray med uppmätt dos och en grön skyddslock. RHINOCORT 100 mcg AQUA (budesonid) Nässpray 32 mcg ( NDC 0186-1070-08) ger 120 doserade sprayer efter initial priming; netto fyllvikt 8,6 g. RHINOCORT 100 mcg AQUA (budesonid) nässpray 32 mcg flaska har fyllts med ett överskott för att klara primingaktiviteten. Flaskan ska kasseras efter 120 sprayningar efter initial priming, eftersom mängden budesonid som tillförs per spray därefter kan vara avsevärt mindre än den märkta dosen. Varje spray levererar 32 mcg budesonid till patienten.
RHINOCORT 100 mcg AQUA (budesonid) nässpray ska förvaras i kontrollerad rumstemperatur, 20 till 25°C (68 till 77°F) med ventilen uppåt. Frys inte. Skydda från ljus. Skaka försiktigt före användning. Spraya inte i ögonen.
Distribuerad av: AstraZeneca LP, Wilmington, DE 19850. Reviderad: 12/2010
BIEFFEKTER
Användning av systemiska och intranasala kortikosteroider kan resultera i följande:
- Näsblod, Candida albicans-infektion, perforering av nasal septum och försämrad sårläkning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Överkänslighet inklusive anafylaxi [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Immunsuppression [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Hyperkorticism och binjuresuppression [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
- Tillväxteffekt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
- Glaukom och grå starr [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Incidensen av vanliga biverkningar i tabell 1 baseras på två amerikansk- och fem icke-amerikanska kontrollerade kliniska prövningar på 1 526 patienter med säsongsbunden eller perenn rinit hos vuxna och barn ≥ 6 år som behandlats med RHINOCORT AQUA (budesonid) nässpray i doser upp till 400 mcg en gång dagligen i 3-6 veckor. Denna population inkluderade 745 kvinnor och 781 män med en medelålder på 31 år (intervallet 6-85 år, 349 var 6
En liknande biverkningsprofil observerades i undergruppen av pediatriska patienter i åldern 6 till 12 år. Dessa patienter ingår i tabell 1.
Två till tre procent (2-3%) av patienterna i kliniska prövningar avbröt behandlingen på grund av biverkningar. Systemiska kortikosteroidbiverkningar rapporterades inte under kontrollerade kliniska studier med RHINOCORT AQUA (budesonid) nässpray.
Om rekommenderade doser överskrids, eller om individer är särskilt känsliga, kan symtom på hyperkorticism, dvs. Gushings syndrom, och binjurebarksuppression uppstå.
Erfarenhet efter marknadsföring
Följande biverkningar har rapporterats under användning av RHINOCORT AQUA (budesonid) nässpray efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering.
Immunsystemets störningar: omedelbara och fördröjda överkänslighetsreaktioner (inklusive anafylaktisk reaktion, urtikaria, hudutslag, dermatit, angioödem och klåda), [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och KONTRAINDIKATIONER ]
Ögonbesvär: glaukom, ökat intraokulärt tryck, grå starr [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Andningsvägar, bröstkorg och mediastinum: perforering av nässkiljeväggen, anosmi, störningar i svalget (halsirritation, halssmärtor, svullen hals, brännande hals och kliande hals) och väsande andning
Hjärtsjukdomar: hjärtklappning
Muskuloskeletala och bindvävssjukdomar: tillväxthämning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ]
LÄKEMEDELSINTERAKTIONER
Hämmare av Cytokrom P450 3A4
Den huvudsakliga metabolismen av kortikosteroider, inklusive budesonid, är via cytokrom P450 (CYP) isoenzym 3A4 (CYP3A4). Efter oral administrering av ketokonazol, en stark hämmare av CYP3A4, ökade den genomsnittliga plasmakoncentrationen av oralt administrerad budesonid. Samtidig administrering av CYP3A4 kan hämma metabolismen av och öka den systemiska exponeringen för budesonid. Försiktighet bör iakttas när man överväger samtidig administrering av RHINOCORT AQUA (budesonid) nässpray med långtidsverkande ketokonazol och andra kända starka CYP3A4-hämmare (t.ex. ritonavir, atazanavir klaritromycin, indinavir itrakonazol, nefazodon nelfinavir-saquinavir, telithromycin) VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och KLINISK FARMAKOLOGI ].
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Lokala nasala effekter
Epistaxis
I kliniska studier av 3 till 52 veckors varaktighet observerades näsblod oftare hos patienter som behandlats med RHINOCORT 100 mikrogram AQUA (budesonid) nässpray än de som fick placebo [se NEGATIVA REAKTIONER ].
Candida infektion
kliniska studier med budesonid administrerat intranasalt har utveckling av lokaliserade infektioner i näsa och svalg med Candida albicans inträffat. När en sådan infektion utvecklas kan den kräva behandling med lämplig lokal eller systemisk terapi och avbrytande av behandlingen med RHINOCORT AQUA (budesonid) nässpray. Patienter som använder RHINOCORT AQUA (budesonid) nässpray under flera månader eller längre bör undersökas regelbundet för tecken på Candida-infektion eller andra tecken på negativa effekter på nässlemhinnan.
Nasal septal perforering
Fall av perforering av nasalt septum har rapporterats efter intranasal applicering av kortikosteroider, inklusive budesonid [se NEGATIVA REAKTIONER ].
Försämrad sårläkning
På grund av kortikosteroiders hämmande effekt på sårläkning bör patienter som nyligen har upplevt nässeptumsår, näskirurgi eller nästrauma inte använda en nasal kortikosteroid förrän läkning har skett.
Överkänslighetsreaktioner inklusive anafylaxi
Överkänslighetsreaktioner inklusive anafylaktisk reaktion, urtikaria, hudutslag, dermatit, angioödem och klåda kan förekomma [se KONTRAINDIKATIONER och BIVERKNINGAR, Erfarenhet efter marknadsföring ].
Immunsuppression
Patienter som tar läkemedel som dämpar immunförsvaret är mer mottagliga för infektioner än friska individer. Vattkoppor och mässling, till exempel, kan ha ett allvarligare eller till och med dödligt förlopp hos känsliga barn eller vuxna som använder kortikosteroider. Hos sådana barn eller vuxna som inte har haft dessa sjukdomar eller blivit ordentligt immuniserade bör särskild försiktighet iakttas för att undvika exponering. Hur dosen, vägen och varaktigheten av administrering av kortikosteroider påverkar risken för att utveckla en spridd infektion är inte känt. Bidraget från den underliggande sjukdomen och/eller tidigare kortikosteroidbehandling till risken är inte heller känt. Vid exponering för vattkoppor kan behandling med varicella zoster immunglobulin (VZIG) eller poolat intravenöst immunglobulin (WIG), beroende på vad som är lämpligt, vara indicerat. Vid exponering för mässling kan profylax med poolat intramuskulärt immunglobulin (IG) vara indicerat. (Ser respektive bipacksedel för fullständig VZIG- och IG-förskrivningsinformation ). Om vattkoppor utvecklas kan behandling med antivirala medel övervägas.
Det kliniska förloppet av vattkoppor eller mässlinginfektion hos patienter på intranasala eller inhalerade kortikosteroider har inte studerats. Även om det inte finns några data för intranasala kortikosteroider, har en klinisk studie undersökt immunsvaret mot varicellavaccinet hos astmapatienter i åldern 12 månader till 8 år som behandlats med budesonid-inhalationssuspension.
En öppen, icke-randomiserad klinisk studie undersökte immunsvaret mot varicellavaccin hos 243 astmapatienter i åldern 12 månader till 8 år som behandlades med budesonid-inhalationssuspension 0,25 mg till 1 mg dagligen (n=151) eller astmabehandling utan kortikosteroider (n=92) (dvs beta-agonister, leukotrienreceptorantagonister eller kromoner). Andelen patienter som utvecklade en seroprotektiv antikroppstiter ≥ 5,0 (gpELISA-värde) som svar på vaccinationen var liknande hos patienter som behandlades med budesonid-inhalationssuspension (85 %) jämfört med patienter som behandlades med astmabehandling utan kortikosteroider (90 %). Ingen patient som behandlats med budesonid-inhalationssuspension utvecklade vattkoppor som ett resultat av vaccination.
Kortikosteroider bör användas med försiktighet, om överhuvudtaget, till patienter med aktiv eller vilande tuberkulosinfektion, obehandlade svamp-, bakterie-, systemiska virus- eller parasitinfektioner; eller okulär herpes simplex.
Effekter på hypotalamus-hypofysen-binjureaxeln
Hyperkorticism och binjuresuppression: När intranasala steroider används i högre doser än rekommenderade eller hos känsliga individer vid rekommenderade doser, kan systemiska kortikosteroideffekter såsom hyperkorticism och binjuresuppression uppträda. Om sådana förändringar inträffar ska dosen av RHINOCORT 100 mcg AQUA (budesonid) nässpray avbrytas långsamt, i enlighet med accepterade rutiner för att avbryta oral kortikosteroidbehandling.
Ersättning av en systemisk kortikosteroid med en topikal kortikosteroid kan åtföljas av tecken på binjurebarksvikt, och dessutom kan vissa patienter uppleva symtom på kortikosteroidabstinens, t.ex. led- och/eller muskelvärk, trötthet, svaghet, illamående, kräkningar, hypotoni, trötthet och depression. Patienter som tidigare behandlats under långa perioder med systemiska kortikosteroider bör avvänjas långsamt när de överförs till topikala kortikosteroider och noggrant övervakas med avseende på akut binjurebarksvikt som svar på stress. Hos de patienter som har astma eller andra kliniska tillstånd som kräver långvarig systemisk kortikosteroidbehandling, kan en för snabb minskning av systemiska kortikosteroider orsaka en allvarlig förvärring av deras symtom.
Interaktioner med starka Cytokrom P450 3A4-hämmare
Försiktighet bör iakttas när man överväger samtidig administrering av RHINOCORT AQUA nässpray med ketokonazol och andra kända starka CYP3A4-hämmare (t.ex. ritonavir, atazanavir, klaritromycin, indinavir, itrakonazol, nefazodon, nelfinavir, saquinavir-effekt relaterad till telitromycin) systemisk exponering för budesonid kan förekomma [se Läkemedelsinteraktioner, KLINISK FARMAKOLOGI ].
Effekt på tillväxt
Intranasala kortikosteroider, inklusive budesonid, kan orsaka en minskning av tillväxthastigheten när de administreras till pediatriska patienter. Övervaka tillväxten rutinmässigt hos pediatriska patienter som får långtidsbehandling med RHINOCORT 100 mcg AQUA (budesonid) nässpray. För att minimera de systemiska effekterna av intranasala kortikosteroider, inklusive RHINOCORT AQUA (budesonid) nässpray, titrera varje patients dos till den lägsta som effektivt kontrollerar hans/hennes symtom [se Användning i specifika populationer, pediatrisk användning ].
Glaukom och grå starr
Glaukom, ökat intraokulärt tryck och grå starr har rapporterats efter intranasal applicering av kortikosteroider, inklusive budesonid. Därför är noggrann övervakning berättigad hos patienter med förändrad syn eller med en historia av ökat intraokulärt tryck, glaukom och/eller grå starr [se NEGATIVA REAKTIONER ].
Information om patientrådgivning
[Ser FDA-godkänd patientmärkning ]
Patienter som behandlas med RHINOCORT 100 mcg AQUA (budesonid) nässpray bör få följande information och instruktioner. Denna information är avsedd att hjälpa patienten med en säker och effektiv användning av läkemedlet. Det är inte ett avslöjande av alla möjliga negativa eller avsedda effekter. För korrekt användning av RHINOCORT 100 mcg AQUA (budesonid) nässpray och för att uppnå maximal förbättring, bör patienten läsa och följa den medföljande FDA-godkända patientmärkningen.
Lokala nasala effekter
Patienter bör informeras om att näsblod och lokaliserade infektioner med Candida albicans förekom i näsa och svalg hos vissa patienter. Om candidiasis utvecklas ska den behandlas med lämplig lokal eller systemisk terapi och avbryta behandlingen med RHINOCORT 100mcg AQUA (budesonid) nässpray. Dessutom är nasala kortikosteroider associerade med perforering av nässeptum och försämrad sårläkning. Patienter som nyligen har upplevt nässår, näskirurgi eller nästrauma ska inte använda RHINOCORT AQUA (budesonid) nässpray förrän läkning har skett [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Överkänslighet inklusive anafylaxi
Patienter bör informeras om att överkänslighetsreaktioner inklusive anafylaktisk reaktion, urtikaria, hudutslag, dermatit, angioödem och klåda har rapporterats vid användning av RHINOCORT AQUA (budesonid) nässpray. Avbryta
RHINOCORT AQUA (budesonid) Nässpray om sådana reaktioner inträffar [se KONTRAINDIKATIONER, VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och NEGATIVA REAKTIONER ].
Immunsuppression
Patienter som tar immunsuppressiva doser av kortikosteroider bör varnas för att undvika exponering för vattkoppor eller mässling och, om de exponeras, att utan dröjsmål rådfråga sin läkare. Patienter bör informeras om potentiell försämring av befintlig tuberkulos, svamp-, bakterie-, virus- eller parasitisk infektion eller okulär herpes simplex [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Minskad tillväxthastighet
Patienter bör informeras om att intranasala kortikosteroider, inklusive budesonid, kan orsaka en minskning av tillväxthastigheten när de administreras till pediatriska patienter. Läkare bör noga följa tillväxten hos barn och ungdomar som tar kortikosteroider oavsett väg [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Glaukom och grå starr
Patienter bör informeras om att långvarig användning av intranasala kortikosteroider, inklusive budesonid, kan öka risken för vissa ögonproblem (grå starr och glaukom). Patienter bör informera sin vårdgivare om en förändring i synen noteras när de använder RHINOCORT AQUA (budesonid) nässpray [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Använd dagligen
Patienter bör använda RHINOCORT 100 mcg AQUA (budesonid) nässpray med jämna mellanrum eftersom dess effektivitet beror på regelbunden användning. Patienter kan notera en förbättring av nasala symtom inom 10 timmar efter första användningen av RHINOCORT AQUA (budesonid) nässpray. Maximal nytta kanske inte uppnås förrän cirka 2 veckor efter påbörjad behandling [se DOSERING OCH ADMINISTRERING ].
Patienter bör ta medicinen enligt anvisningarna och bör inte överskrida den föreskrivna dosen. Patienten bör kontakta läkare om symtomen inte förbättras efter två veckor eller om tillståndet förvärras. Patienter som upplever återkommande episoder av näsblod (näsblod) eller obehag i nässkiljeväggen när de tar denna medicin bör kontakta sin läkare. För korrekt användning av RHINOCORT AQUA (budesonid) nässpray och för att uppnå maximal förbättring, bör patienten läsa och följa den medföljande patientinformationen noggrant. Använd inte RHINOCORT 100mcg AQUA (budesonid) nässpray efter att det märkta antalet sprayer har använts (inklusive priming) eller efter utgångsdatumet som anges på kartongen eller flaskans etikett.
Hur du använder RHINOCORT 100mcg AQUA (budesonid) nässpray
Patienter bör noggrant instrueras om användningen av denna läkemedelsprodukt för att säkerställa optimal dostillförsel [se PATIENTINFORMATION ].
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
en 104-veckors oral studie på Sprague-Dawley-råttor observerades en statistiskt signifikant ökning av incidensen av gliom hos hanråttor som fick en oral dos av budesonid 50 mikrogram/kg/dag (ungefär två gånger den maximala rekommenderade dagliga intranasala dosen i vuxna och barn på en mcg/m2-basis). Ingen tumörframkallande effekt sågs hos hanråttor vid orala doser upp till 25 mikrogram/kg (ungefär lika med den maximala rekommenderade dagliga intranasala dosen hos vuxna och barn på en mikrogram/m2-basis, och hos honråttor vid orala doser upp till 50 mikrogram/kg cirka två gånger den maximala rekommenderade dagliga intranasala dosen till vuxna och barn på mcg/m2-basis). I ytterligare två tvååriga studier på Fischer- och Sprague-Dawley-hanråttor orsakade budesonid inga gliom vid en oral dos på 50 mcg/kg (ungefär två gånger den maximala rekommenderade dagliga intranasala dosen till vuxna och barn på en mcg/m2-basis). Hos Sprague-Dawley-hanråttor orsakade dock budesonid en statistiskt signifikant ökning av förekomsten av hepatocellulära tumörer vid en oral dos på 50 mcg/kg (ungefär två gånger den maximala rekommenderade dagliga intranasala dosen till vuxna och barn på en mcg/m2-basis ). De samtidiga referenskortikosteroiderna (prednisolon och triamcinolonacetonid) i dessa två studier visade liknande fynd.
Det fanns inga tecken på cancerframkallande effekt när budesonid administrerades oralt i 91 veckor till möss i doser upp till 200 mikrogram/kg/dag (ungefär 3 gånger den maximala rekommenderade dagliga intranasala dosen till vuxna och barn på en mikrogram/m2-basis). .
Budesonid var inte mutagent eller klastogent i sex olika testsystem: Ames Salmonella/mikrosomplattest, mus-mikronkärntest, muslymfomtest, kromosomavvikelsetest i humana lymfocyter, könsbundet recessivt dödligt test i Drosophila melanogaster och DNA-reparationsanalys hos råtta hepatocytodling.
Hos råttor hade budesonid ingen effekt på fertiliteten vid subkutana doser upp till 80 mikrogram/kg (ungefär 3 gånger den maximala rekommenderade dagliga intranasala dosen hos vuxna på mcg/m2-basis).
Vid en subkutan dos på 20 mcg/kg/dag (mindre än den maximala rekommenderade dagliga intranasala dosen till vuxna på en mcg/m2-basis), minskar moderns viktökning, prenatal livsduglighet och livsduglighet hos ungar vid födseln och under amning observerades. Inga sådana effekter noterades vid 5 mcg/kg (mindre än den maximala rekommenderade dagliga intranasala dosen hos vuxna på mcg/m2-basis).
Användning i specifika populationer
Graviditet
Teratogena effekter: Graviditetskategori B. Effekten av budesonid på graviditetsresultat hos människa har utvärderats genom bedömningar av födelseregister kopplade till moderns användning av inhalerad budesonid (dvs. PULMICORT TURBUHALER) och intranasalt administrerad budesonid (dvs. RHINOCORT 100mcg AQUA) Nabudesonid. Resultaten från populationsbaserade prospektiva kohortepidemiologiska studier som granskar data från tre svenska register som täcker cirka 99 % av graviditeterna från 1995-2001 (dvs. Svenska medicinska födelseregistret; Register över medfödda missbildningar; Barnkardiologiska register) indikerar ingen ökad risk för totalt sett medfödda missbildningar från användning av inhalerad eller intranasal budesonid under tidig graviditet.
Medfödda missbildningar studerades hos 2 014 spädbarn födda av mödrar som rapporterade användning av inhalerad budesonid för astma i början av graviditeten (vanligtvis 10-12 veckor efter den sista menstruationen), den period då de flesta större organmissbildningar inträffar.1 Frekvensen av övergripande medfödda missbildningar var liknande jämfört med den allmänna befolkningen (3,8 % respektive 3,5 %). Antalet spädbarn födda med orofaciala klyftor och hjärtdefekter liknade det förväntade antalet i den allmänna befolkningen (4 barn mot 3,3 respektive 18 barn mot 17-18). I en uppföljningsstudie som bringade det totala antalet spädbarn till 2 534 skilde sig inte frekvensen av totala medfödda missbildningar bland spädbarn vars mödrar exponerades för inhalerad budesonid under tidig graviditet från frekvensen för alla nyfödda barn under samma period (3,6 % ).2 En tredje studie från Svenska medicinska födelseregistret av 2 968 graviditeter exponerade för inhalerad budesonid, varav majoriteten var exponeringar i första trimestern, rapporterad graviditetsålder, födelsevikt, födelselängd, dödfödslar och flerfödslar liknande för exponerade spädbarn jämfört med icke exponerade spädbarn.3
Medfödda missbildningar studerades hos 2 113 spädbarn födda av mödrar som rapporterade användning av intranasal budesonid under tidig graviditet. Frekvensen av totala medfödda missbildningar var liknande jämfört med den allmänna populationsfrekvensen (4,5 % respektive 3,5 %). Den justerade oddskvoten (OR) var 1,06 (95 % KI 0,86-1,31). Antalet spädbarn födda med orofaciala klyftor liknade det förväntade antalet i den allmänna befolkningen (3 barn respektive 3). Antalet spädbarn som föddes med hjärtfel översteg det förväntade i den allmänna befolkningen (28 barn mot 17,8 respektive). Den systemiska exponeringen från intranasal budesonid är 6 gånger mindre än från inhalerad budesonid och ett samband mellan hjärtdefekter sågs inte med högre exponeringar av budesonid.
Trots djurfynden verkar det som om risken för fosterskador är liten om läkemedlet används under graviditeten. Men eftersom studier på människor inte kan utesluta risken för skada, bör RHINOCORT AQUA (budesonid) nässpray endast användas under graviditet om det verkligen behövs.
Budesonid gav fosterförlust, minskade valpvikter och skelettavvikelser vid en subkutan dos hos kaniner som var cirka 2 gånger den maximala rekommenderade dagliga intranasala dosen hos vuxna på en mcg/m2-basis och vid en subkutan dos hos råttor som var cirka 16 gånger maximal rekommenderad daglig intranasal dos för vuxna på en mcg/m2-basis. Inga teratogena eller embryocidala effekter observerades hos råttor när budesonid administrerades genom inhalation i doser upp till cirka 8 gånger den maximala rekommenderade dagliga intranasala dosen till vuxna på en mcg/m2-basis.
Erfarenhet av orala kortikosteroider sedan de introducerades i farmakologiska doser, i motsats till fysiologiska doser, tyder på att gnagare är mer benägna att få teratogena effekter från kortikosteroider än människor.
Ickeeratogena effekter: Hypoadrenalism kan förekomma hos spädbarn födda av mödrar som får kortikosteroider under graviditeten. Sådana spädbarn bör observeras noggrant.
Ammande mödrar
Budesonid utsöndras i bröstmjölk. Data med budesonid som levereras via torrpulverinhalator indikerar att den totala dagliga orala dosen av budesonid som är tillgänglig i bröstmjölk till spädbarnet är cirka 0,3 % till 1 % av dosen som inhaleras av modern [se KLINISK FARMAKOLOGI, Farmakokinetik, Specialpopulationer, Omvårdnad ]. Inga studier har utförts på ammande kvinnor specifikt med RHINOCORT 100mcg AQUA nässpray; dock förväntas den dos av budesonid som är tillgänglig för spädbarnet i bröstmjölk, i procent av moderns dos, vara liknande. RHINOCORT AQUA (budesonid) nässpray ska endast användas till ammande kvinnor om det är kliniskt lämpligt. Förskrivare bör väga de kända fördelarna med amning för modern och spädbarnet mot de potentiella riskerna med minimal exponering för budesonid hos barnet. Doseringsöverväganden inkluderar recept eller titrering till den lägsta kliniskt effektiva dosen och användning av RHINOCORT 100mcg AQUA (budesonid) nässpray omedelbart efter amning för att maximera tidsintervallet mellan dosering och amning för att minimera spädbarns exponering.
Pediatrisk användning
Säkerhet och effektivitet hos pediatriska patienter under 6 år har inte fastställts.
Kontrollerade kliniska studier har visat att intranasala kortikosteroider kan orsaka en minskning av tillväxthastigheten hos pediatriska patienter. Denna effekt har observerats i avsaknad av laboratoriebevis för undertryckning av hypotalamus-hypofys-binjure (HPA)-axeln, vilket tyder på att tillväxthastigheten är en känsligare indikator på systemisk kortikosteroidexponering hos pediatriska patienter än några vanliga tester av HPA-axelns funktion. . De långsiktiga effekterna av denna minskning av tillväxthastigheten i samband med intranasala kortikosteroider, inklusive effekten på den slutliga vuxenlängden, är okända. Potentialen för tillväxt efter avslutad behandling med intranasala kortikosteroider har inte studerats tillräckligt.
Tillväxten hos pediatriska patienter som får intranasala kortikosteroider, inklusive RHINOCORT 100 mcg AQUA (budesonid) nässpray, bör övervakas rutinmässigt (t.ex. via stadiometri). De potentiella tillväxteffekterna av förlängd behandling bör vägas mot kliniska fördelar och riskerna och fördelarna med alternativa behandlingar. För att minimera de systemiska effekterna av intranasala kortikosteroider, inklusive RHINOCORT AQUA (budesonid) nässpray, bör varje patient titreras till den lägsta dosen som effektivt kontrollerar hans/hennes symtom.
En ettårig placebokontrollerad klinisk tillväxtstudie genomfördes på 229 pediatriska patienter (i åldern 4 till 8 år) för att bedöma effekten av RHINOCORT AQUA (budesonid) nässpray (engångsdos på 64 mikrogram, den rekommenderade startdosen för barn från 6 år och uppåt) på tillväxthastighet. Från en population på 141 patienter som fick RHINOCORT 100 mcg AQUA (budesonid) nässpray och 67 som fick placebo, var punktuppskattningen för tillväxthastighet med RHINOCORT AQUA (budesonid) nässpray 0,25 cm/år lägre än den som noterades med placebo (95 % konfidensintervall) allt från 0,59 cm/år lägre än placebo till 0,08 cm/år högre än placebo).
en studie av astmatiska barn i åldern 5-12 år hade de som behandlades med budesonid administrerat via en torrpulverinhalator 200 mikrogram två gånger dagligen (n=311) en minskning av tillväxten på 1,1 centimeter (0,433 tum) jämfört med de som fick placebo ( n=418) vid slutet av ett år; skillnaden mellan dessa två behandlingsgrupper ökade inte ytterligare under tre års ytterligare behandling. Vid slutet av fyra år hade barn som behandlats med budesonid-torrpulverinhalator och barn som behandlats med placebo liknande tillväxthastigheter. Slutsatserna från denna studie kan förvirras av den ojämlika användningen av kortikosteroider i behandlingsgrupperna och inkluderandet av data från patienter som uppnår puberteten under studiens gång.
De systemiska effekterna av inhalerade kortikosteroider är relaterade till den systemiska exponeringen för sådana läkemedel. Farmakokinetiska studier har visat att hos både vuxna och barn förväntas systemisk exponering för budesonid vid de högsta rekommenderade doserna av RHINOCORT AQUA (budesonid) nässpray inte vara större än exponeringen vid de lägsta rekommenderade doserna via en torrpulverinhalator. Därför förväntas de systemiska effekterna (HPA-axeln och tillväxt) av budesonid tillfört från RHINOCORT AQUA (budesonid) nässpray inte vara större än vad som rapporteras för inhalerad budesonid när det administreras via torrpulverinhalatorn.
Det kan inte uteslutas att RHINOCORT 100 mcg AQUA (budesonid) nässpray kan orsaka tillväxthämning hos känsliga patienter eller vid doser över 64 mcg dagligen. Det rekommenderade dosintervallet för patienter 6 till 11 år är 64 till 128 mikrogram per dag [se DOSERING OCH ADMINISTRERING ].
Geriatrisk användning
Av de 2 461 patienterna i kliniska studier av RHINOCORT 100 mcg AQUA (budesonid) nässpray var 5 % 60 år och äldre. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre försökspersoner, förutom en biverkningsfrekvens som rapporterade näsblod som ökade med åldern. Vidare har annan rapporterad klinisk erfarenhet inte identifierat några andra skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas.
Nedsatt leverfunktion
Formella farmakokinetiska studier med RHINOCORT 100 mcg AQUA (budesonid) nässpray har inte utförts på patienter med nedsatt leverfunktion. Men eftersom budesonid huvudsakligen elimineras av levermetabolism, kan försämrad leverfunktion leda till ackumulering av budesonid i plasma. Därför bör patienter med leversjukdom övervakas noggrant.
ÖVERDOS
Akut överdosering med denna beredningsform är osannolik eftersom en 120 sprayflaska RHINOCORT 100 mcg AQUA (budesonid) nässpray 32 mcg endast innehåller cirka 5,4 mg budesonid. Kronisk överdosering kan resultera i tecken/symtom på hyperkorticism [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
KONTRAINDIKATIONER
RHINOCORT AQUA (budesonid) nässpray är kontraindicerat för patienter med överkänslighet mot något av dess ingredienser [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Budesonid är en antiinflammatorisk kortikosteroid som uppvisar potent glukokortikoidaktivitet och svag mineralokortikoidaktivitet. I standard in vitro- och djurmodeller har budesonid ungefär 200 gånger högre affinitet för glukokortikoidreceptorn och en 1000 gånger högre topikal antiinflammatorisk potens än kortisol (råttkrotonolja öronödemanalys). Som ett mått på systemisk aktivitet är budesonid 40 gånger mer potent än kortisol när det administreras subkutant och 25 gånger mer potent när det administreras oralt i råtttymusinvolutionsanalysen. Den kliniska betydelsen av detta är okänd.
Aktiviteten hos RHINOCORT 100mcg AQUA nässpray beror på moderläkemedlet budesonid. I glukokortikoidreceptoraffinitetsstudier var 22R-formen två gånger så aktiv som 22S-epimeren. In vitro-studier visade att de två formerna av budesonid inte omvandlas till varandra.
Den exakta mekanismen för kortikosteroidverkan på inflammation vid säsongsbunden och perenn allergisk rinit är inte välkänd. Inflammation är en viktig komponent i patogenesen av säsongsbunden och perenn allergisk rinit. Kortikosteroider har ett brett utbud av hämmande aktiviteter mot flera celltyper (t.ex. mastceller, eosinofiler, neutrofiler, makrofager och lymfocyter) och mediatorer (t.ex. histamin, eikosanoider, leukotriener och cytokiner) involverade i allergiska och icke-allergiska medierade inflammation. Dessa antiinflammatoriska effekter av kortikosteroider kan bidra till deras effektivitet vid säsongsbunden och perenn allergisk rinit.
Farmakodynamik
En 3-veckors klinisk studie i säsongsbunden rinit, som jämförde RHINOCORT 100 mcg näsinhalator, oralt intagen budesonid och placebo hos 98 patienter med allergisk rinit på grund av björkpollen, visade att den terapeutiska effekten av RHINOCORT näsinhalator kan hänföras till topikala effekter budesonid.

HPA-axeleffekter
Effekterna av RHINOCORT 100mcg AQUA (budesonid) nässpray på binjurefunktionen har utvärderats i flera kliniska prövningar. I en fyra veckor lång klinisk prövning visade 61 vuxna patienter som fick 256 mikrogram dagligen RHINOCORT AQUA (budesonid) nässpray inga signifikanta skillnader från patienter som fick placebo i plasmakortisolnivåer uppmätt före och 60 minuter efter 0,25 mg intramuskulärt cosyntropin. Det fanns inga konsekventa skillnader i 24-timmars kortisolmätningar i urin hos patienter som fick upp till 400 mikrogram dagligen. Liknande resultat sågs i en studie av 150 barn och ungdomar i åldern 6 till 17 med perenn rinit som behandlades med 256 mikrogram dagligen i upp till 12 månader.
Efter behandling med den rekommenderade maximala dagliga dosen av RHINOCORT AQUA (budesonid) nässpray (256 mcg) i sju dagar, var det en liten, men statistiskt signifikant minskning av området under plasmakortisol-tidkurvan under 24 timmar (AUC0-24h) ) hos friska vuxna frivilliga.
En dosrelaterad suppression av 24-timmars kortisolutsöndring i urin observerades efter administrering av RHINOCORT AQUA (budesonid) nässpraydoser från 100-800 mikrogram dagligen i upp till fyra dagar hos 78 friska vuxna frivilliga. Den kliniska relevansen av dessa resultat är okänd.
Farmakokinetik
Absorption
Efter intranasal administrering av en engångsdos av RHINOCORT AQUA (budesonid) nässpray (128 mcg), inträffar den genomsnittliga maximala plasmakoncentrationen på cirka 0,3 nmol/L cirka 0,5 timmar efter dosering. Jämfört med en intravenös dos når cirka 34 % av den tillförda intranasala dosen den systemiska cirkulationen, varav det mesta absorberas genom nässlemhinnan. Medan budesonid absorberas väl från mag-tarmkanalen, är den orala biotillgängligheten av budesonid låg (~10%), främst på grund av omfattande första passage-metabolism i levern.
Distribution
Distributionsvolymen för budesonid var cirka 2-3 l/kg. Det var 85-90 % bundet till plasmaproteiner. Distributionsvolymen för 22R-epimeren är nästan dubbelt så stor som för 22S-epimeren. Proteinbindningen var konstant över ett koncentrationsområde (1-100 nmol/L) som uppnåddes med, och översteg, rekommenderade doser av RHINOCORT 100 mcg AQUA nässpray. Budesonid visade liten eller ingen bindning till kortikosteroidbindande globulin. Budesonid kom snabbt i jämvikt med röda blodkroppar på ett koncentrationsoberoende sätt med ett blod/plasmaförhållande på cirka 0,8.
Ämnesomsättning
In vitro-studier med humana leverhomogenat har visat att budesonid metaboliseras snabbt och omfattande. Två huvudmetaboliter bildade via cytokrom P450 (CYP) isoenzym 3A4 (CYP3A4)-katalyserad biotransformation har isolerats och identifierats som 16a-hydroxiprednisolon och 6p-hydroxibudesonid. Kortikosteroidaktiviteten för var och en av dessa två metaboliter är mindre än 1 % av moderföreningens. Ingen kvalitativ skillnad mellan in vitro och in vivo metaboliska mönster har upptäckts. Försumbar metabolisk inaktivering observerades i humana lung- och serumberedningar.
Utsöndring/Eliminering
22R-formen av budesonid eliminerades företrädesvis av levern med systemisk clearance på 1,4 l/min mot 1,0 l/min för 22S-formen. Den terminala halveringstiden, 2 till 3 timmar, var densamma för båda epimererna och var oberoende av dos. Budesonid utsöndrades i urin och avföring i form av metaboliter. Ungefär 2/3 av en intranasal radiomärkt dos återfanns i urinen och resten i avföringen. Ingen oförändrad budesonid upptäcktes i urinen.
Specifika populationer
Geriatrisk
Farmakokinetiken för RHINOCORT 100 mcg AQUA (budesonid) nässpray hos geriatriska patienter har inte studerats specifikt.
Pediatrisk
Efter administrering av RHINOCORT 100 mcg AQUA (budesonid) nässpray var tiden för att nå maximala läkemedelskoncentrationer och plasmahalveringstid liknande hos barn och vuxna. Barn hade plasmakoncentrationer ungefär två gånger de som observerades hos vuxna, främst på grund av skillnader i vikt mellan barn och vuxna.
Kön
Ingen specifik farmakokinetisk studie har utförts för att utvärdera effekten av kön på budesonids farmakokinetik. Efter administrering av 400 mcg RHINOCORT 100 mcg AQUA (budesonid) nässpray till 7 manliga och 8 kvinnliga frivilliga i en farmakokinetisk studie fann man dock inga större könsskillnader i de farmakokinetiska parametrarna.
Lopp
Ingen specifik studie har genomförts för att utvärdera effekten av ras på budesonids farmakokinetik.
Ammande mödrar
Fördelningen av budesonid vid oral inhalation från en torrpulverinhalator i doser på 200 eller 400 mikrogram två gånger dagligen under minst 3 månader studerades hos åtta ammande kvinnor med astma från 1 till 6 månader efter förlossningen. Systemisk exponering för budesonid hos dessa kvinnor verkar vara jämförbar med den hos icke-ammande kvinnor med astma från andra studier. Bröstmjölk erhållen under åtta timmar efter dosering visade att den maximala koncentrationen av budesonid för doserna på 400 och 800 mikrogram var 0,39 respektive 0,78 nmol/L och inträffade inom 45 minuter efter dosering. Den uppskattade orala dagliga dosen budesonid från bröstmjölk till spädbarnet var cirka 0,007 och 0,014 mikrogram/kg/dag för de två dosregimer som användes i denna studie, vilket motsvarar cirka 0,3 % till 1 % av dosen som inhalerats av modern. Budesonidnivåer i plasmaprover som erhållits från fem spädbarn cirka 90 minuter efter amning (och cirka 140 minuter efter läkemedelsadministrering till modern) var under kvantifierbara nivåer ( Användning i specifika populationer, ammande mödrar ].
Nedsatt njur- eller leverfunktion
Farmakokinetiken för budesonid har inte undersökts hos patienter med nedsatt njurfunktion. Nedsatt leverfunktion kan påverka elimineringen av kortikosteroider. Budesonids farmakokinetik påverkades av nedsatt leverfunktion, vilket framgår av en fördubblad systemisk tillgänglighet efter oralt intag. Relevansen av detta fynd för intranasalt administrerad budesonid har inte fastställts.
Läkemedelsinteraktioner
Hämmare av cytokrom P450-enzymer
Ketokonazol: Ketokonazol, en stark hämmare av cytokrom P450 (CYP) isoenzym 3A4 (CYP3A4), det huvudsakliga metaboliska enzymet för kortikosteroider, ökade plasmanivåer av oralt intaget budesonid [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och LÄKEMEDELSINTERAKTIONER ].
Cimetidin: Vid rekommenderade doser hade cimetidin, en ospecifik hämmare av CYP-enzymer, en liten men kliniskt obetydlig effekt på farmakokinetiken för oral budesonid.
Djurtoxikologi och/eller farmakologi
Budesonid var teratogen och embryocidal hos kaniner och råttor. Budesonid gav fosterförlust, minskade valpvikter och skelettavvikelser vid en subkutan dos på 25 mcg/kg hos kaniner (ungefär 2 gånger den maximala rekommenderade dagliga intranasala dosen hos vuxna på en mcg/m2-basis) och vid en subkutan dos på 500 mcg /kg hos råttor (ungefär 16 gånger den maximala rekommenderade dagliga intranasala dosen hos vuxna på en mcg/m2-basis). Inga teratogena eller embryocidala effekter observerades hos råttor när budesonid administrerades i inhalationsdoser upp till 250 mikrogram/kg (ungefär 8 gånger den maximala rekommenderade dagliga intranasala dosen till vuxna på en mikrogram/m2-basis).
Kliniska studier
Den terapeutiska effekten av RHINOCORT AQUA (budesonid) nässpray har utvärderats i placebokontrollerade kliniska prövningar av säsongsbetonad och perenn allergisk rinit med 3-6 veckors varaktighet.
Antalet patienter som behandlades med budesonid i dessa studier var 90 män och 51 kvinnor i åldern 6-12 år och 691 män och 694 kvinnor 12 år och äldre. Patienterna var övervägande kaukasiska.
Sammantaget visade resultaten av dessa kliniska prövningar att RHINOCORT AQUA (budesonid) nässpray administrerad en gång dagligen ger statistiskt signifikant minskning av svårighetsgraden av nässymtom på säsongsbunden och perenn allergisk rinit inklusive rinnande näsa, nysningar och nästäppa.
En förbättring av nasala symtom kan noteras hos patienter inom 10 timmar efter första användningen av RHINOCORT 100 mcg AQUA (budesonid) nässpray. Denna tid till debut stöds av en miljöexponeringsenhetsstudie på patienter med säsongsbunden allergisk rinit som visade att RHINOCORT 100 mcg AQUA (budesonid) nässpray ledde till en statistiskt signifikant förbättring av nässymtom jämfört med placebo med 10 timmar. Ytterligare stöd kommer från en klinisk studie av patienter med perenn allergisk rinit som visade en statistiskt signifikant förbättring av nasala symtom för både RHINOCORT AQUA (budesonid) nässpray och för den aktiva komparatorn (mometasonfuroat) jämfört med placebo med 8 timmar. Debut bedömdes också i denna studie med maximal nasal inspiratorisk flödeshastighet och detta effektmått visade inte effekt för någondera aktiv behandling. Även om statistiskt signifikanta förbättringar av nasala symtom jämfört med placebo noterades inom 8-10 timmar i dessa studier, inträffar ungefär hälften till två tredjedelar av den slutliga kliniska förbättringen med RHINOCORT 100 mcg AQUA (budesonid) nässpray under de första 1-2 dagarna, och maximal nytta kanske inte uppnås förrän cirka 2 veckor efter påbörjad behandling.
REFERENSER
Kallen B, Rydhstroem H, Aberg A. Medfödda missbildningar efter användning av inhalerad budesonid i tidig graviditet. Obstet Gynecol 1999; 93:392-395.
2 Ericson A, Kallen B. Användning av läkemedel under graviditet: unik svensk registreringsmetod som kan förbättras. Läkemedelsverket 1999; 1:8-11.
3 Norjavaara E, Gerhardsson de Verdier M. Normala graviditetsutfall i en populationsbaserad studie inklusive 2968 gravida kvinnor exponerade för budesonid. J Allergy Clin Immunol 2003;! 11:736-742.
PATIENTINFORMATION
RHINOCORT 100mcg AQUA (budesonid) ® (RINE-o-cort AH-kwa) (budesonid) Nässpray
Endast för användning i näsan
Läs patientinformationen som medföljer RHINOCORT 100mcg AQUA (budesonid) nässpray innan du börjar använda den och varje gång du får en påfyllning. Det kan komma ny information. Denna information ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling. Om du har frågor om RHINOCORT AQUA (budesonid) nässpray, fråga din läkare eller apotekspersonal.
Vad är RHINOCORT 100mcg AQUA (budesonid) nässpray?
RHINOCORT AQUA (budesonid) Nässpray är ett receptbelagt läkemedel som används för att behandla säsongsbetonade och året runt allergisymptom hos vuxna och barn från 6 år och äldre.
RHINOCORT AQUA Nässpray innehåller budesonid, som är en konstgjord (syntetisk) kortikosteroid. Intranasala kortikosteroider är naturliga hormoner som finns i kroppen som minskar svullnad av nässlemhinnan. När du sprayar RHINOCORT 100mcg AQUA (budesonid) nässpray i näsan, hjälper det till att minska nässymtomen på allergisk rinit (inflammation i nässlemhinnan), såsom täppt näsa, rinnande näsa, klåda och nysningar.
Säkerheten och effektiviteten av RHINOCORT 100mcg AQUA (budesonid) nässpray har inte visats hos barn under 6 år.
Vem bör inte använda RHINOCORT AQUA (budesonid) nässpray?
Använd inte RHINOCORT 100mcg AQUA (budesonid) nässpray:
- om du är allergisk mot budesonid eller något av innehållsämnena i RHINOCORT AQUA nässpray. Se slutet av denna bipacksedel för en fullständig lista över ingredienserna i RHINOCORT AQUA (budesonid) nässpray.
Vad ska jag berätta för min vårdgivare innan jag använder RHINOCORT 100mcg AQUA (budesonid) nässpray?
Innan du använder RHINOCORT AQUA (budesonid) nässpray, berätta för din läkare eller apotekspersonal om du:
- har nyligen varit runt någon med vattkoppor eller mässling
- har leverproblem
- har obehandlade infektioner
- någonsin har haft en infektion som kallas tuberkulos
- har en ögoninfektion
- nyligen har opererats eller en nässkada
- har andra medicinska tillstånd
- är gravid eller planerar att bli gravid. Det är inte känt om RHINOCORT 100mcg AQUA (budesonid) nässpray kommer att skada ditt ofödda barn. Tala med din läkare om du är gravid eller planerar att bli gravid.
- ammar eller planerar att amma. RHINOCORT 100mcg AQUA (budesonid) nässpray kan passera över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar RHINOCORT AQUA (budesonid) nässpray.
Berätta för din vårdgivare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott.
RHINOCORT AQUA (budesonid) Nässpray kan påverka hur andra läkemedel fungerar, och andra läkemedel kan påverka hur RHINOCORT 100 mcg AQUA (budesonid) nässpray fungerar.
Vet vilka mediciner du tar. Ha en lista över dina läkemedel med dig för att visa din vårdgivare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag använda RHINOCORT 100mcg AQUA (budesonid) nässpray?
- RHINOCORT 100mcg AQUA (budesonid) nässpray är endast för användning i näsan. Spraya det inte i dina ögon eller mun.
- Använd RHINOCORT AQUA (budesonid) nässpray precis som din läkare säger åt dig att använda den.
- Det är mycket viktigt att du använder RHINOCORT AQUA (budesonid) nässpray regelbundet. Sluta inte använda RHINOCORT AQUA (budesonid) nässpray eller ändra din dos utan att prata med din läkare, även om du mår bättre.
- Tala med din vårdgivare om dina symtom inte förbättras efter att du tagit RHINOCORT AQUA (budesonid) nässpray i 2 veckor eller om dina symtom blir värre.
- En vuxen bör hjälpa ett litet barn att använda detta läkemedel.
- Se patientens bruksanvisning i slutet av denna bipacksedel för fullständig information om hur du använder RHINOCORT AQUA (budesonid) nässpray.
Vilka är de möjliga biverkningarna av RHINOCORT AQUA (budesonid) nässpray?
RHINOCORT 100mcg AQUA (budesonid) nässpray kan orsaka allvarliga biverkningar inklusive:
- hål i brosket inuti näsan (nässeptumperforering). Berätta för din vårdgivare om du får ett visslande ljud från näsan när du andas.
- långsam sårläkning. Du ska inte använda RHINOCORT 100mcg AQUA (budesonid) nässpray förrän din näsa har läkt om du har ett sår i näsan, om du har opererat näsan eller om din näsa har skadats.
- svampinfektion i näsan.
- allergiska reaktioner. Berätta för din vårdgivare eller få medicinsk hjälp omedelbart om du har:
- hudutslag, rodnad eller svullnad
- kraftig klåda
- svullnad i ansikte, mun och tunga
- immunsystemproblem som kan öka risken för infektioner. Du är mer benägen att få infektioner om du tar mediciner som försvagar din kropps förmåga att bekämpa infektioner. Undvik kontakt med personer som har smittsamma sjukdomar som vattkoppor eller mässling när de använder RHINOCORT AQUA (budesonid) nässpray. Symtom på infektion kan vara feber, smärta, värk, frossa, trötthetskänsla, illamående och kräkningar.
- binjurebarksvikt, Binjureinsufficiens är ett tillstånd där binjurarna inte producerar tillräckligt med steroidhormoner. Symtom på binjurebarksvikt kan inkludera trötthet, svaghet, illamående, kräkningar och lågt blodtryck.
- bromsad eller försenad tillväxt hos barn. Ett barns tillväxt bör kontrolleras regelbundet när du använder RHINOCORT 100mcg AQUA (budesonid) nässpray.
- ögonproblem, såsom glaukom och grå starr. Berätta för din vårdgivare om du har en förändring i synen eller har en historia av ökat intraokulärt tryck, glaukom och/eller grå starr.
Ring din vårdgivare eller få medicinsk hjälp omedelbart om du har symtom på någon av de allvarliga biverkningarna som anges ovan.
De vanligaste biverkningarna av RHINOCORT 100mcg AQUA (budesonid) nässpray inkluderar:
- näsblod
- öm hals
- andningssvårigheter som väsande andning eller hopdragning av bröstet
- hosta
- irritation i näsan
Berätta för din vårdgivare om du har någon biverkning som stör dig eller inte försvinner.
Dessa är inte alla möjliga biverkningar av RHINOCORT 100mcg AQUA (budesonid) nässpray. För mer information, fråga din vårdgivare eller apotekspersonal.
Ring din vårdgivare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
Du kan rapportera biverkningar till AstraZeneca på 1-800-236-9933.
Vad ska jag veta om allergisk rinit?
"Rhinit" betyder inflammation i nässlemhinnan. Det kallas ibland "hösnuva". Allergisk rinit kan orsakas av allergier mot pollen, djurmjäll, husdammskvalster och mögelsporer. Om du har allergisk rinit blir din näsa täppt, rinnande och kliar. Du kan också nysa mycket. Du kan ha röda, kliande, rinnande ögon; kliande hals; eller blockerade, kliande öron.
RHINOCORT AQUA (budesonid) Nässpray hjälper till att lindra dina nasala symtom.
Om du också har kliande, rinnande ögon bör du berätta för din läkare. Han eller hon kan ordinera ytterligare medicin för att behandla dessa symtom.
Hur ska jag förvara RHINOCORT AQUA (budesonid) nässpray?
- Förvara RHINOCORT AQUA (budesonid) nässpray vid 68°F till 77°F (20°C till 25°C).
- Frys inte RHINOCORT AQUA (budesonid) nässpray.
- Skydda RHINOCORT 100mcg AQUA (budesonid) nässpray från ljus.
- Använd inte RHINOCORT 100mcg AQUA (budesonid) nässpray efter att det märkta antalet sprayer har använts (inklusive priming) eller efter utgångsdatumet som anges på kartongen eller flaskans etikett.
- Behåll det gröna skyddslocket på RHINOCORT AQUA (budesonid) nässpray när den inte används. (Snälla se Före användning på baksidan ).
- Förvara RHINOCORT 100mcg AQUA (budesonid) nässpray och alla mediciner utom räckhåll för barn.
Allmän information om säker och effektiv användning av RHINOCORT AQUA (budesonid) nässpray:
Använd inte RHINOCORT 100mcg AQUA (budesonid) nässpray för ett tillstånd som det inte har ordinerats för. Ge inte RHINOCORT AQUA (budesonid) nässpray till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Denna patientinformationsbroschyr sammanfattar den viktigaste informationen om RHINOCORT 100mcg AQUA (budesonid) nässpray. Om du vill ha mer information, prata med din vårdgivare. Du kan fråga din apotekspersonal eller vårdgivare om information om RHINOCORT 100mcg AQUA (budesonid) nässpray som är skriven för vårdpersonal.
För mer information, gå till www.astrazeneca-us.com eller ring AstraZeneca på 1-800-236-9933.
Vilka är ingredienserna i RHINOCORT AQUA (budesonid) nässpray?
Aktiv beståndsdel: budesonid
Inaktiva Ingredienser: Mikrokristallin cellulosa och karboximetylcellulosa natrium, vattenfri dextros, polysorbat 80, dinatriumedetat, kaliumsorbat och renat vatten och saltsyra.
Bruksanvisning för patienten
Endast för användning i näsan. Spraya inte i ögonen eller munnen.
Läs patientens bruksanvisning noggrant innan du börjar använda RHINOCORT 100 mcg AQUA (budesonid) nässpray. Om du har några frågor, fråga din vårdgivare
Bild A 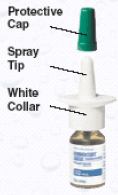
Hur du förbereder din RHINOCORT AQUA (budesonid) nässpray
Innan du använder RHINOCORT AQUA (budesonid) nässpray måste flaskan förberedas. För att förbereda RHINOCORT 100 mcg AQUA (budesonid) nässpray:
1. Dra för att ta bort det gröna skyddslocket från nässprayenheten.
2. Skaka flaskan försiktigt i några sekunder före varje användning.
3. Håll flaskan stadigt, som visas i figur B, med pek- och långfingret på vardera sidan av sprayspetsen och tummen under flaskan.
Bild B 
4. Aktivera pumpen genom att snabbt och bestämt trycka ner den vita kragen samtidigt som du håller i botten på flaskan med tummen.
5. Skaka flaskan försiktigt innan du använder RHINOCORT AQUA (budesonid) nässpray. Pumpen måste grundas genom att trycka ner den vita kragen 8 gånger. Pumpen är nu redo att användas. Om pumpen används dagligen behöver den inte fyllas på igen. Om den inte har använts under 2 dagar i rad, fyll på med 1 spray eller tills en fin spray visas. Om den inte har använts på mer än 14 dagar, skölj sprutspetsen på pumpen med hjälp av rengöringsstegen som anges i slutet av denna broschyr. Efter rengöring grundas om med 2 sprayer eller tills en fin spray uppstår.
Varje flaska RHINOCORT AQUA (budesonid) nässpray innehåller tillräckligt med medicin för att du ska kunna spraya medicin från flaskan 120 gånger efter att flaskan är förberedd.
Du bör inte använda flaskan med RHINOCORT 100mcg AQUA (budesonid) nässpray efter 120 sprayer. Ytterligare sprayer efter 120 kanske inte innehåller rätt mängd läkemedel. Du bör hålla reda på antalet sprayer du använder från varje flaska RHINOCORT 100mcg AQUA Nässpray och slänga eventuellt kvarvarande läkemedel som kan finnas kvar i flaskan. Fyll på ditt recept varje månad.
Hur du använder din RHINOCORT 100mcg AQUA (budesonid) nässpray
Följ dessa instruktioner för daglig användning av RHINOCORT AQUA (budesonid) nässpray:
Bild C 
4. Sätt in sprayspetsen i näsborren (spetsen ska inte nå långt in i näsan). Stäng den andra näsborren med ett finger och luta huvudet något framåt så att sprayen riktar sig mot näsans baksida (se Bild D ).
Bild D 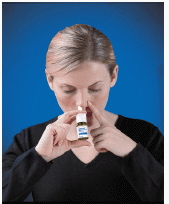
5. För varje spray, aktivera pumpen genom att snabbt och bestämt trycka ner den vita kragen samtidigt som du håller i botten på flaskan med tummen. Andas försiktigt inåt genom näsborren.
6. Efter att ha sprayat in i näsborren, luta huvudet bakåt i några sekunder (se Bild E ).
Bild E 
7. Om en andra spray behövs i samma näsborre, upprepa steg 3 till 6.
8. Upprepa steg 3 till 7 för din andra näsborre.
9. Undvik att blåsa näsan i 15 minuter efter att du använt RHINOCORT 100mcg AQUA (budesonid) nässpray.
10. Torka av sprayspetsen med en ren vävnad (se Bild F ), och sätt tillbaka det gröna skyddslocket. Förvara flaskan i upprätt läge.
Bild F 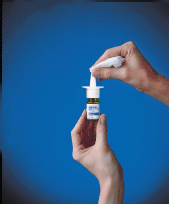
Hur du rengör din RHINOCORT 100mcg AQUA (budesonid) nässpray
Bild G 
Skölj det gröna skyddslocket och sprutmunstycket regelbundet. Att göra detta:
För ytterligare information om RHINOCORT 100mcg AQUA (budesonid) ® nässpray, vänligen ring AstraZenecas informationscenter, måndag till fredag kl. 08.00-18.00 ET, exklusive helgdagar kl. 1-800-236-9933.
