Aristocort 4mg Triamcinolone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Aristocort och hur används det?
Aristocort 4mg är ett receptbelagt läkemedel som används för att behandla symptom på allergiska sjukdomar, artrit, blodsjukdomar, . Aristocort 4mg kan användas ensamt eller tillsammans med andra läkemedel.
Aristocort tillhör en klass av läkemedel som kallas kortikosteroid; Glukokortikoid.
Det är inte känt om Aristocort 4mg är säkert och effektivt för barn yngre än 1 år.
Vilka är de möjliga biverkningarna av Aristocort?
Aristocort kan orsaka allvarliga biverkningar inklusive:
- nässelfeber,
- svårt att andas,
- svullnad av ansikte, läppar, tunga eller svalg,
- försämring av ditt hudtillstånd,
- rodnad, värme, svullnad, sipprar eller allvarlig irritation av behandlad hud,
- suddig syn,
- tunnelseende,
- ögonsmärta,
- ser glorier runt ljus,
- ökad törst,
- ökad urinering,
- torr mun,
- fruktig andedräkt lukt,
- viktökning (särskilt i ansiktet eller övre delen av ryggen och bålen),
- långsam sårläkning,
- tunn eller missfärgad hud,
- ökat kroppsbehåring,
- muskelsvaghet,
- illamående,
- diarre,
- trötthet,
- humörförändringar,
- menstruationsförändringar, och
- sexuella förändringar
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Aristocort inkluderar:
- sveda, klåda, torrhet eller annan irritation av behandlad hud,
- rodnad eller skorpa runt hårsäckarna,
- rodnad eller klåda runt munnen,
- allergisk hudreaktion,
- bristningar,
- acne,
- ökad kroppshårväxt,
- tunn hud eller missfärgning, och
- vitt eller "beskärat" utseende på huden (orsakat av täckning behandlad med ett tätt bandage eller annat täckande)
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Aristocort. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
EJ FÖR ANVÄNDNING HOS NYBAR
INTE FÖR INTRAVENÖS ANVÄNDNING
INNEHÅLLER BENSYLALKOHOL
BESKRIVNING
Aristocort® Forte är en steril suspension av 40 mg/ml triamcinolondiacetat (mikroniserat) suspenderad i en vehikel bestående av:
Saltsyra och/eller natriumhydroxid kan användas under tillverkningen för att justera suspensionens pH till cirka 6.
Triamcinolondiacetat är praktiskt taget olösligt i vatten; löslig i kloroform; svårlöslig i alkohol och i metanol; och lätt löslig i eter. Denna beredning är lämplig för parenteral administrering genom en 23-gauge nål (eller större), men INTE lämplig för intravenös användning. Det kan administreras intramuskulärt, intraartikulärt eller intrasynovialt, beroende på situationen.
Oåterkallelig klumpning uppstår när denna produkt är frusen.
Kemiskt är triamcinolondiacetat 9-fluoro-11ß,16',17,21-tetrahydroxipregna-1,4-dien-3,20-dion 16,21-diacetat.
Molekylvikten är 478,51. Dess strukturformel är:
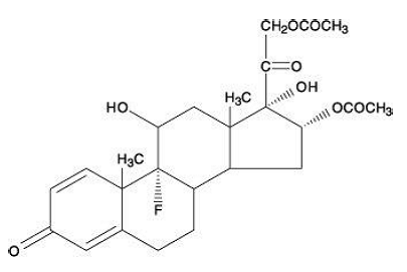
Triamcinolondiacetat förekommer som ett vitt till benvitt, mikrokristallint pulver.
INDIKATIONER
Där oral behandling inte är möjlig, är Aristocort® Forte (triamcinolondiacetat injicerbar suspension), 40 mg/ml, indicerat för intramuskulär användning enligt följande:
Allergiska tillstånd
Kontroll av svåra eller invalidiserande allergiska tillstånd som är svårbehandlade med adekvata försök med konventionell behandling av astma, atopisk dermatit, kontaktdermatit, läkemedelsöverkänslighetsreaktioner, perenn eller säsongsbunden allergisk rinit, serumsjuka, transfusionsreaktioner.
Dermatologiska sjukdomar
Bullös dermatitis herpetiformis, exfoliativ erythrodermi, mycosis fungoides, pemphigus, svår erythema multiforme (Stevens-Johnsons syndrom).
Endokrina störningar
Primär eller sekundär binjurebarkinsufficiens (hydrokortison eller kortison är det valda läkemedlet; syntetiska analoger kan användas tillsammans med mineralokortikoider där så är tillämpligt; i spädbarnsåldern är mineralokortikoidtillskott av särskild vikt), medfödd binjurehyperplasi, hyperkalcemi associerad med cancer, nonsuppurativ tyreoidit.
Gastrointestinala sjukdomar
För att övervaka patienten under en kritisk period av sjukdomen vid regional enterit och ulcerös kolit.
Hematologiska störningar
Förvärvad (autoimmun) hemolytisk anemi, Diamond-Blackfan-anemi, aplasi av ren röda blodkroppar, utvalda fall av sekundär trombocytopeni.
Diverse
Trikinos med neurologisk eller myokardiell inblandning, tuberkulös meningit med subaraknoidal blockering eller överhängande blockering när det används med lämplig antituberkulös kemoterapi.
Neoplastiska sjukdomar
För palliativ behandling av leukemier och lymfom.
Nervsystem
Akuta exacerbationer av multipel skleros; cerebralt ödem i samband med primär eller metastaserande hjärntumör, eller kraniotomi.
Oftalmiska sjukdomar
Sympatisk oftalmi, uveit och okulära inflammatoriska tillstånd som inte svarar på topikala kortikosteroider.
Njursjukdomar
För att inducera diures eller remission av proteinuri vid idiopatisk nefrotiskt syndrom eller det som beror på lupus erythematosus.
Andningssjukdomar
Beryllios, fulminerande eller spridd lungtuberkulos när den används samtidigt med lämplig antituberkulös kemoterapi, idiopatiska eosinofila lunginflammationer, symptomatisk sarkoidos.
Reumatiska sjukdomar
Som tilläggsterapi för kortvarig administrering (för att få patienten över en akut episod eller exacerbation) vid akut giktartrit; akut reumatisk kardit; ankyloserande spondylit; psoriasisartrit; reumatoid artrit, inklusive juvenil reumatoid artrit (utvalda fall kan kräva underhållsbehandling med låga doser). För behandling av dermatomyosit, polymyosit och systemisk lupus erythematosus.
För intraartikulär eller mjukvävnadsadministration
Intraartikulär eller mjukvävnadsadministrering av Aristocort® Forte är indicerat som tilläggsterapi för korttidsadministrering (för att få patienten över en akut episod eller exacerbation) vid akut giktartrit, akut och subakut bursit, akut ospecifik tenosynovit, epikondylit, reumatoid artrit, synovit av artros.
För intralesional administration
Intralesional administrering av Aristocort® Forte är indicerat för alopecia areata; discoid lupus erythematosus; keloider; lokaliserade hypertrofiska, infiltrerade, inflammatoriska lesioner av granuloma annulare, lichen planus, lichen simplex chronicus (neurodermatit) och psoriatiska plack; necrobiosis lipoidica diabeticorum.
Det kan också vara användbart vid cystiska tumörer av en aponeuros eller sena (ganglier).
DOSERING OCH ADMINISTRERING
OBS: INNEHÅLLER BENSYLALKOHOL (se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER: Pediatrisk användning)
På grund av möjliga fysiska inkompatibiliteter bör Aristocort® Forte Sterile Vattensuspension inte spädas eller blandas med andra lösningar.
Allmän
Den initiala intramuskulära dosen av triamcinolondiacetat injicerbar suspension kan variera från 3 till 48 mg per dag beroende på den specifika sjukdomsenhet som behandlas. I vissa överväldigande, akuta, livshotande situationer kan dock administrering i doser som överstiger de vanliga doserna vara motiverade och kan vara i multiplar av de orala doserna.
Det bör betonas att doskraven är varierande och måste anpassas utifrån den sjukdom som behandlas och patientens reaktion. Efter att ett gynnsamt svar noterats, bör den korrekta underhållsdosen bestämmas genom att minska den initiala läkemedelsdosen i små minskningar med lämpliga tidsintervall tills den lägsta dosen som kommer att upprätthålla ett adekvat kliniskt svar uppnås. Situationer som kan göra dosjusteringar nödvändiga är förändringar i klinisk status sekundärt till remissioner eller exacerbationer i sjukdomsprocessen, patientens individuella läkemedelskänslighet och effekten av patientens exponering för stressiga situationer som inte är direkt relaterade till den sjukdomsenhet som behandlas. I den senare situationen kan det vara nödvändigt att öka dosen av kortikosteroiden under en tidsperiod som överensstämmer med patientens tillstånd. Om läkemedlet efter långtidsbehandling ska avbrytas, rekommenderas att det sätts ut gradvis snarare än abrupt.
Vid behandling av akuta exacerbationer av multipel skleros rekommenderas dagliga doser på 160 mg triamcinolon under en vecka följt av 64 mg varannan dag under en månad (se FÖRSIKTIGHETSÅTGÄRDER : Neurologisk/psykiatrisk ).
Hos pediatriska patienter kan initialdosen av triamcinolon variera beroende på den specifika sjukdomsenhet som behandlas. Intervallet för initialdoser är 0,11 till 1,6 mg/kg/dag i tre eller fyra uppdelade doser (3,2 till 48 mg/m² bsa/dag).
I jämförelsesyfte är följande motsvarande milligramdos av de olika glukokortikoider:
Dessa dosförhållanden gäller endast för oral eller intravenös administrering av dessa föreningar. När dessa substanser eller deras derivat injiceras intramuskulärt eller i ledutrymmen, kan deras relativa egenskaper förändras kraftigt.
Specifik
Aristocort® Forte Parenteral är triamcinolondiacetat injicerbar suspension (40 mg/ml) suspenderad i en lämplig vehikel. Suspensionen med full styrka kan användas. Topisk etylkloridspray kan användas lokalt före injektion.
Eftersom denna produkt har utformats för enkel administrering, kan en nål med liten borrning (inte mindre än 23 gauge) användas.
Intramuskulär
Även om Aristocort® Forte Parenteral kan administreras intramuskulärt för initial behandling, föredrar de flesta läkare att justera dosen oralt tills adekvat kontroll uppnås. Intramuskulär administrering ger en fördröjd eller depåverkan som kan användas för att komplettera eller ersätta initial oral terapi. Med intramuskulär terapi möjliggörs större övervakning av mängden steroid som används hos patienten som inte följer ett oralt doseringsschema. Vid underhållsbehandling är patient-till-patient-svaret inte enhetligt och därför måste dosen individualiseras för optimal kontroll.
Den genomsnittliga dosen är 40 mg (1 ml) administrerad intramuskulärt en gång i veckan för tillstånd där antiinflammatorisk verkan önskas.
allmänhet kan en parenteral engångsdos 4 till 7 gånger den orala dagliga dosen förväntas kontrollera patienten från 4 till 7 dagar upp till 3 till 4 veckor. Doseringen bör justeras till den punkt där adekvat men inte nödvändigtvis fullständig lindring av symtomen uppnås.
Intraartikulär och Intrasynovial
Den vanliga dosen varierar från 5 till 40 mg. Genomsnittet för knäet är till exempel 25 mg. Effektens varaktighet varierar från en vecka till 2 månader. Akut inflammerade leder kan dock kräva tätare injektioner.
Ett mindre initialt dosintervall av triamcinolondiacetat injicerbar suspension kan ge den önskade effekten när läkemedlet administreras för att ge en lokaliserad koncentration. Injektionsstället och injektionsvolymen bör noggrant övervägas när triamcinolondiacetat administreras för detta ändamål.
En specifik dos beror till stor del på ledens storlek.
Strikt kirurgisk asepsis är obligatorisk. Läkaren bör vara bekant med anatomiska samband som beskrivs i standardläroböcker. Aristocort® Forte Parenteral kan användas i alla tillgängliga leder utom mellankotorna. I allmänhet rekommenderas intrasynovial terapi under följande omständigheter:
Sådan behandling bör inte anses utgöra ett botemedel, för även om denna metod kommer att lindra ledsymptomen, utesluter den inte behovet av de konventionella åtgärder som vanligtvis används.
Det föreslås att infiltration av mjukvävnaden genom lokalbedövning föregår intraartikulär injektion. En 24 gauge eller större nål på en torr spruta kan sättas in i leden och överflödig vätska sugs upp. Under de första timmarna efter injektionen kan det finnas lokalt obehag i leden men detta följs vanligtvis snabbt av effektiv smärtlindring och förbättring av lokal funktion.
HUR LEVERERAS
Aristocort® Forte (triamcinolondiacetat injicerbar suspension), 40 mg/ml, parenteral, ej för intravenös användning, levereras enligt följande:
NDC 0781-3037-71 40 mg/mL (1 mL Fyll i en 2 mL flaska), lådor med 1 NDC 0781-3037-75 40 mg/mL (5 mL Fyll i en 10 mL flaska), lådor med 1
Skydda från ljus.
FRYS INTE
SKAKA VÄL
Förvaras vid 20°-25°C (68°-77°F) [se USP-kontrollerad rumstemperatur ].
Irreversibel klumpning uppstår när produkten är frusen.
Tillverkad i Kanada av: Sandoz Canada Inc. för Sandoz Inc., Princeton, NJ 08540
BIEFFEKTER
(listad i alfabetisk ordning, under varje underavsnitt)
Allergiska reaktioner
Allergiska eller överkänslighetsreaktioner, anafylaktoida reaktioner, anafylaxi, angioödem.
Kardiovaskulär
Bradykardi, hjärtstillestånd, hjärtarytmier, hjärtförstoring, cirkulationskollaps, kongestiv hjärtsvikt, fettemboli, hypertoni, hypertrofisk kardiomyopati hos för tidigt födda barn, myokardruptur efter nyligen genomförd hjärtinfarkt (se VARNINGAR ), lungödem, synkope, takykardi, tromboembolism, tromboflebit, vaskulit.
Dermatologiskt
Akne, allergisk dermatit, kutan och subkutan atrofi, torr fjällande hud, ekkymoser och petekier, ödem, erytem, hyperpigmentering, hypopigmentering, försämrad sårläkning, ökad svettning, utslag, steril abscess, striae, undertryckta reaktioner på hudtester, tunn ömtålig hud, tunnhår i hårbotten, urtikaria.
Endokrin
Minskad kolhydrat- och glukostolerans, utveckling av cushingoidtillstånd, glykosuri, hirsutism, hypertrichos, ökat behov av insulin eller orala hypoglykemiska medel vid diabetes, manifestationer av latent diabetes mellitus, menstruationsrubbningar, sekundär binjurebark- och hypofysreaktion (särskilt i tider av stress, som vid trauma, kirurgi eller sjukdom), undertryckande av tillväxt hos pediatriska patienter.
Vätske- och elektrolytstörningar
Kongestiv hjärtsvikt hos känsliga patienter, vätskeretention, hypokalemisk alkalos, kaliumförlust, natriumretention.
Gastrointestinala
Utspänd buk, dysfunktion av tarm/blåsa (efter intratekal administrering), förhöjda leverenzymnivåer i serum (vanligtvis reversibel vid utsättning), hepatomegali, ökad aptit, illamående, pankreatit, magsår med möjlig perforation och blödning, perforering av tunn- och tjocktarmen (särskilt hos patienter med inflammatorisk tarmsjukdom), ulcerös esofagit.
Metabolisk
Negativ kvävebalans på grund av proteinkatabolism.
Muskuloskeletala
Aseptisk nekros av lårbens- och humerushuvuden, kalcinos (efter intraartikulär eller intra-lesional användning), Charcot-liknande artropati, förlust av muskelmassa, muskelsvaghet, osteoporos, patologisk fraktur av långa ben, postinjection flare (efter intraartikulär användning ), steroidmyopati, senruptur, kotkompressionsfrakturer.
Neurologisk/psykiatrisk
Kramper, depression, emotionell instabilitet, eufori, huvudvärk, ökat intrakraniellt tryck med papillödem (pseudotumor cerebri) vanligen efter avslutad behandling, sömnlöshet, humörsvängningar, neurit, neuropati, parestesi, personlighetsförändringar, psykiska störningar, svindel. Arachnoidit, meningit, parapares/paraplegi och känselrubbningar har förekommit efter intratekal administrering (se VARNINGAR : Neurologisk ).
Oftalmisk
Exoftalmus, glaukom, ökat intraokulärt tryck, posterior subkapsulär grå starr, sällsynta fall av blindhet i samband med periokulära injektioner.
Övrig
Onormala fettavlagringar, minskat motstånd mot infektion, hicka, ökad eller minskad rörlighet och antal spermier, infektioner på injektionsstället efter icke-steril administrering (se VARNINGAR ), sjukdomskänsla, månens ansikte, viktökning.
LÄKEMEDELSINTERAKTIONER
Aminoglutetimid
Aminoglutetimid kan leda till en förlust av kortikosteroidinducerad binjuresuppression.
Amfotericin B-injektions- och kaliumnedbrytande medel
När kortikosteroider administreras samtidigt med kaliumnedbrytande medel (dvs amfotericin B, diuretika), bör patienterna observeras noggrant med avseende på utveckling av hypokalemi. Det har rapporterats fall där samtidig användning av amfotericin B och hydrokortison följdes av hjärtförstoring och kronisk hjärtsvikt.
Antibiotika
Makrolidantibiotika har rapporterats orsaka en signifikant minskning av clearance av kortikosteroider (se LÄKEMEDELSINTERAKTIONER : Leverenzymhämmare ).
Antikolinesteraser
Samtidig användning av antikolinesterasmedel och kortikosteroider kan ge allvarlig svaghet hos patienter med myasthenia gravis. Om möjligt ska antikolinesteraser sättas ut minst 24 timmar innan kortikosteroidbehandling påbörjas.
Antikoagulantia, Oral
Samtidig administrering av kortikosteroider och warfarin resulterar vanligtvis i hämning av svaret på warfarin, även om det har förekommit några motstridiga rapporter. Därför bör koagulationsindex övervakas ofta för att bibehålla den önskade antikoagulerande effekten.
Antidiabetika
Eftersom kortikosteroider kan öka blodsockerkoncentrationerna kan dosjusteringar av antidiabetika behövas.
Antituberkulära läkemedel
Serumkoncentrationerna av isoniazid kan minska.
Kolestyramin
Kolestyramin kan öka clearance av kortikosteroider.
Cyklosporin
Ökad aktivitet av både ciklosporin och kortikosteroider kan uppstå när de två används samtidigt. Kramper har rapporterats vid denna samtidiga användning.
Digitalis glykosider
Patienter på digitalisglykosider kan löpa ökad risk för arytmier på grund av hypokalemi.
Östrogener, inklusive orala preventivmedel
Östrogener kan minska den hepatiska metabolismen av vissa kortikosteroider och därigenom öka deras effekt.
Leverenzyminducerare (t.ex. barbiturater, fenytoin, karbamazepin, rifampin)
Läkemedel som inducerar cytokrom P450 3A4 enzymaktivitet kan öka metabolismen av kortikosteroider och kräva att dosen av kortikosteroiden ökas.
Leverenzymhämmare (t.ex. ketokonazol, makrolidantibiotika som erytromycin och troleandomycin)
Läkemedel som hämmar cytokrom P450 3A4 enzymaktivitet har potential att resultera i ökade plasmakoncentrationer av kortikosteroider.
Ketokonazol
Ketokonazol har rapporterats avsevärt minska metabolismen av vissa kortikosteroider med upp till 60 %, vilket leder till en ökad risk för kortikosteroidbiverkningar.
Icke-steroida antiinflammatoriska medel (NSAID)
Samtidig användning av aspirin (eller andra icke-steroida antiinflammatoriska medel) och kortikosteroider ökar risken för gastrointestinala biverkningar. Aspirin bör användas med försiktighet i kombination med kortikosteroider vid hypoprotrombinemi. Clearance av salicylater kan öka vid samtidig användning av kortikosteroider.
Hudtest
Kortikosteroider kan undertrycka reaktioner på hudtester.
Vacciner
Patienter på långvarig kortikosteroidbehandling kan uppvisa ett minskat svar på toxoider och levande eller inaktiverade vacciner på grund av hämning av antikroppssvar. Kortikosteroider kan också potentiera replikationen av vissa organismer som finns i levande försvagade vacciner. Rutinadministrering av vacciner eller toxoider bör skjutas upp tills kortikosteroidbehandlingen avbryts om möjligt (se VARNINGAR : Vaccination ).
VARNINGAR
Allvarliga neurologiska biverkningar vid epidural administrering
Allvarliga neurologiska händelser, vissa med dödsfall, har rapporterats vid epidural injektion av kortikosteroider. Specifika rapporterade händelser inkluderar, men är inte begränsade till, ryggmärgsinfarkt, paraplegi, quadriplegi, kortikal blindhet och stroke. Dessa allvarliga neurologiska händelser har rapporterats med och utan användning av fluoroskopi. Säkerheten och effektiviteten av epidural administrering av kortikosteroider har inte fastställts, och kortikosteroider är inte godkända för denna användning
Allmän
Denna produkt innehåller bensylalkohol som är potentiellt giftig när den administreras lokalt till neural vävnad. Exponering för stora mängder bensylalkohol har associerats med toxicitet (hypotension, metabol acidos), särskilt hos nyfödda, och en ökad förekomst av kernicterus, särskilt hos små prematura spädbarn. Det har förekommit sällsynta rapporter om dödsfall, främst hos för tidigt födda barn, i samband med exponering för stora mängder bensylalkohol. Administrering av höga doser av läkemedel som innehåller detta konserveringsmedel måste ta hänsyn till den totala mängden bensylalkohol som administreras. Mängden bensylalkohol vid vilken toxicitet kan uppstå är inte känd. Om patienten behöver mer än de rekommenderade doserna eller andra mediciner som innehåller detta konserveringsmedel, måste läkaren ta hänsyn till den dagliga metaboliska belastningen av bensylalkohol från dessa kombinerade källor (se FÖRSIKTIGHETSÅTGÄRDER : Pediatrisk användning ).
Det är avgörande att lämplig teknik används under administrering av Aristocort® Forte och att man ser till att läkemedlet placeras på rätt sätt.
Sällsynta fall av anafylaktoida reaktioner har förekommit hos patienter som får kortikosteroidbehandling (se NEGATIVA REAKTIONER ).
Ökad dos av snabbverkande kortikosteroider är indicerat för patienter som behandlas med kortikosteroider som utsätts för ovanlig stress före, under och efter den stressiga situationen.
Resultat från en multicenter, randomiserad, placebokontrollerad studie med metylprednisolonhemisuccinat, en IV-kortikosteroid, visade en ökning av tidig (vid 2 veckor) och sen (vid 6 månader) mortalitet hos patienter med kraniellt trauma som var fast beslutna att inte ha andra tydliga indikationer för kortikosteroidbehandling. Höga doser av systemiska kortikosteroider, inklusive Aristocort®, ska inte användas för behandling av traumatisk hjärnskada.
Cardio-renal
Genomsnittliga och stora doser av kortikosteroider kan orsaka förhöjt blodtryck, salt- och vattenretention och ökad utsöndring av kalium. Dessa effekter är mindre sannolikt att uppträda med de syntetiska derivaten förutom när de används i stora doser. Saltrestriktioner i kosten och kaliumtillskott kan vara nödvändiga. Alla kortikosteroider ökar kalciumutsöndringen.
Litteraturrapporter tyder på ett uppenbart samband mellan användning av kortikosteroider och ruptur av den fria väggen i vänster kammare efter en nyligen genomförd hjärtinfarkt; därför bör behandling med kortikosteroider användas med stor försiktighet hos dessa patienter.
Endokrin
Kortikosteroider kan ge reversibel hypotalamus-hypofys-binjureaxelsuppression (HPA) med risk för glukokortikosteroidinsufficiens efter utsättande av behandlingen. Läkemedelsinducerad sekundär binjurebarkinsufficiens kan minimeras genom gradvis minskning av dosen. Denna typ av relativ insufficiens kan kvarstå i månader efter avslutad behandling; Därför bör hormonbehandling återupptas i alla situationer av stress som inträffar under den perioden.
Metaboliskt clearance av kortikosteroider är minskat hos hypotyreospatienter och ökat hos hypertyreoideapatienter. Förändringar i patientens sköldkörtelstatus kan kräva justering av dosen.
Infektioner
Allmän
Patienter som tar kortikosteroider är mer mottagliga för infektioner än friska individer. Det kan finnas minskat motstånd och oförmåga att lokalisera infektion när kortikosteroider används. Infektion med vilken patogen som helst (viral, bakteriell, svamp, protozo eller helminthic) på vilken plats som helst i kroppen kan vara associerad med användning av kortikosteroider enbart eller i kombination med andra immunsuppressiva medel. Dessa infektioner kan vara milda, men kan vara allvarliga och ibland dödliga. Med ökande doser av kortikosteroider ökar förekomsten av infektionskomplikationer. Kortikosteroider kan också maskera vissa tecken på aktuell infektion.
Svampinfektioner
Kortikosteroider kan förvärra systemiska svampinfektioner och bör därför inte användas i närvaro av sådana infektioner om de inte behövs för att kontrollera läkemedelsreaktioner. Det har rapporterats fall där samtidig användning av amfotericin B och hydrokortison följdes av hjärtförstoring och kronisk hjärtsvikt (se FÖRSIKTIGHETSÅTGÄRDER : LÄKEMEDELSINTERAKTIONER : Amfotericin B-injektions- och kaliumnedbrytande medel ).
Särskilda patogener
Latent sjukdom kan aktiveras eller det kan finnas en förvärring av interkurrenta infektioner på grund av patogener, inklusive de som orsakas av Amoeba, Candida, Cryptococcus, Mycobacterium, Nocardia, Pneumocystis, Toxoplasma.
Det rekommenderas att latent amebiasis eller aktiv amebiasis utesluts innan kortikosteroidbehandling påbörjas hos alla patienter som tillbringat tid i tropikerna eller hos någon patient med oförklarlig diarré.
På samma sätt bör kortikosteroider användas med stor försiktighet hos patienter med känt eller misstänkt Strongyloides (trådmask) angrepp. Hos sådana patienter kan kortikosteroidinducerad immunsuppression leda till Strongyloides hyperinfektion och spridning med utbredd larvmigration, ofta åtföljd av svår enterokolit och potentiellt dödlig gramnegativ septikemi.
Kortikosteroider ska inte användas vid cerebral malaria.
Tuberkulos
Användningen av kortikosteroider vid aktiv tuberkulos bör begränsas till de fall av fulminerande eller spridd tuberkulos där kortikosteroiden används för behandling av sjukdomen i kombination med en lämplig antituberkulös behandling.
Om kortikosteroider är indicerade hos patienter med latent tuberkulos eller tuberkulinreaktivitet är noggrann observation nödvändig eftersom reaktivering av sjukdomen kan inträffa. Under långvarig kortikosteroidbehandling bör dessa patienter få kemoprofylax.
Vaccination
Administrering av levande eller levande, försvagade vacciner är kontraindicerat hos patienter som får immunsuppressiva doser av kortikosteroider. Dödade eller inaktiverade vacciner kan administreras. Men svaret på sådana vacciner kan inte förutsägas. Immuniseringsprocedurer kan utföras hos patienter som får kortikosteroider som ersättningsterapi, t.ex. för Addisons sjukdom.
Virala infektioner
Vattkoppor och mässling kan ha ett allvarligare eller till och med dödligt förlopp hos pediatriska och vuxna patienter på kortikosteroider. Hos pediatriska och vuxna patienter som inte har haft dessa sjukdomar bör särskild försiktighet iakttas för att undvika exponering. Bidraget från den underliggande sjukdomen och/eller tidigare kortikosteroidbehandling till risken är inte heller känt. Vid exponering för vattkoppor kan profylax med varicella zoster immunglobulin (VZIG) vara indicerat. Vid exponering för mässling kan profylax med immunglobulin (IG) vara indicerat. (Ser respektive bipacksedel för fullständig VZIG- och IG-förskrivningsinformation .) Om vattkoppor utvecklas bör behandling med antivirala medel övervägas.
Neurologisk
Rapporter om allvarliga biverkningar har associerats med den intratekala administreringsvägen (se NEGATIVA REAKTIONER : Neurologisk/psykiatrisk ).
Oftalmisk
Användning av kortikosteroider kan ge bakre subkapsulära grå starr, glaukom med möjlig skada på synnerverna och kan öka etableringen av sekundära ögoninfektioner på grund av bakterier, svampar eller virus. Användning av systemiska kortikosteroider rekommenderas inte vid behandling av optisk neurit och kan leda till en ökad risk för nya episoder. Kortikosteroider bör användas med försiktighet hos patienter med okulär herpes simplex på grund av möjlig hornhinneperforation. Kortikosteroider ska inte användas vid aktiv okulär herpes simplex.
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Denna produkt, liksom många andra steroidformuleringar, är känslig för värme. Därför bör den inte autoklaveras när det är önskvärt att sterilisera flaskans utsida.
Lägsta möjliga dos av kortikosteroid bör användas för att kontrollera tillståndet under behandling. När minskning av dosen är möjlig bör minskningen ske gradvis.
Eftersom komplikationer av behandling med glukokortikoider är beroende av dosens storlek och behandlingens varaktighet, måste ett risk/nytta-beslut tas i varje enskilt fall om dos och behandlingslängd och om daglig eller intermittent behandling ska användas .
Kaposis sarkom har rapporterats förekomma hos patienter som får kortikosteroidbehandling, oftast för kroniska tillstånd. Utsättning av kortikosteroider kan resultera i klinisk förbättring.
Atrofi vid injektionsstället har rapporterats.
Cardio-renal
Eftersom natriumretention med resulterande ödem och kaliumförlust kan förekomma hos patienter som får kortikosteroider, bör dessa medel användas med försiktighet hos patienter med kronisk hjärtsvikt, hypertoni eller njurinsufficiens.
Endokrin
Läkemedelsinducerad sekundär binjurebarkinsufficiens kan minimeras genom gradvis minskning av dosen. Denna typ av relativ insufficiens kan kvarstå i månader efter avslutad behandling; Därför bör hormonbehandling återupptas i alla situationer av stress som inträffar under den perioden. Eftersom mineralokortikoidutsöndringen kan vara försämrad, bör salt och/eller en mineralokortikoid administreras samtidigt.
Gastrointestinala
Steroider bör användas med försiktighet vid aktivt eller latent magsår, divertikulit, färska intestinala anastomoser och ospecifik ulcerös kolit, eftersom de kan öka risken för en perforation.
Tecken på peritoneal irritation efter gastrointestinal perforation hos patienter som får kortikosteroider kan vara minimala eller saknas.
Det finns en förstärkt effekt på grund av ökad metabolism av kortikosteroider hos patienter med cirros.
Intraartikulär och mjukvävnadsadministration
Intraartikulärt injicerade kortikosteroider kan absorberas systemiskt.
Lämplig undersökning av eventuell ledvätska är nödvändig för att utesluta en septisk process.
En markant ökning av smärta åtföljd av lokal svullnad, ytterligare begränsning av ledrörelser, feber och sjukdomskänsla tyder på septisk artrit. Om denna komplikation uppstår och diagnosen sepsis bekräftas, bör lämplig antimikrobiell behandling sättas in.
Injektion av en steroid på ett infekterat ställe ska undvikas. Lokal injektion av en steroid i en tidigare infekterad led rekommenderas vanligtvis inte.
Muskuloskeletala
Kortikosteroider minskar benbildningen och ökar benresorptionen både genom sin effekt på kalciumreglering (dvs. minskad absorption och ökad utsöndring) och hämning av osteoblastfunktionen. Detta, tillsammans med en minskning av proteinmatrisen i benet sekundärt till en ökning av proteinkatabolism, och minskad könshormonproduktion, kan leda till hämning av bentillväxt hos pediatriska patienter och utveckling av osteoporos i alla åldrar. Särskild hänsyn bör tas till patienter med ökad risk för osteoporos (dvs postmenopausala kvinnor) innan kortikosteroidbehandling påbörjas.
Neurologisk/psykiatrisk
Även om kontrollerade kliniska prövningar har visat att kortikosteroider är effektiva för att påskynda lösningen av akuta exacerbationer av multipel skleros, visar de inte att de påverkar sjukdomens slutliga resultat eller naturliga historia. Studierna visar att relativt höga doser kortikosteroider är nödvändiga för att visa en signifikant effekt. (Ser DOSERING OCH ADMINISTRERING .)
En akut myopati har observerats vid användning av höga doser kortikosteroider, som oftast förekommer hos patienter med störningar i neuromuskulär överföring (t.ex. myasthenia gravis), eller hos patienter som samtidigt behandlas med neuromuskulärt blockerande läkemedel (t.ex. pancuronium). Denna akuta myopati är generaliserad, kan involvera ögon- och andningsmuskler och kan resultera i kvadripares. Förhöjning av kreatininkinas kan förekomma. Klinisk förbättring eller återhämtning efter avslutad kortikosteroidbehandling kan ta veckor till år.
Psykiska störningar kan uppstå när kortikosteroider används, allt från eufori, sömnlöshet, humörsvängningar, personlighetsförändringar och svår depression till uppriktiga psykotiska manifestationer. Även existerande emotionell instabilitet eller psykotiska tendenser kan förvärras av kortikosteroider.
Oftalmisk
Intraokulärt tryck kan bli förhöjt hos vissa individer. Om steroidbehandlingen fortsätter i mer än 6 veckor bör det intraokulära trycket övervakas.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Inga adekvata studier har utförts på djur för att fastställa om kortikosteroider har en potential för karcinogenes eller mutagenes.
Steroider kan öka eller minska motiliteten och antalet spermier hos vissa patienter.
Graviditet
Teratogena effekter
Graviditetskategori C
Kortikosteroider har visat sig vara teratogena hos många arter när de ges i doser som motsvarar den mänskliga dosen. Djurstudier där kortikosteroider har getts till gravida möss, råttor och kaniner har gett en ökad förekomst av gomspalt hos avkomman. Det finns inga adekvata och välkontrollerade studier på gravida kvinnor. Kortikosteroider bör endast användas under graviditet om den potentiella nyttan överväger den potentiella risken för fostret. Spädbarn födda av mödrar som har fått kortikosteroider under graviditeten ska noggrant observeras för tecken på hypoadrenalism.
Ammande mödrar
Systemiskt administrerade kortikosteroider förekommer i bröstmjölk och kan undertrycka tillväxten, störa endogen kortikosteroidproduktion eller orsaka andra ogynnsamma effekter. På grund av risken för allvarliga biverkningar hos ammande spädbarn från kortikosteroider, bör ett beslut fattas om att fortsätta amma eller avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Denna produkt innehåller bensylalkohol som konserveringsmedel. Bensylalkohol, en komponent i denna produkt, har associerats med allvarliga biverkningar och dödsfall, särskilt hos pediatriska patienter. "Giftningssyndromet" (kännetecknat av depression i centrala nervsystemet, metabol acidos, flämtande andningar och höga nivåer av bensylalkohol och dess metaboliter som finns i blodet och urinen) har associerats med bensylalkoholdoser > 99 mg/kg/dag hos nyfödda och nyfödda med låg födelsevikt. Ytterligare symtom kan inkludera gradvis neurologisk försämring, kramper, intrakraniell blödning, hematologiska abnormiteter, hudnedbrytning, lever- och njursvikt, hypotoni, bradykardi och kardiovaskulär kollaps. Även om normala terapeutiska doser av denna produkt ger mängder av bensylalkohol som är avsevärt lägre än de som rapporterats i samband med "flämtningssyndromet", är den minsta mängd bensylalkohol vid vilken toxicitet kan uppstå inte känd. För tidigt födda barn och spädbarn med låg födelsevikt, såväl som patienter som får höga doser, kan vara mer benägna att utveckla toxicitet. Utövare som administrerar detta och andra läkemedel som innehåller bensylalkohol bör överväga den kombinerade dagliga metaboliska belastningen av bensylalkohol från alla källor.
Effekten och säkerheten för kortikosteroider i den pediatriska populationen är baserad på det väletablerade effektförloppet för kortikosteroider som är liknande i pediatriska och vuxna populationer. Publicerade studier ger bevis på effekt och säkerhet hos pediatriska patienter för behandling av nefrotiskt syndrom (> 2 års ålder) och aggressiva lymfom och leukemier (> 1 månads ålder). Andra indikationer för pediatrisk användning av kortikosteroider, t.ex. svår astma och väsande andning, är baserade på adekvata och välkontrollerade prövningar utförda på vuxna, under förutsättning att sjukdomsförloppet och deras patofysiologi anses vara väsentligen lika i båda populationerna.
Biverkningarna av kortikosteroider hos pediatriska patienter liknar de hos vuxna (se NEGATIVA REAKTIONER ). Liksom vuxna bör pediatriska patienter observeras noggrant med frekventa mätningar av blodtryck, vikt, längd, intraokulärt tryck och klinisk utvärdering för förekomst av infektion, psykosociala störningar, tromboembolism, magsår, grå starr och osteoporos. Pediatriska patienter som behandlas med kortikosteroider på valfri väg, inklusive systemiskt administrerade kortikosteroider, kan uppleva en minskning av deras tillväxthastighet. Denna negativa påverkan av kortikosteroider på tillväxten har observerats vid låga systemiska doser och i avsaknad av laboratoriebevis på HPA-axelsuppression (dvs. cosyntropinstimulering och basala kortisolplasmanivåer). Tillväxthastighet kan därför vara en känsligare indikator på systemisk kortikosteroidexponering hos pediatriska patienter än några vanliga tester av HPA-axelns funktion. Den linjära tillväxten hos pediatriska patienter som behandlas med kortikosteroider bör övervakas och de potentiella tillväxteffekterna av förlängd behandling bör vägas mot kliniska fördelar och tillgången på behandlingsalternativ. För att minimera de potentiella tillväxteffekterna av kortikosteroider bör pediatriska patienter titreras till lägsta effektiva dos.
Geriatrisk användning
Kliniska studier inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling.
ÖVERDOS
Behandling av akut överdosering är understödjande och symtomatisk terapi. För kronisk överdosering vid allvarlig sjukdom som kräver kontinuerlig steroidbehandling, kan dosen av kortikosteroiden reduceras endast tillfälligt, eller alternativ dagbehandling kan införas.
KONTRAINDIKATIONER
Aristocort® Forte är kontraindicerat för patienter som är överkänsliga mot någon av komponenterna i denna produkt.
Intramuskulära kortikosteroidpreparat är kontraindicerade för idiopatisk trombocytopen purpura.
Aristocort® Forte är kontraindicerat för intratekal administrering. Rapporter om allvarliga medicinska händelser har associerats med denna administreringsväg.
Arisotcort Forte är kontraindicerat för användning till för tidigt födda barn eftersom formuleringen innehåller bensylalkohol (se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER : Pediatrisk användning ).
Arisotcort Forte är kontraindicerat vid systemiska svampinfektioner, förutom när det administreras som en intraartikulär injektion för lokaliserade ledtillstånd (se VARNINGAR : Infektioner : Svampinfektioner ).
KLINISK FARMAKOLOGI
Glukokortikoider, naturligt förekommande och syntetiska, är binjurebarksteroider som lätt adsorberas från mag-tarmkanalen.
Naturligt förekommande glukokortikoider (hydrokortison och kortison), som också har salthållande egenskaper, används som ersättningsterapi vid binjurebarkbrist. Deras syntetiska analoger används främst för deras antiinflammatoriska effekter vid störningar i många organsystem.
Triamcinolondiacetat saknar i huvudsak mineralkortikoidaktivitet när det administreras i terapeutiska doser, vilket orsakar liten eller ingen natriumretention med minimal eller frånvarande kaliumutsöndring.
PATIENTINFORMATION
Patienter bör varnas för att inte avbryta användningen av kortikosteroider plötsligt eller utan medicinsk övervakning, för att informera läkare om att de tar kortikosteroider och att omedelbart söka läkare om de skulle utveckla feber eller andra tecken på infektion.
Personer som tar kortikosteroider bör varnas för att undvika exponering för vattkoppor eller mässling. Patienter bör också informeras om att om de exponeras bör läkare uppsökas utan dröjsmål.
