Clarinex 5mg Desloratadine Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
CLARINEX® (desloratadin) Tabletter
BESKRIVNING
CLARINEX (desloratadin) tabletter är ljusblå, runda, filmdragerade tabletter innehållande 5 mg desloratadin, ett antihistamin, som ska administreras oralt. CLARINEX 5mg tabletter innehåller även följande hjälpämnen: dibasiskt kalciumfosfatdihydrat USP, mikrokristallin cellulosa NF, majsstärkelse NF, talk USP, karnaubavax NF, vitt vax NF, beläggningsmaterial bestående av laktosmonohydrat, hypromellos, polyetylendioxid, titandioxid, FD&C Blue #2 Aluminium Lake.
CLARINEX oral lösning är en klar orangefärgad vätska som innehåller 0,5 mg/1 ml desloratadin. Den orala lösningen innehåller följande inaktiva ingredienser: propylenglykol USP, sorbitollösning USP, citronsyra (vattenfri) USP, natriumcitratdihydrat USP, natriumbensoat NF, dinatriumedetat USP, renat vatten USP. Den innehåller också strösocker, naturlig och artificiell smak för bubbelgum och FDC Yellow #6 färgämne.
Desloratadin är ett vitt till benvitt pulver som är lätt lösligt i vatten, men mycket lösligt i etanol och propylenglykol. Den har en empirisk formel: C19H19ClN2 och en molekylvikt på 310,8. Det kemiska namnet är 8-klor-6,11-dihydro-11-(4-piperdinyliden)-5H-benso[5,6]cyklohepta[1,2-b]pyridin och har följande struktur:
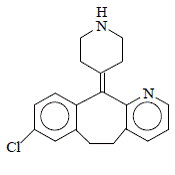
INDIKATIONER
Säsongsbunden allergisk rinit
CLARINEX® är indicerat för lindring av nasala och icke-nasala symtom på säsongsbunden allergisk rinit hos patienter från 2 år och äldre.
Perenn allergisk rinit
CLARINEX är indicerat för lindring av nasala och icke-nasala symtom på perenn allergisk rinit hos patienter 6 månader och äldre.
Kronisk idiopatisk urtikaria
CLARINEX 5mg är indicerat för symtomatisk lindring av klåda, minskning av antalet nässelutslag och storlek på nässelutslag, hos patienter med kronisk idiopatisk urtikaria 6 månaders ålder och äldre.
DOSERING OCH ADMINISTRERING
Även om en oralt sönderfallande tablettformulering av desloratadin kan finnas tillgänglig på marknaden, marknadsförs inte längre CLARINEX® RediTabs® tabletter.
CLARINEX 5 mg tabletter, oral lösning eller RediTabs tabletter kan tas utan hänsyn till måltider. Placera CLARINEX (desloratadine) RediTabs tabletter på tungan och låt sönderfalla innan du sväljer. Tablettsönderfall sker snabbt. Administreras med eller utan vatten. Ta tabletten omedelbart efter att blistern öppnats.
Den åldersanpassade dosen av CLARINEX oral lösning ska administreras med en kommersiellt tillgänglig mättopp eller spruta som är kalibrerad för att leverera 2 mL och 2,5 mL (½ tesked).
Vuxna och ungdomar 12 år och äldre
Den rekommenderade dosen av CLARINEX tabletter eller CLARINEX RediTabs tabletter är en 5 mg tablett en gång dagligen. Den rekommenderade dosen av CLARINEX oral lösning är 2 teskedar (5 mg i 10 ml) en gång dagligen.
Barn 6 till 11 år
Den rekommenderade dosen av CLARINEX oral lösning är 1 tesked (2,5 mg i 5 ml) en gång dagligen. Den rekommenderade dosen av CLARINEX RediTabs tabletter är en 2,5 mg tablett en gång dagligen.
Barn från 12 månader till 5 år
Den rekommenderade dosen av CLARINEX 5 mg oral lösning är ½ tesked (1,25 mg i 2,5 ml) en gång dagligen.
Barn 6 till 11 månaders ålder
Den rekommenderade dosen av CLARINEX oral lösning är 2 ml (1 mg) en gång dagligen.
Vuxna med nedsatt lever- eller njurfunktion
Till vuxna patienter med nedsatt lever- eller njurfunktion rekommenderas en startdos på en 5 mg tablett varannan dag baserat på farmakokinetiska data. Dosrekommendation för barn med nedsatt lever- eller njurfunktion kan inte göras på grund av brist på data [se KLINISK FARMAKOLOGI ].
HUR LEVERERAS
Doseringsformer och styrkor
CLARINEX tabletter är ljusblå, filmdragerade tabletter präglade med ”C5” innehållande 5 mg desloratadin. CLARINEX oral lösning är en klar orangefärgad vätska som innehåller 0,5 mg desloratadin/1 ml.
Förvaring Och Hantering
CLARINEX 5mg tabletter: Präglade "C5", ljusblå, filmdragerade tabletter som är förpackade i plastflaskor av högdensitetspolyeten om 100 ( NDC 0085-1264-01).
CLARINEX 5mg oral lösning: Klar orangefärgad vätska innehållande 0,5 mg/1 ml desloratadin i en 16-ounce bärnstensfärgad glasflaska ( NDC 0085-1334-01) och en 4-ounce bärnstensfärgad glasflaska ( NDC 0085-1334-02).
Lagring
CLARINEX tabletter: Skydda Unit-of-Use-förpackningar och Unit-Dose Hospital Pack från överdriven fukt. Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur ]. Värmekänslig. Undvik exponering vid eller över 30°C (86°F).
CLARINEX oral lösning: Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur ]. Skydda från ljus.
Tillverkad för: Merck Sharp & Dohme Corp., ett dotterbolag till MERCK & CO., INC., Whitehouse Station, NJ 08889, USA. Reviderad: mars 2019
BIEFFEKTER
Följande biverkningar diskuteras mer i detalj i andra avsnitt av etiketten:
- Överkänslighetsreaktioner. [Ser VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under mycket varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i klinisk praxis.
Vuxna Och Tonåringar
Allergisk rinit
I placebokontrollerade multipeldosstudier fick 2834 patienter i åldern 12 år eller äldre CLARINEX tabletter i doser på 2,5 mg till 20 mg dagligen, av vilka 1655 patienter fick den rekommenderade dagliga dosen på 5 mg. Hos patienter som fick 5 mg dagligen var frekvensen av biverkningar likartad för patienter som behandlades med CLARINEX 5 mg och placebobehandlade. Andelen patienter som avbröt i förtid på grund av biverkningar var 2,4 % i CLAINEX 5 mg-gruppen och 2,6 % i placebogruppen. Det förekom inga allvarliga biverkningar i dessa studier på patienter som fick desloratadin. Alla biverkningar som rapporterades av mer än eller lika med 2 % av patienterna som fick den rekommenderade dagliga dosen av CLARINEX 5 mg tabletter (5 mg en gång dagligen), och som var vanligare med CLARINEX tabletter än placebo, listas i tabell 1.
Frekvensen och omfattningen av laboratorieavvikelser och elektrokardiografiska avvikelser var likartade hos patienter som behandlats med CLARINEX och placebo.
Det fanns inga skillnader i biverkningar för subgrupper av patienter som definierats av kön, ålder eller ras.
Kronisk idiopatisk urtikaria
I placebokontrollerade flerdosstudier av kronisk idiopatisk urtikaria fick 211 patienter i åldrarna 12 år eller äldre CLARINEX 5 mg tabletter och 205 fick placebo. Biverkningar som rapporterades av mer än eller lika med 2 % av patienterna som fick CLARINEX 5 mg tabletter och som var vanligare med CLARINEX 5 mg än placebo var (frekvenser för CLARINEX 5 mg respektive placebo): huvudvärk (14 %, 13 %) , illamående (5 %, 2 %), trötthet (5 %, 1 %), yrsel (4 %, 3 %), faryngit (3 %, 2 %), dyspepsi (3 %, 1 %) och myalgi (3 %). %, 1 %).
Pediatrik
Tvåhundrafyrtiosex pediatriska försökspersoner i åldern 6 månader till 11 år fick CLARINEX oral lösning i 15 dagar i tre placebokontrollerade kliniska prövningar. Pediatriska försökspersoner i åldern 6 till 11 år fick 2,5 mg en gång om dagen, försökspersoner i åldern 1 till 5 år fick 1,25 mg en gång om dagen och försökspersoner i åldern 6 till 11 månader fick 1,0 mg en gång dagligen.
Hos försökspersoner i åldern 6 till 11 år rapporterades inga individuella biverkningar av 2 procent eller fler av försökspersonerna.
Hos försökspersoner i åldern 2 till 5 år, rapporterade biverkningar för CLARINEX och placebo hos minst 2 procent av försökspersonerna som fick CLARINEX 5 mg oral lösning och med en frekvens som var högre än placebo, feber (5,5 %, 5,4 %), urinvägsinfektion (3,6 %). %, 0 %) och varicella (3,6 %, 0 %).
Hos försökspersoner i åldern 12 månader till 23 månader, rapporterade biverkningar för CLARINEX 5 mg-produkten och placebo hos minst 2 procent av försökspersonerna som fick CLARINEX oral lösning och med en frekvens som var högre än placebo, feber (16,9 %, 12,9 %), diarré ( 15,4 %, 11,3 %), övre luftvägsinfektioner (10,8 %, 9,7 %), hosta (10,8 %, 6,5 %), ökad aptit (3,1 %, 1,6 %), känslomässig labilitet (3,1 %, 0 %), epistaxis ( 3,1 %, 0 %), parasitisk infektion (3,1 %, 0 %), faryngit (3,1 %, 0 %), makulopapulära utslag (3,1 %, 0 %).
Hos försökspersoner i åldern 6 månader till 11 månader var biverkningar rapporterade för CLARINEX 5 mg och placebo hos minst 2 procent av försökspersonerna som fick CLARINEX 5 mg oral lösning och med en frekvens som var högre än placebo, övre luftvägsinfektioner (21,2 %, 12,9 %), diarré (19,7 %, 8,1 %), feber (12,1 %, 1,6 %), irritabilitet (12,1 %, 11,3 %), hosta (10,6 %, 9,7 %), somnolens (9,1 %, 8,1 %), bronkit (6,1 %, 0 %), öroninflammation (6,1 %, 1,6 %), kräkningar (6,1 %, 3,2 %), anorexi (4,5 %, 1,6 %), faryngit (4,5 %, 1,6 %), sömnlöshet (4,5 %, 0 %), rinorré (4,5 %, 3,2 %), erytem (3,0 %, 1,6 %) och illamående (3,0 %, 0 %).
Det fanns inga kliniskt betydelsefulla förändringar i någon elektrokardiografisk parameter, inklusive QTc-intervallet. Endast en av de 246 pediatriska försökspersonerna som fick CLARINEX 5 mg oral lösning i de kliniska prövningarna avbröt behandlingen på grund av en biverkning.
Erfarenhet efter marknadsföring
Eftersom biverkningar rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering. Följande spontana biverkningar har rapporterats under marknadsföringen av desloratadin:
Hjärtsjukdomar: takykardi, hjärtklappning
Andningsvägar, bröstkorg och mediastinum: dyspné
Hud och subkutan vävnad: utslag, klåda
Störningar i nervsystemet: psykomotorisk hyperaktivitet, rörelsestörningar (inklusive dystoni, tics och extrapyramidala symtom), kramper (rapporterade hos patienter med och utan en känd anfallsstörning)
Immunsystemets störningar: överkänslighetsreaktioner (såsom urtikaria, ödem och anafylaxi)
Undersökningar: förhöjda leverenzymer inklusive bilirubin
Lever och gallvägar: hepatit
Metabolism och näringsstörningar: ökad aptit
LÄKEMEDELSINTERAKTIONER
Hämmare av Cytokrom P450 3A4
kontrollerade kliniska studier resulterade samtidig administrering av desloratadin och ketokonazol, erytromycin eller azitromycin i ökade plasmakoncentrationer av desloratadin och 3-hydroxidesloratadin, men det fanns inga kliniskt relevanta förändringar i säkerhetsprofilen för desloratadin. [Ser KLINISK FARMAKOLOGI ]
Fluoxetin
I kontrollerade kliniska studier resulterade samtidig administrering av desloratadin och fluoxetin, en selektiv serotoninåterupptagshämmare (SSRI), i ökade plasmakoncentrationer av desloratadin och 3-hydroxidesloratadin, men det fanns inga kliniskt relevanta förändringar i säkerhetsprofilen för desloratadin. [Ser KLINISK FARMAKOLOGI ]
Cimetidin
I kontrollerade kliniska studier resulterade samtidig administrering av desloratadin och cimetidin, en histamin H2-receptorantagonist, i ökade plasmakoncentrationer av desloratadin och 3 hydroxydesloratadin, men det fanns inga kliniskt relevanta förändringar i säkerhetsprofilen för desloratadin. [Ser KLINISK FARMAKOLOGI ]
Narkotikamissbruk och beroende
Det finns ingen information som indikerar att missbruk eller beroende förekommer med CLARINEX tabletter.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Överkänslighetsreaktioner
Överkänslighetsreaktioner inklusive hudutslag, klåda, urtikaria, ödem, dyspné och anafylaxi har rapporterats efter administrering av desloratadin. Om en sådan reaktion uppstår, bör behandlingen med CLALINEX 5 mg avbrytas och alternativ behandling bör övervägas. [Ser NEGATIVA REAKTIONER ]
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION ).
Information för patienter
- Patienterna ska instrueras att använda CLARIINEX 5 mg enligt anvisningarna.
- Eftersom det inte finns några livsmedelseffekter på biotillgängligheten, kan patienterna instrueras om att CLARINEX 5 mg tabletter, oral lösning eller RediTabs tabletter kan tas utan hänsyn till måltider.
- Patienter bör rådas att inte öka dosen eller doseringsfrekvensen eftersom studier inte har visat ökad effekt vid högre doser och somnolens kan förekomma.
- Fenylketonurika: CLARINEX RediTabs tabletter innehåller fenylalanin.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenicitetsstudier
Desloratadins karcinogena potential utvärderades med en loratadinstudie på råttor och en desloratadinstudie på möss. I en 2-årig studie på råttor administrerades loratadin i kosten i doser upp till 25 mg/kg/dag (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 30 gånger AUC hos människor vid den rekommenderade dagliga orala dosen). En signifikant högre incidens av hepatocellulära tumörer (kombinerade adenom och karcinom) observerades hos män som fick 10 mg/kg/dag loratadin och hos män och kvinnor som fick 25 mg/kg/dag loratadin. De uppskattade desloratadin- och desloratadinmetabolitexponeringarna hos råttor som fick 10 mg/kg loratadin var cirka 7 gånger AUC hos människor vid den rekommenderade dagliga orala dosen. Den kliniska betydelsen av dessa fynd under långvarig användning av desloratadin är inte känd.
en 2-årig koststudie på möss, visade hanar och honor som gavs upp till 16 mg/kg/dag respektive 32 mg/kg/dag desloratadin ingen signifikant ökning av förekomsten av några tumörer. De uppskattade desloratadin- och desloratadinmetabolitexponeringarna hos möss vid dessa doser var 12 respektive 27 gånger AUC hos människor vid den rekommenderade dagliga orala dosen.
Genotoxicitetsstudier
I genotoxicitetsstudier med desloratadin fanns det inga tecken på genotoxisk potential i en omvänd mutationsanalys (Salmonella/E. coli däggdjursmikrosom bakteriell mutagenicitetsanalys) eller i 2 analyser för kromosomavvikelser (humant perifert blod lymfocyt klastogenicitetsanalys och mikronucle boneus analys av mus ).
Nedsättning av fertilitet
Det fanns ingen effekt på kvinnlig fertilitet hos råttor vid desloratadindoser på upp till 24 mg/kg/dag (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 130 gånger AUC hos människor vid den rekommenderade dagliga orala dosen). En manlig specifik minskning av fertiliteten, påvisad genom minskade kvinnliga befruktningsfrekvenser, minskat antal spermier och rörlighet, och histopatologiska testikelförändringar, inträffade vid en oral desloratadindos på 12 mg/kg hos råttor (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 45 gånger högre än AUC hos människor vid den rekommenderade dagliga orala dosen). Desloratadin hade ingen effekt på fertiliteten hos råttor vid en oral dos på 3 mg/kg/dag (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 8 gånger AUC hos människor vid den rekommenderade dagliga orala dosen).
Användning i specifika populationer
Graviditet
Graviditetskategori C
Det finns inga adekvata och välkontrollerade studier på gravida kvinnor. Eftersom reproduktionsstudier på djur inte alltid förutsäger mänskligt svar, bör desloratadin endast användas under graviditet om det verkligen behövs.
Desloratadin var inte teratogent hos råttor eller kaniner vid cirka 210 respektive 230 gånger ytan under koncentration-tidkurvan (AUC) hos människor vid den rekommenderade dagliga orala dosen. En ökning av förlusten före implantation och ett minskat antal implantationer och foster noterades dock i en separat studie på honråttor med cirka 120 gånger AUC hos människor vid den rekommenderade dagliga orala dosen. Minskad kroppsvikt och långsam upprättande reflex rapporterades hos ungar vid cirka 50 gånger eller högre än AUC hos människor vid den rekommenderade dagliga orala dosen. Desloratadin hade ingen effekt på ungas utveckling vid cirka 7 gånger AUC hos människor vid den rekommenderade dagliga orala dosen. Jämförelse med AUC hänvisade till exponeringen för desloratadin hos kaniner och summan av exponeringen för desloratadin och dess metaboliter hos råttor. [Ser Icke-klinisk toxikologi ]
Ammande mödrar
Desloratadin går över i bröstmjölk; därför bör ett beslut fattas om att avbryta amningen eller att avbryta desloratadin, med hänsyn till fördelarna med läkemedlet för den ammande mamman och den eventuella risken för barnet.
Pediatrisk användning
Den rekommenderade dosen av CLARINEX 5 mg oral lösning för den pediatriska populationen är baserad på en jämförelse av korsstudier av plasmakoncentrationen av CLARINEX 5 mg hos vuxna och pediatriska försökspersoner. Säkerheten för CLARINEX oral lösning har fastställts hos 246 pediatriska försökspersoner i åldern 6 månader till 11 år i tre placebokontrollerade kliniska studier. Eftersom förloppet av säsongsbunden och perenn allergisk rinit och kronisk idiopatisk urtikaria och effekterna av CLARINEX är tillräckligt lika i den pediatriska och den vuxna populationen, tillåter det extrapolering från vuxeneffektdata till pediatriska patienter. Effektiviteten av CLARINEX 5 mg oral lösning i dessa åldersgrupper stöds av bevis från adekvata och välkontrollerade studier av CLARINEX 5 mg tabletter på vuxna. Säkerheten och effektiviteten av CLARINEX 5 mg tabletter eller CLARINEX 5 mg oral lösning har inte visats hos pediatriska patienter yngre än 6 månader. [Ser KLINISK FARMAKOLOGI ]
CLARINEX RediTabs 2,5 mg tablett har inte utvärderats hos pediatriska patienter. Bioekvivalens för CLARINEX 5 mg RediTabs tablett och den tidigare marknadsförda RediTabs tabletten fastställdes hos vuxna. I samband med de beskrivna dosfinnande studierna inom pediatrik, stödjer farmakokinetiska data för CLARINEX 5 mg RediTabs användningen av dosstyrkan på 2,5 mg till pediatriska patienter i åldern 6 till 11 år.
Geriatrisk användning
Kliniska studier av desloratadin inkluderade inte tillräckligt många försökspersoner i åldern 65 år och äldre för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader mellan äldre och yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktigt, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och samtidig sjukdom eller annan läkemedelsbehandling. [Ser KLINISK FARMAKOLOGI ]
Nedsatt njurfunktion
Dosjustering för patienter med nedsatt njurfunktion rekommenderas [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Dosjustering för patienter med nedsatt leverfunktion rekommenderas [se DOSERING OCH ADMINISTRERING och KLINISK FARMAKOLOGI ].
ÖVERDOS
I händelse av överdosering, överväg standardåtgärder för att avlägsna eventuellt oabsorberat läkemedel. Symtomatisk och stödjande behandling rekommenderas. Desloratadin och 3-hydroxidesloratadin elimineras inte genom hemodialys.
Information om akut överdosering är begränsad till erfarenhet från biverkningsrapporter efter marknadsföringen och från kliniska prövningar som utförts under utvecklingen av CLAINEX 5 mg-produkten. I en dosvarierande prövning rapporterades somnolens vid doser på 10 mg och 20 mg/dag.
I en annan studie rapporterades inga kliniskt relevanta biverkningar hos normala manliga och kvinnliga frivilliga som fick enstaka dagliga doser av CLARINEX 45 mg under 10 dagar [se KLINISK FARMAKOLOGI ].

Dödlighet inträffade hos råttor vid orala doser på 250 mg/kg eller mer (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 120 gånger AUC hos människor vid den rekommenderade dagliga orala dosen). Den orala dödliga mediandosen hos möss var 353 mg/kg (uppskattad desloratadinexponering var cirka 290 gånger den humana dagliga orala dosen på mg/m²-basis). Inga dödsfall inträffade vid orala doser upp till 250 mg/kg hos apor (uppskattade exponeringar för desloratadin var cirka 810 gånger den dagliga orala dosen för människor på mg/m²-basis).
KONTRAINDIKATIONER
CLARINEX 5mg tabletter, RediTabs och oral lösning är kontraindicerade hos patienter som är överkänsliga mot detta läkemedel eller mot något av dess ingredienser eller mot loratadin [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och NEGATIVA REAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Desloratadin är en långverkande tricyklisk histaminantagonist med selektiv H1-receptor histaminantagonistaktivitet. Receptorbindningsdata indikerar att vid en koncentration av 2-3 ng/ml (7 nanomolar) visar desloratadin signifikant interaktion med den humana histamin H1-receptorn. Desloratadin hämmade histaminfrisättning från mänskliga mastceller in vitro. Resultat av en radiomärkt vävnadsfördelningsstudie på råttor och en radioligand H1-receptorbindningsstudie på marsvin visade att desloratadin inte lätt passerade blod-hjärnbarriären. Den kliniska betydelsen av detta fynd är okänd.
Farmakodynamik
Wheal Och Flare
Humanhistaminstudier efter enstaka och upprepade doser på 5 mg desloratadin har visat att läkemedlet uppvisar en antihistamineffekt efter 1 timme; denna aktivitet kan pågå så länge som 24 timmar. Det fanns inga tecken på histamininducerad takyfylax i huden inom gruppen desloratadin 5 mg under den 28 dagar långa behandlingsperioden. Den kliniska relevansen av histamintestning av wheal skin är okänd.
Effekter på QTc
Enstaka dagliga doser på 45 mg gavs till normala manliga och kvinnliga frivilliga under 10 dagar. Alla EKG erhållna i denna studie avlästes manuellt på ett förblindat sätt av en kardiolog. Hos CLARIINEX-behandlade försökspersoner var det en ökning av medelhjärtfrekvensen på 9,2 slag per minut jämfört med placebo. QT-intervallet korrigerades för hjärtfrekvens (QTc) med både Bazett- och Fridericia-metoderna. Vid användning av QTc (Bazett) var det en genomsnittlig ökning på 8,1 msek hos patienter som behandlades med CLARIINEX jämfört med placebo. Vid användning av QTc (Fridericia) var det en genomsnittlig ökning på 0,4 msek hos patienter som behandlats med CLAINEX jämfört med placebo. Inga kliniskt relevanta biverkningar rapporterades.
Farmakokinetik
Absorption
Efter oral administrering av en desloratadin 5 mg tablett en gång dagligen i 10 dagar till normala friska frivilliga, inträffade medeltiden till maximala plasmakoncentrationer (Tmax) cirka 3 timmar efter dos och genomsnittliga steady state maximala plasmakoncentrationer (Cmax) och AUC av 4 ng/ml och 56,9 ng.h/ml observerades, respektive. Varken mat eller grapefruktjuice hade någon effekt på biotillgängligheten (Cmax och AUC) av desloratadin.
Den farmakokinetiska profilen för CLARINEX oral lösning utvärderades i en trevägsövergångsstudie på 30 vuxna frivilliga. En engångsdos på 10 ml CLARINEX oral lösning innehållande 5 mg desloratadin var bioekvivalent med en engångsdos på 5 mg CLARINEX tablett. Föda hade ingen effekt på biotillgängligheten (AUC och Cmax) för CLARINEX 5 mg oral lösning.
Den farmakokinetiska profilen för CLARINEX 5 mg RediTabs-tabletter utvärderades i en trevägsövergångsstudie på 24 vuxna frivilliga. En enstaka CLARINEX RediTabs-tablett innehållande 5 mg desloratadin var bioekvivalent med en enstaka 5-mg CLARINEX RediTabs-tablett (ursprunglig formulering) för både desloratadin och 3-hydroxidesloratadin. Mat och vatten hade ingen effekt på biotillgängligheten (AUC och Cmax) för CLARIINEX RediTabs tabletter.
Distribution
Desloratadin och 3-hydroxidesloratadin är cirka 82 % till 87 % respektive 85 % till 89 % bundna till plasmaproteiner. Proteinbindningen av desloratadin och 3-hydroxidesloratadin var oförändrad hos patienter med nedsatt njurfunktion.
Ämnesomsättning
Desloratadin (en huvudmetabolit av loratadin) metaboliseras i stor utsträckning till 3-hydroxidesloratadin, en aktiv metabolit, som därefter glukuronideras. Enzymet/enzymerna som ansvarar för bildandet av 3-hydroxidesloratadin har inte identifierats. Data från kliniska prövningar indikerar att en delmängd av den allmänna befolkningen har en minskad förmåga att bilda 3hydroxidesloratadin och är dåliga metaboliserare av desloratadin. I farmakokinetiska studier (n=3748) var cirka 6 % av försökspersonerna låga metaboliserare av desloratadin (definierat som en patient med ett AUC-förhållande på 3-hydroxidesloratadin till desloratadin mindre än 0,1, eller en försöksperson med en desloratadinhalveringstid som överstiger 50 timmar ). Dessa farmakokinetiska studier inkluderade försökspersoner mellan 2 och 70 år, inklusive 977 försökspersoner i åldrarna 2 till 5 år, 1575 försökspersoner i åldrarna 6 till 11 år och 1196 försökspersoner i åldrarna 12 till 70 år. Det fanns ingen skillnad i förekomsten av dåliga metaboliserare mellan åldersgrupper. Frekvensen av dåliga metaboliserare var högre hos svarta (17 %, n=988) jämfört med kaukasier (2 %, n=1 462) och latinamerikaner (2 %, n=1 063). Medianexponeringen (AUC) för desloratadin hos de dåliga metaboliserarna var ungefär 6 gånger högre än hos de försökspersoner som inte är låga metaboliserare. Patienter som är dåliga metaboliserare av desloratadin kan inte identifieras prospektivt och kommer att exponeras för högre nivåer av desloratadin efter dosering med den rekommenderade dosen av desloratadin. I kliniska säkerhetsstudier med flera doser, där metaboliserarens status identifierades, inkluderades totalt 94 dåliga metaboliserare och 123 normala metaboliserare och behandlades med CLARINEX oral lösning i 15-35 dagar. I dessa studier observerades inga övergripande skillnader i säkerhet mellan dåliga metaboliserare och normala metaboliserare. Även om det inte setts i dessa studier kan en ökad risk för exponeringsrelaterade biverkningar hos patienter som är dåliga metaboliserare inte uteslutas.
Eliminering
Den genomsnittliga plasmaelimineringshalveringstiden för desloratadin var cirka 27 timmar. Cmax och AUC-värden ökade på ett dosproportionellt sätt efter orala enstaka doser mellan 5 och 20 mg. Graden av ackumulering efter 14 dagars dosering överensstämde med halveringstiden och doseringsfrekvensen. En human massbalansstudie dokumenterade en återhämtning av cirka 87 % av dosen 14C-desloratadin, som fördelades jämnt i urin och avföring som metaboliska produkter. Analys av plasma 3hydroxidesloratadin visade liknande värden för Tmax och halveringstid jämfört med desloratadin.
Särskilda populationer
Geriatriska ämnen
Hos äldre försökspersoner (≥65 år gamla; n=17) efter administrering av flera doser av CLARINEX 5 mg tabletter, var medelvärdena för Cmax och AUC för desloratadin 20 % högre än hos yngre försökspersoner (
Pediatriska ämnen
Hos försökspersoner i åldern 6 till 11 år resulterade en engångsdos på 5 ml CLARINEX oral lösning innehållande 2,5 mg desloratadin i plasmakoncentrationer av desloratadin liknande de som uppnåddes hos vuxna som administrerades en enda 5 mg CLARINEX tablett. Hos försökspersoner i åldern 2 till 5 år resulterade en engångsdos på 2,5 ml CLARINEX oral lösning innehållande 1,25 mg desloratadin i plasmakoncentrationer av desloratadin liknande de som uppnåddes hos vuxna som gavs en enda 5 mg CLARINEX tablett. Cmax och AUC för metaboliten (3-hydroxidesloratadin) var dock 1,27 och 1,61 gånger högre för 5 mg oral lösning administrerad till vuxna jämfört med Cmax och AUC som erhölls hos barn 2 till 11 år som fick 1,25- 2,5 mg CLARINEX oral lösning.
En engångsdos på antingen 2,5 ml eller 1,25 ml CLARINEX 5 mg oral lösning innehållande 1,25 mg respektive 0,625 mg desloratadin administrerades till försökspersoner i åldern 6 till 11 månader och 12 till 23 månader. Resultaten av en populationsfarmakokinetisk analys indikerade att en dos på 1 mg för försökspersoner i åldern 6 till 11 månader och 1,25 mg för försökspersoner i åldern 12 till 23 månader krävs för att erhålla plasmakoncentrationer av desloratadin liknande de som uppnås hos vuxna som administreras en enda 5- mg dos av CLARINEX oral lösning.
CLARINEX 5 mg RediTabs 2,5 mg tablett har inte utvärderats hos pediatriska patienter. Bioekvivalens för CLARINEX 5 mg RediTabs tabletter och de ursprungliga CLARINEX 5 mg RediTabs tabletterna fastställdes hos vuxna. I samband med de beskrivna dosfinnande studierna inom pediatrik, stödjer farmakokinetiska data för CLARINEX 5 mg RediTabs tabletter användningen av 2,5 mg dosstyrka hos pediatriska patienter i åldern 6 till 11 år.
Nedsatt njurfunktion
Desloratadins farmakokinetik efter en engångsdos på 7,5 mg karakteriserades hos patienter med mild (n=7; kreatininclearance 51-69 mL/min/1,73 m²), måttlig (n=6; kreatininclearance 34-43 mL/min/1,73 m²) ), och allvarligt (n=6; kreatininclearance 5-29 ml/min/1,73 m²) patienter med nedsatt njurfunktion eller hemodialysberoende (n=6). Hos patienter med lätt och måttligt nedsatt njurfunktion ökade medianvärdet för Cmax och AUC med cirka 1,2 respektive 1,9 gånger jämfört med patienter med normal njurfunktion. Hos patienter med gravt nedsatt njurfunktion eller som var hemodialysberoende ökade Cmax- och AUC-värdena med cirka 1,7 respektive 2,5 gånger. Minimala förändringar i koncentrationer av 3-hydroxidesloratadin observerades. Desloratadin och 3-hydroxidesloratadin avlägsnades dåligt genom hemodialys. Plasmaproteinbindningen av desloratadin och 3-hydroxidesloratadin var oförändrad av nedsatt njurfunktion. Dosjustering för patienter med nedsatt njurfunktion rekommenderas [se DOSERING OCH ADMINISTRERING ].
Nedsatt leverfunktion
Desloratadins farmakokinetik karakteriserades efter en oral engångsdos hos patienter med mild (n=4), måttlig (n=4) och svår (n=4) leverfunktionsnedsättning enligt definitionen av Child-Pugh-klassificeringen av leverfunktion och 8 patienter med normal leverfunktion. Patienter med nedsatt leverfunktion, oavsett svårighetsgrad, hade ungefär en 2,4-faldig ökning av AUC jämfört med normala försökspersoner. Det uppenbara orala clearance av desloratadin hos patienter med mild, måttlig och gravt nedsatt leverfunktion var 37 %, 36 % respektive 28 % av det hos normala försökspersoner. En ökning av den genomsnittliga eliminationshalveringstiden för desloratadin hos patienter med nedsatt leverfunktion observerades. För 3-hydroxidesloratadin skilde sig medelvärdena för Cmax och AUC för patienter med nedsatt leverfunktion inte statistiskt signifikant från patienter med normal leverfunktion. Dosjustering för patienter med nedsatt leverfunktion rekommenderas [se DOSERING OCH ADMINISTRERING ].
Kön
Kvinnliga försökspersoner som behandlats i 14 dagar med CLARINEX 5 mg tabletter hade 10 % och 3 % högre desloratadin Cmax respektive AUC-värden jämfört med manliga försökspersoner. Cmax- och AUC-värdena för 3-hydroxydesloratadin ökade också med 45 % respektive 48 % hos kvinnor jämfört med män. Dessa uppenbara skillnader är dock sannolikt inte kliniskt relevanta och därför rekommenderas ingen dosjustering.
Lopp
Efter 14 dagars behandling med CLARINEX tabletter var Cmax- och AUC-värdena för desloratadin 18 % respektive 32 % högre hos svarta jämfört med kaukasier. För 3-hydroxidesloratadin var det en motsvarande 10 % minskning av Cmax och AUC-värden hos svarta jämfört med kaukasier. Dessa skillnader är sannolikt inte kliniskt relevanta och därför rekommenderas ingen dosjustering.
Läkemedelsinteraktioner
två kontrollerade kliniska farmakologiska studier på friska män (n=12 i varje studie) och kvinnliga (n=12 i varje studie) frivilliga försökspersoner, administrerades desloratadin 7,5 mg (1,5 gånger den dagliga dosen) en gång dagligen samtidigt med erytromycin 500 mg var 8:e timmar eller ketokonazol 200 mg var 12:e timme i 10 dagar. I tre separata kontrollerade, parallella kliniska farmakologiska studier har desloratadin i den kliniska dosen 5 mg administrerats samtidigt med azitromycin 500 mg följt av 250 mg en gång dagligen i 4 dagar (n=18) eller med fluoxetin 20 mg en gång dagligen i 7 dagar efter en 23-dagars förbehandlingsperiod med fluoxetin (n=18) eller med cimetidin 600 mg var 12:e timme i 14 dagar (n=18) under steady-state till normala friska manliga och kvinnliga frivilliga. Även om ökade plasmakoncentrationer (Cmax och AUC0-24 timmar) av desloratadin och 3hydroxidesloratadin observerades (se tabell 2), fanns det inga kliniskt relevanta förändringar i säkerhetsprofilen för desloratadin, bedömd med elektrokardiografiska parametrar (inklusive det korrigerade QT-intervallet). kliniska laboratorietester, vitala tecken och biverkningar.
Djurtoxikologi och/eller farmakologi Studier av reproduktionstoxikologi
Desloratadin var inte teratogent hos råttor vid doser upp till 48 mg/kg/dag (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 210 gånger AUC hos människor vid den rekommenderade dagliga orala dosen) eller hos kaniner vid doser upp till 60 mg/kg/ dag (uppskattad desloratadinexponering var cirka 230 gånger AUC hos människor vid den rekommenderade dagliga orala dosen). I en separat studie noterades en ökning av pre-implantationsförlust och ett minskat antal implantationer och foster hos honråttor vid 24 mg/kg (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 120 gånger AUC hos människor vid den rekommenderade dagliga orala dos). Minskad kroppsvikt och långsam upprättande reflex rapporterades hos ungar vid doser på 9 mg/kg/dag eller mer (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 50 gånger eller högre än AUC hos människor vid den rekommenderade dagliga orala dosen). Desloratadin hade ingen effekt på ungas utveckling vid en oral dos på 3 mg/kg/dag (uppskattad desloratadin- och desloratadinmetabolitexponering var cirka 7 gånger AUC hos människor vid den rekommenderade dagliga orala dosen).
Kliniska studier
Säsongsbunden allergisk rinit
Den kliniska effekten och säkerheten av CLARINEX tabletter utvärderades hos över 2300 patienter i åldern 12 till 75 år med säsongsbunden allergisk rinit. Totalt 1838 patienter fick 2,5 till 20 mg/dag av CLARINEX i 4 dubbelblinda, randomiserade, placebokontrollerade kliniska prövningar av 2 till 4 veckors varaktighet utförda i USA. Resultaten av dessa studier visade effektiviteten och säkerheten av CLARINEX 5 mg vid behandling av vuxna och ungdomar med säsongsbunden allergisk rinit. I en dosvarierande prövning studerades CLARINEX 2,5 till 20 mg/dag. Doser på 5, 7,5, 10 och 20 mg/dag var överlägsna placebo; och ingen ytterligare fördel sågs vid doser över 5,0 mg. I samma studie observerades en ökning av incidensen av somnolens vid doser på 10 mg/dag och 20 mg/dag (5,2 % respektive 7,6 %) jämfört med placebo (2,3 %).
två 4-veckorsstudier av 924 patienter (i åldern 15 till 75 år) med säsongsbetonad allergisk rinit och samtidig astma, förbättrade CLARINEX 5 mg tabletter 5 mg en gång dagligen rinitsymptomen, utan minskning av lungfunktionen. Detta stöder säkerheten vid administrering av CLARINEX 5 mg tabletter till vuxna patienter med säsongsbunden allergisk rinit med mild till måttlig astma.
CLARINEX tabletter 5 mg en gång dagligen minskade signifikant den totala symtompoängen (summan av individuella poäng av nasala och icke-nasala symtom) hos patienter med säsongsbunden allergisk rinit. Se tabell 3.
Det fanns inga signifikanta skillnader i effektiviteten av CLARIINEX 5 mg tabletter 5 mg mellan undergrupper av patienter definierade av kön, ålder eller ras.
Perenn allergisk rinit
Den kliniska effekten och säkerheten av CLARINEX tabletter 5 mg utvärderades hos över 1300 patienter i åldern 12 till 80 år med perenn allergisk rinit. Totalt 685 patienter fick 5 mg/dag av CLARINEX 5 mg i två dubbelblinda, randomiserade, placebokontrollerade kliniska prövningar av 4 veckors varaktighet utförda i USA och internationellt. I en av dessa studier visades CLARINEX 5 mg tabletter 5 mg en gång dagligen signifikant minska den totala symtompoängen hos patienter med perenn allergisk rinit (tabell 4).
Kronisk idiopatisk urtikaria
Effekten och säkerheten av CLARINEX 5 mg tabletter 5 mg en gång dagligen studerades hos 416 patienter med kronisk idiopatisk urtikaria i åldern 12 till 84 år, av vilka 211 fick CLARINEX. I två dubbelblinda, placebokontrollerade, randomiserade kliniska prövningar av sex veckors varaktighet, vid den i förväg specificerade en-veckors primära tidpunktsutvärderingen, minskade CLARINEX tabletter signifikant svårighetsgraden av klåda jämfört med placebo (tabell 5). Sekundära effektmått utvärderades också, och under den första veckan av behandlingen minskade CLARINEX 5 mg tabletter 5 mg de sekundära effektmåtten, "Antal nässelutslag" och "Storleken på den största bikupan", jämfört med placebo.
Den kliniska säkerheten för CLARINEX oral lösning dokumenterades i tre, 15-dagars, dubbelblinda, placebokontrollerade säkerhetsstudier på pediatriska försökspersoner med en dokumenterad historia av allergisk rinit, kronisk idiopatisk urtikaria eller försökspersoner som var kandidater för antihistaminbehandling. I den första studien administrerades 2,5 mg CLARINEX oral lösning till 60 pediatriska försökspersoner i åldern 6 till 11 år. Den andra studien utvärderade 1,25 mg CLARINEX oral lösning administrerat till 55 pediatriska försökspersoner i åldern 2 till 5 år. I den tredje studien administrerades 1,25 mg CLARINEX 5 mg oral lösning till 65 pediatriska försökspersoner i åldern 12 till 23 månader och 1,0 mg CLARINEX oral lösning administrerades till 66 pediatriska försökspersoner i åldern 6 till 11 månader. Resultaten av dessa studier visade på säkerheten för CLARIINEX 5 mg oral lösning hos pediatriska försökspersoner i åldern 6 månader till 11 år.
PATIENTINFORMATION
CLARINEX® (CLA-RI-NEX) (desloratadin) tabletter, RediTabs® och oral lösning
Läs patientinformationen som medföljer CLARINEX® innan du börjar ta den och varje gång du får påfyllning. Det kan komma ny information. Denna bipacksedel är en sammanfattning av informationen för patienter. Din läkare eller apotekspersonal kan ge dig ytterligare information. Denna bipacksedel ersätter inte att tala med din läkare om ditt medicinska tillstånd eller din behandling.
Vad är Clarinex 5mg?
CLARINEX är ett receptbelagt läkemedel som innehåller läkemedlet desloratadin (ett antihistamin).
CLARINEX används för att hjälpa till att kontrollera symptomen på:
- säsongsbunden allergisk rinit (nysningar, täppt näsa, rinnande näsa och klåda i näsan) hos personer 2 år och äldre.
- perenn allergisk rinit (nysningar, täppt näsa, rinnande näsa och klåda i näsan) hos personer 6 månader och äldre.
- kronisk idiopatisk urtikaria (långvarig klåda) och för att minska antalet och storleken av nässelutslag hos personer 6 månader och äldre.
Clarinex är inte avsett för barn yngre än 6 månader.
Vem ska inte ta Clarinex?
Ta inte Clarinex 5 mg om du:
- är allergisk mot desloratadin eller något av innehållsämnena i CLARINEX tabletter, CLARINEX RediTabs® eller CLARINEX oral lösning. Se slutet av denna bipacksedel för en komplett lista över ingredienser.
- är allergiska mot loratadin (Alavert, Claritin).
Tala med din läkare innan du tar detta läkemedel om du har några frågor om huruvida du ska ta detta läkemedel eller inte.
Vad ska jag berätta för min läkare innan jag tar CLALINEX 5mg?
Innan du tar CLARINEX 5 mg, berätta för din läkare om du:
- har lever- eller njurproblem.
- har andra medicinska tillstånd.
- är gravid eller planerar att bli gravid. Det är inte känt om Clarinex 5 mg kommer att skada ditt ofödda barn. Tala med din läkare om du är gravid eller planerar att bli gravid.
- ammar eller planerar att amma. Clarinex 5 mg kan passera över i din bröstmjölk. Tala med din läkare om det bästa sättet att mata ditt barn om du tar CLARIINEX.
Berätta för din läkare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. CLARINEX 5mg kan påverka hur andra läkemedel fungerar, och andra läkemedel kan påverka hur CLARINEX 5mg fungerar. Tala särskilt om för din läkare om du tar:
- ketokonazol (Nizoral)
- erytromycin (Ery-tab, Eryc, PCE)
- azitromycin (Zithromax, Zmax)
- antihistaminer
- fluoxetin (Prozac)
- cimetidin (Tagamet)
Vet vilka mediciner du tar. Håll en lista över dina läkemedel och visa den för din läkare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag ta Clarinex?
- Ta CLARINEX 5mg precis som din läkare säger åt dig att ta det.
- Ändra inte din dos av CLARINEX 5 mg och ta inte oftare än ordinerat.
- CLARINEX 5 mg kan tas med eller utan mat.
- Placera CLARINEX RediTabs Tablet på tungan och låt den lösas upp innan du sväljer. CLARINEX 5mg RediTabs kan tas med eller utan vatten. Ta din CLARINEX 5mg RediTabs tablett direkt efter att du öppnat blisterförpackningen.
- Ta CLARINEX oral lösning med en mättopp eller oral spruta som kan mäta 2 mL eller 2,5 mL. Fråga din apotekspersonal om en droppare eller spruta om du inte har en.
- Om du tar för mycket CLARINEX, kontakta din läkare eller sök läkarvård omedelbart.
Vilka är de möjliga biverkningarna av CLAINEX tabletter?
CLARINEX 5mg kan orsaka allvarliga biverkningar, inklusive:
- Allergiska reaktioner. Sluta ta CLARINEX 5mg och ring din läkare omedelbart eller få akut hjälp om du har något av dessa symtom:
- utslag
- klåda
- nässelfeber
- svullnad av dina läppar, tunga, ansikte och svalg
- andnöd eller andningssvårigheter
De vanligaste biverkningarna av CLARINEX hos vuxna och barn 12 år och äldre med allergisk rinit inkluderar:
- öm hals
- torr mun
- träningsvärk
- trötthet
- sömnighet
- mensvärk
Ökad sömnighet eller trötthet kan uppstå om du tar mer av CLARINEX än din läkare har ordinerat till dig.
Tala om för din läkare om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av CLARIINEX. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara Clarinex 5mg?
- Lagra CLARINEX tabletter mellan 59°F till 86°F (15°C till 30°C).
- CLARINEX tabletter är känsliga för värme. Förvara inte över 86°F (30°C).
- Skydda CLARINEX 5mg tabletter från fukt.
- Lagra CLARINEX 5mg oral lösning mellan 59°F till 86°F (15°C till 30°C). Skydda CLARINEX 5mg oral lösning från ljus.
Ha kvar CLARINEX Tabletter, RediTabs Tabletter , och Oral lösning och alla läkemedel utom räckhåll för barn.
Allmän information om CLARINEX
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en patientinformationsbroschyr. Använd inte Clarinex 5 mg för ett tillstånd som det inte har ordinerats för. Ge inte Clarinex 5 mg till andra personer, även om de har samma tillstånd som du har. Det kan skada dem.
Denna patientinformationsbroschyr sammanfattar den viktigaste informationen om CLARINEX. Om du vill ha mer information, prata med din läkare. Du kan fråga din apotekspersonal eller läkare om information om CLARIINEX som är skriven för vårdpersonal.
För mer information, gå till www.CLARINEX.com
Vilka är ingredienserna i Clarinex 5mg?
Aktiv beståndsdel: desloratadin
Patienter med fenylketonuri: CLARINEX RediTabs tabletter innehåller fenylalanin.
Inaktiva ingredienser i CLARINEX 5mg tabletter: dibasiskt kalciumfosfatdihydrat USP, mikrokristallin cellulosa NF, majsstärkelse NF, talk USP, karnaubavax NF, vitt vax NF, beläggningsmaterial bestående av laktosmonohydrat, hypromellos, titandioxid, polyetylenglykol och FD&C Blue #2 Aluminium Lake.
Inaktiva ingredienser i CLARINEX 5mg oral lösning: propylenglykol USP, sorbitollösning USP, citronsyra (vattenfri) USP, natriumcitratdihydrat USP, natriumbensoat NF, dinatriumedetat USP, renat vatten USP. Den innehåller också strösocker, naturlig och artificiell smak för bubbelgum och FDC Yellow #6 färgämne.
