Flonase Nasal Spray 50mcg Fluticasone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Flonase och hur används det?
Flonase är ett receptbelagt läkemedel som används för att behandla symtom på allergisk rinit (nysningar, rinnande näsa och kliande eller rinnande ögon) och näspolyper. Flonase kan användas ensamt eller tillsammans med andra läkemedel.
Flonase tillhör en klass av läkemedel som kallas kortikosteroider, intranasala, immunsuppressiva, PHD.
Det är inte känt om Flonase är säkert och effektivt hos barn yngre än 4 år.
Vilka är de möjliga biverkningarna av Flonase?
Flonase kan orsaka allvarliga biverkningar inklusive:
- allvarliga eller pågående näsblod,
- bullriga andning,
- rinnande näsa,
- skorpa runt dina näsborrar,
- rodnad, sår eller vita fläckar i munnen eller halsen,
- feber,
- frossa,
- kroppssmärtor,
- suddig syn,
- ögonsmärta,
- ser glorier runt ljus,
- sår som inte läker,
- förvärrad trötthet,
- muskelsvaghet,
- yrsel,
- illamående, och
- kräkningar
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Flonase inkluderar:
- mindre näsblod,
- sveda eller klåda i näsan,
- sår eller vita fläckar inuti eller runt näsan,
- hosta,
- problem att andas,
- huvudvärk,
- ryggont,
- sinus smärta,
- öm hals,
- feber,
- illamående, och
- kräkningar
BESKRIVNING
Den aktiva beståndsdelen i FLONASE Nasal Spray 50mcg är flutikasonpropionat, en kortikosteroid med det kemiska namnet S-(fluoromethyl) 6α,9-difluoro-11β,17-dihydroxy-16α-methyl-3oxoandrosta-1,4-dien-17β-carbothioate , 17-propionat och följande kemiska struktur:
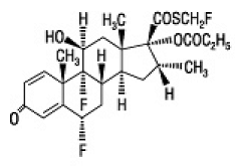
Flutikasonpropionat är ett vitt pulver med en molekylvikt på 500,6 och den empiriska formeln är C25H31F3O5S. Det är praktiskt taget olösligt i vatten, fritt lösligt i dimetylsulfoxid och dimetylformamid och lätt lösligt i metanol och 95 % etanol.
FLONASE Nässpray, 50 mcg är en vattenhaltig suspension av mikrofint flutikasonpropionat för topisk administrering till nässlemhinnan med hjälp av en doserande, finfördelande spraypump. FLONASE Nässpray 50 mcg innehåller även mikrokristallin cellulosa och karboximetylcellulosanatrium, dextros, 0,02 % w/w bensalkoniumklorid, polysorbat 80 och 0,25 % w/w fenyletylalkohol och har ett pH mellan 5 och 7.
Efter initial priming levererar varje aktivering 50 mcg flutikasonpropionat i 100 mg formulering genom näsadaptern.
INDIKATIONER
FLONASE® nässpray är indicerat för behandling av nässymtom på perenn icke-allergisk rinit hos vuxna och pediatriska patienter i åldern 4 år och äldre.
DOSERING OCH ADMINISTRERING
Administrera endast FLONASE nässpray intranasalt. Prime FLONASE nässpray före användning för första gången eller efter en period utan användning (1 vecka eller mer) genom att skaka innehållet väl och släppa ut 6 sprayer i luften bort från ansiktet. Skaka FLONASE nässpray försiktigt före varje användning.
Patienter bör använda FLONASE nässpray med jämna mellanrum eftersom dess effektivitet beror på regelbunden användning. Maximal effekt kan ta flera dagar och enskilda patienter kommer att uppleva en varierande tid till debut och olika grad av symtomlindring.
Vuxna
Den rekommenderade startdosen för vuxna är 2 sprayer (50 mcg flutikasonpropionat vardera) i varje näsborre en gång dagligen (total daglig dos, 200 mcg). Samma totala dagliga dos, 1 spray i varje näsborre administrerad två gånger dagligen (t.ex. kl. 08.00 och 20.00) är också effektiv. Efter de första dagarna kan patienterna kanske minska sin dos till 1 spray i varje näsborre en gång dagligen för underhållsbehandling.
Den maximala totala dagliga dosen bör inte överstiga 2 sprayningar i varje näsborre (total dos, 200 mcg/dag). Det finns inga bevis för att det är mer effektivt att överskrida den rekommenderade dosen.
Ungdomar och barn (i åldern 4 år och äldre)
Den rekommenderade startdosen för ungdomar och barn från 4 år och äldre är 1 spray i varje näsborre en gång dagligen (total daglig dos, 100 mikrogram). Patienter som inte svarar tillräckligt på 1 spray i varje näsborre kan använda 2 sprayer i varje näsborre en gång dagligen (total daglig dos, 200 mcg). När adekvat kontroll har uppnåtts ska dosen minskas till 1 spray i varje näsborre en gång dagligen.
Den maximala totala dagliga dosen bör inte överstiga 2 sprayningar i varje näsborre (200 mcg/dag). Det finns inga bevis för att det är mer effektivt att överskrida den rekommenderade dosen.
HUR LEVERERAS
Doseringsformer och styrkor
FLONASE Nässpray är en nässpraysuspension. Varje 100 mg spray ger 50 mcg flutikasonpropionat.
Förvaring Och Hantering
FLONASE Nässpray, 50 mcg levereras i en bärnstensfärgad glasflaska utrustad med en vit doseringspump, vit näsadapter och grönt dammskydd i en låda med 1 ( NDC 0173-0453-01) med FDA-godkänd Patientmärkning (ser Patientinstruktioner för korrekt aktivering av enheten ). Varje flaska innehåller en nettopåfyllningsvikt på 16 g och kommer att ge 120 manövreringar. Varje aktivering levererar 50 mcg flutikasonpropionat i 100 mg formulering genom näsadaptern. Rätt mängd läkemedel i varje spray kan inte garanteras efter 120 sprayningar, även om flaskan inte är helt tom. Flaskan ska kasseras när det märkta antalet manöverdon har använts.
Förvaras mellan 4° och 30°C (39° och 86°F).
GlaxoSmithKline Research Triangle Park, NC 27709. Reviderad: Jan 2015
BIEFFEKTER
Systemisk och lokal kortikosteroidanvändning kan resultera i följande:
- Näsblod, nässår, Candida albicans-infektion, perforering av nässeptum och försämrad sårläkning [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Grå starr och glaukom [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Immunsuppression [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Hyperkorticism och adrenal suppression [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
- Effekt på tillväxt [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i kliniska prövningar av ett läkemedel inte direkt jämföras med frekvenser i kliniska prövningar av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i praktiken.
I kontrollerade amerikanska kliniska prövningar fick mer än 3 300 försökspersoner med allergisk och icke-allergisk rinit behandling med intranasal flutikasonpropionat. Generellt sett har biverkningar i kliniska prövningar främst associerats med irritation av nässlemhinnorna, och biverkningarna rapporterades med ungefär samma frekvens av patienter som behandlats med placebo. Mindre än 2 % av försökspersonerna i kliniska prövningar avbröt behandlingen på grund av biverkningar; denna frekvens var liknande för vehikelplacebo och aktiva komparatorer.
Säkerhetsdata som beskrivs nedan är baserade på 7 placebokontrollerade kliniska prövningar på försökspersoner med allergisk rinit. De 7 prövningarna inkluderade 536 försökspersoner (57 flickor och 108 pojkar i åldrarna 4 till 11 år, 137 kvinnor och 234 manliga ungdomar och vuxna) som behandlades med FLONASE 200 mikrogram en gång dagligen under 2 till 4 veckor och 2 placebokontrollerade kliniska prövningar som inkluderade 246 (119 kvinnor och 127 manliga ungdomar och vuxna) behandlade med FLONASE 200 mikrogram en gång dagligen under 6 månader (tabell 1). I tabell 1 ingår även biverkningar från 2 studier där 167 barn (45 flickor och 122 pojkar i åldern 4 till 11 år) behandlades med FLONASE 100 mikrogram en gång dagligen i 2 till 4 veckor.
Andra biverkningar med FLONASE nässpray 50 mcg observerade med en incidens mindre än eller lika med 3 % men större än eller lika med 1 % och vanligare än med placebo inkluderade: blod i nässlem, rinnande näsa, buksmärtor, diarré, feber, influensaliknande symtom, värk och smärta, yrsel och bronkit.
Erfarenhet efter marknadsföring
Utöver biverkningar som rapporterats från kliniska prövningar har följande biverkningar identifierats vid användning av intranasal flutikasonpropionat efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering. Dessa händelser har valts för inkludering på grund av antingen deras allvarlighetsgrad, frekvens av rapportering eller orsakssamband med flutikasonpropionat eller en kombination av dessa faktorer.
Allmänna störningar och villkor för administrationsplatsen
Överkänslighetsreaktioner, inklusive angioödem, hudutslag, ödem i ansikte och tunga, klåda, urtikaria, bronkospasm, väsande andning, dyspné och anafylaxi/anafylaktoida reaktioner, som i sällsynta fall var allvarliga.
Öron- och labyrintsjukdomar
Förändring eller förlust av smak- och/eller luktsinne och, sällan, perforering av nässeptum, nässår, ont i halsen, irritation och torrhet i halsen, hosta, heshet och röstförändringar.
Ögonstörningar
Torrhet och irritation, konjunktivit, dimsyn, glaukom, ökat intraokulärt tryck och grå starr.
Fall av tillväxthämning har rapporterats för intranasala kortikosteroider, inklusive FLONASE [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
LÄKEMEDELSINTERAKTIONER
Hämmare av Cytokrom P450 3A4
Flutikasonpropionat är ett substrat för CYP3A4. Användning av starka CYP3A4-hämmare (t.ex. ritonavir, atazanavir, klaritromycin, indinavir, itrakonazol, nefazodon, nelfinavir, saquinavir, ketokonazol, telitromycin, conivaptan, lopinavir, nefazodon, voriconazole, voriconazole, voriconazole, voriconazole, voriconazole, voriconazole, voriconazole, voriconazole, voriconazole, voriconazole, oriconazole, voriconazole) with ad system sprayic FLONASE rekommenderas inte förstärkt nasal effekt av FLONASE. kan inträffa.
Ritonavir
En läkemedelsinteraktionsstudie med flutikasonpropionat vattenhaltig nässpray på friska försökspersoner har visat att ritonavir (en stark CYP3A4-hämmare) signifikant kan öka plasmaexponeringen för flutikasonpropionat, vilket resulterar i signifikant minskade serumkortisolkoncentrationer [se KLINISK FARMAKOLOGI ]. Under användning efter marknadsföring har det förekommit rapporter om kliniskt signifikanta läkemedelsinteraktioner hos patienter som får flutikasonpropionatprodukter, inklusive FLONASE, med ritonavir, vilket resulterat i systemiska kortikosteroideffekter inklusive Cushings syndrom och binjuresuppression.
Ketokonazol
Samtidig administrering av oralt inhalerat flutikasonpropionat (1 000 mcg) och ketokonazol (200 mg en gång dagligen) resulterade i en 1,9-faldig ökning av plasmaflutikasonpropionatexponeringen och en 45 % minskning av plasmakortisolytan under kurvan (AUC), men hade ingen effekt. på urinutsöndring av kortisol.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Lokala nasala effekter
Epistaxis
kliniska prövningar av 2 till 26 veckors varaktighet observerades näsblod oftare hos patienter som behandlats med FLONASE nässpray än de som fick placebo [se NEGATIVA REAKTIONER ].
Nässår
Fall av nässår efter marknadsföring har rapporterats hos patienter som behandlats med FLONASE nässpray [se NEGATIVA REAKTIONER ].
Candida infektion
I kliniska prövningar med flutikasonpropionat administrerat intranasalt har utveckling av lokaliserade infektioner i näsa och svalg med Candida albicans inträffat. När en sådan infektion utvecklas kan den kräva behandling med lämplig lokal terapi och utsättande av FLONASE nässpray. Patienter som använder FLONASE nässpray under flera månader eller längre bör undersökas regelbundet för tecken på Candida-infektion eller andra tecken på negativa effekter på nässlemhinnan.
Nasal septal perforering
Fall av perforering av nässeptum efter marknadsföring har rapporterats hos patienter som behandlats med FLONASE nässpray [se NEGATIVA REAKTIONER ].
Försämrad sårläkning
På grund av den hämmande effekten av kortikosteroider på sårläkning, bör patienter som nyligen har upplevt nässår, näskirurgi eller nästrauma undvika att använda FLONASE nässpray tills läkning har skett.
Glaukom och grå starr
Användning av intranasala och inhalerade kortikosteroider kan leda till utveckling av glaukom och/eller grå starr. Därför är noggrann övervakning berättigad hos patienter med förändrad syn eller med en historia av ökat intraokulärt tryck, glaukom och/eller grå starr.
Överkänslighetsreaktioner inklusive anafylaxi
Överkänslighetsreaktioner (t.ex. anafylaxi, angioödem, urtikaria, kontaktdermatit och hudutslag) har rapporterats efter administrering av FLONASE nässpray. Avbryt FLONASE
Nässpray om sådana reaktioner inträffar [se KONTRAINDIKATIONER ]. I sällsynta fall kan omedelbara överkänslighetsreaktioner inträffa efter administrering av FLONASE nässpray.
Immunsuppression
Personer som använder läkemedel som dämpar immunförsvaret är mer mottagliga för infektioner än friska individer. Vattkoppor och mässling, till exempel, kan ha ett allvarligare eller till och med dödligt förlopp hos känsliga barn eller vuxna som använder kortikosteroider. Hos sådana barn eller vuxna som inte har haft dessa sjukdomar eller blivit ordentligt immuniserade bör särskild försiktighet iakttas för att undvika exponering. Hur dosen, vägen och varaktigheten av administrering av kortikosteroider påverkar risken för att utveckla en spridd infektion är inte känt. Bidraget från den underliggande sjukdomen och/eller tidigare kortikosteroidbehandling till risken är inte heller känt. Om en patient exponeras för vattkoppor kan profylax med varicella zoster immunglobulin (VZIG) vara indicerat. Om en patient exponeras för mässling kan profylax med poolat intramuskulärt immunglobulin (IG) vara indicerat. (Ser den fullständiga förskrivningsinformationen för VZIG och IG. Om vattkoppor utvecklas kan behandling med antivirala medel övervägas.
Intranasala kortikosteroider bör användas med försiktighet, om överhuvudtaget, till patienter med aktiva eller vilande tuberkulösa infektioner i luftvägarna; systemiska svamp-, bakterie-, virus- eller parasitinfektioner; eller okulär herpes simplex.
Hyperkorticism och binjuresuppression
När intranasala kortikosteroider används i högre doser än rekommenderade eller till känsliga individer i rekommenderade doser, kan systemiska kortikosteroideffekter som hyperkorticism och binjurebarksuppression uppträda. Om sådana förändringar inträffar ska dosen av FLONASE nässpray avbrytas långsamt i enlighet med accepterade förfaranden för att avbryta oral kortikosteroidbehandling.
Ersättning av en systemisk kortikosteroid med en topikal kortikosteroid kan åtföljas av tecken på binjurebarksvikt. Dessutom kan vissa patienter uppleva symtom på kortikosteroidabstinens (t.ex. led- och/eller muskelsmärta, trötthet, depression). Patienter som tidigare behandlats under långa perioder med systemiska kortikosteroider och övergått till topikala kortikosteroider bör övervakas noggrant för akut binjurebarksvikt som svar på stress. Hos patienter som har astma eller andra kliniska tillstånd som kräver långvarig systemisk kortikosteroidbehandling, kan snabba minskningar av systemiska kortikosteroiddoser orsaka en allvarlig förvärring av deras symtom.
Läkemedelsinteraktioner med starka Cytokrom P450 3A4-hämmare
Användning av starka cytokrom P450 3A4 (CYP3A4)-hämmare (t.ex. ritonavir, atazanavir, klaritromycin, indinavir, itrakonazol, nefazodon, nelfinavir, sakinavir, ketokonazol, telitromycin, conivaptan, lopinavir, lopinavir, nefazodon Na rekommenderas inte med vor FL nefconazolase) ökade systemiska kortikosteroidbiverkningar kan förekomma [se LÄKEMEDELSINTERAKTIONER , KLINISK FARMAKOLOGI ].
Effekt På Tillväxt
Intranasala kortikosteroider kan orsaka en minskning av tillväxthastigheten när de administreras till pediatriska patienter [se Användning i specifika populationer ]. Övervaka tillväxten rutinmässigt hos pediatriska patienter som får FLONASE nässpray. För att minimera de systemiska effekterna av intranasala kortikosteroider, inklusive FLONASE nässpray, titrera varje patients dos till den lägsta dos som effektivt kontrollerar hans/hennes symtom [se DOSERING OCH ADMINISTRERING , Användning i specifika populationer ].
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION och bruksanvisning ).
Lokala nasala effekter
Informera patienterna om att behandling med FLONASE Nasal Spray 50mcg kan leda till biverkningar, som inkluderar näsblod och nässår. Candidainfektion kan också förekomma vid behandling med FLONASE nässpray. Dessutom har FLONASE Nasal Spray 50mcg associerats med perforering av nässeptum och försämrad sårläkning. Patienter som nyligen har upplevt nässår, näskirurgi eller nästrauma ska inte använda FLONASE nässpray 50 mcg förrän läkning har skett [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Glaukom och grå starr
Informera patienterna om att glaukom och grå starr är förknippade med nasal och inhalerad kortikosteroidanvändning. Rekommendera patienter att meddela sin vårdgivare om en förändring i synen noteras när de använder FLONASE nässpray [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Överkänslighetsreaktioner, inklusive anafylaxi
Informera patienter om att överkänslighetsreaktioner, inklusive anafylaxi, angioödem, urtikaria, kontaktdermatit och hudutslag, kan uppstå efter administrering av FLONASE nässpray. Om sådana reaktioner uppstår ska patienterna avbryta användningen av FLONASE nässpray [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Immunsuppression
Varna patienter som är på immunsuppressiva doser av kortikosteroider för att undvika exponering för vattkoppor eller mässling och om de utsätts för att konsultera sin vårdgivare utan dröjsmål. Informera patienter om potentiell försämring av befintlig tuberkulos; svamp-, bakterie-, virus- eller parasitinfektioner; eller okulär herpes simplex [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Minskad tillväxthastighet
Informera föräldrar om att FLONASE nässpray 50 mcg kan orsaka en minskning av tillväxthastigheten när den administreras till pediatriska patienter. Läkare bör noga följa tillväxten hos barn och ungdomar som tar kortikosteroider oavsett väg [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Pediatrisk användning ].
Använd dagligen för bästa effekt
Informera patienterna om att de ska använda FLONASE Nasal Spray 50mcg regelbundet. FLONASE Nässpray 50mcg har, liksom andra kortikosteroider, ingen omedelbar effekt på rinitsymptom. Maximal förmån kan inte uppnås på flera dagar. Patienter bör inte öka den ordinerade dosen utan bör kontakta sin vårdgivare om symtomen inte förbättras eller om tillståndet förvärras.
Håll spray borta från ögon och mun
Informera patienterna om att undvika att spraya FLONASE nässpray i deras ögon och mun.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Flutikasonpropionat visade ingen tumörframkallande potential hos möss vid orala doser upp till 1 000 mcg/kg (ungefär 20 gånger MRHDID hos vuxna och ungefär 10 gånger MRHDID hos barn på mcg/m² basis) under 78 veckor eller hos råttor vid inhalationsdoser högre till 57 mcg/kg (ungefär 2 gånger MRHDID hos vuxna och ungefär lika med MRHDID hos barn på en mcg/m² basis) under 104 veckor.
Flutikasonpropionat inducerade inte genmutation i prokaryota eller eukaryota celler in vitro. Ingen signifikant klastogen effekt sågs i odlade humana perifera lymfocyter in vitro eller i mikrokärntestet hos mus.
Inga tecken på nedsatt fertilitet observerades hos han- och honråttor vid subkutana doser upp till 50 mikrogram/kg (ungefär 2 gånger MRHDID hos vuxna på en mikrogram/m² basis). Prostatavikten reducerades signifikant vid en subkutan dos på 50 mcg/kg.
Kliniska studier
Perenn icke-allergisk rinit
Tre randomiserade, dubbelblinda, parallellgrupps-, placebokontrollerade vehikelstudier utfördes på 1 191 försökspersoner för att undersöka regelbunden användning av FLONASE nässpray 50 mcg hos försökspersoner med perenn icke-allergisk rinit. Dessa studier utvärderade försökspersoners betygsatta totala nasala symptompoäng (TNSS) som inkluderade nasal obstruktion, postnasalt dropp, rinorré hos patienter som behandlats under 28 dagars dubbelblind terapi och i 1 av de 3 försöken under 6 månaders öppen behandling. Två av dessa studier visade att försökspersoner som behandlats med FLONASE nässpray (100 mcg två gånger dagligen) uppvisade statistiskt signifikanta minskningar av TNSS jämfört med försökspersoner som behandlats med vehikel.
Användning i specifika populationer
Graviditet
Teratogena effekter
Graviditetskategori C. Det finns inga adekvata och välkontrollerade studier med FLONASE nässpray på gravida kvinnor. Kortikosteroider har visat sig vara teratogena hos laboratoriedjur när de administreras systemiskt i relativt låga dosnivåer. Eftersom reproduktionsstudier på djur inte alltid förutsäger mänskligt svar, bör FLONASE nässpray endast användas under graviditet om den potentiella nyttan överväger den potentiella risken för fostret. Kvinnor bör rådas att kontakta sin läkare om de blir gravida medan de tar FLONASE nässpray.
Möss och råttor vid doser av flutikasonpropionat cirka 1 respektive 4 gånger den maximala rekommenderade humana dagliga intranasala dosen (MRHDID) för vuxna (på en mg/m²-basis vid moderns subkutana doser på 45 respektive 100 mcg/kg/dag) visade fostertoxicitet som är karakteristisk för potenta kortikosteroidföreningar, inklusive embryonal tillväxtretardation, omphalocele, gomspalt och retarderad kraniell förbening. Ingen teratogenicitet sågs hos råttor vid doser upp till 3 gånger MRHDID (på en mg/m²-basis vid moderns inhalationsdoser upp till 68,7 mcg/kg/dag).
Hos kaniner observerades fostrets viktminskning och gomspalt vid en dos av flutikasonpropionat cirka 0,3 gånger MRHDID för vuxna (på en mg/m²-basis vid en subkutan dos av modern på 4 mikrogram/kg/dag). Emellertid har inga teratogena effekter rapporterats vid doser av flutikasonpropionat upp till cirka 20 gånger MRHDID för vuxna (på mg/m² vid en oral dos för modern upp till 300 mikrogram/kg/dag). Inget flutikasonpropionat detekterades i plasma i denna studie, vilket överensstämmer med den etablerade låga biotillgängligheten efter oral administrering [se KLINISK FARMAKOLOGI ].
Flutikasonpropionat passerade placentan efter subkutan administrering till möss och råttor och oral administrering till kaniner.
Erfarenhet av orala kortikosteroider sedan de introducerades i farmakologiska, i motsats till fysiologiska doser, tyder på att gnagare är mer benägna att få teratogena effekter från kortikosteroider än människor. Dessutom, eftersom det finns en naturlig ökning av kortikosteroidproduktionen under graviditeten, kommer de flesta kvinnor att behöva en lägre exogen kortikosteroiddos och många kommer inte att behöva kortikosteroidbehandling under graviditeten.
Icke-ratogena effekter
Hypoadrenalism kan förekomma hos spädbarn födda av mödrar som får kortikosteroider under graviditeten. Sådana spädbarn bör övervakas noggrant.
Ammande mödrar
Det är inte känt om flutikasonpropionat utsöndras i human bröstmjölk. Andra kortikosteroider har dock upptäckts i bröstmjölk. Subkutan administrering till lakterande råttor av tritierat flutikasonpropionat i en dos på cirka 0,4 gånger MRHDID för vuxna på mg/m²-basis resulterade i mätbar radioaktivitet i mjölk.
Eftersom det inte finns några data från kontrollerade studier om användning av intranasal FLONASE nässpray 50 mcg av ammande mödrar, bör försiktighet iakttas när FLONASE nässpray 50 mcg administreras till en ammande kvinna.
Pediatrisk användning
Säkerheten och effektiviteten av FLONASE nässpray hos barn från 4 år och äldre har fastställts [se NEGATIVA REAKTIONER , KLINISK FARMAKOLOGI ].Sexhundrafemtio (650) försökspersoner i åldrarna 4 till 11 år och 440 försökspersoner i åldrarna 12 till 17 år studerades i amerikanska kliniska prövningar med flutikasonpropionat nässpray. Säkerheten och effektiviteten av FLONASE Nasal Spray 50mcg hos barn yngre än 4 år har inte fastställts.
Effekter på tillväxt
Kontrollerade kliniska prövningar har visat att intranasala kortikosteroider kan orsaka en minskning av tillväxthastigheten när de administreras till pediatriska patienter. Denna effekt observerades i avsaknad av laboratoriebevis för undertryckning av hypotalamus-hypofys-binjureaxeln (HPA), vilket tyder på att tillväxthastigheten är en känsligare indikator på systemisk kortikosteroidexponering hos pediatriska patienter än några vanliga tester av HPA-axelns funktion. De långsiktiga effekterna av denna minskning av tillväxthastigheten i samband med intranasala kortikosteroider, inklusive effekten på den slutliga vuxenlängden, är okända. Potentialen för tillväxt efter avslutad behandling med intranasala kortikosteroider har inte studerats tillräckligt. Tillväxten hos pediatriska patienter som får intranasala kortikosteroider, inklusive FLONASE nässpray, bör övervakas rutinmässigt (t.ex. via stadiometri). De potentiella tillväxteffekterna av förlängd behandling bör vägas mot de kliniska fördelarna som erhålls och riskerna förknippade med alternativa behandlingar. För att minimera de systemiska effekterna av intranasala kortikosteroider, inklusive FLONASE nässpray, bör varje patients dos titreras till den lägsta dos som effektivt kontrollerar hans/hennes symtom.
En 1-årig placebokontrollerad studie genomfördes på 150 pediatriska försökspersoner (i åldern 3 till 9 år) för att bedöma effekten av FLONASE nässpray (enkel daglig dos på 200 mikrogram) på tillväxthastigheten. Från den primära populationen som fick FLONASE nässpray (n = 56) och placebo (n = 52), var punktuppskattningen för tillväxthastighet med FLONASE nässpray 50 mcg 0,14 cm/år lägre än placebo (95 % KI: -0,54, 0,27 cm) /år). Således noterades ingen statistiskt signifikant effekt på tillväxten jämfört med placebo. Inga tecken på kliniskt relevanta förändringar i HPA-axelns funktion eller bentäthet observerades enligt 12-timmars kortisolutsöndring i urin respektive dubbelenergi röntgenabsorptiometri.
Potentialen för FLONASE nässpray 50mcg att orsaka tillväxthämning hos känsliga patienter eller när det ges i högre än rekommenderade doser kan inte uteslutas.
Geriatrisk användning
Ett begränsat antal försökspersoner i åldern 65 år och äldre (n = 129) eller 75 år och äldre (n = 11) har behandlats med FLONASE nässpray i kliniska prövningar. Även om antalet försökspersoner är för litet för att tillåta separat analys av effekt och säkerhet, liknade de biverkningar som rapporterades i denna population de som rapporterats av yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktigt, vanligtvis med början i den nedre delen av doseringsintervallet, vilket återspeglar den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion, och av samtidig sjukdom eller annan läkemedelsbehandling.
Nedsatt leverfunktion
Formella farmakokinetiska prövningar med användning av FLONASE nässpray 50 mcg har inte utförts på patienter med nedsatt leverfunktion. Eftersom flutikasonpropionat huvudsakligen elimineras av levermetabolism, kan försämrad leverfunktion leda till ackumulering av flutikasonpropionat i plasma. Därför bör patienter med leversjukdom övervakas noggrant.

Nedsatt njurfunktion
Formella farmakokinetiska prövningar med användning av FLONASE nässpray har inte utförts på patienter med nedsatt njurfunktion.
ÖVERDOS
Kronisk överdosering kan resultera i tecken/symtom på hyperkorticism (se FÖRSIKTIGHETSÅTGÄRDER ). Intranasal administrering av 2 mg (10 gånger den rekommenderade dosen) flutikasonpropionat två gånger dagligen i 7 dagar till friska frivilliga försökspersoner tolererades väl. Enstaka orala doser upp till 16 mg har studerats på frivilliga försökspersoner utan några akuta toxiska effekter rapporterade. Upprepade orala doser upp till 80 mg dagligen i 10 dagar hos frivilliga och upprepade orala doser upp till 10 mg dagligen i 14 dagar hos patienter tolererades väl. Biverkningarna var av mild eller måttlig svårighetsgrad, och incidensen var likartad i aktiva och placebobehandlingsgrupper. Akut överdosering med denna beredningsform är osannolik eftersom 1 flaska FLONASE (flutikasonpropionat) nässpray innehåller cirka 8 mg flutikasonpropionat.
De orala och subkutana medianletala doserna hos möss och råttor var >1 000 mg/kg (>20 000 respektive >41 000 gånger den maximala rekommenderade dagliga intranasala dosen hos vuxna och >10 000 respektive >20 000 gånger den högsta rekommenderade dagliga intranasala dosen dos till barn på mg/m2-basis).
KONTRAINDIKATIONER
FLONASE (flutikasonpropionat) Nässpray är kontraindicerat för patienter med överkänslighet mot något av dess ingredienser.
KLINISK FARMAKOLOGI
Handlingsmekanism
Flutikasonpropionat är en syntetisk trifluorerad kortikosteroid med antiinflammatorisk aktivitet. Flutikasonpropionat har visat sig in vitro uppvisa en bindningsaffinitet för den humana glukokortikoidreceptorn som är 18 gånger så stor som för dexametason, nästan dubbelt så stor som beklometason-17-monopropionat (BMP), den aktiva metaboliten av beklometasondipropionat, och över 3 gånger så stor som av budesonid. Data från McKenzie vasokonstriktoranalysen på människa överensstämmer med dessa resultat. Den kliniska betydelsen av dessa fynd är okänd.
Den exakta mekanismen genom vilken flutikasonpropionat påverkar rinitsymptom är inte känd. Kortikosteroider har visat sig ha ett brett spektrum av effekter på flera celltyper (t.ex. mastceller, eosinofiler, neutrofiler, makrofager, lymfocyter) och mediatorer (t.ex. histamin, eikosanoider, leukotriener, cytokiner) involverade i inflammation. I 7 studier på vuxna har FLONASE nässpray minskat antalet eosinofiler i nässlemhinnan hos 66 % av patienterna (35 % för placebo) och basofiler hos 39 % av patienterna (28 % för placebo). Det direkta sambandet mellan dessa fynd och långvarig symtomlindring är inte känt.
Farmakodynamik
HPA-axeleffekt
De potentiella systemiska effekterna av FLONASE nässpray 50 mcg på HPA-axeln utvärderades. FLONASE Nässpray 50 mcg givet som 200 mcg en gång dagligen eller 400 mcg två gånger dagligen jämfördes med placebo eller oralt prednison 7,5 eller 15 mg givet på morgonen. FLONASE nässpray vid någon av doserna under 4 veckor påverkade inte binjuresvaret på 6-timmars cosyntropinstimulering, medan båda doserna av oralt prednison signifikant minskade svaret på cosyntropin.
Hjärtets elektrofysiologi
En studie speciellt utformad för att utvärdera effekten av FLONASE på QT-intervallet har inte utförts.
Farmakokinetik
Aktiviteten hos FLONASE Nasal Spray 50mcg beror på moderläkemedlet flutikasonpropionat. På grund av den låga biotillgängligheten via den intranasala vägen erhölls majoriteten av de farmakokinetiska data via andra administreringsvägar.
Absorption
Indirekta beräkningar indikerar att flutikasonpropionat som levereras intranasalt har en absolut biotillgänglighet på i genomsnitt mindre än 2 %. Försök med oral dosering av märkta och omärkta läkemedel har visat att den orala systemiska biotillgängligheten av flutikasonpropionat är försumbar (
Distribution
Efter intravenös administrering var den initiala dispositionsfasen för flutikasonpropionat snabb och förenlig med dess höga lipidlöslighet och vävnadsbindning. Distributionsvolymen var i genomsnitt 4,2 l/kg.
Andelen flutikasonpropionat bundet till humana plasmaproteiner var i genomsnitt 99 %. Flutikasonpropionat är svagt och reversibelt bundet till erytrocyter och är inte signifikant bundet till humant transkortin.
Eliminering
Efter intravenös dosering visade flutikasonpropionat polyexponentiell kinetik och hade en terminal halveringstid på cirka 7,8 timmar. Det totala blodclearancen av flutikasonpropionat är hög (genomsnitt: 1 093 ml/min), med njurclearance som utgör mindre än 0,02 % av det totala.
Ämnesomsättning: Den enda cirkulerande metaboliten som detekteras hos människa är 17β-karboxylsyraderivatet av flutikasonpropionat, som bildas genom CYP3A4-vägen. Denna metabolit hade mindre affinitet (ungefär 1/2 000) än moderläkemedlet för glukokortikoidreceptorn hos human lungcytosol in vitro och försumbar farmakologisk aktivitet i djurstudier. Andra metaboliter som upptäckts in vitro med användning av odlade humana hepatomceller har inte detekterats hos människa.
Exkretion: Mindre än 5 % av en radiomärkt oral dos utsöndrades i urinen som metaboliter, medan resten utsöndrades i feces som moderläkemedel och metaboliter.
Särskilda populationer
Flutikasonpropionat nässpray har inte studerats i några speciella populationer och inga könsspecifika farmakokinetiska data har erhållits.
Läkemedelsinteraktioner
Hämmare av Cytokrom P450 3A4: Ritonavir: Flutikasonpropionat är ett substrat för CYP3A4. Samtidig administrering av flutikasonpropionat och den starka CYP3A4-hämmaren, ritonavir, rekommenderas inte baserat på en multipeldos, korsad läkemedelsinteraktionsstudie på 18 friska försökspersoner. Flutikasonpropionat vattenhaltig nässpray (200 mcg en gång dagligen) administrerades samtidigt i 7 dagar med ritonavir (100 mg två gånger dagligen). Plasmakoncentrationer av flutikasonpropionat efter enbart vattenhaltig nässpray av flutikasonpropionat var odetekterbara (
Ketokonazol: Samtidig administrering av oralt inhalerat flutikasonpropionat (1 000 mcg) och ketokonazol (200 mg en gång dagligen) resulterade i en 1,9-faldig ökning av plasmaflutikasonpropionatexponeringen och en 45 % minskning av plasmakortisol AUC, men hade ingen effekt på urinutsöndringen av kortisol.
Erytromycin: I en läkemedelsinteraktionsstudie med flera doser påverkade inte samtidig administrering av oralt inhalerat flutikasonpropionat (500 mcg två gånger dagligen) och erytromycin (333 mg 3 gånger dagligen) farmakokinetiken för flutikasonpropionat.
PATIENTINFORMATION
FLONASE® [flow'naz] (flutikasonpropionat) Nässpray, 50 mcg
Läs patientinformationen som medföljer FLONASE nässpray innan du börjar använda den och varje gång du får påfyllning. Det kan komma ny information. Denna patientinformation ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling.
Vad är FLONASE nässpray?
FLONASE Nässpray 50mcg är ett receptbelagt läkemedel som används för att behandla icke-allergiska nässymtom som rinnande näsa, täppt näsa, nysningar och näsklåda hos vuxna och barn från 4 år och äldre.
Det är inte känt om FLONASE Nasal Spray 50mcg är säkert och effektivt för barn yngre än 4 år.
Vem bör inte använda FLONASE Nässpray 50mcg?
Använd inte FLONASE nässpray 50 mcg om du är allergisk mot flutikasonpropionat eller någon av ingredienserna i FLONASE nässpray. Se "Vilka är ingredienserna i FLONASE Nasal Spray 50mcg?" nedan för en komplett lista över ingredienser.
Vad ska jag berätta för min vårdgivare innan jag använder FLONASE Nasal Spray 50mcg?
Berätta för din vårdgivare om alla dina hälsotillstånd, inklusive om du:
- har eller har haft nässår, näsoperation eller nässkada.
- har ögonproblem, såsom grå starr eller glaukom.
- har problem med immunförsvaret.
- är allergiska mot någon av ingredienserna i FLONASE nässpray, andra läkemedel eller livsmedelsprodukter. Ser "Vilka är ingredienserna i FLONASE nässpray?" nedan för en komplett lista över ingredienser.
- har någon typ av virus-, bakterie- eller svampinfektion.
- utsätts för vattkoppor eller mässling.
- har andra medicinska tillstånd.
- är gravid eller planerar att bli gravid. Det är inte känt om FLONASE nässpray kan skada ditt ofödda barn.
- ammar eller planerar att amma. Det är inte känt om FLONASE Nässpray 50 mcg går över i din bröstmjölk och om det kan skada ditt barn.
Berätta för din vårdgivare om alla mediciner du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. FLONASE Nässpray och vissa andra läkemedel kan interagera med varandra. Detta kan orsaka allvarliga biverkningar. Särskilt tala om för din vårdgivare om du tar antimykotika eller anti-HIV-läkemedel.
Vet vilka mediciner du tar. Håll en lista över dem för att visa din vårdgivare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag använda FLONASE nässpray?
Läs steg-för-steg-instruktionerna för användning av FLONASE nässpray i slutet av denna patientinformation.
- FLONASE nässpray är endast för användning i näsan. Spraya det inte i dina ögon eller mun.
- Barn ska använda FLONASE nässpray med hjälp av en vuxen, enligt instruktioner från barnets vårdgivare.
- Använd FLONASE Nässpray 50mcg precis som din läkare säger till dig. Använd inte FLONASE nässpray oftare än föreskrivet.
- FLONASE Nässpray kan ta flera dagars regelbunden användning för att dina rinitsymptom ska bli bättre. Om dina symtom inte förbättras eller förvärras, ring din vårdgivare.
- Du kommer att få de bästa resultaten om du fortsätter att använda FLONASE nässpray regelbundet varje dag utan att missa en dos. När du börjar må bättre kan din läkare minska din dos. Låt bli sluta använda FLONASE Nasal Spray 50mcg om inte din läkare säger åt dig att göra det.
Vilka är de möjliga biverkningarna av FLONASE Nasal Spray 50mcg?
FLONASE Nässpray 50mcg kan orsaka allvarliga biverkningar, inklusive:
- näsa problem. Näsproblem kan innefatta:
- näsblod.
- sår (sår) i näsan.
- en viss svampinfektion i näsan, munnen och/eller halsen (trast).
- hål i brosket i näsan (perforering av nässeptum). Symtom på perforering av nässeptum kan inkludera:
- skorpa i näsan
- näsblod
- rinnande näsa
- ett visslande ljud när du andas
- långsam sårläkning. Du ska inte använda FLONASE nässpray förrän näsan har läkt om du har ett sår i näsan, har opererat näsan eller om näsan har skadats.
- ögonproblem inklusive glaukom och grå starr. Du bör göra regelbundna ögonundersökningar medan du använder FLONASE nässpray.
- allvarliga allergiska reaktioner. Ring din vårdgivare eller få akut medicinsk vård om du får något av följande tecken på en allvarlig allergisk reaktion:
- utslag
- nässelfeber
- svullnad av ditt ansikte, mun och tunga
- andningsproblem
- försvagat immunförsvar och ökad chans att få infektioner (immunsuppression). Att ta mediciner som försvagar ditt immunförsvar ökar risken för att du får infektioner och kan förvärra vissa infektioner. Dessa infektioner kan innefatta tuberkulos (TB), okulära herpes simplex-infektioner och infektioner orsakade av svampar, bakterier, virus och parasiter. Undvik kontakt med personer som har en smittsam sjukdom som vattkoppor eller mässling när du använder FLONASE nässpray. Om du kommer i kontakt med någon som har vattkoppor eller mässling, kontakta din vårdgivare direkt. Symtom på en infektion kan inkludera:
- feber
- känner mig trött
- smärta
- illamående
- värkar
- kräkningar
- frossa
- sänkta steroidhormonnivåer (binjurebarksvikt). Binjureinsufficiens uppstår när dina binjurar inte producerar tillräckligt med steroidhormoner. Detta kan hända när du slutar ta orala kortikosteroidläkemedel (som prednison) och börjar ta läkemedel som innehåller en inhalerad steroid (som FLONASE nässpray). Symtom på binjurebarksvikt kan inkludera:
- känner mig trött
- brist på energi
- svaghet
- illamående och kräkningar
- lågt blodtryck
- bromsad tillväxt hos barn. Ett barns tillväxt bör kontrolleras ofta.
De vanligaste biverkningarna av FLONASE Nasal Spray 50mcg inkluderar:
- huvudvärk
- illamående och kräkningar
- öm hals
- problem att andas
- näsblod
- hosta
- näsa brännande eller klåda
Berätta för din vårdgivare om eventuella biverkningar som stör dig eller inte försvinner.
Dessa är inte alla biverkningar med FLONASE nässpray. Fråga din vårdgivare eller apotekspersonal för mer information.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur förvarar jag FLONASE nässpray 50mcg?
- Förvara FLONASE mellan 39°F och 86°F (4°C och 30°C).
Förvara FLONASE Nässpray 50mcg och alla läkemedel utom räckhåll för barn.
Allmän information om säker och effektiv användning av FLONASE nässpray.
Läkemedel skrivs ibland ut för ändamål som inte nämns i en patientinformationsbroschyr. Använd inte FLONASE nässpray för ett tillstånd som det inte har ordinerats för. Ge inte din FLONASE nässpray till andra personer, även om de har samma tillstånd som du har. Det kan skada dem.
Denna patientinformationsbroschyr sammanfattar den viktigaste informationen om FLONASE nässpray. Om du vill ha mer information, prata med din vårdgivare. Du kan fråga din apotekspersonal eller vårdgivare om information om FLONASE nässpray som är skriven för vårdpersonal.
För mer information om FLONASE nässpray, ring 1-888-825-5249.
Vilka är ingredienserna i FLONASE Nasal Spray 50mcg?
Aktiv ingrediens: flutikasonpropionat.
Inaktiva ingredienser: mikrokristallin cellulosa, karboximetylcellulosanatrium, dextros, 0,02 % w/w bensalkoniumklorid, polysorbat 80 och 0,25 % w/w fenyletylalkohol.
Användningsinstruktioner
FLONASE® [flow'naz] (flutikasonpropionat) Nässpray, 50 mcg
FLONASE Nässpray 50mcg är endast för användning i näsan.
Läs denna information innan du börjar använda din FLONASE nässpray.
Delar av din FLONASE nässpray (Se bild A)
Bild A 
Din FLONASE Nässpray 50mcg måste förberedas innan du använder den för första gången och när du inte har använt den på en vecka eller mer.
Så här förbereder du din FLONASE nässpray
- Skaka flaskan försiktigt och ta sedan bort dammskyddet (se bild B).
Bild B 
- Håll flaskan som visas (se figur C) med näsapplikatorn pekande bort från dig och med pekfingret och långfingret på vardera sidan av näsapplikatorn och tummen under flaskan.
- Tryck ner och släpp 6 gånger tills en fin spray visas (se figur C). Pumpen är nu klar att användas.
Bild C 
Använd din FLONASE nässpray:
Steg 1 . Blås näsan för att rensa näsborrarna.
Steg 2 . Stäng 1 näsborre. Luta huvudet något framåt och håll flaskan upprätt och för försiktigt in näsapplikatorn i den andra näsborren (se figur D).
Bild D 
Steg 3 Börja andas in genom näsan och medan du andas in trycker du fast och snabbt ner applikatorn en gång för att släppa sprayen. För att få en full dos, använd pekfingret och långfingret för att spraya samtidigt som du stödjer flaskans bas med tummen. Undvik att spraya i ögonen. Andas in försiktigt genom näsborren (se figur E).
Bild E 
Steg 4 . Andas ut genom munnen.
Steg 5 . Om en andra spray behövs i den näsborren, upprepa steg 2 till 4.
Steg 6 . Upprepa steg 2 till 5 i den andra näsborren.
Steg 7 . Torka av näsapplikatorn med en ren väv och sätt tillbaka dammskyddet (se figur F).
Bild F 
Använd inte denna flaska för mer än det märkta antalet sprayer även om flaskan inte är helt tom. Innan du slänger flaskan bör du prata med din vårdgivare för att se om det behövs påfyllning. Ta inte extra doser eller sluta ta FLONASE Nässpray 50mcg utan att prata med din läkare.
Rengöring av din FLONASE nässpray:
Din nässpray ska rengöras minst 1 gång i veckan.
1. Ta bort dammskyddet och dra sedan försiktigt uppåt för att frigöra näsapplikatorn.
2. Tvätta applikatorn och dammskyddet under varmt kranvatten. Låt torka i rumstemperatur.
3. Sätt tillbaka applikatorn och dammskyddet på flaskan.
4. Om näsapplikatorn blir blockerad kan den tas bort och lämnas i blöt i varmt vatten. Skölj näsapplikatorn med kallt kranvatten. Torka näsapplikatorn och sätt tillbaka den på flaskan. Försök inte att låsa upp näsapplikatorn genom att sätta in en stift eller annat vasst föremål.
Förvara din FLONASE nässpray:
- Förvara FLONASE nässpray 50 mcg mellan 39°F och 86°F (4°C och 30°C).
- Använd inte din FLONASE nässpray efter det datum som anges som "EXP" på etiketten eller kartongen.
