Precose 25mg, 50mg Acarbose Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Precose 50mg och hur används det?
Precose (akarbostabletter) är en oral alfa-glukosidashämmare som används för att behandla typ 2-diabetes. Precose 50mg används ibland i kombination med insulin eller andra diabetesmediciner du tar via munnen. Precose 25mg finns i generisk form.
Vilka är biverkningarna av Precose 25mg?
Vanliga biverkningar av Precose inkluderar:
- diarre,
- gas,
- uppblåsthet,
- orolig mage, eller
- magsmärtor under de första veckorna av behandlingen eftersom din kropp anpassar sig till denna medicin men vanligtvis förbättras med tiden.
Andra biverkningar av Precose 50 mg inkluderar hudutslag eller klåda. Tala om för din läkare om du har sällsynta men mycket allvarliga biverkningar av Precose 25mg inklusive:
- ovanlig trötthet,
- ihållande illamående eller kräkningar,
- svår mag- eller buksmärta,
- rektal blödning,
- gulnande ögon eller hud, eller
- mörk urin.
BESKRIVNING
PRECOSE® (akarbostabletter) är en oral alfa-glukosidashämmare för användning vid behandling av typ 2-diabetes mellitus. Akarbos är en oligosackarid som erhålls från fermenteringsprocesser av en mikroorganism, Actinoplanes utahensis, och är kemiskt känd som O-4,6-dideoxi4-[[(1S,4R,5S,6S)-4,5,6-trihydroxi- 3-(hydroximetyl)-2-cyklohexen-l-yl]amino]a-D-glukopyranosyl-(1-→4)-0-a-D-glukopyranosyl-(1-→4)-D-glukos. Det är ett vitt till benvitt pulver med en molekylvikt på 645,6. Akarbos är lösligt i vatten och har ett pKa på 5,1. Dess empiriska formel är C25H43NO18 och dess kemiska struktur är som följer:
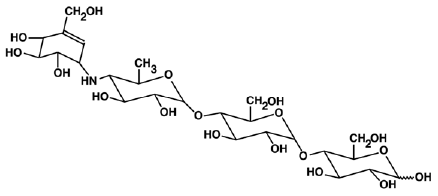
PRECOSE 50 mg finns som 25 mg, 50 mg och 100 mg tabletter för oral användning. De inaktiva ingredienserna är stärkelse, mikrokristallin cellulosa, magnesiumstearat och kolloidal kiseldioxid.
INDIKATIONER
PRECOSE är indicerat som ett komplement till kost och träning för att förbättra glykemisk kontroll hos vuxna med typ 2-diabetes mellitus.
DOSERING OCH ADMINISTRERING
Det finns ingen fast dosregim för behandling av diabetes mellitus med PRECOSE eller något annat farmakologiskt medel. Doseringen av PRECOSE 25 mg måste anpassas utifrån både effektivitet och tolerans, samtidigt som den rekommenderade maximala dosen på 100 mg inte överskrids. PRECOSE ska tas tre gånger dagligen i början (med första tuggan) av varje huvudmåltid.
PRECOSE bör startas med en låg dos, med gradvis dosökning enligt beskrivningen nedan, både för att minska gastrointestinala biverkningar och för att möjliggöra identifiering av den minsta dos som krävs för adekvat glykemisk kontroll av patienten. Om den föreskrivna kosten inte följs kan tarmbiverkningarna intensifieras. Om starkt plågsamma symtom utvecklas trots att den föreskrivna diabetiska dieten följs, måste läkare konsulteras och dosen tillfälligt eller permanent minskas.
Under behandlingsstart och dostitrering (se nedan), kan en timme postprandial plasmaglukos användas för att bestämma det terapeutiska svaret på PRECOSE och identifiera den minsta effektiva dosen för patienten. Därefter bör glykosylerat hemoglobin mätas med cirka tre månaders intervall. Det terapeutiska målet bör vara att sänka nivåerna av både postprandial plasmaglukos och glykosylerat hemoglobin till normala eller nära normala genom att använda den lägsta effektiva dosen av PRECOSE, antingen som monoterapi eller i kombination med sulfonylureider, insulin eller metformin.
Initial dosering
Den rekommenderade startdosen av PRECOSE 25 mg är 25 mg ges oralt tre gånger dagligen i början (med första tuggan) av varje huvudmåltid. Vissa patienter kan dock dra nytta av mer gradvis dostitrering för att minimera gastrointestinala biverkningar. Detta kan uppnås genom att påbörja behandlingen med 25 mg en gång per dag och därefter öka administreringsfrekvensen för att uppnå 25 mg tid.
Underhållsdosering
När en dos på 25 mg tre gånger har uppnåtts, bör dosen av PRECOSE 50 mg justeras med 4–8 veckors intervall baserat på en timme postprandiala glukos eller glykosylerat hemoglobinnivåer och på tolerans. Dosen kan ökas från 25 mg tid till 50 mg tid. Vissa patienter kan ha nytta av att ytterligare öka dosen till 100 mg tid. Underhållsdosen varierar från 50 mg tid till 100 mg tid. Men eftersom patienter med låg kroppsvikt kan ha ökad risk för förhöjda serumtransaminaser bör endast patienter med kroppsvikt > 60 kg övervägas för dostitrering över 50 mg tid (se FÖRSIKTIGHETSÅTGÄRDER ). Om ingen ytterligare minskning av postprandial glukos eller glykosylerat hemoglobinnivåer observeras med titrering till 100 mg tid, bör man överväga att sänka dosen. När en effektiv och tolererad dos har fastställts bör den bibehållas.
Maximal dosering
Den maximala rekommenderade dosen för patienter ≤ 60 kg är 50 mg tid. Den maximala rekommenderade dosen för patienter > 60 kg är 100 mg tid.
Patienter som får sulfonureider eller insulin
Sulfonylureamedel eller insulin kan orsaka hypoglykemi. PRECOSE givet i kombination med en sulfonylurea eller insulin kommer att orsaka en ytterligare sänkning av blodsockret och kan öka risken för hypoglykemi. Om hypoglykemi inträffar bör lämpliga justeringar av dosen av dessa medel göras.
HUR LEVERERAS
PRECOSE finns som 25 mg, 50 mg eller 100 mg runda tabletter utan skåror. Varje tablettstyrka är vit till gulfärgad. 25 mg tabletten är kodad med ordet "PRECOSE" på ena sidan och "25" på den andra sidan. Tabletten på 50 mg är kodad med orden "PRECOSE" och "50" på samma sida. 100 mg tabletten är kodad med orden "PRECOSE" och "100" på samma sida. PRECOSE finns i flaskor med styrkan 100 och 50 mg i endosförpackningar om 100.
Förvaras inte över 25°C (77°F). Skydda mot fukt. För flaskor, förvara behållaren väl tillsluten.
Bayer HealthCare Pharmaceuticals Inc. Wayne, NJ 07470. Tillverkad i Tyskland. 11/11
BIEFFEKTER
Matsmältningskanalen
Gastrointestinala symtom är de vanligaste reaktionerna på PRECOSE. I placebokontrollerade studier i USA var incidensen av buksmärtor, diarré och flatulens 19 %, 31 % respektive 74 % hos 1255 patienter som behandlades med PRECOSE 50–300 mg tid, medan motsvarande incidens var 9 %, 12 % och 29 % av 999 placebobehandlade patienter.
en ettårig säkerhetsstudie, under vilken patienter förde dagbok över gastrointestinala symtom, tenderade buksmärtor och diarréer att återgå till nivåerna före behandlingen med tiden, och frekvensen och intensiteten av flatulens tenderade att avta med tiden. De ökade symtomen i mag-tarmkanalen hos patienter som behandlas med PRECOSE 50 mg är en manifestation av verkningsmekanismen för PRECOSE och är relaterade till förekomsten av osmält kolhydrat i den nedre mag-tarmkanalen.
Om den föreskrivna kosten inte följs kan tarmbiverkningarna intensifieras. Om starkt plågsamma symtom utvecklas trots att den föreskrivna diabetiska dieten följs, måste läkare konsulteras och dosen tillfälligt eller permanent minskas.
Förhöjda serumtransaminasnivåer
Ser FÖRSIKTIGHETSÅTGÄRDER .
Andra onormala laboratoriefynd
Små minskningar av hematokrit inträffade oftare hos PRECOSE-behandlade patienter än hos placebobehandlade patienter, men var inte associerade med minskningar av hemoglobin. Låga serumkalciumnivåer och låga plasmanivåer av vitamin B6 var associerade med PRECOSE 50 mg-behandling men tros vara antingen falska eller utan klinisk betydelse.
Rapporter om biverkningar efter marknadsföring
Ytterligare biverkningar som rapporterats från världsomspännande erfarenheter efter marknadsföring inkluderar fulminant hepatit med dödlig utgång, överkänsliga hudreaktioner (till exempel hudutslag, erytem, exantem och utikaria), ödem, ileus/subileus, gulsot och/eller hepatit och tillhörande leverskador, trombocytopeni och pneumatos cystoides intestinalis (se FÖRSIKTIGHETSÅTGÄRDER ).
Pneumatosis Cystoides Intestinalis
Det har förekommit sällsynta rapporter efter marknadsföring av pneumatosis cystoides intestinalis i samband med användning av alfa-glukosidashämmare, inklusive Precose. Pneumatosis cystoides intestinalis kan uppvisa symtom på diarré, slemutsläpp, rektal blödning och förstoppning. Komplikationer kan inkludera pneumoperitoneum, volvulus, intestinal obstruktion, intussusception, intestinal blödning och tarmperforation. Om pneumatosis cystoides intestinalis misstänks, avbryt Precose 25mg och utför lämplig diagnostisk bildtagning.
LÄKEMEDELSINTERAKTIONER
Vissa läkemedel tenderar att producera hyperglykemi och kan leda till förlust av blodsockerkontrollen. Dessa läkemedel inkluderar tiazider och andra diuretika, kortikosteroider, fenotiaziner, sköldkörtelprodukter, östrogener, orala preventivmedel, fenytoin, nikotinsyra, sympatomimetika, kalciumkanalblockerande läkemedel och isoniazid. När sådana läkemedel administreras till en patient som får PRECOSE 25 mg, bör patienten observeras noga med avseende på förlust av blodsockerkontrollen. När sådana läkemedel tas ut från patienter som får PRECOSE 50 mg i kombination med sulfonylureider eller insulin, bör patienterna observeras noggrant med avseende på tecken på hypoglykemi.
Patienter som får sulfonureider eller insulin: Sulfonylureamedel eller insulin kan orsaka hypoglykemi. PRECOSE 25 mg givet i kombination med en sulfonylurea eller insulin kan orsaka en ytterligare sänkning av blodsockret och kan öka risken för hypoglykemi. Om hypoglykemi inträffar bör lämpliga justeringar av dosen av dessa medel göras. I mycket sällsynta fall har individuella fall av hypoglykemisk chock rapporterats hos patienter som fått PRECOSE-behandling i kombination med sulfonylureider och/eller insulin.
Intestinala adsorbenter (till exempel träkol) och matsmältningsenzympreparat som innehåller kolhydratspjälkande enzymer (till exempel amylas, pankreatin) kan minska effekten av PRECOSE och bör inte tas samtidigt.
PRECOSE 25 mg har visat sig förändra biotillgängligheten av digoxin när de administreras samtidigt, vilket kan kräva justering av digoxindosen. (Ser KLINISK FARMAKOLOGI , Läkemedelsinteraktioner .)
VARNINGAR
Ingen information lämnas
FÖRSIKTIGHETSÅTGÄRDER
Allmän
Makrovaskulära resultat
Det har inte gjorts några kliniska studier som har fastställt avgörande bevis för minskning av makrovaskulär risk med PRECOSE 25 mg eller något annat antidiabetiskt läkemedel.
Hypoglykemi
På grund av dess verkningsmekanism bör PRECOSE när det administreras ensamt inte orsaka hypoglykemi i fastande eller postprandialt tillstånd. Sulfonylureamedel eller insulin kan orsaka hypoglykemi. Eftersom PRECOSE 50 mg givet i kombination med en sulfonylurea eller insulin kommer att orsaka en ytterligare sänkning av blodsockret, kan det öka risken för hypoglykemi. Hypoglykemi förekommer inte hos patienter som får enbart metformin under vanliga användningsförhållanden, och ingen ökad incidens av hypoglykemi observerades hos patienter när PRECOSE 50 mg lades till metforminbehandling.
Oral glukos (dextros), vars absorption inte hämmas av PRECOSE, bör användas istället för sackaros (rörsocker) vid behandling av mild till måttlig hypoglykemi. Sackaros, vars hydrolys till glukos och fruktos hämmas av PRECOSE, är olämpligt för snabb korrigering av hypoglykemi. Allvarlig hypoglykemi kan kräva användning av antingen intravenös glukosinfusion eller glukagoninjektion.
Förhöjda serumtransaminasnivåer
långtidsstudier (upp till 12 månader, och inklusive PRECOSE 25 mg doser upp till 300 mg tid) utförda i USA, framkom behandlingsförhöjningar av serumtransaminaser (ASAT och/eller ALAT) över den övre normalgränsen (ULN) ), mer än 1,8 gånger ULN och mer än 3 gånger ULN inträffade hos 14 %, 6 % respektive 3 % av PRECOSE-behandlade patienter jämfört med 7 %, 2 % respektive 1 %, av placebobehandlade patienter. Även om dessa skillnader mellan behandlingar var statistiskt signifikanta, var dessa förhöjningar asymtomatiska, reversibla, vanligare hos kvinnor och var i allmänhet inte associerade med andra tecken på leverdysfunktion. Dessutom verkade dessa serumtransaminashöjningar vara dosrelaterade. I amerikanska studier inklusive PRECOSE 50 mg doser upp till den maximalt godkända dosen på 100 mg tid, var behandlingsuppkomna höjningar av ASAT och/eller ALAT, oavsett svårighetsgrad, likartade mellan PRECOSE-behandlade patienter och placebobehandlade patienter (p ≥ 0,496) .
Under cirka 3 miljoner patientår av internationell erfarenhet efter marknadsföring med PRECOSE 50 mg, har 62 fall av serumtransaminashöjningar > 500 IE/L (varav 29 associerade med gulsot) rapporterats. Fyrtioen av dessa 62 patienter fick behandling med 100 mg tid eller mer och 33 av 45 patienter för vilka vikt rapporterades vägde
Förlust av kontroll över blodsocker
När diabetespatienter utsätts för stress som feber, trauma, infektion eller operation, kan en tillfällig förlust av kontrollen över blodsockret uppstå. Vid sådana tillfällen kan tillfällig insulinbehandling vara nödvändig.
Laboratorietester
Terapeutisk respons på PRECOSE bör övervakas med regelbundna blodsockertest. Mätning av glykosylerade hemoglobinnivåer rekommenderas för övervakning av långvarig glykemisk kontroll.
PRECOSE 25 mg, särskilt vid doser över 50 mg tid, kan ge upphov till förhöjda serumtransaminaser och, i sällsynta fall, hyperbilirubinemi. Det rekommenderas att serumtransaminasnivåerna kontrolleras var tredje månad under det första behandlingsåret med PRECOSE och med jämna mellanrum därefter. Om förhöjda transaminaser observeras kan en minskning av dosen eller utsättande av behandlingen vara indicerat, särskilt om förhöjningarna kvarstår.
Nedsatt njurfunktion
Plasmakoncentrationer av PRECOSE hos frivilliga med nedsatt njurfunktion ökade proportionellt i förhållande till graden av nedsatt njurfunktion. Långtidsstudier på diabetespatienter med signifikant njurdysfunktion (serumkreatinin > 2,0 mg/dL) har inte utförts. Därför rekommenderas inte behandling av dessa patienter med PRECOSE 50 mg.
Karcinogenes, mutagenes och försämring av fertilitet
Åtta karcinogenicitetsstudier utfördes med akarbos. Sex studier utfördes på råttor (två stammar, Sprague-Dawley och Wistar) och två studier utfördes på hamstrar.
den första råttstudien fick Sprague-Dawley-råttor akarbos i foder i höga doser (upp till cirka 500 mg/kg kroppsvikt) under 104 veckor. Behandling med akarbos resulterade i en signifikant ökning av förekomsten av njurtumörer (adenom och adenokarcinom) och benigna Leydigcelltumörer. Denna studie upprepades med liknande resultat. Ytterligare studier utfördes för att separera direkta karcinogena effekter av akarbos från indirekta effekter till följd av kolhydratundernäring inducerad av de stora doser av akarbos som används i studierna. I en studie med Sprague-Dawley-råttor blandades akarbos med foder men kolhydratbrist förhindrades genom tillsats av glukos till kosten.

en 26-månaders studie av Sprague-Dawley-råttor administrerades akarbos genom daglig sondmatning efter måltid för att undvika de farmakologiska effekterna av läkemedlet. I båda dessa studier förekom inte den ökade förekomsten av njurtumörer som hittades i de ursprungliga studierna. Akarbos gavs också i mat och genom sondmatning efter måltid i två separata studier på Wistar-råttor. Ingen ökad förekomst av njurtumörer hittades i någon av dessa Wistar-råttstudier. I två utfodringsstudier av hamstrar, med och utan glukostillskott, fanns det heller inga tecken på cancerogenicitet.
Akarbos inducerade inte någon DNA-skada in vitro i CHO-kromosomavvikelseanalysen, bakteriell mutagenesanalys (Ames) eller en DNA-bindningsanalys. In vivo upptäcktes ingen DNA-skada i det dominanta dödliga testet hos möss av hankön eller mikrokärntestet på mus.
Fertilitetsstudier utförda på råttor efter oral administrering gav ingen ogynnsam effekt på fertiliteten eller på den totala förmågan att fortplanta sig.
Graviditet
Teratogena effekter: Graviditetskategori B.
Säkerheten för PRECOSE hos gravida kvinnor har inte fastställts. Reproduktionsstudier har utförts på råttor i doser upp till 480 mg/kg (motsvarande 9 gånger exponeringen hos människor, baserat på läkemedelsnivåer i blodet) och har inte visat några tecken på nedsatt fertilitet eller fostret skada på grund av akarbos. Hos kaniner kan minskad viktökning hos modern, troligen ett resultat av den farmakodynamiska aktiviteten av höga doser av akarbos i tarmarna, ha varit orsaken till en liten ökning av antalet embryonala förluster. Kaniner som fick 160 mg/kg akarbos (motsvarande 10 gånger dosen hos människa, baserat på kroppsyta) visade dock inga tecken på embryotoxicitet och det fanns inga tecken på teratogenicitet vid en dos som var 32 gånger dosen hos människa (baserat på kropp). ytarea). Det finns dock inga adekvata och välkontrollerade studier av PRECOSE 25 mg på gravida kvinnor. Eftersom reproduktionsstudier på djur inte alltid förutsäger det mänskliga svaret, bör detta läkemedel endast användas under graviditet om det verkligen behövs. Eftersom aktuell information starkt tyder på att onormala blodsockernivåer under graviditet är associerade med en högre förekomst av medfödda anomalier samt ökad neonatal sjuklighet och dödlighet, rekommenderar de flesta experter att insulin används under graviditeten för att hålla blodsockernivåerna så nära normala som möjligt. .
Ammande mödrar
En liten mängd radioaktivitet har hittats i mjölken från lakterande råttor efter administrering av radiomärkt akarbos. Det är inte känt om detta läkemedel utsöndras i modersmjölk. Eftersom många läkemedel utsöndras i bröstmjölk bör PRECOSE 25 mg inte ges till en ammande kvinna.
Pediatrisk användning
Säkerhet och effektivitet för PRECOSE 25 mg hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Av det totala antalet försökspersoner i kliniska studier med PRECOSE 25 mg i USA var 27 % 65 år och äldre, medan 4 % var 75 år och äldre. Inga övergripande skillnader i säkerhet och effektivitet observerades mellan dessa försökspersoner och yngre försökspersoner. Den genomsnittliga steady-state area under the curve (AUC) och maximala koncentrationer av akarbos var cirka 1,5 gånger högre hos äldre jämfört med unga frivilliga; dessa skillnader var dock inte statistiskt signifikanta.
ÖVERDOS
Till skillnad från sulfonylureider eller insulin kommer en överdos av PRECOSE inte att resultera i hypoglykemi. En överdos kan resultera i övergående ökningar av flatulens, diarré och bukbesvär som snart avtar. I fall av överdosering ska patienten inte ges drycker eller måltider som innehåller kolhydrater (polysackarider, oligosackarider och disackarider) under de kommande 4–6 timmarna.
KONTRAINDIKATIONER
PRECOSE 25mg är kontraindicerat hos patienter med känd överkänslighet mot läkemedlet. Precose 25 mg är kontraindicerat hos patienter med diabetisk ketoacidos eller cirros. PRECOSE 25mg är också kontraindicerat hos patienter med inflammatorisk tarmsjukdom, kolonsår, partiell tarmobstruktion eller hos patienter som är predisponerade för tarmobstruktion. Dessutom är PRECOSE kontraindicerat till patienter som har kroniska tarmsjukdomar associerade med markanta störningar i matsmältningen eller absorptionen och till patienter som har tillstånd som kan försämras till följd av ökad gasbildning i tarmen.
KLINISK FARMAKOLOGI
Akarbos är en komplex oligosackarid som fördröjer nedbrytningen av intagna kolhydrater, vilket resulterar i en mindre ökning av blodsockerkoncentrationen efter måltider. Som en konsekvens av plasmaglukosreduktionen, minskar PRECOSE nivåerna av glykosylerat hemoglobin hos patienter med typ 2-diabetes mellitus. Systemisk icke-enzymatisk proteinglykosylering, som återspeglas av nivåer av glykosylerat hemoglobin, är en funktion av genomsnittlig blodglukoskoncentration över tiden.
Handlingsmekanism
motsats till sulfonylureider ökar inte PRECOSE 50 mg insulinutsöndringen. Den antihyperglykemiska effekten av akarbos är resultatet av en kompetitiv, reversibel hämning av alfa-amylas i bukspottkörteln och membranbundna intestinala alfa-glukosidhydrolasenzymer. Pankreatisk alfa-amylas hydrolyserar komplex stärkelse till oligosackarider i tunntarmens lumen, medan de membranbundna intestinala alfa-glukosidaserna hydrolyserar oligosackarider, trisackarider och disackarider till glukos och andra monosackarider i tunntarmens gräns. Hos diabetespatienter resulterar denna enzymhämning i en försenad glukosabsorption och en sänkning av postprandial hyperglykemi.
Eftersom dess verkningsmekanism är annorlunda, är effekten av PRECOSE för att förbättra glykemisk kontroll additiv till effekten av sulfonylureider, insulin eller metformin när de används i kombination. Dessutom minskar PRECOSE 50 mg de insulinotropa och viktökande effekterna av sulfonylureider.
Akarbos har ingen hämmande aktivitet mot laktas och skulle följaktligen inte förväntas inducera laktosintolerans.
Farmakokinetik
Absorption
en studie av 6 friska män absorberades mindre än 2 % av en oral dos av akarbos som aktivt läkemedel, medan cirka 35 % av den totala radioaktiviteten från en 14C-märkt oral dos absorberades. I genomsnitt 51 % av en oral dos utsöndrades i avföringen som oabsorberad läkemedelsrelaterad radioaktivitet inom 96 timmar efter intag. Eftersom akarbos verkar lokalt i mag-tarmkanalen, är denna låga systemiska biotillgänglighet av moderföreningen terapeutiskt önskvärd. Efter oral dosering av friska frivilliga med 14C-märkt akarbos, uppnåddes maximala plasmakoncentrationer av radioaktivitet 14–24 timmar efter dosering, medan maximala plasmakoncentrationer av aktivt läkemedel uppnåddes efter cirka 1 timme. Den fördröjda absorptionen av akarbosrelaterad radioaktivitet återspeglar absorptionen av metaboliter som kan bildas av antingen tarmbakterier eller intestinal enzymatisk hydrolys.
Ämnesomsättning
Akarbos metaboliseras uteslutande i mag-tarmkanalen, främst av tarmbakterier, men även av matsmältningsenzymer. En del av dessa metaboliter (cirka 34 % av dosen) absorberades och utsöndrades därefter i urinen. Minst 13 metaboliter har separerats kromatografiskt från urinprover. De viktigaste metaboliterna har identifierats som 4-metylpyrogallolderivat (det vill säga sulfat-, metyl- och glukuronidkonjugat). En metabolit (bildad genom klyvning av en glukosmolekyl från akarbos) har också alfa-glukosidashämmande aktivitet. Denna metabolit, tillsammans med modersubstansen, som utvinns från urinen, står för mindre än 2 % av den totala administrerade dosen.
Exkretion
Den del av akarbos som absorberas som intakt läkemedel utsöndras nästan fullständigt av njurarna. När akarbos gavs intravenöst återfanns 89 % av dosen i urinen som aktivt läkemedel inom 48 timmar. Däremot återfanns mindre än 2 % av en oral dos i urinen som aktivt (det vill säga modersubstans och aktiv metabolit) läkemedel. Detta överensstämmer med moderläkemedlets låga biotillgänglighet. Halveringstiden för plasmaeliminering av akarbosaktivitet är cirka 2 timmar hos friska frivilliga. Följaktligen sker inte läkemedelsackumulering med tre gånger om dagen (tid) oral dosering.
Särskilda populationer
Den genomsnittliga steady-state area under the curve (AUC) och maximala koncentrationer av akarbos var cirka 1,5 gånger högre hos äldre jämfört med unga frivilliga; dessa skillnader var dock inte statistiskt signifikanta. Patienter med gravt nedsatt njurfunktion (Clcr
Läkemedelsinteraktioner
Studier på friska frivilliga har visat att PRECOSE inte har någon effekt på vare sig farmakokinetiken eller farmakodynamiken för nifedipin, propranolol eller ranitidin. PRECOSE störde inte absorptionen eller dispositionen av sulfonylureaglyburid hos diabetespatienter. PRECOSE kan påverka digoxins biotillgänglighet och kan kräva dosjustering av digoxin med 16 % (90 % konfidensintervall: 8-23 %), minska genomsnittlig Cmax för digoxin med 26 % (90 % konfidensintervall: 16–34 %) och sänka genomsnittligt dalvärde koncentrationer av digoxin med 9 % (90 % konfidensgräns: 19 % minskning till 2 % ökning). (Ser FÖRSIKTIGHETSÅTGÄRDER: LÄKEMEDELSINTERAKTIONER .)
Mängden metformin som absorberades när du tog PRECOSE var bioekvivalent med mängden som absorberades när du tog placebo, vilket indikeras av plasma-AUC-värden. Den maximala plasmanivån av metformin minskade dock med cirka 20 % när man tog PRECOSE på grund av en liten fördröjning i absorptionen av metformin. Det finns liten om någon kliniskt signifikant interaktion mellan PRECOSE och metformin.
Kliniska tester
Klinisk erfarenhet från dossökningsstudier på patienter med typ 2-diabetes mellitus som endast behandlas med diet
Resultat från sex kontrollerade, fasta doser, monoterapistudier av PRECOSE vid behandling av typ 2-diabetes mellitus, som involverade 769 PRECOSE-behandlade patienter, kombinerades och ett vägt genomsnitt av skillnaden från placebo i den genomsnittliga förändringen från baslinjen i glykosylerat hemoglobin ( HbA1c) beräknades för varje dosnivå enligt nedan:
Även om studier använde en maximal dos på 200 eller 300 mg tid, är den maximala rekommenderade dosen för patienter 60 kg är 100 mg tid
Resultaten från dessa sex monoterapistudier med fasta doser kombinerades också för att härleda ett vägt medelvärde av skillnaden från placebo i genomsnittlig förändring från baslinjen för en timme postprandiala plasmaglukosnivåer som visas i följande figur:
Figur 1 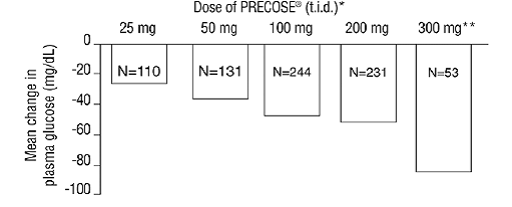
* PRECOSE 50 mg skilde sig statistiskt signifikant från placebo vid alla doser med avseende på effekt på en timme postprandial plasmaglukos. ** 300 mg tid PRECOSE 50 mg regimen var överlägsen lägre doser, men det fanns inga statistiskt signifikanta skillnader från 50 till 200 mg tid
Klinisk erfarenhet av typ 2-diabetes mellituspatienter på monoterapi eller i kombination med sulfonureider, metformin eller insulin
PRECOSE studerades som monoterapi och som kombinationsbehandling med sulfonylurea, metformin eller insulinbehandling. Behandlingseffekterna på HbA1c-nivåer och en timmes postprandiala glukosnivåer är sammanfattade för fyra placebokontrollerade, dubbelblinda, randomiserade studier utförda i USA i tabell 2 respektive 3. De placebo-subtraherade behandlingsskillnaderna, som sammanfattas nedan, var statistiskt signifikanta för båda variablerna i alla dessa studier.
Studie 1 (n=109) involverade patienter på bakgrundsbehandling med enbart diet. Den genomsnittliga effekten av tillägget av PRECOSE till dietbehandling var en förändring av HbA1c på -0,78 % och en förbättring av en timmes postprandial glukos på -74,4 mg/dL.
I studie 2 (n=137) var medeleffekten av tillägget av PRECOSE 25 mg till maximal sulfonylureabehandling en förändring i HbA1c på -0,54 % och en förbättring av en timmes postprandial glukos på -33,5 mg/dL.
studie 3 (n=147) var den genomsnittliga effekten av tillägg av PRECOSE 50 mg till maximal metforminbehandling en förändring av HbA1c på -0,65 % och en förbättring av en timmes postprandial glukos på -34,3 mg/dL.
Studie 4 (n=145) visade att PRECOSE tillsatt patienter på bakgrundsbehandling med insulin resulterade i en genomsnittlig förändring av HbA1c på -0,69 % och en förbättring av en timmes postprandial glukos på -36,0 mg/dL.
En ettårig studie av PRECOSE som monoterapi eller i kombination med sulfonylurea, metformin eller insulinbehandling genomfördes i Kanada där 316 patienter inkluderades i den primära effektanalysen (Figur 2). I diet-, sulfonylurea- och metformingrupperna var den genomsnittliga minskningen av HbA1c producerad genom tillsats av PRECOSE 50 mg statistiskt signifikant efter sex månader, och denna effekt var ihållande efter ett år. Hos de PRECOSE-behandlade patienterna på insulin fanns en statistiskt signifikant minskning av HbA1c efter sex månader och en trend mot en minskning efter ett år.
figur 2 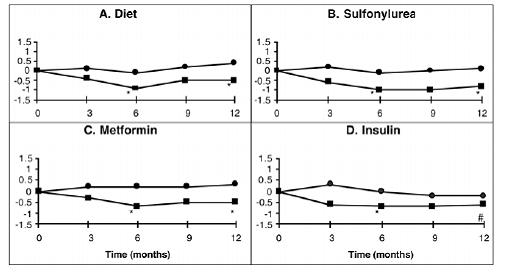
Figur 2: Effekter av PRECOSE (III) och Placebo (III) på genomsnittlig förändring av HbA1c-nivåer från baslinjen under en ettårig studie på patienter med typ 2-diabetes mellitus när de används i kombination med: (A) enbart diet; (B) sulfonylurea; (C) metformin; eller (D) insulin. Behandlingsskillnader efter 6 och 12 månader testades: * p
PATIENTINFORMATION
Patienterna ska uppmanas att ta PRECOSE 50 mg oralt tre gånger om dagen i början (med den första tuggan) av varje huvudmåltid. Det är viktigt att patienterna fortsätter att följa kostinstruktioner, ett regelbundet träningsprogram och regelbundna tester av urin och/eller blodsocker.
PRECOSE i sig orsakar inte hypoglykemi även när det ges till patienter i fastande tillstånd. Sulfonylurea-läkemedel och insulin kan dock sänka blodsockernivåerna tillräckligt för att orsaka symtom eller ibland livshotande hypoglykemi. Eftersom PRECOSE givet i kombination med en sulfonylurea eller insulin kommer att orsaka en ytterligare sänkning av blodsockret, kan det öka den hypoglykemiska potentialen hos dessa medel. Hypoglykemi förekommer inte hos patienter som får enbart metformin under vanliga användningsförhållanden, och ingen ökad incidens av hypoglykemi observerades hos patienter när PRECOSE lades till metforminbehandling. Risken för hypoglykemi, dess symtom och behandling samt tillstånd som predisponerar för dess utveckling bör förstås väl av patienter och ansvariga familjemedlemmar. Eftersom PRECOSE 50 mg förhindrar nedbrytningen av bordssocker, bör patienter ha en lättillgänglig källa till glukos (dextros, D-glukos) för att behandla symtom på lågt blodsocker när de tar PRECOSE i kombination med en sulfonylurea eller insulin.
Om biverkningar uppstår med PRECOSE utvecklas de vanligtvis under de första veckorna av behandlingen. De är oftast milda till måttliga gastrointestinala effekter, såsom flatulens, diarré eller bukbesvär, och avtar i allmänhet i frekvens och intensitet med tiden.
