Elocon 5g Mometasone Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Elocon 5g och hur används det?
Elocon (mometasonfuroat) kräm, 0,1 % är en topikal kräm, lotion eller salva för kortikosteroider indikerad för att lindra de inflammatoriska och klåda manifestationerna av kortikosteroidkänsliga dermatoser hos patienter som är 2 år eller äldre.
Vilka är biverkningarna av Elocon 5g?
Vanliga biverkningar av Elocon inkluderar:
- hudutslag,
- klåda,
- brinnande,
- rodnad,
- torrhet,
- tunnare eller mjukgörande av din hud,
- hudutslag eller irritation runt munnen,
- svullna hårsäckar,
- spindelådror,
- domningar eller stickningar,
- förändringar i färg på behandlad hud,
- blåsor,
- finnar,
- skorpbildning av behandlad hud, eller
- bristningar.
BESKRIVNING
ELOCON (mometasonfuroat) Kräm, 0,1 % innehåller mometasonfuroat för lokal användning. Mometasonfuroat är en syntetisk kortikosteroid med antiinflammatorisk aktivitet.
Kemiskt sett är mometasonfuroat 9α,21-diklor-11β,17-dihydroxi-16a-metylpregna-1,4-dien3,20-dion 17-(2-furoat), med den empiriska formeln C27 H30CI2O6, en molekylvikt på 521,4 och följande strukturformel:
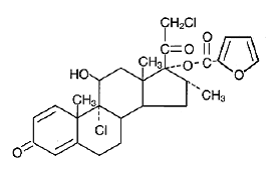
Mometasonfuroat är ett vitt till benvitt pulver som är praktiskt taget olösligt i vatten, något lösligt i oktanol och måttligt lösligt i etylalkohol.
Varje gram ELOCON 5g grädde, 0,1 % innehåller 1 mg mometasonfuroat i en vit till benvit krämbas av aluminiumstärkelseoktenylsuccinat (gamma bestrålad), hexylenglykol, hydrerat sojabönlecitin, fosforsyra, renat vatten, mjuk titandioxid, paraffin och vitt vax.
INDIKATIONER
ELOCON® Cream är en kortikosteroid indicerad för lindring av de inflammatoriska och klådande manifestationerna av kortikosteroidkänsliga dermatoser hos patienter som är 2 år eller äldre.
DOSERING OCH ADMINISTRERING
Applicera en tunn film av ELOCON Cream på de drabbade hudområdena en gång dagligen. ELOCON Cream kan användas till pediatriska patienter som är 2 år eller äldre. Eftersom säkerhet och effekt av ELOCON Cream inte har fastställts hos pediatriska patienter under 2 års ålder; användning i denna åldersgrupp rekommenderas inte [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER och Användning i specifika populationer ].
Behandlingen ska avbrytas när kontroll uppnåtts. Om ingen förbättring ses inom 2 veckor kan omprövning av diagnosen bli nödvändig. Säkerhet och effekt av ELOCON Cream hos pediatriska patienter under mer än 3 veckors användning har inte fastställts.
ELOCON Cream ska inte användas med ocklusiva förband såvida inte en läkare har ordinerat det. ELOCON 5g Cream ska inte appliceras i blöjområdet om barnet fortfarande behöver blöjor eller plastbyxor, eftersom dessa plagg kan utgöra ocklusiv förband.
ELOCON Cream är endast för lokal användning. Det är inte för oral, oftalmisk eller intravaginal användning.
Undvik användning i ansikte, ljumskar eller axiller.
HUR LEVERERAS
Doseringsformer och styrkor
Grädde, 0,1%. Varje gram ELOCON Cream innehåller 1 mg mometasonfuroat i en vit till benvit slät och homogen krämbas.
Förvaring Och Hantering
ELOCON kräm är vit till benvit till färgen och levereras i 15 gram (NDC 0085-3149-01) och 50 gram ( NDC 0085-3149-03) rör.
Förvara vid 25°C (77°F); utflykter tillåtna till 15-30°C (59-86°F) [se USP-kontrollerad rumstemperatur ]. Undvik överdriven värme.
Tillverkad för: Merck Sharp & Dohme Corp., ett dotterbolag till Merck & Co., Inc., Whitehouse Station, NJ 08889, USA. Tillverkad av: Schering-Plough Labo NV Heist-op-den-Berg, Belgien. Reviderad: april 2013
BIEFFEKTER
Eftersom kliniska prövningar genomförs under mycket varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i klinisk praxis.
I kontrollerade kliniska prövningar som involverade 319 försökspersoner var incidensen av biverkningar associerade med användning av ELOCON 5g Cream 1,6 %. Rapporterade reaktioner inkluderade sveda, klåda och hudatrofi. Rapporter om rosacea i samband med användningen av ELOCON 5g Cream har också inkommit. I kontrollerade kliniska prövningar (n=74) som involverade pediatriska försökspersoner i åldern 2 till 12 år var förekomsten av biverkningar i samband med användning av ELOCON 5g Cream cirka 7 %. Rapporterade reaktioner inkluderade sveda, klåda och furunkulos.
Följande biverkningar har rapporterats vara möjligen eller troligen relaterade till behandling med ELOCON 5g Cream under kliniska prövningar hos 4 % av 182 pediatriska försökspersoner i åldern 6 månader till 2 år: minskade glukokortikoidnivåer, 2; parestesi, 2; follikulit, 1; moniliasis, 1; bakteriell infektion, 1; huddepigmentering, 1. Följande tecken på hudatrofi observerades också bland 97 patienter som behandlats med ELOCON Cream i en klinisk prövning: glans, 4; telangiektasi, 1; förlust av elasticitet, 4; förlust av normala hudmärken, 4; tunnhet, 1; och blåmärken, 1.
Följande ytterligare lokala biverkningar har rapporterats med topikala kortikosteroider, men kan förekomma oftare vid användning av ocklusiva förband. Dessa reaktioner är: irritation, torrhet, follikulit, hypertrikos, acneiforma utbrott, hypopigmentering, perioral dermatit, allergisk kontaktdermatit, sekundär infektion, striae och miliaria.
LÄKEMEDELSINTERAKTIONER
Inga läkemedelsinteraktionsstudier har utförts med ELOCON Cream.
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Effekter på det endokrina systemet
Systemisk absorption av topikala kortikosteroider kan ge reversibel undertryckning av hypotalamus-hypofys-binjureaxeln (HPA) med risk för glukokortikosteroidinsufficiens. Detta kan inträffa under behandlingen eller efter att behandlingen avbryts. Manifestationer av Cushings syndrom, hyperglykemi och glukosuri kan också produceras hos vissa patienter genom systemisk absorption av topikala kortikosteroider under behandling. Faktorer som predisponerar en patient som använder en topikal kortikosteroid för HPA-axelsuppression inkluderar användningen av högpotenta steroider, stora behandlingsytor, långvarig användning, användning av ocklusiva förband, förändrad hudbarriär, leversvikt och ung ålder.
På grund av potentialen för systemisk absorption kan användning av topikala kortikosteroider kräva att patienterna utvärderas regelbundet för HPA-axelsuppression. Detta kan göras genom att använda stimuleringstestet för adrenokortikotropt hormon (ACTH).
I en studie som utvärderade effekterna av mometasonfuroatkräm på HPA-axeln applicerades 15 gram två gånger dagligen i 7 dagar på sex vuxna patienter med psoriasis eller atopisk dermatit. Resultaten visar att läkemedlet orsakade en lätt sänkning av binjurekortikosteroidsekretionen.
Om HPA-axelsuppression noteras, bör ett försök göras att gradvis dra ut läkemedlet, minska frekvensen av applicering eller att ersätta en mindre potent kortikosteroid. Återhämtning av HPA-axelns funktion sker i allmänhet omedelbart efter utsättning av topikala kortikosteroider. I sällsynta fall kan tecken och symtom på glukokortikosteroidinsufficiens förekomma, vilket kräver kompletterande systemiska kortikosteroider.
Pediatriska patienter kan vara mer mottagliga för systemisk toxicitet från ekvivalenta doser på grund av deras större förhållande mellan hudyta och kroppsmassa [se Användning i specifika populationer ].
Allergisk kontaktdermatit
Om irritation uppstår ska ELOCON Cream avbrytas och lämplig behandling inledas. Allergisk kontaktdermatit med kortikosteroider diagnostiseras vanligtvis genom att observera ett misslyckande att läka snarare än att notera en klinisk exacerbation som med de flesta topikala produkter som inte innehåller kortikosteroider. En sådan observation bör bekräftas med lämpliga diagnostiska lapptester.
Samtidiga hudinfektioner
Om samtidiga hudinfektioner förekommer eller utvecklas, bör ett lämpligt svampdödande eller antibakteriellt medel användas. Om ett gynnsamt svar inte uppstår omedelbart, bör användningen av ELOCON 5g Cream avbrytas tills infektionen har kontrollerats adekvat.

Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Långtidsstudier på djur har inte utförts för att utvärdera den cancerframkallande potentialen hos ELOCON 5g Cream. Långtidsstudier av karcinogenicitet av mometasonfuroat utfördes genom inhalation på råttor och möss. I en 2-årig karcinogenicitetsstudie på Sprague Dawley-råttor visade mometasonfuroat ingen statistiskt signifikant ökning av tumörer vid inhalationsdoser upp till 67 mcg/kg (ungefär 0,04 gånger den uppskattade maximala kliniska topiska dosen från ELOCON 5g kräm på en mcg/m²-basis ). I en 19-månaders karcinogenicitetsstudie på schweiziska CD-1 möss visade mometasonfuroat ingen statistiskt signifikant ökning av förekomsten av tumörer vid inhalationsdoser upp till 160 mikrogram/kg (ungefär 0,05 gånger den uppskattade maximala kliniska topiska dosen från ELOCON Cream på en mcg/m²).
Mometasonfuroat ökade kromosomavvikelser i en in vitro analys av äggstocksceller från kinesisk hamster, men ökade inte kromosomavvikelser i en lungcellsanalys av kinesisk hamster in vitro. Mometasonfuroat var inte mutagent i Ames-testet eller muslymfomanalysen och var inte klastogent i en in vivo-musmikronukleusanalys, en kromosomavvikelsetest för benmärg hos råtta eller en kromosomavvikelseanalys av manliga könsceller hos män. Mometasonfuroat inducerade inte heller oplanerad DNA-syntes in vivo i råtthepatocyter.
I reproduktionsstudier på råttor orsakades ingen försämring av fertiliteten hos han- eller honråttor genom subkutana doser upp till 15 mikrogram/kg (ungefär 0,01 gånger den uppskattade maximala kliniska topiska dosen från ELOCON 5g kräm, på mikrogram/m²).
Användning i specifika populationer
Graviditet
Fosterskadliga effekter - Graviditetskategori C
Det finns inga adekvata och välkontrollerade studier på gravida kvinnor. Därför ska ELOCON 5g Cream endast användas under graviditet om den potentiella nyttan motiverar den potentiella risken för fostret.
Kortikosteroider har visat sig vara teratogena hos laboratoriedjur när de administreras systemiskt i relativt låga dosnivåer. Vissa kortikosteroider har visat sig vara teratogena efter dermal applicering på laboratoriedjur.
Vid administrering till gravida råttor, kaniner och möss ökade mometasonfuroat fostermissbildningar. Doserna som gav missbildningar minskade också fostrets tillväxt, mätt som lägre fostervikt och/eller försenad förbening. Mometasonfuroat orsakade också dystoki och relaterade komplikationer när det administrerades till råttor under slutet av dräktigheten.
Hos möss orsakade mometasonfuroat gomspalt vid subkutana doser på 60 mcg/kg och högre. Fosteröverlevnaden minskade med 180 mcg/kg. Ingen toxicitet observerades vid 20 mcg/kg. (Doser på 20, 60 och 180 mcg/kg i musen är cirka 0,01, 0,02 och 0,05 gånger den uppskattade maximala kliniska topiska dosen från ELOCON Cream på en mcg/m²-basis.)
Hos råttor producerade mometasonfuroat navelbråck vid topiska doser på 600 mcg/kg och högre. En dos på 300 mcg/kg gav förseningar i ossifikationen, men inga missbildningar. (Doser på 300 och 600 mcg/kg hos råtta är ungefär 0,2 och 0,4 gånger den uppskattade maximala kliniska topiska dosen från ELOCON 5g Cream på en mcg/m² basis.)
Hos kaniner orsakade mometasonfuroat flera missbildningar (t.ex. böjda framtassar, gallblåsan, navelbråck, hydrocefali) vid topiska doser på 150 mcg/kg och över (ungefär 0,2 gånger den uppskattade maximala kliniska topiska dosen från ELOCON Cream på en mcg/mcg m²). I en oral studie ökade mometasonfuroat resorptionerna och orsakade gomspalt och/eller huvudmissbildningar (hydrocefali och välvt huvud) vid 700 mcg/kg. Vid 2800 mcg/kg avbröts eller resorberades de flesta kullarna. Ingen toxicitet observerades vid 140 mcg/kg. (Doser på 140, 700 och 2800 mcg/kg hos kanin är ungefär 0,2, 0,9 och 3,6 gånger den uppskattade maximala kliniska topiska dosen från ELOCON 5g Cream på en mcg/m²-basis.)
När råttor fick subkutana doser av mometasonfuroat under hela graviditeten eller under de senare stadierna av graviditeten orsakade 15 mikrogram/kg långvarig och svår förlossning och minskade antalet levande födda, födelsevikt och tidig överlevnad av valparna. Liknande effekter observerades inte vid 7,5 mikrogram/kg. (Doser på 7,5 och 15 mcg/kg i råtta är ungefär 0,005 och 0,01 gånger den uppskattade maximala kliniska topiska dosen från ELOCON Cream på en mcg/m² basis.)
Ammande mödrar
Systemiskt administrerade kortikosteroider förekommer i bröstmjölk och kan undertrycka tillväxten, störa endogen kortikosteroidproduktion eller orsaka andra ogynnsamma effekter. Det är inte känt om topikal administrering av kortikosteroider kan resultera i tillräcklig systemisk absorption för att producera detekterbara mängder i bröstmjölk. Eftersom många läkemedel utsöndras i bröstmjölk bör försiktighet iakttas när ELOCON 5g Cream ges till en ammande kvinna.
Pediatrisk användning
ELOCON Cream kan användas med försiktighet till pediatriska patienter som är 2 år eller äldre, även om säkerhet och effekt av läkemedelsanvändning i mer än 3 veckor inte har fastställts. Eftersom säkerhet och effekt av ELOCON 5g Cream inte har fastställts hos pediatriska patienter under 2 år, rekommenderas inte användning i denna åldersgrupp.
en pediatrisk studie behandlades 24 patienter med atopisk dermatit, varav 19 försökspersoner i åldern 2 till 12 år, med ELOCON Cream en gång dagligen. Majoriteten av försökspersonerna klarade sig inom 3 veckor. ELOCON 5g kräm orsakade HPA-axelsuppression hos cirka 16 % av pediatriska försökspersoner i åldrarna 6 till 23 månader, som visade normal binjurefunktion genom Cortrosyn-test innan behandlingen påbörjades, och behandlades i cirka 3 veckor under en medelkroppsyta på 41 % (intervall 15 %-94 %). Kriterierna för suppression var: basal kortisolnivå på ≤ 5 mcg/dL, 30-minuters efterstimuleringsnivå på ≤ 18 mcg/dL, eller en ökning med KLINISK FARMAKOLOGI ].
På grund av ett högre förhållande mellan hudyta och kroppsmassa löper pediatriska patienter en större risk än vuxna att drabbas av HPA-axelsuppression och Cushings syndrom när de behandlas med topikala kortikosteroider. De löper därför också större risk för binjurebarksvikt under och/eller efter utsättande av behandlingen. Pediatriska patienter kan vara mer mottagliga än vuxna för hudatrofi, inklusive striae, när de behandlas med topikala kortikosteroider. Pediatriska patienter som applicerar topikala kortikosteroider på mer än 20 % av kroppsytan löper högre risk att dämpa HPA-axeln.
HPA-axelsuppression, Cushings syndrom, linjär tillväxthämning, fördröjd viktökning och intrakraniell hypertoni har rapporterats hos pediatriska patienter som får topikala kortikosteroider. Manifestationer av binjuresuppression hos barn inkluderar låga plasmakortisolnivåer och frånvaro av svar på ACTH-stimulering. Manifestationer av intrakraniell hypertoni inkluderar utbuktande fontaneller, huvudvärk och bilateralt papillödem.
ELOCON Cream ska inte användas vid behandling av blöjeksem.
Geriatrisk användning
Kliniska studier av ELOCON 5g Cream inkluderade 190 försökspersoner som var 65 år och äldre och 39 försökspersoner som var 75 år och äldre. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre patienter, och annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. Större känslighet hos vissa äldre individer kan dock inte uteslutas.
ÖVERDOS
Topiskt applicerad ELOCON Cream kan absorberas i tillräckliga mängder för att ge systemiska effekter [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
KONTRAINDIKATIONER
Ingen.
KLINISK FARMAKOLOGI
Handlingsmekanism
Liksom andra topikala kortikosteroider har mometasonfuroat antiinflammatoriska, klådstillande och vasokonstriktiva egenskaper. Mekanismen för den antiinflammatoriska aktiviteten hos topikala steroider är i allmänhet oklar. Kortikosteroider tros emellertid verka genom induktion av fosfolipas A2-hämmande proteiner, gemensamt kallade lipokortiner. Det antas att dessa proteiner kontrollerar biosyntesen av potenta mediatorer av inflammation såsom prostaglandiner och leukotriener genom att hämma frisättningen av deras vanliga prekursor arakidonsyra. Arakidonsyra frisätts från membranfosfolipider av fosfolipas A2.
Farmakodynamik
Studier gjorda med ELOCON 5g Cream indikerar att den är i medelstor styrka jämfört med andra topikala kortikosteroider.
en studie som utvärderade effekterna av mometasonfuroatkräm på HPA-axeln applicerades 15 gram två gånger dagligen i 7 dagar på sex vuxna patienter med psoriasis eller atopisk dermatit. Krämen applicerades utan ocklusion på minst 30 % av kroppsytan. Resultaten visade att läkemedlet orsakade en lätt sänkning av binjurekortikosteroidsekretionen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Nittiosju pediatriska försökspersoner i åldrarna 6 till 23 månader med atopisk dermatit inkluderades i en öppen säkerhetsstudie på HPA-axeln. ELOCON Cream applicerades en gång dagligen i cirka 3 veckor över en genomsnittlig kroppsyta på 41% (intervall 15%-94%). Hos cirka 16 % av försökspersonerna som visade normal binjurefunktion genom Cortrosyn-test innan behandlingen påbörjades, observerades binjurebarkundertryckning i slutet av behandlingen med ELOCON 5g Cream. Kriterierna för suppression var: basal kortisolnivå på ≤ 5 mcg/dL, 30-minuters efterstimuleringsnivå på ≤ 18 mcg/dL, eller en ökning med Användning i specifika populationer ].
Farmakokinetik
Omfattningen av perkutan absorption av topikala kortikosteroider bestäms av många faktorer inklusive vehikeln och den epidermala barriärens integritet. Studier på människor indikerar att cirka 0,4 % av den applicerade dosen av ELOCON 5g Cream kommer in i cirkulationen efter 8 timmars kontakt med normal hud utan ocklusion. Inflammation och/eller andra sjukdomsprocesser i huden kan öka perkutan absorption.
Kliniska studier
Säkerheten och effekten av ELOCON 5g Cream för behandling av kortikosteroidkänsliga dermatoser utvärderades i två randomiserade, dubbelblinda, vehikelkontrollerade kliniska prövningar, en mot psoriasis och en mot atopisk dermatit. Totalt 366 försökspersoner (12-81 år), varav 177 fick ELOCON Cream och 181 försökspersoner fick vehikelkräm, utvärderades i dessa studier. ELOCON Cream eller fordonskrämen applicerades en gång dagligen i 21 dagar.
De två försöken visade att ELOCON 5g Cream är effektiv vid behandling av psoriasis och atopisk dermatit.
PATIENTINFORMATION
Informera patienter om följande:
- Använd ELOCON 5g Cream enligt anvisningar från läkaren. Den är endast för extern användning.
- Undvik kontakt med ögonen.
- Använd inte ELOCON Cream på ansikte, armhålor eller ljumskar såvida inte läkaren har ordinerat det.
- Använd inte ELOCON 5g Cream för någon annan sjukdom än den som den ordinerats för.
- Det behandlade hudområdet bör inte förbindas eller på annat sätt täckas eller lindas in så att det är ocklusivt, såvida inte läkaren bestämmer det.
- Rapportera alla tecken på lokala biverkningar till läkaren.
- Rekommendera patienter att inte använda ELOCON 5g Cream vid behandling av blöjeksem. Applicera inte ELOCON Cream i blöjområdet, eftersom blöjor eller plastbyxor kan utgöra ocklusiv förband.
- Avbryt behandlingen när kontroll uppnås. Om ingen förbättring ses inom 2 veckor, kontakta läkare.
- Använd inte andra kortikosteroidhaltiga produkter med ELOCON Cream utan att först rådgöra med läkaren.
