Microzide 25mg Hydrochlorothiazide Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Microzide 25mg och hur används det?
Microzide är ett receptbelagt läkemedel som används för att behandla symtom på högt blodtryck (hypertoni) och svullnad (ödem). Microzide kan användas ensamt eller tillsammans med andra läkemedel.
Microzide tillhör en klass av läkemedel som kallas diuretika, tiazid.
Det är inte känt om Microzide är säkert och effektivt för barn under 6 månaders ålder.
Vilka är de möjliga biverkningarna av Microzide?
Microzide kan orsaka allvarliga biverkningar inklusive:
- yrsel,
- ögonsmärta,
- synproblem,
- gulfärgning av huden eller ögonen (gulsot),
- blek hud,
- lätt att få blåmärken,
- ovanlig blödning (näsa, mun, slida eller ändtarm),
- andnöd,
- väsande andning,
- hosta med skummande slem,
- bröstsmärta,
- torr mun,
- törst,
- dåsighet,
- brist på energi,
- rastlöshet,
- muskelsmärta eller svaghet,
- snabb puls,
- illamående,
- kräkningar,
- lite eller ingen urin,
- feber,
- öm hals,
- svullnad i ansiktet eller tungan,
- brännande i ögonen, och
- hudsmärta följt av ett rött eller lila hudutslag som sprider sig (särskilt i ansiktet eller överkroppen) och orsakar blåsor och fjällning
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Microzide inkluderar:
- illamående,
- kräkningar,
- aptitlöshet,
- diarre,
- förstoppning,
- muskelspasm,
- yrsel och
- huvudvärk
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Microzide. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
MICROZIDE® (hydroklortiazid, USP 12,5 mg) är 3,4-dihydroderivatet av klortiazid. Dess kemiska namn är 6-klor-3,4-dihydro-2H-1,2,4-bensotiadiazin-7-sulfonamid 1,1-dioxid. Dess empiriska formel är C7H8CIN304S2; dess molekylvikt är 297,74; och dess strukturformel är:
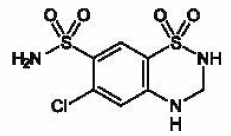
Det är ett vitt, eller praktiskt taget vitt, kristallint pulver som är svagt lösligt i vatten, men fritt lösligt i natriumhydroxidlösning.
MICROZIDE (hydroklortiazidkapsel) tillhandahålls som 12,5 mg kapslar för oral användning.
Inaktiva Ingredienser : kolloidal kiseldioxid, majsstärkelse, laktosmonohydrat, magnesiumstearat. Gelatinkapslar innehåller D&C Red No. 28, D&C Yellow No. 10, FD&C Blue No. 1, gelatin, titandioxid. Kapslarna är tryckta med ätbart bläck som innehåller svart järnoxid, D&C Yellow No. 10, FD&C Blue No. 1, FD&C Blue No. 2, FD&C Red No. 40.
INDIKATIONER
MICROZIDE (hydroklortiazidkapsel) är indicerat för behandling av hypertoni antingen som det enda terapeutiska medlet eller i kombination med andra antihypertensiva läkemedel. Till skillnad från kaliumsparande kombinationsdiuretika kan MICROZIDE (hydroklortiazidkapsel) användas till de patienter där utvecklingen av hyperkalemi inte kan riskeras, inklusive patienter som tar ACE-hämmare.
Användning under graviditet
Rutinmässig användning av diuretika hos en annars frisk kvinna är olämplig och utsätter mor och foster för onödiga faror. Diuretika förhindrar inte utvecklingen av toxemi vid graviditet, och det finns inga tillfredsställande bevis för att de är användbara vid behandling av utvecklad toxemi.
Ödem under graviditeten kan uppstå av patologiska orsaker eller från de fysiologiska och mekaniska konsekvenserna av graviditeten. Diuretika är indicerat under graviditet när ödem beror på patologiska orsaker, precis som de är i frånvaro av graviditet. Beroende ödem under graviditeten till följd av begränsning av venöst återflöde av den expanderade livmodern behandlas korrekt genom höjning av de nedre extremiteterna och användning av stödslang; användning av diuretika för att sänka intravaskulär volym i detta fall är ologiskt och onödigt. Det finns hypervolemi under normal graviditet som varken är skadlig för fostret eller modern (i avsaknad av hjärt-kärlsjukdom), men som är förknippad med ödem, inklusive generaliserat ödem hos majoriteten av gravida kvinnor. Om detta ödem ger obehag, ger ökad liggande ofta lindring. I sällsynta fall kan detta ödem orsaka extremt obehag som inte lindras av vila. I dessa fall kan en kort kur med diuretika ge lindring och kan vara lämplig.
DOSERING OCH ADMINISTRERING
För kontroll av hypertoni : Den initiala dosen för vuxna av MICROZIDE (hydroklortiazidkapsel) är en kapsel som ges en gång dagligen oavsett om den ges ensam eller i kombination med andra blodtryckssänkande medel. Totala dagliga doser större än 50 mg rekommenderas inte.
HUR LEVERERAS
MICROZIDE (hydroklortiazid kapsel) Kapslar är #4 Teal Opaque/Teal Opaque tvådelade hårda gelatinkapslar präglade med MICROZIDE (hydroklortiazidkapsel) och 12,5 mg i svart bläck. De levereras i flaskor om 100 st med barnsäkra förslutningar ( NDC 52544-622-01).
Dispensera i en tät, ljusbeständig behållare enligt definitionen i USP.
Förvara utom räckhåll för barn.
Förvara vid 20°-25°C (68°-77°F). [Se USP-kontrollerad rumstemperatur.] Skydda mot ljus, fukt, frysning, -20°C (-4°F). Förvara behållaren väl tillsluten.
Adressera medicinska förfrågningar till: WATSON., Medical Communications PO Box 1953, Morristown, NJ 07962-1953. 800-272-5525. Tillverkad av: Watson Pharma Private Limited. Verna, Salcette, Goa 403 722 INDIEN. Distribueras av: Watson Pharma, Inc. Morristown, NJ 07962 USA. Reviderad: februari 2011
BIEFFEKTER
Biverkningarna associerade med hydroklortiazid har visats vara dosrelaterade. I kontrollerade kliniska prövningar var de biverkningar som rapporterades med doser på 12,5 mg hydroklortiazid en gång dagligen jämförbara med placebo. Följande biverkningar har rapporterats för doser av hydroklortiazid 25 mg och mer och, inom varje kategori, är de listade efter fallande svårighetsgrad.
Kroppen som helhet : Svaghet.
Kardiovaskulär : Hypotoni inklusive ortostatisk hypotoni (kan förvärras av alkohol, barbiturater, narkotika eller antihypertensiva läkemedel).
Matsmältningskanalen Pankreatit, gulsot (intrahepatisk kolestatisk gulsot), diarré, kräkningar, sialadenit, kramper, förstoppning, magirritation, illamående, anorexi.
Hematologiska : Aplastisk anemi, agranulocytos, leukopeni, hemolytisk anemi, trombocytopeni.
Överkänslighet : Anafylaktiska reaktioner, nekrotiserande angiit (vaskulit och kutan vaskulit), andnöd inklusive pneumonit och lungödem, ljuskänslighet, feber, urtikaria, hudutslag, purpura.
Metabolisk : Elektrolytobalans (se FÖRSIKTIGHETSÅTGÄRDER ), hyperglykemi, glykosuri, hyperurikemi.
Muskuloskeletala : Muskelspasm.
Nervsystemet/Psykiatrisk : Vertigo, parestesi, yrsel, huvudvärk, rastlöshet.
Njur : Njursvikt, nedsatt njurfunktion, interstitiell nefrit (se VARNINGAR ).
Hud : Erythema multiforme inklusive Stevens-Johnsons syndrom, exfoliativ dermatit inklusive toxisk epidermal nekrolys, alopeci.
Särskilda sinnen Övergående dimsyn, xantopsi.
Urogenital : Impotens.
Närhelst biverkningarna är måttliga eller svåra, bör tiaziddoseringen minskas eller behandlingen sättas ut.
LÄKEMEDELSINTERAKTIONER
När de ges samtidigt kan följande läkemedel interagera med tiaziddiuretika:
Alkohol, barbiturater eller narkotika - Potentiering av ortostatisk hypotoni kan förekomma.
Antidiabetiska läkemedel - (orala medel och insulin) dosjustering av det antidiabetiska läkemedlet kan behövas.
Andra antihypertensiva läkemedel - additiv effekt eller potentiering.
Kolestyramin och kolestipolhartser – Kolestyramin- och kolestipolhartser binder hydroklortiaziden och minskar dess absorption från mag-tarmkanalen med upp till 85 respektive 43 procent.
Kortikosteroid, ACTH - intensifierad elektrolytförlust, särskilt hypokalemi.
Pressoraminer (t.ex. noradrenalin) - eventuellt minskat svar på pressoraminer men inte tillräckligt för att utesluta användningen av dem.
Skelettmuskelavslappnande medel, icke-depolariserande (t.ex. tubokurarin) möjlig ökad känslighet för muskelavslappnande medel.
Litium - bör i allmänhet inte ges tillsammans med diuretika. Diuretika minskar det renala clearance av litium och ökar kraftigt risken för litiumtoxicitet. Se bipacksedeln för litiumpreparat före användning av sådana preparat med MICROZIDE (hydroklortiazidkapsel).
Icke-steroida antiinflammatoriska läkemedel - Hos vissa patienter kan administrering av icke-steroida antiinflammatoriska medel minska de diuretiska, natriuretiska och antihypertensiva effekterna av loop-, kaliumsparande och tiaziddiuretika. När MICROZIDE (hydroklortiazidkapsel) och icke-steroida antiinflammatoriska medel används samtidigt, bör patienterna observeras noggrant för att avgöra om den önskade effekten av diuretikumet uppnås.
Interaktioner med läkemedel/laboratorietest
Tiazider bör avbrytas innan tester för bisköldkörtelfunktion utförs (se FÖRSIKTIGHETSÅTGÄRDER, Allmänt ).
VARNINGAR
Diabetes och hypoglykemi: Latent diabetes mellitus kan bli manifest och diabetiker som får tiazider kan behöva justera sin insulindos.
Njursjukdom: Kumulativa effekter av tiaziderna kan utvecklas hos patienter med nedsatt njurfunktion. Hos sådana patienter kan tiazider utlösa azotemi.
FÖRSIKTIGHETSÅTGÄRDER
Status för elektrolyt- och vätskebalans
I publicerade studier har kliniskt signifikant hypokalemi varit genomgående mindre vanlig hos patienter som fått 12,5 mg hydroklortiazid än hos patienter som fått högre doser. Icke desto mindre bör periodisk bestämning av serumelektrolyter utföras hos patienter som kan löpa risk att utveckla hypokalemi. Patienter bör observeras för tecken på vätske- eller elektrolytrubbningar, t.ex. hyponatremi, hypokloremisk alkalos och hypokalemi och hypomagnesemi.
Varningstecken eller symtom på vätske- och elektrolytobalans inkluderar muntorrhet, törst, svaghet, slöhet, dåsighet, rastlöshet, muskelsmärtor eller kramper, muskeltrötthet, hypotoni, oliguri, takykardi och gastrointestinala störningar såsom illamående och kräkningar.
Hypokalemi kan utvecklas, särskilt vid snabb diures när allvarlig cirros förekommer, vid samtidig användning av kortikosteroid eller adrenokortikotropt hormon (ACTH) eller efter långvarig behandling. Interferens med adekvat oralt elektrolytintag kommer också att bidra till hypokalemi. Hypokalemi och hypomagnesemi kan provocera fram ventrikulära arytmier eller sensibilisera eller överdriva hjärtats reaktion på de toxiska effekterna av digitalis. Hypokalemi kan undvikas eller behandlas genom tillskott av kalium eller ökat intag av kaliumrika livsmedel.
Utspädd hyponatremi är livshotande och kan förekomma hos ödematösa patienter i varmt väder; lämplig terapi är vattenbegränsning snarare än saltadministrering, förutom i sällsynta fall då hyponatremin är livshotande. Vid faktisk saltutarmning är lämplig ersättning den terapi man väljer.
Hyperurikemi
Hyperurikemi eller akut gikt kan utlösas hos vissa patienter som får tiaziddiuretika.
Nedsatt leverfunktion
Tiazider ska användas med försiktighet till patienter med nedsatt leverfunktion. De kan utlösa leverkoma hos patienter med allvarlig leversjukdom.
Parathyroid sjukdom
Kalciumutsöndring minskas av tiazider, och patologiska förändringar i bisköldkörtlarna, med hyperkalcemi och hypofosfatemi, har observerats hos ett fåtal patienter på långvarig tiazidbehandling.
Karcinogenes, Mutagenes, Nedsatt fertilitet
Tvååriga utfodringsstudier på möss och råttor utförda under överinseende av National Toxicology Program (NTP) avslöjade inga tecken på cancerframkallande potential hos hydroklortiazid hos möss av honkön (vid doser upp till cirka 600 mg/kg/dag) eller hos hanar. och honråttor (vid doser på cirka 100 mg/kg/dag). NTP fann dock tvetydiga bevis för hepatokarcinogenicitet hos möss av hankön. Hydroklortiazid var inte genotoxiskt in vitro i Ames mutagenicitetsanalysen av Salmonella typhimurium-stammarna TA 98, TA 100, TA 1535, TA 1537 och TA 1538 och i äggstockstestet för kinesisk hamster (CHO) för kromosomavvikelser med användning av vibrationer, eller könscellskromosomer från mus, benmärgskromosomer från kinesisk hamster och genen Drosophila könsbundna recessiva dödliga egenskaper. Positiva testresultat erhölls endast i in vitro CHO Sister Chromatid Exchange (klastogenicitet) och i muslymfomcellsanalyser (mutagenicitet), med användning av koncentrationer av hydroklortiazid från 43 till 1300 mcg/ml, och i Aspergillus nidulans icke-disjunktionsanalys kl. en ospecificerad koncentration.
Hydroklortiazid hade inga negativa effekter på fertiliteten hos möss och råttor av båda könen i studier där dessa arter exponerades, via sin diet, för doser på upp till 100 respektive 4 mg/kg, före befruktningen och under hela graviditeten.
Graviditet
Teratogena effekter
Graviditetskategori B: Studier där hydroklortiazid administrerades oralt till gravida möss och råttor under deras respektive perioder av större organogenes i doser upp till 3000 respektive 1000 mg hydroklortiazid/kg gav inga tecken på skada på fostret.
Det finns dock inga adekvata och välkontrollerade studier på gravida kvinnor. Eftersom reproduktionsstudier på djur inte alltid förutsäger mänskligt svar, bör detta läkemedel endast användas under graviditet om det verkligen behövs.
Icke-ratogena effekter
Tiazider passerar placentabarriären och uppträder i navelsträngsblod. Det finns risk för fetal eller neonatal gulsot, trombocytopeni och möjligen andra biverkningar som har inträffat hos vuxna.
Ammande mödrar
Tiazider utsöndras i bröstmjölk. På grund av risken för allvarliga biverkningar hos ammande spädbarn bör ett beslut fattas om att avbryta amningen eller att avbryta behandlingen med hydroklortiazid, med hänsyn till läkemedlets betydelse för modern.
Pediatrisk användning
Säkerhet och effektivitet hos pediatriska patienter har inte fastställts.
Användning för äldre
En större blodtryckssänkning och en ökning av biverkningar kan observeras hos äldre (dvs > 65 år) med hydroklortiazid. Därför rekommenderas att påbörja behandlingen med den lägsta tillgängliga dosen av hydroklortiazid (12,5 mg). Om ytterligare titrering krävs, bör steg om 12,5 mg användas.
ÖVERDOS
De vanligaste tecknen och symtomen som observeras är de som orsakas av elektrolytbrist (hypokalemi, hypokloremi, hyponatremi) och uttorkning till följd av överdriven diures. Om digitalis också har administrerats kan hypokalemi accentuera hjärtarytmier.
händelse av överdosering bör symtomatiska och stödjande åtgärder vidtas. Kräkning bör induceras eller magsköljning utföras. Korrigera uttorkning, elektrolytobalans, leverkoma och hypotoni genom etablerade procedurer. Vid behov, ge syrgas eller konstgjord andning vid andningsnedsättning. Graden i vilken hydroklortiazid avlägsnas genom hemodialys har inte fastställts.
Den orala LD50 för hydroklortiazid är högre än 10 g/kg hos mus och råtta.
KONTRAINDIKATIONER
Hydroklortiazid är kontraindicerat hos patienter med anuri. Överkänslighet mot denna produkt eller andra sulfonamidbaserade läkemedel är också kontraindicerat.
KLINISK FARMAKOLOGI
Hydroklortiazid blockerar reabsorptionen av natrium- och kloridjoner och ökar därigenom mängden natrium som passerar den distala tubuli och volymen vatten som utsöndras. En del av det ytterligare natrium som presenteras i distala tubuli byts ut där mot kalium- och vätejoner. Vid fortsatt användning av hydroklortiazid och utarmning av natrium tenderar kompensatoriska mekanismer att öka detta utbyte och kan ge överdriven förlust av kalium-, väte- och kloridjoner. Hydroklortiazid minskar också utsöndringen av kalcium och urinsyra, kan öka utsöndringen av jodid och kan minska glomerulär filtrationshastighet. Metaboliska toxiciteter associerade med överdrivna elektrolytförändringar orsakade av hydroklortiazid har visats vara dosrelaterade.
Farmakokinetik och metabolism
Hydroklortiazid absorberas väl (65 % till 75 %) efter oral administrering. Absorptionen av hydroklortiazid minskar hos patienter med kronisk hjärtsvikt.
Maximala plasmakoncentrationer observeras inom 1 till 5 timmar efter dosering och varierar från 70 till 490 ng/ml efter orala doser på 12,5 till 100 mg. Plasmakoncentrationerna är linjärt relaterade till den administrerade dosen. Koncentrationerna av hydroklortiazid är 1,6 till 1,8 gånger högre i helblod än i plasma. Bindning till serumproteiner har rapporterats vara cirka 40 % till 68 %. Halveringstiden för plasmaeliminering har rapporterats vara 6 till 15 timmar. Hydroklortiazid elimineras primärt via njurarna. Efter orala doser på 12,5 till 100 mg uppträder 55 % till 77 % av den administrerade dosen i urinen och mer än 95 % av den absorberade dosen utsöndras i urinen som oförändrat läkemedel. Hos patienter med njursjukdom ökar plasmakoncentrationerna av hydroklortiazid och eliminationshalveringstiden förlängs.
När MICROZIDE (hydroklortiazidkapsel) administreras tillsammans med mat minskar dess biotillgänglighet med 10 %, den maximala plasmakoncentrationen minskas med 20 % och tiden till maximal koncentration ökar från 1,6 till 2,9 timmar.
Farmakodynamik
Akuta antihypertensiva effekter av tiazider tros bero på en minskning av blodvolymen och hjärtminutvolymen, sekundärt till en natriuretisk effekt, även om en direkt vasodilaterande mekanism också har föreslagits. Vid kronisk administrering återgår plasmavolymen till det normala, men det perifera vaskulära motståndet minskar. Den exakta mekanismen för den antihypertensiva effekten av hydroklortiazid är inte känd.
Tiazider påverkar inte normalt blodtryck. Effekten börjar inom 2 timmar efter dosering, maximal effekt observeras efter cirka 4 timmar och aktiviteten kvarstår i upp till 24 timmar.
Kliniska studier
en 4-veckors dubbelblind, placebokontrollerad, parallell gruppstudie med 87 patienter, hade patienter som fick MICROZIDE (hydroklortiazidkapsel) sänkningar av sittande systoliska och diastoliska blodtryck som var signifikant högre än de som sågs hos patienter som fick placebo. I publicerade placebokontrollerade studier som jämförde 12,5 mg hydroklortiazid med 25 mg, bevarade dosen på 12,5 mg det mesta av den placebokorrigerade blodtryckssänkningen som sågs med 25 mg.
PATIENTINFORMATION
Ingen information lämnas. Vänligen se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER sektioner.
