Proscar 5mg Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Proscar 5mg och hur används det?
Proscar är ett receptbelagt läkemedel som används för att behandla symtom på benign prostatahyperplasi och androgen alopeci. Detta läkemedel är endast avsett för män. Proscar 5mg kan användas ensamt eller tillsammans med andra mediciner.
Proscar tillhör en klass av läkemedel som kallas 5-alfa-reduktashämmare.
Det är inte känt om Proscar 5mg är säkert och effektivt för barn.
Vilka är de möjliga biverkningarna av Proscar 5mg?
Proscar kan orsaka allvarliga biverkningar inklusive:
- allvarligt eller pågående illamående,
- svårt att andas,
- svullnad av ansikte, läppar, tunga eller svalg,
- bröstklumpar,
- bröstsmärtor eller ömhet,
- flytningar från bröstvårtan, och
- andra bröstförändringar
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Proscar inkluderar:
- förlorat intresse för sex,
- impotens,
- problem med att få orgasm, och
- onormal utlösning
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Proscar. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
PROSCAR (finasteride), en syntetisk 4-azasteroidförening, är en specifik hämmare av steroid typ II 5α-reduktas, ett intracellulärt enzym som omvandlar androgenet testosteron till 5α-dihydrotestosteron (DHT).
Finasterid är 4-azaandrost-1-en-17-karboxamid, N-(1,1-dimetyletyl)-3-oxo-,(5a,17ß)-. Den empiriska formeln för finasterid är C23H36N2O2 och dess molekylvikt är 372,55. Dess strukturformel är:
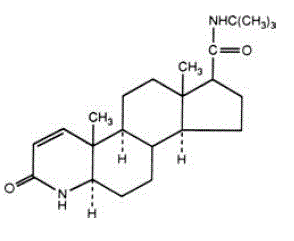
Finasteride är ett vitt kristallint pulver med en smältpunkt nära 250°C. Det är fritt lösligt i kloroform och i lägre alkohollösningsmedel, men är praktiskt taget olösligt i vatten.
PROSCAR (finasterid) tabletter för oral administrering är filmdragerade tabletter som innehåller 5 mg finasterid och följande inaktiva ingredienser: vattenhaltig laktos, mikrokristallin cellulosa, förgelatinerad stärkelse, natriumstärkelseglykolat, hydroxipropylcellulosa LF, hydroxipropylmetylcellulosa, titandioxid, magnesiumstearat , talk, docusate natrium, FD&C Blue 2 aluminium lake och gul järnoxid.
INDIKATIONER
Monoterapi
PROSCAR® är indicerat för behandling av symptomatisk benign prostatahyperplasi (BPH) hos män med förstorad prostata till:
- Förbättra symtomen
- Minska risken för akut urinretention
- Minska risken för behov av operation inklusive transuretral resektion av prostata (TURP) och prostatektomi.
Kombination med Alpha-Blocker
PROSCAR 5 mg administrerat i kombination med alfablockeraren doxazosin är indicerat för att minska risken för symtomatisk progression av BPH (en bekräftad ≥4 poängs ökning av symtompoängen hos American Urological Association (AUA).
Användningsbegränsningar
PROSCAR är inte godkänt för att förebygga prostatacancer.
DOSERING OCH ADMINISTRERING
PROSCAR kan administreras med eller utan måltider.
Monoterapi
Den rekommenderade dosen av PROSCAR är en tablett (5 mg) en gång om dagen [se Kliniska studier ].
Kombination med Alpha-Blocker
Den rekommenderade dosen av PROSCAR är en tablett (5 mg) som tas en gång om dagen i kombination med alfablockeraren doxazosin [se Kliniska studier ].
HUR LEVERERAS
Doseringsformer och styrkor
5-mg blå, modifierade äppelformade, filmdragerade tabletter, med koden MSD 72 på ena sidan och PROSCAR 5mg på den andra.
Förvaring Och Hantering
nr 3094 - PROSCAR tabletter 5 mg är blå, modifierade äppelformade, filmdragerade tabletter, med koden MSD 72 på ena sidan och PROSCAR på den andra. De levereras enligt följande:
NDC 0006-0072-31 flaskor med 30 användningsenheter NDC 0006-0072-58 användningsenhet flaskor med 100 st.
Förvaring Och Hantering
Förvara i rumstemperatur under 30°C (86°F). Skydda från ljus och håll behållaren väl tillsluten.
Kvinnor ska inte hantera krossade eller trasiga PROSCAR 5 mg tabletter när de är gravida eller kan vara gravida på grund av möjligheten till absorption av finasterid och den efterföljande potentiella risken för ett manligt foster [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER  och Användning i specifika populationer ].
Distribueras av: Merck Sharp & Dohme Corp., ett dotterbolag till MERCK & CO., INC., Whitehouse Station, NJ 08889, USA. Reviderad: juni 2021
BIEFFEKTER
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar genomförs under mycket varierande förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i de kliniska prövningarna av ett annat läkemedel och återspeglar kanske inte frekvensen som observerats i klinisk praxis.
4-årig placebokontrollerad studie (PLESS)
I PLESS utvärderades 1524 patienter behandlade med PROSCAR och 1516 patienter behandlade med placebo för säkerhet under en period av 4 år. De vanligaste rapporterade biverkningarna var relaterade till sexuell funktion. 3,7 % (57 patienter) som behandlades med PROSCAR 5 mg och 2,1 % (32 patienter) som behandlades med placebo avbröt behandlingen som ett resultat av biverkningar relaterade till sexuell funktion, vilka är de vanligast rapporterade biverkningarna.
Tabell 1 visar de enda kliniska biverkningar som prövaren ansåg vara möjligen, troligtvis eller definitivt läkemedelsrelaterade, för vilka incidensen på PROSCAR 5 mg var ≥1 % och högre än placebo under studiens 4 år. Under år 2-4 av studien fanns det ingen signifikant skillnad mellan behandlingsgrupperna i incidensen av impotens, minskad libido och ejakulationsstörning.
Fas III-studier och 5-åriga öppna förlängningar
Biverkningsprofilen i de 1-åriga, placebokontrollerade, fas III-studierna, de 5-åriga öppna förlängningarna och PLESS var likartade.
Studie om medicinsk terapi av prostatasymtom (MTOPS).
I MTOPS-studien randomiserades 3047 män med symtomatisk BPH till att få PROSCAR 5 mg/dag (n=768), doxazosin 4 eller 8 mg/dag (n=756), kombinationen av PROSCAR 5 mg/dag och doxazosin 4 eller 8 mg/dag (n=786), eller placebo (n=737) i 4 till 6 år. [Se en Kliniska studier .]
Incidensen av läkemedelsrelaterade biverkningar som rapporterats av ≥2 % av patienterna i någon behandlingsgrupp i MTOPS-studien listas i Tabell 2.
De individuella biverkningarna som uppträdde mer frekvent i kombinationsgruppen jämfört med var för sig var: asteni, postural hypotoni, perifert ödem, yrsel, minskad libido, rinit, onormal utlösning, impotens och onormal sexuell funktion (se tabell 2). Av dessa var förekomsten av onormal ejakulation hos patienter som fick kombinationsbehandling jämförbar med summan av incidensen av denna negativa upplevelse som rapporterats för de två monoterapierna.
Kombinationsbehandling med finasterid och doxazosin förknippades inte med några nya kliniska biverkningar.
Fyra patienter i MTOPS rapporterade den negativa upplevelsen av bröstcancer. Tre av dessa patienter fick endast finasterid och en fick kombinationsbehandling. [Se en Långtidsdata .]
MTOPS-studien var inte specifikt utformad för att göra statistiska jämförelser mellan grupper för rapporterade negativa upplevelser. Dessutom kan direkta jämförelser av säkerhetsdata mellan MTOPS-studien och tidigare studier av de enskilda medlen inte vara lämpliga baserat på skillnader i patientpopulation, dosering eller dosregim och andra procedur- och studiedesignelement.
Långtidsdata
Höggradig prostatacancer
PCPT-studien var en 7-årig randomiserad, dubbelblind, placebokontrollerad studie som inkluderade 18 882 män ≥55 år med en normal digital rektalundersökning och en PSA ≤3,0 ng/ml. Män fick antingen PROSCAR (finasterid 5 mg) eller placebo dagligen. Patienterna utvärderades årligen med PSA och digitala rektalundersökningar. Biopsier utfördes för förhöjd PSA, en onormal digital rektalundersökning eller slutet av studien. Incidensen av Gleason-poäng 8-10 prostatacancer var högre hos män som behandlades med finasterid (1,8 %) än hos de som behandlades med placebo (1,1 %) [se INDIKATIONER  och VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. I en 4-årig placebokontrollerad klinisk prövning med en annan 5α-reduktashämmare (dutasterid, AVODART) observerades liknande resultat för Gleason score 8-10 prostatacancer (1 % dutasterid mot 0,5 % placebo).
Ingen klinisk nytta har visats hos patienter med prostatacancer som behandlats med PROSCAR.
Bröstcancer
Under den 4- till 6-åriga placebo- och komparatorkontrollerade MTOPS-studien som omfattade 3047 män, fanns det 4 fall av bröstcancer hos män som behandlats med finasterid men inga fall hos män som inte behandlats med finasterid. Under den 4-åriga, placebokontrollerade PLESS-studien som inkluderade 3040 män, fanns det 2 fall av bröstcancer hos placebobehandlade män men inga fall hos män som behandlades med finasterid. Under den 7 år långa placebokontrollerade prostatacancerpreventionsprövningen (PCPT) som omfattade 18 882 män, var det 1 fall av bröstcancer hos män som behandlades med finasterid och 1 fall av bröstcancer hos män som behandlades med placebo. Förhållandet mellan långvarig användning av finasterid och manlig bröstneoplasi är för närvarande okänt.
Sexuell funktion
Det finns inga bevis för ökade sexuella biverkningar med ökad behandlingstid med PROSCAR. Nya rapporter om läkemedelsrelaterade sexuella biverkningar minskade med behandlingens varaktighet.
Erfarenhet efter marknadsföring
Följande ytterligare biverkningar har rapporterats efter marknadsföring av PROSCAR. Eftersom dessa händelser rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering:
- överkänslighetsreaktioner, såsom klåda, urtikaria och angioödem (inklusive svullnad av läppar, tunga, svalg och ansikte)
- testikulär smärta
- hematospermi
- sexuell dysfunktion som fortsatte efter avslutad behandling, inklusive erektil dysfunktion, minskad libido och ejakulationsrubbningar (t.ex. minskad ejakulationsvolym). Dessa händelser rapporterades sällan hos män som tog PROSCAR för behandling av BPH. De flesta män var äldre och tog samtidig medicinering och/eller hade samtidiga tillstånd. Den oberoende roll PROSCAR 5 mg spelar i dessa händelser är okänd.
- manlig infertilitet och/eller dålig sädeskvalitet rapporterades sällan hos män som tog PROSCAR 5 mg för behandling av BPH. Normalisering eller förbättring av dålig sädeskvalitet har rapporterats efter utsättande av finasterid. PROSCARs oberoende roll i dessa händelser är okänd.
- depression
- manlig bröstcancer.
Följande ytterligare biverkning relaterad till sexuell dysfunktion som fortsatte efter avslutad behandling har rapporterats efter marknadsföring med finasterid i lägre doser som används för att behandla skallighet hos män. Eftersom händelsen rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta dess frekvens eller fastställa ett orsakssamband till läkemedelsexponering:
- orgasmstörningar
LÄKEMEDELSINTERAKTIONER
Cytochrome P450-Linked Drug Metabolizing Enzyme System
Inga läkemedelsinteraktioner av klinisk betydelse har identifierats. Finasterid verkar inte påverka det cytokrom P450-kopplade läkemedelsmetaboliserande enzymsystemet. Föreningar som har testats på människa har inkluderat antipyrin, digoxin, propranolol, teofyllin och warfarin och inga kliniskt betydelsefulla interaktioner hittades.
Annan samtidig terapi
Även om specifika interaktionsstudier inte utfördes, användes PROSCAR 5 mg samtidigt i kliniska studier med paracetamol, acetylsalicylsyra, α-blockerare, angiotensin-konverterande enzym (ACE)-hämmare, analgetika, antikonvulsiva medel, beta-adrenerga blockerare, diuretika, kalcium. kanalblockerare, hjärtnitrater, HMG-CoA-reduktashämmare, icke-steroida antiinflammatoriska läkemedel (NSAID), bensodiazepiner, H2Â-antagonister och kinolon-anti-infektionsmedel utan bevis för kliniskt signifikanta negativa interaktioner.
VARNINGAR
Ingår som en del av "FÖRSIKTIGHETSÅTGÄRDER" Sektion
FÖRSIKTIGHETSÅTGÄRDER
Effekter på prostataspecifikt antigen (PSA) och användningen av PSA vid upptäckt av prostatacancer
kliniska studier minskade PROSCAR serum-PSA-koncentrationen med cirka 50 % inom sex månader efter behandling. Denna minskning är förutsägbar över hela intervallet av PSA-värden hos patienter med symtomatisk BPH, även om den kan variera hos individer.
För tolkning av seriella PSA hos män som tar PROSCAR bör en ny PSA-baslinje fastställas minst sex månader efter påbörjad behandling och PSA övervakas regelbundet därefter. Varje bekräftad ökning från det lägsta PSA-värdet under behandling med PROSCAR 5 mg kan signalera förekomst av prostatacancer och bör utvärderas, även om PSA-nivåerna fortfarande ligger inom det normala intervallet för män som inte tar en 5α-reduktashämmare. Bristande efterlevnad av PROSCAR-behandling kan också påverka PSA-testresultaten. För att tolka ett isolerat PSA-värde hos patienter som behandlats med PROSCAR 5 mg i sex månader eller mer, bör PSA-värdena fördubblas för jämförelse med normala intervall hos obehandlade män. Dessa justeringar bevarar användbarheten av PSA för att upptäcka prostatacancer hos män som behandlas med PROSCAR.
PROSCAR kan också orsaka minskningar av serum-PSA i närvaro av prostatacancer.
Förhållandet mellan fritt och totalt PSA (procent fritt PSA) förblir konstant även under påverkan av PROSCAR. Om läkare väljer att använda procent fritt PSA som ett hjälpmedel för att upptäcka prostatacancer hos män som genomgår finasteridbehandling verkar ingen justering av dess värde vara nödvändig.
Ökad risk för höggradig prostatacancer
Män från 55 år och äldre med en normal digital rektalundersökning och PSA ≤3,0 ng/ml vid baslinjen som tog finasterid 5 mg/dag i den 7-åriga prostatacancerpreventionsprövningen (PCPT) hade en ökad risk för Gleason-poäng 8-10 prostatacancer (finasterid 1,8 % vs placebo 1,1 %). [Se en INDIKATIONER  och NEGATIVA REAKTIONER .] Liknande resultat observerades i en 4-årig placebokontrollerad klinisk prövning med en annan 5α-reduktashämmare (dutasterid, AVODART) (1 % dutasterid mot 0,5 % placebo). 5α-reduktashämmare kan öka risken för utveckling av höggradig prostatacancer. Huruvida effekten av 5α-reduktashämmare för att minska prostatavolymen, eller studierelaterade faktorer, påverkade resultaten av dessa studier har inte fastställts.
Exponering Av Kvinnor
Risk för manligt foster
PROSCAR är kontraindicerat till gravida kvinnor och kvinnor som potentiellt kan vara gravida och inte indicerat för användning till kvinnor. Baserat på djurstudier och verkningsmekanismen kan PROSCAR 5mg orsaka onormal utveckling av yttre könsorgan hos ett manligt foster om det administreras till en gravid kvinna. Kvinnor som är gravida eller potentiellt kan vara gravida ska inte hantera krossade eller trasiga PROSCAR 5 mg tabletter. PROSCAR 5mg tabletter är belagda och kommer att förhindra kontakt med den aktiva ingrediensen under normal hantering, förutsatt att tabletterna inte har brutits eller krossats. Om en gravid kvinna kommer i kontakt med krossade eller trasiga PROSCAR 5mg tabletter, ska kontaktytan tvättas omedelbart med tvål och vatten. [Se en KONTRAINDIKATIONER , Användning i specifika populationer , KLINISK FARMAKOLOGI , och HUR LEVERERAS .]
Pediatriska Patienter Och Kvinnor
PROSCAR är inte indicerat för användning hos pediatriska patienter [se Användning i specifika populationer  och KLINISK FARMAKOLOGI ] eller honor [se även VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer , KLINISK FARMAKOLOGI , och HUR LEVERERAS ].
Effekt på spermaegenskaper
Behandling med PROSCAR under 24 veckor för att utvärdera spermaparametrar hos friska frivilliga manliga försökspersoner visade inga kliniskt betydelsefulla effekter på spermiekoncentration, rörlighet, morfologi eller pH. En medianminskning på 0,6 ml (22,1 %) av ejakulatvolymen med en åtföljande minskning av total sperma per ejakulat observerades. Dessa parametrar förblev inom det normala intervallet och var reversibla vid avbrytande av behandlingen med en genomsnittlig tid på 84 veckor att återgå till baslinjen.
Övervägande av andra urologiska tillstånd
Innan behandling med PROSCAR 5 mg påbörjas bör andra urologiska tillstånd som kan orsaka liknande symtom övervägas. Dessutom kan prostatacancer och BPH samexistera.
Patienter med stor kvarvarande urinvolym och/eller kraftigt minskat urinflöde bör övervakas noggrant med avseende på obstruktiv uropati. Dessa patienter kanske inte är kandidater för finasteridbehandling.
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION ).
Ökad risk för höggradig prostatacancer
Patienterna bör informeras om att det fanns en ökning av höggradig prostatacancer hos män som behandlats med 5α-reduktashämmare indikerade för BPH-behandling, inklusive PROSCAR 5 mg, jämfört med de som behandlades med placebo i studier som tittade på användningen av dessa läkemedel för att förhindra prostata cancer [se INDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , och NEGATIVA REAKTIONER ].
Exponering av honor - risk för manligt foster
Läkare bör informera patienter om att kvinnor som är gravida eller potentiellt kan vara gravida inte bör hantera krossade eller trasiga PROSCAR-tabletter på grund av möjligheten till absorption av finasterid och den efterföljande potentiella risken för det manliga fostret. PROSCAR tabletter är belagda och kommer att förhindra kontakt med den aktiva ingrediensen under normal hantering, förutsatt att tabletterna inte har brutits eller krossats. Om en kvinna som är gravid eller potentiellt kan vara gravid kommer i kontakt med krossade eller trasiga PROSCAR-tabletter, ska kontaktytan tvättas omedelbart med tvål och vatten [se KONTRAINDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer  och HUR LEVERERAS ].
Ytterligare instruktioner
Läkare bör informera patienter om att volymen av ejakulat kan minska hos vissa patienter under behandling med PROSCAR. Denna minskning verkar inte störa normal sexuell funktion. Emellertid kan impotens och minskad libido förekomma hos patienter som behandlas med PROSCAR [se NEGATIVA REAKTIONER ].
Läkare bör instruera sina patienter att omedelbart rapportera eventuella förändringar i deras bröst såsom knölar, smärta eller flytningar från bröstvårtan. Bröstförändringar inklusive bröstförstoring, ömhet och neoplasmer har rapporterats [se NEGATIVA REAKTIONER ].
Läkare bör instruera sina patienter att läsa patientbipacksedeln innan behandlingen med PROSCAR 5mg påbörjas och att läsa om den varje gång receptet förnyas så att de är medvetna om aktuell information för patienter om PROSCAR.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
Inga tecken på en tumörframkallande effekt observerades i en 24 månader lång studie på Sprague-Dawley-råttor som fick doser av finasterid upp till 160 mg/kg/dag hos hanar och 320 mg/kg/dag hos honor. Dessa doser gav en respektive systemisk exponering hos råttor på 111 och 274 gånger den som observerades hos människor som fick den rekommenderade dosen för människa på 5 mg/dag. Alla exponeringsberäkningar baserades på beräknad AUC(0-24 h) för djur och medel-AUC(0-24 h) för människa (0,4 μg•h/ml).
en 19-månaders karcinogenicitetsstudie på CD-1-möss observerades en statistiskt signifikant (p≤0,05) ökning av incidensen av testikel-Leydigcelladenom vid 228 gånger den mänskliga exponeringen (250 mg/kg/dag). Hos möss vid 23 gånger den mänskliga exponeringen, uppskattad (25 mg/kg/dag) och hos råttor vid 39 gånger den mänskliga exponeringen (40 mg/kg/dag) observerades en ökning av förekomsten av Leydig-cellshyperplasi. En positiv korrelation mellan de proliferativa förändringarna i Leydig-cellerna och en ökning av serum-LH-nivåer (2 till 3 gånger över kontroll) har visats hos båda gnagararterna som behandlats med höga doser finasterid. Inga läkemedelsrelaterade Leydig-cellförändringar sågs hos vare sig råttor eller hundar som behandlats med finasterid under 1 år vid 30 och 350 gånger (20 mg/kg/dag respektive 45 mg/kg/dag) eller hos möss som behandlats i 19 månader kl. 2,3 gånger den mänskliga exponeringen, uppskattad (2,5 mg/kg/dag).
Mutagenes
Inga tecken på mutagenicitet observerades i en bakteriell mutagenesanalys in vitro, en mutagenesanalys för däggdjursceller eller i en alkalisk elueringsanalys in vitro. I en in vitro-analys av kromosomavvikelser, med äggstocksceller från kinesisk hamster, var det en liten ökning av kromosomavvikelser. Dessa koncentrationer motsvarar 4000-5000 gånger de maximala plasmanivåerna hos människa med en total dos på 5 mg. I en in vivo-kromosomavvikelseanalys på möss observerades ingen behandlingsrelaterad ökning av kromosomavvikelsen med finasterid vid den maximalt tolererade dosen på 250 mg/kg/dag (228 gånger den mänskliga exponeringen) som fastställts i karcinogenicitetsstudierna.
Nedsättning av fertilitet
Hos könsmogna hankaniner behandlade med finasterid vid 543 gånger den mänskliga exponeringen (80 mg/kg/dag) i upp till 12 veckor sågs ingen effekt på fertilitet, spermieantal eller ejakulationsvolym. Hos könsmogna hanråttor som behandlats med 61 gånger den mänskliga exponeringen (80 mg/kg/dag), fanns det inga signifikanta effekter på fertiliteten efter 6 eller 12 veckors behandling; men när behandlingen fortsatte i upp till 24 eller 30 veckor, var det en uppenbar minskning av fertilitet, fruktsamhet och en tillhörande signifikant minskning av vikten av sädesblåsor och prostata. Alla dessa effekter var reversibla inom 6 veckor efter avslutad behandling. Ingen läkemedelsrelaterad effekt på testiklar eller på parningsprestanda har setts hos råttor eller kaniner. Denna minskning av fertiliteten hos finasteridbehandlade råttor är sekundär till dess effekt på accessoriska könsorgan (prostata och sädesblåsor) vilket resulterar i att en sädespropp inte bildas. Spädproppen är väsentlig för normal fertilitet hos råttor och är inte relevant hos människa.
Användning i specifika populationer
Graviditet
Risksammanfattning
PROSCAR är kontraindicerat till gravida kvinnor och inte indicerat för användning till kvinnor. Baserat på djurstudier och verkningsmekanismen kan PROSCAR 5mg orsaka onormal utveckling av yttre könsorgan hos ett manligt foster om det administreras till en gravid kvinna [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER  och KLINISK FARMAKOLOGI ].
I en embryo-fosterutvecklingsstudie på råttor, var det en dosberoende ökning av hypospadi som inträffade hos 3,6 till 100 % av manliga avkommor till dräktiga råttor som fick oral finasterid under perioden av större organogenes i doser på cirka 0,1 till 86 gånger det maximala rekommenderad humandos (MRHD) på 5 mg/dag (baserat på AUC vid djurdoser på 0,1 till 100 mg/kg/dag).
Minskade vikter av prostata och sädesblåsor, fördröjd preputial separation och övergående utveckling av bröstvårtan observerades också hos manliga avkommor vid orala maternala doser ungefär 0,03 gånger MRHD (baserat på AUC vid djurdos på 0,03 mg/kg/dag), tillsammans med minskat anogenitalt avstånd hos manliga avkommor vid orala maternala doser ungefär 0,003 gånger MRHD (baserat på AUC vid djurdos på 0,003 mg/kg/dag).
PROSCAR är en typ II 5α-reduktashämmare som förhindrar omvandling av testosteron till 5α-dihydrotestosteron (DHT), ett hormon som är nödvändigt för normal utveckling av manliga könsorgan. Om detta läkemedel används under graviditet, eller om patienten blir gravid medan du tar detta läkemedel, bör patienten informeras om den potentiella faran för det manliga fostret.
Onormal utveckling av manlig könsorgan är en förväntad konsekvens när omvandling av testosteron till 5α-dihydrotestosteron (DHT) hämmas av 5α-reduktashämmare. Dessa resultat liknar de som rapporterats hos manliga spädbarn med genetisk 5α-reduktasbrist. Kvinnor kan exponeras för finasterid genom kontakt med krossade eller trasiga PROSCAR-tabletter eller sperma från en manlig partner som tar PROSCAR. När det gäller finasteridexponering genom huden är PROSCAR 5mg tabletter belagda och kommer att förhindra hudkontakt med finasterid under normal hantering om tabletterna inte har krossats eller brutits. Kvinnor som är gravida eller potentiellt kan vara gravida ska inte hantera krossade eller trasiga PROSCAR 5 mg tabletter på grund av möjlig exponering av ett manligt foster. När det gäller potentiell finasteridexponering genom sperma har tre studier genomförts som mätte finasteridkoncentrationer i sperma hos män som fick PROSCAR 5 mg/dag. I dessa studier uppskattades den högsta mängden finasterid i sperma vara 50 till 100 gånger mindre än dosen finasterid (5 μg) som inte hade någon effekt på cirkulerande DHT-nivåer hos män [se Data  och KLINISK FARMAKOLOGI ].
Data
Mänskliga data
2 studier på friska försökspersoner (n=69) som fick PROSCAR 5 mg/dag i 6-24 veckor varierade finasteridkoncentrationerna i sperma från odetekterbar ( KLINISK FARMAKOLOGI ].
Djurdata
en embryo-fosterutvecklingsstudie fick gravida råttor finasterid under perioden av större organogenes (dräktighetsdagar 6 till 17). Vid moderns doser av oral finasterid cirka 0,1 till 86 gånger den maximala rekommenderade humana dosen (MRHD) på 5 mg/dag (baserat på AUC vid djurdoser på 0,1 till 100 mg/kg/dag) fanns en dosberoende ökning av hypospadi som förekom hos 3,6 till 100 % av manliga avkommor. Exponeringsmultiplar uppskattades med hjälp av data från icke-gravida råttor. Dag 16 till 17 av dräktigheten är en kritisk period hos fosterhanråttor för differentiering av de yttre könsorganen. Vid orala maternala doser ungefär 0,03 gånger MRHD (baserat på AUC vid djurdos på 0,03 mg/kg/dag), hade manliga avkommor minskade prostata- och sädesblåsorvikter, försenad preputial separation och övergående bröstvårtor. Minskat anogenitalt avstånd inträffade hos hanavkommor till dräktiga råttor som fick cirka 0,003 gånger MRHD (baserat på AUC vid en djurdos på 0,003 mg/kg/dag). Inga abnormiteter observerades hos kvinnliga avkommor vid någon modern dos av finasterid.
Inga utvecklingsavvikelser observerades hos avkommor till obehandlade honor som parades med finasteridbehandlade råttor av hankön som fick cirka 61 gånger MRHD (baserat på AUC vid djurdos på 80 mg/kg/dag). Något minskad fertilitet observerades hos hanavkommor efter administrering av cirka 3 gånger MRHD (baserat på AUC vid djurdos på 3 mg/kg/dag) till honråttor under sen dräktighet och laktation. Inga effekter på fertiliteten sågs hos kvinnliga avkommor under dessa förhållanden.
Inga tecken på yttre genitalmissbildningar hos män eller andra abnormiteter observerades hos kaninfoster som exponerats för finasterid under perioden av större organogenes (dräktighetsdagar 6-18) vid moderns orala doser upp till 100 mg/kg/dag (exponeringsnivåerna för finasterid var inte mätt i kaniner). Denna studie kanske inte har inkluderat den kritiska perioden för finasterideffekter på utvecklingen av manliga yttre könsorgan hos kanin.
Fostereffekterna av moderns finasteridexponering under perioden för embryonal och fosterutveckling utvärderades hos rhesusapa (dräktighetsdagar 20-100), i en art- och utvecklingsperiod som mer förutsäger specifika effekter hos människor än studierna på råttor och kaniner. Intravenös administrering av finasterid till gravida apor i doser så höga som 800 ng/dag (uppskattad maximal blodkoncentration på 1,86 ng/ml eller cirka 143 gånger den högsta uppskattade exponeringen av gravida kvinnor för finasterid från sperma från män som tog 5 mg/dag) resulterade i inga avvikelser hos manliga foster. Som bekräftelse på relevansen av rhesusmodellen för mänsklig fosterutveckling, oral administrering av en dos finasterid (2 mg/kg/dag eller cirka 18 000 gånger de högsta uppskattade blodnivåerna av finasterid från sperma från män som tar 5 mg/dag) till gravida apor resulterade i yttre genitalavvikelser hos manliga foster. Inga andra abnormiteter observerades hos manliga foster och inga finasteridrelaterade abnormiteter observerades hos kvinnliga foster vid någon dos.
Laktation
Risksammanfattning
PROSCAR är inte indicerat för användning till kvinnor.
Kvinnor Och Hanar Av Reproduktionspotential
Infertilitet
Kvinnor
PROSCAR är inte indicerat för användning till kvinnor.
Män
Behandling med PROSCAR under 24 veckor för att utvärdera spermaparametrar hos friska frivilliga manliga försökspersoner visade inga kliniskt betydelsefulla effekter på spermiekoncentration, rörlighet, morfologi eller pH. En medianminskning på 0,6 ml (22,1 %) av ejakulatvolymen med en åtföljande minskning av total sperma per ejakulat observerades. Dessa parametrar höll sig inom det normala intervallet och var reversibla vid avbrytande av behandlingen med en genomsnittlig tid på 84 veckor för att återgå till baslinjen [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Det har förekommit rapporter efter marknadsföring av manlig infertilitet och/eller dålig sädeskvalitet; normalisering eller förbättring av sädeskvaliteten har rapporterats efter avslutad behandling med finasterid [se NEGATIVA REAKTIONER ].
Pediatrisk användning
PROSCAR 5mg är inte indicerat för användning till pediatriska patienter.
Säkerhet och effektivitet hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Av det totala antalet försökspersoner som ingick i PLESS var 1480 och 105 försökspersoner 65 respektive över och 75 respektive över. Inga övergripande skillnader i säkerhet eller effektivitet observerades mellan dessa försökspersoner och yngre patienter, och annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. Ingen dosjustering är nödvändig hos äldre [se KLINISK FARMAKOLOGI  och Kliniska studier ].
Nedsatt leverfunktion
Försiktighet bör iakttas vid administrering av PROSCAR till patienter med leverfunktionsavvikelser, eftersom finasterid metaboliseras i stor utsträckning i levern [se KLINISK FARMAKOLOGI ].
Nedsatt njurfunktion
Ingen dosjustering är nödvändig hos patienter med nedsatt njurfunktion [se KLINISK FARMAKOLOGI ].
ÖVERDOS
Patienter har fått engångsdoser av PROSCAR 5 mg upp till 400 mg och flera doser av PROSCAR 5 mg upp till 80 mg/dag i tre månader utan biverkningar. Tills ytterligare erfarenhet erhållits kan ingen specifik behandling för en överdos med PROSCAR rekommenderas.
Signifikant dödlighet observerades hos han- och honmöss vid orala enstaka doser på 1500 mg/m2 (500 mg/kg) och hos hon- och hanråttor vid orala enstaka doser på 2360 mg/m2 (400 mg/kg) och 5900 mg/m2 (1000 mg/kg).
KONTRAINDIKATIONER
PROSCAR är kontraindicerat i följande:
- Överkänslighet mot någon komponent i detta läkemedel.
- Graviditet. Användning av Finasteride är kontraindicerat hos kvinnor när de är eller kan vara gravida. På grund av förmågan hos typ II 5α-reduktashämmare att hämma omvandlingen av testosteron till 5α-dihydrotestosteron (DHT), kan finasterid orsaka abnormiteter i de yttre könsorganen hos ett manligt foster hos en gravid kvinna som får finasterid. Om detta läkemedel används under graviditet, eller om graviditet inträffar medan du tar detta läkemedel, bör den gravida kvinnan informeras om den potentiella faran för det manliga fostret. [Se även VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer , och HUR LEVERERAS .] Hos honråttor har låga doser finasterid administrerade under graviditeten orsakat abnormiteter i de yttre könsorganen hos manliga avkommor.
KLINISK FARMAKOLOGI
Handlingsmekanism
Utvecklingen och förstoringen av prostatakörteln är beroende av den potenta androgenen, 5α-dihydrotestosteron (DHT). Typ II 5α-reduktas metaboliserar testosteron till DHT i prostatakörteln, levern och huden. DHT inducerar androgena effekter genom att binda till androgenreceptorer i cellkärnorna i dessa organ.
Finasteride är en kompetitiv och specifik hämmare av typ II 5α-reduktas med vilken den långsamt bildar ett stabilt enzymkomplex. Omsättningen från detta komplex är extremt långsam (t½ ∼ 30 dagar). Detta har visats både in vivo och in vitro. Finasterid har ingen affinitet för androgenreceptorn. Hos människa minskar de 5α-reducerade steroidmetaboliterna i blod och urin efter administrering av finasterid.
Farmakodynamik
Hos människa ger en oral engångsdos på 5 mg PROSCAR en snabb minskning av serumkoncentrationen av DHT, med maximal effekt observerad 8 timmar efter den första dosen. Undertryckandet av DHT upprätthålls under hela 24-timmars doseringsintervallet och med fortsatt behandling. Daglig dosering av PROSCAR med 5 mg/dag i upp till 4 år har visat sig minska DHT-koncentrationen i serum med cirka 70 %. Den genomsnittliga cirkulerande nivån av testosteron ökade med cirka 10-20% men förblev inom det fysiologiska intervallet. I en separat studie på friska män som behandlades med finasterid 1 mg per dag (n=82) eller placebo (n=69), ökade de genomsnittliga cirkulerande nivåerna av testosteron och östradiol med cirka 15 % jämfört med baslinjen, men dessa förblev inom fysiologiskt område.
Hos patienter som fick PROSCAR 5 mg/dag observerades ökningar på cirka 10 % av luteiniserande hormon (LH) och follikelstimulerande hormon (FSH), men nivåerna höll sig inom det normala intervallet. Hos friska frivilliga förändrade inte behandling med PROSCAR 5 mg svaret av LH och FSH på gonadotropinfrisättande hormon, vilket tyder på att hypotalamus-hypofys-testikelaxeln inte påverkades.
Hos patienter med BPH har PROSCAR ingen effekt på cirkulerande nivåer av kortisol, prolaktin, sköldkörtelstimulerande hormon eller tyroxin. Ingen kliniskt betydelsefull effekt observerades på plasmalipidprofilen (dvs totalt kolesterol, lågdensitetslipoproteiner, högdensitetslipoproteiner och triglycerider) eller benmineraltäthet.
Vuxna män med genetiskt ärftlig typ II 5α-reduktasbrist har också minskade nivåer av DHT. Förutom de associerade urogenitala defekterna vid födseln har inga andra kliniska avvikelser relaterade till typ II 5α-reduktasbrist observerats hos dessa individer. Dessa individer har en liten prostatakörtel under hela livet och utvecklar inte BPH.
Hos patienter med BPH som behandlats med finasterid (1-100 mg/dag) i 7-10 dagar före prostatektomi, uppmättes ett ungefär 80 % lägre DHT-innehåll i prostatavävnad som togs bort vid operation, jämfört med placebo; koncentrationen av testosteron i vävnaden ökade upp till 10 gånger jämfört med nivåerna före behandling, jämfört med placebo. Intraprostatiskt innehåll av PSA minskade också.
Hos friska frivilliga män som behandlats med PROSCAR 5 mg under 14 dagar, resulterade avbrott av behandlingen i att DHT-nivåerna återgick till nivåerna före behandlingen inom cirka 2 veckor. Hos patienter som behandlats i tre månader återgick prostatavolymen, som minskade med cirka 20 %, till nära baslinjevärdet efter cirka tre månaders avbrytande av behandlingen.
Farmakokinetik
Absorption
I en studie av 15 friska unga försökspersoner var den genomsnittliga biotillgängligheten för finasterid 5 mg tabletter 63 % (intervall 34-108 %), baserat på förhållandet mellan area under kurvan (AUC) i förhållande till en intravenös (IV) referensdos . Maximal plasmakoncentration av finasterid var i genomsnitt 37 ng/ml (intervall, 27-49 ng/ml) och nåddes 1-2 timmar efter dosering. Biotillgängligheten av finasterid påverkades inte av mat.
Distribution
Den genomsnittliga distributionsvolymen vid steady-state var 76 liter (intervall, 44-96 liter). Ungefär 90 % av cirkulerande finasterid är bundet till plasmaproteiner. Det finns en långsam ackumuleringsfas för finasterid efter upprepad dosering. Efter dosering med 5 mg/dag finasterid i 17 dagar var plasmakoncentrationerna av finasterid 47 och 54 % högre än efter den första dosen hos män 45-60 år (n=12) och ≥70 år (n=12) , respektive. Genomsnittliga dalkoncentrationer efter 17 dagars dosering var 6,2 ng/ml (intervall, 2,49,8 ng/ml) respektive 8,1 ng/ml (intervall, 1,8-19,7 ng/ml) i de två åldersgrupperna. Även om steady state inte uppnåddes i denna studie var den genomsnittliga dalplasmakoncentrationen i en annan studie på patienter med BPH (medelålder 65 år) som fick 5 mg/dag 9,4 ng/ml (intervall, 7,1-13,3 ng/ml; n= 22) efter över ett års dosering.
Finasterid har visat sig passera blod-hjärnbarriären men verkar inte fördelas fördelaktigt till CSF.
2 studier på friska försökspersoner (n=69) som fick PROSCAR 5 mg/dag i 6-24 veckor varierade finasteridkoncentrationerna i sperma från odetekterbar ( Användning i specifika populationer ].
Ämnesomsättning
Finasterid metaboliseras i stor utsträckning i levern, främst via enzymunderfamiljen cytokrom P450 3A4. Två metaboliter, t-butylsidokedjans monohydroxylerade och monokarboxylsyrametaboliter, har identifierats som inte har mer än 20 % av finasterids 5α-reduktasinhiberande aktivitet.
Exkretion
Hos friska unga försökspersoner (n=15) var medelplasmaclearance av finasterid 165 ml/min (intervall, 70279 ml/min) och genomsnittlig eliminationshalveringstid i plasma var 6 timmar (intervall, 3-16 timmar). Efter en oral dos av 14C-finasterid till människa (n=6), utsöndrades i genomsnitt 39 % (intervall, 32-46 %) av dosen i urinen i form av metaboliter; 57 % (intervall, 51-64 %) utsöndrades i avföringen.
Den genomsnittliga terminala halveringstiden för finasterid hos försökspersoner ≥70 år var cirka 8 timmar (intervall, 6-15 timmar; n=12), jämfört med 6 timmar (intervall, 4-12 timmar; n=12) hos försökspersoner 45-60 års ålder. Som ett resultat var medel-AUC(0-24 timmar) efter 17 dagars dosering 15 % högre hos försökspersoner ≥70 år än hos försökspersoner 45-60 år (p=0,02).
Pediatrisk
Finasterids farmakokinetik har inte undersökts hos patienter
Finasteride är inte indicerat för användning hos pediatriska patienter [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer ].
Kön
Finasteride är inte indicerat för användning hos kvinnor [se KONTRAINDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer , och HUR LEVERERAS ].
Geriatrisk
Ingen dosjustering är nödvändig hos äldre. Även om eliminationshastigheten av finasterid är minskad hos äldre, har dessa fynd ingen klinisk betydelse. [Se en Farmakokinetik  och Användning i specifika populationer .]
Lopp
Effekten av ras på finasterids farmakokinetik har inte studerats.
Nedsatt leverfunktion
Effekten av nedsatt leverfunktion på finasterids farmakokinetik har inte studerats. Försiktighet bör iakttas vid administrering av PROSCAR 5 mg till patienter med leverfunktionsavvikelser, eftersom finasterid metaboliseras i stor utsträckning i levern. Nedsatt njurfunktion
Ingen dosjustering är nödvändig hos patienter med nedsatt njurfunktion. Hos patienter med kroniskt nedsatt njurfunktion, med kreatininclearance från 9,0 till 55 ml/min, liknade AUC, maximal plasmakoncentration, halveringstid och proteinbindning efter en engångsdos av 14C-finasterid de värden som erhölls hos friska frivilliga. Urinutsöndring av metaboliter minskade hos patienter med nedsatt njurfunktion. Denna minskning var associerad med en ökning av fekal utsöndring av metaboliter. Plasmakoncentrationerna av metaboliter var signifikant högre hos patienter med nedsatt njurfunktion (baserat på en 60 % ökning av total radioaktivitet AUC). Finasterid har dock tolererats väl hos BPH-patienter med normal njurfunktion som fått upp till 80 mg/dag under 12 veckor, där exponeringen av dessa patienter för metaboliter förmodligen skulle vara mycket större.
Kliniska studier
Monoterapi
PROSCAR 5 mg/dag utvärderades initialt hos patienter med symtom på BPH och förstorad prostata genom digital rektal undersökning i två 1-åriga, placebokontrollerade, randomiserade, dubbelblinda studier och deras 5-åriga öppna förlängningar.
PROSCAR 5mg utvärderades ytterligare i PROSCAR Long-Term Efficacy and Safety Study (PLESS), en dubbelblind, randomiserad, placebokontrollerad, 4-årig multicenterstudie. 3040 patienter mellan 45 och 78 år, med måttliga till svåra symtom på BPH och förstorad prostata vid digital rektal undersökning, randomiserades till studien (1524 till finasterid, 1516 till placebo) och 3016 patienter kunde utvärderas med avseende på effekt. 1883 patienter fullföljde den 4-åriga studien (1000 i finasteridgruppen, 883 i placebogruppen).
Effekt på symtompoäng
Symtomen kvantifierades med hjälp av en poäng som liknar American Urological Association Symptom Score, som utvärderade både obstruktiva symtom (försämring av storlek och kraft i strömmen, känsla av ofullständig blåstömning, försenad eller avbruten urinering) och irritationssymtom (nokturi, dagtidsfrekvens, behov att anstränga eller pressa urinflödet) genom att betygsätta på en skala från 0 till 5 för sex symtom och en skala från 0 till 4 för ett symptom, för en total möjlig poäng på 34.
Patienter i PLESS hade måttliga till svåra symtom vid baslinjen (medelvärde på cirka 15 poäng på en 0-34 poängs skala). Patienter randomiserade till PROSCAR som förblev på behandling i 4 år hade en genomsnittlig (± 1 SD) minskning av symtompoängen på 3,3 (± 5,8) poäng jämfört med 1,3 (± 5,6) poäng i placebogruppen. (Se figur 1.) En statistiskt signifikant förbättring av symtompoängen var uppenbar efter 1 år hos patienter som behandlades med PROSCAR kontra placebo (–2,3 mot – 1,6), och denna förbättring fortsatte under år 4.
Figur 1 Symtompoäng i PLESS
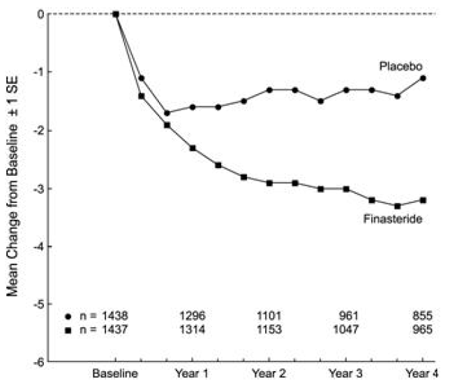
Resultat som setts i tidigare studier var jämförbara med de som sågs i PLESS. Även om en tidig förbättring av urinvägssymtom sågs hos vissa patienter, var en terapeutisk prövning på minst 6 månader i allmänhet nödvändig för att bedöma om ett gynnsamt svar på symtomlindring hade uppnåtts. Förbättringen av BPH-symtom sågs under det första året och bibehölls under ytterligare 5 år av öppna förlängningsstudier.
Effekt på akut urinretention och behovet av kirurgi
PLESS utvärderades också effekten genom att utvärdera behandlingsmisslyckanden. Behandlingssvikt definierades prospektivt som BPH-relaterade urologiska händelser eller klinisk försämring, bristande förbättring och/eller behov av alternativ behandling. BPH-relaterade urologiska händelser definierades som urologiska kirurgiska ingrepp och akut urinretention som kräver kateterisering. Fullständig information om händelsen var tillgänglig för 92 % av patienterna. Följande tabell (tabell 5) sammanfattar resultaten.
Jämfört med placebo var PROSCAR associerat med en signifikant lägre risk för akut urinretention eller behov av BPH-relaterad kirurgi [13,2% för placebo jämfört med 6,6% för PROSCAR; 51 % minskning i risk, 95 % KI: (34 till 63 %)]. Jämfört med placebo var PROSCAR 5 mg associerat med en signifikant lägre risk för operation [10,1 % för placebo jämfört med 4,6 % för PROSCAR; 55 % minskning av risken, 95 % CI: (37 till 68 %)] och med en signifikant lägre risk för akut urinretention [6,6 % för placebo mot 2,8 % för PROSCAR; 57 % minskning i risk, 95 % KI: (34 till 72 %)]; se figurerna 2 och 3.
Figur 2 Procent av patienter som opereras för BPH, inklusive TURP
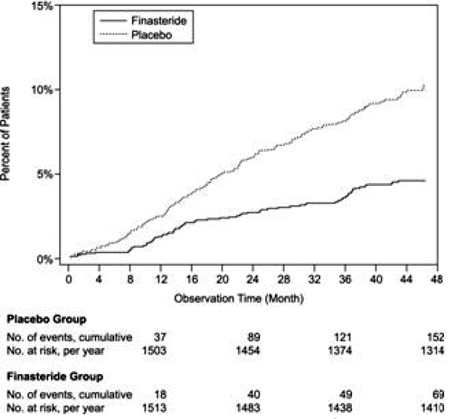
Figur 3 Procent av patienter som utvecklar akut urinretention (spontan och utfälld)
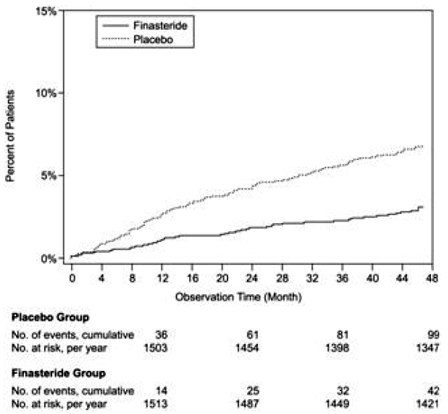
Effekt på maximalt urinflöde
Hos patienter i PLESS som förblev på terapi under studiens varaktighet och hade utvärderbara urinflödesdata, ökade PROSCAR 5 mg den maximala urinflödeshastigheten med 1,9 mL/sek jämfört med 0,2 mL/sek i placebogruppen.
Det fanns en tydlig skillnad mellan behandlingsgrupperna i maximal urinflödeshastighet till förmån för PROSCAR 5 mg efter månad 4 (1,0 vs 0,3 ml/sek) som bibehölls under hela studien. I de tidigare 1-årsstudierna var ökningen av maximalt urinflöde jämförbar med PLESS och bibehölls under det första året och under ytterligare 5 år av öppna förlängningsstudier.
Effekt på prostatavolym
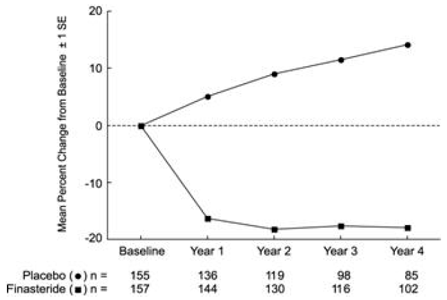
PLESS utvärderades prostatavolymen årligen med magnetisk resonanstomografi (MRT) hos en undergrupp av patienter. Hos patienter som behandlades med PROSCAR 5 mg och som kvarstod på behandling, minskade prostatavolymen jämfört med både baslinjen och placebo under hela den fyraåriga studien. PROSCAR minskade prostatavolymen med 17,9 % (från 55,9 cc vid baslinjen till 45,8 cc vid 4 år) jämfört med en ökning med 14,1 % (från 51,3 cc till 58,5 cc) i placebogruppen (p
Resultat som setts i tidigare studier var jämförbara med de som sågs i PLESS. Medelprostatavolymen vid baslinjen varierade mellan 40-50 cc. Minskningen av prostatavolymen sågs under det första året och bibehölls under ytterligare fem år av öppna förlängningsstudier.
Figur 4 Prostatavolym i PLESS
Prostatavolym som en prediktor för terapeutiskt svar
En metaanalys som kombinerar 1-års data från sju dubbelblinda, placebokontrollerade studier av liknande design, inklusive 4491 patienter med symtomatisk BPH, visade att hos patienter behandlade med PROSCAR, storleken på symtomsvaret och graden av förbättring i maximal urinflödeshastigheten var högre hos patienter med förstorad prostata vid baslinjen.
Kombination med Alpha-Blocker-terapi
Studien Medical Therapy of Prostatic Symptoms (MTOPS) var en dubbelblind, randomiserad, placebokontrollerad, multicenter, 4 till 6-årig studie (i genomsnitt 5 år) på 3047 män med symtomatisk BPH, som randomiserades till att få PROSCAR 5 mg/dag (n=768), doxazosin 4 eller 8 mg/dag (n=756), kombinationen av PROSCAR 5 mg/dag och doxazosin 4 eller 8 mg/dag (n=786), eller placebo (n=737 ). Alla deltagare genomgick veckotitrering av doxazosin (eller dess placebo) från 1 till 2 till 4 till 8 mg/dag. Endast de som tolererade dosnivån på 4 eller 8 mg hölls på doxazosin (eller dess placebo) i studien. Deltagarens slutliga tolererade dos (antingen 4 mg eller 8 mg) administrerades med början i slutet av vecka 4. Den sista doxazosindosen administrerades en gång per dag, vid sänggåendet.
Medelåldern för patienten vid randomisering var 62,6 år (±7,3 år). Patienterna var kaukasiska (82 %), afroamerikanska (9 %), latinamerikanska (7 %), asiatiska (1 %) eller indianer (
Det primära effektmåttet var ett sammansatt mått på den första förekomsten av något av följande fem utfall: en ≥4 poäng bekräftad ökning från baslinjen i symtompoäng, akut urinretention, BPH-relaterad njurinsufficiens (kreatininökning), återkommande urinvägsinfektioner eller urosepsis eller inkontinens. Jämfört med placebo resulterade behandling med PROSCAR 5mg, doxazosin eller kombinationsbehandling i en minskning av risken för att uppleva en av dessa fem utfallshändelser med 34 % (p=0,002), 39 % (p
Majoriteten av händelserna (274 av 351; 78 %) var en bekräftad ökning av symtompoäng på ≥4 poäng, kallad progression av symtompoäng. Risken för progression av symtompoäng minskade med 30 % (p=0,016), 46 % (p
Figur 5 Kumulativ förekomst av en 4-punkts ökning av AUA-symtompoäng efter behandlingsgrupp
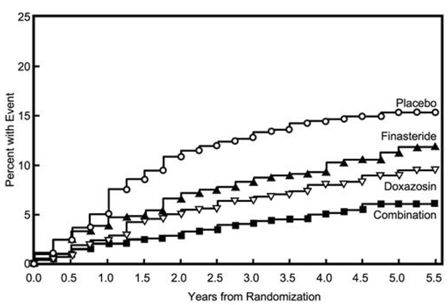
Behandling med PROSCAR 5mg, doxazosin eller kombinationen av PROSCAR med doxazosin, minskade medelvärdet av symtompoängen från baslinjen vid år 4. Tabell 7 visar den genomsnittliga förändringen från baslinjen för AUA-symtompoäng efter behandlingsgrupp för patienter som förblev på behandling i fyra år.
Resultaten av MTOPS överensstämmer med resultaten av den 4-åriga, placebokontrollerade studien PLESS [se Monoterapi ] i att behandling med PROSCAR minskar risken för akut urinretention och behovet av BPH-relaterad operation. Vid MTOPS minskade risken för att utveckla akut urinretention med 67 % hos patienter som behandlades med PROSCAR jämfört med patienter som behandlades med placebo (0,8 % för PROSCAR och 2,4 % för placebo). Dessutom minskade risken för att behöva BPH-relaterad invasiv behandling med 64 % hos patienter som behandlades med PROSCAR jämfört med patienter som behandlades med placebo (2,0 % för PROSCAR 5 mg och 5,4 % för placebo).
Sammanfattning av kliniska studier
Data från dessa studier, som visar förbättring av BPH-relaterade symtom, minskning av behandlingsmisslyckande (BPH-relaterade urologiska händelser), ökade maximala urinflödeshastigheter och minskad prostatavolym, tyder på att PROSCAR stoppar sjukdomsprocessen av BPH hos män med en förstorad prostata.
PATIENTINFORMATION
Ingen information lämnas. Vänligen se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER sektion.
