Behandling för hår: Avodart 0.5mg Dutasteride Användning, biverkningar och dosering. Pris i onlineapotek. Generiska läkemedel utan recept.
Vad är Avodart 0,5 mg och hur används det?
Avodart 0,5 mg är ett receptbelagt läkemedel som används för att behandla symtomen på en förstorad prostata (benign prostatahyperplasi). Avodart kan användas ensamt eller tillsammans med andra läkemedel.
Avodart 0,5 mg tillhör en klass av läkemedel som kallas 5-alfa-reduktashämmare.
Det är inte känt om Avodart 0,5 mg är säkert och effektivt för barn.
Vilka är biverkningarna av Avodart?
Biverkningar av Avodart 0,5 mg inkluderar:
- nässelfeber,
- svårt att andas,
- svullnad i ansiktet eller halsen,
- feber,
- öm hals,
- brännande ögon,
- hudsmärta och
- röda eller lila hudutslag med blåsor och fjällning
Få medicinsk hjälp omedelbart om du har något av symtomen som anges ovan.
De vanligaste biverkningarna av Avodart 0,5 mg inkluderar:
- minskad libido (sexlust),
- minskad mängd sperma som frigörs under sex,
- impotens (problem att få eller behålla erektion), och
- ömhet eller förstoring i brösten
Tala om för läkaren om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar av Avodart. För mer information, fråga din läkare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
BESKRIVNING
AVODART 0,5 mg är en syntetisk 4-azasteroidförening som är en selektiv hämmare av både typ 1 och typ 2 isoformerna av steroid 5 alfa-reduktas, ett intracellulärt enzym som omvandlar testosteron till DHT.
Dutasterid är kemiskt betecknad som (5α,17β)-N-{2,5 bis(trifluorometyl)fenyl}-3-oxo-4-azaandrost-1-en-17-karboxamid. Den empiriska formeln för dutasterid är C27H30F6N2O2, som representerar en molekylvikt på 528,5 med följande strukturformel:
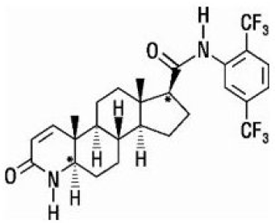
Dutasterid är ett vitt till ljusgult pulver med en smältpunkt på 242° till 250°C. Det är lösligt i etanol (44 mg/ml), metanol (64 mg/ml) och polyetylenglykol 400 (3 mg/ml), men det är olösligt i vatten.
Varje AVODART 0,5 mg mjuk gelatinkapsel, administrerad oralt, innehåller 0,5 mg dutasterid löst i en blandning av mono-diglycerider av kaprylsyra/kaprinsyra och butylerad hydroxitoluen. De inaktiva hjälpämnena i kapselskalet är järn(III)oxid (gul), gelatin (från certifierade BSE-fria nötkreaturskällor), glycerin och titandioxid. De mjuka gelatinkapslarna är tryckta med ätbart rött bläck.
INDIKATIONER
Monoterapi
AVODART (dutasterid) mjuka gelatinkapslar är indicerade för behandling av symptomatisk benign prostatahyperplasi (BPH) hos män med förstorad prostata för att:
- förbättra symtomen,
- minska risken för akut urinretention (AUR), och
- minska risken för behov av BPH-relaterad operation.
Kombination med alfa-adrenerg antagonist
AVODART i kombination med den alfa-adrenerga antagonisten, tamsulosin, är indicerat för behandling av symtomatisk BPH hos män med förstorad prostata.
Användningsbegränsningar
AVODART 0,5 mg är inte godkänt för att förebygga prostatacancer.
DOSERING OCH ADMINISTRERING
Kapslarna ska sväljas hela och inte tuggas eller öppnas, eftersom kontakt med kapselinnehållet kan leda till irritation av munhålans slemhinna. AVODART kan administreras med eller utan mat.
Monoterapi
Den rekommenderade dosen av AVODART är 1 kapsel (0,5 mg) en gång dagligen.
Kombination med alfa-adrenerg antagonist
Den rekommenderade dosen av AVODART 0,5 mg är 1 kapsel (0,5 mg) en gång dagligen och tamsulosin 0,4 mg en gång dagligen.
HUR LEVERERAS
Doseringsformer och styrkor
0,5 mg, ogenomskinliga, matt gula, gelatinkapslar märkta med "GX CE2" i rött bläck på ena sidan.
Förvaring Och Hantering
AVODART mjuka gelatinkapslar 0,5 mg är avlånga, ogenomskinliga, matt gula, gelatinkapslar märkta med "GX CE2" med rött ätbart bläck på ena sidan, förpackade i flaskor med 30 ( NDC 0173-0712-15) och 90 ( NDC 0173-0712-04) med barnsäkra stängningar.
Förvara vid 25°C (77°F); utflykter tillåtna till 15° till 30°C (59° till 86°F) [se USP-kontrollerad rumstemperatur ].
Dutasterid absorberas genom huden. AVODART 0,5 mg kapslar ska inte hanteras av kvinnor som är gravida eller som kan bli gravida på grund av risken för absorption av dutasterid och den efterföljande potentiella risken för ett manligt foster under utveckling [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Tillverkad för: GlaxoSmithKline Research Triangle Park. Reviderad: januari 2020
BIEFFEKTER
Erfarenhet av kliniska prövningar
Eftersom kliniska prövningar utförs under vitt skilda förhållanden, kan biverkningsfrekvenser som observerats i de kliniska prövningarna av ett läkemedel inte direkt jämföras med frekvenser i den kliniska prövningen av ett annat läkemedel och återspeglar kanske inte de frekvenser som observerats i praktiken.
Från kliniska prövningar med AVODART 0,5 mg som monoterapi eller i kombination med tamsulosin:
- De vanligaste biverkningarna som rapporterades hos försökspersoner som fick AVODART 0,5 mg var impotens, minskad libido, bröststörningar (inklusive bröstförstoring och ömhet) och ejakulationsrubbningar. De vanligaste biverkningarna som rapporterades hos försökspersoner som fick kombinationsbehandling (AVODART 0,5 mg plus tamsulosin) var impotens, minskad libido, bröststörningar (inklusive bröstförstoring och ömhet), ejakulationsrubbningar och yrsel. Ejakulationsstörningar förekom signifikant mer hos patienter som fick kombinationsbehandling (11 %) jämfört med de som fick AVODART (2 %) eller tamsulosin (4 %) som monoterapi.
- Avbrytande av prövningen på grund av biverkningar inträffade hos 4 % av försökspersonerna som fick AVODART 0,5 mg och 3 % av försökspersonerna som fick placebo i placebokontrollerade prövningar med AVODART. Den vanligaste biverkningen som ledde till att prövningen avbröts var impotens (1 %).
- den kliniska prövningen som utvärderade kombinationsterapin, upphörde prövningen på grund av biverkningar hos 6 % av försökspersonerna som fick kombinationsbehandling (AVODART plus tamsulosin) och 4 % av försökspersonerna som fick AVODART 0,5 mg eller tamsulosin som monoterapi. Den vanligaste biverkningen i alla behandlingsgrupper som ledde till att försöket avbröts var erektil dysfunktion (1 % till 1,5 %).
Monoterapi
Över 4 300 manliga försökspersoner med BPH tilldelades slumpmässigt att få placebo eller 0,5 mg dagliga doser av AVODART i 3 identiska 2-åriga, placebokontrollerade, dubbelblinda, fas 3-behandlingsstudier, var och en följt av en 2-årig öppen prövning. förlängning. Under den dubbelblinda behandlingsperioden exponerades 2 167 manliga försökspersoner för AVODART 0,5 mg, inklusive 1 772 exponerade under 1 år och 1 510 exponerade under 2 år. När de öppna förlängningarna inkluderades exponerades 1 009 manliga försökspersoner för AVODART 0,5 mg i 3 år och 812 exponerades i 4 år. Befolkningen var i åldern 47 till 94 år (medelålder: 66 år) och mer än 90 % var vita. Tabell 1 sammanfattar kliniska biverkningar som rapporterats hos minst 1 % av försökspersonerna som fick AVODART och med en högre incidens än patienter som fick placebo.
Långtidsbehandling (upp till 4 år)
Höggradig prostatacancer
REDUCE-studien var en randomiserad, dubbelblind, placebokontrollerad studie som inkluderade 8 231 män i åldern 50 till 75 år med ett serum-PSA på 2,5 ng/ml till 10 ng/ml och en negativ prostatabiopsi under de senaste 6 månaderna. Försökspersoner randomiserades till att få placebo (n = 4 126) eller 0,5 mg dagliga doser av AVODART (n = 4 105) i upp till 4 år. Medelåldern var 63 år och 91 % var vita. Försökspersonerna genomgick protokollförordnade schemalagda prostatabiopsier vid 2 och 4 års behandling eller hade "för orsaksbiopsier" vid icke-schemalagda tider om det var kliniskt indicerat. Det fanns en högre incidens av Gleason score 8-10 prostatacancer hos män som fick AVODART (1,0 %) jämfört med män som fick placebo (0,5 %) [se INDIKATIONER OCH ANVÄNDNING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. I en 7-årig placebokontrollerad klinisk prövning med en annan 5 alfa-reduktashämmare (finasterid 5 mg, PROSCAR) observerades liknande resultat för Gleason poäng 8-10 prostatacancer (finasterid 1,8 % mot placebo 1,1 %).
Ingen klinisk nytta har visats hos patienter med prostatacancer som behandlats med AVODART.
Reproduktions- och bröststörningar
I de 3 pivotala placebokontrollerade BPH-studierna med AVODART 0,5 mg, vart fjärde år, fanns inga tecken på ökade sexuella biverkningar (impotens, minskad libido och utlösningsstörning) eller bröststörningar med längre behandlingstid. Bland dessa 3 studier fanns 1 fall av bröstcancer i dutasteridgruppen och 1 fall i placebogruppen. Inga fall av bröstcancer rapporterades i någon behandlingsgrupp i den 4-åriga CombAT-studien eller den 4-åriga REDUCE-studien.
Förhållandet mellan långvarig användning av dutasterid och manlig bröstneoplasi är för närvarande okänt.
Kombination med alfablockerare (CombAT)
Över 4 800 manliga försökspersoner med BPH tilldelades slumpmässigt att få 0,5 mg AVODART 0,5 mg, 0,4 mg tamsulosin eller kombinationsbehandling (0,5 mg AVODART plus 0,4 mg tamsulosin) administrerat en gång dagligen i en 4-årig dubbelblind studie. Totalt fick 1 623 försökspersoner monoterapi med AVODART; 1 611 försökspersoner fick monoterapi med tamsulosin; och 1 610 försökspersoner fick kombinationsterapi. Befolkningen var i åldern 49 till 88 år (medelålder: 66 år) och 88% var vita. Tabell 2 sammanfattar biverkningar som rapporterats hos minst 1 % av försökspersonerna i kombinationsgruppen och med en högre incidens än patienter som får monoterapi med AVODART 0,5 mg eller tamsulosin.
Hjärtfel
CombAT, efter 4 års behandling, var incidensen av den sammansatta termen hjärtsvikt i kombinationsterapigruppen (12/1 610; 0,7 %) högre än i båda monoterapigrupperna: AVODART 0,5 mg, 2/1 623 (0,1 %) och tamsulosin, 9/1 611 (0,6%). Sammansatt hjärtsvikt undersöktes också i en separat 4-årig placebokontrollerad studie som utvärderade AVODART hos män med risk för utveckling av prostatacancer. Incidensen av hjärtsvikt hos försökspersoner som tog AVODART 0,5 mg var 0,6 % (26/4 105) jämfört med 0,4 % (15/4 126) hos patienter på placebo. En majoritet av försökspersonerna med hjärtsvikt i båda studierna hade samsjukligheter förknippade med en ökad risk för hjärtsvikt. Därför är den kliniska betydelsen av de numeriska obalanserna vid hjärtsvikt okänd. Inget orsakssamband mellan AVODART ensamt eller i kombination med tamsulosin och hjärtsvikt har fastställts. Ingen obalans observerades i incidensen av övergripande kardiovaskulära biverkningar i någon av studierna.
Erfarenhet efter marknadsföring
Följande biverkningar har identifierats efter användning av AVODART efter godkännande. Eftersom dessa reaktioner rapporteras frivilligt från en population av osäker storlek är det inte alltid möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till läkemedelsexponering. Dessa reaktioner har valts för inkludering på grund av en kombination av deras allvarlighetsgrad, rapporteringsfrekvens eller potentiellt orsakssamband med AVODART.
Immunsystemets störningar
Överkänslighetsreaktioner, inklusive utslag, klåda, urtikaria, lokalt ödem, allvarliga hudreaktioner och angioödem.
Neoplasmer
Manlig bröstcancer.
Psykiatriska störningar
Deppigt humör.
Reproduktionssystemet och bröststörningar
Testikelsmärta och testikelsvullnad.
LÄKEMEDELSINTERAKTIONER
Cytokrom P450 3A-hämmare
Dutasterid metaboliseras i stor utsträckning hos människor av isoenzymer cytokrom P450 (CYP)3A4 och CYP3A5. Effekten av potenta CYP3A4-hämmare på dutasterid har inte studerats. På grund av risken för läkemedelsinteraktioner, var försiktig när du förskriver AVODART till patienter som tar potenta, kroniska CYP3A4-enzymhämmare (t.ex. ritonavir) [se KLINISK FARMAKOLOGI ].
Alfa-adrenerga antagonister
Administrering av AVODART i kombination med tamsulosin eller terazosin har ingen effekt på steady-state farmakokinetiken för någon av alfaadrenerga antagonister. Effekten av administrering av tamsulosin eller terazosin på dutasterids farmakokinetiska parametrar har inte utvärderats.
Kalciumkanalantagonister
Samtidig administrering av verapamil eller diltiazem minskar dutasteridclearance och leder till ökad exponering för dutasterid. Förändringen i exponeringen för dutasterid anses inte vara kliniskt signifikant. Ingen dosjustering rekommenderas [se KLINISK FARMAKOLOGI ].
Kolestyramin
Administrering av en engångsdos på 5 mg AVODART 0,5 mg följt 1 timme senare av 12 g kolestyramin påverkar inte den relativa biotillgängligheten av dutasterid [se KLINISK FARMAKOLOGI ].
Digoxin
AVODART 0,5 mg förändrar inte farmakokinetiken vid steady-state för digoxin när det administreras samtidigt i en dos på 0,5 mg/dag i 3 veckor [se KLINISK FARMAKOLOGI ].
Warfarin
Samtidig administrering av AVODART 0,5 mg/dag i 3 veckor med warfarin förändrar inte steady-state farmakokinetiken för S- eller R-warfarinisomererna eller påverkar effekten av warfarin på protrombintiden [se KLINISK FARMAKOLOGI ].
VARNINGAR
Ingår som en del av FÖRSIKTIGHETSÅTGÄRDER sektion.
FÖRSIKTIGHETSÅTGÄRDER
Effekter på prostataspecifikt antigen (PSA) och användningen av PSA vid upptäckt av prostatacancer
kliniska prövningar minskade AVODART 0,5 mg serum-PSA-koncentrationen med cirka 50 % inom 3 till 6 månaders behandling. Denna minskning var förutsägbar över hela intervallet av PSA-värden hos patienter med symtomatisk BPH, även om den kan variera hos individer. AVODART 0,5 mg kan också orsaka minskningar av serum-PSA i närvaro av prostatacancer. För att tolka seriella PSA hos män som tar AVODART 0,5 mg, bör en ny PSA-baslinje fastställas minst 3 månader efter påbörjad behandling och PSA övervakas regelbundet därefter. Varje bekräftad ökning från det lägsta PSA-värdet under AVODART kan signalera förekomst av prostatacancer och bör utvärderas, även om PSA-nivåerna fortfarande ligger inom det normala intervallet för män som inte tar en 5 alfareduktashämmare. Underlåtenhet att följa AVODART kan också påverka PSA-testresultaten.
För att tolka ett isolerat PSA-värde hos en man som behandlats med AVODART 0,5 mg i 3 månader eller mer, bör PSA-värdet fördubblas för jämförelse med normala värden hos obehandlade män. Det fria totala PSA-förhållandet (procent fritt PSA) förblir konstant, även under påverkan av AVODART. Om läkare väljer att använda procent fritt PSA som ett hjälpmedel vid upptäckt av prostatacancer hos män som får AVODART, verkar ingen justering av dess värde vara nödvändig.
Samtidig administrering av dutasterid och tamsulosin resulterade i liknande förändringar av serum-PSA som monoterapi med dutasterid.
Ökad risk för höggradig prostatacancer
Hos män i åldrarna 50 till 75 år med en tidigare negativ biopsi för prostatacancer och en baslinje PSA mellan 2,5 ng/ml och 10,0 ng/ml som tog AVODART i den 4-åriga studien Reduction by Dutasteride of Prostate Cancer Events (REDUCE) fanns det en ökad förekomst av Gleason score 810 prostatacancer jämfört med män som tar placebo (AVODART 1,0 % mot placebo 0,5 %) [se INDIKATIONER OCH ANVÄNDNING , NEGATIVA REAKTIONER ]. I en 7-årig placebokontrollerad klinisk prövning med en annan 5 alfa-reduktashämmare (finasterid 5 mg, PROSCAR) observerades liknande resultat för Gleason poäng 8-10 prostatacancer (finasterid 1,8 % mot placebo 1,1 %).
alfa-reduktashämmare kan öka risken för utveckling av höggradig prostatacancer. Huruvida effekten av 5 alfa-reduktashämmare för att minska prostatavolymen eller prövningsrelaterade faktorer påverkade resultaten av dessa prövningar har inte fastställts.
Utvärdering för andra urologiska sjukdomar
Innan behandling med AVODART 0,5 mg påbörjas bör andra urologiska tillstånd som kan orsaka liknande symtom övervägas. Dessutom kan BPH och prostatacancer samexistera.
Transdermal exponering av AVODART 0,5 mg hos gravida kvinnor – risk för manligt foster
AVODART kapslar ska inte hanteras av kvinnor som är gravida eller kan vara gravida. Dutasterid kan absorberas genom huden och kan resultera i oavsiktlig fosterexponering och potentiell risk för ett manligt foster. Om en gravid kvinna kommer i kontakt med läckande dutasteridkapslar ska kontaktytan tvättas omedelbart med tvål och vatten [se Användning i specifika populationer ]. Dutasterid kan absorberas genom huden baserat på djurstudier [se Icke-klinisk toxikologi ].
Blod donation
Män som behandlas med AVODART ska inte donera blod förrän det har gått minst 6 månader efter deras sista dos. Syftet med denna uppskjutna period är att förhindra administrering av dutasterid till en gravid kvinnlig transfusionsmottagare.
Effekt på spermaegenskaper
Effekterna av dutasterid 0,5 mg/dag på spermaegenskaperna utvärderades hos friska män under 52 veckors behandling och 24 veckors uppföljning efter behandlingen. Vid 52 veckor, jämfört med placebo, resulterade dutasteridbehandling i genomsnittlig minskning av totalt spermieantal, spermavolym och spermiemotilitet; effekterna på det totala antalet spermier var inte reversibla efter 24 veckors uppföljning. Spermiekoncentration och spermiemorfologi var opåverkade och medelvärden för alla spermaparametrar förblev inom det normala intervallet vid alla tidpunkter. Den kliniska betydelsen av effekten av dutasterid på spermaegenskaperna för en enskild patients fertilitet är inte känd [se Användning i specifika populationer ].
Information om patientrådgivning
Rekommendera patienten att läsa den FDA-godkända patientmärkningen ( PATIENTINFORMATION ).
PSA-övervakning
Informera patienterna om att AVODART minskar PSA-nivåerna i serum med cirka 50 % inom 3 till 6 månader efter behandlingen, även om det kan variera för varje individ. För patienter som genomgår PSA-screening kan ökningar av PSA-nivåer under behandling med AVODART signalera förekomsten av prostatacancer och bör utvärderas av en vårdgivare [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Ökad risk för höggradig prostatacancer
Informera patienterna om att det fanns en ökning av höggradig prostatacancer hos män som behandlats med 5 alfa-reduktashämmare (som är indikerade för BPH-behandling), inklusive AVODART 0,5 mg, jämfört med de som behandlats med placebo i studier som tittade på användningen av dessa läkemedel för att minska risken för prostatacancer [se INDIKATIONER OCH ANVÄNDNING , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , NEGATIVA REAKTIONER ].
Transdermal exponering av AVODART hos gravida eller potentiellt gravida kvinnor – risk för manligt foster
Informera patienterna om att AVODART 0,5 mg kapslar inte ska hanteras av kvinnor som är gravida eller potentiellt kan vara gravida på grund av risken för absorption av dutasterid och den efterföljande potentiella risken för ett manligt foster under utveckling. Dutasterid kan absorberas genom huden och kan resultera i oavsiktlig fosterexponering. Om en gravid eller potentiellt gravid kvinna kommer i kontakt med läckande AVODART 0,5 mg kapslar, ska kontaktytan tvättas omedelbart med tvål och vatten [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer ].
Effekter på spermaparametrar
Informera män om att AVODART 0,5 mg kan påverka spermiernas egenskaper men effekten på fertiliteten är okänd [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer ].
Blod donation
Informera män som behandlats med AVODART 0,5 mg att de inte ska donera blod förrän minst 6 månader efter sin sista dos för att förhindra att gravida kvinnor får dutasterid genom blodtransfusion [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Serumnivåer av dutasterid kan detekteras i 4 till 6 månader efter avslutad behandling [se KLINISK FARMAKOLOGI ].
AVODART är ett varumärke som ägs av eller licensieras till GSK-gruppen av företag.
De andra varumärkena som anges är varumärken som ägs av eller licensieras till sina respektive ägare och ägs inte av eller licensieras till GSK-gruppen av företag. Tillverkarna av dessa varumärken är inte anslutna till och stöder inte GSK-gruppen av företag eller dess produkter.
Icke-klinisk toxikologi
Karcinogenes, Mutagenes, Nedsatt fertilitet
Carcinogenes
En 2-årig karcinogenicitetsstudie utfördes på B6C3F1-möss i doser på 3, 35, 250 och 500 mg/kg/dag för män och 3, 35 och 250 mg/kg/dag för honor; en ökad förekomst av benigna hepatocellulära adenom noterades vid 250 mg/kg/dag (290 gånger MRHD av en 0,5 mg daglig dos) endast hos honmöss. Två av de tre huvudsakliga humana metaboliterna har upptäckts hos möss. Exponeringen för dessa metaboliter hos möss är antingen lägre än hos människor eller är inte känd.
en 2-årig karcinogenicitetsstudie på Han Wistar-råttor, vid doser på 1,5, 7,5 och 53 mg/kg/dag hos hanar och 0,8, 6,3 och 15 mg/kg/dag hos honor, skedde en ökning av Leydig-celler adenom i testiklarna vid 135 gånger MRHD (53 mg/kg/dag och mer). En ökad förekomst av Leydig-cellshyperplasi var närvarande vid 52-faldigt MRHD (doser av hanråtta på 7,5 mg/kg/dag och mer). En positiv korrelation mellan proliferativa förändringar i Leydig-cellerna och en ökning av cirkulerande luteiniserande hormonnivåer har visats med 5 alfa-reduktashämmare och överensstämmer med en effekt på hypotalamus-hypofys-testikelaxeln efter 5 alfa-reduktashämmare. Vid tumörframkallande doser ökade nivåerna av luteiniserande hormon hos råttor med 167 %. I denna studie testades de viktigaste humana metaboliterna för karcinogenicitet vid cirka 1 till 3 gånger den förväntade kliniska exponeringen.
Mutagenes
Dutasterid testades för genotoxicitet i en bakteriell mutagenesanalys (Ames-test), en kromosomavvikelseanalys i äggstocksceller från kinesisk hamster och en mikronukleusanalys på råttor. Resultaten indikerade inte någon genotoxisk potential hos moderläkemedlet. Två stora mänskliga metaboliter var också negativa i antingen Ames-testet eller ett förkortat Ames-test.
Nedsättning av fertilitet
Behandling av könsmogna hanråttor med dutasterid vid 0,1 gånger MRHD (djurdoser på 0,05 mg/kg/dag eller mer i upp till 31 veckor) baserat på genomsnittlig serumkoncentration resulterade i dos- och tidsberoende minskningar av fertilitet vid alla doser ; minskat antal cauda epididymala (absoluta) spermier men inte spermiekoncentrationen (vid 50 och 500 mg/kg/dag); minskad vikt av epididymis, prostata och sädesblåsor; och mikroskopiska förändringar (cytoplasmatisk vakuolering av tubulärt epitel i epididymiderna och/eller minskat cytoplasmatiskt innehåll av epitel, i överensstämmelse med minskad sekretorisk aktivitet i prostata och sädesblåsor) i reproduktionsorganen vid alla doser i frånvaro av paternal toxicitet. Fertilitetseffekterna reverserades av återhämtningsvecka 6 vid alla doser, och antalet spermier var normalt i slutet av en 14-veckors återhämtningsperiod. De mikroskopiska förändringarna var inte längre närvarande vid återhämtningsvecka 14 vid 0,1 gånger MRHD och återfanns delvis i de återstående behandlingsgrupperna. Låga nivåer av dutasterid (0,6 till 17 ng/ml) detekterades i serum från obehandlade honråttor parade med behandlade hanar (10 till 500 mg/kg/dag i 29 till 30 veckor) vilket är 16 till 110 gånger MRHD baserat på genomsnittlig serumkoncentration. Ingen feminisering inträffade hos hanavkommor till obehandlade honråttor som parades med behandlade hanråttor även om detekterbara blodnivåer av dutasterid observerades hos honråttorna.
en fertilitetsstudie på honråttor med dosering 4 veckor före parning genom tidig dräktighet, resulterade oral administrering av dutasterid i doser på 0,05, 2,5, 12,5 och 30 mg/kg/dag i minskad kullstorlek på grund av ökade resorptioner och feminisering av manliga foster (minskat anogenitalt avstånd) vid 2 till 10 gånger MRHD (djurdoser på 2,5 mg/kg/dag eller mer) baserat på genomsnittlig serumkoncentration, i närvaro av maternell toxicitet (minskad kroppsviktsökning). Fosterkroppsvikten reducerades också med cirka 0,02 gånger MRHD (råttdos på 0,05 mg/kg/dag eller mer) baserat på genomsnittlig serumkoncentration, utan effekt utan effekt, i frånvaro av maternell toxicitet.
Användning i specifika populationer
Graviditet
Risksammanfattning
AVODART 0,5 mg är kontraindicerat för användning under graviditet eftersom det kan skada det manliga fostret [se KONTRAINDIKATIONER ]. AVODART är inte indicerat för användning till kvinnor.
AVODART 0,5 mg är en 5 alfa-reduktashämmare som förhindrar omvandling av testosteron till dihydrotestosteron (DHT), ett hormon som är nödvändigt för normal utveckling av manliga könsorgan. Avvikelser i könsorganen hos manliga foster är en förväntad fysiologisk konsekvens av hämning av denna omvandling. Dessa resultat liknar observationer hos manliga spädbarn med genetisk 5 alfa-reduktasbrist.
I den allmänna befolkningen i USA är den uppskattade bakgrundsrisken för allvarliga fosterskador och missfall i kliniskt erkända graviditeter 2 % till 4 % respektive 15 % till 20 %.
reproduktionsstudier på djur hämmade dutasterid den normala utvecklingen av yttre könsorgan hos manliga avkommor när det gavs till råttor eller kaniner under organogenesen vid mindre än den maximala rekommenderade humana dosen (MRHD) på 0,5 mg dagligen, i frånvaro av maternell toxicitet. Vid 15 gånger MRHD observerades förlängd graviditet, minskad reproduktionsorganvikt och försenad pubertet hos manliga avkommor, med ingen effektnivåer mindre än MRHD på 0,5 mg dagligen. Ökad placentavikt hos kaniner observerades också, med nivåer utan effekt lägre än MRHD på 0,5 mg dagligen (se Data ).
Även om dutasterid utsöndras i mänsklig sperma, är läkemedelskoncentrationen i den mänskliga kvinnliga partnern ungefär 100 gånger lägre än koncentrationer som ger avvikelser i manliga könsorgan i djurstudier (se Data ). Hos apor som doserats under organogenesen i blodkoncentrationer som är jämförbara med eller över nivåer som en mänsklig kvinnlig partner uppskattas exponeras för, påverkades inte manliga avkommor med yttre könsorgan negativt. Ingen feminisering inträffade hos hanavkommor till obehandlade honråttor som parats med behandlade hanråttor även om detekterbara blodnivåer av dutasterid observerades hos honråttorna [se Icke-klinisk toxikologi ].
Data
Mänskliga data
Den högsta uppmätta spermakoncentrationen av dutasterid hos behandlade män var 14 ng/ml. Även om dutasterid detekteras i sperma, om en kvinna på 50 kg utsätts för 5 ml sperma och 100 % absorption, skulle kvinnans förväntade dutasteridkoncentration i blodet genom sperma vara cirka 0,0175 ng/ml. Denna koncentration är ungefär 100 gånger lägre än blodkoncentrationer som ger avvikelser i manliga könsorgan i djurstudier. Dutasterid är mycket proteinbundet i mänsklig sperma (mer än 96 %), vilket kan minska mängden dutasterid som är tillgänglig för vaginal absorption.
Djurdata
en embryo-fosterutvecklingsstudie på råttor resulterade oral administrering av dutasterid vid 10 gånger mindre än MRHD på 0,5 mg dagligen (baserat på genomsnittliga blodnivåer hos män) i feminisering av manliga könsorgan hos fostret (minskat anogenitalt avstånd vid 0,05 mg). /kg/dag, med avsaknad av en nivå utan effekt) i frånvaro av maternell toxicitet. Dessutom inträffade bröstvårtans utveckling, hypospadi och utbredda preputiala körtlar hos foster hos mödrar som behandlats med doser på 2,5 mg/kg/dag eller mer (ungefär 15 gånger MRHD). Minskad fostrets kroppsvikt och tillhörande fördröjd förbening i närvaro av maternell toxicitet (minskad kroppsviktsökning) observerades vid modern exponering cirka 15 gånger MRHD (dos på 2,5 mg/kg/dag eller mer). En ökning av dödfödda ungar observerades hos mödrar som behandlades med 30 mg/kg/dag (ungefär 111 gånger MRHD), med en nolleffektnivå på 12,5 mg/kg/dag.
en studie av embryo-fosterutveckling av kanin, administrerades doser 28 gånger MRHD (doser på 30 mg/kg/dag eller mer), baserat på genomsnittliga blodnivåer hos män, oralt på dräktighetsdagarna 7 till 29 (under organogenesen och den sena period med utveckling av yttre könsorgan). Histologisk utvärdering av genitalpapillen hos foster visade tecken på feminisering av det manliga fostret såväl som sammansmälta skallben och ökade placentavikter vid alla doser i frånvaro av maternell toxicitet. En andra studie av embryo-fosterutveckling på kaniner som doserats under hela graviditeten (organogenes och senare period med utveckling av yttre könsorgan [dräktighetsdagar 6 till 29]) med 0,3 gånger MRHD (doser på 0,05 mg/kg/dag eller mer, utan ingen effektnivå), gav också bevis på feminisering av könsorganen hos manliga foster och ökade placentavikter vid alla doser i frånvaro av maternell toxicitet.
en embryo-fosterutvecklingsstudie exponerades dräktiga rhesusapor intravenöst under organogenesen (dräktighetsdagar 20 till 100) för en dutasteridnivå i blodet som var jämförbar med eller över den uppskattade dutasteridexponeringen för en kvinnlig partner. Dutasterid administrerades på dräktighetsdagarna 20 till 100 (under organogenes) i doser på 400, 780, 1 325 eller 2 010 ng/dag (12 apor/grupp). Ingen feminisering av manliga yttre könsorgan hos apavkommor observerades. Minskning av fostrets binjurevikt, minskning av fostrets prostatavikt och ökningar av fostrets ovarie- och testikelvikter observerades vid den högsta testade dosen. Baserat på den högsta uppmätta spermakoncentrationen av dutasterid hos behandlade män (14 ng/ml), representerar dessa doser hos apan upp till 16 gånger den potentiella maximala exponeringen av en 50 kg kvinnlig hona för 5 ml sperma dagligen från en dutasterid- behandlad hane, förutsatt 100% absorption. Dosnivåerna (på ng/kg-basis) som administreras till apor i denna studie är 32 till 186 gånger den nominella (ng/kg) dos som en hona potentiellt skulle exponeras för via sperma. Det är inte känt om kaniner eller rhesusapor producerar någon av de viktigaste mänskliga metaboliterna.
en oral pre- och postnatal utvecklingsstudie på råttor observerades feminisering av manliga könsorgan. Minskat anogenitalt avstånd observerades vid 0,05 gånger MRHD och mer (0,05 mg/kg/dag och mer), med avsaknad av en no-effect-nivå, baserat på genomsnittliga blodnivåer hos män som en uppskattning av AUC. Hypospadi och utveckling av bröstvårtor observerades vid 2,5 mg/kg/dag eller mer (14 gånger MRHD eller mer, med en nivå utan effekt vid 0,05 mg/kg/dag). Doser på 2,5 mg/kg/dag och mer resulterade också i förlängd dräktighet hos föräldrarnas honor, en ökning av tiden till balano-preputial separation hos manliga avkommor, en minskning av tiden till vaginal öppenhet för kvinnliga avkommor och en minskning av prostata- och seminal vesikelvikter hos manliga avkommor. Ökade dödfödslar och minskad neonatal livsduglighet hos avkommor noterades vid 30 mg/kg/dag (102 gånger MRHD i närvaro av maternell toxicitet [minskad kroppsvikt]).
Laktation
Risksammanfattning
AVODART är inte indicerat för användning till kvinnor. Det finns ingen tillgänglig information om förekomsten av dutasterid i bröstmjölk, effekterna på det ammade barnet eller effekterna på mjölkproduktionen.
Kvinnor Och Hanar Av Reproduktionspotential
Infertilitet
Män
Effekterna av dutasterid 0,5 mg/dag på spermaegenskaperna utvärderades hos normala frivilliga i åldern 18 till 52 år (n = 27 dutasterider, n = 23 placebo) under 52 veckors behandling och 24 veckors uppföljning efter behandling. Vid 52 veckor var den genomsnittliga procentuella minskningen från baslinjen i totalt spermieantal, spermavolym och spermiemotilitet 23 %, 26 % respektive 18 % i dutasteridgruppen när det justerades för förändringar från baslinjen i placebogruppen. Spermiekoncentration och spermiemorfologi var opåverkade. Efter 24 veckors uppföljning förblev den genomsnittliga procentuella förändringen av totalt spermieantal i dutasteridgruppen 23 % lägre än baseline. Medan medelvärden för alla spermaparametrar vid alla tidpunkter höll sig inom de normala intervallen och inte uppfyllde fördefinierade kriterier för en kliniskt signifikant förändring (30 %), hade 2 försökspersoner i dutasteridgruppen en minskning av antalet spermier på mer än 90 % från baslinjen vid 52 veckor, med partiell återhämtning vid 24-veckorsuppföljningen. Den kliniska betydelsen av dutasterids effekt på spermaegenskaperna för en enskild patients fertilitet är inte känd [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ].
Pediatrisk användning
AVODART 0,5 mg är inte indicerat för användning till pediatriska patienter. Säkerhet och effektivitet hos pediatriska patienter har inte fastställts.
Geriatrisk användning
Av 2 167 manliga försökspersoner som behandlades med AVODART 0,5 mg i 3 kliniska prövningar var 60 % i åldern 65 år och äldre och 15 % var 75 år och äldre. Inga övergripande skillnader i säkerhet eller effekt observerades mellan dessa försökspersoner och yngre försökspersoner. Andra rapporterade kliniska erfarenheter har inte identifierat skillnader i svar mellan äldre och yngre patienter, men större känslighet hos vissa äldre individer kan inte uteslutas [se KLINISK FARMAKOLOGI ].
Nedsatt njurfunktion
Ingen dosjustering är nödvändig för AVODART 0,5 mg hos patienter med nedsatt njurfunktion [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunktion
Effekten av nedsatt leverfunktion på dutasterids farmakokinetik har inte studerats. Eftersom dutasterid metaboliseras i stor utsträckning kan exponeringen vara högre hos patienter med nedsatt leverfunktion. I en klinisk prövning där 60 försökspersoner fick 5 mg (10 gånger den terapeutiska dosen) dagligen under 24 veckor, observerades dock inga ytterligare biverkningar jämfört med de som observerades vid den terapeutiska dosen på 0,5 mg [se KLINISK FARMAKOLOGI ].
ÖVERDOS
I försök med frivilliga har engångsdoser av dutasterid upp till 40 mg (80 gånger den terapeutiska dosen) under 7 dagar administrerats utan betydande säkerhetsproblem. I en klinisk prövning administrerades dagliga doser på 5 mg (10 gånger den terapeutiska dosen) till 60 försökspersoner under 6 månader utan ytterligare biverkningar än de som sågs vid terapeutiska doser på 0,5 mg.
Det finns ingen specifik motgift mot dutasterid. I fall av misstänkt överdosering bör därför symtomatisk och stödjande behandling ges vid behov, med hänsyn till dutasterids långa halveringstid.
KONTRAINDIKATIONER
AVODART 0,5 mg är kontraindicerat för användning i:

- Graviditet. Dutasterid är kontraindicerat hos kvinnor som är gravida. I reproduktions- och utvecklingstoxicitetsstudier på djur hämmade dutasterid utvecklingen av manliga foster yttre könsorgan. Därför kan AVODART 0,5 mg orsaka fosterskada när det administreras till en gravid kvinna [se VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER , Användning i specifika populationer ].
- Patienter med tidigare påvisad kliniskt signifikant överkänslighet (t.ex. allvarliga hudreaktioner, angioödem) mot AVODART eller andra 5 alfa-reduktashämmare [se NEGATIVA REAKTIONER ].
KLINISK FARMAKOLOGI
Handlingsmekanism
Dutasterid hämmar omvandlingen av testosteron till DHT. DHT är det androgen som primärt ansvarar för den initiala utvecklingen och efterföljande förstoring av prostatakörteln. Testosteron omvandlas till DHT av enzymet 5 alfa-reduktas, som finns som 2 isoformer, typ 1 och typ 2. Typ 2 isoenzymet är primärt aktivt i reproduktiva vävnader, medan typ 1 isoenzymet också ansvarar för testosteronomvandlingen i hud och lever.
Dutasterid är en kompetitiv och specifik hämmare av både typ 1 och typ 2 5 alfa-reduktas isoenzymer, med vilka den bildar ett stabilt enzymkomplex. Dissociation från detta komplex har utvärderats under betingelser in vitro och in vivo och är extremt långsam. Dutasterid binder inte till den mänskliga androgenreceptorn.
Farmakodynamik
Effekt på 5 alfa-dihydrotestosteron och testosteron
Den maximala effekten av dagliga doser av dutasterid på minskningen av DHT är dosberoende och observeras inom 1 till 2 veckor. Efter 1 och 2 veckors daglig dosering med dutasterid 0,5 mg reducerades median-DHT-koncentrationerna i serum med 85 % respektive 90 %. Hos patienter med BPH som behandlats med dutasterid 0,5 mg/dag i 4 år var medianminskningen av serum-DHT 94 % efter 1 år, 93 % efter 2 år och 95 % vid både 3 och 4 år. Medianökningen av serumtestosteron var 19 % vid både 1 och 2 år, 26 % vid 3 år och 22 % vid 4 år, men medel- och mediannivåerna förblev inom det fysiologiska intervallet.
Hos patienter med BPH som behandlats med 5 mg/dag av dutasterid eller placebo i upp till 12 veckor före transuretral resektion av prostata, var genomsnittliga DHT-koncentrationer i prostatavävnad signifikant lägre i dutasteridgruppen jämfört med placebo (784 och 5 793 pg/g) P
Vuxna män med genetiskt ärftlig typ 2 5 alfa-reduktasbrist har också minskade DHT-nivåer. Dessa 5 alfa-reduktasbristade män har en liten prostatakörtel under hela livet och utvecklar inte BPH. Förutom de associerade urogenitala defekterna vid födseln har inga andra kliniska avvikelser relaterade till 5-alfa-reduktasbrist observerats hos dessa individer.
Effekter på andra hormoner
Hos friska frivilliga gav 52 veckors behandling med dutasterid 0,5 mg/dag (n = 26) ingen kliniskt signifikant förändring jämfört med placebo (n = 23) i könshormonbindande globulin, östradiol, luteiniserande hormon, follikelstimulerande hormon, tyroxin (fritt T4) och dehydroepiandrosteron. Statistiskt signifikanta, baseline-justerade medelökningar jämfört med placebo observerades för totalt testosteron efter 8 veckor (97,1 ng/dL, P
Andra effekter
Plasmalipidpanel och bentäthet utvärderades efter 52 veckors dutasterid 0,5 mg en gång dagligen hos friska frivilliga. Det förelåg ingen förändring i benmineraldensitet mätt med dubbelenergiröntgenabsorptiometri jämfört med varken placebo eller baslinje. Dessutom var plasmalipidprofilen (dvs totalt kolesterol, lågdensitetslipoproteiner, högdensitetslipoproteiner, triglycerider) opåverkad av dutasterid. Inga kliniskt signifikanta förändringar i binjurens hormonsvar på stimulering av adrenokortikotropt hormon (ACTH) observerades i en undergruppspopulation (n = 13) av den 1-åriga studien med friska frivilliga.
Farmakokinetik
Absorption
Efter administrering av en engångsdos på 0,5 mg av en mjuk gelatinkapsel, tar tiden till maximala serumkoncentrationer (Tmax) av dutasterid inom 2 till 3 timmar. Absolut biotillgänglighet hos 5 friska försökspersoner är cirka 60 % (intervall: 40 % till 94 %). När läkemedlet administreras med mat minskade de maximala serumkoncentrationerna med 10 % till 15 %. Denna minskning har ingen klinisk betydelse.
Distribution
Farmakokinetiska data efter enstaka och upprepade orala doser visar att dutasterid har en stor distributionsvolym (300 till 500 L). Dutasterid är starkt bundet till plasmaalbumin (99,0%) och alfa-1 surt glykoprotein (96,6%).
I ett försök med friska försökspersoner (n = 26) som fick dutasterid 0,5 mg/dag i 12 månader, var spermadutasteridkoncentrationerna i genomsnitt 3,4 ng/ml (intervall: 0,4 till 14 ng/ml) vid 12 månader och, i likhet med serum, uppnåddes stabila - ange koncentrationer vid 6 månader. I genomsnitt fördelades 11,5 % av serumkoncentrationerna av dutasterid efter 12 månader i sperma.
Metabolism och eliminering
Dutasterid metaboliseras i stor utsträckning hos människor. In vitro-studier visade att dutasterid metaboliseras av isoenzymer CYP3A4 och CYP3A5. Båda dessa isoenzymer producerade metaboliterna 4'-hydroxidutasterid, 6-hydroxidutasterid och 6,4'-dihydroxidutasterid. Dessutom bildades 15-hydroxidutasteridmetaboliten av CYP3A4. Dutasterid metaboliseras inte in vitro av humana cytokrom P450 isoenzymer CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 och CYP2E1. I humant serum efter dosering till steady state, oförändrad dutasterid, 3 huvudmetaboliter (4'-hydroxidutasterid, 1,2-dihydrodutasterid och 6-hydroxidutasterid), och 2 mindre metaboliter (6,4'-dihydroxidutasterid och 15 -hydroxidutasterid), som bedömts genom masspektrometrisk respons, har upptäckts. Den absoluta stereokemin för hydroxyltillsatserna i 6 och 15 positionerna är inte känd. In vitro är 4'-hydroxidutasterid- och 1,2-dihydrodutasterid-metaboliterna mycket mindre potenta än dutasterid mot båda isoformerna av humant 5-alfa-reduktas. Aktiviteten för 6β-hydroxidutasterid är jämförbar med den för dutasterid.
Dutasterid och dess metaboliter utsöndrades huvudsakligen i feces. Som procent av dosen var det cirka 5 % oförändrad dutasterid (~1% till ~15%) och 40% som dutasteridrelaterade metaboliter (~2% till ~90%). Endast spårmängder av oförändrad dutasterid hittades i urinen (
Den terminala halveringstiden för dutasterid är cirka 5 veckor vid steady state. Den genomsnittliga steady-state serumkoncentrationen av dutasterid var 40 ng/ml efter 0,5 mg/dag under 1 år. Efter daglig dosering uppnår serumkoncentrationerna av dutasterid 65 % av steady-state-koncentrationen efter 1 månad och cirka 90 % efter 3 månader. På grund av den långa halveringstiden för dutasterid förblir serumkoncentrationerna detekterbara (större än 0,1 ng/ml) i upp till 4 till 6 månader efter avslutad behandling.
Specifika populationer
Pediatriska patienter
Dutasterids farmakokinetik har inte undersökts hos personer yngre än 18 år.
Geriatriska patienter
Ingen dosjustering är nödvändig hos äldre. Farmakokinetiken och farmakodynamiken för dutasterid utvärderades hos 36 friska manliga försökspersoner i åldern 24 till 87 år efter administrering av en engångsdos på 5 mg dutasterid. I denna endosstudie ökade dutasterids halveringstid med åldern (cirka 170 timmar hos män i åldern 20 till 49 år, cirka 260 timmar hos män i åldern 50 till 69 år och cirka 300 timmar hos män äldre än 70 år). Av 2 167 män som behandlades med dutasterid i de tre pivotala studierna var 60 % 65 år och äldre och 15 % var 75 år och äldre. Inga övergripande skillnader i säkerhet eller effekt observerades mellan dessa patienter och yngre patienter.
Manliga Och Kvinnliga Patienter
AVODART är kontraindicerat under graviditet och är inte indicerat för användning till kvinnor [se KONTRAINDIKATIONER , VARNINGAR OCH FÖRSIKTIGHETSÅTGÄRDER ]. Farmakokinetiken för dutasterid hos kvinnor har inte studerats.
Rasliga och etniska grupper
Effekten av ras på dutasterids farmakokinetik har inte studerats.
Patienter med nedsatt njurfunktion
Effekten av nedsatt njurfunktion på dutasterids farmakokinetik har inte studerats. Mindre än 0,1 % av en steady-state 0,5 mg dos av dutasterid återfinns dock i human urin, så ingen dosjustering förväntas för patienter med nedsatt njurfunktion.
Patienter med nedsatt leverfunktion
Effekten av nedsatt leverfunktion på dutasterids farmakokinetik har inte studerats. Eftersom dutasterid metaboliseras i stor utsträckning kan exponeringen vara högre hos patienter med nedsatt leverfunktion.
Läkemedelsinteraktionsstudier
Cytokrom P450-hämmare
Inga kliniska läkemedelsinteraktionsstudier har utförts för att utvärdera effekten av CYP3A-enzymhämmare på dutasterids farmakokinetik. Baserat på in vitro-data kan dock blodkoncentrationerna av dutasterid öka i närvaro av hämmare av CYP3A4/5 såsom ritonavir, ketokonazol, verapamil, diltiazem, cimetidin, troleandomycin och ciprofloxacin.
Dutasterid hämmar inte in vitro-metabolismen av modellsubstrat för de huvudsakliga humana cytokrom P450-isoenzymerna (CYP1A2, CYP2C9, CYP2C19, CYP2D6 och CYP3A4) vid en koncentration av 1 000 ng/ml, 25 gånger högre än i humana serumkoncentrationer. .
Alfa-adrenerga antagonister
I en ensekvens, crossover-studie på friska frivilliga, hade administrering av tamsulosin eller terazosin i kombination med AVODART ingen effekt på steady-state farmakokinetiken för någon av alfaadrenerga antagonister. Även om effekten av administrering av tamsulosin eller terazosin på dutasterids farmakokinetiska parametrar inte utvärderades, var den procentuella förändringen i DHT-koncentrationer liknande för AVODART 0,5 mg enbart jämfört med kombinationsbehandlingen.
Kalciumkanalantagonister
en populationsfarmakokinetikanalys noterades en minskning av clearance av dutasterid vid samtidig administrering med CYP3A4-hämmarna verapamil (-37 %, n = 6) och diltiazem (-44 %, n = 5). Däremot sågs ingen minskning av clearance när amlodipin, en annan kalciumkanalantagonist som inte är en CYP3A4-hämmare, administrerades samtidigt med dutasterid (+7 %, n = 4).
Minskningen av clearance och efterföljande ökning av exponeringen för dutasterid i närvaro av verapamil och diltiazem anses inte vara kliniskt signifikant. Ingen dosjustering rekommenderas.
Kolestyramin
Administrering av en engångsdos på 5 mg AVODART 0,5 mg följt 1 timme senare av 12 g kolestyramin påverkade inte den relativa biotillgängligheten av dutasterid hos 12 normala frivilliga.
Digoxin
I en studie med 20 friska frivilliga förändrade inte AVODART 0,5 mg farmakokinetiken vid steady-state för digoxin när det administrerades samtidigt i en dos på 0,5 mg/dag under 3 veckor.
Warfarin
en studie med 23 friska frivilliga förändrade 3 veckors behandling med AVODART 0,5 mg/dag inte farmakokinetiken vid steady-state för S- eller R-warfarinisomererna eller påverkade warfarins effekt på protrombintiden när det administrerades med warfarin.
Annan samtidig terapi
Även om specifika interaktionsstudier inte utfördes med andra substanser, tog cirka 90 % av försökspersonerna i de 3 randomiserade, dubbelblinda, placebokontrollerade säkerhets- och effektprövningarna som fick AVODART andra läkemedel samtidigt. Inga kliniskt signifikanta biverkningar kunde tillskrivas kombinationen av AVODART och samtidig behandling när AVODART administrerades samtidigt med antihyperlipidemikalier, angiotensinomvandlande enzym (ACE)-hämmare, beta-adrenerga blockerare, kalciumkanalblockerare, kortikosteroider, diuretika, icke-steroida antikroppar. -inflammatoriska läkemedel (NSAID), fosfodiesteras typ V-hämmare och kinolonantibiotika.
Djurtoxikologi och/eller farmakologi
Toxikologiska studier i centrala nervsystemet
Till råttor och hundar resulterade upprepad oral administrering av dutasterid i att vissa djur visade tecken på ospecifik, reversibel, centralt medierad toxicitet utan associerade histopatologiska förändringar vid exponeringar som var 425 respektive 315 gånger den förväntade kliniska exponeringen (för moderläkemedlet). .
Kanin dermal absorption
I en dermal farmakokinetikstudie på kanin resulterade dermal absorption av dutasterid i CAPMUL (glyceryloleat) hos kaniner i serumkoncentrationer på 2,7 till 40,5 mcg/h/mL för doser på 1 till 20 mg/ml, respektive, eller 56 % till 1 000 av applicerad dutasterid för att absorberas under tilltäppta och långvariga förhållanden. AVODART mjuka gelatinkapslar administrerade oralt innehåller 0,5 mg dutasterid löst i en blandning av mono-diglycerider av kapryl/kaprinsyra och butylerad hydroxitoluen. Dutasterid i vatten absorberades minimalt hos kaniner (2 000 mg/kg).
Kliniska studier
Monoterapi
AVODART 0,5 mg/dag (n = 2 167) eller placebo (n = 2 158) utvärderades hos manliga försökspersoner med BPH i tre 2-åriga multicenter, placebokontrollerade, dubbelblinda studier, var och en med 2-åriga öppna förlängningar ( n = 2 340). Mer än 90 % av försökspopulationen var vit. Försökspersonerna var minst 50 år gamla med ett serum-PSA ≥1,5 ng/ml och
Effekt på symtompoäng
Symtomen kvantifierades med hjälp av AUA-SI, ett frågeformulär som utvärderar urinvägssymtom (ofullständig tömning, frekvens, intermittens, brådskande, svag ström, ansträngning och nocturia) genom att betygsätta på en skala från 0 till 5 för en total möjlig poäng på 35, med högre numeriska totala symtompoäng som representerar större svårighetsgrad av symtomen. Baslinje AUA-SI-poängen i de tre försöken var cirka 17 enheter i båda behandlingsgrupperna.
Försökspersoner som fick dutasterid uppnådde statistiskt signifikant förbättring av symtomen jämfört med placebo efter månad 3 i 1 prövning och efter månad 12 i de andra 2 pivotala prövningarna. Vid månad 12 var den genomsnittliga minskningen från baslinjen i totala symtompoäng för AUA-SI över de tre poolade försöken -3,3 enheter för dutasterid och -2,0 enheter för placebo med en genomsnittlig skillnad mellan de två behandlingsgrupperna på -1,3 (intervall: -1,1) till -1,5 enheter i var och en av de tre försöken, P
Dessa försök var prospektivt utformade för att utvärdera effekter på symtom baserat på prostatastorlek vid baslinjen. Hos män med prostatavolymer ≥40 cc var den genomsnittliga minskningen -3,8 enheter för dutasterid och -1,6 enheter för placebo, med en medelskillnad mellan de två behandlingsgrupperna på -2,2 vid månad 24. Hos män med prostatavolymer
Figur 1: AUA-SI-poängförändring från baslinje (randomiserade, dubbelblinda, placebokontrollerade försök sammanslagna)
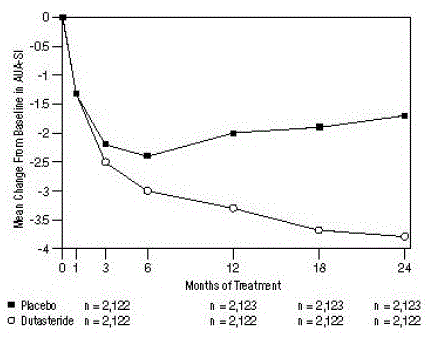
en AUA-SI-poäng varierar från 0 till 35.
Effekt på akut urinretention och behovet av BPH-relaterad kirurgi
Effekten utvärderades också efter 2 års behandling genom förekomsten av AUR som kräver kateterisering och BPH-relaterad urologisk kirurgi. Jämfört med placebo var AVODART associerat med en statistiskt signifikant lägre incidens av AUR (1,8 % för AVODART mot 4,2 % för placebo, P
Figur 2: Procent av försökspersonerna som utvecklar akut urinretention under en 24-månadersperiod (randomiserade, dubbelblinda, placebokontrollerade försök sammanslagna)
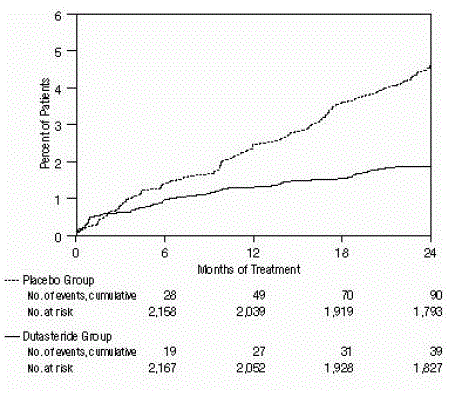
Figur 3: Procent av försökspersoner som har opererats för benign prostatahyperplasi under en 24-månadersperiod (slumpmässiga, dubbelblinda, placebokontrollerade försök sammanslagna)
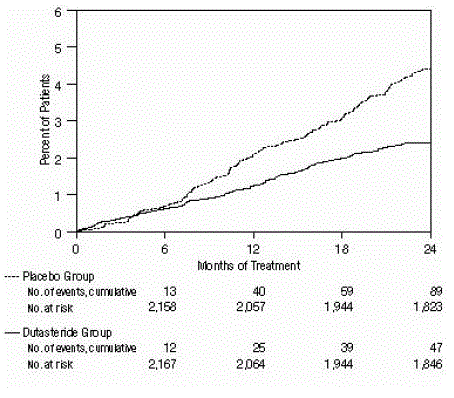
Effekt på prostatavolym
En prostatavolym på minst 30 cc mätt med transrektalt ultraljud krävdes för inträde i försöket. Medelprostatavolymen vid inträde i försöket var cirka 54 cc.
Statistiskt signifikanta skillnader (AVODART 0,5 mg jämfört med placebo) noterades vid den tidigaste prostatavolymmätningen efter behandling i varje försök (månad 1, månad 3 eller månad 6) och fortsatte till och med månad 24. Vid månad 12 var den genomsnittliga procentuella förändringen i prostatavolymen i de tre sammanslagna försöken var -24,7 % för dutasterid och -3,4 % för placebo; medelskillnaden (dutasterid minus placebo) var -21,3 % (intervall: -21,0 % till -21,6 % i var och en av de tre studierna, P
Figur 4: Prostatavolymförändring i procent från baslinjen (randomiserade, dubbelblinda, placebokontrollerade försök sammanslagna)
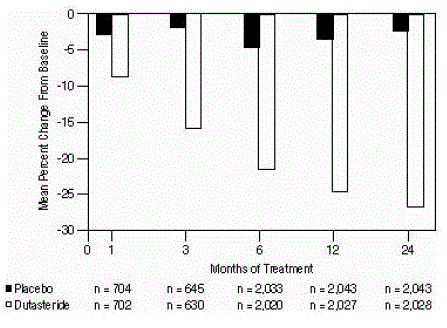
Effekt på maximalt urinflöde
En genomsnittlig maximal urinflödeshastighet (Qmax) på ≤15 ml/sek krävdes för inträde i försöket. Qmax var cirka 10 ml/sek vid baslinjen över de tre pivotala studierna.
Skillnaderna mellan de två grupperna var statistiskt signifikanta från baslinjen vid månad 3 i alla tre försöken och bibehölls till och med månad 12. Vid månad 12 var den genomsnittliga ökningen av Qmax över de tre sammanslagna försöken 1,6 mL/sek för AVODART 0,5 mg och 0,7 mL /sek för placebo; medelskillnaden (dutasterid minus placebo) var 0,8 ml/sek (intervall: 0,7 till 1,0 ml/sek i var och en av de 3 försöken, P
Figur 5: Qmax-förändring från baslinjen (randomiserade, dubbelblinda, placebokontrollerade försök poolade)
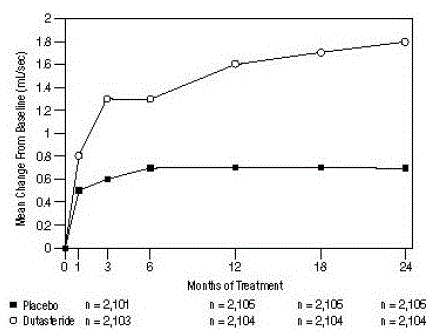
Sammanfattning av kliniska prövningar
Data från 3 stora, välkontrollerade effektstudier visar att behandling med AVODART (0,5 mg en gång dagligen) minskar risken för både AUR och BPH-relaterade kirurgiska ingrepp jämfört med placebo, förbättrar BPH-relaterade symtom, minskar prostatavolymen och ökar den maximala urinflödeshastigheter. Dessa data tyder på att AVODART 0,5 mg stoppar sjukdomsprocessen av BPH hos män med förstorad prostata.
Kombination med alfablockerare (CombAT)
Effekten av kombinationsbehandling (AVODART 0,5 mg/dag plus tamsulosin 0,4 mg/dag, n = 1 610) jämfördes med AVODART 0,5 mg enbart (n = 1 623) eller enbart tamsulosin (n = 1 611) i ett 4-årigt multicenter, randomiserat , dubbelblind försök. Kriterierna för inträde i studien liknade de dubbelblinda, placebokontrollerade effektprövningarna för monoterapi som beskrivs i avsnitt 14.1. Åttioåtta procent (88%) av den inskrivna försökspopulationen var vita. Ungefär 52 % av försökspersonerna hade tidigare exponering för behandling med 5 alfa-reduktas-hämmare eller alfa-adrenerga antagonister. Av de 4 844 försökspersoner som slumpmässigt tilldelades behandling, avslutade 69 % av försökspersonerna i kombinationsgruppen, 67 % i gruppen som fick AVODART 0,5 mg och 61 % i tamsulosingruppen 4 års dubbelblind behandling.
Effekt på symtompoäng
Symtomen kvantifierades med hjälp av de första 7 frågorna i International Prostate Symptom Score (IPSS) (identiskt med AUA-SI). Baslinjepoängen var cirka 16,4 enheter för varje behandlingsgrupp. Kombinationsterapi var statistiskt överlägsen var och en av monoterapibehandlingarna när det gällde minskande symtompoäng vid månad 24, den primära tidpunkten för detta effektmått. Vid månad 24 var medelförändringarna från baslinjen (±SD) i IPSS totala symtompoäng -6,2 (±7,14) för kombination, -4,9 (±6,81) för AVODART och -4,3 (±7,01) för tamsulosin, med en genomsnittlig skillnad mellan kombination och AVODART 0,5 mg av -1,3 enheter (P
Figur 6: Internationell prostatasymtompoäng förändring från baslinjen under en 48-månadersperiod (randomiserad, dubbelblind, parallellgruppsförsök [CombAT-försök])
![International Prostate Symptom Score Change from Baseline over a 48Month Period (Randomized, Double-blind, Parallel-Group Trial [CombAT Trial]) - Illustration](/pics/6a6a769c423e717e43596c5286d65d2e.jpg)
Effekt på akut urinretention eller behovet av BPH-relaterad kirurgi
Efter 4 års behandling gav kombinationsbehandling med AVODART 0,5 mg och tamsulosin ingen fördel jämfört med monoterapi med AVODART för att minska förekomsten av AUR eller BPH-relaterad kirurgi.
Effekt på maximalt urinflöde
Baslinje Qmax var cirka 10,7 ml/sekund för varje behandlingsgrupp. Kombinationsterapi var statistiskt överlägsen var och en av monoterapibehandlingarna när det gällde att öka Qmax vid månad 24, den primära tidpunkten för detta effektmått. Vid månad 24 var medelökningarna från baslinjen (±SD) i Qmax 2,4 (±5,26) mL/sek för kombination, 1,9 (±5,10) mL/sek för AVODART 0,5 mg och 0,9 (±4,57) mL/sek för tamsulosin, med en medelskillnad mellan kombination och AVODART på 0,5 mL/sek (P = 0,003; [95 % KI: 0,17, 0,84]), och mellan kombination och tamsulosin på 1,5 mL/sek (P
Den ytterligare förbättringen av Qmax för kombinationsbehandling jämfört med monoterapi med AVODART 0,5 mg var inte längre statistiskt signifikant vid månad 48.
Figur 7: Qmax-förändring från baslinjen under en 24-månadersperiod (randomiserad, dubbelblind, parallellgruppsförsök [CombAT-försök])
![Qmax Change from Baseline over a 24-Month Period (Randomized, Double-blind, Parallel-Group Trial [CombAT Trial]) - Illustration](/pics/e02ab0fece56d06bb371df5a825f3da6.jpg)
Effekt på prostatavolym
Medelprostatavolymen vid inträde i försöket var cirka 55 cc. Vid månad 24, den primära tidpunkten för detta effektmått, var de genomsnittliga procentuella förändringarna från baslinjen (±SD) i prostatavolymen -26,9 % (±22,57) för kombinationsbehandling, -28,0 % (±24,88) för AVODART 0,5 mg och 0 % (±31,14) för tamsulosin, med en medelskillnad mellan kombination och AVODART 0,5 mg på 1,1 % (P = NS; [95 % KI: -0,6, 2,8]), och mellan kombination och tamsulosin på -26,9 % (P
PATIENTINFORMATION
AVODART (av o dart) (dutasterid) kapslar
AVODART 0,5 mg är endast avsett för män.
Läs denna patientinformation innan du börjar ta AVODART 0,5 mg och varje gång du får påfyllning. Det kan komma ny information. Denna information ersätter inte att prata med din vårdgivare om ditt medicinska tillstånd eller din behandling.
Vad är AVODART 0,5 mg?
AVODART 0,5 mg är ett receptbelagt läkemedel som innehåller dutasterid. AVODART 0,5 mg används för att behandla symtomen på benign prostatahyperplasi (BPH) hos män med en förstorad prostata för att:
- förbättra symtomen,
- minska risken för akut urinretention (en fullständig blockering av urinflödet),
- minska risken för behov av BPH-relaterad operation.
Vem ska INTE ta AVODART?
Ta inte AVODART om du är:
- gravid eller kan bli gravid. AVODART 0,5 mg kan skada ditt ofödda barn. Gravida kvinnor bör inte röra AVODART kapslar. Om en kvinna som är gravid med ett manligt barn får tillräckligt med AVODART 0,5 mg i kroppen genom att svälja eller röra vid AVODART, kan det manliga barnet födas med könsorgan som inte är normala. Om en gravid kvinna eller kvinna i fertil ålder kommer i kontakt med läckande AVODART 0,5 mg kapslar, ska kontaktytan omedelbart tvättas med tvål och vatten.
- ett barn eller en tonåring.
- allergisk mot dutasterid eller något av innehållsämnena i AVODART. Se slutet av denna bipacksedel för en komplett lista över ingredienser i AVODART.
- allergisk mot andra 5 alfa-reduktashämmare, till exempel PROSCAR (finasteride) ® tabletter.
Vad ska jag berätta för min vårdgivare innan jag tar AVODART 0,5 mg?
Innan du tar AVODART 0,5 mg, berätta för din läkare om du:
- har leverproblem
Berätta för din vårdgivare om alla läkemedel du tar, inklusive receptbelagda och receptfria läkemedel, vitaminer och växtbaserade kosttillskott. AVODART och andra läkemedel kan påverka varandra och orsaka biverkningar. AVODART 0,5 mg kan påverka hur andra läkemedel fungerar och andra läkemedel kan påverka hur AVODART 0,5 mg fungerar.
Vet vilka mediciner du tar. Håll en lista över dem för att visa din vårdgivare och apotekspersonal när du får ett nytt läkemedel.
Hur ska jag ta AVODART?
- Ta 1 AVODART kapsel en gång om dagen.
- Svälj AVODART 0,5 mg kapslar hela. Krossa, tugga eller öppna inte AVODART 0,5 mg kapslar eftersom innehållet i kapseln kan irritera dina läppar, mun eller svalg.
- Du kan ta AVODART 0,5 mg med eller utan mat.
- Om du missar en dos kan du ta den senare samma dag. Återställ inte den missade dosen genom att ta 2 doser nästa dag.
Vad ska jag undvika när jag tar AVODART 0,5 mg?
- Du ska inte donera blod medan du tar AVODART eller under 6 månader efter att du har slutat med AVODART. Detta är viktigt för att förhindra att gravida kvinnor får AVODART genom blodtransfusioner.
Vilka är de möjliga biverkningarna av AVODART?
AVODART kan orsaka allvarliga biverkningar, inklusive:
- Sällsynta och allvarliga allergiska reaktioner, inklusive:
- svullnad av ansikte, tunga eller svalg
- allvarliga hudreaktioner, såsom hudflossning
Få medicinsk hjälp omedelbart om du har dessa allvarliga allergiska reaktioner.
- Högre chans för en allvarligare form av prostatacancer.
De vanligaste biverkningarna av AVODART inkluderar:
- problem med att få eller behålla erektion (impotens)*
- minskad sexlust (libido)*
- utlösningsproblem*
- förstorade eller smärtsamma bröst. Om du märker bröstklumpar eller flytningar från bröstvårtan bör du prata med din läkare.
*Vissa av dessa händelser kan fortsätta efter att du slutat ta AVODART.
Nedstämdhet har rapporterats hos patienter som får AVODART.
AVODART 0,5 mg har visat sig minska antalet spermier, spermavolym och spermierörelser. Effekten av AVODART 0,5 mg på manlig fertilitet är dock inte känd.
Prostata-specifikt antigen (PSA) test: Din vårdgivare kan kontrollera dig för andra prostataproblem, inklusive prostatacancer innan du börjar och medan du tar AVODART. Ett blodprov som kallas PSA (prostataspecifikt antigen) används ibland för att se om du kan ha prostatacancer. AVODART kommer att minska mängden PSA som mäts i ditt blod. Din vårdgivare är medveten om denna effekt och kan fortfarande använda PSA för att se om du kan ha prostatacancer. Ökning av dina PSA-nivåer under behandling med AVODART (även om PSA-nivåerna ligger inom det normala intervallet) bör utvärderas av din vårdgivare.
Berätta för din vårdgivare om du har någon biverkning som stör dig eller som inte försvinner.
Dessa är inte alla möjliga biverkningar med AVODART. För mer information, fråga din vårdgivare eller apotekspersonal.
Ring din läkare för medicinsk rådgivning om biverkningar. Du kan rapportera biverkningar till FDA på 1-800-FDA-1088.
Hur ska jag förvara AVODART 0,5 mg?
- Förvara AVODART 0,5 mg kapslar i rumstemperatur (59°F till 86°F eller 15°C till 30°C).
- AVODART 0,5 mg kapslar kan bli deformerade och/eller missfärgade om de förvaras vid höga temperaturer.
- Använd inte AVODART 0,5 mg om dina kapslar är deformerade, missfärgade eller läcker.
- Kasta säkert medicin som inte längre behövs.
Förvara AVODART 0,5 mg och alla läkemedel utom räckhåll för barn.
Läkemedel skrivs ibland ut för andra ändamål än de som anges i en bipacksedel. Använd inte AVODART 0,5 mg för ett tillstånd som det inte har ordinerats för. Ge inte AVODART till andra personer, även om de har samma symtom som du har. Det kan skada dem.
Denna bipacksedel sammanfattar den viktigaste informationen om AVODART. Om du vill ha mer information, prata med din vårdgivare. Du kan fråga din apotekspersonal eller vårdgivare om information om AVODART 0,5 mg som är skriven för vårdpersonal.
För mer information, gå till www.AVODART.com eller ring 1-888-825-5249.
Vilka är ingredienserna i AVODART 0,5 mg?
Aktiv beståndsdel: dutasterid.
Inaktiva Ingredienser : butylerad hydroxitoluen, järnoxid (gul), gelatin (från certifierade BSE-fria nötkreaturskällor), glycerin, mono-diglycerider av kaprylsyra/kaprinsyra, titandioxid och ätbart rött bläck.
Hur fungerar AVODART?
Prostatatillväxt orsakas av ett hormon i blodet som kallas dihydrotestosteron (DHT). AVODART sänker DHT-produktionen i kroppen, vilket leder till att den förstorade prostatan krymper hos de flesta män. Medan vissa män har färre problem och symtom efter 3 månaders behandling med AVODART, är en behandlingsperiod på minst 6 månader vanligtvis nödvändig för att se om AVODART 0,5 mg fungerar för dig.
Denna patientinformation har godkänts av US Food and Drug Administration.
